Lutrate Depot 22,5 Mg Prášek A Rozp. Pro Inj. Susp. S Prodl. Účinkem
Sp.zn.sukls109411/2015 a k sp.zn.sukls111952/2015
Příbalová informace: informace pro uživatele
Lutrate Depot 22,5 mg prášek a rozpouštědlo pro injekční suspenzi s prodlouženým účinkem
Leuprorelini acetas
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Lutrate Depot a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Lutrate Depot používat
3. Jak se přípravek Lutrate Depot používá
4. Možné nežádoucí účinky
5 Jak přípravek Lutrate Depot uchovávat
6. Obsah balení a další informace
1. Co je přípravek Lutrate Depot a k čemu se používá
Přípravek Lutrate Depot je injekční lahvička obsahující bílý prášek, z něhož se připraví suspenze pro injekční aplikaci do svalu. Přípravek Lutrate Depot obsahuje léčivou látku leuprorelin (též nazývaný leuprolid), který patří do skupiny léčiv zvaných agonisté hormonu uvolňujícího luteinizační hormon (LHRH) (léčiva snižující hladinu testosteronu - pohlavního hormonu).
Váš lékař Vám předepsal přípravek Lutrate Depot k paliativní léčbě pokročilého nádoru prostaty.
2. Čemu musíte věnovat pozornost, než začnete přípravek Lutrate Depot používat
Nepoužívejte přípravek Lutrate Depot
- jestliže jste alergický (hypersensitivní) na LHRH, agonisty LHRH nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6). Alergická reakce se může projevit jako vyrážka, svědění, potíže s dýcháním nebo otoky tváře, rtů, krku nebo jazyka.
- j estliže j ste j iž podstoupil orchiektomii (odstranění varlat).
- j ste -li žena nebo dítě.
- Přípravek Lutrate Depot nesmí být k léčbě nádoru prostaty používán samotný, pokud je utlačena mícha nebo se nádor již rozšířil k páteři.
Upozornění a opatření
• Před podáním přípravku Lutrate Depot se poraďte se svým lékařem nebo lékárníkem.
• V průběhu prvních týdnů léčby se u Vás může projevit zhoršení stavu, které se ale v průběhu léčby zlepší. Příznaky mohou zahrnovat: dočasné zvýšení hladin testosteronu (mužský hormon), návaly horka, bolest kostí, poruchy nervového systému (včetně deprese) nebo obstrukce (zamezení nebo ztížení průchodnosti) močových cest.
• Pokud cítíte, že se u Vás projevila alergická reakce (dušnost, astma, alergická rýma, otok tváře, kopřivka, vyrážka na kůži), přestaňte přípravek používat a informujte svého lékaře.
• Informujte svého lékaře, pokud trpíte některou z komplikací uvedených níže, nebo pokud u Vás existuje riziko některé z komplikací, protože je možné, že Váš lékař Vás bude častěji kontrolovat:
• nevysvětlený výskyt modřin nebo krvácení nebo se cítíte celkově špatně. Tyto symptomy mohou, i když vzácně, značit změny v počtu červených nebo bílých krvinek.
• metabolické onemocnění,
• problémy se srdcem nebo bušení srdce,
• diabetes (cukrovka).
• Váš lékař by měl být informován, pokud jste někdy v minulosti měl adenom hypofýzy (nezhoubný nádor podvěsku mozkového). Po počátečním podání podobných přípravků pacientům s adenomem hypofýzy byly popsány případy hypofyzární apoplexie (krvácení) (částečná ztráta tkáně hypofýzy). Hypofyzární apoplexie se může projevit jako náhlá bolest hlavy, meningismus (příznaky podobné dráždění mozkových blan, zejm. ztuhlost šíjových svalů), poruchy vidění až slepota a někdy i porucha vědomí.
• Informujte svého lékaře, pokud trpíte krvácivou poruchou, trombocytopenií (dlouhodobý úbytek krevních destiček) nebo jste léčen antikoagulancii (léky proti srážení krve). Vzhledem k tomu, že při léčbě leuprorelinem byly hlášeny změny v játrech a také žloutenka (žlutá oční bělma a žlutá kůže), může být zapotřebí monitorovat funkci jater v průběhu léčby.
• Během léčby leuprorelinem byly hlášeny zlomeniny páteře, ochrnutí, nízký nebo vysoký krevní tlak.
• U pacientů používajících přípravek Lutrate Depot byly hlášeny případy deprese, která může být závažná. Pokud používáte přípravek Lutrate Depot a rozvine se u Vás depresivní nálada, informujte svého lékaře.
• V souvislosti s léčbou leuprorelinem bylo hlášeno i snížení hustoty kostí (křehké nebo slabší kosti). Váš lékař může zvážit přidání některého antiandrogenu k léčbě přípravkem Lutrate Depot. Dále bude Váš lékař kontrolovat stav žil, zda nevzniká zánět (tromboflebitida), a bude sledovat známky možných problémů se srážlivostí krve a otoky (rukou, chodidel nebo kotníků). Existuje zvýšené riziko jejich vzniku v případě současného podávání přípravku Lutrate Depot a antiandrogenního přípravku.
• Informujte svého lékaře, pokud budete cítit tlak v míše a/nebo budete mít potíže s močením a/nebo se u Vás projeví hematurie (krev v moči). Váš lékař pak, bude-li to nezbytné, bude aplikovat další opatření k prevenci neurologických komplikací (např. mravenčení v rukou či chodidlech, ochrnutí) nebo ucpání močové trubice (trubice vedoucí z močového měchýře ven z těla). Během prvních týdnů léčby budete pod pečlivým dohledem.
• Mohou se u Vás vyskytnout změny metabolismu (např. nesnášenlivost glukózy nebo zhoršení již existující cukrovky), změny tělesné hmotnosti nebo kardiovaskulární potíže.
• Pacienti s metabolickým nebo kardiovaskulárním onemocněním a zejména pacienti, kteří prodělali městnavé srdeční selhání (stav, kdy srdce není schopno zásobovat zbytek těla dostatkem krve), by měli být v průběhu léčby leuprorelinem pečlivě monitorováni.
• V průběhu léčby budete podroben krevním testům, aby se prokázalo, že léčba je účinná.
• Může se u Vás projevit snížení libida (pohlavní touha), návaly horka a někdy může dojít i ke zmenšení velikosti varlat a ke snížení jejich funkce.
• Plodnost se může po ukončení léčby přípravkem Lutrate Depot opět obnovit.
• Vzhledem k tomu, že přípravek Lutrate Depot může ovlivnit některé laboratorní testy, ujistěte se, že Váš lékař je informován o tom, že používáte přípravek Lutrate Depot.
• Křeče se mohou objevit u pacientů náchylných ke křečím (u nichž se již křeče v minulosti objevily nebo pacienti s epilepsií, obtížemi s mozkovými cévami, anomáliemi či nádory centrálního nervového systému) nebo u pacientů užívajících léky, které mohou křeče vyvolat, v menší míře se mohou křeče objevit i u pacientů, kteří tyto charakteristiky nemají.
• Informujte, prosím, svého lékaře, pokud trpíte některým z následujících onemocnění:
Jakékoliv srdeční či cévní onemocnění, včetně poruch srdečního rytmu (arytmie), nebo léčba těchto onemocnění. Při používání Lutrate Depot může být zvýšeno riziko poruch srdečního rytmu.
Další léčivé přípravky a přípravek Lutrate Depot
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat. Váš lékař pak bude moci rozhodnout, co je pro Vás vhodné při podávání přípravku Lutrate Depot.
Přípravek Lutrate Depot a souběžně užívané přípravky k léčbě poruch srdečního rytmu (např. chinidin, prokainamid, amiodaron a sotalol) se mohou navzájem ovlivňovat. Přípravek Lutrate Depot může zvyšovat riziko poruch srdečního rytmu, pokud je používán s dalšími přípravky (např. metadon (užívaný k úlevě od bolesti nebo jako část odvykací terapie), moxifloxacin (antibiotikum), antipsychotika užívaná k léčbě závažných duševních poruch).
Těhotenství a kojení
Přípravek Lutrate Depot není určen k podávání ženám.
Jeho podání v průběhu těhotenství je kontraindikováno, neboť může vyvolat spontánní potrat.
Řízení dopravních prostředků a obsluha strojů
Nebyly provedeny žádné studie vlivu přípravku Lutrate Depot na schopnost řídit dopravní prostředky a obsluhovat stroje.
Během léčby se mohou objevit poruchy vidění a závratě. Pokud pocítíte takové příznaky, neřiďte dopravní prostředky a neobsluhujte stroje.
Přípravek Lutrate Depot obsahuje méně než 1 mmol sodíku (23 mg) v jedné dávce, což znamená, že je v podstatě bez obsahu sodíku.
3. Jak se přípravek Lutrate Depot používá Dávkování
Přípravek Lutrate Depot musí být podán pod dohledem lékaře nebo kvalifikovaného zdravotnického pracovníka.
Dospělí včetně starších osob:
Doporučená dávka přípravku Lutrate Depot je jedna injekce jednou za tři měsíce.
Před podáním je prášek naředěn na suspenzi a ta je podána v jedné injekci intramuskulárně (do svalu) jednou za tři měsíce.
Místo vpichu se má pravidelně střídat.
Přípravek Lutrate Depot smí být podán pouze intramuskulárně (do svalu). Nesmí se podávat žádným jiným způsobem.
Použití u dětí: Přípravek Lutrate Depot není určen k podávání dětem.
Váš lékař určí intenzitu léčby.
Jestliže jste použil více přípravku Lutrate Depot, než jste měl
Taková situace je nepravděpodobná, protože Váš lékař nebo zdravotní sestra znají správnou dávku. Pokud ale máte podezření, že Vám byla podána dávka větší, než by měla, informujte ihned svého lékaře, aby mohl případně aplikovat příslušná opatření.
Jestliže jste zapomněl použít přípravek Lutrate Depot
Je velmi důležité nezapomenout na podání přípravku Lutrate Depot. Jestliže jste na injekci zapomněl, kontaktujte svého lékaře ihned, jakmile si vzpomenete a lékař Vám podá další injekci.
Jestliže jste přestal používat přípravek Lutrate Depot
Léčba přípravkem Lutrate Depot je dlouhodobá a při přerušení léčby můžete pocítit zhoršení symptomů onemocnění. Proto nepřerušujte léčbu předčasně bez souhlasu Vašeho lékaře.
Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Informujte ihned svého lékaře, pokud se u Vás objeví náhlé sípání, potíže s dýcháním, otoky očních víček, tváře nebo rtů, vyrážka nebo svědění (zejména pokud postihne celé tělo).
Hlášeny byly níže uvedené nežádoucí účinky.
Velmi časté (mohou postihnout více než 1 osobu z 10):
Návaly horka a reakce v místě vpichu.
Časté (mohou postihnout až 1 osobu z 10):
Studený pot, hyperhidróza (zvýšené pocení), pruritus (svědění), únava, insomnie (nespavost), snížená sexuální touha, pocit točení (závrať), návaly horka, nevolnost (pocit na zvracení), průjem, snížená chuť k jídlu, erektilní disfunkce, astenie (nedostatek nebo ztráta síly), bolest kostí, bolest v kloubech a reakce v místě vpichu, jako je bolest, zatvrdnutí, erytém (zarudnutí kůže). Bolesti močových cest, snížení proudu moči, častá potřeba močit, při dlouhodobé léčbě leuprorelinem změny nálady a deprese, změny jaterních enzymů, zvýšená hladina triglyceridů v krvi (vysoká hladina lipidů v krvi) a zvýšená hladina cukru v krvi.
Méně časté (mohou postihnout až 1 osobu ze 100):
Vysoká hladina cholesterolu, poruchy spánku, třesavka, změny chuti k jídlu, mravenčení (změny pocitu na kůži), bolest hlavy, letargie (ospalost), rozostřené vidění, zánět pohrudnice, zvonění v uších (tinnitus), bolest v horní části břicha, zácpa, pupínky, vyrážka, generalizovaný pruritus (svědění po celém těle), noční pocení, bolest zad, bolest svalů, bolest krku, bolesti prsních bradavek, bolesti v pánvi, atrofie (zmenšení) varlat, poruchy varlat, pocity horka, při krátkodobé léčbě leuprorelinem změny nálady. Změny krevních hodnot a změny EKG (prodloužení intervalu QT) a reakce v místě vpichu, jako jsou kopřivka, pocit tepla a krvácení.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
Webové stránky: http://www.sukl.cz/nahlasit-nezadouci-ucinek
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Lutrate Depot uchovávat
Váš lékař nebo lékárník jsou informováni, jak uchovávat přípravek Lutrate Depot.
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte při teplotě do 25 °C. Chraňte před mrazem.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce, injekční lahvičce a předplněné injekční stříkačce za zkratkou EXP. Předplněná injekční stříkačka a injekční lahvička mají stejnou dobu použitelnosti. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Nevyhazujte žádné léčivé přípravky do odpadních vod. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Lutrate Depot obsahuje
Léčivou látkou je leuprorelini acetas. Jedna injekční lahvička obsahuje leuprorelini acetas 22,5 mg. Koncentrace naředěného přípravku je 11,25 mg/ml.
Dalšími složkami jsou polysorbát 80, mannitol (E 421), sodná sůl karmelosy (E466), triethyl-citrát, kyselina polymléčná.
Rozpouštědlo (předplněná injekční stříkačka) obsahuje mannitol (E421), vodu na injekci, hydroxid sodný (k úpravě pH) a kyselinu chlorovodíkovou (k úpravě pH).
Jak přípravek Lutrate Depot vypadá a co obsahuje toto balení
Jedno balení přípravku obsahuje jednu injekční lahvičku s 22,5 mg leuprorelin-acetátu, jednu předplněnou injekční stříkačku s 2 ml rozpouštědla, jeden adaptační systém a jednu sterilní jehlu velikosti 20G.
Držitel rozhodnutí o registraci
Angelini Pharma Osterreich GmbH Gewerbestrasse 18 - 20 Gewerbegebiet Klein-Engersdorf 2102 Bisamberg Rakousko
Výrobce
GP-PHARM, S.A.
Pol ind Els Vinyets -els Fogars. Sector 2 Carretera comarcal 244, km22 08777 Sant Quintí de Mediona Španělsko
Tento léčivý přípravek byl schválen v dalších státech Evropské ekonomické oblasti pod následujícími názvy:
Lutrate Depot Trimestral 22.5 mg polvo y disolvente para suspensión de liberación prolongada inyectable
Lutrate Depot 22.5 mg pulver und losungsmittel zur Herstellung einer Depot-Injektionssuspension
Lutrate Depot 22.5 mg/2 ml pó e veículo para suspensao injectável de liberta^ao prolongada
Lutrate Depot 22.5 mg Kóvig Kai Sia^úxng yra napaoKsn^ svsaípon svairop^paxog napaxsxapévng anoSsapsnang
Politrate 22.5 mg Polvere e solvente per sospensione iniettabile a rilascio prolungato
Politrate 22.5 mg pulver och vatska till injektionvaska, suspension
Politrate Depot 22.5 mg
Lutrate Depot
Lutrate 22.5 mg
Leuprorelin 3-month Depot 22.5 mg powder and solvent for prolonged-release suspension for injection
Politrate Depot 22.5 mg powder and solvent for prolonged-release suspension for injection
Lutrate Depot 22.5 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
Leuproreline Lutrate Depot 22.5 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Lutrate Depot
Španělsko:
Německo:
Portugalsko:
Řecko:
Itálie:
Švédsko:
Maďarsko:
Dánsko:
Finsko:
Irsko:
Velká Británie:
Belgie:
Nizozemsko:
Norsko:
Rakousko: Lutrate Depot 22.5 mg pulver und losungsmittel zur herstellung einer Depot-
inj ektionssuspension
Estonsko: Lutrate Depot 22.5 mg
Litva: Lutrate Depot 22.5 mg milteliai ir tirpiklis pailginto atpalaidavimo injekcinei
Lotyšsko: Lutrate Depot 22.5 mg pulveris un škidinátajs ilgstošas darbibas injekciju suspensijas
pagatavošanai
Česká republika: Lutrate Depot 22.5 mg prášek a rozpouštědlo pro injekční suspenzi s prodlouženým účinkem
Polsko: Lutrate Depot
Slovenská republika: Lutrate Depot 22.5 mg
Rumunsko Lutrate Depot 22.5 mg pulbere §i solvent pentru suspensie injectabilá cu eliberare
prelungitá
Bulharsko: Lutrate Depot
Tato příbalová informace byla naposledy revidována: 14.8.2015
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Jak připravit injekci?
Postupujte přesně podle následujících instrukcí.
Aseptická technika je nezbytná pro přípravu suspenze.
Důležité:
Po rekonstituci rozpouštědlem musí být přípravek ihned aplikován.
Přípravek je určen pouze k jednorázovému podání.
Ověřte si, že obsah kitu odpovídá popisu v příbalové informaci.
Balení obsahuje:
Jednu injekční lahvičku přípravku Lutrate Depot (leuprorelini acetas), prášek pro injekční suspenzi Jednu předplněnou injekční stříkačku s rozpouštědlem pro suspenzi (0,8% roztok mannitolu na injekci). Jeden adaptační systém pro rekonstituci s jednou sterilní jehlou pro jednorázové použití.
1
g
Odstraňte kryt z injekční lahvičky.
2

Nasaďte adaptační systém (fialový) na injekční lahvičku až do slyšitelného zacvaknutí.
3
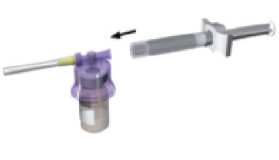
Připojte bílou úchytku k injekční stříkačce s rozpouštědlem. Sejměte gumový kryt ze stříkačky a připojte ji k adaptačnímu systému.
4
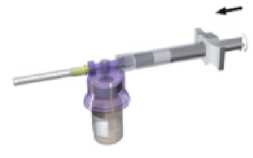
Držte stříkačku, dobře spojenou s injekční lahvičkou, ve vzpřímené poloze a zvolna stlačujte píst, abyste přemístili všechno rozpouštědlo do lahvičky.
7
I
5
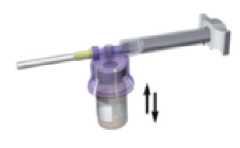
S injekční lahvičkou, stále spojenou se stříkačkou, jemně třepejte po dobu asi jedné minuty do získání homogenní mléčně bílé suspenze.

Otáčením horní části adaptačního systému proti směru hodinových ručiček odpojte stříkačku a jehlu. Léčivý přípravek je připraven k aplikaci.
6

Otočte celý systém dnem vzhůru a opatrně vytahujte píst, abyste natáhli suspenzi léčiva z injekční lahvičky do injekční stříkačky.
8

Očistěte místo vpichu tampóny vlhčenými alkoholem a nechte kůži oschnout. Aplikujte injekci suspenze intramuskulárně do vnějšího horního kvadrantu hýžďového svalu.
Na stěnách injekční lahvičky mohou ulpět zbytky přípravku, což není na závadu. Během výroby přípravku je injekční lahvička naplněna nadbytkem přípravku, aby se zajistila konečná dávka 22,5 mg leuprorelin-acetátu.
7