Fibclot 1,5 G
sp. zn. sukls10610/2015
Příbalová informace: informace pro pacienta Fibclot 1,5 g
Prášek a rozpouštědlo pro injekční/mfuzní roztok
fibrinogenum humanum
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4.
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Fibclot a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Fibclot používat
3. Jak se přípravek Fibclot používá
4. Možné nežádoucí účinky
5. Jak přípravek Fibclot uchovávat
6. Obsah balení a další informace
1. Co je přípravek Fibclot a k čemu se používá Co je přípravek Fibclot
Léčivý přípravek Fibclot patří do skupiny hemostatik (léky používané ke zmírnění nebo zastavení krvácení). Léčivou látkou je lidský fibrinogen, bílkovina, která se přirozeně vyskytuje v těle. Úlohou této bílkoviny je zajistit normální srážení krve a zabránit příliš dlouhému krvácení.
K čemu se přípravek Fibclot používá
Používá se k nahrazení chybějícího lidského fibrinogenu, a tím k prevenci a léčbě krvácení (hemoragií) u pacientů s vrozeným nedostatkem fibrinogenu.
Vrozený nedostatek fibrinogenu je dědičné onemocnění charakterizované nižší než normální hladinou bílkoviny zvané fibrinogen nebo jejím úplným chyběním. Tento nedostatek může vést k dlouhotrvajícím krvácením.
2. Čemu musíte věnovat pozornost, než začnete přípravek Fibclot používat Nepoužívejte přípravek Fibclot
jestliže jste alergický(á) na lidský fibrinogen nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6 „Obsah balení a další informace”).
Informujte prosím svého lékaře, jestliže jste alergický(á) na jakýkoli lék.
Upozornění a opatření:
Před použitím přípravku Fibclot se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou.
Riziko krevních sraženin
Při vysoké dávce nebo opakovaném podávání může tento lék zvyšovat riziko vzniku krevních sraženin v krevních cévách.
Váš lékař proto posoudí přínos tohoto léku ve srovnání s rizikem vzniku krevních sraženin, zejména:
• jestliže jste prodělal(a) srdeční záchvat (ischemická choroba srdeční nebo infarkt myokardu v anamnéze),
• jestliže máte onemocnění jater,
• jestliže jste právě prodělal(a) operaci (pacienti po operaci),
• jestliže brzy podstoupíte operaci (pacienti před operací),
• u novorozenců,
• jestliže je u Vás větší pravděpodobnost vzniku krevních sraženin, než je normální.
Váš lékař rovněž může požadovat provedení dalších testů s ohledem na toto riziko.
Riziko alergií
Váš lékař Vás bude informovat o varovných příznacích alergické reakce (viz bod 4. „Možné nežádoucí účinky”). Jestliže se objeví některý z těchto účinků, musí se podávání tohoto léčivého přípravku ihned ukončit.
Virová bezpečnost
Tento lék se vyrábí z lidské plazmy (tekutá část krve).
Při výrobě léčivých přípravků z lidské krve nebo plazmy se dodržují určitá opatření zabraňující přenosu infekce na pacienty. Ta zahrnují:
• pečlivý výběr dárců krve a plazmy, aby bylo vyloučeno riziko přenosu infekčních onemocnění,
• testování každého darovaného vzorku a směsných vzorků plazmy na známky virových infekcí,
• zajištění takových výrobních postupů při zpracování krve a plazmy, které zajišťují zničení nebo odstranění virů
Přes všechna tato opatření při přípravě léků vyráběných z lidské krve nebo plazmy nelze možnost přenosu infekce zcela vyloučit. To platí i pro jakékoli neznámé nebo nově vznikající viry či jiné druhy infekcí.
Přijatá opatření se považují za účinná vůči obaleným virům, jako je virus lidské imunodeficience (virus HIV neboli virus způsobující AIDS), virus hepatitidy B a virus hepatitidy C, a vůči neobalenému viru hepatitidy A.
Přijatá opatření mohou mít omezený užitek vůči neobaleným virům, jako je parvovirus B19. Infekce způsobená parvovirem B19 může být závažná pro těhotné ženy (infekce plodu) a pro jedince, jejichž imunitní systém je oslabený nebo kteří trpí určitým typem anemie (např. srpkovitá anemie nebo hemolytická anemie).
Váš lékař Vám může doporučit, abyste zvážil(a) možnost očkování proti hepatitidě A a B, jestliže pravidelně/opakovaně používáte přípravky vyrobené z lidské plazmy.
Důrazně se doporučuje, aby vždy, když Vám bude aplikován tento přípravek, byl zaznamenán název a číslo šarže přípravku z důvodu evidence použitých šarží.
Děti a dospívající
Pro děti a dospívající platí stejná upozornění a opatření.
Další léčivé přípravky a přípravek Fibclot
Informujte svého lékaře nebo lékárníka o všech lécích, které používáte, které jste v nedávné době používal(a) nebo které možná budete používat, včetně volně prodejných léků.
Dosud nebylo pozorováno žádné vzájemné působení mezi tímto přípravkem a jinými léčivými přípravky. Přípravek se však nemá mísit s jinými látkami ani s jinými léčivými přípravky.
Těhotenství a kojení
• Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek používat. Tento přípravek máte používat během těhotenství a kojení pouze na doporučení svého lékaře.
• Jestliže během léčby zjistíte, že jste těhotná, poraďte se se svým lékařem, neboť pouze lékař může rozhodnout, zda je nutné pokračovat v léčbě.
Řízení dopravních prostředků a obsluha strojů
Tento léčivý přípravek nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
Přípravek Fibclot obsahuje až 3 mmol (nebo 69 mg) sodíku v jedné injekční lahvičce.
Nutno vzít v úvahu u pacientů na dietě s nízkým obsahem sodíku.
3. Jak se přípravek Fibclot používá
Léčba má být zahájena pod dohledem lékaře se zkušenostmi s léčbou vrozeného nedostatku fibrinogenu.
Dávka
Váš lékař určí vhodnou dávku a frekvenci podávání v závislosti na:
• Vaší tělesné hmotnosti,
• závažnosti Vaší poruchy,
• místě a rozsahu krvácení či povaze Vaší operace,
• Vašem zdravotním stavu.
Váš lékař Vám doporučí podstoupit během léčby krevní testy na kontrolu hladiny fibrinogenu.
Na základě výsledků těchto testů se může Váš lékař rozhodnout upravit dávku a frekvenci Vašich injekcí.
Frekvence podávání
Váš lékař určí, jak často se musí injekce podávat.
Váš lékař upraví počet injekcí na základě závažnosti Vašeho krvácení a účinnosti léčby.
Informace ohledně frekvence a době léčby v různých situacích jsou uvedeny na konci této příbalové informace v části vyhrazené pro zdravotnické pracovníky.
Způsob podání:
Tento léčivý přípravek se podává injekcí do žíly. Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
Jestliže Vám bylo podáno více přípravku Fibclot, než mělo
Aby se zamezilo riziku předávkování, bude Vám Váš lékař provádět pravidelné krevní testy ke kontrole hladiny fibrinogenu.
V případě předávkování nelze vyloučit riziko abnormální tvorby sraženin v krvi.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Riziko alergických reakcí: stejně jako u jakéhokoli nitrožilně podávaného přípravku obsahujícího bílkovinu může dojít k alergickým reakcím. V některých případech tyto reakce přešly v závažnou alergickou reakci.
Varovnými příznaky alergických reakcí jsou:
• otok obličeje nebo hrdla,
• pocit pálení a brnění v místě injekce,
• třesavka,
• zčervenání, svědění a vyrážka,
• rychlá srdeční frekvence, nízký krevní tlak,
• mimořádná únava (letargie),
• pocit na zvracení zvracení,
• neklid,
• tíseň na hrudi,
• pocit brnění a píchání,
• sípot (jako při astmatu).
Pokud se objeví některý z těchto účinků, uvědomte lékaře, který, v závislosti na typu a závažnosti reakce, okamžitě ukončí léčbu tímto přípravkem a/nebo zahájí vhodnou léčbu._
Krevní sraženiny: v krevním oběhu může docházet k tvorbě krevních sraženin. To může mít za
následek:
• srdeční záchvat, jehož varovnými příznaky jsou náhlá bolest na hrudi nebo dýchavičnost,
• cévní mozkovou příhodu, jejímiž varovnými příznaky jsou náhlý nástup svalové slabosti, ztráta citlivosti a/nebo rovnováhy, snížená bdělost nebo obtíže při mluvení,
• závažný stav zvaný plicní embolie, jejímiž varovnými příznaky jsou bolest na hrudi, dýchací obtíže nebo vykašlávání krve,
• sraženinu v žíle (žilní trombóza), jejímiž varovnými příznaky jsou zčervenání, pocit tepla, bolest, citlivost nebo otok na jedné nebo obou nohách.
Pokud se objeví některý z těchto účinků, uvědomte lékaře, který, v závislosti na typu a závažnosti reakce, okamžitě ukončí léčbu tímto přípravkem a/nebo zahájí vhodnou léčbu._
Následující nežádoucí účinky jsou časté (méně než 1 z 10 infuzí):
• bolest hlavy.
Následující nežádoucí účinky jsou méně časté (méně než 1 ze 100 infuzí):
• alergická reakce (včetně anafylaktického šoku, bledosti, zvracení, kašle, nízkého krevního tlaku, třesavky, kopřivky (urtikarie), viz také bod „Riziko alergických reakcí”),
• závrať,
• ušní šelest
• porucha oběhu krve (hluboká žilní trombóza, povrchová tromboflebitida),
• dechové potíže (astma),
• kožní vyrážka, zčervenání kůže, podráždění kůže, noční pocení,
• pocit horka.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
webové stránky: http://www.sukl.cz/nahlasit-nezadouci-ucinek
Nahlášením nežádoucích účinků můžete pomoci přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Fibclot uchovávat
• Uchovávejte tento přípravek mimo dohled a dosah dětí.
• Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na štítku a na krabičce. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
• Uchovávejte při teplotě do 25 °C. Chraňte před mrazem.
• Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem a vlhkem.
• Byla prokázána stabilita po dobu 24 hodin při teplotě 25 °C. Přípravek se však má použít ihned po rekonstituci.
• Nepoužívejte tento přípravek, pokud je rekonstituovaný roztok zakalený nebo obsahuje usazeniny.
• Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek Fibclot obsahuje
Léčivou látkou je fibrinogenum humanum, jedna injekční lahvička obsahuje nominálně fibrinogenum humanum 1,5 g. Po rekonstituci ve 100 ml vody na injekci obsahuje přípravek Fibclot nominálně fibrinogenum humanum (lidský fibrinogen) 15 mg/ml
Dalšími složkami jsou arginin-hydrochlorid, isoleucin, lysin-hydrochlorid, glycin, dihydrát natrium-citrátu a rozpouštědlo (voda na injekci).
Jak přípravek Fibclot vypadá a co obsahuje toto balení
Tento léčivý přípravek se dodává ve formě prášku a rozpouštědla pro injekční/infuzní roztok ve skleněných injekčních lahvičkách a s převodním systémem.
Rekonstituovaný roztok má být téměř bezbarvý, lehce opalizující (s perlovitým leskem).
Držitel rozhodnutí o registraci:
Laboratoire Fran^ais du Fractionnement et des Biotechnologies 3 Avenue des Tropiques, ZA de Courtabmuf, 91940 Les Ulis, Francie Tel.: +33(0) 1 69 82 70 10 Fax: +33(0) 1 69 82 19 03
Výrobce:
LFB BIOMEDICAMENTS
59 rue de Trévise, 59000 Lille, Francie
Tento léčivý přípravek je v členských státech EHP registrován pod těmito názvy:
Německo, Rakousko, Řecko, Španělsko, Velká Británie: FibCLOT Dánsko, Finsko, Lucembursko, Maďarsko, Nizozemsko, Norsko, Švédsko: Fibclot Belgie: Fibclot 1,5 g, poudre et solvant pour solution injectable/pour perfusion Česká republika, Slovenská republika: Fibclot 1,5 g Itálie: Fibriclotte
Tato příbalová informace byla naposledy revidována: 4.5.2016.
Léčba se má zahajovat pod dohledem lékaře se zkušenostmi s léčbou poruch koagulace.
Dávkování
Dávkování a doba trvání substituční terapie závisí na závažnosti poruchy, místě a rozsahu krvácení a na klinickém stavu pacienta.
Je třeba stanovit (fUnkční) hladinu fibrinogenu, aby bylo možné vypočítat individuální dávkování. Dávka a četnost podání se mají stanovit u každého pacienta individuálně na základě pravidelného měření hladiny plazmatického fibrinogenu, neustálého sledování klinického stavu pacienta a jiných použitých substitučních terapií.
Normální hladina plazmatického fibrinogenu se pohybuje v rozmezí 1,5 - 4,5 g/l. U vrozené hypofibrinogenemie nebo afibrinogenemie představuje kritickou hladinu plazmatického fibrinogenu, pod kterou může dojít ke krvácením, přibližně hodnota 0,5 - 1,0 g/l.
V případě velké chirurgické intervence je nezbytné přesné sledování substituční terapie pomocí koagulačních testů.
Léčba krvácení a perioperační profylaxe u pacientů s vrozenou hypofibrinogenemií nebo afibrinogenemií a se známým sklonem ke krvácení.
K léčbě nechirurgických krvácivých příhod se doporučuje zvýšit hladinu fibrinogenu na 1 g/l a udržet fibrinogen na této hladině, dokud není hemostáza pod kontrolou, a na hladině vyšší než 0,5 g/l, dokud nedojde k úplnému zhojení.
K prevenci nadměrného krvácení během chirurgických zákroků se doporučuje profylaktická léčba na zvýšení hladiny fibrinogenu na 1 g/l a udržování fibrinogenu na této hladině, dokud není hemostáza pod kontrolou, a na hladině vyšší než 0,5 g/l, dokud nedojde k úplnému zhojení.
V případě chirurgického zákroku nebo léčby nechirurgického krvácení se dávka vypočítá takto:
dávka (g) = (cílová hladina (g/l) - výchozí hladina (g/l)) x 0,043 x tělesná hmotnost (kg). přičemž 0,043 odpovídá 1/recovery ((g/l)/(g/kg)).
V případě naléhavé situace, kdy výchozí hladina fibrinogenu není známa, je doporučená počáteční dávka 0,05 g na kg tělesné hmotnosti podávaná intravenózně.
Následné dávkování (dávky a četnost injekcí) se upraví podle klinického stavu pacienta a laboratorních výsledků.
Biologický poločas fibrinogenu je 3-4 dny. Při absenci spotřeby tak není opakovaná léčba lidským fibrinogenem obvykle nutná. Vzhledem k tomu, že v případě opakovaného podání za účelem profylaxe dochází k nahromadění přípravku, se má dávka a četnost podávání stanovit na základě terapeutických cílů lékaře pro daného pacienta.
Pediatrická populace
Nelze učinit žádná doporučení ohledně dávkování u dětí.
Rekonstituce:
Řiďte se aktuálními pokyny pro aseptický postup.
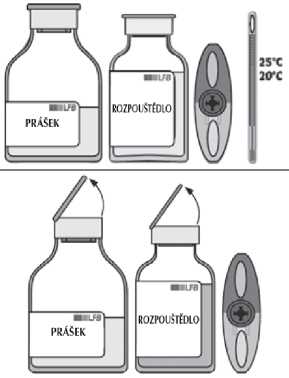
V případě potřeby zahřejte obě injekční lahvičky (s práškem a rozpouštědlem) na pokojovou teplotu.
Sejměte ochranné víčko z injekční lahvičky s rozpouštědlem a z injekční lahvičky s práškem.
Dezinfikujte povrch obou zátek.
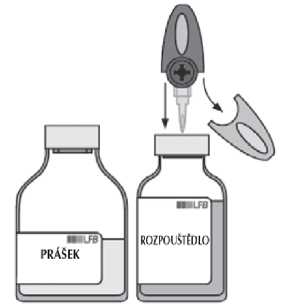
Sejměte průsvitný ochranný kryt z převodního systému a obnažený ostrý hrot zaveďte za současného otáčení zcela skrz střed zátky injekční lahvičky s rozpouštědlem.
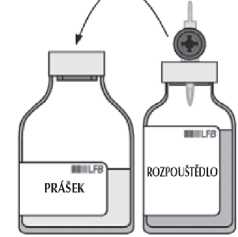
Sejměte šedý ochranný kryt z druhého konce převodního systému. Otočte lahvičku s rozpouštědlem a rychle protlačte volný konec ostrého hrotu skrz střed zátky injekční lahvičky s práškem, aby rozpouštědlo mohlo přetéci do prášku.
Dbejte na to, aby byl hrot neustále ponořen v rozpouštědle, aby se zabránilo předčasnému uvolnění podtlaku.
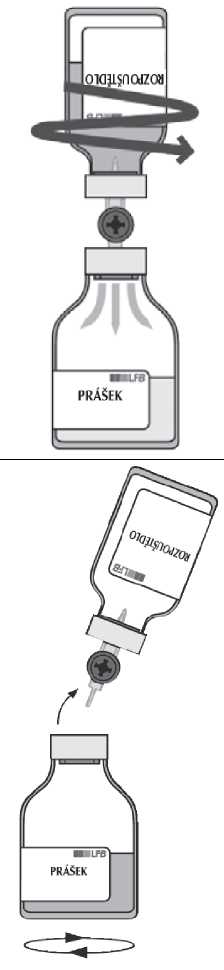
Během přetékání směrujte krouživým horizontálním pohybem proud rozpouštědla po celém povrchu prášku a podél stěny injekční lahvičky. Ujistěte se, že veškeré rozpouštědlo přeteklo. Podtlak se na konci převádění automaticky uvolní sterilním vzduchem, pronikajícím vzduchovým otvorem převodního systému.
Oddělte prázdnou injekční lahvičku (od rozpouštědla) s převodním systémem.
Několik minut lahvičkou s přípravkem jemně kružte, abyste zabránili vzniku pěny, dokud se prášek zcela nerozpustí.
Rekonstituovaný přípravek se musí před podáním vizuálně zkontrolovat, zda neobsahuje částice. Rekonstituovaný roztok má být téměř bezbarvý, lehce opalizující. Nepoužívejte roztoky, které jsou zakalené nebo obsahují usazeniny.
Podání:
Přípravek Fibclot má být podáván pouze intravenózně, v jedné dávce, ihned po rekonstituci, rychlostí do 4 ml/min.
Pokud se rekonstituovaný roztok ihned nepodá, nemá doba uchovávání přesáhnout 24 hodin při pokojové teplotě (maximálně 25 °C).
Doporučuje se použít infuzní set s nesterilizujícím 15pm filtrem.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
Tento léčivý přípravek nesmí být mísen s jinými léčivými přípravky a má se podávat samostatnou injekcí/infuzní linkou.
8