Enstilar 50 Mikrogramů/G + 0,5 Mg/G
Sp.zn. sukls44050/2015
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. NÁZEV PŘÍPRAVKU
Enstilar 50 mikrogramů/g + 0,5 mg/g Kožní pěna
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden gram kožní pěny obsahuje calcipotriolum 50 mikrogramů (jako calcipotriolum monohydricum) a betamethasonum 0,5 mg (jako betamethasoni dipropionas).
Pomocná látka se známým účinkem: butylhydroxytoluen (E321) 50 mikrogramů/g kožní pěny.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Kožní pěna.
Po stlačení aplikátoru se tvoří bílá až téměř bílá pěna.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Topická léčba psoriasis vulgaris u dospělých.
4.2 Dávkování a způsob podání
Dávkování
Enstilar se má nanášet jednou denně na postižená místa. Doporučená délka léčby jsou 4 týdny. Maximální denní dávka přípravku Enstilar nemá překročit 15 g, tj. jedna 60g nádobka má vystačit na nejméně 4 dny. 15 g odpovídá množství, které je z nádobky aplikováno, pokud je aplikátor zcela stlačen po dobu zhruba jedné minuty. Dvousekundová aplikace odpovídá přibližně množství 0,5 g. Pro představu, 0,5 g pěny má pokrýt plochu kůže odpovídající přibližně velikosti dlaně dospělého člověka.
Pokud jsou kromě přípravku Enstilar používány další topické přípravky s obsahem kacipotriolu, celková denní dávka kalcipotriolu nemá překročit 1 5 g.
Celková ošetřená plocha těla nemá překročit 30 %.
Zvláštní skupiny pacientů
Porucha funkce ledvin a jater
Bezpečnost a účinnost přípravku Enstilar u pacientů s těžkou poruchou funkce ledvin nebo těžkými poruchami funkce jater nebyla hodnocena.
Pediatrická populace
Bezpečnost a účinnost přípravku Enstilar u dětí mladších 18 let nebyla stanovena. Nejsou dostupné žádné údaje.
Způsob podání Kožní podání.
Před použitím je třeba nádobku protřepat po dobu několika sekund. Přípravek Enstilar se aplikuje ze vzdálenosti nejméně 3 cm od kůže. Pěnu lze aplikovat držením nádobky v jakémkoliv směru kromě horizontálního.
Enstilar se má aplikovat přímo na postižené oblasti kůže a jemně vmasírovat. Po použití přípravku Enstilar je třeba si umýt ruce (pokud nejsou ruce ošetřovanou oblastí ), aby se zamezilo neúmyslnému rozšíření na jiné části těla. Je třeba se vyvarovat aplikace pod okluzivní obvaz, jelikož dochází ke zvýšené systémové absorpci kortikosteroidů. Koupání ani sprchování bezprostředně po aplikaci přípravku Enstilar se nedoporučuje.
4.3 Kontraindikace
Hypersenzitivita na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Enstilar je kontraindikován u erytrodermické a pustulózní psoriázy.
Vzhledem k obsahu kalcipotriolu je Enstilar kontraindikován u pacientů se zjištěnými poruchami metabolismu vápníku (viz bod 4.4).
Vzhledem k obsahu kortikosteroidu je Enstilar kontraindikován při následujících stavech: virové (např. herpetické infekce nebo varicella) kožní léze, mykotické nebo bakteriální kožní infekce, parazitární infekce, kožní projevy tuberkulózy, periorální dermatitida, atrofická kůže, atrofické strie, fragilita kožních žil, ichthyóza, acne vulgaris, acne rosacea, rosacea, vředy a rány (viz bod 4.4).
4.4 Zvláštní upozornění a opatření pro použití
Účinky na endokrinní systém
Kvůli systémové absorpci se mohou objevit i během topické léčby kortikosteroidy nežádoucí účinky, které byly pozorovány u systémové léčby kortikosteroidy, jako je suprese kůry nadledvin nebo porucha kompenzace diabetu mellitu.
Je nutné se vyhnout aplikaci pod okluzivní obvaz, jelikož se tím zvyšuje systémová absorpce kortikosteroidů. Je nutné se vyhnout aplikaci na velké plochy poškozené kůže, na sliznice nebo do kožních záhybů, protože se tím zvyšuje systémová absorpce kortikosteroidů (viz bod 4.8).
Účinky na metabolismus vápníku
Vzhledem k obsahu kalcipotriolu se může při překročení maximální denní dávky (15 g) vyskytnout hyperkalcemie. Po přerušení léčby se hladina vápníku v séru normalizuje. Pokud dávka přípravku Enstilar nepřekračuje maximální denní dávku (15 g), je riziko hyperkalcemie minimální. (viz bod 4.2).
Místní nežádoucí účinky
Enstilar obsahuje silný steroid skupiny III, a proto se musí vyloučit současná léčba jinými steroidy ve stejné ošetřované oblasti.
Kůže obličeje a genitálií je velmi citlivá na kortikosteroidy. Tento léčivý přípravek se nemá na tyto oblasti používat.
Pacient musí být poučen o správném použití léčivého přípravku, aby se vyhýbal aplikaci a náhodnému přenosu na obličej, do úst a do očí. Aby se zabránilo náhodnému zanesení do těchto míst, je nutné si po každé aplikaci umýt ruce.
Souběžné infekce kůže
Pokud jsou léze sekundárně infikovány, je nutno je léčit antibiotiky. Zhorší-li se však infekce, léčbu kortikosteroidy je nutno ukončit (viz bod 4.3).
Přerušení léčby
Při léčbě psoriázy topickými kortikosteroidy existuje po přerušení léčby riziko generalizované pustulózní psoriázy nebo rebound fenoménu. Lékařský dohled má proto pokračovat i po přerušení léčby.
Dlouhodobé použití
Při dlouhodobé léčbě je zvýšené riziko lokálních a systémových nežádoucích účinků kortikosteroidů. V případě nežádoucích účinků spojovaných s dlouhodobou léčbou kortikosteroidy se má léčba přerušit (viz bod 4.8).
Nehodnocené použití
Neexistují zkušenosti s použitím přípravku Enstilar u kapkovité psoriázy.
Expozice UV záření
Během léčby přípravkem Enstilar se doporučuje lékařům, aby pacientům doporučili vyhýbat se nadměrné expozici přirozenému nebo umělému slunečnímu záření. Topický kalcipotriol se má používat s UV zářením pouze v případě, že lékař ve spolupráci s pacientem rozhodne, že potenciální přínosy převáží potenciální rizika (viz bod 5.3).
Nežádoucí reakce na pomocnou látku
Enstilar obsahuje pomocnou látku butylhydroxytoluen (E321), který může způsobit místní kožní reakce (např. kontaktní dermatitidu), nebo podráždění očí a sliznic.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Žádné studie interakcí nebyly s přípravkem Enstilar provedeny.
4.6 Fertilita, těhotenství a kojení
O použití přípravku Enstilar u těhotných žen není dostatek údajů. Při perorálním podávání u zvířat studie neodhalily teratogenní účinky, avšak objevila se reprodukční toxicita (viz bod 5.3). Studie s glukokortikoidy na zvířatech ukázaly reprodukční toxicitu (viz bod 5.3), ale řada epidemiologických studií (méně než 300 ukončených těhotenství) neodhalila vrozené anomálie u dětí narozených ženám léčených kortikosteroidy během těhotenství. Potenciální riziko pro člověka není jisté. Proto se Enstilar může používat během těhotenství pouze, pokud očekávaný přínos vyváží případné riziko.
Kojení
Betamethason přechází do mateřského mléka, nicméně riziko nežádoucích účinků u dítěte se při terapeutických dávkách zdá být nepravděpodobné. O vylučování kalcipotriolu do mateřského mléka nejsou žádné údaje. Při předepisování přípravku Enstilar kojícím ženám je zapotřebí opatrnosti. Pacientka má být upozorněna, že během kojení nemá aplikovat Enstilar na pokožku prsou.
Fertilita
Studie účinku perorálního podávání kalcipotriolu nebo betamethason-dipropionátu potkanům neprokázaly poškození samčí či samičí fertility (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Enstilar nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Odhad četností výskytu nežádoucích účinků je založen na souhrnné analýze údajů z klinických studií.
Nejčastěji hlášeným nežádoucím účinkem při léčbě jsou reakce v místě aplikace.
Nežádoucí účinky jsou uvedeny podle MedDRA tříd orgánových systémů (SOC) a jednotlivé nežádoucí účinky jsou uvedeny počínaje nejčastěji hlášenými. V rámci každé skupiny četnosti se nežádoucí účinky uvádějí v pořadí podle klesající závažnosti.
Velmi časté (> 1/10)
Časté (> 1/100 až < 1/10)
Méně časté (> 1/1 000 až < 1/100)
Vzácné (> 1/10 000 až < 1/1 000)
Velmi vzácné (< 1/10 000)
Není známo (z dostupných údajů nelze určit)
|
Infekce a manifestace | |
|
Méně časté > 1/1 000 až < 1/100 |
folikulitida |
|
Poruchy imunitního systému | |
|
Vzácné > 1/10 000 až < 1/1 000 |
hypersenzitivita |
|
Poruchy metabolismu a výživy | |
|
Méně časté > 1/1 000 až < 1/100 |
hyperkalcemie* |
|
Poruchy kůže a podkožní tkáně | |
|
Méně časté > 1/1 000 až < 1/100 |
kožní hypopigmentace |
|
Není známo |
změny barvy vlasů** |
|
Celkové poruchy a reakce v místě aplikace | |
|
Méně časté > 1/1 000 až < 1/100 |
rebound fenomén svědění v místě aplikace podráždění v místě aplikace |
Byla pozorována mírná hyperkalcemie.
** U kombinovaných přípravků s obsahem kalcipotriolu a betamethasonu bylo hlášeno přechodné zbarvení bílých a šedivých vlasů dožluta v místě aplikace.
Následující nežádoucí účinky jsou považovány za související s farmakologickou třídou kalcipotriolu a betamethasonu:
Kalcipotriol:
Nežádoucí účinky zahrnují reakce v místě aplikace, pruritus, podráždění kůže, pocit pálení a píchání, suchou kůži, erytém, vyrážku, dermatitidu, zhoršení psoriázy, fotosenzitivitu a hypersenzitivní reakce včetně velmi vzácných případů angioedému a faciálního edému.
Po topickém podání se mohou velmi vzácně rozvinout systémové účinky způsobující hyperkalcemii nebo hyperkalciurii (viz. bod 4.4).
Betamethason (jako dipropionát):
Po topickém podání, zejména při dlouhodobém používání, se mohou vyskytnout lokální reakce včetně atrofie kůže, teleangiektazie, strií, folikulitidy, hypertrichózy, periorální dermatitidy, alergické kontaktní dermatitidy, depigmentace a koloidních milií.
Při léčbě psoriázy lokálními kortikosteroidy existuje riziko vzniku generalizované pustulózní psoriázy.
Systémové reakce po topickém použití kortikosteroidů j sou u dospělých vzácné, avšak mohou být závažné. Zejména po dlouhodobé léčbě se může vyskytnout adrenokortikální suprese, katarakta, infekce, poruchy kompenzace diabetů mellitu a zvýšení nitroočního tlaku. Systémové reakce se vyskytují častěji při aplikaci pod okluzi (plastová fólie, kožní záhyby), při aplikaci na velké plochy a při dlouhodobé léčbě (viz bod 4.4).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek.
4.9 Předávkování
Používání vyšších než doporučených dávek může způsobit zvýšení hladiny vápníku v séru, která se upraví po přerušení léčby. Symptomy hyperkalcemie zahrnují polyurii, zácpu, svalovou slabost, zmatenost a kóma.
Rozsáhlé dlouhodobé používání topických kortikosteroidů může vést k adrenokortikální supresi, která je obvykle reverzibilní. V těchto případech může být indikována symptomatická léčba.
V případě chronické toxicity se musí léčba kortikosteroidy ukončovat postupně.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antipsoriatika, jiná antipsoriatika k lokální aplikaci, kalcipotriol, kombinace.
ATC kód: D05AX52
Mechanismus účinku
Enstilar kožní pěna kombinuje farmakologický účinek kalcipotriol-hydrátu jakožto syntetického analogu vitaminu D3 a betamethason-dipropionátu jakožto syntetického kortikosteroidu.
Účinek vitaminu D a jeho analog u psoriázy spočívá zejména v potlačení proliferace keratinocytů a indukci diferenciace keratocytů. Základní antiproliferativní mechanismus vitaminu D v keratinocytech zahrnuje indukci faktoru inhibice růstu transformující růstového faktoru TGF-P a inhibitorů cyklin-dependentní kináz s následným pozastavením růstu ve fázi G1 buněčného cyklu a „down“ regulace dvou proliferačních faktorů časné růstové odpovědi egr-1 a polo-like kinázy PLK-2.
Navíc má vitamin D imunomodulační účinek, potlačuje aktivaci a diferenciaci Th17/Th1 buněk zatímco indukuje odpověď Th2/Treg.
U psoriázy kortikosteroidy potlačují imunitní odpověď, zejména prozánětlivých cytokinů a chemokinů, a tím inhibují aktivaci T buněk. Na molekulární úrovni kortikosteroidy působí prostřednictvím intracelulárního receptoru pro glukokortikoidy a působí protizánětlivě díky transrepresi prozánětlivých transkripčních faktorů jako je nukleární faktor kB, aktivační protein AP-1, a interferon regulující faktor IRF-3.
Kombinací kalcipotriol-monohydrátu a betamethason-dipropionátu je dosažen vyšší protizánětlivý a antiproliferativní efekt než u jednotlivých látek.
Farmakodynamické účinky
U pacientů s rozsáhlou psoriázou na těle a v kapiliciu, kteří byli léčeni maximálními dávkami po dobu až 4 týdnů, byla odpověď nadledvin na ACTH stanovena měřením hladiny sérového kortizolu. Žádný z 35 pacientů neměl snížené hladiny sérového kortizolu 30 nebo 60 minut po ACTH stimulaci. Proto se zdá, že riziko adrenální suprese při používání přípravku Enstilar u rozsáhlé psoriasis vulgaris po dobu 4 týdnů je nízké. Stejně tak nebyly zaznamenány žádné abnormality metabolismu vápníku při používání přípravku Enstilar v léčbě rozsáhlé psoriasis vulgaris po dobu 4 týdnů.
Klinická, účinnost
Účinnost přípravku Enstilar při aplikaci jednou denně byla sledována ve třech randomizovaných, dvojitě zaslepených nebo trojitě zaslepených, čtyřtýdenních klinických studiích zahrnujících více než 1 100 subjektů s alespoň mírnou formou psoriázy (stanoveno dle Physician’s Global Assessment of disease severity (PGA) na těle (a též kapiliciu ve Studii 2), postihující alespoň 2 % plochy těla (body surface area-BSA) s modifikovaným indexem PASI - Psoriasis Area Severity Index (m-PASI) nejméně 2. Globální hodnocení lékaře vychází z 5bodové škály (nepřítomné, téměř nepřítomné, mírné, středně závažné a závažné) založené na průměrné psoriatrické lézi. Skóre m-PASI je skóre složené z hodnocení závažnosti (erytém, šupiny, indurace) a lokalizace ploch (vyjma obličeje a kožních záhybů).
Počet pacientů v každé ze tří studií a počet pacientů randomizovaných v každé léčebné skupině je uveden v tabulkách níže.
Primárním parametrem účinnosti (primární endpoint) byli pacienti s „úspěšnou léčbou“ („nepřítomné“ nebo „téměř nepřítomné“ u pacientů s alespoň středně závažným onemocněním, „nepřítomné“ u pacientů s mírným onemocněním ze začátku sledování) podle PGA v týdnu 4.
Charakteristiky onemocnění na počátku sledování
|
Studie 1 (N=426) |
Studie 2 (N=302) |
Studie 3 (N=376) | |
|
Počáteční závažnost onemocnění (PGA): Mírné Středně závažné Závažné |
65 (15,3 %) 319 (74,9 %) 42 (9,9 %) |
41 (13,6 %) 230 (76,2 %) 31 (10,3 %) |
63 (16,8 %) 292 (77,7 %) 21 (5,6 %) |
|
Střední hodnota BSA (rozmezí) |
7,5% (2-30 %) |
7,1% (2-28 %) |
7,5% (2-30 %) |
|
Střední hodnota m-PASI (rozmezí) |
7,5 (2,0-47,0) |
7,6 (2,0-28,0) |
6,8 (2,0-22,6) |
Procento pacientů s „úspěšnou léčbou“ (podle PGA) na těle v týdnu 4
|
Enstilar |
Vehikulum pěna |
Betamethason -dipropionát v pěnovém vehikulu |
Kalcipotriol v pěnovém vehikulu |
Daivobet mast |
Vehikulum mast | |
|
Studie 1 |
(N=323) 53,3 % |
(N=103) 4,8 % | ||||
|
Studie 2 |
(N=100) 45,0 % |
(N=101) 30,7 % |
(N=101) 14,9 % | |||
|
Studie 3 |
(N=141) 54,6 % |
(N=49) 6,1 % |
(N=135) 43,0 % |
(N=51) 7,8 % |
Výsledky pro primární endpoint „úspěšná léčba“ (PGA) těla v týdnu 4 ukázaly, že přípravek Enstilar je statisticky významně účinnější než všechny srovnávané přípravky a odpovědi byly zaznamenány ve všech kategoriích závažnosti onemocnění.
Ve Studii 2 byl zkoumán účinek přípravku Enstilar na psoriázu v kapiliciu jako procento pacientů s „úspěšnou léčbou“ podle PGA v kapiliciu v týdnu 4.
Procento pacientů s „úspěšnou léčbou“ (podle PGA) v kapiliciu v týdnu 4
|
Enstilar |
Betamethason- |
Kalcipotriol | |
|
dipropionát |
v pěnovém vehikulu | ||
|
v pěnovém vehikulu | |||
|
Studie 2 |
(N=100) |
(N=100) |
(N=101) |
|
53,0 % |
47,5 % |
35,6 % |
Enstilar byl statisticky významně účinnější ve srovnání s kalcipotriolem a byl také spojený s vyšší účinností léčby než betamethason-dipropionát, ale srovnání s ním nebylo statisticky významné.
Účinek přípravku Enstilar na svědění a spánek ovlivněný svěděním byl sledován ve Studii 1 s použitím vizuální analogové škály (VAS) v rozmezí od 0 mm (žádné svědění/žádná ztráta spánku z důvodu svědění) až 100 mm (nejhorší svědění, jaké si lze představit/největší možná ztráta spánku). Statisticky významný vyšší počet pacientů ve skupině léčené přípravkem Enstilar dosáhlo 70% snížení svědění a ztráty spánku v souvislosti se svěděním v porovnání s vehikulem ode dne 3 až po celou dobu léčby.
Procento pacientů, kteří dosáhli alespoň 70% snížení svědění ve srovnání se stavem na počátku léčby ve Studii 1 (pacienti, kteří udávali svědění na začátku léčby)
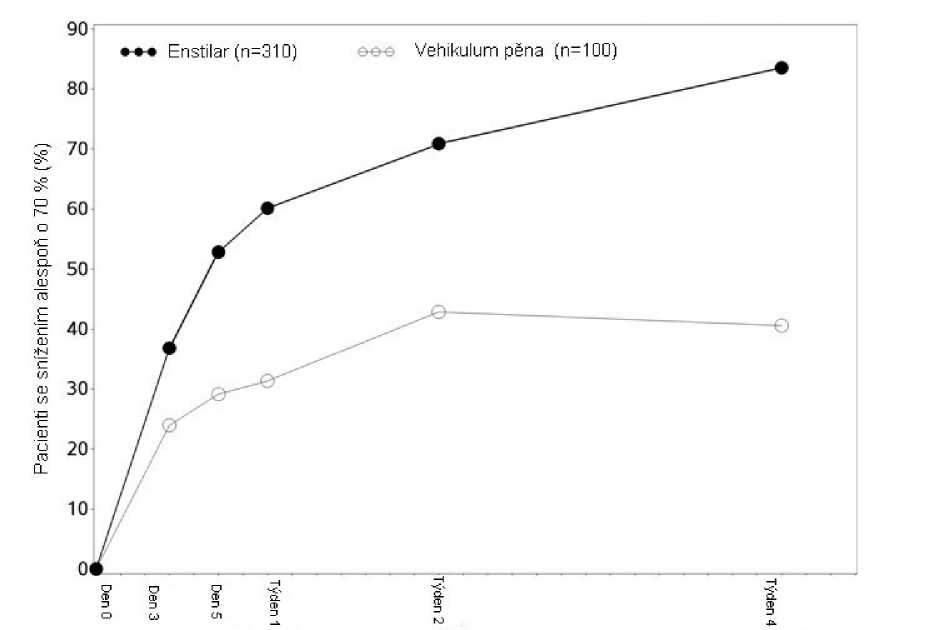
Vliv přípravku Enstilar na kvalitu života byl hodnocen ve Studii 1 za použití obecného dotazníku EQ-5D-5L a dermatologicky specifického dotazníku DLQI. Bylo prokázáno statisticky významné zlepšení
kvality života u přípravku Enstilar ve DLQI od týdnu 1 až po celou dobu léčby a u EQ-5D-5L v týdnu 4.
5.2 Farmakokinetické vlastnosti
Po systémové expozici j sou obě léčivé látky - kalcipotriol a betamethason-dipropionát - rychle a ve velkém rozsahu metabolizovány.
Hlavní cestou vylučování kalcipotriolu je stolice (potkani a miniprasata) a u betamethason-dipropionátu je to moč (potkani a myši). U potkanů ukázaly studie tkáňové distribuce s radioaktivně značeným kalcipotriolem a betamethason-dipropionátem, že ledviny a játra vykazují nejvyšší hodnoty radioaktivity.
Rozsah perkutánní absorpce dvou léčivých látek po lokální aplikaci přípravku Enstilar byl hodnocen ve studii osy hypothalamus-hypofýza-nadledviny u subjektů s rozsáhlým postižením psoriasis vulgaris (viz bod 5.1). Kalcipotriol a betamethason-dipropionát byly pod dolní hranicí měřitelnosti u většiny vzorků 35 pacientů, u kterých byla jednou denně léčena rozsáhlá psoriáza postihující tělo a kapilicium. Kalcipotriol byl měřitelný v určitém časovém období u jednoho pacienta, betamethason-dipropionát u 5 pacientů a metabolity kalcipotriolu byly detekovatelné u tří pacientů a metabolity betamethason-dipropionátu u 27 pacientů.
5.3 Předklinické údaje vztahující se k bezpečnosti
Studie s kortikosteroidy na zvířatech vykazovaly reprodukční toxicitu (rozštěp patra, malformace kostry). Ve studiích reprodukční toxicity při dlouhodobém perorálním podávání kortikosteroidů potkanům byla zjištěná prodloužená březost a prodloužený a těžký porod. Navíc byl pozorován pokles přežívání potomstva, snížení tělesné hmotnosti a nižší přírůstek tělesné hmotnosti. Nedošlo k žádnému snížení fertility. Význam pro člověka není znám.
Kalcipotriol vykazoval maternální a fetální toxicitu u potkanů a králíků při podávání perorálních dávek 54 pg/kg/den resp. 12 pg/kg/den. Fetální abnormality pozorované u současné maternální toxicity zahrnovaly známky nedostatečné skeletální vyspělosti (neúplná osifikace pubických kostí a článků prstů předních končetin, zvětšená fontanela) a zvýšený výskyt nadpočetných žeber.
Odhadovaná systémová expozice po topickém podání přípravku Enstilar pacientům s psoriázou je zanedbatelná ve srovnání s koncentracemi kalcipotriolu podaného perorálně ve studiích in vivo a riziko reprodukční toxicity u člověka po expozici terapeutickým dávkám přípravku Enstilar je nepatrné.
Na základě konvenčních studií bezpečnosti, toxicity po opakovaném podání a genotoxicity neklinické údaje neodhalily žádné zvláštní riziko pro člověka.
Studie dermální kancerogenity kalcipotriolu u myší a perorální kancerogenity u potkanů neodhalila žádné zvláštní riziko pro člověka.
Studie foto(ko)kancerogenity na myších naznačují, že kalcipotriol může posílit účinek UV záření na tvorbu kožních nádorů.
Studie dermální kancerogenity u myší a perorální kancerogenity u potkanů neodhalila žádné zvláštní riziko betamethason-dipropionátu pro člověka.
Enstilar způsobil mírnou až středně závažnou iritaci kůže ve studii lokální snášenlivosti u miniprasat.
FARMACEUTICKÉ ÚDAJE
6.
6.1 Seznam pomocných látek
tekutý parafín
stearopolypropylenglykol 1125
tokoferol-alfa
bílá vazelína
butylhydroxytoluen (E321) butan
methyl-ether
6.2 Inkompatibility Neuplatňuje se.
6.3 Doba použitelnosti
2 roky
Po prvním otevření: 6 měsíců.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 30 °C.
Varování:
Extrémně hořlavý aerosol.
Tlaková nádobka: může se roztrhnout, pokud je vystavena horku.
Chraňte před slunečním zářením.
Nevystavujte teplotám nad 50 °C.
Nepropichujte nebo nepalte ani po vyprázdnění.
Nestříkejte do otevřeného ohně nebo jiného zdroje vznícení.
Neuchovávejte v blízkosti vzniku jisker, otevřeného ohně nebo jiného zdroje vznícení.
V blízkosti nádobky nekuřte.
6.5 Druh obalu a obsah balení
Hliníková nádobka s vnitřní stranou potaženou polyamid-imidovým lakem, opatřená kontinuálním ventilem a aplikátorem. Nádobka obsahuje 60 g pěny, nejsou zahrnuty hnací plyny.
Velikost balení: 60 g, 2x 60 g.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
LEO Pharma A/S Industriparken 55 DK-2750 Ballerup Dánsko
8. REGISTRAČNÍ ČÍSLO(A) 46/254/16-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
8.6.2016
10. DATUM REVIZE TEXTU 8.6.2016
10