Britaject Pen 10 Mg/Ml Injekční Roztok
Sp. zn. sukls138274/2015
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Britaject PEN 10 mg/ml injekční roztok *
* V textu zkráceno jako Britaject Pen
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml obsahuje 10 mg apomorfini hydrochloridum hemihydricum
Jedna 3 ml zásobní vložka obsahuje 30 mg apomorfini hydrochloridum hemihydricum.
Pomocné látky: hydrogensiřičitan sodný 0,93 mg v ml Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční roztok.
Roztok je čirý, prakticky bezbarvý, bez zápachu a bez viditelných částic. pH = 3,0 až 4,0
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Léčba motorických fluktuací (fenomén „on-off‘) u pacientů s Parkinsonovou chorobou, u kterých není tato choroba dostatečně pod kontrolou díky lékařským přípravkům určeným k léčbě Parkinsonovy choroby.
4.2 Dávkování a způsob podání
Volba pacientů vhodných pro injekce perem Britaject PEN:_
Pacienti zvolení pro léčbu perem Bitaject PEN by měli být schopni rozpoznat vznik svých „off" příznaků a měli by být schopni si dle potřeby sami aplikovat injekci nebo by ji měl aplikovat jejich ošetřovatel.
Je nezbytné, aby pacient dostával domperidon, obvykle 20 mg třikrát denně, po dobu alespoň dva dny před zahájením léčby.
Podávání apomorfinu by se mělo zahájit pod kontrolou odborné ambulance. Pacienty by měl vést lékař se zkušenostmi s léčbou Parkinsonovy choroby (např. neurolog). Léčba pacienta s levodopou, s nebo bez agonistů dopaminu, by se měla optimalizovat před zahájením léčby pomocí pera Britaject.
Dospělí
Podávání
Britaject PEN 10 mg/ml injekční roztok je určený pro subkutánní podání pomocí intermitentní bolusové injekce.
Apomorfin se nesmí používat intravenózní cestou.
Nepoužívejte, pokud roztok zezelenal. Roztok před použitím vizuálně zkontrolujte. Použijte pouze čirý, bezbarvý roztok bez viditelných pevných částic.
Stanovení prahové dávky
Odpovídající dávka pro každého pacienta je stanovena pomocí dávkovacího schématu s narůstající dávkou. Doporučuje se následující plán: -
1 mg apomorfin hydrochloridu (0,1 ml), což je asi 15 - 20 mikrogramů/kg, je možné injikovat podkožně během hypokinetického neboli „off“ období a pacient je sledován po dobu 30 minut s ohledem na motorickou odpověď.
Pokud není získána žádná odpověď nebo neadekvátní odpověď, je vstříknuta druhá dávka
2 mg apomorfin hydrochloridu (0,2 ml) subkutánně a pacient je sledován s ohledem na adekvátní odpověď po dobu dalších 30 minut.
Dávka se může zvýšit narůstající injekcí s minimálně čtyřicetiminutovým intervalem mezi následujícími injekcemi, do dosažení uspokojivé motorické odpovědi.
Zavedení léčby
Po určení vhodné dávky je možné podat jednu subkutánní injekci do dolní části břicha nebo zevní části stehna při prvních známkách epizody „off“. Není možné vyloučit, že se může u různých injekčních míst u jednoho jedince vstřebávání lišit. Pacienta je pak třeba odpovídajícím způsobem sledovat po dobu další hodiny, aby se zhodnotila kvalita jejich odpovědi na léčbu. Změna dávky může být uskutečněna dle odpovědi pacienta.
Optimální dávka apomorfin hydrochloridu se liší mezi jedinci, ale jakmile je stanovena, zůstává relativně konstantní pro každého pacienta.
Opatření týkající se trvalé léčby
Denní dávka přípravku Britaject PEN se liší výrazně mezi pacienty, typicky v rozmezí od 3 do 30 mg, podané jako 1 - 10 injekcí a někdy až jako 12 samostatných injekcí denně.
Doporučuje se, aby celková denní dávka apomorfin hydrochloridu nepřevyšovala 100 mg a jednotlivý bolus by neměl převyšovat 10 mg.
V klinických studiích bylo obvykle možné provést určité snížení dávky levodopy. Tento účinek se liší výrazně mezi pacienty a je třeba ho opatrně řídit zkušeným lékařem.
Jakmile byla léčba zavedena, může být u některých pacientů dávka domperidonu postupně snižována, ale úspěšně vysazena pouze u několika pacientů bez jakéhokoliv zvracení nebo hypotenze.
Děti a adolescenti:
Britaject PEN 10 mg/ml injekční roztok je kontraindikován u dětí a adolescentů ve věku pod 18 let (viz bod 4.3).
Starší lidé:
Starší lidé jsou dobře zastoupeni v populaci pacientů s Parkinsonovou chorobou a představují vysoký podíl studovaných subjektů v klinických studiích přípravku Britaject PEN. Léčba starších pacientů s přípravkem Britaject PEN se nelišila od léčby mladších pacientů. Při léčbě starších pacientů je ale doporučeno věnovat zvýšenou pozornost počáteční fázi léčby, protože zde existuje riziko vzniku posturální hypotenze.
Porucha ledvin:
Plán dávkování podobný plánu doporučenému pro dospělé a starší osoby je možné používat pro léčbu pacientů s poruchou ledvin (viz bod 4.4).
4.3 Kontraindikace
U pacientů s respirační depresí, demencí, psychotickými chorobami nebo jaterní insuficiencí.
Léčba apomorfin hydrochloridem nesmí být podávána pacientům, kteří mají „on“ odpověď na levodopu, která je charakterizována těžkou dyskinezí nebo dystonií.
Britajec PEN by se neměl podávat pacientům, kteří mají známou hypersenzitivitu na apomorfin nebo jakékoliv pomocné látky v léčivém přípravku.
Britaject PEN je kontraindikován u dětí a adolescentů ve věku pod 18 let.
4.4 Zvláštní upozornění a opatření pro použití
Apomorfin hydrochlorid by se měl podávat s opatrností pacientům s renální, plicní nebo kardiovaskulární chorobou a osobám, které jsou náchylné ke vzniku nevolnosti a zvracení.
Zvláštní opatrnost je doporučena během zahájení léčby u starších anebo oslabených pacientů.
Vzhledem k tomu, že může apomorfin způsobovat hypotenzi, dokonce i když se podává s domperidonem, je třeba opatrnosti u pacientů s preexistujícím srdečním onemocněním nebo u pacientů, kteří užívají léčivé přípravky, jako jsou antihypertenziva, zejména u pacientů s preexistující posturální hypotenzí.
Vzhledem k tomu, že apomorfin, zejména ve vysoké dávce, může mít potenciální vliv na prodloužení QT intervalu, je třeba opatrnosti při léčbě pacientů ohrožených arytmií torsades de pointes.
Apomorfin je spojen s lokálními podkožními účinky. Tyto je možné někdy snížit změnou injekčních míst nebo případně použitím ultrazvuku (pokud je k dispozici) na oblasti nodularity a indurace.
U pacientů léčených apomorfinem byly hlášené hemolytické anémie a trombocytopénie. Pravidelně je třeba provádět hematologické testy, jako například u levodopy, při současném podávání s apomorfinem.
Je třeba opatrnosti při kombinaci apomorfinu s dalšími léčivými přípravky, zejména s těmi s úzkým terapeutickým rozmezím (viz bod 4.5).
U mnoha pacientů s Parkinsonovou chorobou koexistují neuropsychiatrické problémy. Existují důkazy, že u některých pacientů mohou být neuropsychiatrické poruchy zhoršené apomorfinem.
Je třeba zvláštní opatrnosti při použití apomorfinu u těchto pacientů.
Apomorfin byl spojován se somnolencí a jiní agonisté dopaminu mohou být spojeni s náhlým vznikem epizod spánku, zejména u pacientů s Parkinsonovou chorobou. Pacienti musí být o tom informováni a je třeba je poučit, aby dbali při řízení nebo obsluze strojů během léčby apomorfinem opatrnosti. Pacienti, u nichž došlo k somnolenci, nesmí řídit nebo obsluhovat stroje. Dále je možné zvážit snížení dávky nebo ukončení léčby.
Poruchy kontroly impulzů (Impulse control disorder, ICD)
Pacienti by měli být pravidelně monitorováni z důvodu možnosti rozvoje poruch kontroly impulzů. Pacienti a jejich ošetřovatelé by měli být upozorněni, že u pacientů léčených agonisty dopaminu včetně apomorfinu se mohou objevit symptomy ICD včetně patologického hráčství, zvýšeného libida, hypersexuality, nutkavého utrácení nebo nakupování, záchvatovitého a nutkavého přejídání. Pokud se tyto příznaky objeví, mělo by se zvážit snížení dávky nebo postupné vysazení přípravku.
Britaject PEN 10 mg/ml injekční roztok obsahuje hydrogensiřičitan sodný, který může vzácně způsobovat těžké alergické reakce a bronchospasmus.
Tento léčivý přípravek obsahuje méně než 1 mmol sodíku (23mg) ve 10 ml, tj. v podstatě „bez sodíku“.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Pacienti zvolení pro léčbu apomorfin hydrochloridem téměř s jistotou užívají souběžnou léčbu pro svou Parkinsonovu chorobu. V iniciálních stádiích terapie apomorfin hydrochloridem by měli být pacienti monitorováni vzhledem k neobvyklým nežádoucím účinkům nebo příznakům potenciace účinku.
Neuroleptické léčivé přípravky mohou mít antagonistický účinek, pokud se používají s apomorfinem. Existuje potenciální interakce mezi klozapinem a apomorfinem, nicméně klozapin může být používán také k redukci příznaků neuropsychiatrických komplikací.
Možné účinky apomorfinu na plazmatické koncentrace jiných léků nebyly studovány. Proto je třeba opatrnosti při kombinaci apomorfinu s dalšími léčivými přípravky, zejména s těmi s úzkým terapeutickým rozmezím.
Antihypertenzivní a kardioaktivní léčivé přípravky
I když se podávají spolu s domperidonem, apomorfin může potenciovat antihypertenzivní účinky těchto léků. (Viz bod 4.4).
Doporučuje se nepodávat apomorfin s jinými léky, o nichž je známo, že prodlužují QT interval.
4.6 Těhotenství a kojení
Neexistují zkušenosti s použitím apomorfinu u těhotných žen.
Reprodukční studie u zvířat neukazují žádné teratogenní účinky, ale dávky podané potkanům, které jsou toxické pro matku, mohou vést k selhání dýchání u novorozence. Potenciální riziko pro člověka není známo. Viz bod 5.3
Britaject PEN by se neměl používat během těhotenství, pokud to není jednoznačně nutné.
Není známo, je-li apomorfin vylučován do lidského mléka. Rozhodnutí, zda pokračovat či přestat s kojením nebo pokračovat či přestat s terapií přípravkem Britaject PEN je třeba provést se zohledněním přínosu kojení pro dítě a přínosu terapie přípravkem Britaject PEN pro ženu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Apomorfin HCl má malý nebo mírný vliv na schopnost řídit a obsluhovat stroje.
Pacienti léčení apomorfmem, kteří trpí somnolencí anebo epizodami náhlého spánku, musí být informováni o tom, že nemají řídit nebo se zapojovat do aktivit (například obsluhy strojů), kde může porucha pozornosti vystavovat je nebo jiné riziku závažného poškození nebo smrti, pokud pacienti takové recidivující potíže a somnolenci nepřekonají (viz bod 4.4).
4.8 Nežádoucí účinky
Velmi časté (>1/10)
Časté (>1/100 až < 1/10)
Méně časté (>1/1000 až <1/100)
Vzácné (>1/10000 až <1/1000)
Velmi vzácné (<1/10 000)
Neznámé (není možné odhadnout z dostupných údajů).
Poruchy krve a lymfatického systému
Méně časté:
U pacientů léčených apomorfinem byly hlášené hemolytická anémie a trombocytopénie. Vzácné:
Během léčby apomorfin hydrochloridem se vzácně objevila eosinofilie.
Poruchy imunitního systému
Vzácné:
V důsledku přítomnosti disiřičitanu sodného se mohou objevit alergické reakce (zahrnující anafylaxi a bronchospasmus).
Psychiatrické poruchy
Časté:
Neuropsychiatrické poruchy jsou časté u pacientů s parkinsonismem. Britaject PEN by se měl u těchto pacientů používat se zvláštní opatrností. Během terapie apomorfin hydrochloridem se objevily neuropsychiatrické poruchy (zahrnující přechodnou mírnou zmatenost a zrakové halucinace).
Neznámé:
Poruchy kontroly impulzů
U pacientů léčených agonisty dopaminu včetně apomorfinu se mohou objevit symptomy jako patologické hráčství, zvýšené libido, hypersexualita, nutkavé utrácení nebo nakupování a záchvatovité a nutkavé přejídání (viz bod 4.4).
Poruchy nervového systému
Časté:
Na začátku léčby se může objevit přechodná sedace s každou dávkou apomorfin hydrochloridu, která obvykle ustupuje během prvních několika týdnů.
Apomorfin je spojen se somnolencí.
Také byly hlášeny závratě nebo motání hlavy.
Méně časté:
Apomorfin může vyvolávat dyskineze během období „on", které mohou být v některých případech závažné a u několika pacientů mohou vést k ukončení terapie.
Apomorfin je spojována s epizodami náhlého nástupu spánku. Viz také bod 4.4.
Cévní poruchy
Méně časté:
Posturální hypotenze je zaznamenávána vzácně a obvykle je přechodná (viz bod 4.4).
Respirační, hrudní a mediastinální poruchy
Časté:
Během léčby apomorfinem bylo pozorováno zívání.
Méně časté:
Byly hlášeny potíže s dýcháním.
Gastrointestinální poruchy
Časté:
Nevolnost a zvracení, zejména při prvním zahájení léčby apomorfinem, obvykle jako důsledek vynechání domperidonu (viz bod 4.2).
Poruchy kůže a podkožní tkáně
Méně časté:
Byly hlášeny místní a generalizované vyrážky.
Celkové poruchy a reakce v místě aplikace
Velmi časté:
U většiny pacientů se vyskytují reakce v místě injekce, zejména při trvalém použití. Tyto mohou zahrnovat podkožní uzlíky, induraci, erytém, citlivost a panniculitis. Také se mohou vyskytnout různé další místní reakce (jako je podráždění, svědění, modřiny a bolesti).
Méně časté:
Byly hlášeny nekrózy v místě injekce a ulcerace.
Neznámé:
Byl hlášen periferní edém.
Vyšetření
Méně časté:
U pacientů, kteří dostávali apomorfin, byl hlášen výskyt pozitivního Coombsova testu.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
4.9 Předávkování
Je k dispozici málo klinických zkušeností s předávkováním apomorfinem touto cestou. Příznaky předávkování je možné léčit empiricky, jak je naznačeno níže:
Nadměrné zvracení je možné léčit domperidonem.
Depresi dýchání je možné léčit naloxonem.
Hypotenze: Je třeba využít odpovídající opatření, například zvednutí nohou postele v místě dolních končetin.
Bradykardii je možné léčit atropinem.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Agonisté dopaminu ATC klasifikace: N04B C07
Apomorfin je přímý stimulans dopaminových receptorů a zatímco má agonistické účinky na D1 i D2 receptory, nesdílí transportní nebo metabolické cesty s levodopou.
I když u intaktních experimentálních zvířat potlačuje podání apomorfinu rychlost výbojů nigro-striatálních buněk a u nízké dávky byla pozorována redukce lokomoční aktivity (během současné presynaptické inhibice uvolňování endogenního dopaminu) jeho účinky na parkinsonskou motorickou poruchu jsou pravděpodobně zprostředkovány na postsynaptické receptorové úrovni. Tento bifázický účinek byl také pozorován u člověka.
5.2 Farmakokinetické vlastnosti
Po subkutánní injekci apomorfinu je možné jeho cestu popsat pomocí dvojkompartmentového modelu, s distribučním poločasem 5 (± 1,1) minut a poločasem eliminace 33 (± 3,9) minut. Klinická odpověď koreluje dobře s hladinami apomorfinu v cerebrospinální tekutině. Distribuce léku je nejlépe popsána pomocí dvojkompartmentového modelu. Apomorfin se rychle a kompletně vstřebává z podkožní tkáně, koreluje s rychlým vznikem klinických účinků (4 - 12 minut) a krátké trvání klinického účinku léku (asi 1 hodina) je vysvětleno jeho rychlou clearance. Metabolismus apomorfinu probíhá prostřednictvím glukuronidace a sulfonace u minimálně deseti procent celkového množství. Jiné cesty nebyly popsány.
5.3 Předklinické údaje vztahující se k bezpečnosti
Studie toxicity opakované subkutánní dávky neukazují žádné zvláštní riziko pro člověka mimo informací uvedených v ostatních částech tohoto SPC.
Studie genotoxicity in vitro ukázaly mutagenní a klastogenní účinky, nejpravděpodobněji v důsledku produktů, které vznikají oxidací apomorfinu. Nicméně apomorfin nebyl genotoxický v provedených studiích in vivo.
Účinek apomorfinu na reprodukci byl hodnocen u potkanů. Apomorfin nebyl teratogenní u těchto druhů, ale bylo zaznamenáno, že dávky, které jsou toxické pro matku, mohou způsobovat ztrátu mateřské péče a poruchu dýchání novorozence.
Nebyly provedeny žádné studie karcinogenity.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
hydrogensiřičitan sodný (E222)_
Kyselina chlorovodíková (37%), koncentrovaná
(PRO ÚPRAVU PH NA 3,0 - 4,0)_
Voda na injekci_
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto tento léčivý přípravek nesmí být používán v kombinaci s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
2 roky
48 hodin po prvním otevření.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 25 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před světlem.
Přípravek je třeba uchovávat ve stejných podmínkách po otevření a mezi jednotlivým vytažením.
6.5 Druh obalu a velikost balení
Zásobní vložka
Pero Britaject PEN 10 mg/ml je jednorázové vícedávkové injekční pero se zabudovanou zásobní vložkou z čirého skla (typ I) obsahující čirý injekční roztok. Skleněná zásobní vložka je uzavřena na jednom konci pístem z bromobutylové gumy a na druhém konci bromobutyl/Almembránou.
Jedno pero obsahuje 3 ml injekčního roztoku.
Balení obsahuje 1, 5 nebo 10 x 3 ml pera v tvarované plastové vložce v papírové krabičce.
Na trhu nemusí být všechny velikosti balení.
6.6 Návod pro použití přípravku, zacházení s ním a k jeho likvidaci
Britaject PEN
Nepoužívejte, pokud roztok zezelenal.
Zlikvidujte každé pero nejpozději do 48 hodin po prvním použití.
(viz schéma).

* Toto balení NEOBSAHUJE jehly pro použití s Vaším perem. Používejte jehly do pera, které nejsou kratší než 12mm (%”) a nejsou tenčí než 0,36mm (28 G). Jehly do pera, které jsou doporučené pro použití s inzulinovými pery, jsou kompatibilní s perem Britaject PEN.
JAK SE PERO BRITAJECT PEN POUŽÍVÁ
Pečlivě si přečtěte všechny pokyny.
Důležité: Netahejte za dávkovači kroužek (viz 1) dříve, než nastavíte dávku (viz JAK NASTAVIT SPRÁVNOU DÁVKU)
PŘIPOJENI JEHLY
(a) Před použitím pera budete potřebovat chirurgické tampony a jednu jehlu s ochranným kuželem (viz 2). Vytáhněte pero z krabičky a odstraňte zevní pouzdro (viz

3).
(b) Otřete membránu (viz 4) chirurgickým tamponem.
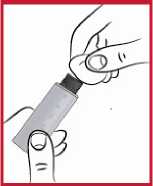
(c) Sloupněte papír z konusu jehly (viz 2) a našroubujte konus po směru chodu hodinových ručiček na membránu. Tím se zajistí upevnění jehly.
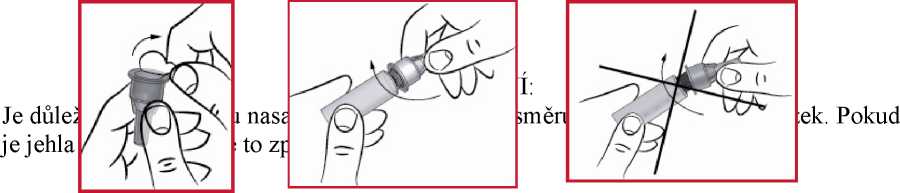
(d) Odstraňte ochranný kužel (viz 5), ale neodhazujte ho. V této fázi neodstraňujte ochranný kryt jehly (viz 6).
|
\ | |
|
\ |
(e) Znovu nasaďte zevní pouzdro pera tviz 3t
(viz schéma).
i otočte po směru chodu hodinových
(f) Stiskněte dávkovací krouže ručiček, dokud šipka nebude ukazovat předepsanou dávku (viz 7, 8). Potom uvolněte tlak na kroužek. Dávka je nyní nastavena a nemusíte ji znovu nastavovat pro následující injekce.
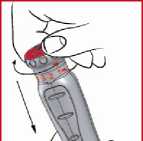
Důležité: Pokud přejdete svou předepsanou dávku při otáčení kroužku, pokračujte v mačkání a otáčení ve stejném směru, dokud na ni nenarazíte znovu. Nikdy netahejte a neotáčejte dávkovacím kroužkem ve stejný okamžik.
Pokud je vaše předepsaná dávka 1 mg, je nezbytné pero „odstříknouť před vpíchnutím první dávky. Proveďte to vyprázdněním první 1 mg dávky do papírového kapesníku a ten vyhoďte. Pokud je první potřebná dávka vyšší než 1 mg, potom není nutné pero „odstřikovať.
INJEKČNÍ APLIKACE
(viz schéma).
(g) Vytáhněte dávkovací kroužek (viz 1) co nejdále. Zkontrolujte červenou stupnici na pístu a vstřikujte pouze, pokud nejvyšší viditelné číslo odpovídá požadované dávce. Nikdy se nesnažte změnit dávku, když je dávkovací kroužek vytažen. V případě chybného nastavení dávky vystříkněte nesprávnou dávku do papírového kapesníku. Poté nastavte správnou dávku tak, jak je popsáno v odstavci „JAK NASTAVIT SPRÁVNOU DÁVKU“.
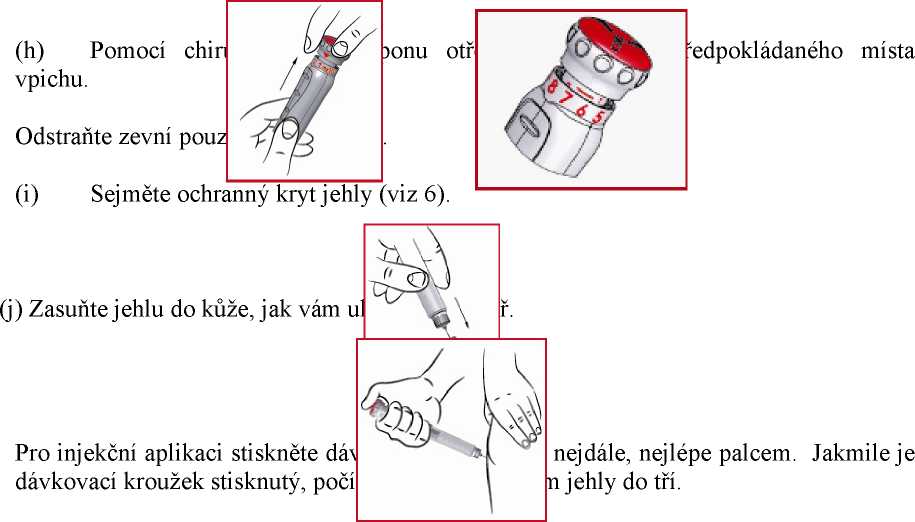
(k) Sejměte a vyhoďte jehlu pomocí ochranného kužele (viz 5). To se provede výměnou ochranného kužele na použité jehle a jemným zatlačením. Jakmile je zajištěná, můžete jehlu odšroubovat proti směru chodu hodinových ručiček. Vyhoďte jehlu na bezpečné místo, například do koše na ostré předměty nebo do prázdné uzavíratelné nádoby (např. od rozpustné kávy).
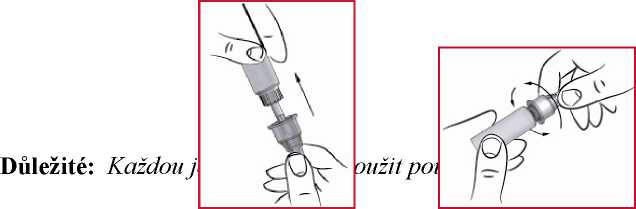
PŘÍPRAVA PRO DALŠÍ INJEKCI:
Zkontrolujte, že v zásobní vložce zbývá dostatek apomorfinu pro další injekci (viz 9). Pokud ano, zasuňte novou jehlu stejným způsobem, jako předtím. (Nezapomeňte si uschovat ochranný kužel).
Pokud není k dispozici dostatek apomorfinu pro další injekci, připravte si další pero. Nakonec na použité pero nasaďte zpátky zevní pouzdro.

7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Britannia Pharmaceuticals Limited,
200 Longwater Avenue, Green Park, Reading, Berkshire, RG2 6GP Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
27/787/11-C
9. DATUM REGISTRACE/PRODLOUŽENÍ REGISTRACE
07.12.2011
10. DATUM REVIZE TEXTU
31.7.2015
14