Zoledronic Acid Ibigen 4 Mg Prášek A Rozpouštědlo Pro Infuzní Roztok
zastaralé informace, vyhledat novějšísp.zn.sukls 223984/2011
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. NÁZEV PŘÍPRAVKU
Zoledronic Acid IBIGEN 4 mg prášek a rozpouštědlo pro infuzní roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna lahvička obsahuje acidum zoledronicum 4 mg, což odpovídá acidum zoledronicum dihemihydricum 4,66 mg.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Prášek a rozpouštědlo pro infuzní roztok Bílý až téměř bílý prášek a čirý, bezbarvý roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
• Prevence kostních příhod (patologických zlomenin, kompresivních zlomenin obratlů, radiační nebo chirurgická léčba kostí nebo cemiehyperkalcemie vyvolaná nádorovým onemocněním) u dospělých pacientů s pokročilým maligním onemocněním postihujícím kosti.
• Léčba dospělých pacientů s hyperkalcemií vyvolanou nádorovým onemocněním (TIH).
4.2 Dávkování a způsob podání
Přípravek Zoledronic acid IBIGEN musí být předpisován a podáván pacientům pouze zdravotnickými pracovníky se zkušenostmi s intravenózní aplikací bisfosfonátů.
Přípravek Zoledronic acid IBIGEN rekonstituovaný roztok nesmí být mísen s infuzními roztoky obsahujícími kalcium nebo jiné bivalentní kationty, jako je laktátový Ringerův roztok, a musí být podáván jako samostatný intravenózní roztok oddělenou infuzní linkou.
Prevence kostních příhod u pacientů s pokročilým maligním onemocněním postihujícím kosti
Dospělí a starší lidé
Doporučená dávka k prevenci kostních příhod u pacientů s pokročilým maligním onemocněním postihujícím kosti je 4 mg rekonstituovaného a dále naředěného infuzního roztoku přípravku Zoledronic Acid IBIGEN (naředěného 100 ml 0,9 % roztoku chloridu sodného nebo 5 % roztoku glukózy) podávaného nejméně 15minutovou intravenózní infuzí každé 3 až 4 týdny.
Pacientům má být také perorálně podán denně doplněk 500 mg kalcia a 400 mj. vitamínu D.
Při rozhodování, zda léčit pacienty s kostními metastázami za účelem prevence kostních příhod, je nutno vzít v úvahu, že se účinky léčby projeví za 2-3 měsíce.
Léčba TIH
Dospělí a starší lidé
Doporučená dávka při léčbě hyperkalcemie (kalcium v séru korigované na albumin > 12,0 mg/dl nebo 3,0 mmol/l) je 4 mg rekonstituovaného a dále naředěného infuzního roztoku přípravku Zoledronic Acid IBIGEN (naředěného 100 ml 0,9 % roztoku chloridu sodného nebo 5 % roztoku glukózy) podaného jednorázovou intravenózní infuzí v trvání nejméně 15 minut. Před podáním a po podání přípravku Zoledronic Acid IBIGEN musí být udržována dobrá hydratace pacienta.
Porucha funkce ledvin
TIH:
U pacientů s TIH trpících současně závažným zhoršením funkce ledvin se smí o léčbě přípravkem Zoledronic acid IBIGEN uvažovat až po zhodnocení rizika a přínosu léčby. Pacienti s hladinou kreatininu v séru > 400 pmol/l nebo > 4,5 mg/dl byli z klinických studií vyloučeni. U pacientů s TIH se sérovým kreatininem > 400 pmol/l nebo > 4,5 mg/dl není nutná úprava dávkování (viz bod 4.4).
Prevence kostních příhod u pacientů s pokročilou formou maligního onemocnění postihujícím kosti:
U pacientů s mnohočetným myelomem nebo metastázami solidních nádorů do kostí musí být při zahájení léčby přípravkem Zoledronic acid IBIGEN stanoven sérový kreatinin a clearance kreatininu (CLcr). CLcr se vypočte ze sérového kreatininu pomocí Cockcroft-Gaultova vzorce. Přípravek Zoledronic acid IBIGEN se nedoporučuje podávat pacientům, kteří již před zahájením léčby trpí závažným poškozením funkce ledvin, které je u této populace definováno jako CLcr < 30 ml/min. Pacienti s hladinou kreatininu v séru > 265 pmol/l nebo > 3,0 mg/dl byli vyloučeni z klinických studií přípravku Zoledronic Acid IBIGEN. U pacientů s kostními metastázami a s mírným nebo středním postižením funkce ledvin před zahájením léčby, které bylo pro tuto skupinu pacientů definováno jako CLcr 30 - 60 ml/min, se doporučuje následující dávkování přípravku Zoledronic acid IBIGEN (viz bod 4.4):
Výchozí hodnoty clearance kreatininu (ml/min) Doporučená dávka* přípravku Zoledronic Acid
IBIGEN
|
> 60 |
4,0 mg |
|
50-60 |
3,5 mg* |
|
40-49 |
3,3 mg* |
|
30-39 |
3,0 mg* |
* Dávky byly vypočteny z předpokládané AUC 0,66 (mg-hod/l) (CLcr = 75 ml/min). Při podávání snížených dávek pacientům se zhoršenou funkcí ledvin je možné očekávat dosažení stejných AUC, jaké byly pozorovány u pacientů s clearance kreatininu 75 ml/min.
Po zahájení léčby musí být stanovován sérový kreatinin před podáním každé dávky přípravku Zoledronic acid IBIGEN a při zhoršení reálních funkcí musí být léčba přerušena. V klinických studiích bylo zhoršení funkcí ledvin definováno následovně:
- U pacientů s normální výchozí hodnotou sérového kreatininu (< 1,4 mg/dl nebo < 124 pmol/l) jako zvýšení o 0,5 mg/dl nebo 44 pmol/l;
- U pacientů s abnormálním výchozími hodnotami sérového kreatininu (> 1,4 mg/dl nebo > 124 pmol/l) jako zvýšení o 1,0 mg/dl nebo 88 pmol/l.
V klinických studiích bylo podávání kyseliny zoledronové znovu zahájeno pouze tehdy, pokud se hodnota kreatininu vrátila do rozmezí 10 % od výchozí hodnoty (viz bod 4.4). Léčba přípravkem
Zoledronic acid IBIGEN má být obnovena stejnou dávkou, která byla podávána před přerušením léčby.
Pediatrická populace
Bezpečnost a účinnost kyseliny zoledronové u dětí ve věku 1 rok až 17 let nebyla stanovena. V současnosti dostupné údaje jsou popsány v bodech 4.4 a 5.1, ale na jejich základě nelze doporučit dávkování u dětí.
Způsob podání
Intravenózní podání
Přípravek Zoledronic acid IBIGEN 4 mg prášek pro infuzní roztok s rozpouštědlem, rekonstituovaný a dále naředěný ve 100 ml (viz bod 6.6) se má podávat jako jednorázová intravenózní infuze po dobu alespoň 15 minut.
U pacientů s mírnou až středně těžkou poruchou funkce ledvin se doporučují snížené dávky přípravku Zoledronic acid IBIGEN (viz bod “Dávkování” výše a bod 6.3).
Instrukce pro přípravu snížených dávek přípravku Zoledronic acid IBIGEN
Odeberte odpovídající objem rekonstituovaného roztoku (4 mg/5ml) dle potřeby:
- 4,4 ml pro dávku 3,5 mg
- 4,1 ml pro dávku 3,3 mg
- 3,8 ml pro dávku 3,0 mg
Informace o rekonstituci a ředění přípravku Zoledronic Acid IBIGEN viz bod 6.6. Odebrané množství rekonstituovaného roztoku musí být dále naředěno ve 100 ml sterilního injekčního roztoku 0,9% chloridu sodného nebo v roztoku 5% glukózy. Dávka musí být podána v jedné intravenózní infuzi po dobu nejméně 15 minut.
Použití kyseliny zoledronové u pediatrických pacientů bylo hodnoceno ve 2 klinických studiích v léčbě závažné osteogenesis imperfecta (viz bod 5.1). Přípravek Zoledronic Acid IBIGEN nemá být používán u pediatrické populace, jelikož bezpečnost a účinnost u dětí nebyla stanovena (viz body 4.4 a 5.1).
Před a po podání přípravku Zoledronic acid IBIGEN musí být pacienti dobře hydratováni.
4.3 Kontraindikace
• Hypersenzitivita na léčivou látku, jiné bisfosfonáty nebo na kteroukoli pomocnou látku v přípravku Zoledronic Acid IBIGEN (viz bod 6.1.)
• Kojení (viz bod 4.6)
4.4 Zvláštní upozornění a opatření pro použití
Obecná
Před podáním přípravku Zoledronic acid IBIGEN musí být posouzen stav hydratace pacientů.
U pacientů s rizikem srdečního selhání je nutno zamezit nadměrnému přísunu tekutin.
Po zahájení terapie Zoledronic acid IBIGEN musí být pečlivě sledovány standardní metabolické parametry související s hyperkalcemií, jako jsou sérové hladiny kalcia, fosfátu a hořčíku. Jestliže se vyskytne hypokalcemie, hypofosfatemie nebo hypomagnesemie, může být nutná krátkodobá substituční léčba. Pacienti s neléčenou hyperkalcemií mají obvykle do jisté míry poškozenou funkci ledvin, proto je nutné uvažovat o pečlivém sledování ledvinných funkcí.
Přípravek Zoledronic Acid IBIGEN obsahuje stejnou léčivou látku jako přípravek Aclasta (kyselina zoledronová). Pacienti léčení přípravkem Zoledronic acid IBIGEN nemají být současně léčeni přípravkem Aclasta nebo jiným bisfosfonátem, protože kombinované účinky těchto látek nejsou známy.
Bezpečnost a účinnost kyseliny zoledronové u pediatrických pacientů nebyla stanovena (viz bod 5.1). Renální insufícience
U pacientů s TIH s prokázaným zhoršením renální funkce musí být velmi dobře posouzen jejich stav a zváženo, zda přínos léčby přípravkem Zoledronic acid IBIGEN převáží možné riziko léčby.
Při rozhodnutí léčit pacienty s kostními metastázami pro prevenci kostních příhod je nutno vzít v úvahu, že nástup léčebného účinku je za 2 až 3 měsíce.
Stejně jako u jiných bisfosfonátů, při léčbě kyselinou zoledronovou byly hlášeny poruchy funkce ledvin. Mezi faktory, které mohou zvyšovat riziko zhoršení ledvinných funkcí, patří dehydratace, již existující poškození funkce ledvin, opakované cykly podávání kyseliny zoledronové nebo jiných bisfosfonátů a podávání jiných nefrotoxických léčivých přípravků. Přestože je toto riziko sníženo při podávání přípravku Zoledronic Acid IBIGEN v dávce 4 mg po dobu delší než 15 minut, může se poškození ledvin přesto vyskytnout. U pacientů po úvodní nebo jednorázové dávce 4 mg přípravku Zoledronic Acid IBIGEN bylo hlášeno zhoršení ledvinných funkcí a progrese do ledvinného selhání s nutností dialýzy. Zvýšení kreatininu v séru se může u některých pacientů vyskytnout po opakovaném podání přípravku Zoledronic Acid IBIGEN v dávkách, doporučených k prevenci kostních příhod, i když méně často.
Před každou aplikací přípravku Zoledronic acid IBIGEN musí být pacientům stanovena hladina sérového kreatininu. U pacientů s kostními metastázami a s mírným až středně závažným poškozením funkce ledvin se doporučuje zahájit léčbu nižšími dávkami přípravku Zoledronic Acid IBIGEN. U pacientů, u kterých bylo v průběhu léčby přípravkem Zoledronic acid IBIGEN prokázáno zhoršení funkce ledvin, musí být léčba kyselinou zoledronovou přerušena do doby, než se hladina sérového kreatininu vrátí na hodnoty, které se nebudou lišit o více než 10 % od výchozí hodnoty (viz bod 4.2). Léčba přípravkem Zoledronic Acid IBIGEN má být znovu zahájena stejnou dávkou, jaká byla podávaná před přerušením léčby.
Vzhledem k možnému vlivu bisfosfonátů včetně kyseliny zoledronové na funkci ledvin se pro nedostatek klinických údajů o bezpečnosti u pacientů se závažným poškozením funkce ledvin již před zahájením léčby (v klinických studiích definovaných hladinou kreatininu v séru > 400 pmol/l nebo >
4,5 mg/dl u pacientů s TIH a > 265 pmol/l nebo > 3,0 mg/dl u pacientů s karcinomem a kostními metastázami) a pouze omezenému množství farmakokinetických údajů u pacientů s existujícím závažným renálním poškozením (clearance kreatininu < 30 ml/min) se použití přípravku Zoledronic Acid IBIGEN u pacientů se závažným poškozením funkce ledvin nedoporučuje.
Hepatální insufícience
U pacientů se závažnou jaterní insuficiencí je k dispozici jen omezené množství klinických údajů, a proto nemohla být dána specifická doporučení pro tuto skupinu pacientů.
Osteonekróza čelisti
Byly hlášeny případy osteonekrózy čelisti, zejména u pacientů s maligním onemocněním, kteří byli léčeni bisfosfonáty včetně kyseliny zoledronová. Mnoho těchto pacientů bylo také léčeno chemoterapií a kortikosteroidy. Většina hlášených případů byla spojena se stomatologickým výkonem, jako např. zubní extrakcí. Mnoho pacientů mělo známky lokální infekce včetně osteomyelitidy.
U pacientů s rizikovými faktory (např. rakovinou, chemoterapií, kortikosteroidy, špatnou ústní hygienou) je nutno zvážit před zahájením léčby bisfosfonáty stomatologické vyšetření spolu s preventivním zubním ošetřením.
Pokud je to možné, je nutno se u těchto pacientů během léčby vyhnout invazivním stomatologickým výkonům. U pacientů, kde se osteonekróza čelisti rozvine během léčby bisfosfonáty, může stomatologický výkon zhoršit stav. Neexistují data, která by dokládala, že vysazení bisfosfonátové léčby snižuje u pacientů vyžadujících stomatologický výkon riziko osteonekrózy čelisti. Plán léčby každého pacienta je nutno založit na individuálním klinickém posouzení poměru přínosu a rizika ošetřujícím lékařem.
Atypické zlomeniny femuru
V souvislosti s léčbou bisfosfonáty byly hlášeny atypické subtrochanterické a diafyzární zlomeniny femuru, zejména u pacientů dlouhodobě léčených pro osteoporózu. Tyto příčné nebo krátké šikmé zlomeniny se mohou objevit kdekoli v celé délce femuru od oblasti těsně pod malým trochanterem až do části těsně nad suprakondylickým rozšířením. Tyto zlomeniny se objevují po minimálním traumatu nebo bez souvislosti s ním a u některých pacientů se mohou projevovat bolestí ve stehně nebo třísle, často sdružené na zobrazovacích vyšetřeních s obrazem typickým pro stresové zlomeniny (neobvyklé nízkotraumatické zlomeniny, v angličtině známé jako insufficiency fractures“), týdny až měsíce před manifestací kompletní zlomeniny femuru.. Zlomeniny jsou často oboustranné, proto je nutné u pacientů léčených bisfosfonáty, kteří utrpěli zlomeninu diafýzy femuru, vyšetřit i kontralaterální femur. Rovněž bylo zaznamenáno špatné hojení těchto zlomenin. U pacientů, u kterých je podezření na atypickou zlomeninu femuru, je třeba při hodnocení jejich stavu zvážit i přerušení léčby bisfosfonáty, a to na základě zhodnocení prospěchu a rizika léčby u jednotlivého pacienta.
Pacienty je třeba poučit, aby během léčby bisfosfonáty hlásili jakoukoli bolest v oblasti stehna, boku nebo třísla, a všechny pacienty, u kterých se tyto příznaky objeví, je třeba vyšetřit s ohledem na možnou inkompletní zlomeninu femuru.
Bolesti muskuloskeletálního systému
Po uvedení na trh byly u pacientů léčených bisfosfonáty hlášeny silné až zneschopňující bolesti kostí, kloubů a/nebo svalů. Nicméně tato hlášení byla řídká. Do této kategorie léčiv patří i kyselina zoledronová. Doba do počátku nástupu projevů nežádoucích účinků od zahájení léčby se pohybovala od jednoho dne až po několik měsíců. Jakmile byla léčba přerušena, většině pacientů se od příznaků ulevilo. Podskupina pacientů zaznamenala opětovný návrat symptomů poté, co byla znovu léčena stejným lékem nebo jiným bisfosfonátem.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
V klinických studiích byla kyselina zoledronová podávána souběžně s běžně používanými protinádorovými léky, diuretiky, antibiotiky a analgetiky, aniž by byl pozorován výskyt klinicky zjevných interakcí. In vitro (viz bod 5.2) nebyla patrná vazba kyseliny zoledronové na plazmatické bílkoviny, ani nebyla zjištěna inhibice lidských enzymů cytochromu P450, ale formální klinické studie interakcí nebyly provedeny. Při souběžném podávání bisfosfonátů s aminoglykosidy se doporučuje opatrnost, protože může dojít k aditivnímu účinku obou léků s následným snížením hladiny vápníku v séru na delší dobu, než je žádoucí.
Opatrnost je také nutná, pokud je přípravek Zoledronic Acid IBIGEN podáván s jinými potenciálně nefrotoxickými léčivými přípravky. Je také nutné věnovat zvýšenou pozornost možnému rozvoji hypomagnesemie během léčby.
U pacientů s mnohočetným myelomem může být zvýšené riziko poškození ledvin při souběžném podávání intravenózních bisfosfonátů s thalidomidem.
4.6 Fertilita, těhotenství a kojení
Adekvátní údaje o podávání kyseliny zoledronové těhotným ženám nejsou k dispozici. Reprodukční studie provedené s kyselinou zoledronovou na zvířatech prokázaly reprodukční toxicitu (viz bod 5.3). Potenciální riziko pro člověka není známé. Přípravek Zoledronic acid IBIGEN nemá být během těhotenství podáván.
Kojení
Není známo, jestli kyselina zoledronová přechází do mateřského mléka. Přípravek Zoledronic acid IBIGEN je kontraindikován u kojících žen (viz bod 4.3).
Fertilita
Potenciální nežádoucí účinky kyseliny zoledronové na fertilitu v parentální a F1 generaci byly hodnoceny u potkanů. Došlo k výrazným farmakologickým účinkům, které je možné považovat za součást inhibice metabolizace vápníku v kostech a které se projevily peripartální hypokalcemií, což je skupinový účinek bisfosfonátů, dystocií a předčasným ukončením studie. Z tohoto důvodu nemohl být stanoven konečný vliv kyseliny zoledronové na fertilitu u lidí.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nežádoucí účinky, jako j sou závratě a ospalost, mohou mít vliv na schopnost řídit nebo obsluhovat stroje, proto je třeba dbát zvýšené opatrnosti při řízení a obsluze strojů během používání přípravku Zoledronic acid IBIGEN.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Během tří dnů po podání kyseliny zoledronové byly často hlášeny reakce akutní fáze s příznaky zahrnujícími bolest kostí, horečku, únavu, artralgii, myalgii a ztuhlost, tyto příznaky obvykle ustupují během několika dní (viz popis vybraných nežádoucích účinků).
Následují významná identifikovaná rizika přípravku Zoledronic Acid IBIGEN ve schválených indikacích:
Porucha funkce ledvin, osteonekróza čelisti, reakce akutní fáze, hypokalcemie, oční nežádoucí účinky, fibrilace síní, anafylaxe. Frekvence pro každé z těchto identifikovaných rizik jsou uvedeny v Tab. 1.
Seznam nežádoucích účinků v tabulce
Následující nežádoucí účinky uvedené v Tab. 1 byly shromážděny z klinických studií a hlášení po uvedení na trh, převážně při dlouhodobé léčbě 4 mg kyseliny zoledronové:
Tab. 1
Následuj ící nežádoucí účinky j sou hodnoceny dle uvedených četností, j ako první j sou vždy uvedeny ty nejčastější, dle následující klasifikace: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1000 až <1/100), vzácné (>1/10000 až <1/1000), velmi vzácné (<1/10000), není známo (z dostupných údajů nelze určit).
Poruchy krve a lymfatického systému
|
Časté: | |
|
Méně časté: |
Trombocytopenie, leukopenie |
|
Vzácné: |
Pancytopenie |
Poruchy imunitního systému
|
Méně časté: |
Hypersenzitivní reakce |
|
Vzácné: |
Angioneurotický edém |
Psychiatrické poruchy
|
Méně časté: |
Úzkost, poruchy spánku |
|
Vzácné: |
Poruchy nervového systému
|
Časté: | |
|
Méně časté: Poruchy oka |
Závratě, parestézie, poruchy chuti, hypestézie, hyperestézie, třes, somnolence |
|
Časté: |
Konjunktivitida |
|
Méně časté: |
Rozmazané vidění, skleritida a zánět očnice |
|
Velmi vzácné: Srdeční poruchy |
Uveitida, episkleritida |
|
Méně časté: |
Hypertenze, hypotenze, fibrilace síní, hypotenze vedoucí k synkopě či oběhovému kolapsu |
|
Vzácné: |
Bradykardie |
Respirační, hrudní a mediastinálníporuchy
Méně časté: Dušnost, kašel, bronchokonstrikce
Gastrointestinální poruchy
|
Časté: | |
|
Méně časté: |
Průjem, zácpa, bolest břicha, dyspepsie, stomatitida, sucho v ústech |
Poruchy kůže a podkožní tkáně
Méně časté: Pruritus, vyrážka (včetně erytematózní a makulámí vyrážky), zvýšené pocení
Poruchy svalové a kosterní soustavy a pojivové tkáně
Časté: Bolest kostí, myalgie, artralgie, generalizovaná boest
Méně časté: Svalové křeče, osteonekróza čelisti*
Poruchy ledvin a močových cest
Časté: Zhoršení ledvinných funkcí
Méně časté: Akutní renální selhání, hematurie, proteinurie
Celkové poruchy a reakce v místě aplikace
Časté:
Méně časté:
Vyšetření Velmi časté: Časté:
Méně časté: Vzácné:
Horečka, příznaky podobné chřipce (včetně únavy, zimnice, malátnosti a zčervenání)
Asténie, periferní edém, reakce v místě vpichu injekce (včetně bolesti, podráždění, otoku, zduření), bolest na hrudi, zvýšení hmotnosti, anafylaktická reakce/šok, kopřivka
Hypofosfatemie
Zvýšená hladina kreatininu a močoviny v krvi Hypomagnesemie, hypokalémie Hyperkalemie, hypernatremie
* Na základě klinických studií s určením možných případů osteonekrózy čelisti. Jelikož tato hlášení jsou předmětem zkreslujících faktorů, není možno spolehlivě stanovit kauzální souvislost s expozicí tomuto léčivému přípravku.
Popis vybraných nežádoucích účinků
Porucha funkce ledvin
Léčba kyselinou zoledronovou byla spojena s hlášeními renální dysfunkce. Faktory, které mohou zvýšit potenciál ke zhoršení funkce ledvin, zahrnují dehydrataci, již existující poškození ledvin, mnohočetné cykly kyseliny zoledronové nebo jiných bisfosfonátů a souběžné užívání nefrotoxických léčivých přípravků nebo použití kratší doby infuze, než je v současné době doporučováno. Zhoršení funkce ledvin, progrese k renálnímu selhání a dialýze byly hlášeny u pacientů po počáteční dávce nebo jednotlivé dávce 4 mg kyseliny zoledronové (viz bod 4.4).
Osteonekróza čelisti
Byly hlášeny případy osteonekrózy (zejména čelistí), zejména u pacientů s maligním onemocněním léčených léčivými přípravky inhibujícími kostní resorpci, jako je kyselina zoledronová. Mnoho těchto pacientů mělo příznaky lokální infekce včetně osteomyelitidy a většina hlášení se týkala pacientů s karcinomem po extrakci zubu nebo jiném stomatochirurgickém výkonu. Osteonekróza čelistí má mnohonásobně dokumentované rizikové faktory včetně diagnózy rakoviny, souběžných terapií (například chemoterapie, radioterapie, kortikosteroidy) a dalších přidružených onemocnění (např. anémie, koagulopatie, infekce, již existující onemocnění dutiny ústní). Ačkoliv kauzalita nebyla prokázána, je doporučeno vyhnout se stomatologickému výkonu, protože hojení může být prodlouženo (viz bod 4.4).
Fibrilace síní
V jedné 3leté, randomizované, dvojitě zaslepené kontrolované studii, která hodnotila účinnost a bezpečnost kyseliny zoledronové 5 mg podávané jednou ročně oproti placebu při léčbě postmenopauzální osteoporózy (PMO), byl celkový výskyt fibrilace síní 2,5 % (96 z 3862) u pacientů používajících kyselinu zoledronovou 5 mg a 1,9 % (75 z 3852) u pacientů s placebem. Poměr vážných případů fibrilace síní byl 1,3 % (51 z 3862) u pacientů užívajících kyselinu zoledronovou 5 mg a 0,6 % (22 z 3852) u pacientů užívajících placebo. Tento účinek pozorovaný v této studii nebyl zaznamenán v jiných studiích s kyselinou zoledronovou, včetně studií s kyselinu zoledronovu 4 mg podávanou každé 3-4 týdny onkologickým pacientům. Mechanismus původu zvýšeného výskytu fibrilace síní v této jediné klinické studii není známý.
Reakce akutní fáze
Tento nežádoucí účinek se skládá ze souboru příznaků, které zahrnují horečku, myalgii, bolest hlavy, bolest končetin, nauzeu, zvracení, průjem a artralgii. Nastupuje za < 3 dny po infuzi kyseliny zoledronové a reakce je také známá pod názvy „flu-like syndrom“ (syndrom podobný chřipce) nebo „post-dose“ syndrom (příznaky po podání dávky).
Atypické zlomeniny femuru
Po uvedení přípravku na trh byly hlášeny následující nežádoucí účinky (frekvence vzácná):
Atypické subtrochanterické a diafyzární zlomeniny femuru (skupinový nežádoucí účinek bisfosfonátů).
4.9 Předávkování
Klinické zkušenosti s akutním předávkováním kyselinou zoledronovou jsou omezené. Pacienti, kteří dostávali vyšší dávky, než je doporučená dívka, musí být pečlivě sledováni, protože bylo pozorováno poškození renálních funkcí (včetně renálního selhání) a odchylky v hladinách sérových koncentrací elektrolytů (včetně vápníku, fosforu a hořčíku). V případě hypokalcemie se dle klinické indikace může podat infuze kalcium-glukonátu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Bisfosfonáty, ATC kód: M05 BA 08
Kyselina zoledronová patří do skupiny bisfosfonátů, které působí primárně v kostech. Je to inhibitor osteoklastické resorpce kostí.
Selektivní působení bisfosfonátů v kostech spočívá v jejich vysoké afinitě k mineralizované kosti, ale přesný mechanizmus účinku vedoucího k inhibici osteoklastické aktivity zůstává stále neobjasněn. V dlouhodobých studiích na zvířatech inhibovala kyselina zoledronová kostní resorpci bez nežádoucího ovlivnění tvorby, mineralizace nebo mechanických vlastností kostí.
Kromě inhibice kostní resorpce má kyselina zoledronová navíc některé protinádorové vlastnosti, které by mohly přispívat k celkové účinnosti léčby kostních metastáz. V preklinických studiích byly prokázány následující vlastnosti:
- In vivo: inhibice osteoklastické kostní resorpce, která ovlivňuje vnitřní mikroprostředí kostní dřeně a zhoršuje tak podmínky pro růst nádorových buněk, antiangiogenetický účinek, analgetický účinek.
- In vitro: Inhibice osteoblastické proliferace, přímý cytostatický a pro-apoptotický účinek na nádorové buňky, synergický cytostatický účinek spolu s ostatními protinádorovými léky, antiadhezivní/antiinvazivní působení.
Výsledky klinických studií prevence kostních příhod u pacientů s pokročilým maligním onemocněním postihujícím kosti
První randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie srovnávala kyselinu zoledronovou s placebem v prevenci kostních příhod (SRE = Skeletal Related Events) u pacientů s karcinomem prostaty. Kyselina zoledronová 4 mg významně snížila počet pacientů, u kterých došlo k výskytu alespoň jedné kostní příhody (SRE), prodloužila medián času do první SRE o > 5 měsíců a snížila roční výskyt příhod na pacienta - míru onemocnění kostí. Analýzy mnohočetných příhod ukázaly ve srovnání s placebem 36 % snížení rizika vývoje SRE ve skupině s kyselinou zoledronovou. Pacienti dostávající kyselinu zoledronovou 4 mg hlásili nižší nárůst bolestivosti než ti, kteří dostávali placebo, rozdíl dosáhl významnosti ve 3., 9., 21. a 24. měsíci. U pacientů léčených kyselinou zoledronovou nižší výskyt patologických zlomenin. U pacientů s blastickými lézemi byl léčebný efekt méně zřejmý. Výsledky účinnosti jsou uvedeny v Tab. 2.
Ve druhé studii, kde byly zahrnuty jiné solidní nádory než karcinomy prsu a prostaty, snížila kyselina zoledronová 4 mg významně počet pacientů s SRE a prodloužila medián času do první kostní příhody na > 2 měsíce a snížila poměr kostní morbidity. Analýza mnohočetných příhod ukázala 30,7 % snížení rizika ve vývoji kostních příhod ve skupině léčené kyselinou zoledronovou 4 mg ve srovnání s placebem. Výsledky účinnosti jsou uvedeny v Tab. 3
Tab. 2: Výsledky účinnosti (pacienti s karcinomem prostaty užívající hormonální terapii)
|
Jakákoli SRE (+TIH) |
Fraktury* |
Radioterapie kostí | ||||
|
Kyselina zoledronová 4 mg |
Placebo |
Kyselina zoledronová 4 mg |
Placebo |
Kyselina zoledronová 4 mg |
Placebo | |
|
N |
214 |
208 |
214 |
208 |
214 |
208 |
|
Podíl pacientů s SRE (%) |
38 |
49 |
17 |
25 |
26 |
33 |
|
Hodnota p |
0,028 |
0,052 |
0,119 | |||
|
Medián času do SRE (dny) |
488 |
321 |
NR |
NR |
NR |
640 |
|
Hodnota p |
0,009 |
0,020 |
0,055 | |||
|
Míra postižení kosti |
0,77 |
1,47 |
0,20 |
0.45 |
0.42 |
0.89 |
Hodnota p 0,005 0,023 0,060
|
Snížení rizika |
36 |
- |
NA |
NA |
NA |
NA |
|
mnohočetných příhod** (%) |
Hodnota p 0,002 NA NA
* Zahrnuje vertebrální i nevertebrální zlomeniny
** Všechny kostní příhody, celkový počet stejně jako doba do každé události během studie NR Nebylo dosaženo NA Není aplikovatelné
Tab. 3: Výsledky účinnosti (solidní nádory jiné než nádory prsu a prostaty)
|
Jakákoli SRE (+TIH) |
Fraktury* |
Radioterapie kostí | ||||
|
Kyselina zoledronová 4 mg |
Placebo |
Kyselina zoledronová 4 mg |
Placebo |
Kyselina zoledronová 4 mg |
Placebo | |
|
N |
257 |
250 |
257 |
250 |
257 |
250 |
|
Podíl pacientů s SRE (%) |
39 |
48 |
16 |
22 |
29 |
34 |
|
hodnota p |
0,039 |
0,064 |
0,173 | |||
|
Medián času do SRE (dny) |
236 |
155 |
NR |
NR |
424 |
307 |
|
hodnota p |
0,009 |
0,020 |
0,079 | |||
|
Míra postižení kostí |
1,74 |
2,71 |
0,39 |
0.63 |
1.24 |
1.89 |
|
hodnota p |
0,012 |
0,066 |
0,099 | |||
|
Snížení rizika mnohočetných příhod ** (%) |
30,7 |
NA |
NA |
NA |
NA | |
|
hodnota p |
0,003 |
NA |
NA | |||
* Zahrnuje vertebrální i nevertebrální zlomeniny
** Všechny kostní příhody, celkový počet stejně jako doba do každé události během studie NR Nebylo dosaženo NA Není aplikovatelné
Ve třetí randomizované dvojitě zaslepené studii fáze III byla srovnávána kyselina zoledronová 4 mg nebo 90 mg pamidronátu při podávání každé 3 až 4 týdny pacientům s mnohočetným myelomem nebo karcinomem prsu s nejméně jednou kostní lézí. Výsledky ukázaly, že kyselina zoledronová 4 mg měla v prevenci SRE srovnatelnou účinnost jako 90 mg pamidronátu. Analýza mnohočetných příhod odhalila významné snížení rizika u pacientů léčených kyselinou zoledronovou 4 mg o 16 % ve srovnání s pacienty, kteří dostávali pamidronát. Výsledky účinnosti jsou uvedeny v Tab. 4.
Tab. 4: Výsledky účinnosti (pacienti s nádorem prsu a mnohočetným myelomem)
|
Jakákoli SRE (+TIH) |
Fraktury* |
Radioterapie kostí | ||||
|
Kyselina zoledronová 4 mg |
Pam 90 mg |
Kyselina zoledronová 4 mg |
Pam 90 mg |
Kyselina zoledronová 4 mg |
Pam 90 mg | |
|
N |
561 |
555 |
561 |
555 |
561 |
555 |
|
Podíl pacientů s SRE (%) |
48 |
52 |
37 |
39 |
19 |
24 |
|
hodnota p |
0,198 |
0,653 |
0,037 | |||
|
Medián času do SRE (dny) |
376 |
356 |
NR |
714 |
NR |
NR |
|
hodnota p |
0,151 |
0,672 |
0,026 | |||
|
Míra postižení kostí |
1,04 |
1,39 |
0,53 |
0.60 |
0.47 |
0.71 |
|
hodnota p |
0,084 |
0,614 |
0,015 | |||
|
Snížení rizika mnohočetných příhod** (%) |
16 |
NA |
NA |
NA |
NA | |
|
hodnota p |
0,030 |
NA |
NA | |||
* Zahrnuje vertebrální i nevertebrální zlomeniny
** Všechny kostní příhody, celkový počet stejně jako doba do každé události během studie NR Nebylo dosaženo NA Není aplikovatelné
Kyselina zoledronová byla též hodnocena ve dvojitě zaslepené, randomizované, placebem kontrolované studii u 228 pacientů s dokumentovanými kostními metastázami u karcinomu prsu ke zjištění účinku 4 mg kyseliny zoledronové na riziko vzniku kostních příhod (SRE) počítané jako poměr celkového počtu kostních příhod (vyjma hyperkalcemie a po zohlednění předchozích zlomenin) vůči celkovému sledovanému období. Pacienti dostávali po dobu jednoho roku každé čtyři týdny buď 4 mg kyseliny zoledronové nebo placebo. Pacienti byli rovnoměrně rozděleni do skupin léčených kyselinou zoledronovou nebo placebem.
Podíl SRE (kostní příhody/osoba rok) byl 0,628 u kyseliny zoledronové a 1,096 u placeba. Podíl pacientů s nejméně jednou příhodou SRE (vyjma hyperkalcemie) byl 29,8 % ve skupině léčené kyselinou zoledronovou proti 49,6 % ve skupině s placebem (p=0,003). Medián času do zjištění první příhody SRE nebyl v rameni léčby kyselinou zoledronovou na konci studie dosažen a byl signifikantně prodloužen ve srovnání s placebem (p=0,007). Kyselina zoledronová snížila riziko příhod SRE o 41 % dle analýz mnohočetných příhod (poměr rizika=0,59, p=0,019) ve srovnání s placebem.
Ve skupině léčené kyselinou zoledronovou bylo po 4 týdnech a při každém následujícím měření v průběhu léčby pozorováno statisticky významné zlepšení v hodnocení bolesti (použitím Brief Pain Inventory BPI) ve srovnání s placebem (Obr. 1). Hodnocení bolesti ve skupině s kyselinou zoledronovou bylo trvale pod úrovní počátečního stavu a bylo provázeno trendem ke snižování užívání analgetik.
Obr. 1: Průměrná změna oproti počátečnímu stavu skóre dle BPI. Statisticky signifikantní rozdíly jsou vyznačeny (*p<0,05) pro porovnání mezi léčbami (4 mg kyselina zoledronová vs. placebo).
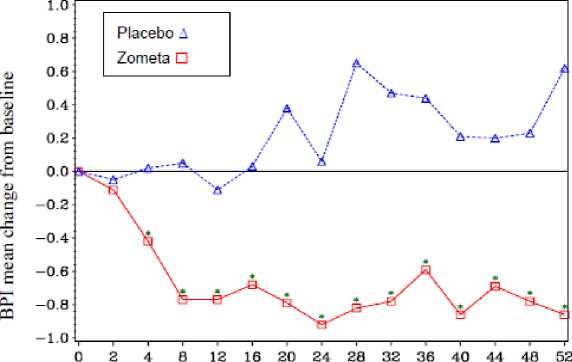
Time on study (weeks)
Výsledky klinického hodnocení léčby TIH
V klinických studiích bylo u hyperkalcemie vyvolané nádorovým onemocněním (TIH) prokázáno, že působení kyseliny zoledronové je charakterizováno poklesem hladiny kalcia v séru a vylučováním kalcia močí. V studii fáze I pro vyhledávání dávky u pacientů s mírnou až střední hyperkalcemií indukovanou nádorovým onemocněním (TIH) byly testované účinné dávky v rozmezí přibližně 1,22,5 mg.
Ke zhodnocení účinků 4 mg kyseliny zoledronové proti 90 mg pamidronátu byly výsledky dvou pilotních multicentrických studií u pacientů s TIH kombinovány v předem naplánované analýze. Po dávce kyseliny zoledronové 8 mg byla rychlejší normalizace hodnot kalcia v séru pozorována již 4. den a po dávce kyseliny zoledronové 4 mg a 8 mg i 7. den. Byla pozorována následující procenta odpovědí:
Tab. 5: Procento kompletních odpovědí ve dnech v kombinovaných TIH studiích
|
4. den |
7. den |
10. den | |
|
Kyselina zoledronová 4 mg (N=86) |
45,3% (p=0,104) |
82,6% (p=0,005)* |
88,4% (p=0,002)* |
|
Kyselina zoledronová 8 mg (N=90) |
55,6% (p=0,021)* |
83,3% (p=0,010)* |
86,7% (p=0,015)* |
|
Pamidronát 90 mg (N=99) |
33,3% |
63,6% |
69,7% |
|
*hodnota p v porovnání s pamidronátem | |||
Střední doba k dosažení normokalcemie byla 4 dny. Střední doba do relapsu (opětovné zvýšení albuminem korigované hladiny kalcia v séru na > 2,9 mmol/l) byla u pacientů léčených kyselinou zoledronovou 30 až 40 dnů proti 17 dnům u pacientů léčených pamidronátem 90 mg (p-hodnoty: 0,001 pro 4 mg a 0,007 pro 8 mg kyseliny zoledronové). Mezi dvěma dávkami kyseliny zoledronové nebyl nalezen statistický rozdíl.
V klinických studiích bylo 69 pacientů s relapsem nebo neodpovídajících na počáteční léčbu (kyselina zoledronová 4 mg, 8 mg nebo pamidronát 90 mg) přeléčeno 8 mg kyseliny zoledronové. Procento odpovědí byla u těchto pacientů přibližně 52 %. Pro srovnání s dávkou 4 mg kyseliny zoledronové nejsou dostupné údaje, protože tito pacienti byli přeléčeni pouze dávkou 8 mg kyseliny zoledronové.
V klinických studiích provedených u pacientů s hyperkalcemií indukovanou nádorovým onemocněním (TIH) byl celkový bezpečnostní profil mezi všemi 3 léčenými skupinami (kyselina zoledronová 4 a 8 mg a pamidronát 90 mg) podobný v typech i závažnosti.
Pediatrická populace
Výsledky klinické studie v léčbě těžké formy osteogenesis imperfecta u pediatrických pacientů ve věku 1 až 17 let
Účinky intravenózně podávané kyseliny zoledronové v léčbě těžké formy osteogenesis imperfecta (typ I, III a IV) u pediatrických pacientů (věk 1 až 17 let) byly srovnány s intravenózně podávaným pamidronátem v jedné mezinárodní, multicentrické, randomizované, otevřené studii se 74 pacienty v rameni s kyselinou zoledronovou a 76 pacienty v rameni s pamidronátem. Doba léčby ve studii byla 12 měsíců, léčbě předcházelo 4-9 týdnů období skríninku, během kterých byla po dobu nejméně 2 týdnů podávána suplementace vitaminu D a kalcia. V tomto klinickém programu byli pacienti ve věku 1 až méně než 3 roky léčeni dávkou 0,025 mg/kg kyseliny zoledronové (až do maximální jednotlivé dávky 0,35 mg) každé 3 měsíce a pacienti ve věku 3-17 let byli léčeni dávkou 0,05 mg/kg kyseliny zoledronové (až do maximální jednotlivé dávky 0,83 mg) každé 3 měsíce. Studie byla prodloužena za účelem vyhodnocení dlouhodobé celkové a renální bezpečnosti podávání kyseliny zoledronové jednou nebo dvakrát ročně v průběhu 12 měsíců prodloužené léčby u dětí, které dokončily 1 rok léčby kyselinou zoledronovou nebo pamidronátem v základní studii.
Primárním cílovým parametrem účinnosti ve studii bylo sledování procentuální změny původního stavu kostní denzity bederní páteře (BMD) po 12 měsících léčby. Očekávané účinky léčby na BMD byly podobné, ale design studie nepostačoval k prokázání non-inferiority kyseliny zoledronové. Především nedošlo k jasnému prokázání účinnosti na výskyt zlomenin nebo bolesti. Nežádoucí účinky zlomenin dlouhých kostí dolních končetin byly hlášené u přibližně 24 % (femur) a 14 % (tibia) pacientů s těžkou formou osteogenesis imperfecta léčených kyselinou zoledronovou oproti 12 % a 5 % pacientů s těžkou formou osteogenesis imperfecta léčených pamidronátem, bez ohledu na typ poruchy a kauzalitu, ale souhrnný výskyt zlomenin u pacientů léčených kyselinou zoledronovou a pamidronátem byl srovnatelný: 43 % (32/74) oproti 41 % (31/76). Vyhodnocení rizika zlomenin je ztíženo tím, že zlomeniny jsou častým jevem u pacientů s těžkou formou osteogenesis imperfecta jako součást průběhu onemocnění.
Nežádoucí účinky sledované u této populace byly podobné účinkům dříve zjištěným u dospělých pacientů s pokročilými malignitami ovlivňujícími kosti (viz bod 4.8). Nežádoucí účinky řazené podle četností jsou uvedené v Tab. 6. Je použita následující běžná klasifikace: velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1000 až <1/100), vzácné (>1/10000 až <1/1000), velmi vzácné (<1/10000), není známo (z dostupných údajů nelze určit).
Tab. 6: Nežádoucí účinky sledované u pediatrických pacientů s těžkou formou osteogenesis imperfecta1
|
Poruchy nervového systému Časté: | |
|
Srdeční poruchy Časté: | |
|
Respirační, hrudní a mediastinálníporuchy Časté: |
Nasofaryngitida |
|
Gastrointestinální poruchy Velmi časté: Časté: | |
|
Poruchy kosterní a svalové soustavy a pohybové tkáně Časté: |
Bolest v končetinách, artralgie, bolest kostí a svalů |
|
Celkové poruchy a reakce v místě aplikace Velmi časté: Časté: | |
|
Vyšetření Velmi časté: Časté: |
Hypokalcemie Hypofosfatemie |
'Nežádoucí účinky s četností < 5 % byly zhodnoceny z medicínského hlediska a bylo prokázáno, že tyto případy odpovídají stanovenému bezpečnostnímu profilu kyseliny zoledronové (viz bod 4.8).
U pediatrických pacientů s těžkou formou osteogenesis imperfecta se zdá být použití kyseliny zoledronové v porovnání s pamidronátem spojené s výraznějším rizikem reakce akutní fáze, hypokalcemie a neobjasněné tachykardie, ale tento rozdíl se snižuje po následných infuzích.
Evropská léková agentura zrušila povinnost předložit výsledky studií s kyselinou zoledronovou u všech podskupin pediatrické populace v léčbě hyperkalcemie navozené nádorovým onemocněním a prevenci kostních příhod u pacientů s pokročilými maligními onemocněními postihujícími kosti (viz bod 4.2 informace o pediatrickém použití)
5.2 Farmakokinetické vlastnosti
Následující farmakokinetické údaje získané po jednorázové a opakované 5 a 15 minutové infuzi 2, 4, 8 a 16 mg kyseliny zoledronové u 64 pacientů s kostními metastázami neprokázaly závislost na dávce.
Po zahájení infuze kyseliny zoledronové stoupá rychle koncentrace kyseliny zoledronové v plazmě a dosahuje vrcholu před ukončením infuze, následuje rychlý pokles a za 4 hodiny je koncentrace v plazmě < 10 % vrcholové koncentrace a za 24 hodin klesne hladina v plazmě na < 1 %, načež následuje dlouhé období nízké koncentrace, která nepřesahuje 0,1 % vrcholové koncentrace, před druhou infuzí kyseliny zoledronové 28. den.
Kyselina zoledronová podaná intravenózní infuzí je vylučována třífázovým procesem: rychlé dvojfázové vymizení z krevního oběhu s poločasem t/a 0,24 a t/ P 1,87 hodiny je následováno dlouhou fází vylučování s terminálním poločasem vylučování t/ y 146 hodin. Po opakovaném podání léku za 28 dnů nebyla pozorována akumulace kyseliny zoledronové v plazmě. Kyselina zoledronová není metabolizována a je vylučována nezměněná ledvinami. Během prvních 24 hodin bylo močí vyloučeno 39 ± 16 % aplikované dávky, zatímco zbytek byl vázán převážně v kostní tkáni. Z kostní tkáně je látka velmi pomalu uvolňována zpět do krevního oběhu a vylučována ledvinami. Celková tělesná clearance je 5,04 ± 2,5 l/h, není závislá na dávce ani ovlivněna pohlavím, věkem, rasou a tělesnou hmotností. Prodloužení doby infuze z 5 na 15 minut způsobí na konci infuze 30% pokles koncentrace kyseliny zoledronové, ale plocha pod křivkou plazmatické koncentrace versus čas není ovlivněna.
Variabilita farmakokinetických parametrů kyseliny zoledronové mezi jednotlivými pacienty je vysoká, stejně jako je tomu u ostatních bisfosfonátů.
U pacientů s hyperkalcemií nebo s jaterní nedostatečností nejsou dostupné farmakokinetické údaje. Kyselina zoledronová neinhibuje lidské P450 enzymy in vitro, nevykazuje biotransformaci a ve studiích na zvířatech bylo < 3 % z aplikované dávky nalezeno ve stolici, což předpokládá, že játra nebudou hrát významnou úlohu ve farmakokinetice kyseliny zoledronové.
Renální clearance kyseliny zoledronové korelovala s clearance kreatininu, renální clearance představuje 75 ± 33 % clearance kreatininu, jejíž průměr byl u 64 studovaných pacientů s nádorovým onemocněním 84 ± 29 ml/min (rozmezí 22 až 143 ml/min). Populační analýza ukázala, že u pacientů s clearance kreatininu 20 ml/min (závažné poškození ledvin), nebo 50 ml/min (středně závažné poškození) je možné odhadnout, že clearance kyseliny zoledronové by byla 37 %, nebo 72 % u pacientů, u nichž byla clearance kreatininu 84 ml/min. U pacientů se závažným postižením ledvin (clearance kreatininu < 30 ml/min) je dostupné jen omezené množství údajů.
Afinita kyseliny zoledronové k buňkám krve nebyla prokázána a vazba na plazmatické proteiny je nízká (přibližně 56 %) a je nezávislá na koncentraci kyseliny zoledronové.
Zvláštní populace
Pediatričtí pacienti
Omezené farmakokinetické údaje u dětí s těžkou formou osteogenesis imperfecta naznačují, že farmakokinetika kyseliny zoledronové je u dětí ve věku 3 až 17 let při obdobném dávkování v mg/kg podobná farmakokinetice u dospělých pacientů. Věk, tělesná hmotnost, pohlaví a clearance kreatininu neměly vliv na systémovou expozici kyseliny zoledronové.
5.3 Předklinické údaje vztahující se k bezpečnosti
Akutní toxicita.
Nejvyšší neletální jednorázová intravenózní dávka byla pro myši 10 mg/kg a u potkanů 0,6 mg/kg tělesné hmotnosti.
Subchronická a chronická toxicita
Kyselina zoledronová byla dobře snášena, pokud byla aplikována subkutánně potkanům a intravenózně psům v dávce 0,02 mg/kg denně po dobu 4 týdnů. Dávka 0,001 mg/kg/den aplikovaná subkutánně potkanům a intravenózní dávka 0,005 mg/kg aplikovaná jednou za 2-3 dny psům po dobu 52 týdnů byla také dobře snášena.
Nejčastějšími nálezy po opakovaném podání studovaných dávek zvířatům v době růstu bylo téměř po všech dávkách zvýšení spongiózy v metafýzách dlouhých kostí. Tyto nálezy reflektují farmakologické antiresorpční vlastnosti sloučeniny.
Hranice bezpečnosti z hlediska účinku na ledviny byly při dlouhodobém opakovaném parenterálním podávání experimentálním zvířatům velmi úzké. Kumulativní hladiny bez nežádoucího účinku (NOAELs = no adverse event levels) po jednorázovém podání (1,6 mg/kg) a po opakovaném podávání až po dobu 1 měsíce (0,06 až 0,6 mg/kg/den) nenaznačily působení na ledviny v dávkách ekvivalentních nebo přesahujících nejvyšší dávky určené pro humánní aplikaci. Dlouhodobé opakované podávání kyseliny zoledronové v dávkách přesahujících nejvyšší předpokládané terapeutické dávky mělo toxické účinky na jiné orgány včetně zažívacího traktu, jater, ledvin, plic a místa intravenózní injekce.
Reprodukční toxicita
Kyselina zoledronová byla při subkutánním podání dávek > 0,2 mg/kg potkanům teratogenní. Ačkoli teratogenita nebo fetotoxicita nebyla pozorována u králíků, byla zjištěna toxicita u březích samic. U potkanů byla pozorována po nejnižší dávce (0,01 mg/kg tělesné hmotnosti) dystokie.
Mutagenita a kancerogenní účinek
V provedených testech mutagenity a kancerogenity nebyl pro kyselinu zoledronovou pozorován ani mutagenní ani kancerogenní účinek.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Lahvička s práškem: mannitol (E421), dihydrát natrium-citrátu Ampulka s rozpouštědlem: voda na injekci
6.2 Inkompatibility
Aby se zabránilo možným inkompatibilitám, musí být přípravek Zoledronic acid IBIGEN ředěn 0,9% roztokem chloridu sodného nebo 5% roztokem glukózy.
Rekonstituovaný roztok přípravku Zoledronic acid IBIGEN nesmí být mísen s infuzními roztoky obsahujícími kalcium nebo jiné dvojmocné kationty, jako je laktátový Ringerův roztok, a má být podávána jako samostatný intravenózní roztok oddělenou infuzní linkou.
Studie se skleněnými láhvemi a některými typy infuzních vaků a infuzních linek vyrobených z polyvinylchloridu, polyethylenu a polypropylenu (předplněné 0,9 % roztokem chloridu sodného nebo 5 % roztokem glukózy) neprokázaly inkompatibilitu s přípravkem Zoledronic Acid IBIGEN.
6.3 Doba použitelnosti
18 měsíců
Z mikrobiologického hlediska má být přípravek použit okamžitě. Pokud není použit okamžitě, je doba uchovávání a podmínky před použitím v plné zodpovědnosti uživatele a doba uchovávání by neměla být delší než 24 hodiny při teplotě 2°C - 8°C, pokud ředění neprobíhalo za kontrolovaných a aseptických podmínek.
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Podmínky uchovávání rekonstituovaného infuzního roztoku viz bod 6.3.
6.5 Druh obalu a obsah balení
Přípravek Zoledronic Acid IBIGEN 4 mg prášek pro infuzní roztok s rozpouštědlem je dodáván v balení obsahujícím 1 lahvičku s práškem pro infuzní roztok a 1 ampulku s vodou na injekci.
Lahvička s práškem: 6 ml lahvička z bezbarvého skla, sklo hydrolytické třídy I (Ph.Eur.)
Ampulka s rozpouštědlem: 5 ml ampulka z bezbarvého skla.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Prášek musí být nejprve rekonstituován v lahvičce pomocí 5 ml vody na injekci z přiložené ampulky (finální objem: 5,2 ml). Před odebrání roztoku musí být prášek zcela rozpuštěn. Potřebné množství rekonstituovaného roztoku má být dále naředěno ve 100 ml roztoku, který neobsahuje kalcium (0,9% roztok chloridu sodného nebo 5% roztok glukózy). Pokud je roztok vyjmut z chladničky, před podáním má být ponechán do dosažení pokojové teploty.
Během přípravy infuze musí být dodržen aseptický postup. Pouze pro jednorázové použití.
Smí být použit pouze čirý, bezbarvý roztok bez částic.
Zdravotnickým pracovníkům se důrazně doporučuje, aby nelikvidovali nepoužitý přípravek Zoledronic acid IBIGEN v lokálním odpadovém systému.
Všechen nepoužitý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Ibigen S.r.l Via Fossignano, 2 04011 Aprilia (LT)
Itálie
8. REGISTRAČNÍ ČÍSLO
87/226/13-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 5.6.2013
10. DATUM REVIZE TEXTU
5.6.2013
18