Vistabel
sp.zn. sukls206720/2014
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. NÁZEV PŘÍPRAVKU
VISTABEL, 4 jednotky definované dle Allerganu/0,1 ml, Prášek pro injekční roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Botulini toxinum typus A1....................4 jednotky definované dle Allerganu na 0,1 ml
rekonstituovaného roztoku.
1 Clostridium botulinum
Jednotky Allerganu nejsou použitelné pro jiné přípravky obsahující botulotoxin.
Injekční lahvička s 50 jednotkami.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Prášek pro injekční roztok. Popis přípravku: bílý lyofilizát
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Pokud má závažnost níže uvedených vrásek na obličeji důležitý psychologický dopad na dospělé
pacienty, je VISTABEL indikován k dočasnému zlepšení vzhledu:
• Středně výrazných až výrazných svislých vrásek mezi obočím, které jsou patrné při maximálním zamračení (glabelární vrásky)
• Středně výrazných až výrazných vějířkovitých vrásek, které jsou patrné při širokém úsměvu (havraní stopy)
• Středně výrazných až výrazných vějířkovitých vrásek, které jsou patrné při širokém úsměvu současně se svislými vráskami mezi obočím, které jsou patrné při maximálním zamračení.
4.2 Dávkování a způsob podání
Dávkování
Viz konkrétní doporučení pro jednotlivé indikace uvedené níže.
Jednotky botulotoxinu nejsou u jednotlivých přípravků obsahujících botulotoxin zaměnitelné. Dávky doporučené v jednotkách definovaných dle Allerganu se liší od jiných přípravků obsahujících botulotoxin.
Starší _ pacienti
Klinické údaje z fáze 3 pro VISTABEL jsou u pacientů starších 65 let omezené (viz bod 5.1).
Při použití u starších pacientů není třeba dávku upravovat.
Pediatrická populace
Bezpečnost a účinnost přípravku VISTABEL při léčbě svislých (glabelárních) vrásek mezi obočím, které jsou patrné při maximálním zamračení nebo vějířkovitých vrásek, které jsou patrné při širokém úsměvu,u osob mladších 18 let nebyla prokázána. Použití přípravku VISTABEL se u osob mladších 18 let nedoporučuje (viz bod 4.4).
Způsob podání
VISTABEL by měli podávat pouze lékaři s příslušnou kvalifikací, doloženou odbornou znalostí léčby a s použitím požadovaného vybavení.
Po rekonstituci se VISTABEL musí používat pouze pro jedno podání injekce(í) na pacienta.
Přebytek nevyužitého přípravku se musí zlikvidovat způsobem podrobně popsaným v bodě 6.6.
Měla by být přijata zvláštní opatření pro přípravu přípravku, stejně tak jako pro jeho podání a inaktivaci a likvidaci zbývajícího nepoužitého roztoku (viz bod 4.4 a 6.6).
Doporučený objem injekce na jedno svalové místo je 0,1 ml. Viz rovněž rekonstituční tabulka v bodě 6.6.
Pokyny k použití injekčních lahviček, zacházení s nimi a k jejich likvidaci jsou uvedeny v bodě 6.6.
Je třeba ujistit se, zda VISTABEL není aplikován do krevního řečiště při jeho aplikaci do svislých vrásek mezi obočím, které jsou patrné při maximálním zamračení (glabelární vrásky) nebo do vějířkovitých vrásek, které jsou patrné při širokém úsměvu (havraní stopy), viz bod 4.4.
Návod k aplikaci injekcí k léčbě glabelárních vrásek, které _jsou _patrné _při maximálním zamračení:
Rekonstituovaný VISTABEL (50 jednotek/1,25 ml) je injekčně podáván sterilní jehlou o síle 30 G. 0,1 ml (4 jednotky) do každého z pěti míst vpichu (viz obrázek č. 1): 2 injekce do každého musculus corrugator a 1 injekce do musculus procerus v celkové dávce 20 jednotek.
Před injekcí je nutné pevně přiložit palec nebo ukazováček pod okraj orbity, aby se pod ní zabránilo extravazaci. Jehla by měla být během injekce orientována superiorně a mediálně. Aby se snížilo riziko ptózy očního víčka, nesmí být překročena dávka 4 jednotky do jednoho místa vpichu a rovněž nesmí být překročen počet míst vpichu. Navíc se musíte vyhnout injekci v blízkosti levator palpebrae superioris, zvláště u pacientů s většími komplexy obočí a depresoru (depressor supercilii). Injekce do musculus corrugator se musí provádět v centrální části tohoto svalu, ve vzdálenosti nejméně 1 cm nad obloukem obočí.
Obrázek č. 1:
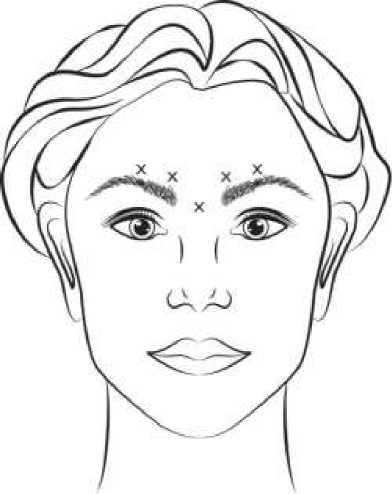
Zlepšení závažnosti glabelámích vrásek , které jsou patrné při maximálním zamračení obecně nastává do jednoho týdne po léčbě. Účinek se prokázal až do 4 měsíců od injekce.
Léčebné intervaly by neměly být častější než každé tři měsíce. V případě selhání léčby nebo sníženého účinku po opakovaných injekcích je zapotřebí použít alternativní léčebné metody.
Návod k aplikaci injekcí k léčbě vějířkovitých vrásek, které jsou patrné při širokém úsměvu:
Rekonstituovaný VISTABEL (50 jednotek/1,25 ml) je injekčně podáván sterilní jehlou o síle 30 G. 0,1 ml (4 jednotky) do každého ze 3 míst vpichu na každé straně (celkem 6 míst vpichu) do laterálního musculus orbicularis oculi v celkové dávce 24 jednotek s celkovým objemem 0,6 ml (12 jednotek na každou stranu).
Aby se snížilo riziko ptózy očního víčka, nesmí být překročena dávka 4 jednotky do jednoho místa vpichu a rovněž tak nesmí být překročen počet míst vpichu. Navíc injekce má být vedena temporálně k okraji orbity tak, aby byla zajištěna bezpečná vzdálenost od svalů, které jsou odpovědné za elevaci víčka.
Injekce má být s hrotem jehly zkoseným směrem vzhůru a od oka. První injekce (A) má být aplikována přibližně 1,5 až 2,0 cm temporálně od spánkové kosti a zevního očního koutku a od spánkové kosti a okraje orbity. Jestliže jsou vějířkovité vrásky nad zevním koutkem a pod ním, aplikujte injekci podle zobrazení na obrázku č. 2. Pokud jsou vějířkovité vrásky především pod zevním koutkem, aplikujte injekci podle zobrazení na obrázku č. 3.
Obrázek č. 2: Obrázek č. 3
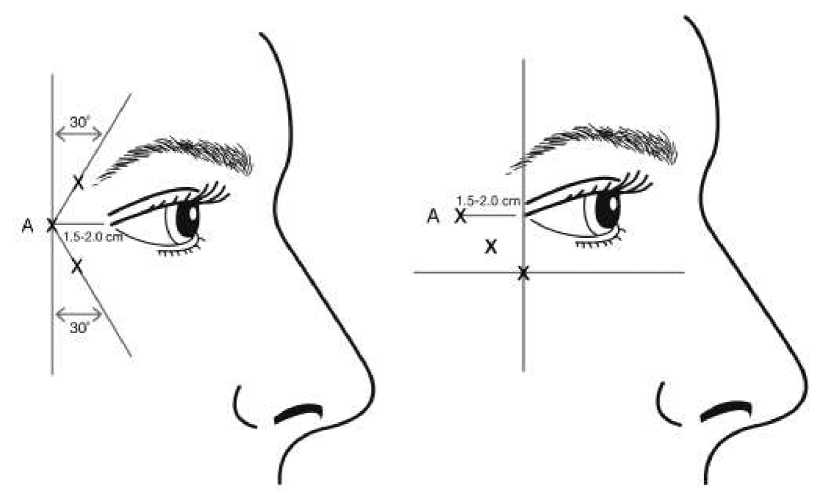
Při léčbě glabelámích vrásek, které jsou patrné při maximálním zamračení a vějířkovitých vrásek, které jsou patrné při širokém úsměvu současně, je dávka pro léčbu vějířkovitých vrásek 24 jednotek a pro léčbu glabelárních vrásek 20 jednotek (viz Návod k aplikaci injekcí k léčbě glabelárních vrásek a obrázek č. 1) v celkové dávce 44 jednotek s celkovým objemem 1,1 ml.
Ke zlepšení výraznosti vějířkovitých vrásek, které jsou patrné při širokém úsměvu, při hodnocení zkoušejícím, došlo během jednoho týdne po léčbě. Léčebný účinek byl prokázán v mediánu 4 měsíců po aplikaci injekce.
Interval mezi dvěma léčbami nesmí být kratší než tři měsíce.
Obecné informace
V případě selhání léčby po první léčebné návštěvě, tj. za jeden měsíc po injekci nedojde k významnému zlepšení vůči výchozímu stavu, je možné zvážit následující přístupy:
• Analýza příčin selhání, např. injekce do nesprávného svalu, nesprávná injekční technika, tvorba protilátek neutralizujících toxin, nedostatečná dávka;
• Přehodnocení významnosti léčby botulotoxinem typu A;
Pokud nedojde k výskytu žádných vedlejších účinků v souvislosti s prvním léčebným zákrokem, proveďte druhý léčebný zákrok, přičemž je nutné zachovat nejméně tříměsíční interval mezi dvěma léčebnými zákroky.
V případě nedostatečné dávky u léčby glabelárních vrásek, které jsou patrné při maximálním zamračení, zahajte druhý léčebný zákrok úpravou celkové dávky až na 40 či 50 jednotek, přičemž vezměte v úvahu analýzu selhání předchozí léčby.
Účinnost a bezpečnost opakovaného podání přípravku VISTABEL nad rámec 12 měsíců nebyla hodnocena.
4.3 Kontraindikace
VISTABEL je kontraindikován
- u osob se známou přecitlivělostí na Clostridium botulinum typ A nebo na kteroukoliv složku přípravku;
- v případě myastenia gravis nebo Eatonova - Lambertova syndromu
- v přítomnosti infekce v navrhovaných místech injekce.
4.4 Zvláštní upozornění a zvláštní opatření pro použití
Konkrétní opatření je zapotřebí přijmout pro přípravu a podání přípravku společně s inaktivací a likvidací zbývajícího nepoužitého roztoku (viz bod 4.2 a 6.6).
Tento léčivý přípravek obsahuje méně než 1 mmol sodíku (23 mg) v jedné dávce, to je v podstatě “bez obsahu sodíku“.
Před podáním přípravku VISTABEL je nutné znát všechny důležité anatomické vztahy a změny způsobené dřívějšími operačními výkony a je nutné se vyhnout aplikaci do zranitelných anatomických struktur.
Nesmí se překračovat doporučené dávkování ani zkracovat intervaly mezi aplikacemi přípravku VISTABEL.
Velmi vzácně se po podání injekce botulotoxinu vyskytuje anafylaktická reakce. Proto by měl být připraven epinefrin (adrenalin) a další prostředky pro zvládnutí anafylaktického šoku.
Pacienti s nerozpoznaným neuromuskulárním onemocněním mohou být ohroženi zvýšeným rizikem klinicky význmných systémových účinků včetně závažné dysfágie a respiračního selhání a to při obvyklých dávkách botulotoxinu A. V někrerých z těchto případů dysfágie trvala několik měsíců a vyžadovala umístění žaludeční sondy (viz bod 4.3).
Zvýšené opatrnosti při použití přípravku VISTABEL je rovněž zapotřebí při léčbě pacientů s amyotrofickou laterální sklerózou nebo s periferními neuromuskulárními poruchami.
Velmi vzácně byly u botulotoxinu hlášeny nežádoucí účinky pravděpodobně spojené s rozšířením toxinu daleko od místa podání (viz bod 4.8). U pacientů léčených terapeutickými dávkami se může projevit nadměrná svalová slabost. Polykací a dechové obtíže jsou závažné a mohou vést k úmrtí. Injekce přípravku VISTABEL se nedoporučuje u pacientů s dysfagií a aspirací v anamnéze.
Pacienti nebo ošetřovatelé by měli být upozorněni, aby vyhledali okamžitě lékařskou pomoc, pokud vzniknou poruchy polykání, řeči nebo dýchání.
Příliš časté nebo vysoké dávky mohou zvýšit riziko tvorby protilátek. Tvorba protilátek může vést k selhání léčby botulini toxinum typu A i při jiných indikacích.
Jak lze očekávat u jakéhokoliv injekčního výkonu, může být injekce spojena s bolestí v místě vpichu, zánětem, parestézií, hypoestézií, citlivostí, otokem/edémem, erytémem, lokalizovanou infekcí, krvácením a/nebo podlitinami. Bolest a/nebo strach z injekce mohou vyvolat vasovagální odpověď včetně přechodné symptomatické hypotenze a synkopy.
Opatrnost při použití přípravku VISTABEL je nutná, pokud je v místě plánované injekce zánět nebo je v cílovém svalu přítomna výrazná slabost nebo atrofie.
Je třeba zajistit, aby VISTABEL nebyl aplikován do krevního řečiště a to jak v případě aplikace do glabelárních vrásek, které jsou patrné při maximálním zamračení nebo při aplikaci do havraních stop, které jsou patrné při širokém úsměvu , viz bod 4.2.
Po léčbě může hrozit riziko ptózy očního víčka, viz bod 4.2 ohledně návodu k aplikaci injekcí a minimalizace tohoto rizika.
Použití přípravku VISTABEL se nedoporučuje u osob mladších 18 let. U pacientů starších 65 let jsou pro přípravek Vistabel k dispozici omezené údaje z klinických studií fáze 3.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Účinek botulotoxinu může být teoreticky potencován aminoglykosidovými antibiotiky, spectinomycinem nebo jinými přípravky, které interferují s neuromuskulárním přenosem (např. neuromuskulární blokátory).
Vzájemný účinek různých botulotoxinových serotypů podaných ve stejnou dobu nebo během několika měsíců není známý. Nadměrná neuromuskulární slabost může být exacerbována při podání jiného botulotoxinu a to v době, kdy ještě nebyl rozpoznán účinek botulotoxinu podaného dříve.
Nebyly provedeny žádné specifické testy, které by doložily možnost klinických interakcí s jinými přípravky. Nebyly hlášeny u této indikace žádné další klinicky významné interakce.
4.6 Fertilita, těhotenství a kojení
Adekvátní údaje o podávání botulotoxinu typu A těhotným ženám nejsou k dispozici. Studie se zvířaty prokázaly reprodukční toxicitu (viz bod 5.3). Potenciální riziko pro člověka není známé.
VISTABEL se nedoporučuje podávat v těhotenství a u žen ve fertilním věku, které nepoužívají antikoncepci.
Kojení
Není známo, zda se VISTABEL vylučuje do lidského mateřského mléka. Během kojení se nedoporučuje VISTABEL používat.
Fertilita
Nejsou k dispozici odpovídající údaje o účincích používání botulotoxinu typu A na plodnost žen ve fertilním věku. Studie na potkaních samcích a samicích prokázaly snížení plodnosti (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly provedeny žádné studie týkající se účinku na schopnost řídit a používat stroje.
VISTABEL může způsobovat astenii, svalovou slabost, závratě a poruchy vidění, které mohou mít vliv na řízení a obsluhování strojů.
4.8 Nežádoucí účinky
a) Celkové
V klinických kontrolovaných studiích glabelárních vrásek, které jsou patrné při maximálním zamračení, byly nežádoucí účinky po léčbě přípravkem VISTABEL hlášeny u 23,5 % pacientů (placebo: 19,2 %). V léčebném cyklu 1 ze stěžejních kontrolovaných klinických studií vějířkovitých vrásek, které jsou patrné při širokém úsměvu (tzv. havraních stop), byly takové příhody hlášeny u 7,6 % (24 jednotek k léčbě pouze vějířkovitých vrásek) a 6,2 % (44 jednotek: 24 jednotek k léčbě vějířkovitých vrásek podávaných současně s 20 jednotkami k léčbě glabelárních vrásek) pacientů v porovnání s 4,5 % u placeba.Nežádoucí účinky mohou souviset s léčbou, injekční technikou nebo s obojím. Obecně nežádoucí účinky vznikly během několika prvních dní po injekci a byly přechodné. Většina nežádoucích hlášených příhod měla mírnou až střední závažnost.
Očekávané farmakologické působení botulotoxinu se projevuje lokální svalovou slabostí. Nicméně, byla hlášena slabost přilehlých svalů a/nebo svalů vzdálených od místa vpichu injekce.
Blefaroptóza, která může souviset s injekční technikou, je ve shodě s farmakologickým působením VISTABELU. Jak lze očekávat u jakéhokoliv injekčního výkonu, lze pozorovat v souvislosti s injekcí bolest/pálení/štípání, edém a/nebo modřiny. Po injekci botulotoxinu byly hlášena také horečka a chřipkový syndrom.
b) Nežádoucí reakce - četnost
Nežádoucí účinky jsou klasifikovány podle třídy orgánových systémů a podle frekvence výskytu do následujících kategorií:
Velmi časté (> 1/10); Časté (> 1/100, < 1/10); Méně časté (> 1/1 000, < 1/100); Vzácné (> 1/10 000, < 1/1 000); Velmi vzácné (< 1/10 000).
Glabelární vrásky
|
Třídy orgánových systémů |
Preferovaná terminologie |
Frekvence |
|
Infekce a infestace |
Infekce |
Méně časté |
|
Psychiatrické poruchy |
Úzkost |
Méně časté |
|
Poruchy nervového systému |
Bolest hlavy, parestézie |
Časté |
|
Závratě |
Méně časté | |
|
Poruchy očí |
Ptóza očního víčka |
Časté |
|
Blefaritida, bolest oka, poruchy vidění (včetně rozmazaného vidění) |
Méně časté | |
|
Gastrointestinální poruchy |
Časté | |
|
Sucho v ústech |
Méně časté | |
|
Poruchy kůže a podkožní tkáně |
Erytém, napětí kůže |
Časté |
|
Otoky (obličeje, očního víčka, periorbitální otoky), fotosenzitivita, svědění, suchá kůže |
Méně časté | |
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Lokalizovaná svalová slabost |
Časté |
|
Záškuby svalů |
Méně časté | |
|
Celkové poruchy a reakce v místě aplikace |
Bolest v obličeji, otok v místě injekce, ekchymóza, bolest v místě injekce, podráždění v místě injekce |
Časté |
|
Chřipkové příznaky, astenie, horečka |
Méně časté |
Vějířkovité vrásky
Následující nežádoucí účinky byly hlášeny v dvojitě zaslepených, placebem kontrolovaných klinických studiích po injekci přípravku VISTABEL 24 jednotek u samotných vějířkovitých vrásek kolem očí:
|
Třídy orgánových systémů |
Preferovaná terminologie |
Frekvence |
|
Poruchy očí |
Otok očního víčka |
Časté |
|
Celkové poruchy a reakce v místě aplikace |
Krvácení v místě aplikace injekce*, hematom v místě aplikace injekce* |
Časté |
|
Bolest v místě aplikace injekce*, parestezie v místě aplikace injekce |
Méně časté |
*nežádoucí účinky spojené se zákrokem
Následující nežádoucí účinky byly hlášeny v dvojitě zaslepených, placebem kontrolovaných klinických studiích po injekci přípravku VISTABEL 44 jednotek (současná léčba vějířkovitých vrásek kolem očí a glabelárních vrásek):
|
Třídy orgánových systémů |
Preferovaná terminologie |
Frekvence |
|
Celkové poruchy a reakce v místě aplikace |
Hematom v místě aplikace injekce* |
Časté |
|
Krvácení v místě aplikace injekce*, bolest v místě aplikace injekce* |
Méně časté |
*nežádoucí účinky spojené se zákrokem
Nebyly pozorovány žádné změny týkající v celkovém bezpečnostním profilu po opakovaném podání.
c) Postmarketingová data (frekvence výskytu není známa)
Po uvedení přípravku na trh pro léčbu glabelárních vrásek, vějířkovitých vrásek a v jiných klinických indikacích byly hlášeny následující nežádoucí reakce nebo lékařsky relevantní nežádoucí účinky:
|
Třídy orgánových systémů |
Preferovaná terminologie |
|
Poruchy imunitního systému |
Anafylaxe, angioedém, sérová nemoc, kopřivka |
|
Poruchy metabolismu a výživy | |
|
Poruchy nervového systému |
Brachiální plexopatie, dysfonie, dysartrie, , hypestezie, svalová slabost, myastenia gravis, periferní neuropatie, parestezie, radikulopatie, synkopa, faciální paréza |
|
Poruchy oka |
Glaukom s uzavřeným úhlem (při léčbě blefarospasmu), lagoftalmus, strabismus, rozmazané vidění a poruchy zraku |
|
Poruchy ucha a labyrintu |
Hypoakuze, tinnitus, závratě |
|
Respirační, hrudní a mediastinální poruchy |
Aspirační pneumonie, dušnost, bronchospasmus, respirační deprese a respirační selhání |
|
Gastrointestinální poruchy |
Bolest břicha, průjem, sucho v ústech, dysfagie, nauzea, zvracení |
|
Poruchy kůže a podkožní tkáně |
Alopecie, psoriatiformní dermatitida, multiformní erytém, hyperhidróza, madaróza, svědění, vyrážka |
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Svalová atrofie, myalgie |
|
Celkové poruchy a reakce v místě aplikace |
Velmi vzácně byly u botulotoxinu hlášeny nežádoucí účinky pravděpodobně spojené s rozšířením toxinu daleko od místa podání (například svalová slabost, dysfagie, zácpa nebo aspirační pneumonie, která může být smrtelná) (viz bod 4.4).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
4.9 Předávkování
Předávkování přípravkem VISTABEL je relativní pojem a závisí na dávce, oblasti vpichu a vlastnostech podkožní tkáně. Nebyly pozorovány žádné případy systémové toxicity vyplývající z náhodné injekce botulotoxinu typu A. Zvýšené dávky mohou způsobit lokální nebo vzdálenou celkovou a silnou neuromuskulární paralýzu. Nebyl hlášen žádný případy požití botulotoxinu typu A.
Bezprostředně po injekci nejsou patrny známky předávkování. Pokud dojde k náhodné injekci nebo požití přípravku, je nutné u pacienta několik dní sledovat známky a příznaky systémové slabosti nebo svalové paralýzy.
Hospitalizace je nutná u pacientů s příznaky otravy botulotoxinem typu A (generalizovaná slabost, ptóza, diplopie, poruchy řeči a polykání nebo parézy respiračních svalů).
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Myorelaxans, periferně účinná látka ATC kód: M03A X01.
Botulotoxin typu A (neurotoxin Clostridium botulinum) blokuje periferní uvolňování acetylcholinu na presynaptických zakončeních cholinergních nervů štěpením SNAP-25, proteinu nezbytného k úspěšnému spojení a uvolnění acetylcholinu z vesikul v nervových zakončeních, což vede k denervaci svalu a tím k paralýze.
Po injekci se toxin rychle a s vysokou afinitou váže na specifické receptory buněčného povrchu. Potom následuje přenos toxinu přes plasmatickou membránu receptory zprostředkovanou endocytózu. Nakonec se toxin uvolňuje do cytosolu. Tento pozdější proces je provázen postupnou inhibicí uvolňováním acetylcholinu, klinické příznaky se projevují během 2-3 dnů, s maximálním účinkem patrným 5-6 týdnů po injekci.
Zotavení po intramuskulární injekci nastává obvykle během 12 týdnů, když nervové zakončení vyroste a znovu se spojí s koncovou ploténkou.
Klinické údaje:
Glabelární vrásky
Do klinických studií bylo zařazeno 537 pacientů se středně až silně závažnými glabelárními vráskami, které jsou patrné při maximálním zamračení.
Injekce přípravku VISTABEL významně snížily závažnost glabelárních vrásek, které jsou patrné při maximálním zamračení až na 4 měsíce podle měření zkoušejícího, které spočívalo v hodnocení glabelární vrásky při maximálním zamračení a globálním hodnocením změny vzhledu glabelárních vrásek, které jsou patrné při maximálním zamračení. Žádný z klinických koncových bodů nezahrnoval objektivní hodnocení psychologického dopadu. Třicet dnů po injekci považovali zkoušející 80 % (325/405) pacientů léčených VISTABELEM za respondenty na léčbu (žádná nebo mírná závažnost při maximálním svraštění) v porovnání se 3 % (4/132) pacientů léčených placebem. V témže časovém bodě mělo 89 % (362/405) pacientů léčených VISTABELEM pocit, že mají střední či větší zlepšení v porovnání se 7 % (9/132) pacientů léčených placebem.
Injekce VISTABELU rovněž významně snížily závažnost glabelárních vrásek v klidu. Z 537 zařazených pacientů mělo 39 % (210/537) středně až silně závažné glaberální vrásky v klidu (15 % nemělo v klidu žádné vrásky). Z nich bylo za třicet dnů po injekci 74 % (119/161) pacientů léčených VISTABELEM považováno za respondenty na léčbu (žádná nebo mírná závažnost) v porovnání se 20 % (10/49) pacientů léčených placebem.
Klinické údaje z fáze 3 pro VISTABEL jsou u pacientů starších 65 let omezené. Pouze 6,0 % (32/537) subjektů bylo starších 65 let a účinnost získaných výsledků byla u této populace nižší.
Vějířkovité vrásky
Do studií bylo zařazeno 1362 pacientů buď pouze se středně výraznými až výraznými vějířkovitými vráskami patrnými při širokém úsměvu (N = 445, studie 191622-098) nebo spolu se středně výraznými až výraznými glabelárními vráskami patrnými při maximálním zamračení (N = 917, studie 191622-099).
Injekce přípravku VISTABEL výrazně snížily závažnost vějířkovitých vrásek, patrných při širokém úsměvu, v porovnání s placebem ve všech časových okamžicích (p < 0,001) až po dobu 5 měsíců. Měření vycházelo z podílu pacientů dosahujících stupně závažnosti vějířkovitých vrásek hodnocených jako žádné nebo mírně výrazné vrásky patrné při širokém úsměvu v obou stěžejních studiích, a to do 150. dne (konec studie) ve studii 191622-098 a do 120. dne (konec prvního léčebného cyklu) ve studii 191622-099). U obou hodnocení, jak hodnocení zkoušejícím tak hodnocení samotným subjektem, byl podíl subjektů dosahujících stupně závažnosti vějířkovitých vrásek patrných při širokém úsměvu, hodnocené jako žádné nebo mírně výrazné vrásky, vyšší u pacientů se středně výraznými vějířkovitými vráskami, které jsou patrné při širokém úsměvu při výchozím stavu v porovnání s pacienty se závažně výraznými vějířkovitými vráskami, které jsou patrné při širokém úsměvu při výchozím stavu. V tabulce č. 1 jsou shrnuty výsledky ve 30. dni, tj. časovém okamžiku primárního cílového parametru účinnosti.
Do studie 191622-104 (navázání na studii 191622-099) bylo zařazeno 101 pacientů dříve randomizováných do skupiny s placebem, během které obdrželi první léčbu v dávce 44 jednotek. Pacienti léčení přípravkem VISTABEL měli statisticky významný přínos z léčby při primárním cílovém parametru účinnosti v porovnání s placebem ve 30. dni po první aktivní léčbě. Míra léčebné odpovědi byla podobná míře odpovědi u skupiny s dávkou 44 jednotek ve 30. dni po první aktivní léčbě ve studii 191622-099. Celkem 123 pacientů obdrželo čtyři cykly přípravku VISTABEL v dávce 44 jednotek k léčbě vějířkovitých a glabelárních vrásek.
Tabulka č. 1.: 30. Den; Hodnocení vějířkovitých vrásek při širokém úsměvu podle zkoušejícího a samotného pacienta - míra respondentů (% pacientů dosahujících stupně závažnosti vějířkovitých vrásek hodnocených jako žádné nebo mírné vrásky)
|
Klinická studie |
Dávka |
VISTABEL |
Placebo |
VISTABEL |
Placebo |
|
Hodnocení zkoušejícím |
Hodnocení samotným pacientem | ||||
|
191622-098 |
24 jednotek (vějířkovité vrásky) |
66,7 %* (148/222) |
6,7 % (15/223) |
58,1 %* (129/222) |
5,4 % (12/223) |
|
191622-099 |
24 jednotek (vějířkovité vrásky) |
54,9 %* (168/306) |
3,3 % (10/306) |
45,8 %* (140/306) |
3,3 % (10/306) |
|
44 jednotek (24 jednotek vějířkovité vrásky; 20 jednotek glabelární vrásky) |
59,0 %* (180/305) |
3,3 % (10/306) |
48,5 %* (148/305) |
3,3 % (10/306) | |
|
*p < 0,001 (V] |
STABEL oproti placebu) | ||||
Zlepšení vzhledu vějířkovitých vrásek, patrných při širokém úsměvu, oproti výchozímu stavu hodnocené samotným subjektem bylo pozorováno u přípravku VISTABEL (24 jednotek a 44 jednotek) v porovnání s placebem ve 30. dni a ve všech časových okamžicích v každém léčebném cyklu u obou stěžejních studií (p < 0,001).
Léčba přípravkem VISTABEL v dávce 24 U rovněž významně snížila závažnost vějířkovitých vrásek v klidu. Z 528 léčených pacientů mělo 63 % (330/528) středně výrazné až výrazné vějířkovité vrásky v klidu při výchozím stavu. Z toho bylo 58 % (192/330) pacientů léčených přípravkem VISTABEL považováno za respondenty na léčbu (žádné nebo mírné vrásky) 30 dní po aplikaci injekce v porovnání s 11 % (39/352) pacientů léčených placebem.
U přípravku VISTABEL (24 jednotek a 44 jednotek) bylo také pozorováno zlepšení ohledně věku a atraktivity hodnocené samotným subjektem v porovnání s placebem za použití dotazníku o výsledcích obličejových vrásek (Facial Line Outcomes, FLO-11) při primárním cílovém parametru ve 30. dni (p < 0,001) a ve všech následujících časových okamžicích u obou stěžejních studií.
Ve stěžejních studiích bylo 3,9 % (53/1362) pacientů starších 65 let. Pacienti v této věkové skupině vykazovali 36% odpověď (ve 30. dni) na léčbu přípravkem VISTABEL (24 jednotek a 44 jednotek), hodnocenou zkoušejícím. Při analýze podle věkových skupin < 50 let a > 50 let vykázaly obě populace statisticky významné zlepšení v porovnání s placebem. Odpověď na léčbu přípravkem VISTABEL v dávce 24 jednotek, hodnocená zkoušejícím, byla nižší u skupiny subjektů ve věku > 50 let než u subjektů ve věku < 50 let (42,0% a 71,2%, v uvedeném pořadí).
Celková odpověď na léčbu vějířkovitých vrásek přípravkem VISTABEL, patrných při širokém úsměvu je nižší (60%) než bylo pozorováno u léčby glabelárních vrásek, patrných při maximálním zamračení (80%).
U 916 pacientů (517 pacientů s dávkou 24 jednotek a 399 pacientů s dávkou 44 jednotek) léčených přípravkem VISTABEL byl proveden rozbor vzorků ke stanovení tvorby protilátek proti hodnocenému léčivu. U žádného pacienta nedošlo k vytvoření neutralizujících protilátek.
5.2 Farmakokinetické vlastnosti
a) Obecná charakteristika léčivé látky:
Studie distribuce u potkanů naznačují pomalou difusi botulotoxinu typu A označeného I125 po injekci do m. gastrocnemius, po které následoval rychlý systémový metabolismus a vyloučení močí. Množství radioaktivně značeného materiálu ve svalu se snížilo na polovinu za přibližně 10 hodin. V místě vpichu se radioaktivita vázala na velké molekuly proteinů, zatímco v plazmě se vázala na malé molekuly, což naznačuje rychlý systémový metabolismus substrátu. Během 24 hodin od podání dávky je 60 % radioaktivity vyloučeno močí. Toxin se pravděpodobně metabolizuje proteázami a molekulární složky se opětovně využijí v normální metabolické cestě.
Klasické studie absorpce, distribuce, biotransformace a eliminace (ADME) léčivé látky nebyly vzhledem k povaze přípravku prováděny.
b) Charakteristika po podání u pacientů:
Je pravděpodobné, že může nastat malá systémová distribuce terapeutických dávek VISTABELU. Klinické studie používající elektromyografickou techniku ukázaly zvýšení elektrofyziologické neuromuskulární aktivity ve svalech vzdálených od místa injekce, která nebyla provázena klinickými příznaky či symptomy.
5.3 Předklinické údaje vztahující se k bezpečnosti
V reprodukčních studiích u myší, potkanů a králíků byla pozorována embryotoxicita při podávání vysokých dávek (zpožděná osifikace a snížená fetální hmotnost).
U těchto druhů nebyly pozorovány žádné teratogenní účinky.
Nežádoucí účinky na samčí plodnost a samičí estrogenní cyklus a fertilitu byly pozorovány u potkanů pouze při podání vysokých dávek.
Studie na akutní toxicitu, toxicitu po opakovaném podání, lokální toleranci, mutagenicitu, antigenicitu a krevní kompatibilitu neprokázaly při podávání klinicky relevantních dávek žádné neobvyklé místní nebo celkové nežádoucí účinky.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Lidský albumin Chlorid sodný
6.2 Inkompatibility
Protože nebyly provedeny studie inkompatibility, nesmí být VISTABEL mísen s žádnými jinými léčivými přípravky.
6.3 Doba použitelnosti
3 roky.
Po rekonstituci se doporučuje roztok okamžitě použít. Nicméně byla prokázána chemická a fyzikální stabilita po dobu 24 hodin při teplotě 2 °C - 8 °C.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C).
Podmínky uchovávání rekonstituovaného léčivého přípravku viz bod 6.3.
6.5 Druh obalu a obsah balení
Prášek v injekční lahvičce (sklo typu I) se zátkou (chlorbutylový kaučuk), těsněním (hliník);
Injekční lahvička 50 jednotek definovaných dle Allerganu botulotoxinu typu A - balení s jednou nebo balení se dvěma lahvičkami
Na trhu nemusí být všechny velikosti balení
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Rekonstituce má být provedena v souladu s pravidly správné praxe, zvlášte pak s ohledem na aseptické podmínky.
VISTABEL se musí rekonstituovat injekčním roztokem 0,9 % chloridu sodného bez konzervačních látek. Podle dále uvedené rekonstituční tabulky se musí do injekční stříkačky natáhnout požadované množství injekčního roztoku chloridu sodného 9 mg/ml (0,9 %), aby se získal rekonstituovaný roztok o koncentraci 4 jednotky/0,1 ml;
|
Množství rozpouštědla přidaného do injekční lahvičky 50 jednotek (roztok chloridu sodného 0,9 %) |
Výsledná dávka (jednotek na 0,1 ml) |
|
1,25 ml |
4,0 jednotky |
Střední část pryžové zátky se musí očistit alkoholem.
Aby se zabránilo denaturaci přípravku VISTABEL, je roztok připraven pomalým injekčním vstřikováním rozpouštědla do injekční lahvičky a jemným otáčením injekční lahvičky, aby se zabránilo tvorbě bublin. Injekční lahvička se musí zlikvidovat, pokud vakuum nevytáhne rozpouštědlo do injekční lahvičky. Jakmile dojde k rekonstituci, roztok je nutné před použitím vizuálně prohlédnout. Podán může být pouze čirý, bezbarvý až slabě žlutý roztok bez částic.
Je nutné, aby se VISTABEL používal pouze pro léčbu jednoho jediného pacienta během jediného léčebného zákroku
Postup pro bezpečnou likvidaci použitých injekčních lahviček, injekčních stříkaček a materiálů:
Bezprostředně po použití a před likvidací se musí inaktivovat nepoužitý rekonstituovaný roztok VISTABEL v injekční lahvičce a/nebo injekční stříkačce 2 ml roztoku chlornanu sodného naředěného na 0,5% nebo 1% a musí se zlikvidovat v souladu s místními požadavky.
Použité injekční lahvičky, injekční stříkačky a materiály by se neměly vyprazdňovat a musí se ukládat do vhodných nádob a likvidovat jako zdravotnický biorizikový materiál v souladu s místními požadavky.
Doporučení v případě nehody při manipulaci s botulotoxinem:
V případě nehody při manipulaci s přípravkem, práškem či rekonstituovaným roztokem, se musí
neprodleně naplnit příslušná opatření popsaná dále.
• Toxin je velmi citlivý na teplo a určité chemické látky.
• Jakékoliv rozlité množství se musí vytřít: buď absorpčním materiálem napuštěným roztokem chlornanu sodného (roztok Javel) v případě vakuově vysušeného přípravku nebo suchým absorpčním materiálem v případě rekonstituovaného přípravku.
• Kontaminované povrchy se musí vyčistit absorpčním materiálem napuštěným roztokem chlornanu sodného (roztok Javel) a poté osušit.
• Jestliže bude injekční lahvička rozbita, posbírejte kusy skla a vytřete přípravek, jak je shora uvedeno, dejte pozor, abyste se nepořezali.
• Jestliže se rozlije, omyjte roztokem chlornanu sodného, poté důkladně opláchněte velkým množstvím vody.
• Při vniknutí do očí důkladně oči propláchněte velkým množstvím vody nebo roztokem pro výplach očí.
• Jestliže dojde k poranění obsluhy (pořezání, bodnutí), postupujte, jak je uvedeno shora a podnikněte příslušná lékařská opatření podle injekčně podané dávky.
Tento návod k použití přípravku, zacházení s ním se musí přísně dodržovat.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
ALLERGAN PHARMACEUTICALS IRELAND
Westport
County Mayo
Irsko
8. REGISTRAČNÍ ČÍSLO(A)
63/688/07-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
7.11.2007/16.5.2008
10. DATUM REVIZE TEXTU
24.2.2015
13