Lifsar Pulmojet 50 Mikrogramů/500 Mikrogramů
Sp.zn.sukls71467/2014
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. NÁZEV PŘÍPRAVKU
Lifsar Pulmojet 50 mikrogramů/500 mikrogramů prášek k inhalaci
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna inhalace poskytuje dodanou dávku (dávku vycházející z náustku) salmeterolum 45 mikrogramů (jako salmeteroli xinafoas) a fluticasoni propionas 465 mikrogramů. To odpovídá odměřené dávce salmeterolum 50 mikrogramů (jako salmeteroli xinafoas) a fluticasoni propionas 500 mikrogramů.
Pomocná látka se známým účinkem: obsahuje až 7 mg monohydrátu laktosy na odměřenou dávku.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Prášek k inhalaci.
Inhalátor obsahuje bílý prášek. Tělo inhalátoru je šedé a bílé s šedým podstavcem a náustkem, bílým krytem a fialovým nebo šedým spodním krytem.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek Lifsar Pulmojet je indikován k symptomatické léčbě dospělých pacientů s chronickou obstrukční plicní nemocí (CHOPN), s prebronchodilatační hodnotou FEV1 < 60 % náležité hodnoty a s anamnézou opakujících se exacerbací, kteří mají významné příznaky navzdory pravidelné bronchodilatační terapii.
Přípravek Lifsar Pulmojet je určen pouze pro dospělé ve věku 18 let a starší.
4.2 Dávkování a způsob podání Dávkování
Cesta podání: inhalační podání
Pacienty je třeba poučit, že pro optimální prospěch je třeba používat přípravek Lifsar Pulmojet pravidelně, každý den, dokonce i tehdy, pokud nejsou přítomny žádné příznaky.
Přípravek Lifsar Pulmojet je k dispozici pouze v síle 50 mikrogramů salmeterolu a 500 mikrogramů flutikason-propionátu v jedné odměřené dávce.
Doporučené dávky
Dospělí:
Jedna inhalace 50 mikrogramů salmeterolu a 500 mikrogramů flutikason-propionátu dvakrát denně.
Zvláštní skupiny pacientů
Není zapotřebí upravovat dávku u starších pacientů nebo u pacientů s poruchou funkce ledvin.
O použití přípravku Lifsar Pulmojet u pacientů s poruchou funkce jater nejsou k dispozici žádné údaje.
Pediatrická populace
Přípravek Lifsar Pulmojet není určen k použití u dětí a dospívajících mladších 18 let.
Způsob podání
Pacienty je třeba poučit o správném použití inhalátoru (viz příbalová informace pro pacienty).
Náustek
Otvory pro
přívod vzduchu
s indikátorem
pro kontrolu
Okénko
počtu dávek
připravenosti
dávky
Poznámka: Číselný údaj zobrazený v okénku s indikátorem počtu dávek se vztahuje k počátečnímu počtu inhalací (60) v daném inhalátoru a zůstává stejný, i když je inhalátor prázdný. Zelený proužek v okénku s indikátorem počtu dávek ukazuje, kolik inhalací přibližně zbývá (viz níže text v části „Kdy je třeba inhalátor vyměnit“).
Základní pravidla pro použití přípravku Lifsar Pulmojet
1. OTEVŘENÍ: Odstranit bílý kryt.
2. INHALACE: Obemknout rty náustek a hluboce se nadechnout.
3. UZAVŘENÍ DO ZACVAKNUTÍ: Našroubovat kryt náustku na inhalátor a dotáhnout, až se
ozve cvaknutí.
Návod k použití
Obr. 03
Obr. 05
1. OTEVŘENÍ
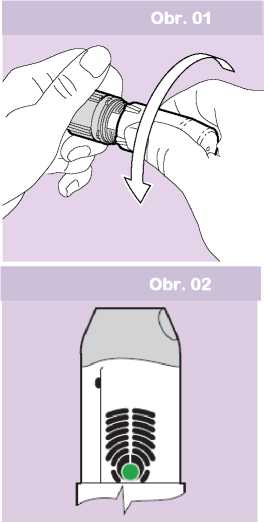
• Uchopit inhalátor do obou rukou: jednou rukou za šedý
podstavec a druhou za ochranný bílý kryt. Inhalátor lze držet v jakékoliv poloze.
• Odšroubovat bílý ochranný kryt od šedého podstavce
otáčením obou části v opačném směru (Obr. 01). Pacient ucítí slabý odpor, jakmile je kryt odšroubován do jedné poloviny.
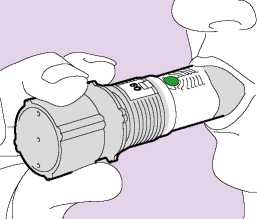
• Zelený indikátor v okénku pro kontrolu připravenosti dávky
potvrzuje, že inhalátor je připraven k použití (Obr. 02).
2. INHALACE
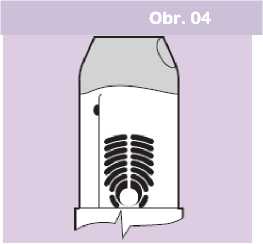
• Uchopit inhalátor pevně za šedý podstavec tak, aby
podstavec směřoval od úst. Pomalu vydechnout tak dlouho, dokud to bude pohodlné.
Pacient nesmí přes inhalátor dýchat.
• Obemknout rty šedý náustek (Obr. 03) tak, aby rty
nezakrývaly některý z otvorů pro přívod vzduchu. Pacient nesmí náustek žvýkat nebo kousat.
• Pacient musí vdechnout dávku ústy (nikoli nosem), tak
hluboce a silně, jak jen bude schopen.
• Pacient se má nadechovat tak dlouho, dokud neuslyší slabé
„lupnutí“. Slabé „lupnutí“ během inhalace signalizuje, že dávka byla uvolněna.
• Pacient má poté zadržet dech na 5 až 10 sekund nebo tak
dlouho, dokud to nezačne být nepohodlné, a následně má pomalu vydechnout nosem a začít normálně dýchat.
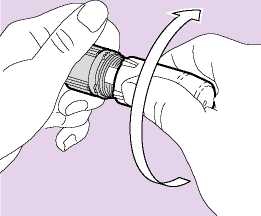
• Zelený indikátor v okénku pro kontrolu připravenosti dávky
by měl nyní zmizet, což ukazuje, že dávka byla úspěšně aplikována (Obr. 04).
3. UZAVŘENÍ DO ZACVAKNUTÍ
• Nasadit bílý ochranný kryt zpět na šedý podstavec a
šroubovat, dokud se neozve cvaknutí (Obr. 05).
• Je důležité zašroubovat kryt až nadoraz, dokud se neozve
cvaknutí, protože se tím aktivuje další dávka léku. Rysky na krytu a podstavci by měly být v poloze proti sobě.
• Pokud je na základě pokynů lékaře zapotřebí více než jedna
inhalace, pacient zopakuje výše uvedené kroky.
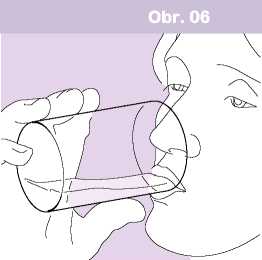
• Pacienty je třeba poučit, že si mají po poslední inhalaci každé dávky vypláchnout ústa vodou (a po vypláchnutí vodu vyplivnout) a/nebo si vyčistit zuby, aby se minimalizovalo riziko orofaryngeální kandidózy a chrapotu (Obr. 06).
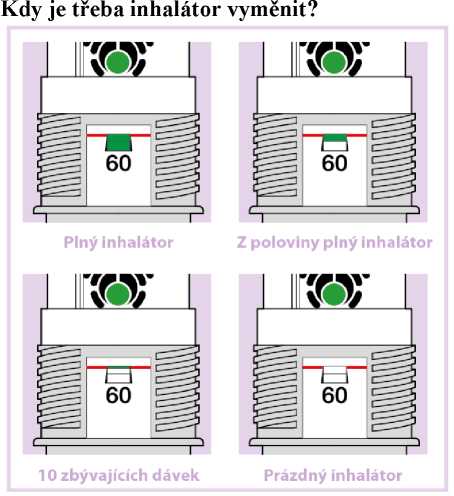
Počáteční počet inhalací v inhalátoru (60) je znázorněn v okénku s indikátorem počtu dávek (Obr. 07). Tento údaj zůstává stejný i tehdy, pokud je inhalátor prázdný.
Zelený proužek v okénku s indikátorem počtu dávek ukazuje, kolik inhalací léku v inhalátoru přibližně zbývá. Držte inhalátor kolmo ve výšce očí a zkontrolujte, kolik dávek zbývá v zásobníku.
Jakmile se zelený proužek dostane na úroveň červené linie, znamená to, že v inhalátoru zbývá přibližně 10 inhalací. (Obr. 07 - 10 zbývajících dávek). Pacient může i nadále používat inhalátor, ale měl by navštívit lékaře a vyzvednout si nový předpis.
Jakmile zelený proužek zcela zmizí, je inhalátor prázdný (Obr. 07 - Prázdný inhalátor)
Čištění inhalátoru
• Náustek lze čistit otřením čistým suchým hadříkem. Nepoužívejte k čištění náustku vodu ani
jinou tekutinu.
• V době, kdy se inhalátor nepoužívá, musí být bílý ochranný kryt inhalátoru vždy zavřený.
• Chraňte inhalátor před vlhkostí.
Další informace o inhalátoru
• Bílý ochranný kryt se otáčí a „cvaká“ dokonce i tehdy, když je inhalátor prázdný.
• Zvuk slyšitelný při zatřepání inhalátorem vzniká pohybem vysoušedla, a nikoli vlastního léku.
Podle tohoto zvuku proto nelze poznat, kolik léku v inhalátoru zbývá.
• Inhalátor nelze nastavit na aplikaci více než jedné dávky.
• Pokud inhalátor upadne bez krytu, je zapotřebí kryt znovu nasadit před aplikací další dávky.
4.3 Kontraindikace
Hypersenzitivita na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Dochází-li u pacientů s CHOPN k exacerbaci, je obvykle indikována léčba systémovými kortikosteroidy, pacienti mají být proto poučeni, aby vyhledali lékařskou pomoc, pokud se příznaky během používání přípravku Lifsar Pulmojet zhorší.
Léčba přípravkem Lifsar Pulmojet nesmí být náhle ukončena kvůli možné exacerbaci.
U pacientů s CHOPN se může přerušení terapie rovněž pojit se symptomatickou dekompenzací a musí na ni dohlížet lékař.
Přípravek Lifsar Pulmojet, stejně jako ostatní inhalační přípravky obsahující kortikosteroidy, je třeba podávat s opatrností u pacientů s aktivním nebo klidovou formou plicní tuberkulózy a mykotické, virové či jiné infekce dýchacích cest. Je nezbytné okamžitě zavést vhodnou léčbu, pokud je indikována.
Vzácně může přípravek Lifsar Pulmojet ve vysokých terapeutických dávkách vyvolat srdeční arytmie, jako např. supraventrikulární tachykardii, extrasystoly a fibrilaci síní, a mírné přechodné snížení draslíku v séru. Proto se musí přípravek Lifsar Pulmojet používat opatrně u pacientů s těžkými kardiovaskulárními poruchami nebo abnormálním srdečním rytmem a u pacientů s diabetem mellitem, tyreotoxikózou, nekorigovanou hypokalemií nebo u pacientů s predispozicí k hypokalemii.
Velmi vzácně bylo hlášeno zvýšení hladiny glukosy v krvi (viz bod 4.8) a tuto skutečnost musí vzít v úvahu lékař předepisující tento lék pacientům s diabetem mellitem.
Stejně jako u ostatních inhalačních přípravků může dojít ke vzniku paradoxního bronchospasmu, který se projevuje okamžitým zhoršením pískotů (hvízdavého dýchání) a zhoršením dušnosti po podání dávky. Paradoxní bronchospasmus je reakcí na rychle působící bronchodilatancia a musí být ihned léčen. Léčba přípravkem Lifsar Pulmojet musí být okamžitě ukončena, pacient vyšetřen a v případě nutnosti má být nasazena jiná léčba.
U léčby p2 agonisty byly hlášeny farmakologické vedlejší účinky, jako jsou třes, palpitace a bolest hlavy, které bývají však přechodné a jejich výskyt se snižuje při pravidelné léčbě.
Systémové účinky se mohou vyskytnout u kteréhokoli inhalačního kortikosteroidu, zvláště při vysokých dávkách předepsaných dlouhodobě. Pravděpodobnost výskytu těchto účinků je mnohem menší než při podávání perorálních kortikosteroidů. Možné systémové účinky zahrnují Cushingův syndrom, Cushingovu nemoc, adrenální supresi, snížení kostní minerální denzity, kataraktu, glaukom a vzácněji i řadu psychických nebo behaviorálních účinků, včetně psychomotorické hyperaktivity, poruch spánku, úzkosti, deprese nebo agresivity (zvláště u dětí). Proto je důležité, aby pacienti byli pravidelně sledováni a aby se dávka inhalačního kortikosteroidů snížila na nejnižší dávku, při které je zachována účinná kontrola nemoci.
Dlouhodobá léčba pacientů vysokými dávkami inhalačních kortikosteroidů může vést k adrenální supresi a akutní adrenální krizi. Velmi vzácné případy adrenální suprese a akutní adrenální krize byly rovněž popsány u dávek flutikason-propionátu mezi 500 mikrogramů a méně než 1000 mikrogramů. Situace, které by mohly potencionálně spustit akutní adrenální krizi, zahrnují trauma, chirurgický zákrok, infekci nebo jakékoli rychlé snížení dávkování. Příznaky, které se objeví, jsou obvykle nespecifické a mohou zahrnovat nechutenství, bolest břicha, pokles tělesné hmotnosti, únavu, bolest hlavy, nauzeu, zvracení, hypotenzi, poruchy vědomí, hypoglykemii a záchvaty. V obdobích stresové zátěže nebo elektivních chirurgických výkonů je třeba zvažovat doplňkové krytí systémovým kortikosteroidem.
Přínos z inhalační léčby flutikason-propionátem by měl zahrnovat minimalizaci potřeby perorálně podávaných kortikosteroidů, u pacientů převedených z perorálních kortikosteroidů však může po značnou dobu přetrvávat riziko poškození funkční rezervy nadledvin. U těchto pacientů je proto zapotřebí zvýšená opatrnost a pravidelné sledování funkce nadledvin. Riziko může být přítomno také u pacientů, kteří mají v anamnéze urgentní léčbu vysokými dávkami kortikosteroidů. Tuto možnost reziduálního zhoršení je třeba vzít v úvahu vždy v případě naléhavého stavu a v určitých elektivních situacích s vysokou pravděpodobností stresové zátěže, a musí být zvážena náležitá léčba kortikosteroidy. Před elektivním výkonem může být zapotřebí konziliární vyšetření pro zhodnocení rozsahu poruchy funkce nadledvin.
Ritonavir může výrazně zvýšit koncentraci flutikason-propionátu v plazmě. Proto je třeba se vyhýbat současnému podávání, pokud předpokládaný přínos pro pacienta nepřeváží riziko systémových vedlejších účinků léčby kortikosteroidy. Existuje rovněž zvýšené riziko systémových vedlejších účinků, jakmile se kombinuje flutikason-propionát s jinými silnými inhibitory CYP3A (viz bod 4.5).
Ve studii TORCH u pacientů s CHOPN používajících salmeterol/flutikason-propionát 50/500 mikrogramů 2x denně ve srovnání s placebem a ve studiích SCO40043 a SCO100250 u pacientů užívajících nižší, pro CHOPN neschválenou dávku salmeterol/flutikason-propionát 50/250 mikrogramů 2x denně ve srovnání se salmeterolem 50 mikrogramů 2x denně, byl hlášen zvýšený výskyt infekcí dolních cest dýchacích (zvláště pneumonie a bronchitidy) (viz body 4.8 a bod 5.1). Podobná incidence pneumonie ve skupině se salmeterolem/flutikason-propionátem byla pozorována napříč všemi klinickými studiemi. Ve studii TORCH byli starší pacienti, pacienti s nižším body mass indexem (<25 kg/m2) a pacienti s velmi závažnou formou onemocnění (FEV1 < 30 % náležité hodnoty) více ohrožení rizikem vzniku pneumonie bez ohledu na léčbu. U pacientů s CHOPN mají lékaři být ostražití pro možnost vývoje pneumonie a dalších infekcí dolních cest dýchacích, jelikož klinické rysy těchto infekcí a exacerbací se často překrývají. Jestliže pacient se závažnou formou CHOPN prodělal pneumonii, léčba přípravkem Lifsar Pulmojet má být přehodnocena.
Údaje z velké klinické studie (Salmeterol Multi-Center Asthma Research Trial, SMART) naznačily, že u afroamerických pacientů je zvýšené riziko závažných respiračních nežádoucích příhod nebo úmrtí při užívání salmeterolu ve srovnání s placebem (viz bod 5.1). Není známo, zda to bylo zapříčiněno farmakogenetickými či jinými faktory. Proto je třeba požádat pacienty černošského afrického nebo afrokaribského původu, aby pokračovali v léčbě, ale aby vyhledali lékařskou pomoc, jakmile astmatické příznaky nejsou pod kontrolou nebo se zhoršují při používání přípravku Lifsar Pulmojet.
Souběžné užívání systémově podávaného ketokonazolu významně zvyšuje systémovou expozici salmeterolu. To může vést ke zvýšení výskytu systémových účinků (např. prodloužení intervalu QTc a palpitacím). Souběžné léčbě ketokonazolem nebo jinými silnými inhibitory CYP3A4 je proto třeba se vyhnout, pokud přínosy léčby salmeterolem nepřeváží potenciálně zvýšené riziko systémových vedlejších účinků (viz bod 4.5).
Přípravek Lifsar Pulmojet obsahuje monohydrát laktosy až 7 mg v jedné dávce. Toto množství obvykle nezpůsobuje problémy u osob s intolerancí laktosy. Pacienti se vzácnými dědičnými problémy s intolerancí galaktosy, vrozeným deficitem laktázy nebo malabsorpcí glukosy a galaktosy by tento přípravek neměli užívat.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Beta-adrenergní blokátory mohou oslabit nebo antagonizovat účinek salmeterolu. Je třeba se vyhýbat neselektivním i selektivním beta-blokátorům, pokud neexistují přesvědčivé důvody pro jejich použití. Léčba p2 agonisty může vést k potenciálně závažné hypokalemii. Tento účinek může být zesílen současnou léčbou xantinovými deriváty, kortikosteroidy a diuretiky.
Souběžné použití jiných beta-adrenergních léků může mít potencionálně aditivní účinek.
Flutikason-propionát
Za normálních okolností se nízkých koncentrací flutikason-propionátu v plazmě dosáhne po inhalačním podání vzhledem k extenzivnímu metabolismu látky během prvního průchodu a vysoké systémové clearance zprostředkované izoenzymem 3A4 cytochromu P450 ve střevech a játrech. Proto jsou klinicky významné interakce s jinými léčivými přípravky, zprostředkované flutikason-propionátem, nepravděpodobné.
Ve studii interakce u zdravých jedinců užívajících intranazální flutikason-propionát s ritonavirem (velmi silný inhibitor cytochromu P450 3A4) v dávce 100 mg dvakrát denně, došlo ke zvýšení koncentrace flutikason-propionátu v plazmě více než stonásobně, což vedlo k nápadně sníženým koncentracím kortizolu v séru. Informace o této interakci chybí u inhalačního flutikason-propionátu, ale očekává se značné zvýšení plazmatických hladin flutikason-propionátu. Byly hlášeny případy Cushingova syndromu a adrenální suprese. Této kombinaci je třeba se vyhýbat, pokud výhody nepřeváží zvýšené riziko systémových vedlejších účinků léčby kortikosteroidy.
V malé studii se zdravými dobrovolníky o něco slabší inhibitor CYP3A ketokonazol způsobil zvýšení expozice flutikason-propionátu po jednorázové inhalaci o 150 %. To vedlo k většímu snížení plazmatické hladiny kortisolu v porovnání se samotným podáním flutikason-propionátu. Očekává se také, že souběžná léčba jinými silnými inhibitory CYP3A, jako je itrakonazol, a středně silnými inhibitory CYP3A, jako je erythromycin, rovněž zvýší systémovou expozici flutikason-propionátu a riziko systémových nežádoucích účinků. Pokud je to možné, doporučuje se při podávání opatrnost a dlouhodobé léčbě těmito léky je třeba se vyhnout.
Salmeterol
Silné inhibitory CYP3A4
Souběžné podávání ketokonazolu (400 mg perorálně jednou denně) a salmeterolu (50 mikrogramů inhalačně dvakrát denně) 15 zdravým subjektům po dobu 7 dnů vedlo k významnému zvýšení plazmatické expozice salmeterolu (1,4 násobku Cmax a 15 násobku AUC). To může vést ke zvýšení výskytu dalších systémových účinků léčby salmeterolem (např. k prodloužení intervalu QT a k palpitacím) ve srovnání s léčbou samotným salmeterolem nebo ketokonazolem (viz bod 4.4).
Nebyly pozorovány žádné klinicky významné účinky na krevní tlak, srdeční frekvenci a hladinu glukosy a draslíku v krvi. Současné podávání s ketakonazolem nezvýšilo eliminační poločas salmeterolu, ani nezvýšilo nahromadění salmeterolu při opakovaném dávkování.
Souběžnému podávání ketokonazolu je třeba se vyvarovat, pokud výhody nepřeváží potencionálně zvýšené riziko systémových vedlejších účinků léčby salmeterolem. Pravděpodobně existuje podobné riziko interakce s dalšími silnými inhibitory CYP3A4 (jako jsou itrakonazol, telithromycin, ritonavir).
Středně silné inhibitory CYP 3A4
Souběžné podávání erythromycinu (500 mg perorálně třikrát denně) a salmeterolu (50 mikrogramů inhalačně dvakrát denně) 15 zdravým subjektům po dobu 6 dnů vedlo k malému, statisticky nevýznamnému zvýšení expozice salmeterolu (1,4 násobku Cmax a 1,2 násobku AUC). Souběžné podávání s erythromycinem nebylo spojeno s žádnými vážnými nežádoucími účinky.
4.6 Fertilita, těhotenství a kojení
Fertilita
Neexistují žádné údaje u lidí. Studie na zvířatech však neprokázaly žádné účinky salmeterolu nebo flutikason-propionátu na fertilitu.
Menší množství údajů získaných u těhotných žen (výsledky z 300-1000 těhotenství) neukazují na malformační nebo fetoneonatální toxicitu salmeterolu a flutikason- propionátu. Studie na zvířatech ukázaly reprodukční toxicitu po podávání B2 agonisty adrenoreceptorů a glukokortikosteroidů (viz bod 5.3).
Podávání přípravku Lifsar Pulmojet těhotným ženám se má zvážit jen v případě, pokud očekávaný přínos pro matku je větší než možné riziko pro plod.
Při léčbě těhotných žen se má používat nejnižší účinná dávka flutikason-propionátu potřebná k zachování přiměřené kontroly nemoci.
Kojení
Není známo, zda se salmeterol a flutikason-propionát a jejich metabolity vylučují do mateřského mléka.
Studie ukázaly, že se salmeterol a flutikason-propionát a jejich metabolity vylučují do mléka samic potkanů.
Riziko pro kojené novorozence/kojence nelze vyloučit. Je třeba se rozhodnout, zda přerušit kojení nebo přerušit léčbu přípravkem Lifsar Pulmojet, a vzít přitom v úvahu výhody kojení pro dítě a výhody léčby pro ženu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Přípravek Lifsar Pulmojet nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Přípravek Lifsar Pulmojet obsahuje salmeterol a flutikason-propionát, lze očekávat typ a závažnost nežádoucích účinků pojících se s každou z těchto léčivých látek. Při souběžném podávání těchto dvou látek se neobjevují žádné další nežádoucí účinky.
Nežádoucí účinky, které se pojí se salmeterolem/flutikason-propionátem, jsou uvedeny níže a jsou seřazeny podle třídy orgánových systémů a podle četnosti. Četnosti jsou definovány následovně: Velmi časté (> 1/10); časté (>1/100 a < 1/10); méně časté (> 1/1 000 a < 1/100); vzácné (> 1/10 000 až < 1/1 000) velmi vzácné (< 1/10 000) a neznámé (z dostupných údajů nelze určit). Četnosti byly odvozeny z údajů v klinických studiích. Výskyt u placeba se nebral v úvahu.
|
Třída orgánových systémů |
Nežádoucí účinky |
Frekvence výskytu |
|
Infekce a infestace |
Kandidóza dutiny ústní a hrdla |
Časté |
|
Časté u’5 | ||
|
Bronchitida |
Časté 1 3 | |
|
Poruchy imunitního systému |
Hypersenzitivní reakce s následujícími projevy: - Kožní hypersenzitivní reakce - Respirační příznaky (dyspnoe) - Angioedém (edém obličeje a orofaryngeální edém) , - Anafylaktické reakce včetně anafylaktického šoku - Respirační příznaky (bronchospasmus) |
Méně časté Vzácné |
|
Endokrinní poruchy |
Cushingův syndrom, Cushingova nemoc, adrenální suprese, retardace růstu u dětí a dospívajících, pokles minerální kostní denzity |
Vzácné 4 |
|
Poruchy metabolismu a výživy |
Hypokalemie |
Časté 3 |
|
Hyperglykemie |
Méně časté 4 | |
|
Psychiatrické poruchy |
Úzkost, porucha spánku |
Méně časté |
|
Změny chování, včetně psychomotorické hyperaktivity a podrážděnosti (převážně u dětí) |
Vzácné | |
|
Deprese, agresivita (převážně u dětí) |
Neznámé | |
|
Poruchy nervového systému |
Velmi časté 1 | |
|
Méně časté |
|
Poruchy oka |
Katarakta |
Méně časté |
|
Glaukom |
Vzácné 4 | |
|
Srdeční poruchy |
Palpitace, tachykardie, fibrilace síní, angina pectoris |
Méně časté |
|
Srdeční arytmie (včetně supraventrikulární tachykardie a extrasystol) |
Vzácné | |
|
Respirační, hrudní a mediastinální poruchy |
Nazofaryngitida |
Velmi časté 2,3 |
|
Podráždění hrdla, chrapot/dysfonie |
Časté | |
|
Sinusitida |
Časté1,3 | |
|
Paradoxní bronchospasmus |
Vzácné 4 | |
|
Poruchy kůže a podkožní tkáně |
Kontuze |
Časté 1,3 |
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Svalové křeče, artralgie, myalgie |
Časté |
|
Traumatické zlomeniny |
Časté 1,3 |
1 Hlášené často u placeba
2 Hlášené velmi často u placeba
3Hlášeno během 3 let ve studii s CHOPN
4 Viz bod 4.4
5 Viz bod 5.1
Popis vybraných nežádoucích účinků
Byly hlášeny farmakologické nežádoucí účinky léčby B2 agonisty, jako je třes, palpitace a bolest hlavy, které však mají přechodnou tendenci a snižují se při pravidelné terapii.
Stejně jako u ostatních inhalačních přípravků může dojít ke vzniku paradoxního bronchospasmu se zhoršením hvízdavého dýchání (pískoty) a dušnosti po podání dávky. Paradoxní bronchospasmus je reakcí na rychle působící bronchodilatancia a musí být ihned léčen. Léčba přípravkem Lifsar Pulmojet musí být okamžitě ukončena, pacient vyšetřen a v případě nutnosti má být nasazena jiná léčba.
Vzhledem k obsahu flutikason-propionátu se může u některých pacientů vyskytnout chrapot a kandidóza (moučnivka) dutiny ústní a hrdla a vzácně u některých pacientů i jícnu. Chrapot i výskyt kandidózy lze zmírnit výplachem dutiny ústní vodou a/nebo vyčištěním zubů po použití přípravku. Symptomatickou kandidózu dutiny ústní a hrdla lze léčit lokální antimykotickou léčbou při současném pokračování podávání přípravku Lifsar Pulmojet.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
Webové stránky: http://www.sukl.cz/nahlasit-nezadouci-ucinek
4.9 Předávkování
K dispozici nejsou žádné údaje z klinických hodnocení týkající se předávkování přípravkem Lifsar Pulmojet, níže jsou však uvedeny údaje o předávkování jednotlivými léčivými látkami:
Mezi známky a příznaky předávkování salmeterolu patří závrať, zvýšení systolického krevního tlaku, třes, bolest hlavy a tachykardie. Jestliže musí být léčba přípravkem Lifsar Pulmojet přerušena v důsledku předávkování p agonistickou složkou přípravku, je třeba zvážit zajištění vhodné náhradní léčby kortikosteroidy. Navíc může dojít ke vzniku hypokalemie, a proto je zapotřebí sledovat hladiny draslíku v séru. Dále je třeba zvážit substituci draslíku.
Akutní: inhalace dávek flutikason-propionátu převyšujících doporučené dávky může vést k dočasné supresi adrenální funkce. Urgentní zásah není nutný, neboť adrenální funkce se za několik dní obnoví, jak potvrzují měření kortizolu v plazmě.
Chronické předávkování inhalačním flutikason-propionátem: Viz bod 4.4: riziko suprese adrenální funkce: Je třeba monitorovat adrenální rezervu a může být nutná léčba systémovými kortikosteroidy. Po stabilizaci je třeba pokračovat v léčbě inhalačním kortikosteroidem v doporučené dávce.
V případech akutního i chronického předávkování flutikason-propionátem je třeba pokračovat v léčbě přípravkem Lifsar Pulmojet ve vhodné dávce pro udržení kontroly příznaků.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Sympatomimetika inhalační; Sympatomimetika v kombinaci s kortikosteroidy nebo jinými léky, s výjimkou anticholinergik.
ATC kód: R03AK06.
Mechanismus účinku a farmakodynamické účinky:
Přípravek Lifsar Pulmojet obsahuje salmeterol a flutikason-propionát, které mají různé mechanismy účinku. Mechanismy účinku obou léčiv jsou popsány níže:
Salmeterol:
Salmeterol je selektivní dlouhodobě působící (12 hodin) B2 agonista adrenoreceptorů s dlouhým postranním řetězcem, který se váže na zevní místo receptoru.
Salmeterol navozuje dlouhodobější bronchodilataci, která trvá nejméně 12 hodin, než doporučené dávky konvenčních krátkodobě působících B2 agonistů.
Flutikason-propionát:
Flutikason-propionát podávaný inhalačně v doporučených dávkách má glukokortikoidní protizánětlivý účinek v plicích, což vede ke snížení příznaků a exacerbací astmatu s méně nežádoucími účinky, než když jsou kortikosteroidy podávány systémově.
Klinická účinnost a bezpečnost
Klinické studie u CHOPN
TORCH byla 3letá studie pro vyhodnocení účinků léčby salmeterolem/flutikason-propionátem 50/500 mikrogramů podávaného dvakrát denně, salmeterolem 50 mikrogramů dvakrát denně, flutikason-propionátem (FP) 500 mikrogramů dvakrát denně nebo placebem na úmrtnost z jakékoli příčiny u pacientů s CHOPN. Pacienti s CHOPN s úvodní (prebronchodilatační) FEV1 < 60 % náležité hodnoty byli randomizováni k dvojitě zaslepené medikaci. Během studie byla pacientům povolena obvyklá léčba CHOPN, s výjimkou jiných inhalačních kortikosteroidů, dlouhodobě působících bronchodilatancií a dlouhodobého podávání systémových kortikosteroidů. Status přežití byl určen po 3 letech u všech pacientů bez ohledu na ukončení léčby zahnuté do studie. Primárním výsledkem byla redukce úmrtnosti z jakékoliv příčiny po 3 letech u salmeterolu/flutikason-propionátu proti placebu.
|
Placebo N=1524 |
Salmeterol 50 N=1 521 |
FP 500 N=1 534 |
Salmeterol/FP 50/500 N=1 533 | |
|
Úmrtnost z jakékoliv příčiny po 3 letech | ||||
|
Počet úmrtí (%) |
231 |
205 |
246 |
193 |
|
(15,2 %) |
(13,5 %) |
(16,0 %) |
(12,6 %) | |
|
Poměr rizika vs. placebo (kortikosteroidy) |
Neuvádí se |
0,879 (0,73; 1,06) |
1,060 (0,89; 1,27) |
0,825 (0,68; 1,00) |
|
P hodnota |
0,180 |
0,525 |
0,0521 | |
|
Poměr rizika Salmeterol + FP 50/500 vs. Složky (kortikosteroidy) |
Neuvádí se |
0,932 (0,77; 1,13) |
0,774 (0,64; 0,93) |
Neuvádí se |
|
P hodnota |
0,481 |
0,007 | ||
|
1Nesignifikantní P hodnota po adjustaci pro 2 předběžné analýzy při srovnání primární účinnosti z long-rank analýzy stratifikované podle kuřáctví. | ||||
Byl pozorován trend ke zlepšenému přežití u pacientů léčených salmeterolem/flutikason-propionátem ve srovnání s placebem pod dobu 3 let, i když nedosáhl úrovně statistické významnosti p < 0,05.
Procento pacientů, kteří zemřeli během 3 let v důsledku příčin pojících se s CHOPN, bylo 6,0 % u placeba, 6,1 % u salmeterolu, 6,9 % u FP a 4,7 % u salmeterolu/ flutikason-propionátu.
Průměrný počet středních až těžkých exacerbací za rok se významně snížil léčbou salmeterolem/flutikason-propionátem ve srovnání s léčbou salmeterolem, FP a placebem (průměrná hodnota v salmeterol/flutikason-propionátové skupině 0,85 ve srovnání s 0,97 ve skupině salmeterolu, 0,93 v FP skupině a 1,13 u placeba). To znamená redukci četnosti středních až těžkých exacerbací o 25 % (95% CI: 19 % až 31 %; p < 0,001) ve srovnání s placebem, o 12 % ve srovnání se salmeterolem (95% CI:5 % až 19 %, p = 0,002) a o 9 % ve srovnání s FP (95% CI: 1 % až 16 %, p = 0,024). Salmeterol a flutikason-propionát významně snížily četnost exacerbací ve srovnání s placebem o 15 % (95% CI: 7 % až 22 %; p < 0,001), příp. o 18 % (95% CI: 11% to 24%; p < 0,001).
Kvalita života vztahující se ke zdravotnímu stavu měřená St. George's Respiratory Questionnaire (SGRQ), se zlepšila u všech aktivních léčebných postupů ve srovnání s placebem. Průměrné zlepšení za tři roky u salmeterolu/flutikason-propionátu ve srovnání s placebem činilo -3,1 jednotek (95% CI: -
4,1 až -2,1; p < 0,001), ve srovnání se salmeterolem -2,2 jednotky (p < 0,001) a ve srovnání s flutikason-propionátem 1,2 jednotky (p = 0,017). Snížení o 4 jednotky se považuje za klinicky významné.
Odhadovaná 3letá pravděpodobnost výskytu pneumonie hlášená jako nežádoucí účinek činila 12,3 % u placeba, 13,3 % u salmeterolu, 18,3 % u FP a 19,6 % u salmeterolu/flutikason-propionátu (stupeň rizika u salmeterolu/flutikason-propionátu vs. placebo: 1,64, 95% CI: 1,33 až 2,01; p < 0,001). Nedošlo ke zvýšení úmrtí v souvislosti s pneumonií; úmrtí v průběhu léčby, která byla posouzena jako primárně způsobená pneumonií, činila 7 u placeba, 9 u salmeterolu, 13 u flitikason-propionátu a 8 u salmeterolu/flutikason-propionátu. Neexistoval signifikantní rozdíl v pravděpodobnosti výskytu zlomenin kostí (5,1 % u placeba, 5,1 % u salmeterolu, 5,4 % u flutikason-propionátu a 6,3 % u salmeterolu/flutikason-propionátu; stupeň rizika u salmeterolu/flutikason-propionátu vs. placebo:
1,22, 95% CI: 0,87 až 1,72; p = 0,248).
Placebem kontrolované klinické studie v průběhu 6 a 12 měsíců prokázaly, že pravidelné používání salmeterolu/flutikason-propionátu 50/500 mikrogramů zlepšuje plicní funkce a snižuje dušnost a nutnost podávání úlevové medikace.
Studie SCO40043 a SCO100250 byly randomizované, dvojitě zaslepené, opakované studie paralelních skupin, srovnávající vliv salmeterolu/flutikason-propionátu 50/250 mikrogramů dvakrát denně (dávka není schválená pro léčbu CHOPN v Evropské unii) se salmeterolem 50 mikrogramů dvakrát denně na roční míru výskytu středně těžkých/těžkých exacerbací u subjektů s CHOPN s FEVi nižším než 50 % náležité hodnoty a exacerbacemi v anamnéze. Středně těžká/těžká exacerbace byla definována jako zhoršení příznaků, které vyžaduje léčbu perorálními kortikosteroidy a/nebo antibiotiky nebo hospitalizaci pacienta.
Studie měly 4týdenní run-in období, kdy všechny subjekty obdržely open-label salmeterol/flutikason-propionát 50/250 na standardizaci farmakoterapie CHOPN a na stabilizaci onemocnění před randomizací do zaslepené studie léku po dobu 52 týdnů. Subjekty byly randomizovány v poměru 1:1 do skupiny užívající salmeterol/flutikason-propionát 50/250 (celkové ITT n=776) nebo salmeterol (celkové ITT n 778). Před run-in periodou subjekty přerušily předchozí medikaci CHOPN s výjimkou krátkodobě působících bronchodilatancií. Použití souběžných inhalačních dlouhodobě působících bronchodilatacií (B2 agonisté a anticholinergika), kombinace ipratropium/salbutamol, perorálních B2 agonistů a přípravků s theofylinem nebylo během léčby povoleno. Podávání perorálních kortikosteroidů a antibiotik bylo povoleno v případě akutní léčby exacerbace CHOPN se specifickými pokyny pro jejich použití. V průběhu studie subjekty užívaly salbutamol v případě potřeby.
Výsledky obou studií ukazují, že léčba salmeterolem/flutikason-propionátem 50/250 vedla k signifikantně nižšímu ročnímu výskytu středně těžkých/těžkých exacerbací CHOPN v porovnání se salmeterolem (SCO40043: 1,06 a 1,53 /subjekt za rok, respektive, poměr výskytu 0,70, 95% CI: 0,58 do 0,83, p < 0,001; SCO100250: 1,10 a 1,59/subjekt za rok, respektive, poměr výskytu 0,70, 95% CI: 0,58 do 0,83, p < 0,001). Výsledky sekundárních parametrů účinnosti (doba do objevení první středně těžké/těžké exacerbace, roční výskyt exacerbací vyžadujících perorální kortikosteroidy a (AM) FEV1 před první ranní dávkou) byly významně příznivější pro salmeterol/flutikason-propionát 50/250 mikrogramů dvakrát denně než pro salmeterol. Profily nežádoucích účinků byly podobné s výjimkou vyššího výskytu pneumonií a známých lokálních nežádoucích účinků (kandidóza a dysfonie) ve skupině salmeterol/flutikason-propionátu 50/250 mikrogramů dvakrát denně ve srovnání se salmeterolem. Nežádoucí účinky související s pneumonií byly hlášeny u 55 (7 %) subjektů v případě salmeterol/flutikason-propionátu 50/250 mikrogramů dvakrát denně a u 25 (3 %) v případě salmeterolu. Ve studii TORCH měla zvýšená incidence hlášených pneumonií se salmeterolem/flutikason-propionátem 50/250 mikrogramů dvakrát denně stejný rozsah jako incidence hlášená při léčbě salmeterolem/flutikason-propionátem 50/500 mikrogramů dvakrát denně.
5.2 Farmakokinetické vlastnosti
Pro účely farmakokinetiky tedy lze obě látky hodnotit odděleně.
Salmeterol:
Salmeterol působí lokálně v plicích, a proto léčebné účinky nelze posuzovat podle plazmatických hladin. Kromě toho jsou dostupné pouze omezené údaje o farmakokinetice salmeterolu kvůli technické obtížnosti jeho stanovení v plazmě, jelikož plazmatické koncentrace dosahované po inhalačním podání terapeutických dávek jsou velmi nízké (přibližně 200 pikogramů/ml nebo méně).
Flutikason-propionát:
Absolutní biologická dostupnost jedné dávky inhalačního flutikason-propionátu u zdravých subjektů kolísá zhruba od 5 do 11 % nominální dávky v závislosti na použitém inhalátoru. U pacientů s astmatem nebo CHOPN byl při inhalaci flutikason-propionátem sledován nižší stupeň systémové expozice.
K systémové absorpci dochází hlavně plícemi a je zpočátku rychlá a potom pomalá. Zbytek inhalační dávky může být spolknut, ale k systémové expozici přispívá minimálně, protože perorální biologická dostupnost je z důvodu nízké rozpustnosti ve vodě a presystémové metabolizace menší než 1 %. Se stoupající inhalační dávkou dochází k lineárnímu zvýšení systémové expozice.
Dispozice flutikason-propionátu je charakterizována vysokou plasmatickou clearance (1 150 ml/min.), velkým distribučním objemem v ustáleném stavu (přibližně 300 l) a terminálním poločasem přibližně 8 hodin.
Vazba na plazmatické proteiny je 91 %.
Flutikason-propionát je ze systémové cirkulace odstraňován velmi rychle. Hlavní cestou je metabolizace na neúčinný metabolit kyselinu karboxylovou prostřednictvím cytochromu P450 (izoenzym CYP3A4). Další neidentifikované metabolity se nacházejí také ve stolici.
Renální clearance flutikason-propionátu je zanedbatelná. Méně než 5 % dávky se vylučuje močí, hlavně ve formě metabolitů. Hlavní část dávky se vylučuje stolicí ve formě metabolitů a nezměněného léčiva.
5.3 Předklinické údaje vztahující se k bezpečnosti
Jedinými bezpečnostními obavami při používání u člověka, vyplývajícími ze studií na zvířatech u salmeterol-xinafoátu a flutikason-propionátu podávaných odděleně, se týkají zvýšeného farmakologického účinku.
V reprodukčních studiích na zvířatech bylo prokázáno, že glukokortikosteroidy vyvolávají malformace (rozštěp patra, malformace skeletu). Nezdá se však, že by výsledky experimentálních studií na zvířatech byly relevantní pro podávání doporučených dávek u člověka. Studie se salmeterol-xinafoátem na zvířatech prokázaly embryofetální toxicitu pouze při vysokých expozičních hladinách. Při současném podávání obou léčivých látek v dávkách, o nichž je známo, že vyvolávají abnormality indukované glukokortikoidy, byl u potkanů zjištěn zvýšený výskyt transponované umbilikální arterie a inkompletní osifikace okcipitální kosti.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek Monohydrát laktosy.
6.2 Inkompatibility Neuplatňuje se.
6.3 Doba použitelnosti 2 roky
Doba použitelnosti po prvním otevření: 30 dní.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v dobře uzavřeném obalu, aby byl přípravek chráněn před vlhkostí.
6.5 Druh obalu a obsah balení
Každá krabička obsahuje jeden inhalátor Lifsar Pulmojet s 60 dávkami (inhalacemi). Tělo inhalátoru je šedé a bílé se šedivým podstavcem a náustkem, s bílým krytem a fialovým nebo šedým spodním krytem a je vyroben z 6 různých plastových materiálů: polypropylen/poly ethylen/ akrylonitrilbutadienstyren/termoplastický elastomer/polybutylentereftalát a silikon.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Zentiva, k. s., U Kabelovny 130, 102 37 Praha, Česká republika
8. REGISTRAČNÍ ČÍSLO
14/358/16-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
31.8.2016
10. DATUM REVIZE TEXTU
31.8.2016
14