Levosert
Sp.zn.sukls197684/2013
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. NÁZEV PŘÍPRAVKU
Levosert
20 mikrogramů/24 hodin, intrauterinní inzert
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Léčivou látkou je levonorgestrelum.
Intrauterinní inzert obsahuje levonorgestrelum 52 mg. Počáteční rychlost uvolňování je přibližně 20 mikrogramů za den a snižuje se po 3 letech na přibližně 12 mikrogramů za den.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Intrauterinní inzert (IUS) uvolňující levonorgestrel.
Přípravek se skládá ze zavaděče a IUS s levonorgestrelem, který je umístěn na hrotu zavaděče. Součástí zavaděče je zaváděcí trubička, píst, patka, tělo a posuvná část. Inzert se skládá bílého nebo téměř bílého hormon-elastomerového jádra umístěného na tělísku ve tvaru T. Jádro je kryto neprůhlednou trubičkou, která řídí uvolňování levonorgestrelu. Tělísko ve tvaru T má na jednom konci smyčku a na druhém konci dvě raménka. Ke smyčce jsou připojena vlákna pro vyjmutí.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Kontracepce.
Silné menstruační krvácení. Přípravek Levosert může být zvláště vhodný u žen se silným menstruačním krvácením, které požadují (reverzibilní) kontracepci.
4.2 Dávkování a způsob podání Začátek léčby
U žen ve fertilním věku se má přípravek Levosert zavést do dutiny děložní během prvních sedmi dnů od začátku menstruace. Může být nahrazen novým systémem kdykoli během cyklu.
Zavedení po porodu: Aby se snížilo riziko perforace, je třeba zavedení po porodu odložit až do kompletní involuce dělohy. Nesmí být zavedeno dříve, než 6 týdnů po porodu. Pokud má pacientka silné poporodní krvácení a/nebo bolest, je třeba před zavedením vyloučit infekci nebo jiné příčiny. Přípravek Levosert může být zaveden také ihned po potratu v prvním trimestru.
V indikaci kontracepce a silného menstruačního krvácení je přípravek Levosert účinný po dobu 3 let. Proto je třeba jej po 3 letech používání odstranit.
Pokud si uživatelka přeje ve stejné metodě pokračovat, může být ihned zaveden nový systém a v tomto případě není třeba žádná další ochrana.
Před zavedením je třeba pacientku informovat o účinnosti, rizicích a nežádoucích účincích přípravku Levosert. Musí být provedeno gynekologické vyšetření, včetně vyšetření prsů a vyloučení těhotenství. Je třeba vyloučit cervikální infekci a onemocnění přenosná pohlavním stykem. Je třeba určit polohu dělohy a velikost děložní dutiny. Je třeba pečlivě dodržovat pokyny pro zavádění. Pacientku je třeba vyšetřit šest týdnů po zavedení a poté jednou ročně nebo častěji, pokud je to klinicky indikováno. Přípravek Levosert není doporučen u pacientek před začátkem menarche.
Pediatrická populace
Přípravek Levosert nebyl studován u pacientek mladších než 16 let.
Návod k použití přípravku a zacházení s ním
Levosert je dodáván ve sterilním obalu, který nesmí být otevřen, dokud to není třeba z důvodu jeho zavedení. S přípravkem je třeba po otevření sterilního obalu zacházet asepticky. Pokud je uzávěr sterilního balení narušený, přípravek je třeba znehodnotit (viz bod 6.6 informace pro likvidaci přípravku).
Jak se přípravek Levosert zavádí
Doporučuje se, aby přípravek Levosert zaváděl jen lékař/zdravotnický pracovník, který má již zkušenosti se zaváděním IUS s levonorgestrelem a/nebo je v zavádění IUS s levonorgestrelem dostatečně proškolený.
V případě obtížného zavádění a/nebo neobvyklé bolesti či krvácení během zavádění nebo následně po něm postupujte podle bodu 4.4.
Přípravek Levosert se dodává sterilní, sterilizace se provádí pomocí etylenoxidu. Přípravek znovu nesterilizujte. Jen pro jednorázové užití. Nepoužívejte, pokud je vnitřní obal poškozený nebo otevřený. Nezavádějte po datu uvedeném na štítku.
Přípravek Levosert se zavádí do dutiny děložní za použití přiloženého zavaděče (obrázek 1) a je třeba pečlivě dodržovat pokyny pro zavádění.
Následující pokyny pro zavádění jsou uložené také v krabičce s IUS.
Popis
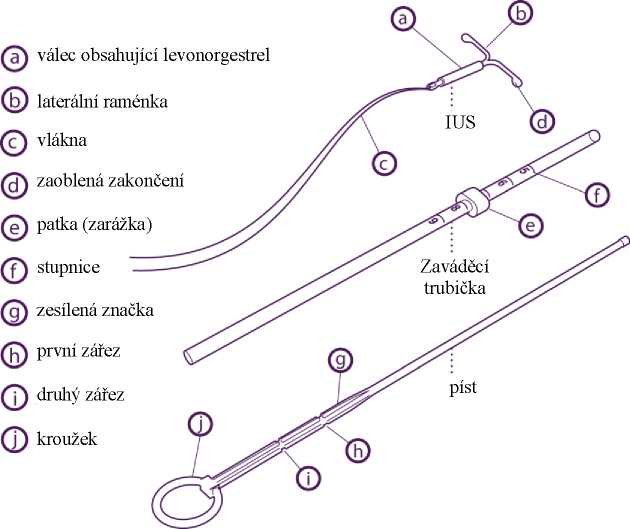
Podmínky pro použití
1. U žen ve fertilním věku se má přípravek Levosert zavést do dutiny děložní během prvních sedmi dnů od začátku menstruace. Může být nahrazen novým systémem kdykoli během cyklu.
2. Doporučuje se, aby přípravek Levosert zaváděl jen lékař/zdravotnický pracovník, který je v zavádění dostatečně proškolený a který si před zaváděním přípravku Levosert pečlivě pročetl tyto pokyny.
3. Přípravek Levosert se dodává ve sterilním balení. Nepoužívejte jej, pokud je vnitřní obal poškozený nebo otevřený.
4. Gynekologickým vyšetřením určete pozici dělohy (anteverze, retroverze) a její velikost. Vylučte těhotenství a kontraindikace.
5. Zaveďte do pochvy poševní zrcadla, použijte vhodný dezinfekční roztok k výplachu vaginy a očištění hrdla děložního.
6. Pokud je diagnostikována cervikální stenóza, užijte cervikální dilatátory. Neužívejte násilí, abyste překonali rezistenci.
7. Uchopte cervix vhodným nástrojem a mírným tahem stáhněte hrdlo a narovnejte dělohu.
8. Změřte délku dutiny děložní hysterometrií. Pokud je délka dělohy < 5,5 cm, ukončete proceduru.
Příprava pro zavedení
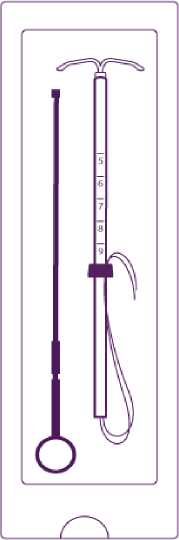
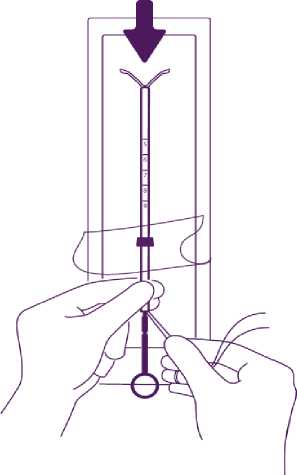
Zaveďte píst a IUD do zaváděcí trubičky
Částečně otevřete blistr (asi do 1/3 od spodní strany) a zaveďte píst do zaváděcí trubičky. Uvolněte vlákna z patky. Tahem za vlákna zatáhněte IUD do trubičky. Raménka tělíska musí zůstat v horizontální poloze, rovnoběžně s plochou stranou patky (zarážky).
Umístěte spodní hranu patky (zarážky) na správné místo
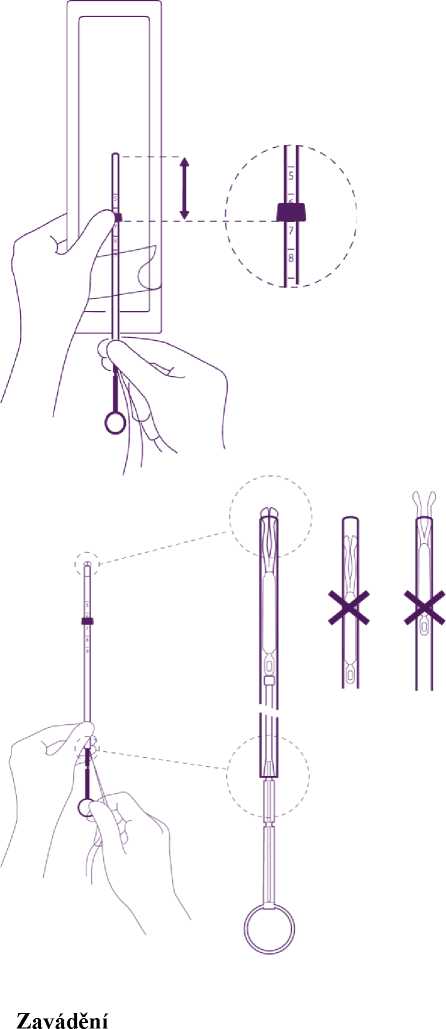
Pozice modré patky (zarážky) a spodní hrany patky (zarážky) označuje hodnotu zjištěnou při hysterometrii. Plochá strana patky musí vždy zůstat paralelně s raménky. To umožní správné otevření ramének v dutině děložní.
Upravte pozici IUD v zaváděcí trubičce
Pro upravení pozice IUD držte pevně píst a táhněte za vlákna a pohybujte trubičkou.
Zaoblená zakončení laterálních ramének musí být těsně proti sobě, mírně nad horním okrajem zaváděcí trubičky (viz detailní obrázek č. 1) a distální okraj trubičky musí být v místě prvního zářezu na pístu (viz detailní obrázek č. 2). Pokud není trubička v úrovni prvního zářezu na pístu, musíte zatáhnout za vlákna silněji.
Zavedení tělíska do cervikálního kanálu až je modrá patka v kontaktu s cervíxem
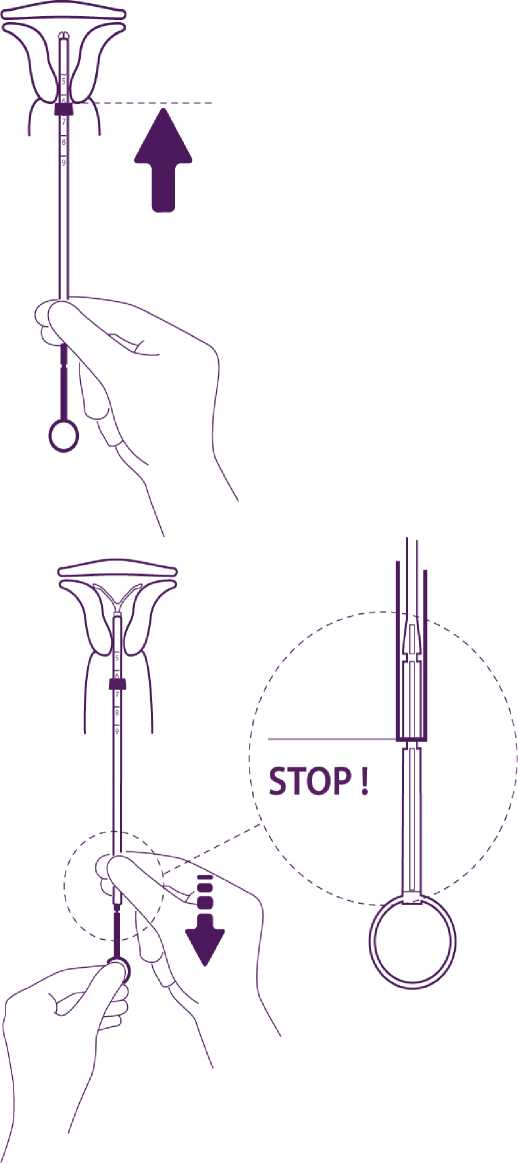
Vytáhněte celé tělísko z blistru a přitom držte pevně píst a trubičku spolu ve správně upravené pozici.
Zaveďte soustavu do cervikálního kanálu až se modrá patka (zarážka) dotýká hrdla.
Uvolnění ramének nitroděložního tělíska
Držte píst, uvolněte vlákno a táhněte zaváděcí trubičku dolů, až její dolní konec dosáhne druhého zářezu na pístu.
Zatlačte IUD proti fundu
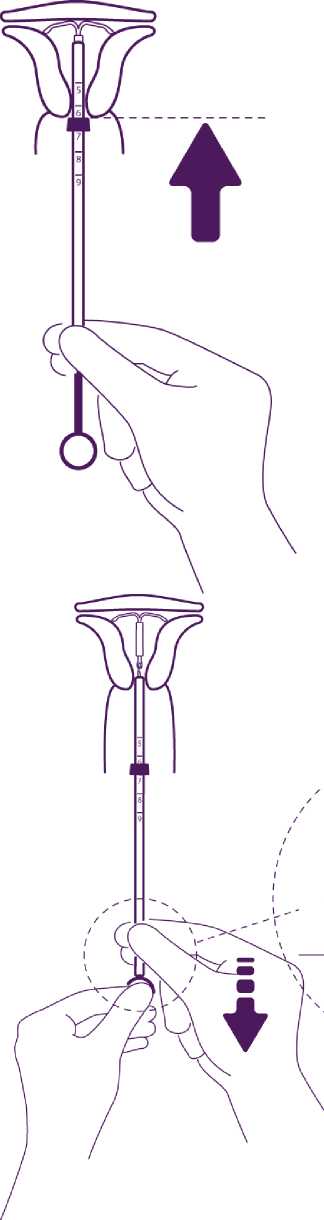
STOP!
Sní
Pro umístění IUD v děložní dutině zatlačte současně na zaváděcí trubičku a píst, až se modrá patka (zarážka) opět dotkne hrdla.
Přípravek Levosert je pak v dutině děložní správně umístěn.
Uvolnění IUD z trubičky do dutiny děložní
Aniž byste pohybovali pístem, zatáhněte zaváděcí trubičku dolů až ke kroužku pístu.
Mírný odpor znamená průchod rozšířené části pístu. Nicméně zatáhněte trubičku až
V
dolů ke kroužku.
t
Přípravek Levosert je pak zcela uvolněný
I #
ze zaváděcí trubičky.
Odstraňte postupně součásti zavaděče a ustřihněte vlákna
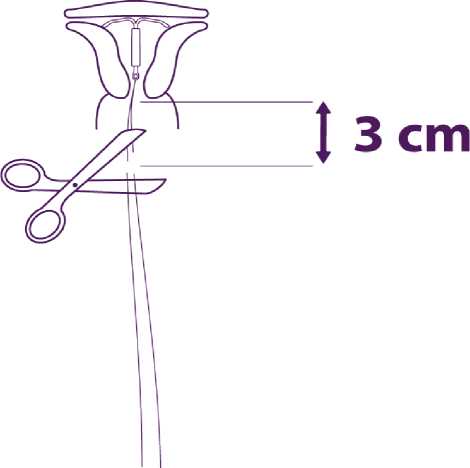
Odstraňte postupně nejdříve píst a poté zaváděcí trubičku,
Ustřihněte vlákna asi 3 cm od cervixu.
DŮLEŽITÉ!
V případě obtížného zavádění a/nebo neobyčejně silné bolesti nebo krvácení během zavádění nebo po něm je třeba provést fyzikální a ultrasonografické vyšetření k vyloučení perforace těla dělohy nebo cervixu. V případě potřeby systém odstraňte a zaveďte nový, sterilní systém. Prosím nahlaste našemu farmakovigilančnímu oddělení jakýkoli případ perforace dělohy nebo problémy se zaváděním:
e-mail: safety.cz@richtergedeon.cz tel.: +420 261 141 215
Jak přípravek Levosert vyjmout
Přípravek Levosert se odstraňuje jemným tahem za vlákna pomocí peanu. Pokud nejsou vlákna viditelná a tělísko je v dutině děložní, může být odstraněno za použití úzkého peanu. To si může vyžádat dilataci děložního kanálu.
Po vyjmutí přípravku Levosert je třeba zkontrolovat, zda je systém intaktní. Při obtížném vyjímání byly hlášeny jednotlivé případy, kdy váleček obsahující hormon sklouzl přes horizontální (laterální) raménka a ta byla tímto ukryta uvnitř válečku. Pokud bylo ověřeno, že je systém kompletní, není v této situaci třeba žádný další zásah. Kuličky na konci ramének obvykle zabrání kompletnímu oddělení válečku od T-těla systému.
4.3 Kontraindikace
- Těhotenství nebo suspektní těhotenství;
- Současná nebo rekurentní infekce v oblasti pánve;
- Aktuální zánět v oblasti genitálu;
- Poporodní endometritida;
- Infikovaný potrat během posledních 3 měsíců;
- Cervicitida, cervikální dysplazie;
- Suspektní nebo potvrzené zhoubné bujení dělohy nebo děložního hrdla;
- Tumor j ater nebo j iné akutní nebo závažné onemocnění j ater;
- Vrozené nebo získané anomálie dělohy včetně myomů, pokud deformují děložní dutinu;
- Diagnosticky neobjasněné abnormální genitální krvácení;
- Stavy spojené se zvýšenou náchylností k infekcím;
- Závažné arteriální onemocnění probíhající nebo v anamnéze, jako je cévní mozková příhoda nebo infarkt myokardu;
- Potvrzené nebo suspektní hormonálně dependentní tumory, jako je karcinom prsu (viz bod 4.4);
- Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1;
- Akutní malignity postihující krev nebo leukemie kromě období remise;
- Nedávná trofoblastická nemoc, dokud j sou hladiny hCG zvýšené.
4.4 Zvláštní upozornění a opatření pro použití Lékařské vyšetření
Před zavedením je třeba odebrat kompletní osobní a rodinnou anamnézu. Na základě této anamnézy, kontraindikací a upozornění pro použití je třeba provést fyzikální vyšetření. Je třeba změřit puls a krevní tlak a bimanuálním vyšetřením určit polohu dělohy. Pacientku je třeba opakovaně vyšetřit 6 týdnů po zavedení přípravku a další vyšetření je třeba provádět v případě klinické indikace a přizpůsobit je spíše každé ženě individuálně, než je provádět rutinně. Před zavedením je třeba vyloučit těhotenství a řádně vyléčit genitální infekce. Ženu je třeba poučit, že přípravek Levosert nechrání před HIV (AIDS) a jinými sexuálně přenosnými nemocemi (prosím, podívejte se do bodu níže týkajícího se infekcí v oblasti pánve).
Ženu je třeba poučit, aby se dostavovala na screeningové vyšetření hrdla děložního a prsů, které odpovídá jejímu věku.
Stavy, kdy je třeba použít přípravek Levosert s opatrností
Pokud je přítomen kterýkoli z následujících stavů nebo dojde-li během léčby k jeho prvnímu výskytu, je třeba užít přípravek Levosert s opatrností po konzultaci s odborníkem nebo je třeba zvážit odstranění přípravku:
- Migréna s aurou
- Neobvykle silná nebo častá bolest hlavy
- Žloutenka
- Výrazné zvýšení krevního tlaku
- Malignity postihující krev nebo leukemie v remisi
- Užívání dlouhodobé kortikosteroidní léčby
- Symptomatické funkční ovariální cysty v anamnéze
- Závažné arteriální onemocnění aktivní nebo v anamnéze, jako je cévní mozková příhoda nebo infarkt myokardu
- Závažné nebo mnohonásobné rizikové faktory arteriálního onemocnění
- Trombotické arteriální nebo jakékoli současné embolické onemocnění
- Venózní tromboembolismus
Obecně je třeba ženy používající přípravek Levosert vést k tomu, aby přestaly kouřit.
Upozornění a opatření pro zavedení/vyjmutí
Obecná informace: Zavedení a vyjmutí tělíska může být spojeno s bolestí a krvácením. V případě obtížného zavádění a/nebo neobyčejně silné bolesti nebo krvácení během zavádění nebo po něm, je třeba provést fyzikální a ultrasonografické vyšetření k vyloučení perforace těla dělohy nebo cervixu (viz také „Perforace“).
Výkon může navodit mdlobu v důsledku vazovagální reakce nebo záchvat u pacientek s epilepsií V případě časných příznaků vazovagální ataky může být potřeba zavádění přerušit nebo systém odstranit. V případě potřeby je třeba ženu uložit do polohy na zádech, s hlavou níže a dolními končetinami zdviženými do vertikální polohy, aby se obnovil cerebrální průtok krve. Je třeba udržovat volné dýchací cesty; musí být stále po ruce dýchací přístroj (ambuvak). Přetrvávající bradykardii je možné korigovat intravenózním podáním atropinu. Je možné podat kyslík, je-li dostupný.
Perforace: Může dojít k perforaci děložního těla nebo hrdla, nejčastěji během zavádění. To může být spojeno se silnou bolestí a neustávajícím krvácením. Pokud je podezření na perforaci, systém musí být co nejdříve odstraněn. Riziko perforace může být zvýšeno při poporodním zavádění (viz bod 4.2), u kojících žen a u žen s fixní retroverzí dělohy.
Infekční onemocnění v oblasti pánve: Mezi známé rizikové faktory zánětlivého onemocnění pánve patří sexuální promiskuita, častý sexuální styk a mladý věk. Zánětlivá onemocnění pánve mohou mít závažné důsledky, protože mohou poškodit fertilitu a zvýšit riziko vzniku mimoděložního těhotenství.
U žen používajících Levosert, u kterých se objeví příznaky a známky naznačující zánětlivé onemocnění pánve, je třeba nasadit vhodnou antibiotickou léčbu. Není třeba Levosert vyjímat, ledaže by příznaky nezačaly ustupovat do 72 hodin nebo si žena přála Levosert vyjmout. Pokud žena trpí rekurentní endometritidou nebo rekurentními infekcemi v oblasti pánve nebo pokud je akutní infekce závažná, je třeba tělísko Levosert odstranit.
Komplikace vedoucí k selhání
Vypuzení tělíska: K příznakům částečného nebo úplného vypuzení jakéhokoli IUS patří krvácení nebo bolest. Systém však může být z děložní dutiny vypuzen, aniž by si toho žena všimla. I částečné vypuzení systému může snížit účinnost přípravku Levosert. Vzhledem k tomu, že tělísko Levosert snižuje intenzitu menstruačního krvácení, zesílené krvácení může svědčit o jeho vypuzení.
Systém Levosert, který se nenachází ve správné poloze, by měl být vyjmut a měl by být zaveden nový systém. Ženu je třeba poučit, jak má kontrolovat vlákna přípravku Levosert.
Ztracená vlákna: Jestliže kontrolní vlákna nejsou při následném vyšetření viditelná, je třeba nejprve vyloučit možnost těhotenství. Vlákna mohou být vtažena do dělohy nebo do cervikálního kanálu a mohou se znovu objevit během další menstruace. Jestliže bylo vyloučeno těhotenství, lze obvykle vlákna najít při jemné sondáži pomocí vhodného nástroje. Pokud se vlákna nenajdou, je možné, že byla odtržena nebo že tělísko bylo vypuzeno. Pro stanovení polohy IUS lze využít ultrazvuk nebo rentgen.
Nepravidelnosti krvácení
Nepravidelné krvácení: S přípravkem Levosert je obvykle dosaženo během 3 až 6 měsíců léčby významného snížení ztráty krve menstruací. Silnější menstruace nebo neočekávané krvácení může naznačovat vypuzení tělíska. Pokud menoragie přetrvává, je třeba ženu opět vyšetřit. Je třeba zkontrolovat dutinu děložní pomocí ultrazvuku. Je třeba také zvážit potřebu endometriální biopsie.
Protože se během prvních měsíců léčby může objevit u premenopauzálních žen nepravidelné krvácení/špinění, doporučuje se před zavedením přípravku Levosert vyloučit patologii endometria.
Kdy je třeba u žen ve fertilním věku zvážit možnost těhotenství: Pokud se menstruace nedostaví do 6 týdnů od začátku předchozí menstruace, je třeba zvážit, zda nedošlo k otěhotnění. Opakovaný těhotenský test není nutný u pacientek s amenoreou, pokud pro těhotenství nesvědčí další symptomy.
Posouzení léčby menoragie: S přípravkem Levosert je obvykle dosaženo během 3 až 6 měsíců léčby významného snížení ztráty krve menstruací. Pokud není v tomto časovém horizontu dosaženo významné redukce ztráty krve, je třeba vzít v úvahu alternativní způsoby léčby.
Ostatní rizika během používání
Mimoděložní těhotenství: Absolutní riziko vzniku mimoděložního těhotenství u uživatelek IUS s levonorgestrelem je nízké. Nicméně pokud žena otěhotní s přípravkem Levosert in situ, pravděpodobnost výskytu mimoděložního těhotenství se zvyšuje.
Jestliže se vyskytne bolest v podbřišku, měla by se vzít v úvahu možnost mimoděložního těhotenství, zvláště pokud se zároveň nedostaví menstruace nebo pokud žena s amenoreou začne krvácet. Riziko vzniku mimoděložního těhotenství u uživatelek IUS s levonorgestrelem je 0,06 na 100 žen za rok. Toto riziko je nižší, než odhadované riziko u žen užívajících jakoukoli kontracepci, které je 0,3 - 0,5 na 100 žen za rok. Odpovídající číslo pro ženy používající IUS s mědí je 0,12 na 100 žen za rok. U žen s mimoděložním těhotenstvím v anamnéze je vyšší riziko vzniku mimoděložního těhotenství.
Ovariální cysty: U žen ve fertilním věku zůstává obvykle zachován ovulační cyklus s rupturou folikulů. Atrézie folikulu je někdy opožděná a folikulogeneze pokračuje. Tyto zvětšené folikuly nelze klinicky odlišit od ovariálních cyst. Údaje z klinických studií naznačují, že ovariální cysty byly hlášeny jako nežádoucí účinek přibližně u 7 % žen používajících přípravek Levosert, nicméně v některých publikovaných studiích byl hlášen vyšší výskyt ovariálních cyst (což může být ovlivněno faktory, jako je frekvence a kritéria ultrasonografického vyšetření a populací pacientek). Ve většině případů jsou asymptomatické, některé mohou být spojeny s bolestí v oblasti pánve a dyspareunií.
Ve většině případů ovariální cysty spontánně zmizí během dvou až tří měsíců. Pokud se tak nestane, doporučuje se pokračovat v kontrole ultrazvukem a učinit další diagnostická/ terapeutická opatření. Vzácně může být nezbytné provést chirurgický zákrok.
Karcinom prsu: Meta-analýza 54 epidemiologických studií hovoří o lehce zvýšeném relativním riziku (RR = 1,24) diagnózy karcinomu prsu v průběhu užívání kombinovaných perorálních kontraceptiv, a to hlavně u přípravků s obsahem kombinace estrogen-progestogen. Toto zvýšené riziko postupně mizí během 10 let od ukončení užívání kombinovaných perorálních kontraceptiv. Vzhledem k tomu, že karcinom prsu je vzácný u žen do 40 let, zvýšení počtu diagnostikovaných případů karcinomu prsu u současných a dřívějších uživatelek kombinovaných perorálních kontraceptiv je nízké ve srovnání s celkovým rizikem výskytu karcinomu prsu.
Riziko u žen užívajících kontraceptiva obsahující pouze progestogen (antikoncepční tablety obsahující jen progestogen, implantáty a injekční přípravky), včetně přípravku Levosert, je možná podobného rozsahu jako riziko spojené s kombinovanými perorálními kontraceptivy. Nicméně u přípravků obsahujících jen progestogen je průkaz založen na mnohem menší populaci uživatelek, a tak je méně přesvědčivý než u kombinovaných perorálních kontraceptiv.
Obecná informace
Glukosová tolerance: Levonorgestrel v nízkých dávkách může ovlivnit glukosovou toleranci a u diabetiček používajících přípravek Levosert je třeba sledovat koncentraci glukosy v krvi.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Účinek přípravku Levosert může být ovlivněn léky, které indukují jatemí enzymy, včetně barbiturátů, primidonu, fenytoinu, karbamazepinu, griseofulvinu a rifampicinu. Nebyly provedeny žádné interakční studie sledující vliv těchto léků na účinek přípravku Levosert.
4.6 Fertilita, těhotenství a kojení
Použití přípravku Levosert v těhotenství nebo při podezření na těhotenství je kontraindikováno. Pokud žena otěhotní s přípravkem Levosert in situ (viz bod 5: farmakologické vlastnosti), je třeba vyloučit mimoděložní těhotenství (viz bod 4.4), je třeba odstranit přípravek a zvážit ukončení těhotenství, protože je zde zvýšené riziko, že těhotenství bude komplikované (potrat, infekce a sepse). Odstranění přípravku Levosert nebo sondáž dělohy může vyvolat spontánní potrat. Pokud nelze tyto postupy uskutečnit, je třeba ženu o těchto rizicích informovat a následně je třeba tato těhotenství pečlivě sledovat. Ženu je třeba poučit, aby hlásila všechny symptomy, které by mohly znamenat komplikace těhotenství, jako je křečovitá bolest břicha s horečkou.
Lokální expozice levonorgestrelu:
Klinické zkušenosti s těhotenstvím při zavedeném IUS s levonorgestrelem jsou omezené. Dosud však není žádný důkaz pro vznik vrozených vad způsobených lokálním použitím IUS s levonorgestrelem z případů, kdy těhotenství pokračovalo do termínu porodu s IUS in situ.
Kojení
Levonorgestrel při použití IUS s levonorgestrelem je vylučován ve velmi malých množstvích do mateřského mléka. Vzhledem k tomu, že není očekáváno žádné riziko pro dítě, kojení může během používání přípravku Levosert pokračovat.
Vzácně bylo u žen používajících IUS s levonorgestrelem během kojení hlášeno děložní krvácení.
Fertilita
Používání IUS s levonorgestrelem nemění po odstranění IUS fertilitu ženy.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Není známý žádný vliv přípravku Levosert na schopnost řídit motorová vozidla nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Nežádoucí účinky jsou častější během prvních měsíců po zavedení a s délkou používání klesají.
Velmi častými nežádoucími účinky (vyskytují se u více než 10% uživatelek) jsou děložní/vaginální krvácení včetně špinění, oligomenorea, amenorea (viz bod 5.1) a benigní ovariální cysty.
Frekvence výskytu benigních ovariálních cyst závisí na použité diagnostické metodě, v klinických studiích byly diagnostikovány zvětšené folikuly u 12% subjektů používajících IUS s levonorgestrelem. Většina folikulů byla asymptomatická a vymizela během 3 měsíců.
|
Třídy orgánových systémů |
Nežádoucí účinky | |||
|
velmi časté: |
časté: |
iě časté: |
vzácné: | |
|
>1/10 |
>1/100 až <1/10 |
>1/1 000 až |
>1/10 000 až | |
|
Třídy orgánových systémů |
Nežádoucí účinky | |||
|
<1/100 |
<1/1 000 | |||
|
Psychiatrické poruchy |
depresivní nálada nervozita snížení libida |
změna nálady | ||
|
Poruchy nervového systému |
migréna | |||
|
Gastrointestinální poruchy |
bolest břicha nevolnost |
abdominální distenze | ||
|
Poruchy kůže a podkožní tkáně |
akné |
alopecie hirsutismus pruritus ekzém |
kopřivka | |
|
Poruchy svalové a kosterní soustavy a pojivové tkáně | ||||
|
Poruchy reprodukčního systému a prsu |
změny krvácení benigní ovariální cysty |
pánevní bolest dysmenorea vaginální výtok vulvovaginitida citlivost prsů bolest prsů |
zánětlivé onemocnění pánve endometritida cervicitida normální Pap stěr, třída II |
perforace dělohy |
|
Celkové poruchy a reakce v místě aplikace |
vypuzení nitroděložního kontracepčního tělíska |
edém | ||
|
Vyšetření |
zvýšení tělesné hmotnosti | |||
Pokud žena otěhotní s přípravkem Levosert in situ, je zvýšené riziko vzniku mimoděložního těhotenství (viz body „Zvláštní upozornění a opatření pro použití“ a „Fertilita, těhotenství a kojení“)
Navíc byly u uživatelek IUS s levonorgestrelem hlášeny případy karcinomu prsu (četnost neznámá, viz bod 4.4).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
Webové stránky: http://www.sukl.cz/nahlasit-nezadouci-ucinek
4.9 Předávkování
Neuplatňuje se.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: nitroděložní kontraceptiva, plastové IUD s progestogenem ATC kód: G02BA03
Levonorgestrel je progestogen, který je používaný v gynekologii různými způsoby: jako progestogenní část perorálních kontraceptiv, v hormonální substituční léčbě a samostatně jako kontraceptivum v
„minipilulkách“ (perorální antikoncepční tablety obsahující jen progestogen) a v podkožních implantátech. Levonorgestrel může být také podáván přímo do dutiny děložní formou IUS. To umožňuje velmi nízké denní dávky, protože hormon je uvolňován přímo do cílového orgánu.
Kontracepční mechanismus účinku IUS s obsahem levonorgestrelu je založen hlavně na hormonálních účincích vyvolávajících následující změny:
- Prevence proliferace endometria
- Zahuštění cervikálního hlenu, které brání průniku spermií
- U některých žen suprese ovulace.
Očekává se i malý kontracepční přínos daný samotnou přítomností systému v děloze.
Při zavedení podle instrukcí je četnost selhání přípravku Levosert přibližně 0,19 % (95% Cl: 0,05 % -0,75 %) za rok. Četnost selhání se může zvýšit v případě vypuzení přípravku Levosert nebo v případě perforace.
IUS Levosert může být zvláště vhodný jako kontracepce u pacientek se silným menstruačním krvácením a může být úspěšně použitý v léčbě idiopatické menoragie.
Objem menstruačního krvácení byl snížen po 3 měsících užívání u 88 % žen s menoragií. Menoragie způsobená submukózními myomy (fibroidy) může odpovídat méně příznivě. Snížení krvácení podporuje u pacientek s menoragií zvýšení krevního hemoglobinu.
Pravděpodobným mechanismem účinku IUS s levonorgestrelem u idiopatické menoragie vedoucím ke snížení krevních ztrát je prevence proliferace endometria.
Vzorce krvácení
Všechny uživatelky IUS s levonorgestrelem zaznamenaly různé typy změn krvácení (časté, dlouho trvající nebo silné krvácení, špinění, oligomenorea, amenorea). Průměrný počet dní, kdy špiní/měsíc se u žen ve fertilním věku snižuje během prvních šesti měsíců používání postupně z devíti na čtyři dny. Procento žen s dlouhotrvajícím krvácením (více než 8 dní) se během prvních tří měsíců snižuje z 20 % na 3 %. V klinických studiích zaznamenalo 17 % žen během prvního roku používání amenoreu, která trvala nejméně tři měsíce.
5.2 Farmakokinetické vlastnosti
Počáteční uvolňování levonorgestrelu z přípravku Levosert je 20 mikrogramů/24 hodin, uvolňuje se přímo do dutiny děložní. Vzhledem k nízkým koncentracím v plasmě je zde jen malý účinek na metabolismus.
Farmakokinetika levonorgestrelu jako takového byla důkladně zkoumána a publikována v literatuře. Nejlepším odhadem poločasu se zdá být 20 hodin, ačkoli některé studie hlásily hodnoty tak nízké, jako je 9 hodin a jiné zase tak dlouhé, jako je 80 hodin. Dalším důležitým nálezem, také v souladu se zkušeností s jinými syntetickými steroidy, je zaznamenání rozdílů v rychlosti metabolické clearance mezi jednotlivci, a to i při podání intravenózní cestou. Levonorgestrel se silně váže na proteiny (hlavně na sexuální hormony vázající globulin (SHBG)) a je rozsáhle metabolizován na velké množství neaktivních metabolitů.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje neodhalily žádné jiné zvláštní riziko pro člověka, než jsou informace uvedené v jiných částech SPC. Tyto údaje jsou založeny na konvenčních studiích bezpečné farmakologie, toxicity po opakovaných dávkách, genotoxicity, karcinogenního potenciálu a reprodukční toxicity a toxicity vývoje.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Dimetikon T etrapropoxysilan Stannosium-oktanoát Dimetikonový elastomer Dimetikonová membrána Polyethylen Síran barnatý Polypropylen Ftalocyaninová modř
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
4 roky
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v původním obalu.
6.5 Druh obalu a obsah balení
Intrauterinní inzert Levosert a zavaděč jsou jednotlivě zataveny v blistru (polyester) s odtrhovacím uzávěrem (TYVEK-polyethylen).
6.6 Zvláštní opatření pro likvidaci přípravku
Technika zavádění se liší od jiných nitroděložních tělísek, je třeba se věnovat nacvičení správné techniky zavádění. Speciální instrukce pro zavádění jsou uloženy v balení.
Přípravek Levosert je dodáván ve sterilním balení, které nemá být otevřeno, dokud to zavádění nevyžaduje. S každým systémem je třeba zacházet asepticky. Pokud je uzávěr sterilního obalu poškozen, je třeba systém zlikvidovat v souladu s místními požadavky pro zacházení s nebezpečným odpadem. Stejně tak je třeba zlikvidovat zavaděč tělíska Levosert. S vnějším papírovým obalem a vnitřním blistrem je možné zacházet jako s domácím odpadem.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Gedeon Richter Plc.
Gyomroi út 19-21 1103 Budapešť,
Maďarsko
8. REGISTRAČNÍ ČÍSLO
17/285/13-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
3.7.2013
10. DATUM REVIZE TEXTU
23.10.2014
15/15