Leptoprol 5 Mg
Sp.zn. sukls61285/2013
SOUHRN ÚDAJŮ O PŘÍPRAVKU
1. Název přípravku Leptoprol 5 mg
Implantát v předplněné injekční stříkačce
2. Kvalitativní a kvantitativní složení
Jeden implantát obsahuje leuprorelinum 5 mg (ve formě leuprorelini acetas).
Úplný seznam pomocných látek viz bod 6.1.
3. Léková forma
Implantát v předplněné injekční stříkačce
Biodegradabilní bílá až slabě nažloutlá tyčinka válcovitého tvaru (délka 10 mm) v předplněné injekční stříkačce.
4. Klinické údaje
4.1 Terapeutické indikace
Paliativní léčba pacientů s pokročilým hormonálně dependentním karcinomem prostaty.
4.2 Dávkování a způsob podání
Dávkování
Indikace k léčbě má být stanovena a monitoring dlouhodobé léčby prováděn pod dohledem lékaře se zkušeností s onkologickou léčbou.
Doporučená dávka je jednorázová dávka 5 mg přípravku Leptoprol každé 3 měsíce.
Pokud je ve výjimečných případech aplikace odložena až o 4 týdny, nemá to u většiny pacientů vliv na terapeutický účinek (viz bod 5.2).
Zvláštní skupiny pacientů
Není nutná žádná úprava dávkování u pacientů s poruchou funkce ledvin nebo jater, nebo u starších osob.
Pediatrická populace
Přípravek Leptoprol je kontraindikován u dětí a dospívajících, viz bod 4.3.
Způsob podání
Jeden implantát se injikuje podkožně do přední břišní stěny.
Před injekcí lze aplikovat lokální anestetikum.
Doporučuje se, aby aplikace antiandrogenu jako podpůrné terapie byla zahájena asi 5 dní před zahájením terapie přípravkem Leptoprol (viz bod 4.4).
Návod k použití
1. Dezinfikujte místo injekce na přední straně břicha pod linií pupku.
2. Vyjměte injekční stříkačku ze sterilního vaku a zkontrolujte, že implantát je viditelný ve své schránce. V případě potřeby si injekční stříkačku prohlédněte proti světlu nebo jí jemně zatřepejte.
ochranný kryt implantát
-—t-
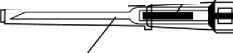
jehla
píst
*

3. Píst injekční stříkačky vytáhněte úplně dozadu do polohy stop. Během tohoto manévru se ozve několik kliknutí. Poté z injekční stříkačky sejměte krytku.
Prosím pozor: píst lze posouvat dopředu k injikaci implantátu pouze tehdy, pokud byl předtím vytažen úplně dozadu do polohy stop!
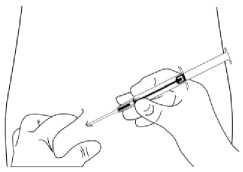
4. Jednou rukou držte tělo injekční stříkačky. Druhou rukou vytvořte na pacientově kůži řasu. Jehlu zaveďte celou pod mírným úhlem, téměř paralelně s kůží, přičemž konus jehly směřuje nahoru do podkožní tkáně přední břišní stěny pod linií pupku.
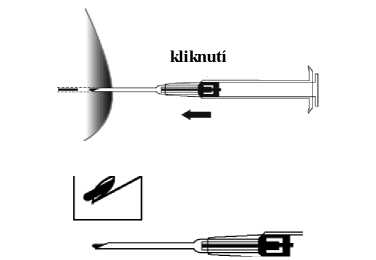
5. Injekční stříkačku opatrně vytáhněte asi 1 cm zpátky (punkční kanál pro implantát). K injikaci implantátu do punkčního kanálu píst zatlačte zcela dopředu, až zapadne na své místo a ozve se kliknutí.
6. Jehlu vytáhněte. Abyste se přesvědčil(a), že byl implantát injikován správně, zkontrolujte, že na hrotu jehly je vidět světle modrý konec pístu.
Na začátku používání a po 3 měsících používání přípravku Leptoprol se musí stanovit sérové hladiny jak PSA, tak testosteronu. Karcinom prostaty je citlivý na androgeny, pokud jsou po 3 měsících koncentrace testosteronu na kastračních hladinách (< 0,5 ng/ml), a pokud došlo k poklesu hodnoty PSA. Lze pozorovat výrazný časný pokles hodnoty PSA (přibližně 80 % výchozí hodnoty) jako dobrý prognostický indikátor dlouhodobé odpovědi na snížení hladin androgenů. Poté je indikována hormonální ablativní léčba (např. přípravek Leptoprol).
Pokud u pacientů se supresí testosteronu zůstávají hodnoty PSA nezměněny nebo pokud došlo k jejich vzestupu, je karcinom prostaty na androgeny necitlivý. V takových případech není pokračování v hormonální ablativní léčbě vhodné.
Pokud však pacient vykázal klinickou odpověď (např. zlepšení bolesti a symptomů dysurie, zmenšení prostaty), je nutno zvážit, zda výsledky nebyly falešně negativní. V těchto vzácných případech je nutno v podávání přípravku Leptoprol pokračovat další 3 měsíce a hodnoty PSA změřit znovu; pacient musí být navíc velmi pečlivě sledován, pokud jde o klinické symptomy.
Léčba pokročilého, hormonálně závislého karcinomu prostaty přípravkem Leptoprol je obecně terapií dlouhodobou.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1 nebo na jiná LHRH analoga.
Potvrzená hormonální independence karcinomu
Přípravek Leptoprol je kontraindikován u žen a pediatrických pacientů.
4.4 Zvláštní upozornění a opatření pro použití
Pacienty s hypertenzí je nutno pečlivě sledovat.
U pacientů léčených agonisty LHRH, jako je přípravek Leptoprol, existuje zvýšené riziko depresivních epizod (které mohou být závažné). Pacienti musí být o tomto riziku informováni, a pokud se příznaky objeví, musí být odpovídajícím způsobem léčeni.
Byly pozorovány alergické a anafylaktické reakce. Zahrnují jak lokální reakce v místě injekce, tak systémové příznaky.
Po chirurgické kastraci přípravek Leptoprol nevyvolává žádné další snížení koncentrace testosteronu.
S ohledem na krátkodobý vzestup sérových koncentrací testosteronu na začátku léčby, což může dočasně zesílit určité příznaky onemocnění, je nutno během prvních týdnů léčby pacienty s rizikem neurologických komplikací, metastáz do míchy a obstrukce močových cest stále sledovat, a to pokud možno jako hospitalizované pacienty.
V počáteční fázi léčby je nutno zvážit dodatečné podávání vhodného antiandrogenu, aby se zmírnily případné následky počátečního výrazného vzestupu testosteronu a zhoršení klinických symptomů.
Terapeutický úspěch je nutno pravidelně sledovat (zejména při prokázané progresi navzdory příslušné léčbě) prostřednictvím klinických vyšetření (digitální rektální vyšetření prostaty, ultrazvuk, scintigrafie skeletu, počítačová tomografie) a kontrolováním fosfátů a/nebo prostatického specifického antigenu (PSA) a sérových koncentrací testosteronu.
Hypogonadismus vyskytující se během dlouhodobé léčby analogy LHRH a/nebo při orchiektomii může vést k osteoporóze se zvýšeným rizikem fraktur, přičemž vznik osteoporózy je výraznější po orchiektomii, kdy jsou zvýšeny hladiny kortisolu, než po podávání analogů LHRH. U vysoce ohrožených pacientů může demineralizaci kostí zabránit dodatečné podávání bisfosfonátu.
U některých pacientů léčených analogy LHRH byla hlášena změna glukózové tolerance. Diabetici musí být během léčby přípravkem Leptoprol velmi pečlivě sledováni.
Androgen-deprivační terapie může prodlužovat QT interval.
Před zahájením léčby přípravkem Leptoprol by měl lékař zvážit poměr přínosů a rizik, včetně rizika torsade de pointes, u pacientů s rizikovými faktory pro prodloužení QT intervalu v anamnéze a u pacientů souběžně užívajících léčivé přípravky, které mohou prodlužovat QT interval (viz bod 4.5).
Pozor by si měli dávat aktivně sportující pacienti, protože přípravek Leptoprol obsahuje látku, která může způsobovat pozitivní výsledek při dopingové kontrole.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Kvůli souvislosti androgen-deprivační terapie a prodlužení QT interval by měla být pečlivě zvážena souběžná léčba přípravkem Leptoprol s léčivými přípravky, o kterých je známo, že prodlužují QT interval, a léčba přípravky, které mohou vyvolat torsade de pointes, jako antiarytmika třídy IA (např. chinidin, disopyramid), třídy III (např. amiodaron, sotalol, dofetilid, ibutilid), methadon, moxifloxacin, antipsychotika a další (viz bod 4.4).
4.6 Fertilita, těhotenství a kojení
Přípravek Leptoprol je určen k používání pouze u mužů.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Tento léčivý přípravek může změnit reaktivitu v takovém rozsahu, dokonce i když je používán, jak bylo zamýšleno, že je narušena schopnost řídit a obsluhovat stroje. Je to z důvodu únavy, která se může vyskytnout u některých pacientů, zejména na začátku léčby, což může být take zapříčiněno základním nádorovým onemocněním. Toto se vztahuje ještě ve větším rozsahu při kombinaci s alkoholem.
4.8 Nežádoucí účinky
Nejdříve je normální krátkodobý vzestup sérové koncentrace testosteronu, který může dočasně zhoršit určité symptomy onemocnění (bolest v kostech nebo zhoršení bolesti v kostech, obstrukce v urinárním traktu a její následky, komprese míchy, svalová slabost v nohou, lymfatický edém). Toto zhoršení příznaků normálně ustupuje spontánně bez nutnosti přerušit léčbu přípravkem Leptoprol.
Nežádoucí účinky se mohou objevit z důvodu nedostatku pohlavních hormonů.
Tabulární přehled nežádoucích účinků:
Nežádoucí účinky jsou uvedeny na základě tříd orgánových systémů a MedDRA konvence četnosti výskytu nežádoucích účinků:
Velmi časté: >1/10 Časté: >1/100, <1/10
Méně časté: >1/1 000, <1/100 Vzácné: >1/10 000, <1/1 000
Velmi vzácné: <1/10 000
Není známo: četnost z dostupných údajů nelze určit
|
Velmi |
Časté |
Méně časté |
Vzácné |
Velmi |
Není | |
|
časté |
vzácné |
známo |
|
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo | |
|
Poruchy imunitního systému |
Generalizo vané alergické reakce (horečka, eozinofilie, kožní |
Anafylaktic ké reakce | ||||
|
Poruchy metabolism a výživy |
Nárůst tělesné hmotnosti |
Snížení chuti k jídlu, zvýšení chuti k jídlu, ztráta tělesné hmotnosti |
Změny v diabetickém metabolické m stavu (zvýšení nebo snížení hodnot krevního cukru) | |||
|
Psychiatrické poruchy |
Změny nálad, deprese; poruchy spánku | |||||
|
Poruchy nervového systému |
Bolest hlavy, parestezie |
tranzitorní dysgeuzie |
Apoplexie hypofýzy po úvodním podání leuprorelin u u pacientů s adenomem hypofýzy* | |||
|
Srdeční poruchy |
Prodloužení QT intervalu (viz body 4.4 a 4.5) | |||||
|
Cévní poruchy |
Návaly horka |
Změny krevního tlaku (hypertenze nebo hypotenze), trombóza | ||||
|
Respirační, hrudní a mediastinální poruchy |
Plicní embolie | |||||
|
Gastrointestin ální poruchy |
Nauzea/ |
|
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo | |
|
Poruchy kůže a podkožních tkání |
Suchost kůže nebo sliznic, noční pocení |
alopecie | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Bolest v kostech |
Bolest kloubů a/nebo zad, myasthenie, bolest v perineu, bolest v nadbřišku | ||||
|
Poruchy ledvin a močových cest |
Nykturie, polakisurie |
Retence moči | ||||
|
Poruchy reprodukčníh o systému a prsu |
Snížení nebo ztráta libida a sexuální potence, zmenšení velikosti varlat |
Gynekomas tie |
Bolest varlat | |||
|
Celkové poruchy a reakce v místě aplikace |
Zvýšené pocení; reakce v místě vpichu, např. zarudnutí, bolest, otok, které se obvykle zmírní i při pokračující léčbe |
Únava, periferní edém, celková slabost |
V ojedinělých případech absces v místě vpichu |
|
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo | |
|
Vyšetření |
Vzestup LDH, transamináz (ALT, AST), gamma-GT a alkalické fosfatázy, které zároveň mohou být projevem základního onemocněn í |
*Apoplexie hypofýzy:
Jako u jiných léčivých přípravků z této skupiny látek existují u pacientů s adenomem hypofýzy hlášení velmi vzácných případů apoplexie hypofýzy po počátečním podání leuprorelinu.
Existují poregistrační hlášení intersticiální pneumonie, zejména v Japonsku.
Vyskytl se ojedinělý případ trombózy centrální retinální arterie.
Zvláštní poznámky
Odpověď na léčbu přípravkem Leptoprol lze sledovat měřením sérových koncentrací testosteronu, kyselé fosfatázy a PSA (prostatický specifický antigen). Hladiny testosteronu se při zahájení léčby zpočátku zvýší, nicméně za 2 týdny poklesnou. Po 2 až 4 týdnech jsou dosažené koncentrace testosteronu srovnatelné s koncentracemi pozorovanými po bilaterální orchiektomii, přičemž poté zůstávají po celou dobu léčby konstantní.
V počáteční fázi léčby se mohou objevit přechodná zvýšení hladin kyselé fosfatázy. Normálních hladin nebo hladin blížících se normálu se obvykle opět dosáhne po pár týdnech.
Hypogonadismus objevující se při dlouhodobé léčbě analogy LHRH a/nebo po orchiektomii může vést k osteoporóze se zvýšeným rizikem fraktur (viz bod 4.4). U vysoce ohrožených pacientů může demineralizaci kostí zabránit dodatečné podávání bisfosfonátu.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv, Šrobárova 48, 100 41 Praha 10, webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek.
4.9 Předávkování
Doposud nebyly pozorovány žádné příznaky předávkování.
Dokonce i při dávkách až do 20 mg leuprorelin-acetátu denně v průběhu 2 let, tak jak to bylo v případě prvních klinických studií, nebyl pozorován žádný další nebo nový nežádoucí účinek, který by se lišil od těch po každodenním podávání 1 mg nebo tříměsíčním podávání 11,25 mg.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Hormony a příbuzné látky, analogy gonadotropin-releasing hormonu ATC kód: L02A E02
Leuprorelin-acetát, léčivá látka obsažená v přípravku Leptoprol, je syntetickým analogem přirozeně se vyskytujícího hypothalamického "uvolňujícího faktoru" LHRH, který řídí uvolňování gonadotropních hormonů LH (luteinizační hormon) a FSH (folikuly stimulující hormon) z předního laloku hypofýzy. Tyto hormony dále stimulují syntézu pohlavních steroidů.
Narozdíl od fyziologického LHRH, který se z hypothalamu uvolňuje pulzním způsobem, leuprorelin-acetát - rovněž známý jako agonista LHRH - blokuje receptory LHRH v hypofýze během dlouhodobé léčby trvale, a po počáteční krátkodobé stimulaci vede k jejich down regulaci. Výsledkem dochází k reverzibilnímu útlumu uvolňování gonadotropinů z hypofýzy s následným poklesem koncentrací testosteronu.
Koncentrace testosteronu jsou sníženy a to ve svém důsledku ovlivňuje růst nádorové tkáně prostaty, který je normálně stimulován dihydrotestosteronem, který se vytváří redukcí testosteronu v prostatických buňkách.
Kontinuální podávání leuprorelin-acetátu vede k poklesu počtu a/nebo citlivosti (tzv. "down regulace") receptorů v hypofýze a v důsledku toho k poklesu koncentrací LH, FSH a DHT. Během tohoto procesu se hladina testosteronu sníží na kastrační úroveň.
Antiandrogenní účinek a inhibice růstu karcinomů prostaty byly rovněž prokázány ve studiích na zvířatech.
Podle preklinických a klinických studií měsíční léčba leuprorelin-acetátem po počáteční stimulaci inhibuje uvolňování gonadotropinů.
U člověka subkutánní podání leuprorelin-acetátu způsobuje počáteční zvýšení LH (luteinizační hormon) a FSH (folikuly stimulující hormon), což se vyznačuje přechodným zvýšením koncentrací testosteronu a dihydrotestosteronu.
Jelikož byla v ojedinělých případech během prvních 3 týdnů pozorována krátkodobá symptomatická zhoršení onemocnění, mělo by se u mužů s karcinomem prostaty zvážit adjuvantní podávání antiandrogenů.
Naproti tomu dlouhodobá léčba leuprorelin-acetátem způsobuje pokles koncentrací LH a FSH u všech pacientů; koncentrace androgenů u mužů se dosahují na podobné úrovni, jako u mužů po bilaterální orchiektomii. Tyto změny se obvykle objeví 2 až 3 týdny po začátku léčby a po celou dobu léčby přetrvávají. Z tohoto důvodu lze pomocí leuprorelin-acetátu zjišťovat hormonální citlivost karcinomů prostaty a případnou terapeutickou hodnotu orchiektomie. Pokud je to nezbytné, může se orchiektomie nahradit každoměsíčním podáváním leuprorelin-acetátu. Do této doby se dařilo udržovat kastrační hladiny testosteronu po kontinuálním podávání leuprorelin-acetátu po dobu 5 let.
5.2 Farmakokinetické vlastnosti
Léčivá látka, leuprorelin-acetát, se kontinuálně uvolňuje z polymeru mléčné kyseliny po dobu až 182 dní (26 týdnů) po injikaci biodegradovatelného implantátu přípravku Leptoprol. Polymer se absorbuje stejným způsobem jako chirurgický šicí materiál.
Během 2 hodin po subkutánní aplikaci jedné dávky přípravku Leptoprol byly naměřeny maximální sérové koncentrace leuprorelinu dosahující 5216 pg/ml (5,2 ng/ml).
AUC během 3měsíční léčby přípravkem Leptoprol byla 32,4 ng/ml*d.
Detekovatelné hladiny v séru jsou přítomny po dobu až 182 dní (26 týdnů) po podání.
Distribuční objem leuprorelinu u mužů je 36 litrů; celková clearance je 139,6 ml/min.
U pacientů s poruchou funkce ledvin nebo jater byly hladiny leuprorelinu v rozmezí hladin pozorovaných u pacientů se zdravými ledvinami nebo játry. U některých pacientů s chronickým selháním ledvin byly naměřeny vyšší sérové hladiny leuprorelinu. Toto zjištění se však nezdá být klinicky nijak relevantní.
5.3 Předklinické údaje vztahující se k bezpečnosti
Preklinické studie přípravku Leptoprol prokázaly účinky na reprodukční orgány, které byly očekávány na základě známých farmakologických vlastností leuprorelinu.
Kancerogenita
U potkanů byl po subkutánní injekci dávek 0,6 až 4 mg/kg/den po dobu 12 a 24 měsíců pozorován na dávce závislý vzestup adenomů hypofýzy. U myší nebyl za 24 měsíců žádný takový účinek pozorován.
Mutagenita
In vitro a in vivo studie leuprorelin-acetátu zaměřené na detekci genetických a chromosomálních mutací nedaly žádné důkazy mutagenního potenciálu.
Reprodukční toxicita
Ve studiích reprodukční toxicity na králících byla pozorována zvýšená fetální mortalita a snížená hmotnost plodů. Účinky na fetální mortalitu jsou předpokládaným důsledkem farmakodynamického účinku této látky.
Lokální snášenlivost
Neklinické studie na psech a králících odhalily dobrou lokální snášenlivost přípravku Leptoprol.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Kyselina polymléčná
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
4 roky
6.4 Zvláštní opatření pro uchovávání Uchovávejte při teplotě do 30 °C.
6.5 Druh obalu a obsah balení
Jednorázová polykarbonátová předplněná injekční stříkačka s pístem z akrylonitril-butadien-styren kopolymeru a s jehlou, hermeticky uzavřená ve vaku z polyetylen tereftalát/Al/PE kompositní fólie.
Velikosti balení: 1x1 implantát s leuprorelinum 5 mg (ve formě leuprorelini acetas)
2x1 implantát s leuprorelinum 5 mg (ve formě leuprorelini acetas)
3x1 implantát s leuprorelinum 5 mg (ve formě leuprorelini acetas)
5x1 implantát s leuprorelinum 5 mg (ve formě leuprorelini acetas)
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Žádné zvláštní požadavky na likvidaci.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Sandoz s.r.o., Praha, Česká republika
8. REGISTRAČNÍ ČÍSLO(A)
44/076/15-C
9. DATUM PRVNÍ REGISTRACE / PRODLOUŽENÍ REGISTRACE
Datum první registrace: 4.2.2015
10. DATUM REVIZE TEXTU
4.2.2015