Haemoctin Sdh 250
sp. zn. sukls123919/2015
Příbalová informace: informace pro uživatele
Haemoctin SDH 250 Haemoctin SDH 500 Haemoctin SDH 1000
Prášek a rozpouštědlo pro injekční roztok
Factor VIII coagulationis humanus (Koagulační faktor VIII derivovaný z lidské plazmy)
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek Haemoctin SDH a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Haemoctin SDH používat
3. Jak se přípravek Haemoctin SDH používá
4. Možné nežádoucí účinky
5. Jak přípravek Haemoctin SDH uchovávat
6. Obsah balení a další informace
Haemoctin SDH je lék odvozený z lidské plazmy. Obsahuje koagulační faktor VIII, který je nutný pro normální průběh srážení krve. Po rekonstituci prášku ve vodě na injekce je roztok připraven k intravenóznímu podání.
Haemoctin SDH je vhodný pro léčbu a profylaxi krvácení s hemofilií A (s dědičným nedostatkem faktoru VIII).
Haemoctin SDH neobsahuje von Willebrandův faktor ve farmakologicky účinném množství, a proto není vhodný pro léčbu von Willebrandovy nemoci.
2
Nepoužívejte přípravek Haemoctin SDH
• jestliže jste alergický(á) na koagulační faktor VIII nebo na kteroukoli další složku tohoto
přípravku (uvedenou v bodě 6). Alergická reakce se může projevovat jako vyrážka, svědění, obtíže při dýchání nebo otoky tváře, rtů, hrdla nebo jazyka.
Upozornění a opatření
Po zahájení léčby přípravkem Haemoctin SDH je možné, že si Váš imunní systém vyvine protilátky (inhibitory) proti faktoru VIII. Tyto inhibitory mohou ovlivňovat účinnost přípravku Haemoctin SDH. Váš lékař bude pravidelně kontrolovat tvorbu inhibitorů pomocí biologického testu (Bethesda testu).
Výskyt inhibitorů faktoru VIII dokazuje neúspěšnost terapie. Množství inhibitorů v těle se vyjadřuje v jednotkách Bethesda (BU) najeden ml krevní plazmy. Riziko vytvoření inhibitorů je závislé na podávání faktoru VIII a je největší během prvních 20 dnů podání. Inhibitory se vzácně tvoří i po více než 100 dnech podání.Případy recidivujících inhibitorů byly pozorovány po přechodu z jednoho faktoru VIII na jiný u dříve léčených pacientů s více než 100 dny expozice, kteří měli v anamnéze tvorbu inhibitoru.
K aplikaci smí být použity pouze přiložené infuzní sety, protože vlivem adsorpce faktoru VIII k vnitřnímu povrchu některých součástí infuzního setu by mohlo dojít k selhání léčby.
Haemoctin SDH nesmí být mísen s jinými léčivými přípravky.
Komplikace související s katetrem: Jestliže je třeba použít centrální žilní vstup (centrál venous access devices, CVAD), musí se uvážit riziko vzniku komplikací souvisejících s CVAD, včetně lokální infekce, bakteriemie a trombózy v místě vstupu katetru.
Bezpečnost vůči virům
V případě léčivých přípravků vyráběných z lidské krve nebo plazmy musí být přijata opatření, aby se zamezilo přenosu infekcí na pacienty. Tato opatření zahrnují:
• pečlivý výběr dárců krve a plazmy, aby bylo jisté, že byli vyloučeni jedinci, kteří by mohli přenášet infekce,
• testování každé darované krve a vzorků plazmy na přítomnost virů/infekcí,
• zařazení kroků při zpracování krve či plazmy, při nichž jsou viry inaktivovány nebo odstraněny. Přes všechna tato opatření při přípravě léků vyráběných z lidské krve nebo plazmy nelze možnost přenosu infekcí zcela vyloučit. To platí rovněž pro neznámé nebo nově objevené viry nebo jiné typy infekcí.
Přijatá opatření se považují za účinná u obalených virů, jako jsou virus lidské imunodeficience (HIV), virus hepatitidy B (HBV) a virus hepatitidy C (HCV), a pro neobalený virus hepatitidy A (HAV). Eliminace/inaktivace viru může mít omezený účinek u jiných neobalených virů, jako je například parvovirus B19. Infekce parvovirem B19 může být závažná pro těhotné ženy (infekce plodu) a u jedinců s imunodeficitem nebo zvýšenou produkcí červených krvinek (např. u srpkovité nebo hemolytické anémie).
Váš lékař Vám může doporučit, abyste zvážil/a očkování proti hepatitidě A a B, jestliže pravidelně/opakovaně dostáváte léky na bázi faktoru VIII derivované z lidské plazmy.
Velice se doporučuje, aby byl při každém podání přípravku Haemoctin SDH pacientovi zaznamenán název a číslo šarže přípravku, aby se zachoval záznam o použitých šaržích.
Další léčivé přípravky a přípravek Haemoctin SDH
Informujte svého lékaře o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Interakce mezi přípravkem Haemoctin SDH a jinými léčivými přípravky nejsou známé.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek používat.
Vzhledem k vzácnému výskytu hemofilie A u žen nejsou k dispozici zkušenosti o používání přípravku Haemoctin SDH během těhotenství nebo kojení. Nebyly provedeny pokusy na zvířatech během těhotenství nebo kojení.
Řízení dopravních prostředků a obsluha strojů
Používání přípravku Haemoctin SDH neovlivňuje schopnost řídit a obsluhovat stroje.
Přípravek Haemoctin SDH obsahuje sodík
Haemoctin SDH 250: Jedna injekční lahvička obsahuje až 16,1 mg (0,70 mmol) sodíku. To je třeba vzít v úvahu, jestliže jste na dietě s nízkým obsahem sodíku.
Haemoctin SDH 500: Jedna injekční lahvička obsahuje až 32,2 mg (1,40 mmol) sodíku. To je třeba vzít v úvahu, jestliže j ste na dietě s nízkým obsahem sodíku.
Haemoctin SDH 1000: Jedna injekční lahvička obsahuje až 32,2 mg (1,40 mmol) sodíku. To je třeba vzít v úvahu, jestliže j ste na dietě s nízkým obsahem sodíku.
Přípravek Haemoctin SDH je určen k intravenóznímu podání (injekcí do žíly). Léčba by měla být zahajována pod dohledem lékaře, který již má s léčbou hemofilie A zkušenosti. Vždy používejte přípravek Haemoctin SDH přesně podle pokynů svého lékaře. Pokud si nejste jistý/á, poraďte se se svým lékařem. Dávkování a délka léčby závisí na závažnosti nedostatku faktoru VIII, místě a rozsahu krvácení a Vašem klinickém stavu. Lékař pro Vás stanoví správnou dávku přípravku.
Ve všech krocích přípravy je nutné pracovat sterilně.
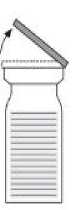
Fig. 1
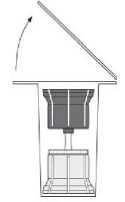
Fig. 2
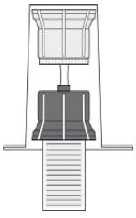
Fig. 3
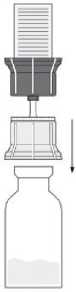
Fig. 4
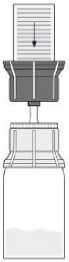
Fig. 5
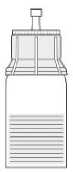
Fig. 6
Rozpouštění koncentrátu:
• Ohřejte rozpouštědlo (vodu na injekci) a prášek
na pokojovou teplotu v neotevřených injekčních lahvičkách. Pokud je používána k zahřívání vodní lázeň, je nutno úzkostlivě dbát, aby voda nepřišla do kontaktu s víčkem nebo zátkou na injekční lahvičky. Jinak může dojít ke kontaminaci přípravku.
• Odstraňte víčka z obou injekčních lahviček tak, aby se odkryla centrální část pryžové zátky (1). Očistěte zátky přípravku
a injekčních lahviček s rozpouštědlem dezinfekčním prostředkem.
• Sejměte uzávěr obalu převodního zařízení (2). Umístěte modrou část převodního zařízení na svisle stojící injekční lahvičku obsahující rozpouštědlo (3).
• Odstraňte zbývající část obalu převodního zařízení. Tak se odhalí průhledná část převodního zařízení.
• Položte injekční lahvičku s přípravkem na rovný povrch.
• Obraťte převodní zařízení s injekční lahvičkou s rozpouštědlem dnem vzhůru. Vtlačte hrot průhledné části adaptéru kolmo dolů skrz zátku injekční lahvičky přípravku (4). Vakuum přítomné v injekční lahvičce s přípravkem způsobí, že rozpouštědlo proteče do injekční lahvičky s přípravkem (5). Okamžitě vyšroubujte modrou část převodního zařízení zároveň s injekční lahvičkou s rozpouštědlem. Zlikvidujte injekční lahvičku s rozpouštědlem
s modrou částí připojeného převodního zařízení (6). Opatrné otáčení injekční lahvičky
napomůže v rozpouštění prášku. S lahvičkou netřeste, je nutné se vyhnout tvorbě pěny! Roztok je čirý nebo lehce opalescentní.
• Rozpuštěný roztok se musí použít ihned po rozpuštění. Roztoky se zákalem nebo viditelnými částicemi se nesmí použít.

Fig. 7
Injekce:
Po rozpuštění prášku podle popisu výše, našroubujte přiloženou injekční stříkačku konektorem typu luer-lock na injekční lahvičku s průhlednou částí převodního zařízení (7). Pak je možné natáhnout rozpuštěný přípravek snadno do injekční stříkačky. Není potřeba zvláštní filtr, neboť převodní zařízení má zabudovaný vlastní filtr.
Opatrně odpojte injekční lahvičku s průhlednou částí převodního zařízení od injekční stříkačky. Přípravek pomalu intravenózně aplikujte pomocí přiložené motýlkové jehly. Rychlost podání injekce nesmí přesáhnout 2-3 ml za minutu.
Po použití motýlkové kanyly použijte ochranné víčko, aby byla další manipulace bezpečná.
Jestliže jste použil/a více přípravku Haemoctin SDH, než jste měl/a
Pokud si myslíte, že jste dostal/a příliš mnoho Haemoctin SDH, informujte svého lékaře, který rozhodne o dalším postupu.
Jestliže jste zapomněl/a užít Haemoctin SDH
V tomto případě musí lékař rozhodnout, zda je nutná další léčba.
Jestliže jste přestal/a užívat přípravek Haemoctin SDH
Nepřestávejte používat přípravek Haemoctin SDH bez porady s lékařem.
Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Okamžitě informuje svého lékaře, jestliže zaznamenáte některý z následujících stavů:
• zarudnutí kůže,
• pálení a bodání v místě vpichu,
• zimnice,
• návaly horka,
• bolest hlavy,
• kopřivka,
• hypotenze,
• letargie,
• nevolnost,
• neklid,
• tachykardie,
• nepříjemné pocity na hrudi,
• brnění,
• zvracení,
• sípání.
Může to být alergická nebo závažná alergická reakce (anafylaktický šok) nebo hypersenzitivní reakce.
Velmi vzácně byly hlášeny následující nežádoucí účinky (méně než 1 uživatel z 10 000)
• Pozitivní protilátky proti faktoru VIII: Pacienti s hemofilií A mohou vytvářet neutralizující protilátky (inhibitory) na faktor VIII. Jestliže se takové inhibitory objeví, znamená to, že léčba má nedostatečnou klinickou odpověď (např. krvácení). V takových případech se doporučuje kontaktovat specializované pracoviště pro hemofilii.
• horečka,
Nežádoucí účinky u dětí a dospívajících
Nežádoucí účinky u dětí budou pravděpodobně stejné jako u dospělých.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv, Šrobárova 48, 100 41 Praha 10, webové stránky: www .sukl.cz/nahlasit-nezadouci -ucinek.
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Haemoctin SDH uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte injekční lahvičky v krabičce, aby byl přípravek chráněn před světlem.
Uchovávejte při teplotě do 25 °C. Chraňte před mrazem.
Přípravek Haemoctin SDH nepoužívejte po uplynutí doby použitelnosti, uvedené na štítku injekční lahvičky a krabičky.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Haemoctin SDH obsahuje
• Léčivou látkou je factor VIII coagulationis humanus
• Dalšími složkami jsou glycin, chlorid sodný, natrium-citrát a chlorid vápenatý.
• Injekční lahvička s rozpouštědlem obsahuje vodu na injekce.
Jak přípravek Haemoctin SDH vypadá a co obsahuje toto balení
Přípravek Haemoctin SDH je dodáván jako lyofilizovaný prášek (lyofilizát). Voda na injekce slouží jako rozpouštědlo. Rozpuštěný přípravek je čirý nebo lehce opalescentní.
Haemoctin SDH 250 obsahuje 1 injekční lahvičku s 250 IU a 1 injekční lahvičku s 5 ml vody na injekce (50 IU/ml)
Haemoctin SDH 500 obsahuje 1 injekční lahvičku s 500 IU a 1 injekční lahvičku s 10 ml vody na injekce (50 IU/ml)
Haemoctin SDH 1000 obsahuje 1 injekční lahvičku s 1000 IU a 1 injekční lahvičku s 10 ml vody na injekce (100 IU/ml)
Jedno balení obsahuje:
• j ednu j ednorázovou inj ekční stříkačku,
• jedno převodní zařízení se zabudovaným filtrem,
• jednu motýlkovou kanylu,
Držitel rozhodnutí o registraci a výrobce
Biotest Pharma GmbH Landsteinerstrasse 5 63303 Dreieich Německo
Tel.: +49 6103 801-0 Fax: +49 6103 801-150 mail@biotest.de
Pro veškeré informace týkající se tohoto přípravku, prosím kontaktujte místního zástupce držitele rozhodnutí o registraci:
Reg-Pharm spol.s.r.o.
Fialková 45 10600 Praha 10 Tel.: 272 654 004 Fax: 272 650 187 info@regpharm.cz
Tato příbalová informace byla naposledy revidována: 01/2016.
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Způsob podání:
Haemoctin SDH je určen k intravenóznímu podání. Doporučuje se, aby rychlost podání injekce nepřesáhla 2-3 ml za minutu.
Dávkování
Dávkování a délka trvání substituční léčby závisí na závažnosti nedostatku faktoru VIII, místě a rozsahu krvácení a klinickém stavu pacienta.
Počet jednotek podaného faktoru VIII se vyjadřuje v mezinárodních jednotkách (IU), které se vztahují k stávající normě WHO pro přípravky na bázi faktoru VIII. Aktivita faktoru VIII v plazmě se vyjadřuje buď jako procento (ve vztahu k normální lidské plazmě), nebo v mezinárodních jednotkách (ve vztahu k mezinárodnímu standardu pro faktor VIII v plazmě).
Jedna mezinárodní jednotka (IU) aktivity faktoru VIII je ekvivalentní množství faktoru VIII v jednom ml normální lidské plazmy. Výpočet požadované dávky faktoru VIII je založen na empirické zkušenosti, že podání 1 mezinárodní jednotky (IU) faktoru VIII na kg tělesné hmotnosti zvýší hladinu plazmatického faktoru VIII o 1 % až 2 % normální aktivity.
Potřebnou dávku lze vypočítat podle následujícího vzorce:
Potřebné jednotky = tělesná hmotnost (kg) x požadované zvýšení hladiny faktoru VIII (%) x 0,5
Podané množství a frekvence podávání se musí řídit klinickou účinností v jednotlivých případech.
V případě následujících krvácivých událostí nesmí aktivita faktoru VIII klesnout pod danou hladinu aktivity plazmy (v % normální hodnoty) po odpovídající dobu. Následující tabulku lze použít jako návod dávkování u krvácivých epizod a při chirurgických výkonech:
|
Stupeň krvácení/ typ chirurgického výkonu |
Požadovaná hladina faktoru VIII (%) |
Četnost dávek (v hodinách)/ trvání léčby (ve dnech) |
|
Krvácení | ||
|
Počáteční hemartróza, krvácení do svalů nebo orální krvácení |
20 - 40 |
Opakovat každých 12 až 24 hodin. Nejméně 1 den, až do vyřešení krvácivé epizody indikované bolestí nebo do zhojení příslušného zranění. |
|
Extenzivnější hemartróza, svalové krvácení nebo hematom |
30 - 60 |
Opakovat každých 12 až 24 hodin po dobu 3 - 4 dnů, nebo až do vyřešení bolestivého a akutního stavu. |
|
Život ohrožující krvácení |
60 - 100 |
Opakovat každých 8 až 24 hodin až stav ohrožení pomine. |
|
Operace | ||
|
Malé včetně extrakce zubů |
30 - 60 |
Každých 24 hodin, alespoň 1 den, až do zhojení. |
|
Velké |
80 - 100 (před a po operaci) |
Opakovat každých 8 až 24 hodin, až do adekvátního zhojení ran, potom léčba po dobu alespoň 7 dalších dnů k udržení aktivity faktoru VIII v hladině 30 - 60 %. |
Během léčby se doporučuje stanovit hladiny faktoru VIII, aby bylo známo, jakou dávku podávat a jak často infuze opakovat. V případě velkých chirurgických výkonů je nevyhnutelné přesné monitorování substituční léčby pomocí koagulačních testů (aktivita plazmatického faktoru VIII). Jednotliví pacienti
mohou mít raznou odpověď na faktor VIII, dosahují různých úrovní in vivo obnovení a vykazují různé poločasy.
Při dlouhodobé profylaxi krvácení u pacientů s těžkou hemofilií A jsou obvyklé dávky 20 až 40 IU faktoru VIII na kg tělesné hmotnosti v 2 až 3denních intervalech. V některých případech, zvláště u mladších pacientů mohou být nezbytné kratší intervaly mezi aplikacemi nebo vyšší dávky.
Pacienti musí být sledováni, zda u nich nedochází k tvorbě inhibitorů faktoru VIII. Jestliže se nedosáhne očekávaných hladin aktivity faktoru VIII v plazmě nebo pokud se nedaří krvácení kontrolovat příslušnou dávkou, je nutné provést test, aby se zjistilo, zda není přítomen inhibitor faktoru VIII. U pacientů s vysokými hladinami inhibitoru faktoru VIII může být léčba neúčinná a je potřeba zvážit jiné možnosti léčby. Léčbu těchto pacientů by měli provádět pouze lékaři se zkušenostmi s léčbou pacientů s hemofilií.
8/8