Fulvestrant Sandoz 250 Mg
Sp.zn.sukls203264/2015
Příbalová informace: informace pro pacienta Fulvestrant Sandoz 250 mg
injekční roztok v předplněné injekční stříkačce fulvestrantum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek Fulvestrant Sandoz a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Fulvestrant Sandoz používat
3. Jak se přípravek Fulvestrant Sandoz používá
4. Možné nežádoucí účinky
5. Jak přípravek Fulvestrant Sandoz uchovávat
6. Obsah balení a další informace
1. Co je přípravek Fulvestrant Sandoz a k čemu se používá
Přípravek Fulvestrant Sandoz obsahuje léčivou látku fulvestrant, který patří do skupiny blokátorů estrogenů.
Estrogeny jsou ženské pohlavní hormony a mohou se v některých případech podílet na růstu karcinomu (zhoubného nádoru) prsu.
Přípravek Fulvestrant Sandoz se používá k léčbě pokročilého nebo metastazujícího karcinomu prsu u žen po menopauze.
2. Čemu musíte věnovat pozornost, než začnete přípravek Fulvestrant Sandoz používat Nepoužívejte přípravek Fulvestrant Sandoz:
• jestliže jste alergická na fulvestrant nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6 „ Co přípravek Fulvestrant Sandoz obsahuje“)
• jestliže jste těhotná nebo kojíte
• máte-li závažné problémy s játry.
Upozornění a opatření
Sdělte svému lékaři, pokud se Vás týká cokoli z následujícího:
• problémy s ledvinami nebo játry
• nízký počet krevních destiček (pomáhají srážet krev) nebo krvácivá porucha
dřívější problémy s krevními sraženinami
• osteoporóza (úbytek kostní hmoty)
• alkoholizmus.
Děti a dospívající
Fulvestrant Sandoz není určen dětem a dospívajícím mladším 18 let.
Další léčivé přípravky a přípravek Fulvestrant Sandoz
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte nebo jste užívala v nedávné době.
Nezapomeňte lékaře informovat zvláště, pokud užíváte antikoagulancia (léky zamezující tvorbě krevních sraženin).
Těhotenství a kojení
Přípravek Fulvestrant Sandoz nesmíte používat, pokud jste těhotná. Pokud byste mohla otěhotnět, je třeba, abyste v průběhu léčby přípravkem Fulvestrant Sandoz používala účinnou antikoncepci.
V průběhu léčby přípravkem Fulvestrant Sandoz nesmíte kojit.
Řízení dopravních prostředků a obsluha strojů
Fulvestrant Sandoz pravděpodobně neovlivní schopnost řídit nebo obsluhovat stroje. Pokud se však po léčbě cítíte unavená, neřiďte ani neobsluhujte stroje.
Přípravek Fulvestrant Sandoz obsahuje 10 % obj. ethanolu (alkoholu), tj. do 1000 mg v jedné dávce, což odpovídá do 20 ml piva nebo 8 ml vína.
Je škodlivý pro alkoholiky.
Je nutno vzít v úvahu u těhotných a kojících žen, dětí a vysoce rizikových skupin, jako jsou pacienti s onemocněním jater nebo ledvin nebo epilepsií.
Přípravek Fulvestrant Sandoz obsahuje 100 mg benzylalkoholu v jednom mililitru. Nesmí se podávat předčasně narozeným dětem nebo novorozencům. U dětí do 3 let věku může vyvolat toxické reakce a alergické reakce.
Přípravek Fulvestrant Sandoz obsahuje 150 mg benzyl-benzoátu v jednom mililitru. Může zvyšovat riziko žloutenky u novorozenců.
3. Jak se přípravek Fulvestrant Sandoz používá
Dávkování určí individuálně Váš lékař.
Doporučená dávka přípravku je 500 mg fulvestrantu (dvě 250mg injekce) podávaných jednou měsíčně s jednou další 500mg dávkou podanou 2 týdny po podání zahajovací dávky.
Váš lékař nebo zdravotní sestra Vám podá Fulvestrant Sandoz jako pomalou nitrosvalovou injekci, po jedné injekci do každé hýždě.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Pokud se objeví následující nežádoucí účinky, můžete potřebovat neodkladnou lékařskou pomoc:
• Alergická reakce (reakce z přecitlivělosti) zahrnující otok obličeje, rtů, jazyka a/nebo hrdla
• Tromboembolismus (zvýšené riziko tvorby krevních sraženin)*
• Zánět jater (hepatitida)
• Selhání jater.
Poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou, pokud si všimnete následujících nežádoucích účinků:
Velmi časté nežádoucí účinky (mohou se objevit u více než 1 z 10 pacientů)
• Reakce v místě injekce, např. bolest a/nebo zánět
• Abnormální hladiny jaterních enzymů (při kontrole krve)*
• Pocit na zvracení (nevolnost)
• Slabost, únava*.
Časté nežádoucí účinky (mohou se objevit až u 1 z 10 pacientů)
• Bolest hlavy
• Návaly horka
• Zvracení, průjem nebo ztráta chuti k jídlu*
• Vyrážka
• Infekce močových cest
• Bolest zad*
• Zvýšený bilirubin (žlučové barvivo, které se tvoří v játrech)
• Tromboembolismus (zvýšené riziko tvorby krevních sraženin)*
• Alergické reakce (reakce z přecitlivělosti) zahrnující otok obličeje, rtů, jazyka a/nebo hrdla.
Méně časté nežádoucí účinky (mohou se objevit až u 1 ze 100 pacientů)
• Snížený počet krevních destiček (trombocytopenie)
• Vaginální (poševní) krvácení, hustý bělavý výtok a kandidóza (kvasinková infekce)
• Tvorba modřin a krvácení v místě vpichu injekce
• Zvýšená hladina GMT, jaterního enzymu, zjištěného při kontrole krve
• Zánět jater (hepatitida)
• Selhání jater.
* Zahrnuje nežádoucí účinky, u kterých nelze přesně určit úlohu přípravku Fulvestrant Sandoz vzhledem k probíhající nemoci.
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv, Šrobárova 48, 100 41 Praha 10,
Webové stránky: http://www.sukl.cz/nahlasit-nezadouci-ucinek.
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Fulvestrant Sandoz uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte v chladničce (2 °C - 8 °C).
Předplněnou injekční stříkačku uchovávejte v původním obalu, aby byl přípravek chráněn před světlem.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce nebo štítku injekční stříkačky za Použitelné do:/EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento léčivý přípravek nepoužívejte, pokud zjistíte, že došlo k jakémukoli zhoršení kvality zařízení nebo jeho obsahu, jako je poškození injekční stříkačky, zakalený roztok, plovoucí částice nebo změna barvy roztoku.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Fulvestrant Sandoz obsahuje
• Léčivou látkou j e fulvestrantum.
Jedna předplněná injekční stříkačka obsahuje fulvestrantum 250 mg v 5 ml roztoku (50 mg/ml).
• Dalšími pomocnými látkami jsou ethanol (96%), benzylalkohol, benzyl-benzoát a panenský ricinový olej.
Jak přípravek Fulvestrant Sandoz vypadá a co obsahuje balení
Fulvestrant Sandoz je čirý bezbarvý až žlutý viskózní injekční roztok v předplněné injekční stříkačce. Fulvestrant Sandoz se dodává v balení obsahující jednu nebo dvě jednotlivě používané předplněné injekční stříkačky. Dále je přiložena sterilní jehla.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
Sandoz s.r.o., U Nákladového nádraží 10, 130 00 Praha 3, Česká republika Výrobce
Lek Pharmaceuticals d.d., Verovškova 57, 1526 Ljubljana, Slovinsko
EBEWE Pharma Ges.m.b.H. Nfg.KG, Mondseestrasse 11, 4866 Unterach, Rakousko
Tento léčivý přípravek byl v zemích EHP registrován pod následujícími názvy:
Portugalsko
Rakousko
Belgie
Bulharsko
Česká republika
Německo
Dánsko
Estonsko
Španělsko
Finsko
Francie
Chorvatsko
Maďarsko
Irsko
Island
Itálie
Lotyšsko
Lucembursko
Nizozemsko
Norsko
Polsko
Rumunsko
Švédsko
Slovinsko
Slovenská republika Velká Británie
Fulvestrant Sandoz Fulvestrant Sandoz 50mg/ml -Infusionslósung in einer Fertigspritze Fulvestrant Sandoz 250 mg oplossing voor injectie, voorgevulde spuit Fulvestrant Sandoz 250 mg/5 ml Solution for injection in pre-filled syringe Fulvestrant Sandoz 250 mg Fulvestrant - 1 A Pharma Fulvestrant Sandoz Fulvestrant Sandoz
Afultrant 250 mg solucion inyectable en jeringa precargada EFG Fulvestrant Sandoz 250 mg injektioneste, liuos esitaytetyssa ruiskussa FULVESTRANT SANDOZ 250 mg, solution injectable en seringue préremplie
Fulvestrant Sandoz 250 mg otopina za injekciju u napunjenoj štrcaljki
Fulvestrant Sandoz 250 mg oldatos injekció eloretóltótt fecskendoben Fulvestrant Rowex 250 mg/5 ml solution for injection in pre-filled syringe Fulvestrant Sandoz 250 mg stungulyf, lausn í áfylltri sprautu
Fulvestrant Sandoz Fulvestrant Sandoz 50 mg/ml injekcinis tirpalas užpildytame švirkšte Fulvestrant Sandoz 250 mg solution
injectable, seringue préremplie
Fulvestrant Sandoz 50 mg/ml,
oplossing voor injectie in voorgevulde injectiespuit
Fulvestrant Sandoz 250 mg
injeksjonsv^ske, oppl0sning I ferdigfylt sprayte
Fulvestrant Sandoz
Fulvestrant Sandoz 250 mg solupe injectabilá in seringá preumplutá
Fulvestrant Sandoz 250 mg injektionsvatska, lósning i fórfylld spruta
Fulvestrant Lek 250 mg raztopina za injiciranje v napolnjeni injekcijski brizgi
Fulvestrant Sandoz 250 mg
Fulvestrant 250 mg, Solution for Injection in pre-filled syringe
Tato příbalová informace byla naposledy revidována: 11.3.2016
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Pokyny pro použití:
Upozornění - bezpečnostní jehlu před použitím neautoklávujte. Ruce musí zůstat po celou dobu použití a při likvidaci stále za jehlou.
Injekční stříkačky se dodávají s bezpečnostní jehlou BD SafetyGlide® nebo Terumo SurGuard®.
Pokyny k bezpečnostní jehle BD SafetyGlide®
Platí pro obě injekční stříkačky:
• Jehlu a injekční stříkačku opatrně vyjměte z obalu.
• Ze špičky válce injekční stříkačky sejměte ochranný kryt.
• Sloupnutím otevřete zevní obal a vyjměte bezpečnostní jehlu (BD SafetyGlide). Bezpečnostní jehlu nasaďte na konektor Luer-Lock.
• Jehlu připojíte otáčením na konektor Luer. Otáčejte, dokud nebude jehla pevně nasazena.
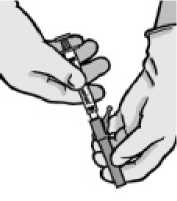
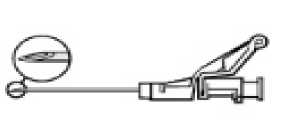
• Krycí štít stáhněte přímým tahem z jehly tak, aby nedošlo k poškození její špičky.
• Z j ehly sej měte pouzdro.
• Držte injekční stříkačku tak, aby jehla směřovala nahoru a jemně tlačte na píst, dokud léčivý přípravek nedosáhne špičky injekční stříkačky. Ve válci nesmí být žádný vzduch.
• Podávejte pomalu intramuskulárně (1 až 2 minuty/injekce) do hýždě. Pro pohodlí při aplikaci je seříznutí hrotu jehly orientováno směrem k rameni páčky.
Po injekci ihned prstem jednou klepněte na rameno páčky, čímž se aktivuje krycí mechanismus.
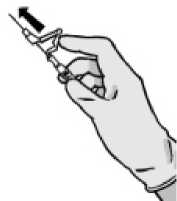
POZNÁMKA: aktivujte směrem od sebe a jiných osob. Musí se ozvat cvaknutí, přičemž vizuálně zkontrolujte, že je špička jehly plně zakryta.
Pokyny k bezpečnostní jehle Terumo SurGuard®
Platí pro obě injekční stříkačky:
• Jehlu a injekční stříkačku opatrně vyjměte z obalu.
• Ze špičky válce injekční stříkačky sejměte krytku.

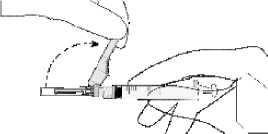
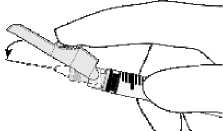
• Injekční stříkačku na jehlu připevněte pomocí aseptického postupu. Uchopte jehlu za její dolní část, nikoli za pouzdro, a injekční stříkačkou otočte ve směru hodinových ručiček.
• Z jehly odtáhněte bezpečnostní štít směrem k válci injekční stříkačky do úhlu ukázaného na obrázku. Poté odstraňte krytku jehly.
• Držte injekční stříkačku tak, aby jehla směřovala nahoru a jemně tlačte na píst, dokud léčivý přípravek nedosáhne špičky injekční stříkačky. Ve válci nesmí být žádný vzduch.
• Podávejte pomalu intramuskulárně (1 až 2 minuty/injekce) do hýždě.
• Po dokončení injekce jehlu vytáhněte z kůže a jednou rukou aktivujte bezpečnostní mechanismus, přičemž využijte některý ze tří postupů:
aktivace prstem
aktivace palcem
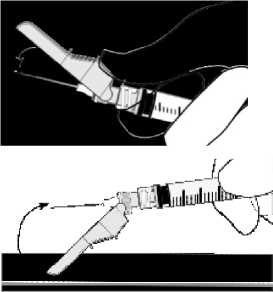
aktivace o povrch
Aktivace se ověří slyšitelným a/nebo hmatatelným „cvaknutím” a lze ji potvrdit vizuálně. Pokud si nejste jistí, že je bezpečnostní štít plně aktivován, tento krok opakujte.
Likvidace
Předplněné injekční stříkačky jsou určeny pouze k jednorázovému použití.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
8/8