Efflumidex Liquifilm
sp. zn.: sukls35258/2013 a sp. zn.: sukls151801/2014
Příbalová informace: informace pro pacienta EFFLUMIDEX Liquifilm 1 mg/ml
oční kapky, suspenze fluorometholonum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek
používat,protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci.Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Efflumidex Liquifilm a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Efflumidex Liquifilm používat
3. Jak se Efflumidex Liquifilm používá
4. Možné nežádoucí účinky
5 Jak uchovávat Efflumidex Liquifilm
6. Obsah balení a další informace
1. CO JE EFFLUMIDEX LIQUIFILM A K ČEMU SE POUŽÍVÁ
Efflumidex Liquifilm jsou oční kapky obsahující steroid určený k léčbě očních zánětů.
2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE EFFLUMIDEX LIQUIFILM POUŽÍVAT
Nepoužívejte Efflumidex Liquifilm:
• Jestliže j ste alergický(á) na fluorometholon, benzalkonium-chlorid nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6)
• pokud trpíte bakteriální, virovou nebo plísňovou infekcí oka
Upozornění a opatření:
Nepoužívejte Efflumidex Liquifilm déle než jeden týden, kromě případů, kdy Vám to Váš oční lékař doporučí.
U dlouhodobého používání může dojít ke zvýšení tlaku uvnitř Vašeho oka (nitrooční tlak), což může vést ke vzniku glaukomu (zelený zákal), vzácně může dlouhodobé používání vést k poškození zrakového nervu, rozmazanému vidění, kataraktě (šedý zákal), delšímu hojení ran nebo rozvoji oční infekce. Bude Vám pravidelně měřen Váš nitrooční tlak.
Jestliže Vám v minulosti byl(a) léčena infekce způsobená virem herpes simplex, Efflumidex Liquifilm používejte pouze pod pečlivým dozorem svého lékaře.
Jestliže je lahvička používána více než jednou osobou, může dojít k rozšíření infekce.
Děti
Bezpečnost a účinnost přípravku u dětí ve věku 2 roky a mladších nebyla dosud prokázána.
Další léčivé přípravky a Efflumidex Liquifilm
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Používáte-li ještě nějaké jiné oční kapky, musí být mezi jejich použitím časový odstup nejméně 5 minut.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek používat.
Váš lékař pak rozhodne, zda byste měla používat Efflumidex Liquifilm během těhotenství nebo kojení.
Řízení dopravních prostředků a obsluha strojů
Nakapání přípravku Efflumidex Liquifilm může způsobit rozmazané vidění.
Pokud tato situace nastane, počkejte s řízením nebo obsluhou strojů do doby, než se vidění upraví.
Efflumidex Liquifilm obsahuje benzalkonium-chlorid jako konzervační látku
Tato látka pak může způsobit zbarvení měkkých kontaktních čoček a též může vyvolat podráždění očí. Pokud nosíte kontaktní čočky, vyjměte je před použitím přípravku Efflumidex Liquifilm z oka a po nakapání počkejte nejméně 15 minut, než je nasadíte zpět.
3. JAK SE EFFLUMIDEX LIQUIFILM POUŽÍVÁ
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka.
Pokud si nejste jistý(á),poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka přípravku je jedna kapka přípravku Efflumidex Liquifilm do léčeného oka dvakrát až čtyřikrát denně nebo i častěji, pokud Vám to doporučí lékař. Během prvních 24-48 hodin Vám může lékař zvýšit dávkování na 2 kapky v hodinových intervalech.
Léčbu není vhodné ukončovat předčasně.
Pokyny pro použití:
Lahvičku nesmíte použít, pokud je před prvním otevřením folie originality porušena.
Před použitím dobře protřepejte. Umyjte si ruce předtím, než otevřete lahvičku.
Použijte oční kapky dle následujících instrukcí.
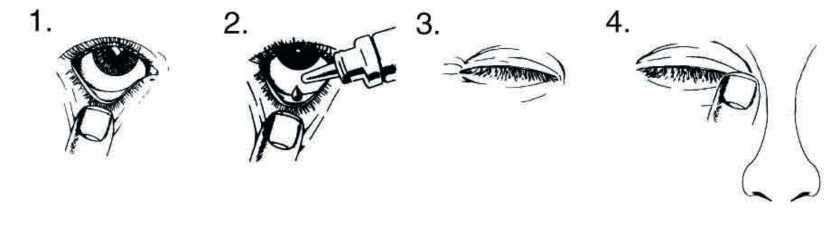
1. Zakloňte hlavu a dívejte se na strop. Jemně stáhněte dolní víčko dolů, aby se vytvořila malá kapsička.
2. Otočte lahvičku dnem vzhůru a zmáčkněte, aby se uvolnila 1-2 kapky do každého léčeného oka.
3. Uvolněte dolní víčko a zavřete oči.
4. Ponechte oko zavřené a stiskněte prstem vnitřní oční koutek proti nosu na dvě minuty. Toto opatření vede ke snížení rizika nežádoucích účinků a ke zvýšení místního účinku léčiva.
5. Opakujte kroky i u druhého oka, pokud také vyžaduje léčbu.
Jestliže kapka Vaše oko minula, opakujte postup znovu.
Abyste zabránili poranění oka a kontaminaci očních kapek, nedovolte, aby se hrot lahvičky dotkl při kapání Vašeho oka, ani ničeho jiného.
Ihned po použití zavřete lahvičku šroubovacím uzávěrem. Papírovým kapesníkem setřete přebytečnou tekutinu z Vaší tváře.
Jestliže jste použil(a) více přípravku Efflumidex Liquifilm, než jste měl(a)
Jestliže jste použil(a) více přípravku Efflumidex Liquifilm než jste měl(a), je nepravděpodobné, že si vážněji ublížíte. Pokud jste si kápl(a) do oka více kapek, než jste měl(a), vypláchněte si oko čistou vodou. Další dávku si vkápněte v obvyklém čase.
Jestliže jste omylem vypil(a) Efflumidex Liquifilm
Jestliže jste omylem vypil(a) Efflumidex Liquifilm, je nepravděpodobné, že si vážněji ublížíte. Postižená osoba má vypít větší množství tekutiny, tak aby došlo k rozředění.
Jestliže jste zapomněl(a) použít Efflumidex Liquifilm
Jestliže jste zapomněl(a) použít Efflumidex Liquifilm, vkápněte si přípravek hned, jakmile si vzpomenete, kromě případu, kdy je již téměř čas na Vaší další dávku. Dále se vraťte ke svému pravidelnému dávkování. Nepoužívejte dvojnásobnou dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste přestal(a) používat Efflumidex Liquifilm
Aby měl Efflumidex Liquifilm správný účinek, má být používán tak, jak je předepsán.
Máte-li jakékoli další otázky týkající se používání tohoto přípravku, přípravku, zeptejte se svého lékaře nebo lékárníka.
4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Jsou známy následující nežádoucí účinky, jejichž frekvence výskytu se může, jak se ukázalo, měnit. Pokud se u Vás vyskytnou poruchy polykání nebo obtížné dýchání, otok rtů, obličeje, krku nebo jazyka, okamžitě kontaktujte svého lékaře nebo jeďte přímo do nemocnice. Tyto příznaky mohou být projevem závažné alergické reakce. Frekvence výskytu alergické reakce není známá.
Účinky na oko
Časté (vyskytují se u méně než 1 pacienta z 10, ale více než u 1 pacienta ze 100)
Zvýšený nitrooční tlak
Frekvence výskytu není známá
Šedý zákal (ztráta průhlednosti oční čočky s částečnou nebo úplnou ztrátou zraku)
Podráždění oka
Zčervenání oka
Svědění oka
Bolest oka
Pocit cizího tělíska v oku Rozmazané vidění Otok víčka nebo oka Výtok z oka
Nadměrné rozšíření zornic
Nadměrná produkce slz Vřed(y) na povrchu oka
Povrchový zánět rohovky s malými tečkovými defekty ( tečkovitá keratitida)
Poruchy zorného pole Druhotné infekce Porucha vidění
Celkové účinky
Frekvence výskytu není známa:
Vyrážka, abnormální chutě, alergické reakce (hypersenzitivita)
Další nežádoucí účinky hlášené u očních kapek obsahujících fosfáty
U pacientů, kteří měli výrazně porušenou rohovku, byly v průběhu léčby velmi vzácně zaznamenány případy kalcifikace rohovky (ukládání vápenatých solí v rohovce projevující se vznikem zakalených skvrn).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek.
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. JAK EFFLUMIDEX LIQUIFILM UCHOVÁVAT
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na štítku lahvičky a na krabičce za „Použitelné do:“.
Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte při teplotě do 25 °C.
Nepoužívejte tento přípravek, pokud si všimnete, že uzávěr je poškozen. Pokud by se tak stalo, roztok může být kontaminován, což může způsobit oční infekci.
Po 4 týdnech od prvního otevření musíte toto balení léčivého přípravku přestat používat, a to i v případě, že v ní nějaké kapky ještě zůstaly. Pro lepší zapamatování si zapište datum otevření na volnou plochu na krabičce.
Aby nedošlo ke kontaminaci, uchovávejte lahvičku pevně uzavřenou.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo do domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. OBSAH BALENÍ A DALŠÍ INFORMACE Co Efflumidex Liquifilm obsahuje
Léčivou látkou je fluorometholonum. Jeden ml očních kapek, suspenze obsahuje fluorometholonum 1 mg.
Pomocnými látkami jsou polyvinylalkohol, benzalkonium-chlorid (konzervační přísada), dinatrium-edetát, chlorid sodný, heptahydrát hydrogenfosforečnanu sodného, monohydrát dihydrogenfosforečnanu sodného, polysorbát 80, roztok hydroxidu sodného 1 mol/l (pro úpravu pH) a čištěná voda.
Jak Efflumidex Liquifilm vypadá a co obsahuje toto balení
Efflumidex Liquifilm je bílá oční suspenze v kapací plastové lahvičce.
Jedna lahvička obsahuje 5 ml roztoku.
Držitel rozhodnutí o registraci a výrobce
Allergan Pharmaceuticals Ireland, Castlebar Road, Westport, Co Mayo, Irsko
Pro další informace o přípravku kontaktujte prosím Vašeho místního zástupce držitele rozhodnutí o registraci:
NEOMED,s.r.o.
Sodomkova 6 102 00 Praha10 Tel: 420 274 008 411 e-mail: info@neomed.cz
Tato příbalová informace byla naposledy revidována
13.5.2015
6/6