Antithrombin Iii Baxalta
sp.zn. sukls131966/2016 a sp.zn. sukls134244/2016
Příbalová informace: informace pro uživatele
ANTITHROMBIN III BAXALTA
Prášek a rozpouštědlo pro infuzní roztok Antithrombinum III
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože
obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné příznaky jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek ANTITHROMBIN III BAXALTA a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek ANTITHROMBIN III BAXALTA používat
3. Jak se přípravek ANTITHROMBIN III BAXALTA používá
4. Možné nežádoucí účinky
5. Jak přípravek ANTITHROMBIN III BAXALTA uchovávat
6. Obsah balení a další informace
1. Co je přípravek ANTITHROMBIN III BAXALTA a k čemu se používá
Přípravek ANTITHROMBIN III BAXALTA patří do farmakoterapeutické skupiny zvané antitrombotika.
Přípravek ANTITHROMBIN III BAXALTA se používá k léčbě vrozeného nebo získaného nedostatku
antithrombinu, který se může vyskytnout u velkého množství různých klinických poruch.
2. Čemu musíte věnovat pozornost, než začnete přípravek ANTITHROMBIN III BAXALTA používat
Nepoužívejte přípravek ANTITHROMBIN III BAXALTA
- jestliže j ste alergický(á) na antithrombin nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže máte v anamnéze heparinem vyvolanou trombocytopenii (tj. pokles krevních destiček).
Upozornění a opatření
Před užitím přípravku ANTITHROMBIN III BAXALTA se poraďte se svým lékařem nebo lékárníkem.
- Prosím sdělte ihned svému lékaři, jestliže zaznamenáte první známky alergické reakce (např. vyrážku, generalizovanou kopřivku, pocit svírání hrudníku, sípání, nízký krevní tlak, projevující se slabostí, pocitem na omdlení). Závažné příznaky mohou vyžadovat neodkladnou léčbu.
- Prosím informujte svého lékaře o všech lécích obsahujících heparin (např. pro léčbu trombózy), které užíváte nebo jste užíval(a) v nedávné době, protože účinek antithrombinu je heparinem značně zesílen.
- Přípravek ANTITHROMBIN III BAXALtA se vyrábí z lidské plazmy. Při podávání léčivých přípravků, připravených z lidské krve nebo plazmy, nelze zcela vyloučit riziko přenosu infekce. To se vztahuje i na patogeny dosud neznámé povahy. Riziko přenosu infekce je však sníženo pečlivým výběrem dárců a jednotlivých odběrů, testováním shromážděné plazmy a procesy inaktivace a odstranění virů.
Další léčivé přípravky a přípravek ANTITHROMBIN III BAXALTA
Prosím informujte svého lékaře o všech lécích obsahujících heparin (např. pro léčbu trombózy), které užíváte nebo jste užíval(a) v nedávné době, protože účinek antithrombinu se heparinem značně zesiluje.
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Přípravek ANTITHROMBIN III BAXALTA s jídlem a pitím
Přípravku se netýká.
Těhotenství a kojení
Prosím informujte svého lékaře, pokud jste těhotná nebo kojíte. Váš lékař rozhodne, zda lze přípravek ANTITHROMBIN III BAXALTA používat během těhotenství nebo kojení.
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
Nebyly pozorovány žádné účinky na schopnost řídit a obsluhovat stroje. Neobsluhujte žádné přístroje nebo stroje.
Přípravek ANTITHROMBIN III BAXALTA obsahuje sodík
Tento přípravek obsahuje přibližně 3,77 mg sodíku/ml. Tato informace může být důležitá u pacientů na dietě s kontrolovaným příjmem sodíku.
3. Jak se přípravek ANTITHROMBIN III BAXALTA používá
Přípravek ANTITHROMBIN III BAXALTA Vám bude podán pouze pod lékařským dohledem. Dávka bude záviset na Vaší tělesné hmotnosti a individuální potřebě. Váš lékař stanoví dávku, kterou byste měl(a) dostat. Přípravek ANTITHROMBIN III BAXALTA Vám bude podáván infuzí do některé žíly.
Použití u dětí
Není k dispozici dostatek údajů k tomu, aby mohlo být doporučeno podávání přípravku ANTITHROMBIN III BAXALTA dětem do 6 let.
Jestliže jste použil(a) více přípravku ANTITHROMBIN III BAXALTA, než jste měl(a)
Příznaky předávkování antithrombinem nebyly zaznamenány.
Jestliže jste zapomněl(a) použít přípravek ANTITHROMBIN III BAXALTA
Přípravku se netýká.
Jestliže jste přestal(a) používat přípravek ANTITHROMBIN III BAXALTA
Přípravku se netýká.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
- Hypersenzitivita nebo alergické reakce (k nimž může patřit angioedém, pálení a píchání v místě infuze, zimnice, zčervenání, generalizovaná kopřivka, bolest hlavy, vyrážka, nízký krevní tlak, otupělost, nevolnost, neklid, zvýšená srdeční frekvence, pocit svírání hrudníku, brnění, zvracení, sípání) byly pozorovány vzácně a mohou v některých případech přejít až do závažné anafylaxe (včetně šoku).
- Ve vzácných případech se objevila horečka.
- Ve vzácných případech by se mohla objevit heparinem vyvolaná a protilátkami zprostředkovaná trombocytopenie (snížení počtu krevních destiček). Může být zaznamenán počet destiček nižší než 100 000/pl nebo pokles počtu destiček o 50 %.
Po uvedení přípravku ANTITHROMBIN III BAXALTA na trh byly zaznamenány následující nežádoucí účinky: třes a návaly horka.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, nebo pokud si všimnete jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, prosím, sdělte to svému lékaři nebo lékárníkovi.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv,
Šrobárova 48, 100 41 Praha 10, webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek ANTITHROMBIN III BAXALTA uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte v chladničce (2°C - 8°C). Chraňte před mrazem. Chraňte před světlem a uchovávejte v původním obalu.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na štítku a krabičce.
Nepoužívejte tento přípravek, pokud si všimnete, že jsou roztoky zakalené nebo obsahují usazeniny.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek ANTITHROMBIN III BAXALTA obsahuje
- Léčivou látkou je antithrombinum III z lidské plazmy.
1 ml rozpuštěného přípravku obsahuje antithrombinum III 50 IU, což odpovídá proteinum 20 - 50 mg
- Pomocnými látkami jsou glukóza, chlorid sodný, dihydrát natrium-citrátu, trometamol a voda na injekci
Jak přípravek ANTITHROMBIN III BAXALTA vypadá a co obsahuje toto balení
Přípravek ANTITHROMBIN III BAXALTA je dodáván jako prášek a rozpouštědlo pro infuzní roztok, obsahující nominálně 500 IU (1000 IU) antithrombinum III z lidské plazmy v jedné injekční lahvičce.
Po rekonstituci v 10 (20 ml) vody na injekci obsahuje 1 ml přibližně antithrombinum III z lidské plazmy 50 IU (500 IU/10 ml, 1000 IU/20 ml).
Přípravek ANTITHROMBIN III BAXALTA je bílý nebo nažloutlý prášek nebo pevná drobivá látka.
Každé balení také obsahuje:
- 1 převodní jehlu
- 1 filtrační jehlu
- 1 zavzdušňovací jehlu
- 1 jehlu k jednorázovému použití
- 1 infuzní set
Velikost balení:
1x 500 IU + 10 ml rozpouštědla 1x 1000 IU + 20 ml rozpouštědla
Držitel rozhodnutí o registraci a výrobce Držitel rozhodnutí o registraci:
Do 30.11.2016
Baxter AG Industriestrasse 67 A-1221 Vídeň Rakousko
Od 1.12.2016
Baxalta Innovations GmbH Industriestrasse 67 A-1221 Vídeň Rakousko
Výrobce:
Baxter AG Industriestrasse 67 A-1221 Vídeň Rakousko
Tato příbalová informace byla naposledy revidována 10.8.2016.
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Dávkování a způsob podání
Léčba by měla být zahájena pod dohledem lékaře se zkušenostmi s léčbou pacientů s nedostatkem antithrombinu.
Dávkování
Při vrozeném nedostatku by mělo být dávkování přizpůsobeno potřebám každého pacienta a měla by se zvážit rodinná anamnéza s ohledem na tromboembolické příhody, aktuální klinické rizikové faktory a výsledky laboratorních vyšetření.
Dávkování a délka trvání substituční terapie u získaného nedostatku závisí na plazmatické hladině antithrombinu, přítomnosti známek zvýšeného obratu, základním onemocnění a závažnosti klinického stavu. Množství, jež má být podáno, a frekvence podání by měly být vždy založeny na klinické účinnosti a laboratorním hodnocení v jednotlivém případě.
Počet podaných jednotek antithrombinum III se vyjadřuje v mezinárodních jednotkách (IU), jež se vztahují k současnému standardu WHO pro antithrombinum III. Aktivita antithrombinum III v plazmě se vyjadřuje buď v procentech (vzhledem k normální lidské plazmě) nebo v mezinárodních jednotkách (vzhledem k mezinárodnímu standardu pro antithrombinum III v plazmě).
Jedna mezinárodní jednotka (IU) aktivity antithrombinum III je ekvivalentní množství antithrombinum III v jednom mililitru normální lidské plazmy. Výpočet požadované dávky antithrombinum III je založen na empirickém zjištění, že 1 mezinárodní jednotka (IU) antithrombinum III na kilogram tělesné hmotnosti zvyšuje aktivitu antithrombinu v plazmě zhruba o 2 %.
Úvodní dávka se stanoví pomocí následujícího vzorce:
Požadovaný počet jednotek = tělesná hmotnost (kg) x (cílová hladina - skutečná aktivita antithrombinu [%]) x 0,5
Úvodní cílová aktivita antithrombinum III závisí na klinickém stavu. Je-li stanovena indikace pro substituci antithrombinum III, mělo by být dávkování dostatečné, aby byla dosažena cílová aktivita antithrombinum III a aby byla udržena účinná hladina. Dávkování by mělo být stanoveno a monitorováno na základě laboratorních testů aktivity antithrombinum III, které by měly být prováděny do stabilizace pacienta minimálně dvakrát denně, poté jednou denně, nejlépe bezprostředně před následující infuzí. Úprava dávkování by měla zohlednit jak známky zvýšeného obratu antithrombinum III podle laboratorních hodnot, tak i klinický průběh. Aktivita antithrombinum III by měla být po dobu trvání léčby udržována nad 80 %, pokud by klinické údaje nesvědčily pro jinou účinnou hladinu.
Obvyklá počáteční dávka při vrozeném nedostatku bývá 30-50 IU/kg.
Poté by měly být dávkování a frekvence i doba trvání léčby upraveny podle biologických údajů a klinické situace.
Pediatrická populace
Není k dispozici dostatek údajů k tomu, aby mohlo být doporučeno podávání přípravku ANTITHROMBIN III BAXALTA dětem do 6 let.
Způsob podání
Přípravek by měl být podáván intravenózně.
Maximální rychlost podání je 5 ml/min.
Návod k použití
Přípravek ANTITHROMBIN III BAXALTA má být rekonstituován bezprostředně před použitím a podáván pouze pomocí přiloženého infuzního setu. Během celého procesu rekonstituce je třeba používat aseptickou techniku. Roztok má být ihned použit (přípravek neobsahuje konzervační látky).
Rekonstituovaný přípravek má být před podáním vizuálně zkontrolován s ohledem na přítomnost částic či změnu zabarvení. Roztok je čirý nebo lehce opalescentní. Zakalené roztoky nebo roztoky obsahující usazeniny nepoužívejte.
Veškerý nepoužitý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky. Rekonstituce prášku:
1. Zahřejte neotevřenou injekční lahvičku s rozpouštědlem (voda na injekci) na pokojovou teplotu (max. 37oC).
2. Odstraňte ochranná víčka z lahviček s práškem a rozpouštědlem (obr. A) a dezinfikujte pryžové zátky obou injekčních lahviček.
3. Sejměte ochranný kryt z jednoho konce přiložené převodní jehly pootočením a povytažením (obr. B). Zapíchněte tento konec jehly skrze pryžovou zátku do injekční lahvičky s rozpouštědlem (obr. C).
4. Sejměte ochranný kryt z druhého konce převodní jehly tak, abyste se přitom nedotkli odkrytého konce.
5. Obraťte injekční lahvičku s rozpouštědlem nad injekční lahvičku s práškem a propíchněte převodní jehlou pryžovou zátku injekční lahvičky s práškem (obr. D). Rozpouštědlo přejde pomocí vakua do injekční lahvičky s koncentrátem.
6. Oddělte obě injekční lahvičky vyjmutím jehly z injekční lahvičky s práškem (obr. E). Lehce protřepejte nebo promíchejte, abyste urychlili rozpouštění.
7. Po úplném rozpuštění prášku vpíchněte do injekční lahvičky přiloženou zavzdušňovací jehlu (obr. F), čímž odstraníte případně vzniklou pěnu. Zavzdušňovací jehlu vyjměte.
Podání:
8. Pootočením a povytažením sejměte ochranný kryt z přiložené filtrační jehly a nasaďte ji na sterilní jednorázovou stříkačku. Natáhněte roztok do stříkačky (obr. G).
9. Odpojte filtrační jehlu od stříkačky a roztok aplikujte pomalu intravenózně (max. rychlost 5 ml/min) pomocí přiložené jehly k jednorázovému použití (nebo pomocí přiloženého infuzního setu).
Stránka 5 z 6
Pokud se neprovádí filtrace během rekonstituce, je třeba použít infuzní set s odpovídajícím filtrem (max. rychlost infuze 5 ml/min).
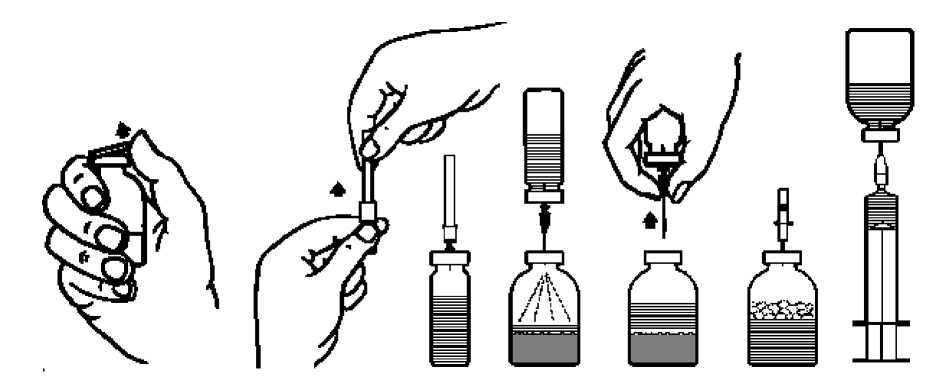
obr. A obr. B
obr. C obr. D obr. E
obr. F obr. G
Inkompatibility
Tento léčivý přípravek nesmí být mísen s jinými léčivými přípravky.
Vzhledem k tomu, že může dojít k selhání léčby v důsledku adsorpce lidského antithrombinu na vnitřní povrchy aplikačního zařízení, smí být použito pouze přiložené příslušenství pro rekonstituci a aplikaci.
Zvláštní upozornění a opatření pro použití
Stejně jako u jiných intravenózních proteinových přípravků jsou možné hypersenzitivní alergické reakce. Pacienti musí být po celou dobu infuze pečlivě monitorováni a všechny příznaky se musí pečlivě sledovat. Pacienti by měli být seznámeni s prvními známkami hypersenzitivních reakcí, k nimž patří vyrážka, generalizovaná kopřivka, tíže na hrudi, sípání, hypotenze a anafylaxe. Objeví-li se po podání tyto symptomy, měli by kontaktovat svého lékaře.
V případě šoku je třeba zahájit standardní léčbu.
Stránka 6 z 6