Yasminelle 0,02 Mg/3 Mg Potahované Tablety
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU
Průhledná folie (celofán) s nálepkou_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Viz vnitřní obal.
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK_
Viz vnitřní obal.
3. SEZNAM POMOCNÝCH LÁTEK_
Viz vnitřní obal.
4. LÉKOVÁ FORMA A OBSAH BALENÍ_
21 potahovaných tablet 3 x 21 potahovaných tablet 6 x 21 potahovaných tablet 13 x 21 potahovaných tablet
5. ZPŮSOB A CESTA/CESTY PODÁNÍ_
Viz vnitřní obal.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO
DOHLED A DOSAH DĚTÍ_
Viz vnitřní obal.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ_
Viz vnitřní obal.
8. POUŽITELNOST_
Viz vnitřní obal.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ_
Viz vnitřní obal.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Viz vnitřní obal.
Viz vnitřní obal.
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
Viz vnitřní obal.
13. ČÍSLO ŠARŽE
Viz vnitřní obal.
14. KLASIFIKACE PRO VÝDEJ
Viz vnitřní obal.
15. NÁVOD K POUŽITÍ
Viz vnitřní obal.
16. INFORMACE V BRAILLOVĚ PÍSMU
Viz vnitřní obal.
Na vnějším obale je na nálepce kromě velikosti balení i EAN kód.
Yasminelle 0,02 mg /3 mg potahované tablety Ethinylestradiolum/drospirenonum
Jedna potahovaná tableta obsahuje:
Ethinylestradiolum (jako betadexum clathratum) 0,020 mg Drospirenonum 3 mg
Tento přípravek obsahuje monohydrát laktosy. Prosíme, přečtěte si příbalovou informaci pro podrobnosti.
21 potahovaných tablet
Perorální podání.
Před použitím si přečtěte příbalovou informaci.
Uchovávejte mimo dohled a dosah dětí.
Použitelné do:
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
Nepoužitelné léčivo vraťte do lékárny.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Bayer Pharma AG D-13342 Berlín Německo
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
17/192/06-C
13. ČÍSLO ŠARŽE
č.š.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
yasminelle
Další informace uvedené na pouzdru
Přečtěte si příbalovou informaci Yasminelle dříve, než začnete tablety užívat. Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
Jak se Yasminelle užívá?
Užívejte jednu tabletu Yasminelle každý den, podle potřeby s malým množstvím vody. Je důležité, abyste užívala tablety každý den přibližně ve stejnou dobu.
Kdy se může stát, že nebudete dále chráněna před otěhotněním?
> Pokud se opozdíte v užití tablety o více než 12 hodin, nebo pokud jste zapomněla užít více tablet Yasminelle
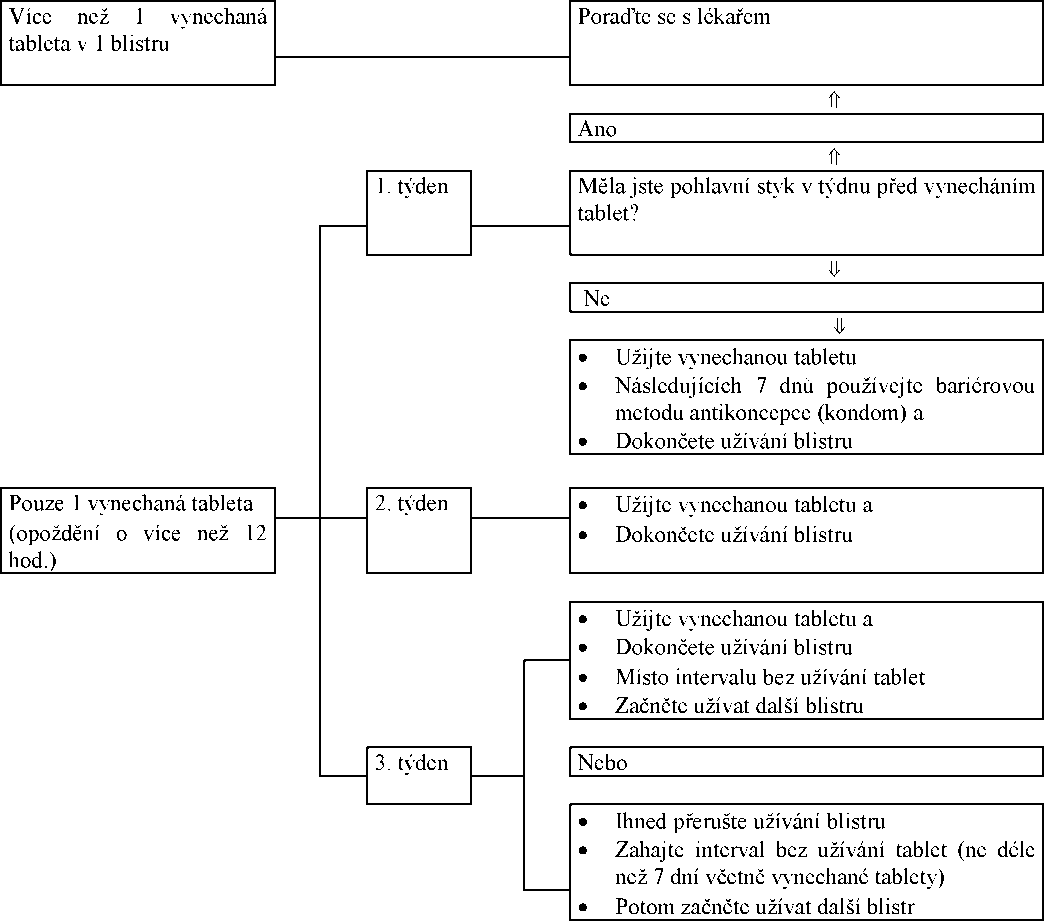
^ Prosíme, prohlédněte si níže uvedený diagram a přečtěte si v příbalové informaci bod „Jestliže jste zapomněla Yasminelle užít“.
> Jestliže jste zvracela nebo máte (měla jste) těžší průjem
^ Prosíme, přečtěte si v příbalové informaci bod „Co dělat v případě zvracení nebo těžšího průjmu:“.
> Jestliže Yasminelle užíváte spolu s jinými léky
^ Prosíme, přečtěte si v příbalové informaci bod „Další léčivé přípravky a přípravek Yasminelle”
Abyste byla chráněna před otěhotněním v případě, že jste zapomněla užít tablety, musíte se řídit pokyny v níže uvedeném diagramu. Prosíme, přečtěte si příbalovou informaci, kde najdete podrobnosti.
Názvy dnů v týdnu
Pondělí
Úterý
Středa
Čtvrtek
Pátek
Sobota
Neděle
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH
VZHLEDEM K TOMU, ŽE KARTONOVÉ POUZDRO PŘEDSTAVUJE VNITŘNÍ OBAL, JE TATO ČÁST UVÁDĚNA JEN PRO INFORMACI.
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
lot
5. JINÉ
7