Vizarsin 100 Mg
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Vizarsin 25 mg potahované tablety Vizarsin 50 mg potahované tablety Vizarsin 100 mg potahované tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 25 mg, 50 mg nebo 100 mg.
Pomocná látka se známým účinkem:
Vizarsin 25 mg potahované tablety
Jedna potahovaná tableta obsahuje 1,9 mg laktosy (ve formě monohydrátu).
Vizarsin 50 mg potahované tablety
Jedna potahovaná tableta obsahuje 3,8 mg laktosy (ve formě monohydrátu).
Vizarsin 100 mg potahované tablety
Jedna potahovaná tableta obsahuje 7,6 mg laktosy (ve formě monohydrátu).
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Potahovaná tableta.
Vizarsin 25 mg potahované tablety: Bílé, podlouhlé tablety, s označením „25“ na jedné straně. Vizarsin 50 mg potahované tablety: Bílé, podlouhlé tablety, s označením „50“ na jedné straně. Vizarsin 100 mg potahované tablety: Bílé, podlouhlé tablety, s označením „100“ na jedné straně.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek Vizarsin je indikován k léčbě erektilní dysfunkce u dospělých mužů, pod kterou rozumíme neschopnost dosáhnout nebo udržet erekci dostatečnou k umožnění pohlavního styku.
Pro dosažení účinku přípravku Vizarsin je nezbytné sexuální dráždění.
4.2 Dávkování a způsob podání
Dávkování
Použití u dospělých:
Doporučená dávka je 50 mg, kterou je třeba užít podle potřeby přibližně jednu hodinu před sexuální aktivitou. Podle účinnosti a snášenlivosti lze dávku zvýšit na 100 mg nebo snížit na 25 mg. Maximální doporučená dávka je 100 mg. Maximální doporučená četnost užití dávky je jedenkrát denně. Pokud je přípravek Vizarsin užit současně s jídlem, může dojít ke zpoždění nástupu účinku ve srovnání se stavem na lačno (viz bod 5.2).
Zvláštní populace
Starší pacienti:
U starších pacientů (> 65 let) není nutná úprava dávek.
Poškození ledvin:
Dávkování popsané v odstavci „Použití u dospělých“ se vztahuje na nemocné s mírnou nebo středně těžkou poruchou ledvin (clearance kreatininu = 30-80 ml/min).
Protože clearance sildenafilu je u nemocných se závažnou poruchou ledvin (clearance kreatininu < 30 ml/min) snížena, doporučuje se zahájit léčbu dávkou 25 mg. Podle účinnosti a snášenlivosti lze dle potřeby dávku postupně zvýšit na 50 mg až 100 mg.
Poškození jater:
Protože clearance sildenafilu je u nemocných s poruchou jater (např. cirhóza) snížena, doporučuje se zahájit léčbu dávkou 25 mg. Podle účinnosti a snášenlivosti lze dle potřeby dávku postupně zvýšit na 50 mg až 100 mg.
Pediatrická populace
Přípravek Vizarsin není určen pro děti a dospívající do 18 let.
Použití u nemocných používajících jiné léčivé přípravky:
S výjimkou ritonaviru, jehož současné užití se sildenafilem není doporučeno (viz bod 4.4), měla by být u nemocných, kteří současně užívají přípravky inhibující CYP3A4, jako počáteční dávka užita dávka 25 mg (viz bod 4.5).
Předtím, než je zahájena léčba sildenafilem, by měli být pacienti léčení alfa-blokátory stabilizováni na této léčbě z důvodu minimalizace možného vzniku posturální hypotenze. Kromě toho je třeba zvážit zahájení léčby sildenafilem dávkou 25 mg (viz body 4.4 a 4.5).
Způsob podání
Perorální podání.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Ve shodě se známými účinky na metabolismus oxidu dusnatého/cyklického guanosin monofosfátu (cGMP) (viz bod 5.1) se ukázalo, že sildenafil je schopen potencovat hypotenzní účinky nitrátů. Jeho současné užití s látkami schopnými uvolňovat oxid dusnatý (jako je amylnitrit) nebo nitráty v jakékoli formě je proto kontraindikováno.
Současné podávání PDE5 inhibitorů, včetně sildenafilu, se stimulátory guanylátcyklázy, jako je riocigvát, je kontraindikováno, protože může potenciálně vést k symptomatické hypotenzi (viz bod 4.5).
Přípravky k léčbě erektilní dysfunkce, mezi které patří sildenafil, by neměly být užívány muži, pro které není sexuální aktivita vhodná (např. nemocní se závažnými kardiovaskulárními poruchami, jako je nestabilní angina pectoris nebo závažné srdeční selhání).
Přípravek Vizarsin je kontraindikován u pacientů, kteří ztratili zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION), bez ohledu na to, zda tato příhoda souvisela s předchozím užitím inhibitoru fosfodiesterázy 5 (PDE5) či nikoli (viz bod 4.4).
Bezpečnost sildenafilu nebyla studována u následujících podskupin nemocných, a proto jeho použití je u nich kontraindikováno do doby, než budou k dispozici další informace: závažná jaterní porucha, hypotenze (TK< 90/50 mm Hg), cévní mozková příhoda nebo infarkt myokardu v nedávné anamnéze a také známé hereditární degenerativní postižení sítnice, jako je např. retinitispigmentosa (malá část těchto nemocných má genetické postižení retinální fosfodiesterázy).
4.4 Zvláštní upozornění a opatření pro použití
Aby bylo možno určit diagnózu erektilní dysfunkce a stanovit možné příčiny, je třeba u nemocného zjistit anamnézu a provést fyzikální vyšetření dříve, než je rozhodnuto o farmakologické léčbě.
Kardiovaskulární rizikové faktory
Před zahájením jakékoli léčby erektilní dysfunkce by měl lékař posoudit kardiovaskulární funkce pacienta, protože sexuální aktivita s sebou nese jisté riziko srdečních příhod. Sildenafil má vazodilatační vlastnosti, jejichž výsledkem je malé a přechodné snížení tlaku krve (viz bod 5.1).
Před předepsáním sildenafilu by měli lékaři pečlivě zvážit, zda některé základní onemocnění u jejich pacientů nemůže být negativně ovlivněno těmito vasodilatačními účinky, a to zejména v kombinaci se sexuální aktivitou. Mezi pacienty se zvýšenou citlivostí na vasodilatancia patří nemocní s obstrukcí odtoku krve z levé komory (např. aortální stenóza, hypertrofická obstrukční kardiomyopatie) nebo pacienti se vzácným syndromem mnohočetné systémové atrofie manifestující se jako závažné zhoršení autonomní regulace krevního tlaku.
Sildenafil zvyšuje hypotenzivní účinek nitrátů (viz bod 4.3).
V období po uvedení přípravku na trh byly hlášeny případy závažných kardiovaskulárních příhod včetně infarktu myokardu, nestabilní anginy pectoris, náhlé srdeční smrti, komorové arytmie, mozkové hemorhagie, přechodných ischemických atak, hypertenze a hypotenze v časové souvislosti
s užitím sildenafilu. Většina z těchto pacientů, ale ne všichni, měla již dříve existující kardiovaskulární rizikové faktory. Rada hlášených příhod vznikla během nebo krátce po pohlavním styku a několik hlášených příhod vzniklo krátce po užití sildenafilu bez souvislosti se sexuální aktivitou. Není možné určit, zda tyto příhody lze přímo vztáhnout k těmto faktorům nebo jiným faktorům.
Priapismus
Přípravky k léčbě erektilní dysfunkce, včetně sildenafilu, je třeba používat opatrně u pacientů s anatomickou deformací penisu (jako je angulace, kavernózní fibróza nebo Peyroneova choroba) nebo u pacientů s onemocněními, která je predisponují k priapismu (jako je srpkovitá anémie, vícečetný myelom nebo leukémie).
Při použití sildenafilu po uvedení přípravku na trh byla hlášena protrahovaná erekce a priapismus.
V případě erekce, která přetrvává déle než 4 hodiny, by měl pacient vyhledat okamžitou lékařskou pomoc. Pokud není priapismus okamžitě léčen, mohl by vést k poškození tkáně penisu a trvalé ztrátě potence.
Současné použití s jinými inhibitory PDE5 či jinými typy léčby erektilní dysfunkce
Bezpečnost a účinnost kombinace sildenafilu s jinými inhibitory PDE5 nebo s jinými léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil či s jinými léčbami erektilní dysfunkce nebyla zjišťována. Proto se případné použití těchto kombinací nedoporučuje.
Účinky na. zrak
V souvislosti s užitím sildenafilu i jiných inhibitorů PDE5 byly spontánně hlášeny případy poruchy zraku (viz bod 4.8). V souvislosti s užitím sildenafilu i jiných inhibitorů PDE5 byly spontánně i z observační studie hlášeny případy vzácného onemocnění nearteritické přední ischemické neuropatie optického nervu (NAION) (viz bod 4.8). Je nutné pacienty poučit, aby v případě náhlé poruchy zraku přestali přípravek Vizarsin užívat a okamžitě vyhledali svého lékaře (viz bod 4.3).
Současné užívání s ritonavirem
Současné užívání sildenafilu s ritonavirem není doporučeno (viz bod 4.5).
Současné užívání s alfa-blokátorv
Při podání sildenafilu pacientům užívajícím alfa-blokátory je třeba opatrnosti, protože souběžné podání může vést u citlivých jedinců k symptomatické hypotenzi (viz bod 4.5). Ta se může nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Předtím, než je zahájena léčba sildenafilem, by měli být pacienti hemodynamicky stabilizováni na léčbě alfa-blokátory z důvodu minimalizace možného vzniku posturální hypotenze. Je třeba zvážit zahájení léčby sildenafilem dávkou 25 mg (viz bod 4.2). Pacienty je třeba poučit o tom, jak jednat, objeví-li se příznaky posturální hypotenze.
Účinek na krvácivost
Studie s lidskými trombocyty ukázaly, že sildenafil potencuje antiagregační účinek dihydrát nitroprusidu sodného in vitro. K dispozici nejsou žádné informace o bezpečnosti podání sildenafilu pacientům s poruchami srážlivosti krve nebo aktivní vředovou chorobou. Proto je podávání sildenafilu těmto pacientům nutné pečlivě uvážit.
Ženy
Přípravek Vizarsin není indikován k použití u žen. Pomocné látky
Přípravek Vizarsin obsahuje laktosu. Pacienti se vzácným dědičným onemocněním intolerance galaktosy, vrozeným deficitem laktázy nebo malabsorpcí glukosy-galaktosy by neměli tento lék užívat.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Účinky jiných léků na sildenafil In vitro studie:
Metabolizmus sildenafilu je zprostředkován hlavně izoformou 3A4 (hlavní cesta) a izoformou 2C9 (vedlejší cesta) cytochromu P450 (CYP). Proto mohou inhibitory těchto izoenzymů snížit clearance sildenafilu a induktory těchto izoenzymů mohou zvýšit clearance sildenafilu.
In vivo studie:
Populační farmakokinetická analýza klinických studií zjistila snížení clearance sildenafilu při současném podání s inhibitory CYP3A4 (jako jsou ketokonazol, erythromycin, cimetidin). Ačkoli nebylo pozorováno zvýšení incidence nežádoucích účinků u těchto pacientů, při souběžném užití sildenafilu s inhibitory CYP3A4 by měla být jako úvodní podána dávka 25 mg.
Při současném podávání inhibitoru HIV proteázy ritonaviru (500 mg 2x denně), což je vysoce účinný inhibitor P450, se sildenafilem (jednorázová dávka 100 mg), došlo v ustáleném stavu k 300% (4násobnému) zvýšení Cmax sildenafilu a 1000% (11násobnému) zvýšení AUC sildenafilu v plazmě. Po 24 hodinách byly plazmatické hladiny sildenafilu ještě přibližně 200 ng/ml, narozdíl od hladiny 5 ng/ml, která je obvyklá, pokud je sildenafil podáván samostatně. Tento nález je ve shodě s význačným účinkem ritonaviru na řadu P450 substrátů. Sildenafil nemá žádný vliv na farmakokinetiku ritonaviru. Na základě těchto farmakokinetických nálezů současné podávání sildenafilu s ritonavirem není doporučeno (viz bod 4.4) a za žádných okolností nesmí nejvyšší dávka sildenafilu v průběhu 48 hodin přesáhnout 25 mg.
Při současném podávání inhibitoru HIV proteázy sachinaviru (1200 mg 3x denně), který je inhibitorem CYP3A4, se sildenafilem (jednorázová dávka 100 mg), došlo ke 140% zvýšení Cmax sildenafilu a 210% zvýšení AUC sildenafilu v plazmě. Sildenafil nemá žádný vliv na farmakokinetiku sachinaviru (viz bod 4.2). Lze očekávat, že účinnější inhibitory CYP3A4, jako je ketokonazol nebo itrakonazol, budou mít výraznější účinky.
Při současném podání jednotlivé dávky 100 mg sildenafilu se středně silným inhibitorem CYP3A4 erythromycinem došlo v ustáleném stavu (500 mg erythromycinu 2x denně po dobu 5 dní) ke zvýšení systémové expozice sildenafilu o 182 % (AUC). U normálních zdravých dobrovolníků mužů nebyl prokázán účinek azithromycinu (v dávce 500 mg denně po dobu 3 dnů) na AUC, Cmax, tmax, konstantu rychlosti vylučování nebo následný poločas sildenafilu či jeho hlavního cirkulujícího metabolitu. Současné podávání cimetidinu (800 mg), což je inhibitor cytochromu P450 a nespecifický inhibitor CYP3A4, a sildenafilu (50 mg) zdravým dobrovolníkům vedlo k 56% zvýšení plazmatických hladin sildenafilu.
Grapefruitový džus, který je slabým inhibitorem metabolizmu CYP3A4 ve střevní stěně, může způsobit mírné zvýšení plazmatických hladin sildenafilu.
Jednorázové dávky antacida (hydroxid hořečnatý/ hydroxid hlinitý) neměly na biologickou dostupnost sildenafilu vliv.
Ačkoli nebyly provedeny specifické interakční studie pro všechny léčivé přípravky, populační farmakokinetická analýza neprokázala žádný účinek souběžné léčby na farmakokinetiku sildenafilu, pokud se uvažovaly skupiny léků jako inhibitory CYP2C9 (např. tolbutamid, warfarin, fenytoin), inhibitory CYP2D6 (např. selektivní inhibitory zpětného vychytávání serotoninu, tricyklická antidepresiva), thiazid a příbuzná diuretika, kličková a draslík šetřící diuretika, ACE inhibitory, blokátory kalciových kanálů, antagonisté beta-adrenoreceptorů nebo induktory metabolismu CYP450 (jako např. rifampicin, barbituráty). Ve studii se zdravými mužskými dobrovolníky vedlo souběžné podání endotelinového antagonisty bosentanu (induktor CYP3A4 [středně silný], CYP2C9 a zřejmě i CYP2C19) v ustáleném stavu (125 mg 2x denně) se sildenafilem v ustáleném stavu (80 mg 3x denně) k 62,6% snížení AUC a 55,4% snížení Cmax sildenafilu. Proto lze při souběžném podání se silnými induktory CYP3A4 jako je rifampicin, očekávat větší snížení plazmatických koncentrací sildenafilu.
Nikorandil je sloučeninou složenou z aktivátoru draslíkového kanálu a nitrátu. Z důvodu přítomnosti nitrátové složky existuje potenciál k závažným interakcím mezi sildenafilem a nikorandilem.
Účinky sildenafilu na jiné léky
In vitro studie:
Sildenafil je slabý inhibitor isoforem 1A2, 2C9, 2C19, 2D6, 2E1 a 3A4 cytochromu P450
(IC50 >150 ^M). Za předpokladu maximálních plazmatických koncentrací cca 1 ^M po doporučených
dávkách není pravděpodobné, že by sildenafil změnil clearance substrátů těchto isoenzymů.
Nejsou žádné údaje o interakci mezi sildenafilem a nespecifickými inhibitory fosfodiesterázy, jako je např. teofylin nebo dipyridamol.
In vivo studie:
Ve shodě se známými účinky na metabolismus oxidu dusnatého/cGMP (viz bod 5.1), se ukázalo, že sildenafil je schopen potencovat hypotenzní účinky nitrátů. Jeho současné užití s látkami schopnými uvolňovat oxid dusnatý nebo s nitráty v jakékoli formě je proto kontraindikováno (viz bod 4.3).
Riocigvát: Předklinické studie ukázaly aditivní systémový účinek při snižování krevního tlaku, když byly inhibitory PDE5 kombinovány s riocigvátem. V klinických studiích bylo prokázáno, že riocigvát zesiluje hypotenzní účinek inhibitorů PDE5. U sledované populace nebyl prokázán příznivý klinický účinek kombinace. Současné užívání riocigvátu s PDE5 inhibitory, včetně sildenafilu, je kontraindikováno (viz bod 4.3).
Při souběžném podání sildenafilu pacientům užívajícím alfa-blokátory je třeba opatrnosti, protože souběžné podání může vést u citlivých jedinců k symptomatické hypotenzi. Ta se může nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu (viz body 4.2 a 4.4). Ve třech specifických studiích lékových interakcí byl pacientům s benigní hyperplazií prostaty (BPH), kteří byli stabilizováni na léčbě doxazosinem, současně podáván alfa-blokátor doxazosin (4 mg a 8 mg) a sildenafil (25 mg, 50 mg a 100 mg).
Během studie bylo u této populace pozorováno průměrné dodatečné snížení krevního tlaku vleže o 7/7 mm Hg, 9/5 mm Hg resp. o 8/4 mm Hg a průměrné dodatečné snížení krevního tlaku ve stoje o 6/6 mm Hg, 11/4 mm Hg resp. o 4/5 mm Hg. Při současném podání sildenafilu a doxazosinu pacientům, stabilizovaným na léčbě doxazosinem, se vzácně objevila hlášení o pacientech, kteří prodělali symptomatickou posturální hypotenzi. Tato hlášení zahrnovala závratě a mdloby, nikoliv však synkopu.
Nebyly prokázány žádné podstatné interakce při současném podání sildenafilu (50 mg) s tolbutamidem (250 mg) nebo s warfarinem (40 mg), které jsou metabolizovány CYP2C9.
Sildenafil (50 mg) nepotencoval prodloužení času krvácivosti způsobené kyselinou acetylsalicylovou (150 mg).
U zdravých dobrovolníků nepotencoval sildenafil (50 mg) hypotenzní účinky alkoholu, pokud průměrné maximální hladiny alkoholu v krvi dosáhly hodnot 80 mg/dl.
Při rozboru následujících skupin antihypertenziv: diuretika, P-blokátory a ACE inhibitory, blokátory receptorů pro angiotensin II, antihypertenzní přípravky (vazodilatačně a centrálně účinkující), blokátory adrenergních neuronů, blokátory kalciových kanálů a a-blokátory, se neprokázal žádný rozdíl v profilu nežádoucích účinků u nemocných užívajících sildenafil ve srovnání s nemocnými užívajícími placebo. Ve specifické interakční studii, ve které byl sildenafil (100 mg) současně podáván s amlodipinem nemocným s hypertenzí, došlo k přídatnému snížení systolického krevního tlaku vleže o 8 mm Hg. Odpovídající přídatné snížení diastolického krevního tlaku vleže bylo 7 mm Hg. Tyto hodnoty přídatného snížení krevního tlaku měly stejný rozsah jako hodnoty, které byly pozorovány, pokud byl sildenafil podáván zdravým dobrovolníkům samostatně (viz bod 5.1).
Sildenafil (100 mg) neovlivňoval farmakokinetiku v ustáleném stavu inhibitorů HIV proteázy sachinaviru a ritonaviru, což jsou oba substráty CYP3A4.
U zdravých mužských dobrovolníků mělo souběžné podání sildenafilu v ustáleném stavu (80 mg 3x denně) a bosentanu (125 mg 2x denně) za následek 49,8% nárůst AUC bosentanu a 42% nárůst Cmax bosentanu.
4.6 Fertilita, těhotenství a kojení
Přípravek Vizarsin není indikován k použití u žen.
Neexistují žádné adekvátní a dobře kontrolované studie u těhotných nebo kojících žen.
V reprodukčních studiích u potkanů a králíků nebyly po perorálním podání sildenafilu zjištěny žádné významné nežádoucí účinky.
Neprojevil se žádný účinek na motilitu nebo morfologii spermií po jednorázových perorálních dávkách 100 mg sildenafilu u zdravých dobrovolníků (viz bod 5.1).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly prováděny žádné studie zjišťující schopnost řídit a obsluhovat stroje.
Závratě a poruchy vidění byly hlášeny jako nežádoucí účinky v klinických studiích se sildenafilem. Nemocní by proto měli znát svoji reakci na přípravek Vizarsin dříve, než budou řídit motorová vozidla nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Bezpečnostní profil sildenafilu byl vytvořen na základě zkušeností 9 570 pacientů v 74 dvojitě zaslepených klinických studiích kontrolovaných placebem. Nejčastěji hlášenými nežádoucími účinky u pacientů užívajících sildenafil v klinických studiích byly bolest hlavy, návaly, dyspepsie, zduření nosní sliznice, závratě, nevolnost, nával horka, poruchy vidění, cyanopsie a rozmazané vidění.
Nežádoucí účinky zjištěné po uvedení přípravku na trh byly získány v období delším než 10 let. Vzhledem k tomu, že držiteli rozhodnutí o registraci nejsou všechny nežádoucí účinky nahlášeny a nejsou tedy zahrnuty v databázi nežádoucích účinků, nelze u nich spolehlivě stanovit četnost.
Souhrn nežádoucích účinků v tabulce
V tabulce jsou podle orgánových systémů a četnosti seřazeny všechny klinicky významné nežádoucí účinky, které se vyskytly v klinických studiích s četností vyšší než u placeba (velmi časté (> 1/10), časté (> 1/100 až < 1/10), méně časté (> 1/1000 až < 1/100), vzácné (> 1/10000 až < 1/1000)).
V každé skupině četností jsou nežádoucí účinky uvedeny v pořadí dle klesající závažnosti.
Tabulka 1: Klinicky významné nežádoucí účinky hlášené s četností vyšší než u placeba z kontrolovaných klinických studií a klinicky významné nežádoucí účinky hlášené po uvedení přípravku na trh
|
Třída orgánových systémů |
Velmi časté (> 1/10) |
Časté (> 1/100 a < 1/10) |
Méně časté (> 1/1000 a < 1/100) |
Vzácné (> 1/10000 a < 1/1000) |
|
Infekce a infestace |
Rinitida | |||
|
Poruchy imunitního systému |
Hypersenzitivita | |||
|
Poruchy nervového systému |
Bolest hlavy |
Závrať |
Somnolence, hypestezie |
Cévní mozková příhoda, tranzitorní ischemická ataka, záchvat, opakovaný záchvat, synkopa |
|
Poruchy oka |
Změny barevného vidění**, poruchy vidění, rozmazané vidění, |
Poruchy slzení***, bolest oka, fotofobie, fotopsie, oční hyperemie, zraková percepce jasu, konjunktivitida |
Nearteritická přední ischemická neuropatie optického nervu (NAION)*, retinální cévní okluze*, retinální krvácení, arteriosklerotická retinopatie, porucha sítnice, glaukom, defekt zorného pole, diplopie, snížená zraková ostrost, myopie, astenopie, sklivcové zákalky, porucha duhovky, mydriáza, halo efekt, edém oka, otok oka, porucha oka, hyperemie spojivky, podráždění oka, abnormální pocit v oku, edém očního víčka, změny zabarvení skléry | |
|
Poruchy ucha a labyrintu |
Vertigo, tinitus |
Hluchota | ||
|
Srdeční poruchy |
palpitace |
Náhlá srdeční smrt*, infarkt myokardu, komorová arytmie , atriální fibrilace, nestabilní angina pectoris |
|
Třída orgánových systémů |
Velmi časté (> 1/10) |
Časté (> 1/100 a < 1/10) |
Méně časté (> 1/1000 a < 1/100) |
Vzácné (> 1/10000 a < 1/1000) |
|
Cévní poruchy |
Zrudnutí, nával horka |
Hypertenze, | ||
|
Respirační, hrudní a mediastinální poruchy |
Zduření nosní sliznice |
Epistaxe, zduření vedlejší nosní dutiny |
Pocit stažení hrdla, otok nosní sliznice, suchost v nose | |
|
Gastrointestinální poruchy |
Refluxní choroba jícnu, zvracení, bolest horní poloviny břicha, sucho v ústech |
Orální hypestezie | ||
|
Poruchy kůže a podkožní tkáně |
Stevens-Johnsonův syndrom (SJS) , toxická epidermální nekrolýza (TEN)* | |||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Myalgie, bolest v končetině | |||
|
Poruchy ledvin a močových cest |
Hematurie | |||
|
Poruchy reprodukčního systému a prsu |
Krvácení z penisu, priapismus*, hematospermie, zvýšená erekce, | |||
|
Celkové poruchy a reakce v místě aplikace |
Bolest na hrudi, únava, pocit horka | |||
|
Vyšetření |
Zvýšená srdeční frekvence |
*Hlášeno pouze po uvedení přípravku na trh
**Distorze barevného vidění: chloropsie, chromatopsie, cyanopsie, erytropsie a xantopsie ***Poruchy slzení: suché oko, porucha slzení a zvýšené slzení
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Symptomy
Ve studiích u zdravých dobrovolníků s jednotlivou dávkou až 800 mg byly nežádoucí účinky podobné nežádoucím účinkům pozorovaným při nižších dávkách, jejich incidence a závažnost však byla zvýšena. Užitím dávky 200 mg nedocházelo ke zvýšené účinnosti, ale zvyšovalo se množství nežádoucích účinků (bolest hlavy, návaly, závratě, dyspepsie, zduření nosní sliznice, porušené vidění).
Opatření
V případech předávkování je nutno podle potřeby zavést standardní podpůrná opatření. Nelze předpokládat, že by dialýza zrychlila clearance, protože sildenafil se váže ve vysoké míře na plazmatické proteiny a nevylučuje se močí.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: urologika, léčiva používaná při poruchách erekce, ATC kód: G04BE03.
Mechanismus účinku
Sildenafil představuje formu perorální léčby erektilní dysfunkce. V přirozených podmínkách, tj. při sexuální stimulaci, obnovuje porušenou erektilní funkci zvýšením přítoku krve do penisu.
Fyziologickým mechanismem při erekci penisu je uvolňování oxidu dusnatého (NO) v corpus cavernosum během sexuální stimulace. Oxid dusnatý aktivuje enzym guanylátcyklázu, výsledkem jsou zvýšené hladiny cyklického guanosinmonofosfátu (cGMP), vedoucí k uvolnění hladkého svalstva v corpus cavernosum, což umožní přítok krve.
Sildenafil je účinný a selektivní inhibitor cGMP specifické fosfodiesterázy typu 5 (PDE5) v corpus cavernosum, kde je PDE5 zodpovědná za degradaci cGMP. Sildenafil má periferní místo účinku na erekci. Sildenafil nemá žádný přímý relaxační účinek na izolované lidské corpus cavernosum, avšak významně zesiluje relaxační účinek NO na tuto tkáň. Při aktivaci dráhy NO/cGMP, k níž při sexuální stimulaci dochází, má inhibice PDE5 sildenafilem za následek zvýšení hladin cGMP v corpus cavernosum. Proto je k zajištění zamýšleného příznivého farmakologického účinku sildenafilu nutná sexuální stimulace.
Farmakodynamické účinky
Studie in vitro prokázaly, že sildenafil je selektivní k PDE5, která se účastní procesu erekce. Jeho účinek je mnohem silnější na PDE5 než na jiné známé izoformy fosfodiesterázy. Má také 10x vyšší selektivitu k PDE5 než k PDE6, která se účastní na kaskádě převodu světla v sítnici. Při maximálních doporučených dávkách má 80x vyšší selektivitu k PDE5 než k PDE1 a více než 700x vyšší selektivitu k PDE5 než PDE2, 3, 4, 7, 8, 9, 10 a 11. Sildenafil má především vyšší (více než 4000x) selektivitu k PDE5 oproti PDE3, což je cAMP-specifická izoforma fosfodiesterázy účastnící se kontroly srdeční kontraktility.
Klinická účinnost a bezpečnost
Pro zhodnocení doby nutné k dosažení erekce při adekvátní sexuální stimulaci byly provedeny dvě klinické studie. Ve studii s penilní plethysmografií (RigiScan) u pacientů na lačno byla po užití sildenafilu střední doba pro dosažení erekce o 60% rigiditě (dostatečné pro pohlavní styk) 25 min. (rozmezí 12-37 min.). V další RigiScan studii byl sildenafil schopen umožnit erekci v odpověď na sexuální stimulaci ještě 4-5 hodin po užití dávky.
Sildenafil působí mírné a přechodné snížení krevního tlaku, které ve většině případů nemá žádný klinický efekt. Po perorální dávce 100 mg sildenafilu bylo průměrné maximální snížení krevního tlaku vleže 8,4 mm Hg. Odpovídající změna diastolického krevního tlaku vleže byla 5,5 mm Hg. Toto snížení krevního tlaku je ve shodě s vazodilatačním účinkem sildenafilu, pravděpodobně následkem zvýšených hladin cGMP v cévní hladké svalovině. Jednotlivé dávky sildenafilu až do 100 mg perorálně neměly žádný klinicky významný účinek na EKG u zdravých dobrovolníků.
Ve studii sledující hemodynamické účinky jednorázové perorální dávky sildenafilu 100 mg u 14 pacientů s těžkou formou ischemické choroby srdeční (ICHS) (stenóza větší než 70% minimálně na jedné koronární tepně) došlo k průměrnému poklesu systolického krevního tlaku v klidu o 7 % a diastolického krevního tlaku o 6 % oproti výchozím hodnotám. Průměrný plicní systolický tlak poklesl o 9 %. Sildenafil neměl žádný účinek na minutový objem a nezhoršoval průtok krve stenotickými koronárními tepnami.
Dvojitě zaslepená, placebem kontrolovaná studie hodnotila odpověď na tělesnou zátěž u 144 pacientů s erektilní dysfunkcí a chronickou stabilní anginou pectoris, kteří pravidelně užívali antianginózní léčivé přípravky (kromě nitrátů). Výsledky při srovnání sildenafilu a placeba neprokázaly žádné klinicky významné rozdíly v době do vzniku stenokardií znemožňujících další zátěž.
U některých jedinců byly 1 hodinu po podání dávky 100 mg pomocí Farnsworthova-Munsellova testu se 100 odstíny barev zjištěny mírné a přechodné změny v rozlišování barev (modrá/zelená), přičemž 2 hodiny po podání již nebyly žádné účinky pozorovatelné. Předpokládaný mechanismus této změny v rozlišování barev souvisí s inhibicí PDE6, která se podílí na kaskádě převodu světla na sítnici. Sildenafil nemá žádný vliv na ostrost zraku ani na citlivost na kontrast. V malé placebem kontrolované studii u pacientů s prokázanou věkem podmíněnou makulární degenerací (n=9) nebyly po sildenafilu (jednorázová dávka, 100 mg) prokázány žádné signifikantní změny při provedených očních vyšetřeních (zraková ostrost, Amslerova mřížka, test rozlišení barev simulující světla na semaforu, Humphreyův perimetr a fotostres).
U zdravých dobrovolníků neměla dávka 100 mg perorálně žádný účinek na motilitu nebo morfologii spermatu (viz bod 4.6).
Další informace o klinických studiích
V klinických studiích byl sildenafil podán více než 8000 nemocným ve věku 19-87 let. Byly zastoupeny následující skupiny nemocných: starší nemocní (19,9 %), nemocní s hypertenzí (30,9 %), diabetici (20,3 %), s ischemickou chorobou srdeční (5,8 %), s hyperlipidemií (19,8 %), poraněním míchy (0,6 %), depresí (5,2 %), nemocní po transuretrální resekci prostaty (3,7 %), radikální prostatektomií (3,3 %). Následující skupiny byly buď vyloučeny z klinických studií, nebo nebyly dostatečně zastoupeny: nemocní po operaci v malé pánvi, po radioterapii, nemocní se závažnou ledvinovou nebo jaterní poruchou a nemocní s některými kardiovaskulárními potížemi (viz bod 4.3).
Ve studiích s fixní dávkou uvádělo zlepšení erekce díky léčbě 62 % pacientů s dávkou 25 mg, 74 % s dávkou 50 mg a 82 % s dávkou 100 mg, a to ve srovnání s 25 % při použití placeba.
V kontrolovaných klinických studiích byl počet nemocných užívajících sildenafil, kteří odstoupili ze studie, nízký a srovnatelný s placebem.
Ve všech studiích byl podíl nemocných uvádějících zlepšení při léčbě sildenafilem následující: erektilní dysfunkce (ED) psychogenního původu (84 %), smíšené ED (77 %), organické ED (68 %), starší nemocní (67 %), diabetici (59 %), ICHS (69 %), hypertenze (68 %), TURP (61 %), radikální prostatektomie (43 %), poranění míchy (83 %), deprese (75 %). V dlouhodobých studiích přetrvávala bezpečnost a účinnost sildenafilu.
5.2 Farmakokinetické vlastnosti
Absorpce
Sildenafil se rychle vstřebává. Maximálních pozorovaných plazmatických koncentrací se dosahuje za 30-120 minut (průměr 60 minut) po podání perorální dávky ve stavu na lačno. Průměrná absolutní biologická dostupnost po perorální dávce je 41 % (rozmezí 25-63 %). Po perorálním podání dávky sildenafilu se hodnoty AUC a Cmax zvyšují úměrně s dávkou v celém rozsahu doporučených dávek (25-100 mg).
Při podání sildenafilu spolu s jídlem se rychlost absorpce snižuje s průměrným zpožděním Tmax o 60 minut a průměrným snížením Cmax o 29 %.
Distribuce
Průměrný distribuční objem při ustáleném stavu (Vss) sildenafilu je 105 l, což naznačuje distribuci do tkání. Po jednorázově podané perorální dávce 100 mg činí průměrná hodnota maximální celkové plazmatické koncentrace sildenafilu přibližně 440 ng/ml (CV 40 %). Protože sildenafil a jeho hlavní cirkulující metabolit N-desmetyl se váží na plazmatické proteiny z 96 %, má to za následek průměrnou hodnotu maximální plazmatické koncentrace volného sildenafilu 18 ng/ml (38 nM). Vazba na proteiny nezávisí na celkové koncentraci léku.
U zdravých dobrovolníků, jimž byl podán sildenafil (jednorázová dávka 100 mg) bylo v ejakulátu 90 minut po podání dávky přítomno méně než 0,0002 % (průměr 188 ng) podané dávky.
Biotransformace
Sildenafil se vylučuje převážně pomocí jatemích mikrosomálních isoenzymů CYP3A4 (hlavní cesta) a CYP2C9 (vedlejší cesta). Hlavní cirkulující metabolit je výsledkem N-demetylace sildenafilu. Tento metabolit vykazuje profil selektivity vůči fosfodiesteráze podobný profilu sildenafilu a in vitro potenci vůči PDE5 ve výši přibližně 50 % mateřské látky. Plazmatické koncentrace tohoto metabolitu dosahují přibližně 40 % hodnot zjištěných u sildenafilu. Metabolit N-desmetyl se dále biotransformuje, s terminálním poločasem přibližně 4 hodin.
Eliminace
Celková clearance sildenafilu z organismu je 41 l/hod. s výsledným terminálním poločasem 3-5 hod. Po perorálním nebo intravenózním podání se sildenafil vylučuje ve formě metabolitů převážně stolicí (přibližně 80 % perorálně podané dávky) a v menší míře močí (přibližně 13 % perorálně podané dávky).
Farmakokinetické vlastnosti u speciálních skupin pacientů Starší pacienti:
Zdraví starší pacienti (65 let a více) vykazovali sníženou clearance sildenafilu, výsledkem byla přibližně o 90 % vyšší plazmatická koncentrace sildenafilu a účinného N-desmetyl metabolitu ve srovnání se zdravými mladými dobrovolníky (18-45 let). Vzhledem k rozdílu vazby na bílkoviny plazmy závislém na věku byl odpovídající vzestup volné plazmatické koncentrace sildenafilu přibližně 40 %.
Renální nedostatečnost:
U dobrovolníků s mírnou až středně těžkou poruchou renální funkce (clearance kreatininu = 3080 ml/min) nebyla farmakokinetika sildenafilu po podání jednorázové dávky 50 mg změněna. Střední AUC a Cmax N-desmetyl metabolitu vzrostla až o 126 %, resp. 73 % ve srovnání s hodnotami věkově srovnatelných dobrovolníků bez poruchy renální funkce. Tyto odlišnosti ale nebyly vzhledem k vysoké mezisubjektové variabilitě statisticky signifikantní. U dobrovolníků se závažnou ledvinnou poruchou (clearance kreatininu < 30 ml/min) byla snížena clearance sildenafilu. To mělo za následek vzestup AUC a Cmax o 100 %, resp. 88 % ve srovnání se stejně starými dobrovolníky bez renální poruchy. Navíc došlo k podstatnému zvýšení hodnot AUC a Cmax o 200 %, resp. 79 % pro N-desmetyl metabolit.
Jaterní nedostatečnost:
U dobrovolníků s mírnou až středně těžkou cirhózou jater (Child-Pugh klasifikace A a B) byla clearance sildenafilu snížena, což vedlo ke zvýšení hodnot AUC (o 84 %) a Cmax (o 47 %) ve srovnání s hodnotami věkově srovnatelných dobrovolníků bez poruchy funkce jater. Farmakokinetika sildenafilu u nemocných se závažnou jaterní poruchou nebyla studována.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity, hodnocení kancerogenního potenciálu, reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Jádro tablety:
Mikrokrystalická celulosa (E460) Hydrogenfosforečnan vápenatý Sodná sůl kroskarmelosy Hypromelosa (E464) Magnesium-stearát (E572)
Potah tablety:
Monohydrát laktosy Hypromelosa (E464)
Oxid titaničitý (E171)
Triacetin (E1518)
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
5 let
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
Blistr (PVC-fólie/Al-fólie): 1 potahovaná tableta, v krabičce.
Blistr (perforovaný jednodávkový blistr, PVC-fólie/Al-fólie): 4 x 1, 8 x 1 nebo 12 x 1 potahovaná tableta, v krabičce.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Smaiješka cesta 6, 8501 Novo mesto, Slovinsko
8. REGISTRAČNÍ ČÍSLO(A)
Vizarsin 25 mg potahované tablety 1 potahovaná tableta: EU/1/09/551/001 4 x 1 potahovaná tableta: EU/1/09/551/002 8 x 1 potahovaná tableta: EU/1/09/551/003 12 x 1 potahovaná tableta: EU/1/09/551/004
Vizarsin 50 mg potahované tablety 1 potahovaná tableta: EU/1/09/551/005 4 x 1 potahovaná tableta: EU/1/09/551/006 8 x 1 potahovaná tableta: EU/1/09/551/007 12 x 1 potahovaná tableta: EU/1/09/551/008
Vizarsin 100 mg potahované tablety 1 potahovaná tableta: EU/1/09/551/009 4 x 1 potahovaná tableta: EU/1/09/551/010 8 x 1 potahovaná tableta: EU/1/09/551/011 12 x 1 potahovaná tableta: EU/1/09/551/012
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 21. září 2009
Datum posledního prodloužení registrace: 16. května 2014
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
NÁZEV PŘÍPRAVKU
1.
Vizarsin 25 mg tablety dispergovatelné v ústech Vizarsin 50 mg tablety dispergovatelné v ústech Vizarsin 100 mg tablety dispergovatelné v ústech
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 25 mg, 50 mg nebo 100 mg.
Pomocné látky se známým účinkem:
Vizarsin 25 mg tablety dispergovatelné v ústech
Jedna tableta dispergovatelná v ústech obsahuje 0,375 mg aspartamu (E951) a 0,00875 mg sorbitolu (E420).
Vizarsin 50 mg tablety dispergovatelné v ústech
Jedna tableta dispergovatelná v ústech obsahuje 0,75 mg aspartamu (E951) a 0,0175 mg sorbitolu (E420).
Vizarsin 100 mg tablety dispergovatelné v ústech
Jedna tableta dispergovatelná v ústech obsahuje 1,5 mg aspartamu (E951) a 0,035 mg sorbitolu (E420).
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Tableta dispergovatelná v ústech.
Vizarsin 25 mg tablety dispergovatelné v ústech: Bílé až téměř bílé, kulaté, mírně bikonvexní tablety, s možnými tmavšími tečkami.
Vizarsin 50 mg tablety dispergovatelné v ústech: Bílé až téměř bílé, kulaté, mírně bikonvexní tablety, s možnými tmavšími tečkami.
Vizarsin 100 mg tablety dispergovatelné v ústech: Bílé až téměř bílé, kulaté, mírně bikonvexní tablety, s možnými tmavšími tečkami.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek Vizarsin je indikován k léčbě erektilní dysfunkce u dospělých mužů, pod kterou rozumíme neschopnost dosáhnout nebo udržet erekci dostatečnou k umožnění pohlavního styku.
Pro dosažení účinku přípravku Vizarsin je nezbytné sexuální dráždění.
4.2 Dávkování a způsob podání
Dávkování
Použití u dospělých:
Doporučená dávka je 50 mg, kterou je třeba užít podle potřeby přibližně jednu hodinu před sexuální aktivitou. Podle účinnosti a snášenlivosti lze dávku zvýšit na 100 mg nebo snížit na 25 mg. Maximální doporučená dávka je 100 mg. Maximální doporučená četnost užití dávky je jedenkrát denně. Pokud je přípravek Vizarsin užit současně s jídlem, může dojít ke zpoždění nástupu účinku ve srovnání se stavem na lačno (viz bod 5.2).
Zvláštní populace
Starší pacienti:
U starších pacientů (> 65 let) není nutná úprava dávek.
Poškození ledvin:
Dávkování popsané v odstavci „Použití u dospělých“ se vztahuje na nemocné s mírnou nebo středně těžkou poruchou ledvin (clearance kreatininu = 30-80 ml/min).
Protože clearance sildenafilu je u nemocných se závažnou poruchou ledvin (clearance kreatininu < 30 ml/min) snížena, doporučuje se zahájit léčbu dávkou 25 mg. Podle účinnosti a snášenlivosti lze dle potřeby dávku postupně zvýšit na 50 mg až 100 mg.
Poškození jater:
Protože clearance sildenafilu je u nemocných s poruchou jater (např. cirhóza) snížena, doporučuje se zahájit léčbu dávkou 25 mg. Podle účinnosti a snášenlivosti lze dle potřeby dávku postupně zvýšit na 50 mg až 100 mg.
Pediatrická populace
Přípravek Vizarsin není určen pro děti a dospívající do 18 let.
Použití u nemocných používajících jiné léčivé přípravky:
S výjimkou ritonaviru, jehož současné užití se sildenafilem není doporučeno (viz bod 4.4), měla by být u nemocných, kteří současně užívají přípravky inhibující CYP3A4, jako počáteční dávka užita dávka 25 mg (viz bod 4.5).
Předtím, než je zahájena léčba sildenafilem, by měli být pacienti léčení alfa-blokátory stabilizováni na této léčbě z důvodu minimalizace možného vzniku posturální hypotenze. Kromě toho je třeba zvážit zahájení léčby sildenafilem dávkou 25 mg (viz body 4.4 a 4.5).
Způsob podání
Perorální podání.
Tableta dispergovatelná v ústech se položí do úst na jazyk, kde dojde k rychlému rozpuštění slinami a je snadné ji spolknout. Je možné ji zapít tekutinou, ale není to nutné. Odstranění neporušené tablety z úst je obtížné. Tableta je křehká, proto by měla být užita ihned po otevření blistru.
Vizarsin tablety dispergovatelné v ústech mohou být užívány jako alternativa k přípravku Vizarsin potahované tablety u pacientů, pro které je obtížné spolknutí potahované tablety.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Ve shodě se známými účinky na metabolismus oxidu dusnatého/cyklického guanosin monofosfátu (cGMP) (viz bod 5.1) se ukázalo, že sildenafil je schopen potencovat hypotenzní účinky nitrátů. Jeho současné užití s látkami schopnými uvolňovat oxid dusnatý (jako je amylnitrit) nebo nitráty v jakékoli formě je proto kontraindikováno.
Současné podávání PDE5 inhibitorů, včetně sildenafilu, se stimulátory guanylátcyklázy, jako je riocigvát, je kontraindikováno, protože může potenciálně vést k symptomatické hypotenzi (viz bod 4.5).
Přípravky k léčbě erektilní dysfunkce, mezi které patří sildenafil, by neměly být užívány muži,
pro které není sexuální aktivita vhodná (např. nemocní se závažnými kardiovaskulárními poruchami, jako je nestabilní angina pectoris nebo závažné srdeční selhání).
Přípravek Vizarsin je kontraindikován u pacientů, kteří ztratili zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION), bez ohledu na to, zda tato příhoda souvisela s předchozím užitím inhibitoru fosfodiesterázy 5 (PDE5)či nikoli (viz bod 4.4).
Bezpečnost sildenafilu nebyla studována u následujících podskupin nemocných, a proto jeho použití je u nich kontraindikováno do doby, než budou k dispozici další informace: závažná jaterní porucha, hypotenze (TK< 90/50 mm Hg), cévní mozková příhoda nebo infarkt myokardu v nedávné anamnéze a také známé hereditární degenerativní postižení sítnice, jako je např. retinitispigmentosa (malá část těchto nemocných má genetické postižení retinální fosfodiesterázy).
4.4 Zvláštní upozornění a opatření pro použití
Aby bylo možno určit diagnózu erektilní dysfunkce a stanovit možné příčiny, je třeba u nemocného zjistit anamnézu a provést fyzikální vyšetření dříve, než je rozhodnuto o farmakologické léčbě.
Kardiovaskulární rizikové faktory
Před zahájením jakékoli léčby erektilní dysfunkce by měl lékař posoudit kardiovaskulární funkce pacienta, protože sexuální aktivita s sebou nese jisté riziko srdečních příhod. Sildenafil má vazodilatační vlastnosti, jejichž výsledkem je malé a přechodné snížení tlaku krve (viz bod 5.1).
Před předepsáním sildenafilu by měli lékaři pečlivě zvážit, zda některé základní onemocnění u jejich pacientů nemůže být negativně ovlivněno těmito vasodilatačními účinky, a to zejména v kombinaci se sexuální aktivitou. Mezi pacienty se zvýšenou citlivostí na vasodilatancia patří nemocní s obstrukcí odtoku krve z levé komory (např. aortální stenóza, hypertrofická obstrukční kardiomyopatie) nebo pacienti se vzácným syndromem mnohočetné systémové atrofie manifestující se jako závažné zhoršení autonomní regulace krevního tlaku.
Sildenafil zvyšuje hypotenzivní účinek nitrátů (viz bod 4.3).
V období po uvedení přípravku na trh byly hlášeny případy závažných kardiovaskulárních příhod včetně infarktu myokardu, nestabilní anginy pectoris, náhlé srdeční smrti, komorové arytmie, mozkové hemorhagie, přechodných ischemických atak, hypertenze a hypotenze v časové souvislosti
s užitím sildenafilu. Většina z těchto pacientů, ale ne všichni, měla již dříve existující kardiovaskulární rizikové faktory. Rada hlášených příhod vznikla během nebo krátce po pohlavním styku a několik hlášených příhod vzniklo krátce po užití sildenafilu bez souvislosti se sexuální aktivitou. Není možné určit, zda tyto příhody lze přímo vztáhnout k těmto faktorům nebo jiným faktorům.
Priapismus
Přípravky k léčbě erektilní dysfunkce, včetně sildenafilu, je třeba používat opatrně u pacientů s anatomickou deformací penisu (jako je angulace, kavernózní fibróza nebo Peyroneova choroba) nebo u pacientů s onemocněními, která je predisponují k priapismu (jako je srpkovitá anémie, vícečetný myelom nebo leukémie).
Při použití sildenafilu po uvedení přípravku na trh byla hlášena protrahovaná erekce a priapismus.
V případě erekce, která přetrvává déle než 4 hodiny, by měl pacient vyhledat okamžitou lékařskou pomoc. Pokud není priapismus okamžitě léčen, mohl by vést k poškození tkáně penisu a trvalé ztrátě potence.
Současné použití s jinými inhibitory PDE5 či jinými typy léčby erektilní dysfunkce
Bezpečnost a účinnost kombinace sildenafilu s jinými inhibitory PDE5 nebo s jinými léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil či s jinými léčbami erektilní dysfunkce nebyla zjišťována. Proto se případné použití těchto kombinací nedoporučuje.
V souvislosti s užitím sildenafilu i jiných inhibitorů PDE5 byly spontánně hlášeny případy poruchy zraku (viz bod 4.8). V souvislosti s užitím sildenafilu i jiných inhibitorů PDE5 byly spontánně i z observační studie hlášeny případy vzácného onemocnění nearteritické přední ischemické neuropatie optického nervu (NAION) (viz bod 4.8). Je nutné pacienty poučit, aby v případě náhlé poruchy zraku přestali přípravek Vizarsin užívat a okamžitě vyhledali svého lékaře (viz bod 4.3).
Současné užívání s ritonavirem
Současné užívání sildenafilu s ritonavirem není doporučeno (viz bod 4.5). Současné užívání s alfa-blokátorv
Při podání sildenafilu pacientům užívajícím alfa-blokátory je třeba opatrnosti, protože souběžné podání může vést u citlivých jedinců k symptomatické hypotenzi (viz bod 4.5). Ta se může nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Předtím, než je zahájena léčba sildenafilem, by měli být pacienti hemodynamicky stabilizováni na léčbě alfa-blokátory z důvodu minimalizace možného vzniku posturální hypotenze. Je třeba zvážit zahájení léčby sildenafilem dávkou 25 mg (viz bod 4.2). Pacienty je třeba poučit o tom, jak jednat, objeví-li se příznaky posturální hypotenze.
Účinek na krvácivost
Studie s lidskými trombocyty ukázaly, že sildenafil potencuje antiagregační účinek dihydrát nitroprusidu sodného in vitro. K dispozici nejsou žádné informace o bezpečnosti podání sildenafilu pacientům s poruchami srážlivosti krve nebo aktivní vředovou chorobou. Proto je podávání sildenafilu těmto pacientům nutné pečlivě uvážit.
Ženy
Přípravek Vizarsin není indikován k použití u žen. Pomocné látky
Přípravek Vizarsin obsahuje aspartam (E951), zdroj fenylalaninu, který může být škodlivý pro lidi trpící fenylketonurií.
Přípravek Vizarsin obsahuje sorbitol (E420). Pacienti se vzácnými dědičnými problémy s intolerancí fruktosy by tento přípravek neměli užívat.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Účinky jiných léků na sildenafil In vitro studie:
Metabolizmus sildenafilu je zprostředkován hlavně izoformou 3A4 (hlavní cesta) a izoformou 2C9 (vedlejší cesta) cytochromu P450 (CYP). Proto mohou inhibitory těchto izoenzymů snížit clearance sildenafilu a induktory těchto izoenzymů mohou zvýšit clearance sildenafilu.
In vivo studie:
Populační farmakokinetická analýza klinických studií zjistila snížení clearance sildenafilu při současném podání s inhibitory CYP3A4 (jako jsou ketokonazol, erythromycin, cimetidin). Ačkoli nebylo pozorováno zvýšení incidence nežádoucích účinků u těchto pacientů, při souběžném užití sildenafilu s inhibitory CYP3A4 by měla být jako úvodní podána dávka 25 mg.
Při současném podávání inhibitoru HIV proteázy ritonaviru (500 mg 2x denně), což je vysoce účinný
inhibitor P450, se sildenafilem (jednorázová dávka 100 mg), došlo v ustáleném stavu k 300% (4násobnému) zvýšení Cmax sildenafilu a 1000% (11násobnému) zvýšení AUC sildenafilu v plazmě.
Po 24 hodinách byly plazmatické hladiny sildenafilu ještě přibližně 200 ng/ml, narozdíl od hladiny 5 ng/ml, která je obvyklá, pokud je sildenafil podáván samostatně. Tento nález je ve shodě s význačným účinkem ritonaviru na řadu P450 substrátů. Sildenafil nemá žádný vliv na farmakokinetiku ritonaviru. Na základě těchto farmakokinetických nálezů současné podávání sildenafilu s ritonavirem není doporučeno (viz bod 4.4) a za žádných okolností nesmí nejvyšší dávka sildenafilu v průběhu 48 hodin přesáhnout 25 mg.
Při současném podávání inhibitoru HIV proteázy sachinaviru (1200 mg 3x denně), který je inhibitorem CYP3A4, se sildenafilem (jednorázová dávka 100 mg), došlo ke 140% zvýšení Cmax sildenafilu a 210% zvýšení AUC sildenafilu v plazmě. Sildenafil nemá žádný vliv na farmakokinetiku sachinaviru (viz bod 4.2). Lze očekávat, že účinnější inhibitory CYP3A4, jako je ketokonazol nebo itrakonazol, budou mít výraznější účinky.
Při současném podání jednotlivé dávky 100 mg sildenafilu se středně silným inhibitorem CYP3A4 erythromycinem došlo v ustáleném stavu (500 mg erythromycinu 2x denně po dobu 5 dní) ke zvýšení systémové expozice sildenafilu o 182 % (AUC). U normálních zdravých dobrovolníků mužů nebyl prokázán účinek azithromycinu (v dávce 500 mg denně po dobu 3 dnů) na AUC, Cmax, tmax, konstantu rychlosti vylučování nebo následný poločas sildenafilu či jeho hlavního cirkulujícího metabolitu. Současné podávání cimetidinu (800 mg), což je inhibitor cytochromu P450 a nespecifický inhibitor CYP3A4, a sildenafilu (50 mg) zdravým dobrovolníkům vedlo k 56% zvýšení plazmatických hladin sildenafilu.
Grapefruitový džus, který je slabým inhibitorem metabolizmu CYP3A4 ve střevní stěně, může způsobit mírné zvýšení plazmatických hladin sildenafilu.
Jednorázové dávky antacida (hydroxid hořečnatý/ hydroxid hlinitý) neměly na biologickou dostupnost sildenafilu vliv.
Ačkoli nebyly provedeny specifické interakční studie pro všechny léčivé přípravky, populační farmakokinetická analýza neprokázala žádný účinek souběžné léčby na farmakokinetiku sildenafilu, pokud se uvažovaly skupiny léků jako inhibitory CYP2C9 (např. tolbutamid, warfarin, fenytoin), inhibitory CYP2D6 (např. selektivní inhibitory zpětného vychytávání serotoninu, tricyklická antidepresiva), thiazid a příbuzná diuretika, kličková a draslík šetřící diuretika, ACE inhibitory, blokátory kalciových kanálů, antagonisté beta-adrenoreceptorů nebo induktory metabolismu CYP450 (jako např. rifampicin, barbituráty). Ve studii se zdravými mužskými dobrovolníky vedlo souběžné podání endotelinového antagonisty bosentanu (induktor CYP3A4 [středně silný], CYP2C9 a zřejmě i CYP2C19) v ustáleném stavu (125 mg 2x denně) se sildenafilem v ustáleném stavu (80 mg 3x denně) k 62,6% snížení AUC a 55,4% snížení Cmax sildenafilu. Proto lze při souběžném podání se silnými induktory CYP3A4 jako je rifampicin, očekávat větší snížení plazmatických koncentrací sildenafilu.
Nikorandil je sloučeninou složenou z aktivátoru draslíkového kanálu a nitrátu. Z důvodu přítomnosti nitrátové složky existuje potenciál k závažným interakcím mezi sildenafilem a nikorandilem.
Účinky sildenafilu na jiné léky
In vitro studie:
Sildenafil je slabý inhibitor isoforem 1A2, 2C9, 2C19, 2D6, 2E1 a 3A4 cytochromu P450
(IC50 >150 ^M). Za předpokladu maximálních plazmatických koncentrací cca 1 ^M po doporučených
dávkách není pravděpodobné, že by sildenafil změnil clearance substrátů těchto isoenzymů.
Nejsou žádné údaje o interakci mezi sildenafilem a nespecifickými inhibitory fosfodiesterázy, jako je např. teofylin nebo dipyridamol.
In vivo studie:
Ve shodě se známými účinky na metabolismus oxidu dusnatého/cGMP (viz bod 5.1) se ukázalo, že sildenafil je schopen potencovat hypotenzní účinky nitrátů. Jeho současné užití s látkami schopnými uvolňovat oxid dusnatý nebo s nitráty v jakékoli formě je proto kontraindikováno (viz bod 4.3).
Riocigvát: Předklinické studie ukázaly aditivní systémový účinek při snižování krevního tlaku, když byly inhibitory PDE5 kombinovány s riocigvátem. V klinických studiích bylo prokázáno, že riocigvát zesiluje hypotenzní účinek inhibitorů PDE5. U sledované populace nebyl prokázán příznivý klinický účinek kombinace. Současné užívání riocigvátu s PDE5 inhibitory, včetně sildenafilu, je kontraindikováno (viz bod 4.3).
Při souběžném podání sildenafilu pacientům užívajícím alfa-blokátory je třeba opatrnosti, protože souběžné podání může vést u citlivých jedinců k symptomatické hypotenzi. Ta se může nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu (viz body 4.2 a 4.4). Ve třech specifických studiích lékových interakcí byl pacientům s benigní hyperplazií prostaty (BPH), kteří byli stabilizováni na léčbě doxazosinem, současně podáván alfa-blokátor doxazosin (4 mg a 8 mg) a sildenafil (25 mg, 50 mg a 100 mg).
Během studie bylo u této populace pozorováno průměrné dodatečné snížení krevního tlaku vleže o 7/7 mm Hg, 9/5 mm Hg resp. o 8/4 mm Hg a průměrné dodatečné snížení krevního tlaku ve stoje o 6/6 mm Hg, 11/4 mm Hg resp. o 4/5 mm Hg. Při současném podání sildenafilu a doxazosinu pacientům, stabilizovaným na léčbě doxazosinem, se vzácně objevila hlášení o pacientech, kteří prodělali symptomatickou posturální hypotenzi. Tato hlášení zahrnovala závratě a mdloby, nikoliv však synkopu.
Nebyly prokázány žádné podstatné interakce při současném podání sildenafilu (50 mg) s tolbutamidem (250 mg) nebo s warfarinem (40 mg), které jsou metabolizovány CYP2C9.
Sildenafil (50 mg) nepotencoval prodloužení času krvácivosti způsobené kyselinou acetylsalicylovou (150 mg).
U zdravých dobrovolníků nepotencoval sildenafil (50 mg) hypotenzní účinky alkoholu, pokud průměrné maximální hladiny alkoholu v krvi dosáhly hodnot 80 mg/dl.
Při rozboru následujících skupin antihypertenziv: diuretika, P-blokátory a ACE inhibitory, blokátory receptorů pro angiotensin II, antihypertenzní přípravky (vazodilatačně a centrálně účinkující), blokátory adrenergních neuronů, blokátory kalciových kanálů a a-blokátory, se neprokázal žádný rozdíl v profilu nežádoucích účinků u nemocných užívajících sildenafil ve srovnání s nemocnými užívajícími placebo. Ve specifické interakční studii, ve které byl sildenafil (100 mg) současně podáván s amlodipinem nemocným s hypertenzí, došlo k přídatnému snížení systolického krevního tlaku vleže o 8 mm Hg. Odpovídající přídatné snížení diastolického krevního tlaku vleže bylo 7 mm Hg. Tyto hodnoty přídatného snížení krevního tlaku měly stejný rozsah jako hodnoty, které byly pozorovány, pokud byl sildenafil podáván zdravým dobrovolníkům samostatně (viz bod 5.1).
Sildenafil (100 mg) neovlivňoval farmakokinetiku v ustáleném stavu inhibitorů HIV proteázy sachinaviru a ritonaviru, což jsou oba substráty CYP3A4.
U zdravých mužských dobrovolníků mělo souběžné podání sildenafilu v ustáleném stavu (80 mg 3x denně) a bosentanu (125 mg 2x denně) za následek 49,8% nárůst AUC bosentanu a 42% nárůst Cmax bosentanu.
4.6 Fertilita, těhotenství a kojení
Přípravek Vizarsin není indikován k použití u žen.
Neexistují žádné adekvátní a dobře kontrolované studie u těhotných nebo kojících žen.
V reprodukčních studiích u potkanů a králíků nebyly po perorálním podání sildenafilu zjištěny žádné významné nežádoucí účinky.
Neprojevil se žádný účinek na motilitu nebo morfologii spermií po jednorázových perorálních dávkách 100 mg sildenafilu u zdravých dobrovolníků (viz bod 5.1).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly prováděny žádné studie zjišťující schopnost řídit a obsluhovat stroje.
Závratě a poruchy vidění byly hlášeny jako nežádoucí účinky v klinických studiích se sildenafilem. Nemocní by proto měli znát svoji reakci na přípravek Vizarsin dříve, než budou řídit motorová vozidla nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Bezpečnostní profil sildenafilu byl vytvořen na základě zkušeností 9 570 pacientů v 74 dvojitě zaslepených klinických studiích kontrolovaných placebem. Nejčastěji hlášenými nežádoucími účinky u pacientů užívajících sildenafil v klinických studiích byly bolest hlavy, návaly, dyspepsie, zduření nosní sliznice, závratě, nevolnost, nával horka, poruchy vidění, cyanopsie a rozmazané vidění.
Nežádoucí účinky zjištěné po uvedení přípravku na trh byly získány v období delším než 10 let. Vzhledem k tomu, že držiteli rozhodnutí o registraci nejsou všechny nežádoucí účinky nahlášeny a nejsou tedy zahrnuty v databázi nežádoucích účinků, nelze u nich spolehlivě stanovit četnost.
Souhrn nežádoucích účinků v tabulce
V tabulce jsou podle orgánových systémů a četnosti seřazeny všechny klinicky významné nežádoucí účinky, které se vyskytly v klinických studiích s četností vyšší než u placeba (velmi časté (> 1/10), časté (> 1/100 až < 1/10), méně časté (> 1/1000 až < 1/100), vzácné (> 1/10000 až < 1/1000)).
V každé skupině četností jsou nežádoucí účinky uvedeny v pořadí dle klesající závažnosti.
Tabulka 1: Klinicky významné nežádoucí účinky hlášené s četností vyšší než u placeba z kontrolovaných klinických studií a klinicky významné nežádoucí účinky hlášené po uvedení přípravku na trh
|
Třída orgánových systémů |
Velmi časté (> 1/10) |
Časté (> 1/100 a < 1/10) |
Méně časté (> 1/1000 a < 1/100) |
Vzácné (> 1/10000 a < 1/1000) |
|
Infekce a infestace |
Rinitida | |||
|
Poruchy imunitního systému |
Hypersenzitivita | |||
|
Poruchy nervového systému |
Bolest hlavy |
Závrať |
Somnolence, hypestezie |
Cévní mozková příhoda, tranzitorní ischemická ataka, záchvat*, opakovaný záchvat*, synkopa |
|
Poruchy oka |
Změny barevného vidění**, poruchy vidění, rozmazané vidění |
Poruchy slzení***, bolest oka, fotofobie, fotopsie, oční hyperemie, zraková percepce jasu, konjunktivitida |
Nearteritická přední ischemická neuropatie optického nervu (NAION)*, retinální cévní okluze*, retinální krvácení, arteriosklerotická retinopatie, poruchy sítnice, glaukom, defekt zorného pole, diplopie, snížená zraková ostrost, myopie, astenopie, sklivcové |
|
Třída orgánových systémů |
Velmi časté (> 1/10) |
Časté (> 1/100 a < 1/10) |
Méně časté (> 1/1000 a < 1/100) |
Vzácné (> 1/10000 a < 1/1000) |
|
zákalky, porucha duhovky, mydriáza, halo efekt, edém oka, otok oka, porucha oka, hyperemie spojivky, podráždění oka, abnormální pocit v oku, edém očního víčka, změny zabarvení skléry | ||||
|
Poruchy ucha a labyrintu |
Vertigo, tinitus |
Hluchota | ||
|
Srdeční poruchy |
palpitace |
Náhlá srdeční smrt*, infarkt myokardu, komorová arytmie*, atriální fibrilace, nestabilní angina pectoris | ||
|
Cévní poruchy |
Zrudnutí, nával horka |
Hypertenze, | ||
|
Respirační, hrudní a mediastinální poruchy |
Zduření nosní sliznice |
Epistaxe, zduření vedlejší nosní dutiny |
Pocit stažení hrdla, otok nosní sliznice, suchost v nose | |
|
Gastrointestinální poruchy |
Refluxní choroba jícnu, zvracení, bolest horní poloviny břicha, sucho v ústech |
Orální hypestezie | ||
|
Poruchy kůže a podkožní tkáně |
Stevens-Johnsonův syndrom (SJS)*, toxická epidermální nekrolýza (TEN)* | |||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Myalgie, bolest v končetině | |||
|
Poruchy ledvin a močových cest |
Hematurie | |||
|
Poruchy reprodukčního systému a prsu |
Krvácení z penisu, priapismus*, hematospermie, zvýšená erekce | |||
|
Celkové poruchy a reakce v místě aplikace |
Bolest na hrudi, únava, pocit horka | |||
|
Vyšetření |
Zvýšená srdeční frekvence |
*Hlášeno pouze po uvedení přípravku na trh
**Distorze barevného vidění: chloropsie, chromatopsie, cyanopsie, erytropsie a xantopsie ***Poruchy slzení: suché oko, porucha slzení a zvýšené slzení
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Symptomy
Ve studiích u zdravých dobrovolníků s jednotlivou dávkou až 800 mg byly nežádoucí účinky podobné
nežádoucím účinkům pozorovaným při nižších dávkách, jejich incidence a závažnost však byla zvýšena. Užitím dávky 200 mg nedocházelo ke zvýšené účinnosti, ale zvyšovalo se množství nežádoucích účinků (bolest hlavy, návaly, závratě, dyspepsie, zduření nosní sliznice, porušené vidění).
Opatření
V případech předávkování je nutno podle potřeby zavést standardní podpůrná opatření. Nelze předpokládat, že by dialýza zrychlila clearance, protože sildenafil se váže ve vysoké míře na plazmatické proteiny a nevylučuje se močí.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: urologika, léčiva používaná při poruchách erekce, ATC kód: G04BE03. Mechanismus účinku
Sildenafil představuje formu perorální léčby erektilní dysfunkce. V přirozených podmínkách, tj. při sexuální stimulaci, obnovuje porušenou erektilní funkci zvýšením přítoku krve do penisu.
Fyziologickým mechanismem při erekci penisu je uvolňování oxidu dusnatého (NO) v corpus cavernosum během sexuální stimulace. Oxid dusnatý aktivuje enzym guanylátcyklázu, výsledkem jsou zvýšené hladiny cyklického guanosinmonofosfátu (cGMP), vedoucí k uvolnění hladkého svalstva v corpus cavernosum, což umožní přítok krve.
Sildenafil je účinný a selektivní inhibitor cGMP specifické fosfodiesterázy typu 5 (PDE5) v corpus cavernosum, kde je PDE5 zodpovědná za degradaci cGMP. Sildenafil má periferní místo účinku na erekci. Sildenafil nemá žádný přímý relaxační účinek na izolované lidské corpus cavernosum, avšak významně zesiluje relaxační účinek NO na tuto tkáň. Při aktivaci dráhy NO/cGMP, k níž při sexuální stimulaci dochází, má inhibice PDE5 sildenafilem za následek zvýšení hladin cGMP v corpus cavernosum. Proto je k zajištění zamýšleného příznivého farmakologického účinku sildenafilu nutná sexuální stimulace.
Farmakodynamické účinky
Studie in vitro prokázaly, že sildenafil je selektivní k PDE5, která se účastní procesu erekce. Jeho účinek je mnohem silnější na PDE5 než na jiné známé izoformy fosfodiesterázy. Má také 10x vyšší selektivitu k PDE5 než k PDE6, která se účastní na kaskádě převodu světla v sítnici. Při maximálních doporučených dávkách má 80x vyšší selektivitu k PDE5 než k PDE1 a více než 700x vyšší selektivitu k PDE5 než PDE2, 3, 4, 7, 8, 9, 10 a 11. Sildenafil má především vyšší (více než 4000x) selektivitu k PDE5 oproti PDE3, což je cAMP-specifická izoforma fosfodiesterázy účastnící se kontroly srdeční kontraktility.
Klinická účinnost a bezpečnost
Pro zhodnocení doby nutné k dosažení erekce při adekvátní sexuální stimulaci byly provedeny dvě klinické studie. Ve studii s penilní plethysmografií (RigiScan) u pacientů na lačno byla po užití sildenafilu střední doba pro dosažení erekce o 60% rigiditě (dostatečné pro pohlavní styk) 25 min. (rozmezí 12-37 min.). V další RigiScan studii byl sildenafil schopen umožnit erekci v odpověď na sexuální stimulaci ještě 4-5 hodin po užití dávky.
Sildenafil působí mírné a přechodné snížení krevního tlaku, které ve většině případů nemá žádný klinický efekt. Po perorální dávce 100 mg per os sildenafilu bylo průměrné maximální snížení krevního tlaku vleže 8,4 mm Hg. Odpovídající změna diastolického krevního tlaku vleže byla
5,5 mm Hg. Toto snížení krevního tlaku je ve shodě s vazodilatačním účinkem sildenafilu, pravděpodobně následkem zvýšených hladin cGMP v cévní hladké svalovině. Jednotlivé dávky sildenafilu až do 100 mg perorálně neměly žádný klinicky významný účinek na EKG u zdravých dobrovolníků.
Ve studii sledující hemodynamické účinky jednorázové perorální dávky sildenafilu 100 mg u 14 pacientů s těžkou formou ischemické choroby srdeční (ICHS) (stenóza větší než 70% minimálně na jedné koronární tepně) došlo k průměrnému poklesu systolického krevního tlaku v klidu o 7 % a diastolického krevního tlaku o 6 % oproti výchozím hodnotám. Průměrný plicní systolický tlak poklesl o 9 %. Sildenafil neměl žádný účinek na minutový objem a nezhoršoval průtok krve stenotickými koronárními tepnami.
Dvojitě zaslepená, placebem kontrolovaná studie hodnotila odpověď na tělesnou zátěž u 144 pacientů s erektilní dysfunkcí a chronickou stabilní anginou pectoris, kteří pravidelně dostávali antianginózní léčivé přípravky (kromě nitrátů). Výsledky neprokázaly žádné klinicky významné rozdíly v době do vzniku stenokardií znemožňujících další zátěž.
U některých jedinců byly 1 hodinu po podání dávky 100 mg pomocí Farnsworthova-Munsellova testu se 100 odstíny barev zjištěny mírné a přechodné změny v rozlišování barev (modrá/zelená), přičemž 2 hodiny po podání již nebyly žádné účinky pozorovatelné. Předpokládaný mechanismus této změny v rozlišování barev souvisí s inhibicí PDE6, která se podílí na kaskádě převodu světla na sítnici. Sildenafil nemá žádný vliv na ostrost zraku ani na citlivost na kontrast. V malé placebem kontrolované studii u pacientů s prokázanou věkem podmíněnou makulární degenerací (n=9) nebyly po sildenafilu (jednorázová dávka, 100 mg) prokázány žádné signifikantní změny při provedených očních vyšetřeních (zraková ostrost, Amslerova mřížka, test rozlišení barev simulující světla na semaforu, Humphreyův perimetr a fotostres).
U zdravých dobrovolníků neměla dávka 100 mg perorálně žádný účinek na motilitu nebo morfologii spermatu (viz bod 4.6).
Další informace o klinických studiích
V klinických studiích byl sildenafil podán více než 8000 nemocným ve věku 19-87 let. Byly zastoupeny následující skupiny nemocných: starší nemocní (19,9 %), nemocní s hypertenzí (30,9 %), diabetici (20,3 %), s ischemickou chorobou srdeční (5,8 %), s hyperlipidemií (19,8 %), poraněním míchy (0,6 %), depresí (5,2 %), nemocní po transuretrální resekci prostaty (3,7 %), radikální prostatektomií (3,3 %). Následující skupiny byly buď vyloučeny z klinických studií, nebo nebyly dostatečně zastoupeny: nemocní po operaci v malé pánvi, po radioterapii, nemocní se závažnou ledvinovou nebo jaterní poruchou a nemocní s některými kardiovaskulárními potížemi (viz bod 4.3).
Ve studiích s fixní dávkou uvádělo zlepšení erekce díky léčbě 62 % pacientů s dávkou 25 mg, 74 % s dávkou 50 mg a 82 % s dávkou 100 mg, a to ve srovnání s 25 % při použití placeba.
V kontrolovaných klinických studiích byl počet nemocných užívajících sildenafil, kteří odstoupili ze studie, nízký a srovnatelný s placebem.
Ve všech studiích byl podíl nemocných uvádějících zlepšení při léčbě sildenafilem následující: erektilní dysfunkce (ED) psychogenního původu (84 %), smíšené ED (77 %), organické ED (68 %), starší nemocní (67 %), diabetici (59 %), ICHS (69 %), hypertenze (68 %), TURP (61 %), radikální prostatektomie (43 %), poranění míchy (83 %), deprese (75 %). V dlouhodobých studiích přetrvávala bezpečnost a účinnost sildenafilu.
5.2 Farmakokinetické vlastnosti
Absorpce
Sildenafil se rychle vstřebává. Maximálních pozorovaných plazmatických koncentrací se dosahuje za 30-120 minut (průměr 60 minut) po podání perorální dávky ve stavu na lačno. Průměrná absolutní biologická dostupnost po perorální dávce je 41 % (rozmezí 25-63 %). Po perorálním podání dávky sildenafilu se hodnoty AUC a Cmax zvyšují úměrně s dávkou v celém rozsahu doporučených dávek (25-100 mg).
Při podání sildenafilu spolu s jídlem se rychlost absorpce snižuje s průměrným zpožděním Tmax o 60 minut a průměrným snížením Cmax o 29 %.
Distribuce
Průměrný distribuční objem při ustáleném stavu (Vss) sildenafilu je 105 l, což naznačuje distribuci do tkání. Po jednorázově podané perorální dávce 100 mg činí průměrná hodnota maximální celkové plazmatické koncentrace sildenafilu přibližně 440 ng/ml (CV 40 %). Protože sildenafil a jeho hlavní cirkulující metabolit N-desmetyl se váží na plazmatické proteiny z 96 %, má to za následek průměrnou hodnotu maximální plazmatické koncentrace volného sildenafilu 18 ng/ml (38 nM). Vazba na proteiny nezávisí na celkové koncentraci léku.
U zdravých dobrovolníků, jimž byl podán sildenafil (jednorázová dávka 100 mg) bylo v ejakulátu 90 minut po podání dávky přítomno méně než 0,0002 % (průměr 188 ng) podané dávky.
Biotransformace
Sildenafil se vylučuje převážně pomocí jaterních mikrosomálních isoenzymů CYP3A4 (hlavní cesta) a CYP2C9 (vedlejší cesta). Hlavní cirkulující metabolit je výsledkem N-demetylace sildenafilu. Tento metabolit vykazuje profil selektivity vůči fosfodiesteráze podobný profilu sildenafilu a in vitro potenci vůči PDE5 ve výši přibližně 50 % mateřské látky. Plazmatické koncentrace tohoto metabolitu dosahují přibližně 40 % hodnot zjištěných u sildenafilu. Metabolit N-desmetyl se dále biotransformuje, s terminálním poločasem přibližně 4 hodin.
Eliminace
Celková clearance sildenafilu z organismu je 41 l/hod. s výsledným terminálním poločasem 3-5 hod. Po perorálním nebo intravenózním podání se sildenafil vylučuje ve formě metabolitů převážně stolicí (přibližně 80 % perorálně podané dávky) a v menší míře močí (přibližně 13 % perorálně podané dávky).
Farmakokinetické vlastnosti u speciálních skupin pacientů Starší pacienti:
Zdraví starší pacienti (65 let a více) vykazovali sníženou clearance sildenafilu, výsledkem byla přibližně o 90 % vyšší plazmatická koncentrace sildenafilu a účinného N-desmetyl metabolitu ve srovnání se zdravými mladými dobrovolníky (18-45 let). Vzhledem k rozdílu vazby na bílkoviny plazmy závislém na věku byl odpovídající vzestup volné plazmatické koncentrace sildenafilu přibližně 40 %.
Renální nedostatečnost:
U dobrovolníků s mírnou až středně těžkou poruchou renální funkce (clearance kreatininu = 3080 ml/min) nebyla farmakokinetika sildenafilu po podání jednorázové dávky 50 mg změněna. Střední AUC a Cmax N-desmetyl metabolitu vzrostla až o 126 %, resp. 73 % ve srovnání s hodnotami věkově srovnatelných dobrovolníků bez poruchy renální funkce. Tyto odlišnosti ale nebyly vzhledem k vysoké mezisubjektové variabilitě statisticky signifikantní. U dobrovolníků se závažnou ledvinnou poruchou (clearance kreatininu < 30 ml/min) byla snížena clearance sildenafilu. To mělo za následek vzestup AUC a Cmax o 100 %, resp. 88 % ve srovnání se stejně starými dobrovolníky bez renální poruchy. Navíc došlo k podstatnému zvýšení hodnot AUC a Cmax o 200 %, resp. 79 % pro N-desmetyl metabolit.
Jaterní nedostatečnost:
U dobrovolníků s mírnou až středně těžkou cirhózou jater (Child-Pugh klasifikace A a B) byla clearance sildenafilu snížena, což vedlo ke zvýšení hodnot AUC (o 84 %) a Cmax (o 47 %) ve srovnání s hodnotami věkově srovnatelných dobrovolníků bez poruchy funkce jater. Farmakokinetika sildenafilu u nemocných se závažnou jaterní poruchou nebyla studována.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity, hodnocení kancerogenního potenciálu, reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Hyprolosa (E463)
Mannitol (E421)
Aspartam (E951)
Neohesperidin-dihydrochalkon (E959)
Silice máty kadeřavé
Silice máty peprné (obsahuje sorbitol (E420))
Krospovidon Křemičitan vápenatý Magnesium-stearát (E572)
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
2 roky
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
6.5 Druh obalu a obsah balení
Vizarsin 25 mg tablety dispergovatelné v ústech
Blistr (odlupovací blistr, orientovaný polyamid/aluminium/PVC//PET/aluminium): 1 tableta dispergovatelná v ústech, v krabičce.
Blistr (odlupovací perforovaný jednodávkový blistr, orientovaný
polyamid/aluminium/PVC//PET/aluminium): 2 x 1, 4 x 1, 8 x 1 nebo 12 x 1 tableta dispergovatelná v ústech, v krabičce.
Vizarsin 50 mg, 100 mg tablety dispergovatelné v ústech
Blistr (odlupovací blistr, orientovaný polyamid/aluminium/PVC//PET/aluminium): 1 tableta dispergovatelná v ústech, v krabičce.
Blistr (odlupovací perforovaný jednodávkový blistr, orientovaný
polyamid/aluminium/PVC//PET/aluminium): 2 x 1, 4 x 1, 8 x 1, 12 x 1 nebo 24 x 1 tableta dispergovatelná v ústech, v krabičce.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Smaiješka cesta 6, 8501 Novo mesto, Slovinsko
8. REGISTRAČNÍ ČÍSLO(A)
Vizarsin 25 mg tablety dispergovatelné v ústech
1 tableta dispergovatelná v ústech: EU/1/09/551/013
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/014 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/015 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/016 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/017
Vizarsin 50 mg tablety dispergovatelné v ústech
1 tableta dispergovatelná v ústech: EU/1/09/551/018
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/019 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/020 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/021 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/022 24 x 1 tableta dispergovatelná v ústech: EU/1/09/551/028
Vizarsin 100 mg tablety dispergovatelné v ústech
1 tableta dispergovatelná v ústech: EU/1/09/551/023
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/024 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/025 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/026 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/027 24 x 1 tableta dispergovatelná v ústech: EU/1/09/551/029
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 21. září 2009
Datum posledního prodloužení registrace: 16. května 2014
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
A. VÝROBCE ODPOVĚDNÝ/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE ODPOVĚDNÝ/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobců odpovědných za propouštění šarží
KRKA, d.d., Novo mesto Šmarješka cesta 6 8501 Novo mesto Slovinsko
TAD Pharma GmbH Heinz-Lohmann-StraBe 5 27472 Cuxhaven Německo
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propouštění dané šarže.
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Neuplatňuje se.
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 25 mg potahované tablety Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 25 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje laktosu.
Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 potahovaná tableta 4 x 1 potahovaná tableta 8 x 1 potahovaná tableta 12 x 1 potahovaná tableta
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ CÍSLO/CÍSLA
1 potahovaná tableta: EU/1/09/551/001 4 x 1 potahovaná tableta: EU/1/09/551/002 8 x 1 potahovaná tableta: EU/1/09/551/003 12 x 1 potahovaná tableta: EU/1/09/551/004
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOVE PÍSMU vizarsin 25 mg
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 25 mg potahované tablety Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Lot:
5. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 50 mg potahované tablety Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 50 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje laktosu.
Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 potahovaná tableta 4 x 1 potahovaná tableta 8 x 1 potahovaná tableta 12 x 1 potahovaná tableta
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ CÍSLO/CÍSLA
1 potahovaná tableta: EU/1/09/551/005 4 x 1 potahovaná tableta: EU/1/09/551/006 8 x 1 potahovaná tableta: EU/1/09/551/007 12 x 1 potahovaná tableta: EU/1/09/551/008
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOVE PÍSMU vizarsin 50 mg
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 50 mg potahované tablety Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Lot:
5. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 100 mg potahované tablety Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 100 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje laktosu.
Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 potahovaná tableta 4 x 1 potahovaná tableta 8 x 1 potahovaná tableta 12 x 1 potahovaná tableta
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ CÍSLO/CÍSLA

13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ 16. INFORMACE V BRAILLOVE PÍSMU vizarsin 100 mg
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 100 mg potahované tablety Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Lot:
5. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 25 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje aspartam (E951) a silici máty peprné (sorbitol (E420)). Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 tableta dispergovatelná v ústech
2 x 1 tableta dispergovatelná v ústech 4 x 1 tableta dispergovatelná v ústech 8 x 1 tableta dispergovatelná v ústech 12 x 1 tableta dispergovatelná v ústech
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání. Nechte tabletu rozpustit v ústech.
1 tableta v blistru:
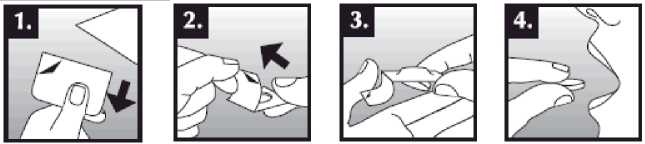
4 tablety v blistru:
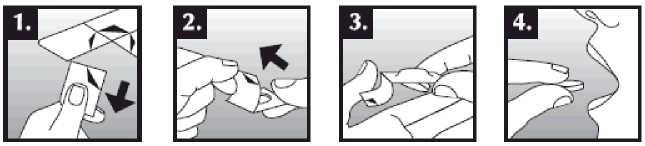
1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně.
4. Jakmile vyjmete tabletu z obalu, položte ji na jazyk.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
1 tableta dispergovatelná v ústech: EU/1/09/551/013
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/014 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/015 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/016 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/017
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
vizarsin 25 mg tablety dispergovatelné v ústech
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR pro jednojazyčné a dvojjazyčné balení_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Lot:
5. JINÉ
1. OHNĚTE A ODTRHNĚTE
2. SLOUPNĚTE
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 50 mg tablety dispergovatelné v ústech Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 50 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje aspartam (E951) a silici máty peprné (sorbitol (E420)). Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 tableta dispergovatelná v ústech
2 x 1 tableta dispergovatelná v ústech 4 x 1 tableta dispergovatelná v ústech 8 x 1 tableta dispergovatelná v ústech 12 x 1 tableta dispergovatelná v ústech 24 x 1 tableta dispergovatelná v ústech
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání. Nechte tabletu rozpustit v ústech.
1 tableta v blistru:
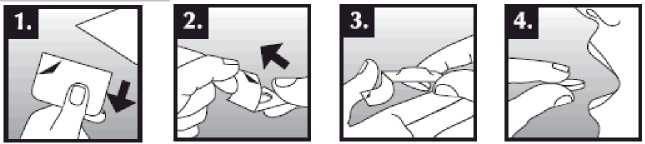
4 tablety v blistru:
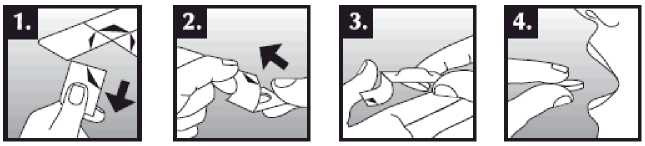
1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
1 tableta dispergovatelná v ústech: EU/1/09/551/018
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/019 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/020 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/021 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/022 24 x 1 tableta dispergovatelná v ústech: EU/1/09/551/028
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR pro jednojazyčné a dvojjazyčné balení_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 50 mg tablety dispergovatelné v ústech Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Lot:
5. JINÉ
1. OHNĚTE A ODTRHNĚTE
2. SLOUPNĚTE
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 100 mg tablety dispergovatelné v ústech Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 100 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje aspartam (E951) a silici máty peprné (sorbitol (E420)). Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 tableta dispergovatelná v ústech
2 x 1 tableta dispergovatelná v ústech 4 x 1 tableta dispergovatelná v ústech 8 x 1 tableta dispergovatelná v ústech 12 x 1 tableta dispergovatelná v ústech 24 x 1 tableta dispergovatelná v ústech
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání. Nechte tabletu rozpustit v ústech.
1 tableta v blistru:
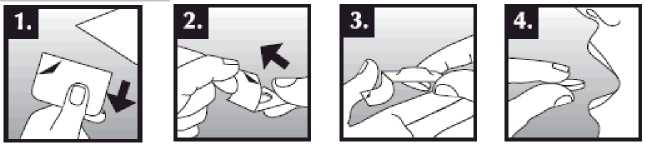
4 tablety v blistru:
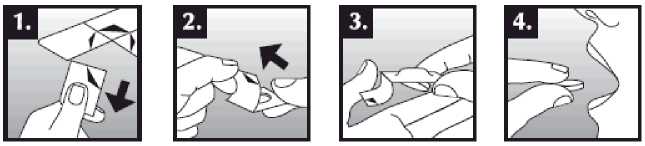
1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
1 tableta dispergovatelná v ústech: EU/1/09/551/023
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/024 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/025 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/026 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/027 24 x 1 tableta dispergovatelná v ústech: EU/1/09/551/029
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR pro jednojazyčné a dvojjazyčné balení_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 100 mg tablety dispergovatelné v ústech Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Lot:
5. JINÉ
1. OHNĚTE A ODTRHNĚTE
2. SLOUPNĚTE
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 25 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje aspartam (E951) a silici máty peprné (sorbitol (E420)). Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 tableta dispergovatelná v ústech
2 x 1 tableta dispergovatelná v ústech 4 x 1 tableta dispergovatelná v ústech 8 x 1 tableta dispergovatelná v ústech 12 x 1 tableta dispergovatelná v ústech
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Perorální podání.
1 tableta v blistru:
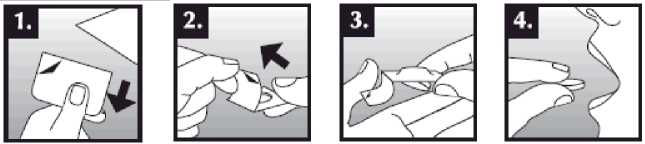
4 tablety v blistru:
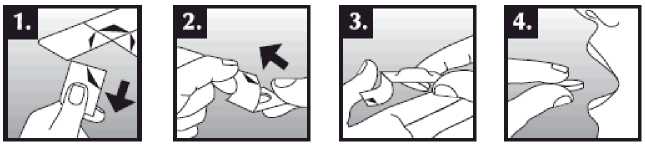
1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně a položte ji na jazyk.
4. Rozpusťte v ústech.
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
1 tableta dispergovatelná v ústech: EU/1/09/551/013
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/014 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/015 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/016 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/017
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR pro trojjazyčné balení_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 25 mg tablety dispergovatelné v ústech Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
|
4. |
ČÍSLO ŠARŽE |
|
Lot: | |
|
5. |
JINÉ |
|
1. |
Odtrhněte |
|
2. |
Sloupněte |
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 50 mg tablety dispergovatelné v ústech Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 50 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje aspartam (E951) a silici máty peprné (sorbitol (E420)). Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 tableta dispergovatelná v ústech
2 x 1 tableta dispergovatelná v ústech 4 x 1 tableta dispergovatelná v ústech 8 x 1 tableta dispergovatelná v ústech 12 x 1 tableta dispergovatelná v ústech 24 x 1 tableta dispergovatelná v ústech
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Perorální podání.
1 tableta v blistru:
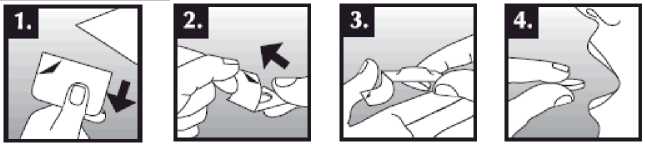
4 tablety v blistru:
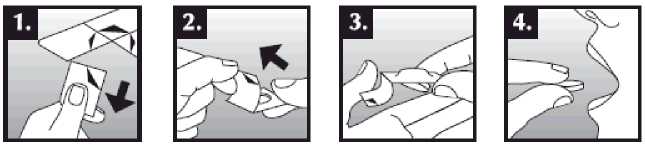
1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně a položte ji na jazyk.
4. Rozpusťte v ústech.
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
1 tableta dispergovatelná v ústech: EU/1/09/551/018
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/019 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/020 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/021 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/022 24 x 1 tableta dispergovatelná v ústech: EU/1/09/551/028
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR pro trojjazyčné balení_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 50 mg tablety dispergovatelné v ústech Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
|
4. |
ČÍSLO ŠARŽE |
|
Lot: | |
|
5. |
JINÉ |
|
1. |
Odtrhněte |
|
2. |
Sloupněte |
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 100 mg tablety dispergovatelné v ústech Sildenafilum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 100 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje aspartam (E951) a silici máty peprné (sorbitol (E420)). Pro další informace si přečtěte příbalovou informaci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 tableta dispergovatelná v ústech
2 x 1 tableta dispergovatelná v ústech 4 x 1 tableta dispergovatelná v ústech 8 x 1 tableta dispergovatelná v ústech 12 x 1 tableta dispergovatelná v ústech 24 x 1 tableta dispergovatelná v ústech
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Perorální podání.
1 tableta v blistru:
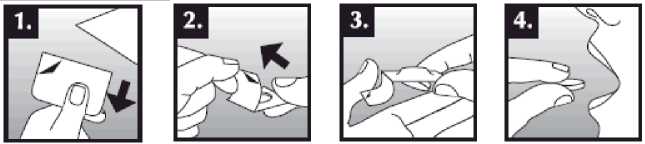
4 tablety v blistru:
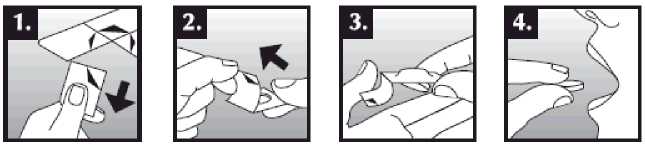
1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně a položte ji na jazyk.
4. Rozpusťte v ústech.
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
1 tableta dispergovatelná v ústech: EU/1/09/551/023
2 x 1 tableta dispergovatelná v ústech: EU/1/09/551/024 4 x 1 tableta dispergovatelná v ústech: EU/1/09/551/025 8 x 1 tableta dispergovatelná v ústech: EU/1/09/551/026 12 x 1 tableta dispergovatelná v ústech: EU/1/09/551/027 24 x 1 tableta dispergovatelná v ústech: EU/1/09/551/029
13. ČÍSLO ŠARŽE
Lot:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH BLISTR pro trojjazyčné balení_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vizarsin 100 mg tablety dispergovatelné v ústech Sildenafilum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
KRKA
3. POUŽITELNOST
EXP:
|
4. |
ČÍSLO ŠARŽE |
|
Lot: | |
|
5. |
JINÉ |
|
1. |
Odtrhněte |
|
2. |
Sloupněte |
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro uživatele
Vizarsin 25 mg potahované tablety
Sildenafilum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Vizarsin a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
3. Jak se přípravek Vizarsin užívá
4. Možné nežádoucí účinky
5. Jak přípravek Vizarsin uchovávat
6. Obsah balení a další informace
1. Co je přípravek Vizarsin a k čemu se používá
Přípravek Vizarsin obsahuje léčivou látku sildenafil, což je lék ze skupiny nazývané inhibitory fosfodiesterázy typu 5 (PDE5). Po jejím užití dochází při odpovídajícím sexuálním vzrušení k uvolnění hladkých svalových vláken kontrolujících přítok krve do penisu, čímž se zvýší přítok krve do tohoto orgánu. Přípravek Vizarsin Vám pomůže navodit erekci jen tehdy, pokud dojde k sexuálnímu dráždění.
Přípravek Vizarsin se používá k léčbě dospělých mužů s poruchami erekce. Tato porucha je také známá pod pojmem impotence. Jedná se o situaci, kdy muž nemůže během sexuálního vzrušení dosáhnout ztopoření penisu nebo je toto ztopoření nedostatečné pro sexuální aktivitu.
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
Neužívejte přípravek Vizarsin:
- jestliže jste alergický na sildenafil nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Informujte svého lékaře, pokud užíváte některý z těchto léků předepisovaný k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu). Nejste-li si jist, zeptejte se svého lékaře nebo lékárníka.
- pokud užíváte léky schopné uvolňovat oxid dusnatý, jako je např. isoamyl-nitrit, protože souběžné užití může také způsobit nebezpečný pokles krevního tlaku.
- jestliže užíváte riocigvát. Tento lék se používá k léčbě plicní arteriální hypertenze (tj. vysokého krevního tlaku v plicích) a chronické tromboembolické plicní hypertenze (tj. vysokého krevního tlaku v plicích sekundárních krevních sraženin). U PDE5 inhibitorů, jako je například přípravek Vizarsin, bylo prokázáno, že zvyšují hypotenzní účinek tohoto léku. Pokud užíváte riocigvát nebo si nejste jisti, informujte svého lékaře.
- pokud máte závažnou srdeční poruchu nebo závažnou poruchu jater.
- pokud jste měl nedávno cévní mozkovou příhodu (mrtvici), srdeční infarkt nebo pokud máte nízký krevní tlak.
- pokud máte vzácnou vrozenou poruchu sítnice (jako např. retinitis pigmentosa).
- pokud jste přišel o zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION).
Upozornění a opatření
Před užitím přípravku Vizarsin se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže:
- trpíte srpkovitou anemií (poruchou červených krvinek), leukemií (nádorové onemocnění bílých krvinek), mnohočetným myelomem (nádorové onemocnění kostní dřeně).
- trpíte deformitou penisu nebo Peyronieovou chorobou.
- máte potíže se srdcem. Váš lékař by měl pečlivě zhodnotit, zda Vaše srdce snese přídatnou zátěž při pohlavním styku.
- máte vředovou chorobu nebo potíže s krvácivostí (např. hemofilii).
- zaznamenáte náhlé zhoršení nebo ztrátu zraku. Přestaňte užívat přípravek Vizarsin a okamžitě vyhledejte svého lékaře.
Současně s přípravkem Vizarsin neužívejte k léčbě poruchy erekce žádný jiný přípravek podávaný ústy nebo místně.
Neužívejte přípravek Vizarsin současně s léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil ani s žádnými jinými inhibitory PDE5.
V případě, že netrpíte poruchou erekce, přípravek Vizarsin neužívejte.
Přípravek Vizarsin není určen pro ženy.
Léčba pacientů s poruchou funkce ledvin nebo jater
Pokud máte poruchu jater nebo ledvin, sdělte tuto skutečnost lékaři. Ten posoudí, zda je nutné dávku přípravku Vizarsin upravit.
Děti a dospívající
Přípravek Vizarsin není určen pro pacienty mladší 18 let.
Další léčivé přípravky a přípravek Vizarsin
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat.
Přípravek Vizarsin může ovlivňovat účinek některých jiných léků, především těch, které jsou určeny k léčení bolesti na hrudníku srdečního původu. V případě náhlých zdravotních problémů byste měl svému lékaři, lékárníkovi nebo zdravotní sestře oznámit, že jste užil přípravek Vizarsin a kdy. Neužívejte přípravek Vizarsin společně s jinými léky, pokud Vám to nedoporučí Váš ošetřující lékař.
Neužívejte přípravek Vizarsin, pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Vždy informujte svého lékaře, lékárníka nebo zdravotní sestru, že užíváte některý z těchto léků předepisovaných k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu).
Neužívejte přípravek Vizarsin, pokud užíváte léky schopné uvolňovat oxid dusnatý, jako např. isoamyl-nitrit („poppers“), protože souběžné užití může způsobit nebezpečný pokles krevního tlaku.
Informujte svého lékaře nebo lékárníka, pokud již užíváte riocigvát.
Pokud užíváte léky, které patří do skupiny inhibitorů proteáz, např. k léčbě HIV, doporučí Vám obvykle Váš lékař přípravek Vizarsin o nejmenší možné síle 25 mg.
Někteří pacienti, užívající alfa-blokátory k léčbě vysokého krevního tlaku nebo zvětšené prostaty, mohou zaznamenat závratě nebo motání hlavy, které může být způsobené nízkým krevním tlakem při rychlém sedání nebo vstávání. Někteří pacienti zaznamenali tyto příznaky při souběžném užití přípravku Vizarsin s alfa-blokátory. Příznaky posturální hypotenze se mohou nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Měl byste pravidelně užívat svou denní dávku alfa-blokátoru, než začnete užívat přípravek Vizarsin, aby se snížila pravděpodobnost nástupu těchto příznaků. Lékař může zahájit Vaši léčbu přípravkem Vizarsin v nižší dávce 25 mg.
Přípravek Vizarsin s jídlem, pitím a alkoholem
Přípravek Vizarsin může být užíván s jídlem i bez jídla. Po požití těžkého jídla se však účinek přípravku Vizarsin může projevit později.
Požití alkoholu může dočasně zhoršit schopnost dosáhnout erekce. Abyste dosáhl co nejvyššího účinku tohoto přípravku, doporučujeme před užitím přípravku Vizarsin nepožívat větší množství alkoholu.
Těhotenství, kojení a plodnost
Přípravek Vizarsin není určen pro použití u žen.
Řízení dopravních prostředků a obsluha strojů
Přípravek Vizarsin může způsobit závratě a narušit vidění. Měl byste proto znát svoji reakci na přípravek Vizarsin před tím, než budete řídit motorová vozidla nebo obsluhovat stroje.
Přípravek Vizarsin obsahuje laktosu
Pokud Vám lékař řekl, že nesnášíte některé cukry, poraďte se s ním, než začnete tento léčivý přípravek užívat.
3. Jak se přípravek Vizarsin užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý, poraďte se se svým lékařem nebo lékárníkem.
Doporučená zahajovací dávka je 50 mg.
Neužívejte více než jednu tabletu přípravku Vizarsin denně.
Užijte přípravek Vizarsin zhruba jednu hodinu před plánovaným pohlavním stykem. Tabletu spolkněte celou a zapijte ji sklenicí vody.
Jestliže cítíte, že přípravek Vizarsin účinkuje příliš silně nebo naopak slabě, sdělte to svému lékaři nebo lékárníkovi.
Přípravek Vizarsin Vám pomůže dosáhnout erekce, jen pokud dojde k sexuálnímu dráždění. Doba, po které začne přípravek účinkovat, je u každého člověka odlišná, ale obvykle se pohybuje mezi půl hodinou až hodinou. Pokud přípravek Vizarsin užijete společně s těžkým jídlem, může se nástup účinku oddálit.
Pokud po užití přípravku Vizarsin nedosáhnete erekce nebo je erekce nedostatečná pro celý pohlavní
styk, poraďte se o dalším postupu se svým lékařem.
Jestliže jste užil více přípravku Vizarsin, než jste měl
Můžete zaznamenat zvýšený výskyt nežádoucích účinků a jejich závažnosti. Dávka vyšší než 100 mg nezlepšuje dále účinnost.
Neužívejte více tablet, než Vám bylo lékařem doporučeno.
Vyhledejte svého lékaře, pokud užijete více tablet, než jste měl.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Nežádoucí účinky hlášené v souvislosti s užitím přípravku Vizarsin bývají obvykle mírné až středně závažné a krátkého trvání.
Pokud se u Vás vyskytl některý z následujících nežádoucích účinků, přestaňte přípravek Vizarsin užívat a okamžitě vyhledejte lékařskou pomoc:
- Alergická reakce - k té dochází méně často (může postihnout až 1 ze 100 pacientů)
Příznaky zahrnují náhlou dýchavičnost, potíže s dýcháním nebo závrať, otok očních víček, obličeje, rtů nebo hrdla.
- Bolest na hrudníku - k té dochází méně často
Pokud se objeví v průběhu nebo po skončení pohlavního styku:
- posaďte se do polosedu a snažte se odpočívat.
- neužívejte na léčbu bolesti na hrudníku nitráty.
- Prodloužená a občas bolestivá erekce - k té dochází vzácně (může postihnout až 1 z 1000 pacientů)
Pokud u Vás dojde k erekci, která trvá déle než 4 hodiny, okamžitě vyhledejte lékaře.
- Náhlé zhoršení nebo ztráta zraku - k tomu dochází vzácně
- Těžké kožní reakce - k těm dochází vzácně
Příznaky mohou zahrnovat silné olupování a otok kůže, tvorbu puchýřů v ústech, na genitálu a kolem očí, horečku.
- Křečové stavy nebo záchvaty - k těm dochází vzácně Další nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 pacientů): bolest hlavy.
Časté (mohou postihnout až 1 z 10 pacientů): nevolnost, zarudnutí v obličeji, nával horka (příznaky zahrnují náhlý pocit horka v horní části těla), zažívací potíže, změny barevného vidění, rozmazané vidění, poruchy vidění, ucpaný nos a závrať.
Méně časté (mohou postihnout až 1 ze 100 pacientů): zvracení, kožní vyrážka, podráždění oka, překrvené/červené oči, bolest očí, vidění záblesků světla, zrakový vjem jasu, citlivost na světlo, slzení očí, bušení srdce, zrychlený srdeční puls, vysoký krevní tlak, nízký krevní tlak, bolest svalů, ospalost, snížená citlivost na dotek, porucha rovnováhy, zvonění v uších, sucho v ústech, ucpané vedlejší dutiny nosní, zánět nosní sliznice (příznaky zahrnují rýmu, kýchání a ucpaný nos), bolest horní poloviny břicha, refluxní choroba jícnu (příznaky zahrnují pálení žáhy), přítomnost krve v moči, bolest paží nebo nohou, krvácení z nosu, pocit horka a únava.
Vzácné (mohou postihnout až 1 z 1000 pacientů): mdloby, cévní mozková příhoda, srdeční infarkt, nepravidelný srdeční puls, dočasné snížení průtoku krve některými částmi mozku, stažení hrdla, znecitlivěná ústa, krvácení na očním pozadí, dvojité vidění, snížená zraková ostrost, neobvyklý pocit v oku, otok oka nebo očního víčka, malé částice nebo tečky ve vidění, vidění světelných kruhů kolem světel, rozšíření zornice, změna zabarvení očního bělma, krvácení z penisu, přítomnost krve ve spermatu, suchost v nose, zduření uvnitř nosu, pocit podrážděnosti a náhlé zhoršení nebo ztráta sluchu.
Po uvedení přípravku na trh byly vzácně hlášeny případy nestabilní anginy pectoris (onemocnění srdce) a náhlé smrti. Je třeba poznamenat, že většina mužů, ale ne všichni, kteří měli tyto nežádoucí účinky, měla potíže se srdcem již před užitím přípravku. Není možné určit, zda tyto příhody měly přímou souvislost s užitím přípravku Vizarsin.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Vizarsin uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za „EXP:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Vizarsin obsahuje
- Léčivou látkou je sildenafilum. Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 25 mg.
- Pomocnými látkami jsou:
Jádro tablety: mikrokrystalická celulosa (E460), hydrogenfosforečnan vápenatý, sodná sůl
kroskarmelosy, hypromelosa (E464), magnesium-stearát (E572).
Potah tablety: monohydrát laktosy, hypromelosa (E464), oxid titaničitý (E171), triacetin (E1518).
Jak přípravek Vizarsin vypadá a co obsahuje toto balení
Potahované tablety Vizarsin 25 mg jsou bílé, podlouhlé a s označením „25“ na jedné straně.
Vizarsin 25 mg potahované tablety se dodávají v krabičkách po 1 potahované tabletě v blistrech a také v krabičkách po 4 x 1, 8 x 1 nebo 12 x 1 potahované tabletě v perforovaných blistrech pro jednotlivé dávky.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
|
Belgie/Belgique/Belgien KRKA Belgium, SA. Tél/Tel: +32 (0) 489 304 091 |
Lietuva UAB KRKA Lietuva Tel: + 370 5 236 27 40 |
|
Btarapna KPKA Etarapna EOOfl Ten.: + 359 (02) 962 34 50 |
Luxembourg/Luxemburg KRKA Belgium, SA. Tél/Tel: +32 (0) 489 304 091 (BE) |
|
Česká republika KRKA ČR, s.r.o. Tel: + 420 (0) 221 115 150 |
Magyarország KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490 |
|
Danmark KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
Malta E. J. Busuttil Ltd. Tel: + 356 21 445 885 |
|
Deutschland TAD Pharma GmbH Tel: + 49 (0) 4721 606-0 |
Nederland KRKA Belgium, SA. Tel: +32 (0) 489 304 091 (BE) |
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. T^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
Espaňa KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmaceutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Románia KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq |
Sverige |
KRKA Sverige AB
Kipa Pharmacal Ltd. T^: + 357 24 651 882
Latvija
KRKA Latvija SIA Tel: + 371 6 733 86 10
Tel: + 46 (0)8 643 67 66 (SE)
United Kingdom
Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888
Tato příbalová informace byla naposledy revidována
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Příbalová informace: informace pro uživatele
Vizarsin 50 mg potahované tablety
Sildenafilum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Vizarsin a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
3. Jak se přípravek Vizarsin užívá
4. Možné nežádoucí účinky
5. Jak přípravek Vizarsin uchovávat
6. Obsah balení a další informace
1. Co je přípravek Vizarsin a k čemu se používá
Přípravek Vizarsin obsahuje léčivou látku sildenafil, což je lék ze skupiny nazývané inhibitory fosfodiesterázy typu 5 (PDE5). Po jejím užití dochází při odpovídajícím sexuálním vzrušení k uvolnění hladkých svalových vláken kontrolujících přítok krve do penisu, čímž se zvýší přítok krve do tohoto orgánu. Přípravek Vizarsin Vám pomůže navodit erekci jen tehdy, pokud dojde k sexuálnímu dráždění.
Přípravek Vizarsin se používá k léčbě dospělých mužů s poruchami erekce. Tato porucha je také známá pod pojmem impotence. Jedná se o situaci, kdy muž nemůže během sexuálního vzrušení dosáhnout ztopoření penisu nebo je toto ztopoření nedostatečné pro sexuální aktivitu.
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
Neužívejte přípravek Vizarsin:
- jestliže jste alergický na sildenafil nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Informujte svého lékaře, pokud užíváte některý z těchto léků předepisovaný k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu). Nejste-li si jist, zeptejte se svého lékaře nebo lékárníka.
- pokud užíváte léky schopné uvolňovat oxid dusnatý, jako je např. isoamyl-nitrit, protože souběžné užití může také způsobit nebezpečný pokles krevního tlaku.
- jestliže užíváte riocigvát. Tento lék se používá k léčbě plicní arteriální hypertenze (tj. vysokého krevního tlaku v plicích) a chronické tromboembolické plicní hypertenze (tj. vysokého krevního tlaku v plicích sekundárních krevních sraženin). U PDE5 inhibitorů, jako je například přípravek Vizarsin, bylo prokázáno, že zvyšují hypotenzní účinek tohoto léku. Pokud užíváte riocigvát nebo si nejste jisti, informujte svého lékaře.
- pokud máte závažnou srdeční poruchu nebo závažnou poruchu jater.
- pokud jste měl nedávno cévní mozkovou příhodu (mrtvici), srdeční infarkt nebo pokud máte nízký krevní tlak.
- pokud máte vzácnou vrozenou poruchu sítnice (jako např. retinitis pigmentosa).
- pokud jste přišel o zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION).
Upozornění a opatření
Před užitím přípravku Vizarsin se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže:
- trpíte srpkovitou anemií (poruchou červených krvinek), leukemií (nádorové onemocnění bílých krvinek), mnohočetným myelomem (nádorové onemocnění kostní dřeně).
- trpíte deformitou penisu nebo Peyronieovou chorobou.
- máte potíže se srdcem. Váš lékař by měl pečlivě zhodnotit, zda Vaše srdce snese přídatnou zátěž při pohlavním styku.
- máte vředovou chorobu nebo potíže s krvácivostí (např. hemofilii).
- zaznamenáte náhlé zhoršení nebo ztrátu zraku. Přestaňte užívat přípravek Vizarsin a okamžitě vyhledejte svého lékaře.
Současně s přípravkem Vizarsin neužívejte k léčbě poruchy erekce žádný jiný přípravek podávaný ústy nebo místně.
Neužívejte přípravek Vizarsin současně s léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil ani s žádnými jinými inhibitory PDE5.
V případě, že netrpíte poruchou erekce, přípravek Vizarsin neužívejte.
Přípravek Vizarsin není určen pro ženy.
Léčba pacientů s poruchou funkce ledvin nebo jater
Pokud máte poruchu jater nebo ledvin, sdělte tuto skutečnost lékaři. Ten posoudí, zda je nutné dávku přípravku Vizarsin upravit.
Děti a dospívající
Přípravek Vizarsin není určen pro pacienty mladší 18 let.
Další léčivé přípravky a přípravek Vizarsin
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat.
Přípravek Vizarsin může ovlivňovat účinek některých jiných léků, především těch, které jsou určeny k léčení bolesti na hrudníku srdečního původu. V případě náhlých zdravotních problémů byste měl svému lékaři, lékárníkovi nebo zdravotní sestře oznámit, že jste užil přípravek Vizarsin a kdy. Neužívejte přípravek Vizarsin společně s jinými léky, pokud Vám to nedoporučí Váš ošetřující lékař.
Neužívejte přípravek Vizarsin, pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Vždy informujte svého lékaře, lékárníka nebo zdravotní sestru, že užíváte některý z těchto léků předepisovaných k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu).
Neužívejte přípravek Vizarsin, pokud užíváte léky schopné uvolňovat oxid dusnatý, jako např. isoamyl-nitrit („poppers“), protože souběžné užití může způsobit nebezpečný pokles krevního tlaku.
Informujte svého lékaře nebo lékárníka, pokud již užíváte riocigvát.
Pokud užíváte léky, které patří do skupiny inhibitorů proteáz, např. k léčbě HIV, doporučí Vám obvykle Váš lékař přípravek Vizarsin o nejmenší možné síle 25 mg.
Někteří pacienti, užívající alfa-blokátory k léčbě vysokého krevního tlaku nebo zvětšené prostaty, mohou zaznamenat závratě nebo motání hlavy, které může být způsobené nízkým krevním tlakem při rychlém sedání nebo vstávání. Někteří pacienti zaznamenali tyto příznaky při souběžném užití přípravku Vizarsin s alfa-blokátory. Příznaky posturální hypotenze se mohou nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Měl byste pravidelně užívat svou denní dávku alfa-blokátoru, než začnete užívat přípravek Vizarsin, aby se snížila pravděpodobnost nástupu těchto příznaků. Lékař může zahájit Vaši léčbu přípravkem Vizarsin v nižší dávce 25 mg.
Přípravek Vizarsin s jídlem, pitím a alkoholem
Přípravek Vizarsin může být užíván s jídlem i bez jídla. Po požití těžkého jídla se však účinek přípravku Vizarsin může projevit později.
Požití alkoholu může dočasně zhoršit schopnost dosáhnout erekce. Abyste dosáhl co nejvyššího účinku tohoto přípravku, doporučujeme před užitím přípravku Vizarsin nepožívat větší množství alkoholu.
Těhotenství, kojení a plodnost
Přípravek Vizarsin není určen pro použití u žen.
Řízení dopravních prostředků a obsluha strojů
Přípravek Vizarsin může způsobit závratě a narušit vidění. Měl byste proto znát svoji reakci na přípravek Vizarsin před tím, než budete řídit motorová vozidla nebo obsluhovat stroje.
Přípravek Vizarsin obsahuje laktosu
Pokud Vám lékař řekl, že nesnášíte některé cukry, poraďte se s ním, než začnete tento léčivý přípravek užívat.
3. Jak se přípravek Vizarsin užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý, poraďte se se svým lékařem nebo lékárníkem.
Doporučená zahajovací dávka je 50 mg.
Neužívejte více než jednu tabletu přípravku Vizarsin denně.
Užijte přípravek Vizarsin zhruba jednu hodinu před plánovaným pohlavním stykem. Tabletu spolkněte celou a zapijte ji sklenicí vody.
Jestliže cítíte, že přípravek Vizarsin účinkuje příliš silně nebo naopak slabě, sdělte to svému lékaři nebo lékárníkovi.
Přípravek Vizarsin Vám pomůže dosáhnout erekce, jen pokud dojde k sexuálnímu dráždění. Doba, po které začne přípravek účinkovat, je u každého člověka odlišná, ale obvykle se pohybuje mezi půl hodinou až hodinou. Pokud přípravek Vizarsin užijete společně s těžkým jídlem, může se nástup účinku oddálit.
Pokud po užití přípravku Vizarsin nedosáhnete erekce nebo je erekce nedostatečná pro celý pohlavní
styk, poraďte se o dalším postupu se svým lékařem.
Jestliže jste užil více přípravku Vizarsin, než jste měl
Můžete zaznamenat zvýšený výskyt nežádoucích účinků a jejich závažnosti. Dávka vyšší než 100 mg nezlepšuje dále účinnost.
Neužívejte více tablet, než Vám bylo lékařem doporučeno.
Vyhledejte svého lékaře, pokud užijete více tablet, než jste měl.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Nežádoucí účinky hlášené v souvislosti s užitím přípravku Vizarsin bývají obvykle mírné až středně závažné a krátkého trvání.
Pokud se u Vás vyskytl některý z následujících nežádoucích účinků, přestaňte přípravek Vizarsin užívat a okamžitě vyhledejte lékařskou pomoc:
- Alergická reakce - k té dochází méně často (může postihnout až 1 ze 100 pacientů)
Příznaky zahrnují náhlou dýchavičnost, potíže s dýcháním nebo závrať, otok očních víček, obličeje, rtů nebo hrdla.
- Bolest na hrudníku - k té dochází méně často
Pokud se objeví v průběhu nebo po skončení pohlavního styku:
- posaďte se do polosedu a snažte se odpočívat.
- neužívejte na léčbu bolesti na hrudníku nitráty.
- Prodloužená a občas bolestivá erekce - k té dochází vzácně (může postihnout až 1 z 1000 pacientů)
Pokud u Vás dojde k erekci, která trvá déle než 4 hodiny, okamžitě vyhledejte lékaře.
- Náhlé zhoršení nebo ztráta zraku - k tomu dochází vzácně
- Těžké kožní reakce - k těm dochází vzácně
Příznaky mohou zahrnovat silné olupování a otok kůže, tvorbu puchýřů v ústech, na genitálu a kolem očí, horečku.
- Křečové stavy nebo záchvaty - k těm dochází vzácně Další nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 pacientů): bolest hlavy.
Časté (mohou postihnout až 1 z 10 pacientů): nevolnost, zarudnutí v obličeji, nával horka (příznaky zahrnují náhlý pocit horka v horní části těla), zažívací potíže, změny barevného vidění, rozmazané vidění, poruchy vidění, ucpaný nos a závrať.
Méně časté (mohou postihnout až 1 ze 100 pacientů): zvracení, kožní vyrážka, podráždění oka, překrvené/červené oči, bolest očí, vidění záblesků světla, zrakový vjem jasu, citlivost na světlo, slzení očí, bušení srdce, zrychlený srdeční puls, vysoký krevní tlak, nízký krevní tlak, bolest svalů, ospalost, snížená citlivost na dotek, porucha rovnováhy, zvonění v uších, sucho v ústech, ucpané vedlejší dutiny nosní, zánět nosní sliznice (příznaky zahrnují rýmu, kýchání a ucpaný nos), bolest horní poloviny břicha, refluxní choroba jícnu (příznaky zahrnují pálení žáhy), přítomnost krve v moči, bolest paží nebo nohou, krvácení z nosu, pocit horka a únava.
Vzácné (mohou postihnout až 1 z 1000 pacientů): mdloby, cévní mozková příhoda, srdeční infarkt, nepravidelný srdeční puls, dočasné snížení průtoku krve některými částmi mozku, stažení hrdla, znecitlivěná ústa, krvácení na očním pozadí, dvojité vidění, snížená zraková ostrost, neobvyklý pocit v oku, otok oka nebo očního víčka, malé částice nebo tečky ve vidění, vidění světelných kruhů kolem světel, rozšíření zornice, změna zabarvení očního bělma, krvácení z penisu, přítomnost krve ve spermatu, suchost v nose, zduření uvnitř nosu, pocit podrážděnosti a náhlé zhoršení nebo ztráta sluchu.
Po uvedení přípravku na trh byly vzácně hlášeny případy nestabilní anginy pectoris (onemocnění srdce) a náhlé smrti. Je třeba poznamenat, že většina mužů, ale ne všichni, kteří měli tyto nežádoucí účinky, měla potíže se srdcem již před užitím přípravku. Není možné určit, zda tyto příhody měly přímou souvislost s užitím přípravku Vizarsin.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Vizarsin uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za „EXP:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Vizarsin obsahuje
- Léčivou látkou je sildenafilum. Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 50 mg.
- Pomocnými látkami jsou:
Jádro tablety: mikrokrystalická celulosa (E460), hydrogenfosforečnan vápenatý, sodná sůl
kroskarmelosy, hypromelosa (E464), magnesium-stearát (E572).
Potah tablety: monohydrát laktosy, hypromelosa (E464), oxid titaničitý (E171), triacetin (E1518).
Jak přípravek Vizarsin vypadá a co obsahuje toto balení
Potahované tablety Vizarsin 50 mg jsou bílé, podlouhlé a s označením „50“ na jedné straně.
Vizarsin 50 mg potahované tablety se dodávají v krabičkách po 1 potahované tabletě v blistrech a také v krabičkách po 4 x 1, 8 x 1 nebo 12 x 1 potahované tabletě v perforovaných blistrech pro jednotlivé dávky.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
|
Belgie/Belgique/Belgien KRKA Belgium, SA. Tél/Tel: +32 (0) 489 304 091 |
Lietuva UAB KRKA Lietuva Tel: + 370 5 236 27 40 |
|
Btarapna KPKA Etarapna EOOfl Ten.: + 359 (02) 962 34 50 |
Luxembourg/Luxemburg KRKA Belgium, SA. Tél/Tel: +32 (0) 489 304 091 (BE) |
|
Česká republika KRKA ČR, s.r.o. Tel: + 420 (0) 221 115 150 |
Magyarország KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490 |
|
Danmark KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
Malta E. J. Busuttil Ltd. Tel: + 356 21 445 885 |
|
Deutschland TAD Pharma GmbH Tel: + 49 (0) 4721 606-0 |
Nederland KRKA Belgium, SA. Tel: +32 (0) 489 304 091 (BE) |
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. T^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
Espaňa KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmaceutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Románia KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq |
Sverige |
KRKA Sverige AB
Kipa Pharmacal Ltd. Tn^: + 357 24 651 882
Latvija
KRKA Latvija SIA Tel: + 371 6 733 86 10
Tel: + 46 (0)8 643 67 66 (SE)
United Kingdom
Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888
Tato příbalová informace byla naposledy revidována
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Příbalová informace: informace pro uživatele
Vizarsin 100 mg potahované tablety
Sildenafilum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Vizarsin a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
3. Jak se přípravek Vizarsin užívá
4. Možné nežádoucí účinky
5. Jak přípravek Vizarsin uchovávat
6. Obsah balení a další informace
1. Co je přípravek Vizarsin a k čemu se používá
Přípravek Vizarsin obsahuje léčivou látku sildenafil, což je lék ze skupiny nazývané inhibitory fosfodiesterázy typu 5 (PDE5). Po jejím užití dochází při odpovídajícím sexuálním vzrušení k uvolnění hladkých svalových vláken kontrolujících přítok krve do penisu, čímž se zvýší přítok krve do tohoto orgánu. Přípravek Vizarsin Vám pomůže navodit erekci jen tehdy, pokud dojde k sexuálnímu dráždění.
Přípravek Vizarsin se používá k léčbě dospělých mužů s poruchami erekce. Tato porucha je také známá pod pojmem impotence. Jedná se o situaci, kdy muž nemůže během sexuálního vzrušení dosáhnout ztopoření penisu nebo je toto ztopoření nedostatečné pro sexuální aktivitu.
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
Neužívejte přípravek Vizarsin:
- jestliže jste alergický na sildenafil nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Informujte svého lékaře, pokud užíváte některý z těchto léků předepisovaný k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu). Nejste-li si jist, zeptejte se svého lékaře nebo lékárníka.
- pokud užíváte léky schopné uvolňovat oxid dusnatý, jako je např. isoamyl-nitrit, protože souběžné užití může také způsobit nebezpečný pokles krevního tlaku.
- jestliže užíváte riocigvát. Tento lék se používá k léčbě plicní arteriální hypertenze (tj. vysokého krevního tlaku v plicích) a chronické tromboembolické plicní hypertenze (tj. vysokého krevního tlaku v plicích sekundárních krevních sraženin). U PDE5 inhibitorů, jako je například přípravek Vizarsin, bylo prokázáno, že zvyšují hypotenzní účinek tohoto léku. Pokud užíváte riocigvát nebo si nejste jisti, informujte svého lékaře.
- pokud máte závažnou srdeční poruchu nebo závažnou poruchu jater.
- pokud jste měl nedávno cévní mozkovou příhodu (mrtvici), srdeční infarkt nebo pokud máte nízký krevní tlak.
- pokud máte vzácnou vrozenou poruchu sítnice (jako např. retinitis pigmentosa).
- pokud jste přišel o zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION).
Upozornění a opatření
Před užitím přípravku Vizarsin se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže:
- trpíte srpkovitou anemií (poruchou červených krvinek), leukemií (nádorové onemocnění bílých krvinek), mnohočetným myelomem (nádorové onemocnění kostní dřeně).
- trpíte deformitou penisu nebo Peyronieovou chorobou.
- máte potíže se srdcem. Váš lékař by měl pečlivě zhodnotit, zda Vaše srdce snese přídatnou zátěž při pohlavním styku.
- máte vředovou chorobu nebo potíže s krvácivostí (např. hemofilii).
- zaznamenáte náhlé zhoršení nebo ztrátu zraku. Přestaňte užívat přípravek Vizarsin a okamžitě vyhledejte svého lékaře.
Současně s přípravkem Vizarsin neužívejte k léčbě poruchy erekce žádný jiný přípravek podávaný ústy nebo místně.
Neužívejte přípravek Vizarsin současně s léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil ani s žádnými jinými inhibitory PDE5.
V případě, že netrpíte poruchou erekce, přípravek Vizarsin neužívejte.
Přípravek Vizarsin není určen pro ženy.
Léčba pacientů s poruchou funkce ledvin nebo jater
Pokud máte poruchu jater nebo ledvin, sdělte tuto skutečnost lékaři. Ten posoudí, zda je nutné dávku přípravku Vizarsin upravit.
Děti a dospívající
Přípravek Vizarsin není určen pro pacienty mladší 18 let.
Další léčivé přípravky a přípravek Vizarsin
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat.
Přípravek Vizarsin může ovlivňovat účinek některých jiných léků, především těch, které jsou určeny k léčení bolesti na hrudníku srdečního původu. V případě náhlých zdravotních problémů byste měl svému lékaři, lékárníkovi nebo zdravotní sestře oznámit, že jste užil přípravek Vizarsin a kdy. Neužívejte přípravek Vizarsin společně s jinými léky, pokud Vám to nedoporučí Váš ošetřující lékař.
Neužívejte přípravek Vizarsin, pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Vždy informujte svého lékaře, lékárníka nebo zdravotní sestru, že užíváte některý z těchto léků předepisovaných k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu).
Neužívejte přípravek Vizarsin, pokud užíváte léky schopné uvolňovat oxid dusnatý, jako např. isoamyl-nitrit („poppers“), protože souběžné užití může způsobit nebezpečný pokles krevního tlaku.
Informujte svého lékaře nebo lékárníka, pokud již užíváte riocigvát.
Pokud užíváte léky, které patří do skupiny inhibitorů proteáz, např. k léčbě HIV, doporučí Vám obvykle Váš lékař přípravek Vizarsin o nejmenší možné síle 25 mg.
Někteří pacienti, užívající alfa-blokátory k léčbě vysokého krevního tlaku nebo zvětšené prostaty, mohou zaznamenat závratě nebo motání hlavy, které může být způsobené nízkým krevním tlakem při rychlém sedání nebo vstávání. Někteří pacienti zaznamenali tyto příznaky při souběžném užití přípravku Vizarsin s alfa-blokátory. Příznaky posturální hypotenze se mohou nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Měl byste pravidelně užívat svou denní dávku alfa-blokátoru, než začnete užívat přípravek Vizarsin, aby se snížila pravděpodobnost nástupu těchto příznaků. Lékař může zahájit Vaši léčbu přípravkem Vizarsin v nižší dávce 25 mg.
Přípravek Vizarsin s jídlem, pitím a alkoholem
Přípravek Vizarsin může být užíván s jídlem i bez jídla. Po požití těžkého jídla se však účinek přípravku Vizarsin může projevit později.
Požití alkoholu může dočasně zhoršit schopnost dosáhnout erekce. Abyste dosáhl co nejvyššího účinku tohoto přípravku, doporučujeme před užitím přípravku Vizarsin nepožívat větší množství alkoholu.
Těhotenství, kojení a plodnost
Přípravek Vizarsin není určen pro použití u žen.
Řízení dopravních prostředků a obsluha strojů
Přípravek Vizarsin může způsobit závratě a narušit vidění. Měl byste proto znát svoji reakci na přípravek Vizarsin před tím, než budete řídit motorová vozidla nebo obsluhovat stroje.
Přípravek Vizarsin obsahuje laktosu
Pokud Vám lékař řekl, že nesnášíte některé cukry, poraďte se s ním, než začnete tento léčivý přípravek užívat.
3. Jak se přípravek Vizarsin užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý, poraďte se se svým lékařem nebo lékárníkem.
Doporučená zahajovací dávka je 50 mg.
Neužívejte více než jednu tabletu přípravku Vizarsin denně.
Užijte přípravek Vizarsin zhruba jednu hodinu před plánovaným pohlavním stykem. Tabletu spolkněte celou a zapijte ji sklenicí vody.
Jestliže cítíte, že přípravek Vizarsin účinkuje příliš silně nebo naopak slabě, sdělte to svému lékaři nebo lékárníkovi.
Přípravek Vizarsin Vám pomůže dosáhnout erekce, jen pokud dojde k sexuálnímu dráždění. Doba, po které začne přípravek účinkovat, je u každého člověka odlišná, ale obvykle se pohybuje mezi půl hodinou až hodinou. Pokud přípravek Vizarsin užijete společně s těžkým jídlem, může se nástup účinku oddálit.
Pokud po užití přípravku Vizarsin nedosáhnete erekce nebo je erekce nedostatečná pro celý pohlavní
styk, poraďte se o dalším postupu se svým lékařem.
Jestliže jste užil více přípravku Vizarsin, než jste měl
Můžete zaznamenat zvýšený výskyt nežádoucích účinků a jejich závažnosti. Dávka vyšší než 100 mg nezlepšuje dále účinnost.
Neužívejte více tablet, než Vám bylo lékařem doporučeno.
Vyhledejte svého lékaře, pokud užijete více tablet, než jste měl.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Nežádoucí účinky hlášené v souvislosti s užitím přípravku Vizarsin bývají obvykle mírné až středně závažné a krátkého trvání.
Pokud se u Vás vyskytl některý z následujících nežádoucích účinků, přestaňte přípravek Vizarsin užívat a okamžitě vyhledejte lékařskou pomoc:
- Alergická reakce - k té dochází méně často (může postihnout až 1 ze 100 pacientů)
Příznaky zahrnují náhlou dýchavičnost, potíže s dýcháním nebo závrať, otok očních víček, obličeje, rtů nebo hrdla.
- Bolest na hrudníku - k té dochází méně často
Pokud se objeví v průběhu nebo po skončení pohlavního styku:
- posaďte se do polosedu a snažte se odpočívat.
- neužívejte na léčbu bolesti na hrudníku nitráty.
- Prodloužená a občas bolestivá erekce - k té dochází vzácně (může postihnout až 1 z 1000 pacientů)
Pokud u Vás dojde k erekci, která trvá déle než 4 hodiny, okamžitě vyhledejte lékaře.
- Náhlé zhoršení nebo ztráta zraku - k tomu dochází vzácně
- Těžké kožní reakce - k těm dochází vzácně
Příznaky mohou zahrnovat silné olupování a otok kůže, tvorbu puchýřů v ústech, na genitálu a kolem očí, horečku.
- Křečové stavy nebo záchvaty - k těm dochází vzácně Další nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 pacientů): bolest hlavy.
Časté (mohou postihnout až 1 z 10 pacientů): nevolnost, zarudnutí v obličeji, nával horka (příznaky zahrnují náhlý pocit horka v horní části těla), zažívací potíže, změny barevného vidění, rozmazané vidění, poruchy vidění, ucpaný nos a závrať.
Méně časté (mohou postihnout až 1 ze 100 pacientů): zvracení, kožní vyrážka, podráždění oka, překrvené/červené oči, bolest očí, vidění záblesků světla, zrakový vjem jasu, citlivost na světlo, slzení očí, bušení srdce, zrychlený srdeční puls, vysoký krevní tlak, nízký krevní tlak, bolest svalů, ospalost, snížená citlivost na dotek, porucha rovnováhy, zvonění v uších, sucho v ústech, ucpané vedlejší dutiny nosní, zánět nosní sliznice (příznaky zahrnují rýmu, kýchání a ucpaný nos), bolest horní poloviny břicha, refluxní choroba jícnu (příznaky zahrnují pálení žáhy), přítomnost krve v moči, bolest paží nebo nohou, krvácení z nosu, pocit horka a únava.
Vzácné (mohou postihnout až 1 z 1000 pacientů): mdloby, cévní mozková příhoda, srdeční infarkt, nepravidelný srdeční puls, dočasné snížení průtoku krve některými částmi mozku, stažení hrdla, znecitlivěná ústa, krvácení na očním pozadí, dvojité vidění, snížená zraková ostrost, neobvyklý pocit v oku, otok oka nebo očního víčka, malé částice nebo tečky ve vidění, vidění světelných kruhů kolem světel, rozšíření zornice, změna zabarvení očního bělma, krvácení z penisu, přítomnost krve ve spermatu, suchost v nose, zduření uvnitř nosu, pocit podrážděnosti a náhlé zhoršení nebo ztráta sluchu.
Po uvedení přípravku na trh byly vzácně hlášeny případy nestabilní anginy pectoris (onemocnění srdce) a náhlé smrti. Je třeba poznamenat, že většina mužů, ale ne všichni, kteří měli tyto nežádoucí účinky, měla potíže se srdcem již před užitím přípravku. Není možné určit, zda tyto příhody měly přímou souvislost s užitím přípravku Vizarsin.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Vizarsin uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za „EXP:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Vizarsin obsahuje
- Léčivou látkou je sildenafilum. Jedna potahovaná tableta obsahuje sildenafili citras odpovídající sildenafilum 100 mg.
- Pomocnými látkami jsou:
Jádro tablety: mikrokrystalická celulosa (E460), hydrogenfosforečnan vápenatý, sodná sůl
kroskarmelosy, hypromelosa (E464), magnesium-stearát (E572).
Potah tablety: monohydrát laktosy, hypromelosa (E464), oxid titaničitý (E171), triacetin (E1518).
Jak přípravek Vizarsin vypadá a co obsahuje toto balení
Potahované tablety Vizarsin 100 mg jsou bílé, podlouhlé a s označením „100“ na jedné straně.
Vizarsin 100 mg potahované tablety se dodávají v krabičkách po 1 potahované tabletě v blistrech a také v krabičkách po 4 x 1, 8 x 1 nebo 12 x 1 potahované tabletě v perforovaných blistrech pro jednotlivé dávky.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
KRKA, d.d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovinsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
|
Belgie/Belgique/Belgien KRKA Belgium, SA. Tél/Tel: +32 (0) 489 304 091 |
Lietuva UAB KRKA Lietuva Tel: + 370 5 236 27 40 |
|
Btarapna KPKA Etarapna EOOfl Ten.: + 359 (02) 962 34 50 |
Luxembourg/Luxemburg KRKA Belgium, SA. Tél/Tel: +32 (0) 489 304 091 (BE) |
|
Česká republika KRKA ČR, s.r.o. Tel: + 420 (0) 221 115 150 |
Magyarország KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490 |
|
Danmark KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
Malta E. J. Busuttil Ltd. Tel: + 356 21 445 885 |
|
Deutschland TAD Pharma GmbH Tel: + 49 (0) 4721 606-0 |
Nederland KRKA Belgium, SA. Tel: +32 (0) 489 304 091 (BE) |
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. T^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
Espaňa KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmaceutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Románia KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq |
Sverige |
KRKA Sverige AB
Kipa Pharmacal Ltd. Tn^: + 357 24 651 882
Latvija
KRKA Latvija SIA Tel: + 371 6 733 86 10
Tel: + 46 (0)8 643 67 66 (SE)
United Kingdom
Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888
Tato příbalová informace byla naposledy revidována
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Příbalová informace: informace pro uživatele
Vizarsin 25 mg tablety dispergovatelné v ústech
Sildenafilum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Vizarsin a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
3. Jak se přípravek Vizarsin užívá
4. Možné nežádoucí účinky
5. Jak přípravek Vizarsin uchovávat
6. Obsah balení a další informace
1. Co je přípravek Vizarsin a k čemu se používá
Přípravek Vizarsin obsahuje léčivou látku sildenafil, což je lék ze skupiny nazývané inhibitory fosfodiesterázy typu 5 (PDE5). Po jejím užití dochází při odpovídajícím sexuálním vzrušení k uvolnění hladkých svalových vláken kontrolujících přítok krve do penisu, čímž se zvýší přítok krve do tohoto orgánu. Přípravek Vizarsin Vám pomůže navodit erekci jen tehdy, pokud dojde k sexuálnímu dráždění.
Přípravek Vizarsin se používá k léčbě dospělých mužů s poruchami erekce. Tato porucha je také známá pod pojmem impotence. Jedná se o situaci, kdy muž nemůže během sexuálního vzrušení dosáhnout ztopoření penisu nebo je toto ztopoření nedostatečné pro sexuální aktivitu.
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
Neužívejte přípravek Vizarsin:
- jestliže jste alergický na sildenafil nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Informujte svého lékaře, pokud užíváte některý z těchto léků předepisovaný k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu). Nejste-li si jist, zeptejte se svého lékaře nebo lékárníka.
- pokud užíváte léky schopné uvolňovat oxid dusnatý, jako je např. isoamyl-nitrit, protože souběžné užití může také způsobit nebezpečný pokles krevního tlaku.
- jestliže užíváte riocigvát. Tento lék se používá k léčbě plicní arteriální hypertenze (tj. vysokého krevního tlaku v plicích) a chronické tromboembolické plicní hypertenze (tj. vysokého krevního tlaku v plicích sekundárních krevních sraženin). U PDE5 inhibitorů, jako je například přípravek Vizarsin, bylo prokázáno, že zvyšují hypotenzní účinek tohoto léku. Pokud užíváte riocigvát nebo si nejste jisti, informujte svého lékaře.
- pokud máte závažnou srdeční poruchu nebo závažnou poruchu jater.
- pokud jste měl nedávno cévní mozkovou příhodu (mrtvici), srdeční infarkt nebo pokud máte nízký krevní tlak.
- pokud máte vzácnou vrozenou poruchu sítnice (jako např. retinitis pigmentosa).
- pokud jste přišel o zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION).
Upozornění a opatření
Před užitím přípravku Vizarsin se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže:
- trpíte srpkovitou anemií (poruchou červených krvinek), leukemií (nádorové onemocnění bílých krvinek), mnohočetným myelomem (nádorové onemocnění kostní dřeně).
- trpíte deformitou penisu nebo Peyronieovou chorobou.
- máte potíže se srdcem. Váš lékař by měl pečlivě zhodnotit, zda Vaše srdce snese přídatnou zátěž při pohlavním styku.
- máte vředovou chorobu nebo potíže s krvácivostí (např. hemofilii).
- zaznamenáte náhlé zhoršení nebo ztrátu zraku. Přestaňte užívat přípravek Vizarsin a okamžitě vyhledejte svého lékaře.
Současně s přípravkem Vizarsin neužívejte k léčbě poruchy erekce žádný jiný přípravek podávaný ústy nebo místně.
Neužívejte přípravek Vizarsin současně s léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil ani s žádnými jinými inhibitory PDE5.
V případě, že netrpíte poruchou erekce, přípravek Vizarsin neužívejte.
Přípravek Vizarsin není určen pro ženy.
Léčba pacientů s poruchou funkce ledvin nebo jater
Pokud máte poruchu jater nebo ledvin, sdělte tuto skutečnost lékaři. Ten posoudí, zda je nutné dávku přípravku Vizarsin upravit.
Děti a dospívající
Přípravek Vizarsin není určen pro pacienty mladší 18 let.
Další léčivé přípravky a přípravek Vizarsin
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat.
Přípravek Vizarsin může ovlivňovat účinek některých jiných léků, především těch, které jsou určeny k léčení bolesti na hrudníku srdečního původu. V případě náhlých zdravotních problémů byste měl svému lékaři, lékárníkovi nebo zdravotní sestře oznámit, že jste užil přípravek Vizarsin a kdy. Neužívejte přípravek Vizarsin společně s jinými léky, pokud Vám to nedoporučí Váš ošetřující lékař.
Neužívejte přípravek Vizarsin, pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Vždy informujte svého lékaře, lékárníka nebo zdravotní sestru, že užíváte některý z těchto léků předepisovaných k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu).
Neužívejte přípravek Vizarsin, pokud užíváte léky schopné uvolňovat oxid dusnatý, jako např. isoamyl-nitrit („poppers“), protože souběžné užití může způsobit nebezpečný pokles krevního tlaku.
Informujte svého lékaře nebo lékárníka, pokud již užíváte riocigvát.
Pokud užíváte léky, které patří do skupiny inhibitorů proteáz, např. k léčbě HIV, doporučí Vám obvykle Váš lékař přípravek Vizarsin o nejmenší možné síle 25 mg.
Někteří pacienti, užívající alfa-blokátory k léčbě vysokého krevního tlaku nebo zvětšené prostaty, mohou zaznamenat závratě nebo motání hlavy, které může být způsobené nízkým krevním tlakem při rychlém sedání nebo vstávání. Někteří pacienti zaznamenali tyto příznaky při souběžném užití přípravku Vizarsin s alfa-blokátory. Příznaky posturální hypotenze se mohou nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Měl byste pravidelně užívat svou denní dávku alfa-blokátoru, než začnete užívat přípravek Vizarsin, aby se snížila pravděpodobnost nástupu těchto příznaků. Lékař může zahájit Vaši léčbu přípravkem Vizarsin v nižší dávce 25 mg.
Přípravek Vizarsin s jídlem, pitím a alkoholem
Přípravek Vizarsin může být užíván s jídlem i bez jídla. Po požití těžkého jídla se však účinek přípravku Vizarsin může projevit později. Před užitím tablety by měla být Vaše ústa prázdná.
Požití alkoholu může dočasně zhoršit schopnost dosáhnout erekce. Abyste dosáhl co nejvyššího účinku tohoto přípravku, doporučujeme před užitím přípravku Vizarsin nepožívat větší množství alkoholu.
Těhotenství, kojení a plodnost
Přípravek Vizarsin není určen pro použití u žen.
Řízení dopravních prostředků a obsluha strojů
Přípravek Vizarsin může způsobit závratě a narušit vidění. Měl byste proto znát svoji reakci na přípravek Vizarsin před tím, než budete řídit motorová vozidla nebo obsluhovat stroje.
Přípravek Vizarsin obsahuje aspartam (E951) a sorbitol (E420)
Aspartam je zdroj fenylalaninu, který může být škodlivý pro lidi trpící fenylketonurií.
Přípravek Vizarsin obsahuje sorbitol. Pokud Vám lékař řekl, že nesnášíte některé cukry, poraďte se se svým lékařem, než začnete tento léčivý přípravek užívat.
3. Jak se přípravek Vizarsin užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý, poraďte se se svým lékařem nebo lékárníkem.
Doporučená zahajovací dávka je 50 mg.
Neužívejte více než jednu tabletu přípravku Vizarsin denně.
Neužívejte přípravek Vizarsin tablety dispergovatelné v ústech společně s jinými lékovými formami přípravku Vizarsin.
Užijte přípravek Vizarsin zhruba jednu hodinu před plánovaným pohlavním stykem.
Vizarsin tablety jsou křehké. Neměly by se protlačovat fólií blistru, protože by se tím mohla tableta poškodit. Nedotýkejte se tablety vlhkou rukou, protože by se tableta mohla rozpadnout. Vyjměte tabletu z obalu následujícím způsobem:
1 tableta v blistru:

4 tablety v blistni:

1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně.
4. Jakmile vyjmete tabletu z obalu, položte ji na jazyk.
Během několika sekund se začne tableta v ústech rozpadat, následně ji můžete s vodou nebo bez vody spolknout. Ústa by měla být při pokládání tablety na jazyk prázdná.
Jestliže cítíte, že přípravek Vizarsin účinkuje příliš silně nebo naopak slabě, sdělte to svému lékaři nebo lékárníkovi.
Přípravek Vizarsin Vám pomůže dosáhnout erekce, jen pokud dojde k sexuálnímu dráždění. Doba, po které začne přípravek účinkovat, je u každého člověka odlišná, ale obvykle se pohybuje mezi půl hodinou až hodinou. Pokud přípravek Vizarsin užijete společně s těžkým jídlem, může se nástup účinku oddálit.
Pokud po užití přípravku Vizarsin nedosáhnete erekce nebo je erekce nedostatečná pro celý pohlavní styk, poraďte se o dalším postupu se svým lékařem.
Jestliže jste užil více přípravku Vizarsin, než jste měl
Můžete zaznamenat zvýšený výskyt nežádoucích účinků a jejich závažnosti. Dávka vyšší než 100 mg nezlepšuje dále účinnost.
Neužívejte více tablet, než Vám bylo lékařem doporučeno.
Vyhledejte svého lékaře, pokud užijete více tablet, než jste měl.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Nežádoucí účinky hlášené v souvislosti s užitím přípravku Vizarsin bývají obvykle mírné až středně závažné a krátkého trvání.
Pokud se u Vás vyskytl některý z následujících nežádoucích účinků, přestaňte přípravek Vizarsin užívat a okamžitě vyhledejte lékařskou pomoc:
- Alergická reakce - k té dochází méně často (může postihnout až 1 ze 100 pacientů)
Příznaky zahrnují náhlou dýchavičnost, potíže s dýcháním nebo závrať, otok očních víček,
obličeje, rtů nebo hrdla.
Bolest na hrudníku - k té dochází méně často
Pokud se objeví v průběhu nebo po skončení pohlavního styku:
- posaďte se do polosedu a snažte se odpočívat.
- neužívejte na léčbu bolesti na hrudníku nitráty.
Prodloužená a občas bolestivá erekce - k té dochází vzácně (může postihnout až 1 z 1000 pacientů)
Pokud u Vás dojde k erekci, která trvá déle než 4 hodiny, okamžitě vyhledejte lékaře. Náhlé zhoršení nebo ztráta zraku - k tomu dochází vzácně
Těžké kožní reakce - k těm dochází vzácně
Příznaky mohou zahrnovat silné olupování a otok kůže, tvorbu puchýřů v ústech, na genitálu a kolem očí, horečku.
Křečové stavy nebo záchvaty - k těm dochází vzácně
Další nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 pacientů): bolest hlavy.
Časté (mohou postihnout až 1 z 10 pacientů): nevolnost, zarudnutí v obličeji, nával horka (příznaky zahrnují náhlý pocit horka v horní části těla), zažívací potíže, změny barevného vidění, rozmazané vidění, poruchy vidění, ucpaný nos a závrať.
Méně časté (mohou postihnout až 1 ze 100 pacientů): zvracení, kožní vyrážka, podráždění oka, překrvené/červené oči, bolest očí, vidění záblesků světla, zrakový vjem jasu, citlivost na světlo, slzení očí, bušení srdce, zrychlený srdeční puls, vysoký krevní tlak, nízký krevní tlak, bolest svalů, ospalost, snížená citlivost na dotek, porucha rovnováhy, zvonění v uších, sucho v ústech, ucpané vedlejší dutiny nosní, zánět nosní sliznice (příznaky zahrnují rýmu, kýchání a ucpaný nos), bolest horní poloviny břicha, refluxní choroba jícnu (příznaky zahrnují pálení žáhy), přítomnost krve v moči, bolest paží nebo nohou, krvácení z nosu, pocit horka a únava.
Vzácné (mohou postihnout až 1 z 1000 pacientů): mdloby, cévní mozková příhoda, srdeční infarkt, nepravidelný srdeční puls, dočasné snížení průtoku krve některými částmi mozku, stažení hrdla, znecitlivěná ústa, krvácení na očním pozadí, dvojité vidění, snížená zraková ostrost, neobvyklý pocit v oku, otok oka nebo očního víčka, malé částice nebo tečky ve vidění, vidění světelných kruhů kolem světel, rozšíření zornice, změna zabarvení očního bělma, krvácení z penisu, přítomnost krve ve spermatu, suchost v nose, zduření uvnitř nosu, pocit podrážděnosti a náhlé zhoršení nebo ztráta sluchu.
Po uvedení přípravku na trh byly vzácně hlášeny případy nestabilní anginy pectoris (onemocnění srdce) a náhlé smrti. Je třeba poznamenat, že většina mužů, ale ne všichni, kteří měli tyto nežádoucí účinky, měla potíže se srdcem již před užitím přípravku. Není možné určit, zda tyto příhody měly přímou souvislost s užitím přípravku Vizarsin.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Vizarsin uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za „EXP:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek Vizarsin obsahuje
- Léčivou látkou je sildenafilum. Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 25 mg.
- Pomocnými látkami jsou hyprolosa (E463), mannitol (E421), aspartam (E951), neohesperidin-dihydrochalkon (E959), silice máty kadeřavé, silice máty peprné (obsahuje sorbitol (E420)), krospovidon, křemičitan vápenatý, magnesium-stearát (E572).
Jak přípravek Vizarsin vypadá a co obsahuje toto balení
Bílé až téměř bílé, kulaté, mírně bikonvexní tablety, s možnými tmavšími tečkami.
Vizarsin tablety dispergovatelné v ústech se dodávají v krabičkách po 1 tabletě dispergovatelné v ústech v blistrech a také v krabičkách po 2 x 1, 4 x 1, 8 x 1 nebo 12 x 1 tabletě dispergovatelné v ústech v perforovaných jednodávkových blistrech.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci
KRKA, d.d., Novo mesto, Smaiješka cesta 6, 8501 Novo mesto, Slovinsko Výrobce
KRKA, d.d., Novo mesto, Šmaiješka cesta 6, 8501 Novo mesto, Slovinsko TAD Pharma GmbH, Heinz-Lohmann-StraBe 5, 27472 Cuxhaven, Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Eunrapnu
KPKA Etnrapnn EOOfl Ten.: + 359 (02) 962 34 50
Česká republika KRKA ČR, s.r.o.
Tel: + 420 (0) 221 115 150
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
Magyarország
KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490
Malta
E. J. Busuttil Ltd.
Tel: + 356 21 445 885
Danmark
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Tel: + 49 (0) 4721 606-0
Tel: +32 (0) 489 304 091 (BE)
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
ElláSa QUALIA PHARMA S.A. T^k: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
Espaňa KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmaceutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Románia KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Knnpoq Kipa Pharmacal Ltd. Tnk: + 357 24 651 882 |
Sverige KRKA Sverige AB Tel: + 46 (0)8 643 67 66 (SE) |
|
Latvija KRKA Latvija SIA Tel: + 371 6 733 86 10 |
United Kingdom Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888 |
Tato příbalová informace byla naposledy revidována
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Příbalová informace: informace pro uživatele
Vizarsin 50 mg tablety dispergovatelné v ústech
Sildenafilum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Vizarsin a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
3. Jak se přípravek Vizarsin užívá
4. Možné nežádoucí účinky
5. Jak přípravek Vizarsin uchovávat
6. Obsah balení a další informace
1. Co je přípravek Vizarsin a k čemu se používá
Přípravek Vizarsin obsahuje léčivou látku sildenafil, což je lék ze skupiny nazývané inhibitory fosfodiesterázy typu 5 (PDE5). Po jejím užití dochází při odpovídajícím sexuálním vzrušení k uvolnění hladkých svalových vláken kontrolujících přítok krve do penisu, čímž se zvýší přítok krve do tohoto orgánu. Přípravek Vizarsin Vám pomůže navodit erekci jen tehdy, pokud dojde k sexuálnímu dráždění.
Přípravek Vizarsin se používá k léčbě dospělých mužů s poruchami erekce. Tato porucha je také známá pod pojmem impotence. Jedná se o situaci, kdy muž nemůže během sexuálního vzrušení dosáhnout ztopoření penisu nebo je toto ztopoření nedostatečné pro sexuální aktivitu.
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
Neužívejte přípravek Vizarsin:
- jestliže jste alergický na sildenafil nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Informujte svého lékaře, pokud užíváte některý z těchto léků předepisovaný k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu). Nejste-li si jist, zeptejte se svého lékaře nebo lékárníka.
- pokud užíváte léky schopné uvolňovat oxid dusnatý, jako je např. isoamyl-nitrit, protože souběžné užití může také způsobit nebezpečný pokles krevního tlaku.
- jestliže užíváte riocigvát. Tento lék se používá k léčbě plicní arteriální hypertenze (tj. vysokého krevního tlaku v plicích) a chronické tromboembolické plicní hypertenze (tj. vysokého krevního tlaku v plicích sekundárních krevních sraženin). U PDE5 inhibitorů, jako je například přípravek Vizarsin, bylo prokázáno, že zvyšují hypotenzní účinek tohoto léku. Pokud užíváte riocigvát nebo si nejste jisti, informujte svého lékaře.
- pokud máte závažnou srdeční poruchu nebo závažnou poruchu jater.
- pokud jste měl nedávno cévní mozkovou příhodu (mrtvici), srdeční infarkt nebo pokud máte nízký krevní tlak.
- pokud máte vzácnou vrozenou poruchu sítnice (jako např. retinitis pigmentosa).
- pokud jste přišel o zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION).
Upozornění a opatření
Před užitím přípravku Vizarsin se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže:
- trpíte srpkovitou anemií (poruchou červených krvinek), leukemií (nádorové onemocnění bílých krvinek), mnohočetným myelomem (nádorové onemocnění kostní dřeně).
- trpíte deformitou penisu nebo Peyronieovou chorobou.
- máte potíže se srdcem. Váš lékař by měl pečlivě zhodnotit, zda Vaše srdce snese přídatnou zátěž při pohlavním styku.
- máte vředovou chorobu nebo potíže s krvácivostí (např. hemofilii).
- zaznamenáte náhlé zhoršení nebo ztrátu zraku. Přestaňte užívat přípravek Vizarsin a okamžitě vyhledejte svého lékaře.
Současně s přípravkem Vizarsin neužívejte k léčbě poruchy erekce žádný jiný přípravek podávaný ústy nebo místně.
Neužívejte přípravek Vizarsin současně s léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil ani s žádnými jinými inhibitory PDE5.
V případě, že netrpíte poruchou erekce, přípravek Vizarsin neužívejte.
Přípravek Vizarsin není určen pro ženy.
Léčba pacientů s poruchou funkce ledvin nebo jater
Pokud máte poruchu jater nebo ledvin, sdělte tuto skutečnost lékaři. Ten posoudí, zda je nutné dávku přípravku Vizarsin upravit.
Děti a dospívající
Přípravek Vizarsin není určen pro pacienty osoby mladší 18 let.
Další léčivé přípravky a přípravek Vizarsin
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat.
Přípravek Vizarsin může ovlivňovat účinek některých jiných léků, především těch, které jsou určeny k léčení bolesti na hrudníku srdečního původu. V případě náhlých zdravotních problémů byste měl svému lékaři, lékárníkovi nebo zdravotní sestře oznámit, že jste užil přípravek Vizarsin a kdy. Neužívejte přípravek Vizarsin společně s jinými léky, pokud Vám to nedoporučí Váš ošetřující lékař.
Neužívejte přípravek Vizarsin, pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Vždy informujte svého lékaře, lékárníka nebo zdravotní sestru, že užíváte některý z těchto léků předepisovaných k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu).
Neužívejte přípravek Vizarsin, pokud užíváte léky schopné uvolňovat oxid dusnatý, jako např. isoamyl-nitrit („poppers“), protože souběžné užití může způsobit nebezpečný pokles krevního tlaku.
Informujte svého lékaře nebo lékárníka, pokud již užíváte riocigvát.
Pokud užíváte léky, které patří do skupiny inhibitorů proteáz, např. k léčbě HIV, doporučí Vám obvykle Váš lékař přípravek Vizarsin o nejmenší možné síle 25 mg.
Někteří pacienti, užívající alfa-blokátory k léčbě vysokého krevního tlaku nebo zvětšené prostaty, mohou zaznamenat závratě nebo motání hlavy, které může být způsobené nízkým krevním tlakem při rychlém sedání nebo vstávání. Někteří pacienti zaznamenali tyto příznaky při souběžném užití přípravku Vizarsin s alfa-blokátory. Příznaky posturální hypotenze se mohou nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Měl byste pravidelně užívat svou denní dávku alfa-blokátoru, než začnete užívat přípravek Vizarsin, aby se snížila pravděpodobnost nástupu těchto příznaků. Lékař může zahájit Vaši léčbu přípravkem Vizarsin v nižší dávce 25 mg.
Přípravek Vizarsin s jídlem, pitím a alkoholem
Přípravek Vizarsin může být užíván s jídlem i bez jídla. Po požití těžkého jídla se však účinek přípravku Vizarsin může projevit později. Před užitím tablety by měla být Vaše ústa prázdná.
Požití alkoholu může dočasně zhoršit schopnost dosáhnout erekce. Abyste dosáhl co nejvyššího účinku tohoto přípravku, doporučujeme před užitím přípravku Vizarsin nepožívat větší množství alkoholu.
Těhotenství, kojení a plodnost
Přípravek Vizarsin není určen pro použití u žen.
Řízení dopravních prostředků a obsluha strojů
Přípravek Vizarsin může způsobit závratě a narušit vidění. Měl byste proto znát svoji reakci na přípravek Vizarsin před tím, než budete řídit motorová vozidla nebo obsluhovat stroje.
Přípravek Vizarsin obsahuje aspartam (E951) a sorbitol (E420)
Aspartam je zdroj fenylalaninu, který může být škodlivý pro lidi trpící fenylketonurií. Přípravek Vizarsin obsahuje sorbitol. Pokud Vám lékař řekl, že nesnášíte některé cukry, poraďte se se svým lékařem, než začnete tento léčivý přípravek užívat.
3. Jak se přípravek Vizarsin užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý, poraďte se se svým lékařem nebo lékárníkem.
Doporučená zahajovací dávka je 50 mg.
Neužívejte více než jednu tabletu přípravku Vizarsin denně.
Neužívejte přípravek Vizarsin tablety dispergovatelné v ústech společně s jinými lékovými formami přípravku Vizarsin.
Užijte přípravek Vizarsin zhruba jednu hodinu před plánovaným pohlavním stykem.
Vizarsin tablety jsou křehké. Neměly by se protlačovat fólií blistru, protože by se tím mohla tableta poškodit. Nedotýkejte se tablety vlhkou rukou, protože by se tableta mohla rozpadnout. Vyjměte tabletu z obalu následujícím způsobem:
1 tableta v blistru:

4 tablety v blistni:

1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně.
4. Jakmile vyjmete tabletu z obalu, položte ji na jazyk.
Během několika sekund se začne tableta v ústech rozpadat, následně ji můžete s vodou nebo bez vody spolknout. Ústa by měla být při pokládání tablety na jazyk prázdná.
Jestliže cítíte, že přípravek Vizarsin účinkuje příliš silně nebo naopak slabě, sdělte to svému lékaři nebo lékárníkovi.
Přípravek Vizarsin Vám pomůže dosáhnout erekce, jen pokud dojde k sexuálnímu dráždění. Doba, po které začne přípravek účinkovat, je u každého člověka odlišná, ale obvykle se pohybuje mezi půl hodinou až hodinou. Pokud přípravek Vizarsin užijete společně s těžkým jídlem, může se nástup účinku oddálit.
Pokud po užití přípravku Vizarsin nedosáhnete erekce nebo je erekce nedostatečná pro celý pohlavní styk, poraďte se o dalším postupu se svým lékařem.
Jestliže jste užil více přípravku Vizarsin, než jste měl
Můžete zaznamenat zvýšený výskyt nežádoucích účinků a jejich závažnosti. Dávka vyšší než 100 mg nezlepšuje dále účinnost.
Neužívejte více tablet, než Vám bylo lékařem doporučeno.
Vyhledejte svého lékaře, pokud užijete více tablet, než jste měl.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Nežádoucí účinky hlášené v souvislosti s užitím přípravku Vizarsin bývají obvykle mírné až středně závažné a krátkého trvání.
Pokud se u Vás vyskytl některý z následujících nežádoucích účinků, přestaňte přípravek Vizarsin užívat a okamžitě vyhledejte lékařskou pomoc:
- Alergická reakce - k té dochází méně často (může postihnout až 1 ze 100 pacientů)
Příznaky zahrnují náhlou dýchavičnost, potíže s dýcháním nebo závrať, otok očních víček,
obličeje, rtů nebo hrdla.
Bolest na hrudníku - k té dochází méně často
Pokud se objeví v průběhu nebo po skončení pohlavního styku:
- posaďte se do polosedu a snažte se odpočívat.
- neužívejte na léčbu bolesti na hrudníku nitráty.
Prodloužená a občas bolestivá erekce - k té dochází vzácně (může postihnout až 1 z 1000 pacientů)
Pokud u Vás dojde k erekci, která trvá déle než 4 hodiny, okamžitě vyhledejte lékaře. Náhlé zhoršení nebo ztráta zraku - k tomu dochází vzácně
Těžké kožní reakce - k těm dochází vzácně
Příznaky mohou zahrnovat silné olupování a otok kůže, tvorbu puchýřů v ústech, na genitálu a kolem očí, horečku.
Křečové stavy nebo záchvaty - k těm dochází vzácně
Další nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 pacientů): bolest hlavy.
Časté (mohou postihnout až 1 z 10 pacientů): nevolnost, zarudnutí v obličeji, nával horka (příznaky zahrnují náhlý pocit horka v horní části těla), zažívací potíže, změny barevného vidění, rozmazané vidění, poruchy vidění, ucpaný nos a závrať.
Méně časté (mohou postihnout až 1 ze 100 pacientů): zvracení, kožní vyrážka, podráždění oka, překrvené/červené oči, bolest očí, vidění záblesků světla, zrakový vjem jasu, citlivost na světlo, slzení očí, bušení srdce, zrychlený srdeční puls, vysoký krevní tlak, nízký krevní tlak, bolest svalů, ospalost, snížená citlivost na dotek, porucha rovnováhy, zvonění v uších, sucho v ústech, ucpané vedlejší dutiny nosní, zánět nosní sliznice (příznaky zahrnují rýmu, kýchání a ucpaný nos), bolest horní poloviny břicha, refluxní choroba jícnu (příznaky zahrnují pálení žáhy), přítomnost krve v moči, bolest paží nebo nohou, krvácení z nosu, pocit horka a únava.
Vzácné (mohou postihnout až 1 z 1000 pacientů): mdloby, cévní mozková příhoda, srdeční infarkt, nepravidelný srdeční puls, dočasné snížení průtoku krve některými částmi mozku, stažení hrdla, znecitlivěná ústa, krvácení na očním pozadí, dvojité vidění, snížená zraková ostrost, neobvyklý pocit v oku, otok oka nebo očního víčka, malé částice nebo tečky ve vidění, vidění světelných kruhů kolem světel, rozšíření zornice, změna zabarvení očního bělma, krvácení z penisu, přítomnost krve ve spermatu, suchost v nose, zduření uvnitř nosu, pocit podrážděnosti a náhlé zhoršení nebo ztráta sluchu.
Po uvedení přípravku na trh byly vzácně hlášeny případy nestabilní anginy pectoris (onemocnění srdce) a náhlé smrti. Je třeba poznamenat, že většina mužů, ale ne všichni, kteří měli tyto nežádoucí účinky, měla potíže se srdcem již před užitím přípravku. Není možné určit, zda tyto příhody měly přímou souvislost s užitím přípravku Vizarsin.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Vizarsin uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za „EXP:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek Vizarsin obsahuje
- Léčivou látkou je sildenafilum. Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 50 mg.
- Pomocnými látkami jsou hyprolosa (E463), mannitol (E421), aspartam (E951), neohesperidin-dihydrochalkon (E959), silice máty kadeřavé, silice máty peprné (obsahuje sorbitol (E420)), krospovidon, křemičitan vápenatý, magnesium-stearát (E572).
Jak přípravek Vizarsin vypadá a co obsahuje toto balení
Bílé až téměř bílé, kulaté, mírně bikonvexní tablety, s možnými tmavšími tečkami.
Vizarsin tablety dispergovatelné v ústech se dodávají v krabičkách po 1 tabletě dispergovatelné v ústech v blistrech a také v krabičkách po 2 x 1, 4 x 1, 8 x 1, 12 x 1 nebo 24 x 1 tabletě dispergovatelné v ústech v perforovaných jednodávkových blistrech.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci
KRKA, d.d., Novo mesto, Smaiješka cesta 6, 8501 Novo mesto, Slovinsko Výrobce
KRKA, d.d., Novo mesto, Šmaiješka cesta 6, 8501 Novo mesto, Slovinsko TAD Pharma GmbH, Heinz-Lohmann-StraBe 5, 27472 Cuxhaven, Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Eunrapnu
KPKA Etnrapnn EOOfl Ten.: + 359 (02) 962 34 50
Česká republika KRKA ČR, s.r.o.
Tel: + 420 (0) 221 115 150
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
Magyarország
KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490
Malta
E. J. Busuttil Ltd.
Tel: + 356 21 445 885
Danmark
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Tel: + 49 (0) 4721 606-0
Tel: +32 (0) 489 304 091 (BE)
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. Tn^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
Espaňa KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmaceutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Románia KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq Kipa Pharmacal Ltd. Tn^: + 357 24 651 882 |
Sverige KRKA Sverige AB Tel: + 46 (0)8 643 67 66 (SE) |
|
Latvija KRKA Latvija SIA Tel: + 371 6 733 86 10 |
United Kingdom Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888 |
Tato příbalová informace byla naposledy revidována
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Příbalová informace: informace pro uživatele
Vizarsin 100 mg tablety dispergovatelné v ústech
Sildenafilum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Vizarsin a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
3. Jak se přípravek Vizarsin užívá
4. Možné nežádoucí účinky
5. Jak přípravek Vizarsin uchovávat
6. Obsah balení a další informace
1. Co je přípravek Vizarsin a k čemu se používá
Přípravek Vizarsin obsahuje léčivou látku sildenafil, což je lék ze skupiny nazývané inhibitory fosfodiesterázy typu 5 (PDE5). Po jejím užití dochází při odpovídajícím sexuálním vzrušení k uvolnění hladkých svalových vláken kontrolujících přítok krve do penisu, čímž se zvýší přítok krve do tohoto orgánu. Přípravek Vizarsin Vám pomůže navodit erekci jen tehdy, pokud dojde k sexuálnímu dráždění.
Přípravek Vizarsin se používá k léčbě dospělých mužů s poruchami erekce. Tato porucha je také známá pod pojmem impotence. Jedná se o situaci, kdy muž nemůže během sexuálního vzrušení dosáhnout ztopoření penisu nebo je toto ztopoření nedostatečné pro sexuální aktivitu.
2. Čemu musíte věnovat pozornost, než začnete přípravek Vizarsin užívat
Neužívejte přípravek Vizarsin:
- jestliže jste alergický na sildenafil nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Informujte svého lékaře, pokud užíváte některý z těchto léků předepisovaný k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu). Nejste-li si jist, zeptejte se svého lékaře nebo lékárníka.
- pokud užíváte léky schopné uvolňovat oxid dusnatý, jako je např. isoamyl-nitrit, protože souběžné užití může také způsobit nebezpečný pokles krevního tlaku.
- jestliže užíváte riocigvát. Tento lék se používá k léčbě plicní arteriální hypertenze (tj. vysokého krevního tlaku v plicích) a chronické tromboembolické plicní hypertenze (tj. vysokého krevního tlaku v plicích sekundárních krevních sraženin). U PDE5 inhibitorů, jako je například přípravek Vizarsin, bylo prokázáno, že zvyšují hypotenzní účinek tohoto léku. Pokud užíváte riocigvát nebo si nejste jisti, informujte svého lékaře.
- pokud máte závažnou srdeční poruchu nebo závažnou poruchu jater.
- pokud jste měl nedávno cévní mozkovou příhodu (mrtvici), srdeční infarkt nebo pokud máte nízký krevní tlak.
- pokud máte vzácnou vrozenou poruchu sítnice (jako např. retinitis pigmentosa).
- pokud jste přišel o zrak v důsledku nearteritické přední ischemické neuropatie optického nervu (NAION).
Upozornění a opatření
Před užitím přípravku Vizarsin se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže:
- trpíte srpkovitou anemií (poruchou červených krvinek), leukemií (nádorové onemocnění bílých krvinek), mnohočetným myelomem (nádorové onemocnění kostní dřeně).
- trpíte deformitou penisu nebo Peyronieovou chorobou.
- máte potíže se srdcem. Váš lékař by měl pečlivě zhodnotit, zda Vaše srdce snese přídatnou zátěž při pohlavním styku.
- máte vředovou chorobu nebo potíže s krvácivostí (např. hemofilii).
- zaznamenáte náhlé zhoršení nebo ztrátu zraku. Přestaňte užívat přípravek Vizarsin a okamžitě vyhledejte svého lékaře.
Současně s přípravkem Vizarsin neužívejte k léčbě poruchy erekce žádný jiný přípravek podávaný ústy nebo místně.
Neužívejte přípravek Vizarsin současně s léčivými přípravky na plicní arteriální hypertenzi (PAH) obsahujícími sildenafil ani s žádnými jinými inhibitory PDE5.
V případě, že netrpíte poruchou erekce, přípravek Vizarsin neužívejte.
Přípravek Vizarsin není určen pro ženy.
Léčba pacientů s poruchou funkce ledvin nebo jater
Pokud máte poruchu jater nebo ledvin, sdělte tuto skutečnost lékaři. Ten posoudí, zda je nutné dávku přípravku Vizarsin upravit.
Děti a dospívající
Přípravek Vizarsin není určen pro pacienty mladší 18 let.
Další léčivé přípravky a přípravek Vizarsin
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval nebo které možná budete užívat.
Přípravek Vizarsin může ovlivňovat účinek některých jiných léků, především těch, které jsou určeny k léčení bolesti na hrudníku srdečního původu. V případě náhlých zdravotních problémů byste měl svému lékaři, lékárníkovi nebo zdravotní sestře oznámit, že jste užil přípravek Vizarsin a kdy. Neužívejte přípravek Vizarsin společně s jinými léky, pokud Vám to nedoporučí Váš ošetřující lékař.
Neužívejte přípravek Vizarsin, pokud užíváte léky nazývané nitráty, protože souběžné užití může způsobit nebezpečný pokles krevního tlaku. Vždy informujte svého lékaře, lékárníka nebo zdravotní sestru, že užíváte některý z těchto léků předepisovaných k úlevě od příznaků anginy pectoris (bolesti na hrudi srdečního původu).
Neužívejte přípravek Vizarsin, pokud užíváte léky schopné uvolňovat oxid dusnatý, jako např. isoamyl-nitrit („poppers“), protože souběžné užití může způsobit nebezpečný pokles krevního tlaku.
Informujte svého lékaře nebo lékárníka, pokud již užíváte riocigvát.
Pokud užíváte léky, které patří do skupiny inhibitorů proteáz, např. k léčbě HIV, doporučí Vám obvykle Váš lékař přípravek Vizarsin o nejmenší možné síle 25 mg.
Někteří pacienti, užívající alfa-blokátory k léčbě vysokého krevního tlaku nebo zvětšené prostaty, mohou zaznamenat závratě nebo motání hlavy, které může být způsobené nízkým krevním tlakem při rychlém sedání nebo vstávání. Někteří pacienti zaznamenali tyto příznaky při souběžném užití přípravku Vizarsin s alfa-blokátory. Příznaky posturální hypotenze se mohou nejpravděpodobněji objevit v průběhu 4 hodin po podání sildenafilu. Měl byste pravidelně užívat svou denní dávku alfa-blokátoru, než začnete užívat přípravek Vizarsin, aby se snížila pravděpodobnost nástupu těchto příznaků. Lékař může zahájit Vaši léčbu přípravkem Vizarsin v nižší dávce 25 mg.
Přípravek Vizarsin s jídlem, pitím a alkoholem
Přípravek Vizarsin může být užíván s jídlem i bez jídla. Po požití těžkého jídla se však účinek přípravku Vizarsin může projevit později. Před užitím tablety by měla být Vaše ústa prázdná.
Požití alkoholu může dočasně zhoršit schopnost dosáhnout erekce. Abyste dosáhl co nejvyššího účinku tohoto přípravku, doporučujeme před užitím přípravku Vizarsin nepožívat větší množství alkoholu.
Těhotenství, kojení a plodnost
Přípravek Vizarsin není určen pro použití u žen.
Řízení dopravních prostředků a obsluha strojů
Přípravek Vizarsin může způsobit závratě a narušit vidění. Měl byste proto znát svoji reakci na přípravek Vizarsin před tím, než budete řídit motorová vozidla nebo obsluhovat stroje.
Přípravek Vizarsin obsahuje aspartam (E951) a sorbitol (E420)
Aspartam je zdroj fenylalaninu, který může být škodlivý pro lidi trpící fenylketonurií.
Přípravek Vizarsin obsahuje sorbitol. Pokud Vám lékař řekl, že nesnášíte některé cukry, poraďte se se svým lékařem, než začnete tento léčivý přípravek užívat.
3. Jak se přípravek Vizarsin užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý, poraďte se se svým lékařem nebo lékárníkem.
Doporučená zahajovací dávka je 50 mg.
Neužívejte více než jednu tabletu přípravku Vizarsin denně.
Neužívejte přípravek Vizarsin tablety dispergovatelné v ústech společně s jinými lékovými formami přípravku Vizarsin.
Užijte přípravek Vizarsin zhruba jednu hodinu před plánovaným pohlavním stykem.
Vizarsin tablety jsou křehké. Neměly by se protlačovat fólií blistru, protože by se tím mohla tableta poškodit. Nedotýkejte se tablety vlhkou rukou, protože by se tableta mohla rozpadnout. Vyjměte tabletu z obalu následujícím způsobem:
1 tableta v blistru:

4 tablety v blistni:

1. Uchopte blistr za okraje a oddělte jednu buňku blistru od zbytku opatrným odtržením podél perforace.
2. Táhněte za označený okraj fólie a fólii úplně sloupněte.
3. Vyklopte tabletu do své dlaně.
4. Jakmile vyjmete tabletu z obalu, položte ji na jazyk.
Během několika sekund se začne tableta v ústech rozpadat, následně ji můžete s vodou nebo bez vody spolknout. Ústa by měla být při pokládání tablety na jazyk prázdná.
Jestliže cítíte, že přípravek Vizarsin účinkuje příliš silně nebo naopak slabě, sdělte to svému lékaři nebo lékárníkovi.
Přípravek Vizarsin Vám pomůže dosáhnout erekce, jen pokud dojde k sexuálnímu dráždění. Doba, po které začne přípravek účinkovat, je u každého člověka odlišná, ale obvykle se pohybuje mezi půl hodinou až hodinou. Pokud přípravek Vizarsin užijete společně s těžkým jídlem, může se nástup účinku oddálit.
Pokud po užití přípravku Vizarsin nedosáhnete erekce nebo je erekce nedostatečná pro celý pohlavní styk, poraďte se o dalším postupu se svým lékařem.
Jestliže jste užil více přípravku Vizarsin, než jste měl
Můžete zaznamenat zvýšený výskyt nežádoucích účinků a jejich závažnosti. Dávka vyšší než 100 mg nezlepšuje dále účinnost.
Neužívejte více tablet, než Vám bylo lékařem doporučeno.
Vyhledejte svého lékaře, pokud užijete více tablet, než jste měl.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Nežádoucí účinky hlášené v souvislosti s užitím přípravku Vizarsin bývají obvykle mírné až středně závažné a krátkého trvání.
Pokud se u Vás vyskytl některý z následujících nežádoucích účinků, přestaňte přípravek Vizarsin užívat a okamžitě vyhledejte lékařskou pomoc:
- Alergická reakce - k té dochází méně často (může postihnout až 1 ze 100 pacientů)
Příznaky zahrnují náhlou dýchavičnost, potíže s dýcháním nebo závrať, otok očních víček,
obličeje, rtů nebo hrdla.
Bolest na hrudníku - k té dochází méně často
Pokud se objeví v průběhu nebo po skončení pohlavního styku:
- posaďte se do polosedu a snažte se odpočívat.
- neužívejte na léčbu bolesti na hrudníku nitráty.
Prodloužená a občas bolestivá erekce - k té dochází vzácně (může postihnout až 1 z 1000 pacientů)
Pokud u Vás dojde k erekci, která trvá déle než 4 hodiny, okamžitě vyhledejte lékaře. Náhlé zhoršení nebo ztráta zraku - k tomu dochází vzácně
Těžké kožní reakce - k těm dochází vzácně
Příznaky mohou zahrnovat silné olupování a otok kůže, tvorbu puchýřů v ústech, na genitálu a kolem očí, horečku.
Křečové stavy nebo záchvaty - k těm dochází vzácně
Další nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 pacientů): bolest hlavy.
Časté (mohou postihnout až 1 z 10 pacientů): nevolnost, zarudnutí v obličeji, nával horka (příznaky zahrnují náhlý pocit horka v horní části těla), zažívací potíže, změny barevného vidění, rozmazané vidění, poruchy vidění, ucpaný nos a závrať.
Méně časté (mohou postihnout až 1 ze 100 pacientů): zvracení, kožní vyrážka, podráždění oka, překrvené/červené oči, bolest očí, vidění záblesků světla, zrakový vjem jasu, citlivost na světlo, slzení očí, bušení srdce, zrychlený srdeční puls, vysoký krevní tlak, nízký krevní tlak, bolest svalů, ospalost, snížená citlivost na dotek, porucha rovnováhy, zvonění v uších, sucho v ústech, ucpané vedlejší dutiny nosní, zánět nosní sliznice (příznaky zahrnují rýmu, kýchání a ucpaný nos), bolest horní poloviny břicha, refluxní choroba jícnu (příznaky zahrnují pálení žáhy), přítomnost krve v moči, bolest paží nebo nohou, krvácení z nosu, pocit horka a únava.
Vzácné (mohou postihnout až 1 z 1000 pacientů): mdloby, cévní mozková příhoda, srdeční infarkt, nepravidelný srdeční puls, dočasné snížení průtoku krve některými částmi mozku, stažení hrdla, znecitlivěná ústa, krvácení na očním pozadí, dvojité vidění, snížená zraková ostrost, neobvyklý pocit v oku, otok oka nebo očního víčka, malé částice nebo tečky ve vidění, vidění světelných kruhů kolem světel, rozšíření zornice, změna zabarvení očního bělma, krvácení z penisu, přítomnost krve ve spermatu, suchost v nose, zduření uvnitř nosu, pocit podrážděnosti a náhlé zhoršení nebo ztráta sluchu.
Po uvedení přípravku na trh byly vzácně hlášeny případy nestabilní anginy pectoris (onemocnění srdce) a náhlé smrti. Je třeba poznamenat, že většina mužů, ale ne všichni, kteří měli tyto nežádoucí účinky, měla potíže se srdcem již před užitím přípravku. Není možné určit, zda tyto příhody měly přímou souvislost s užitím přípravku Vizarsin.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Vizarsin uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za „EXP:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek Vizarsin obsahuje
- Léčivou látkou je sildenafilum. Jedna tableta dispergovatelná v ústech obsahuje sildenafilum 100 mg.
- Pomocnými látkami jsou hyprolosa (E463), mannitol (E421), aspartam (E951), neohesperidin-dihydrochalkon (E959), silice máty kadeřavé, silice máty peprné (obsahuje sorbitol (E420)), krospovidon, křemičitan vápenatý, magnesium-stearát (E572).
Jak přípravek Vizarsin vypadá a co obsahuje toto balení
Bílé až téměř bílé, kulaté, mírně bikonvexní tablety, s možnými tmavšími tečkami.
Vizarsin tablety dispergovatelné v ústech se dodávají v krabičkách po 1 tabletě dispergovatelné v ústech v blistrech a také v krabičkách po 2 x 1, 4 x 1, 8 x 1, 12 x 1 nebo 24 x 1 tabletě dispergovatelné v ústech v perforovaných jednodávkových blistrech.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci
KRKA, d.d., Novo mesto, Smaiješka cesta 6, 8501 Novo mesto, Slovinsko Výrobce
KRKA, d.d., Novo mesto, Šmaiješka cesta 6, 8501 Novo mesto, Slovinsko TAD Pharma GmbH, Heinz-Lohmann-StraBe 5, 27472 Cuxhaven, Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Eunrapnu
KPKA Etnrapnn EOOfl Ten.: + 359 (02) 962 34 50
Česká republika KRKA ČR, s.r.o.
Tel: + 420 (0) 221 115 150
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
Magyarország
KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490
Malta
E. J. Busuttil Ltd.
Tel: + 356 21 445 885
Danmark
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Tel: + 49 (0) 4721 606-0
Tel: +32 (0) 489 304 091 (BE)
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXXáSa QUALIA PHARMA S.A. Tn^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
Espaňa KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmaceutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Románia KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq Kipa Pharmacal Ltd. Tn^: + 357 24 651 882 |
Sverige KRKA Sverige AB Tel: + 46 (0)8 643 67 66 (SE) |
|
Latvija KRKA Latvija SIA Tel: + 371 6 733 86 10 |
United Kingdom Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888 |
Tato příbalová informace byla naposledy revidována
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
103