Vakcína Proti Pandemické Chřipce H5N1 Medimmune
PŘÍLOHA I
SOUHRN ÚDAJŮ O PŘÍPRAVKU
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Podrobnosti o hlášení nežádoucích účinků viz bod 4.8.
1. NÁZEV PŘÍPRAVKU
Vakcína proti pandemické chřipce H5N1 MedImmune Nosní sprej, suspenze
vakcína proti pandemické chřipce (H5N1) (živá atenuovaná, nosní)
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna dávka (0,2 ml) obsahuje:
Reasortant-virus influenzae * (vivum attenuatum) následujícího kmene**: A/Vietnam/1203/2004 (H5N1) kmen
(A/Vietnam/1203/2004, MEDI 0141000136) 107,0±0,5 FFU***
* pomnožený v oplodněných slepičích vejcích ze zdravých chovů drůbeže.
** produkovaných v buňkách VERO pomocí technologie reverzní genetiky. Tento přípravek obsahuje geneticky modifikované organizmy (GMO).
*** fluorescenční fokální jednotky (fluorescent focus units, FFU).
Tato vakcína odpovídá doporučení SZO a rozhodnutí EU pro pandemickou vakcínu.
Tato vakcína může obsahovat zbytky následujících látek: vaječné bílkoviny (např. ovalbumin) a gentamicin.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Nosní sprej, suspenze
Suspenze je bezbarvá až světle žlutá, čirá až opalescentní. Mohou být přítomny malé bílé částice.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Profylaxe chřipky v případě oficiálně potvrzené pandemické situace u dětí a dospívajících ve věku od 12 měsíců do méně než 18 let.
Vakcína proti pandemické chřipce H5N1 MedImmune má být použita podle oficiálních doporučení.
4.2 Dávkování a způsob podání
Dávkování
Děti a dospívající ve věku od 12 měsíců do méně než 18 let 0,2 ml (podáno jako 0,1 ml do každé nosní dírky).
Dětem a dospívajícím se doporučeje podat 2 dávky. Druhá dávka se má podat v odstupu nejméně 4 týdny.
Děti mladší než 12 měsíců
Z důvodů bezpečnosti - ve smyslu zvýšené frekvence hospitalizace a sípotu v této populaci - se Vakcína proti pandemické chřipce H5N1 MedImmune nemá používat u kojenců mladších než 12 měsíců (viz bod 4.8).
Způsob podání
Imunizace se musí uskutečnit nosním podáním.
Vakcínu proti pandemické chřipce H5N1 nepodávejte injekčně.
Vakcína proti pandemické chřipce H5N1 MedImmune se podává jako dávka rozdělená do obou nosních dírek. Po podání jedné poloviny dávky do jedné nosní dírky podejte okamžitě nebo po krátké době druhou polovinu dávky do druhé nosní dírky. Během podávání vakcíny může pacient normálně dýchat - není potřeba aktivně inhalovat nebo potahovat.
Pokyny k podání naleznete v bodě 6.6.
4.3 Kontraindikace
Anamnéza anafylaktické (tj. život ohrožující) reakce na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1 (např. na želatinu), nebo na gentamycin (možné stopové zbytky látky), na vejce nebo vaječné bílkoviny (např. ovalbumin). Nicméně za pandemické situace může být vhodnější podat vakcínu a zajistit, aby bylo v případě potřeby k okamžité dispozici zařízení pro resuscitaci.
4.4 Zvláštní upozornění a opatření pro použití
Opatrnosti je zapotřebí při aplikaci vakcíny osobám se známou hypersenzitivitou (jinou než anafylaktická reakce) na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1 nebo na stopové zbytky látek (gentamycin, vejce nebo vaječné bílkoviny, ovalbumin). Pro případ anafylaktické příhody nebo hypersenzitivity po podání vakcíny musí být vždy k dispozici odpovídající lékařská péče a dohled.
Ohledně Vakcíny proti pandemické chřipce H5N1 MedImmune u dětí a dospívajících mladších 18 let léčených salicyláty nejsou k dispozici žádné údaje. Vzhledem ke spojitosti Reyova syndromu se salicyláty a infekcí divokým chřipkovým virem má zdravotnický personál zhodnotit možná rizika podání vakcíny oproti možným přínosům v pandemické situaci (viz bod 4.5).
Imunitní odpověď u pacientů s endogenně či iatrogenně podmíněnou imunosupresí nemusí být dostatečná.
U osob s klinicky významným imunodeficitem nejsou k dispozici žádné údaje. V pandemické situaci je nutné, aby lékař vyhodnotil potenciální přínos, alternativní možnosti a rizika spojená s podáním vakcíny dětem a dospívajícím s klinicky významným imunodeficitem v důsledku zdravotního stavu nebo imunosupresivní terapie jako například: akutní a chronická leukémie; lymfom; symptomatická infekce HIV; buněčné imunodeficity a podávání glukokortikoidů ve vysokých dávkách.
Bezpečnost živé atenuované vakcíny proti sezónní chřipce (LAIV) u dětí s těžkým astmatem a aktivním sípotem nebyla dostatečně zkoumána. Zdravotnický personál má zhodnotit přínosy a možná rizika podání Vakcíny proti pandemické chřipce H5N1 MedImmune těmto osobám.
Ve studii se sezónní trivalentní živou oslabenou vakcínou proti chřipce (T/LAIV) byl u dětí ve věku od 12-23 měsíců pozorován zvýšený výskyt lékařsky závažného sípotu (viz bod 4.8).
Příjemci vakcíny mají být informováni o tom, že Vakcína proti pandemické chřipce H5N1 MedImmune je vakcínou obsahující živý atenuovaný virus a má tudíž potenciál k přenosu na imunokompromitované osoby. Příjemci valcíny se mají pokusit omezit kontakt s těžce imunokompromitovanými osobami (např. osobami po transplantaci kostní dřeně vyžadující izolaci) na nejvyšší možnou míru po dobu 1-2 týdnů po vakcinaci. Šíření viru H5N1 vakcíny u dospělých bylo velmi omezené. V klinických studiích s Vakcínou proti pandemické chřipce H5N1 MedImmune byl nejvyšší výskyt při izolaci viru vakcíny 1-2 dny po vakcinaci. V případech, kdy je kontakt se závažně imunokompromitovanými osobami nevyhnutelný, je třeba zvážit potenciální riziko přenosu chřipkového viru vakcíny oproti riziku nákazy a přenosu chřipkového viru divokého typu.
Vakcína proti pandemické chřipce H5N1 MedImmune nesmí být podána v průběhu 48 hodin po ukončení léčby chřipkovými antivirotiky.
O bezpečnosti intranazálního podání Vakcíny proti pandemické chřipce H5N1 MedImmune dětem s nekorigovanými malformacemi lebky a obličeje neexistují žádné údaje.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Vakcína proti pandemické chřipce H5N1 MedImmune se nemá podávat dětem a dospívajícím, kterým je podávána léčba salicyláty (viz bod 4.4). U dětí a dospívajících se nemají používat salicyláty po dobu 4 týdnů po vakcinaci, není-li klinicky indikováno, protože byl hlášen výskyt Reyeova syndromu po použití salicylátů během infekce chřipkovým virem divokého typu.
Souběžné podání Vakcíny proti pandemické chřipce H5N1 MedImmune s inaktivovanými vakcínami nebo sezónní vakcínou Fluenz Tetra nebylo hodnoceno.
Data ze zkoumání souběžně podávané trivalentní vakcíny (T/LAIV) s živými atenuovanými vakcínami proti spalničkám, příušnicím, zarděnkám (MMR), planým neštovicím a s perorálně podávanou vakcínou proti polioviru jsou dostupná a potvrzují, že souběžné podání vakcíny proti pandemické chřipce H5N1 MedImmune a těchto živých vakcín může být akceptovatelné.
Na základě potenciálu chřipkových antivirotik snižovat účinnost Vakcíny proti pandemické chřipce H5N1 MedImmune se nedoporučuje podávat vakcínu do 48 hodin po ukončení protivirové léčby chřipky. Podání antivirotik proti chřipce během dvou týdnů po vakcinaci může ovlivnit odpověď na podání vakcíny.
Jestliže se souběžně podávají antivirotika proti chřipce s Vakcínou proti pandemické chřipce H5N1 MedImmune, má být podle potřeby zvážena revakcinace na základě klinického úsudku.
4.6 Fertilita, těhotenství a kojení
Údaje o podávání Vakcíny proti pandemické chřipce H5N1 MedImmune těhotným ženám nejsou dostupné.
Existují omezené údaje o použití T/LAIV a sezónní vakcíny Fluenz Tetra u těhotných žen.
U 138 těhotných žen, které měly záznam o podání T/LAIV v databázi pojistných událostí zdravotního pojištění v USA, nebyl žádný důkaz o významných nežádoucích příhodách. Ve 27 hlášeních v Systému hlášení nežádoucích příhod vakcín (VAERS) v USA o podávání přípravku T/LAIV těhotným ženám nebyly pozorovány žádné neobvyklé vzory komplikací těhotenství nebo událostí u plodu. Podobně ve 113 zprávách o těhotných ženách v systému VAERS, kterým byla podána monovalentní živá intranazální vakcína MedImmune (H1N1) 2009, nebyly v průběhu těhotenství pozorovány žádné neobvyklé komplikace nebo účinky na plod.
Vývojové studie reprodukční toxicity na zvířatech s vakcínami T/LAIV a Fluenz Tetra nenaznačují přímé nebo nepřímé škodlivé účinky. Údaje po uvedení na trh z nechtěného podání sezónních vakcín v průběhu těhotenství poskytují určité ujištění.
Zdravotnický personál má zhodnotit přínosy a možná rizika podání Vakcíny proti pandemické chřipce H5N1 MedImmune těhotným ženám.
Kojení
Není známo, zda se Vakcína proti pandemické chřipce H5N1 MedImmune vylučuje do lidského mateřského mléka. Jelikož se některé viry vylučují do lidského mateřského mléka, vakcína nemá být podávána během kojení.
Fertilita
Neexistují žádné údaje o možných účincích Vakcíny proti pandemické chřipce H5N1 MedImmune na mužskou a ženskou fertilitu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Vakcína proti pandemické chřipce H5N1 MedImmune nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Hodnocení bezpečnostního profilu Vakcíny proti pandemické chřipce H5N1 MedImmune vychází z omezeného počtu dospělých subjektů.
V klinických studiích byl bezpečnostní profil Vakcíny proti pandemické chřipce H5N1 MedImmune byl srovnatelný s bezpečnostním profilem sezónních vakcín T/LAIV a Fluenz Tetra (Další informace viz bod 5.1).
Klinické studie hodnotily výskyt nežádoucích účinků u 59 dospělých ve věku od 18 do 49 let, jimž byla podána alespoň jedna dávka Vakcíny proti pandemické chřipce H5N1 MedImmune. Další údaje byly získány od 289 dospělých zařazených ve studiích kandidátských vakcín na dalších 7 subtypů chřipky a od 240 dospělých a 259 dětí zařazených ve studiích monovalentní vakcíny proti pandemické chřipce 2009 H1N1.
Nejčastějšími nežádoucími účinky pozorovanými v klinických studiích prováděných s Vakcínou proti pandemické chřipce H5N1 MedImmune u zdravých dospělých osob byly bolest hlavy (25,4 %) a infekce horních cest dýchacích (10,2 %).
Pediatrická populace
Seznam nežádoucích účinků
Z klinických studií a poregistračního sledování s T/LAIV a Fluenz Tetra u více než 110000 dětí a dospívajících od 2 do 17 let věku byly hlášeny následující četnosti nežádoucích účinků:
Velmi časté (> 1/10)
Časté (> 1/100 až < 1/10)
Méně časté (> 1/1000 až < 1/100)
Vzácné (> 1/10000 až < 1/1,000)
Velmi vzácné (< 1/10000)
Poruchy imunitního systému
Méně časté: Hypersenzitivní reakce (včetně edému obličeje, kopřivky a velmi vzácných anafylaktických reakcí)
Poruchy metabolismu a výživy Velmi časté: Snížená chuť k jídlu
Poruchy nervového systému Velmi časté: Bolest hlavy
Respirační, hrudní a mediastinální poruchy
Velmi časté: Nazální kongesce/rinorea Méně časté: Epistaxe
Poruchy kůže a podkožní tkáně Méně časté: Vyrážka
Poruchy svalové a kosterní soustavy a pojivové tkáně Časté: Myalgie
Celkové poruchy a reakce v místě aplikace Velmi časté: Malátnost Časté: Horečka
Popis vybraných nežádoucích účinků
Děti mladší než 12 měsíců
Vakcína proti pandemické chřipce H5N1 MedImmune není indikována pro použití u kojenců mladších než 12 měsíců (viz bod 4.2). Bezpečnost a účinnost vakcíny u této populace nebyla stanovena. Nejsou dostupné žádné údaje.
V kontrolované klinické studii (MI-CP111) s aktivní kontrolou provedené s T/LAIV ve srovnání s injekční trivalentní vakcínou proti chřipce byl pozorován zvýšený výskyt případů hospitalizací (z jakékoli příčiny) během 180 dní po poslední dávce vakcinace u dětí ve věku 6-11 měsíců (6,1 % u T/LAIV oproti 2,6 % u injekční vakcíny proti chřipce). Většina případů hospitalizace byla z důvodu infekcí gastrointestinálního a respiračního traktu a došlo k nim po více než 6 týdnech po vakcinaci. Frekvence hospitalizace nebyla zvýšená u pacientů starších než 12 měsíců, kterým byla podána trivalentní živá atenuovaná vakcína proti chřipce (T/LAIV) a frekvence u kojenců a batolat ve věku 12-23 měsíců byla 3,2 % v případě T/LAIV oproti 3,5 % u injekční vakcíny proti chřipce.
Sípot u dětí ve věku do 24 měsíců
Ve stejné studii byl u kojenců a batolat ve věku 6-23 měsíců pozorován během 42 dní zvýšený výskyt případů sípotu (5,9 % u T/LAIV vs. 3,8 % u injekční vakcíny proti chřipce). Obdobná četnost výskytu případů sípotu u kojenců a batolat ve věku 12-23 měsíců byla 5,4 %, resp. 3,6 % pro T/LAIV, resp. injekční vakcínu proti chřipce. Celkem bylo v důsledku lékařsky závažného sípotu hospitalizováno 20 subjektů (12 u T/LAIV, 0,3 %, 8 u injekční vakcíny proti chřipce, 0,2 %). Nebyla hlášena žádná úmrtí v důsledku sípotu a u žádného hospitalizovaného dítěte nebyla potřebná mechanická podpora ventilace nebo přijetí na jednotku intenzivní péče. Četnost sípotu nebyla zvýšena u příjemců T/LAIV ve věku od 24 měsíců.
Chronické stavy
Bezpečnost vakcíny T/LAIV u dětí a dospívajících s mírným až středně těžkým astmatem byla potvrzena, avšak údaje týkající se dětí s jiným plicním onemocněním nebo s chronickým kardiovaskulárním, metabolickým či ledvinovým onemocněním jsou omezené.
Ve studii (D153-P515) u dětí ve věku od 6 do 17 let s astmatem (sezónní T/LAIV: n = 1114, injekční vakcína proti sezónní chřipce: n = 1115) nebyly mezi léčenými skupinami významné rozdíly v četnosti výskytu exacerbací astmatu, střední maximální výdechové rychlosti, skóre dle symptomů astmatu ani skóre dle stupnice nočního probouzení. Četnost výskytu sípotu do 15 dnů po vakcinaci byla nižší u příjemců vakcíny T/LAIV než u příjemců inaktivované vakcíny proti sezónní chřipce (19,5 % vs.
23,8 %, p = 0,02).
Ve studii (AV010) u dětí a dospívajících ve věku od 9 do 17 let s mírným až středně těžkým astmatem (sezónní T/LAIV: n = 24, placebo: n = 24) se primární kritérium bezpečnosti - procentuální změna predikovaného usilovného exspiračního objemu za 1 sekundu (FEVi), měřená před vakcinací a po ní -mezi oběma léčebnými rameny nezměnilo.
Další zvláštní populace:
Jedinci s imunodeficitem
Profil bezpečnosti vakcíny T/LAIV u omezeného počtu subjektů s mírnou až střední poruchou imunity v souvislosti s jinými infekcemi než s HIV, s asymptomatickou nebo mírně symptomatickou infekcí virem HIV nebo karcinomem (solidní nádory a hematologické malignity) byl celkově srovnatelný s profilem bezpečnosti u zdravých jedinců a nepředstavuje nežádoucí vliv. O jedincích s těžkou poruchou imunity nejsou k dispozici žádné údaje (viz bod 4.4). V pandemické situaci je možné uvažovat o použití Vakcíny proti pandemické chřipce H5N1 MedImmune u osob s mírnou až středně těžkou poruchou imunity po zvážení předpokládaných přínosů ve srovnání s možnými riziky u konkrétní osoby.
Zkušenosti po uvedení sezónní T/LAIV na trh
Dále byly velmi vzácně pozorovány případy syndromu Guillain-Barré a exacerbace symptomů Leighova syndromu (mitochondriální encefalomyopatie).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Po uvedení sezónní vakcíny na trh byly občas hlášeny případy podání dvojnásobku doporučené dávky sezónní vakcíny Fluenz Tetra a sezónní trivalentní živé intranazální vakcíny proti chřipce (T(LAIV). Hlášené nežádoucí účinky byly podobné těm, které byly pozorovány u doporučené jedné dávky T/LAIV a Fluenz Tetra.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: vakcíny proti chřipce, živá atenuovaná vakcína; ATC kód: J07BB03
Kmen viru ve Vakcíně proti pandemické chřipce H5N1 MedImmune je (a) přizpůsobený chladu (ca); (b) citlivý na teplotu (ts); and (c) atenuovaný (att). Aby došlo k posílení ochranné imunity, virus musí infikovat sliznici nosohltanu příjemce vakcíny a musí dojít k replikaci viru v těchto buňkách.
Klinické studie
Tato část popisuje klinické zkušenosti pozorované u dospělých ve třech pivotních studiích Vakcíny proti pandemické chřipce H5N1 MedImmune. Za podpůrné studie jsou dále považovány studie s vakcínou 2009 H1N1 LAIV MedImmune proti pandemické chřipce a T/LAIV MedImmune proti sezónní chřipce, neboť všechny tyto vakcíny se vyrábí stejným postupem, podávají se stejnou cestou a byly zkoumány primárně u neočkovaných jedinců.
Paediatric studies
Vakcína H1N1 VAIV proti pandemické chřipce u dětí ve věku 2 až 17 let
V klinické studii MI-CP217 byla hodnocena bezpečnost a popisovaná imunogenita živé atenuované monovalentní vakcíny proti viru chřipky (získané z kmene A/California/7/2009), vyvinuté pro pandemii H1N1 v r. 2009, u celkem 326 randomizovaných subjektů (259 subjektů - monovalentní vakcína; 65 subjektů - placebo) a 324 subjektům byla podána jedna dávka hodnoceného přípravku. 319 z těchto subjektů byla podána druhá dávka (256 subjektům monovalentní vakcína; 63 subjektům placebo).
U dětí bez ohledu na výchozí sérologický status dosahovala sérologická odpověď po podání monovalentní vakcíny hodnot 7,8 %, resp. 11,1 % 15. den resp. 29. den a 32,0 % 57. den. U příjemců placeba bez ohledu na výchozí sérologický status dosahovala sérologická odpověď hodnot 6,3 % 15. den, resp. 29. den a 14,5 % 57. den. Sérologická odpověď byla mírně vyšší u subjektů séronegativních při úvodním vyšetření. Ve sledovací studii prováděné v centrech pro kontrolu nemocí v USA (Griffin et al, 2011) byla stanovena 81,9% účinnost vakcíny LAIV proti pandemické chřipce H1N1 u dětí ve věku od 2 do 9 let (95% CI:13,6; 96,2).
Účinnost T/LAIV
Údaje o účinnosti vakcíny T/LAIV u pediatrické populace zahrnují 9 kontrolovaných studií s více než 20000 kojenců a batolat, dětí a dospívajících, prováděných během 7 chřipkových sezón. Čtyři placebem kontrolované studie zahrnovaly revakcinaci v druhé sezóně. Vakcína T/LAIV prokázala lepší účinnost ve 3 kontrolovaných studiích s aktivní kontrolou ve formě vakcíny proti chřipce podávané injekčně. Souhrn výsledků účinnosti u pediatrické populace je uveden v tabulkách 1 a 2.
Tabulka 1 Účinnost T/LAIV v placebem kontrolovaných pediatrických studiích
|
Číslo studie |
Region |
Věkové rozmezí3 |
Počet účastníků studieb |
Chřipková sezóna |
Účinnost (95% CI)c Shodné kmeny |
Účinnost (95% CI)c Všechny kmeny bez ohledu na shodnost |
|
D153-P502 |
Evropa |
6 až 35 m |
1616 |
2000-2001 |
85,4 % (74,3; 92,2) |
85,9 % (76,3; 92,0) |
|
1090 |
2001-2002 |
88,7 % (82,0; 93,2) |
85,8 % (78,6; 90,9) | |||
|
D153-P504 |
Afrika, Latinská Amerika |
6 až 35 m |
1886 |
2001 |
73,5 % (63,6; 81,0)d |
72,0 % (61,9; 79,8)d |
|
680 |
2002 |
73,6 % (33,3; 91,2) |
46,6 % (14,9; 67,2) | |||
|
D153-P513 |
Asie/Oceánie |
6 až 35 m |
1041 |
2002 |
62,2 % (43,6; 75,2) |
48,6 % (28,8; 63,3) |
|
D153-P522 |
Evropa, Asie/Oceánie, Latinská Amerika |
11 až 24 m |
1150 |
2002-2003 |
78,4 % (50,9; 91,3) |
63,8 % (36,2; 79,8) |
|
D153-P501 |
Asie/Oceánie |
12 až 35 m |
2764 |
2000-2001 |
72,9 % (62,8; 80,5) |
70,1 % (60,9; 77,3) |
|
1265 |
2001-2002 |
84,3 % e (70,1; 92,4) |
64,2 % e (44,2; 77,3) | |||
|
AV006 |
USA |
15 až 71m |
1259 |
1996-1997 |
93,4 % (87,5; 96,5) |
93,4 % (87,5; 96,5) |
|
1358 |
1997-1998 |
100 % (63,1; 100) |
87,1 % (77,7; 92,6)f |
a m = měsíce
b Počet účastníků studie pro analýzu účinnosti v roce 1.
c Snížení počtu kultivačně prokázaných chřipkových onemocnění v porovnání s placebem. d Údaje prezentované v klinické studii D153-P504 jsou pro účastníky studie, kterým byly podány dvě dávky zkoumané vakcíny. U dříve neočkovaných účastníků studie, kteří dostali jednu dávku v 1. roce byla účinnost 57,7 % (95% CI: 44,7; 67,9), resp. 56,3 % (95% CI: 43,1; 66,7), což potvrzuje nutnost podání dvou dávek vakcíny u dříve neočkovaných dětí.
e
U účastníků studie D153-P501, kteří dostali 2 dávky v 1. roce a placebo v 2. roce, byla v 2. roce účinnost 56,2 % (95% CI: 30,5; 72,7), resp. 44,8 % (95% CI: 18,2; 62,9), což potvrzuje nutnost revakcinace ve druhé sezóně.
f Hlavní cirkulující kmen byl antigenově odlišný od kmenu H3N2 obsaženém ve vakcíně; účinnost proti neshodnému kmenu A/H3N2 byla 85,9 % (95% CI:75,3; 91,9).
Relativní účinnost vakcíny T/LAIV v pediatrických studiích s aktivní kontrolou ve formě sezónní vakcíny podávané injekčně
|
Číslo studie |
Region |
Věkové rozmezí® |
Počet účastníků studie |
Chřipková sezóna |
Zvýšená účinnost (95% CI)b Shodné kmeny |
Zvýšená účinnost (95% CI)b Všechny kmeny bez ohledu na shodnost |
|
MI-CP111 |
USA, Evropa, Asie/Oceánie |
6 až 59 m |
7852 |
2004-2005 |
44,5 % (22,4; 60,6) méně případů než s vakcínou podávanou injekčně |
54,9 % (45,4;62,9)c méně případů než s vakcínou podávanou injekčně |
|
D153-P514 |
Evropa |
6 až 71 m |
2085 |
2002-2003 |
52,7 % (21,6; 72,2) méně případů než s vakcínou podávanou injekčně |
52,4 % (24,6; 70,5)d méně případů než s vakcínou podávanou injekčně |
|
D153-P515 |
Evropa |
6 až 17 r |
2211 |
2002-2003 |
34,7 % (3,9; 56,0) méně případů než s vakcínou podávanou injekčně |
31,9% (1,1;53,5) méně případů než s vakcínou podávanou injekčně |
a m = měsíce, r = roky. Věkové rozmezí jak je popsáno v protokolu studie.
b Snížení počtu kultivačně prokázaných chřipkových onemocnění v porovnání s vakcínou proti chřipce podávanou injekčně.
c Vakcína T/LAIV vykázala o 55,7 % (39,9; 67,6) méně případů onemocnění v porovnání s vakcínou proti chřipce podávanou injekčně u 3686 kojenců a batolat ve věku 6-23 měsíců a 54,4 % (41,8; 64,5) méně případů u 4166 dětí ve věku 24-59 měsíců.
d Vakcína T/LAIV vykázala o 64,4 % (1,4; 88,8) méně případů onemocnění v porovnání s vakcínou proti chřipce podávanou injekčně u 476 kojenců a batolat ve věku 6-23 měsíců a o 48,2 % (12,7;70,0) méně případů u 1609 dětí ve věku 24-71 měsíců.
Tabulka 2
Vakcína P/LAIV H5N1
Evropská agentura pro léčivé přípravky udělila odklad povinnosti předložit výsledky studií s Vakcínou proti pandemické chřipce H5N1 MedImmune u jedné nebo více podskupin pediatrické populace při prevenci chřipkové infekce. Informace o použití u dětí viz bod 4.2.
Tento léčivý přípravek byl registrován postupem tzv. podmíněného schválení. Znamená to, že jsou očekávány další důkazy o jeho přínosech. Evropská agentura pro léčivé přípravky každoročně vyhodnotí jakékoli nové informace týkající se tohoto přípravku a tento souhrn údajů o přípravku bude podle potřeby aktualizován.
Studie u dospělých
Dospělí ve věku od 18 do 49 let
V klinické studii CIR 217 byla hodnocena bezpečnost, infekčnost a imunogenita živé atenuované vakcíny získané z izolátu chřipky A/Vietnam/1203/2004 (H5N1) u 21 subjektů, kterým byla podána jedna střední infekční dávka 106,7 tkáňové kultury (TCID50), přičemž 18 z těchto subjektů byla po 4-8 týdnech podána druhá dávka. Dalším 21 subjektům byla podána jedna dávka viru vakcíny 107,5 TCID50, přičemž 19 z těchto subjektů byla po 4-8 týdnech podána druhá dávka. Po 1 nebo 2 dávkách vakcíny 106,7 TCID50 bylau 10 % subjektů zjištěna inhibice hemaglutinace (HAI), IgA séroodpovědi a sekreční IgA odpovědi ve výplachu z nosu u 24 % subjektů. Po 1 nebo 2 dávkách vakcíny 107,5 TCID50 byly u 10 %, resp. 52 % subjektů zjištěny HAI, resp. IgA séroodpovědi a IgA odpovědi
v sekretu z nosní sliznice u 19 % subjektů.
V klinické studii CIR 239 byla hodnocena bezpečnost, infekčnost a imunogenita živé atenuované vakcíny získané z izolátu chřipky A/Hong Kong/213/2003 (H5N1) u 17 subjektů, kterým byla intranazálně v izolaci podána jedna dávka vakcíny 107,5 TCID50, přičemž 16 z těchto subjektů byla po 4-8 týdnech podána druhá dávka. Po první nebo po druhé dávce vakcíny nebyly u žádného subjektu zjištěny HAI odpovědi. Séroodpověď IgA i odpověď ve výplachu z nosu byly zjištěny u 18 % subjektů.
Dospělí ve věku od 22 do 54 let
Klinická studie CIR 277 hodnotila, zda osoby, kterým byly dříve podány živé atenuované vakcíny proti pandemické chřipce H5N1, byly primárně imunizovány, nebo se u nich vytvořila dlouhodobá imunita, kterou by bylo možno zjistit po následném podání inaktivované vakcíny proti H5N1. Do studie bylo zařazeno 69 subjektů v 5 skupinách: Ve skupině 1 bylo 11 subjektů, kterým byly v letech 2006-2007 podány 2 dávky živé atenuované vakcíny proti pandemické chřipce (P/LAIV) s kmenem A/Vietnam/1203/2004 H5N1; ve skupině 2 bylo 10 subjektů, kterým byly v r. 2007 podány 2 dávky P/LAIV s kmenem A/Hong Kong/213/2003 H5N1; ve skupině 3 bylo 8 subjektů, kterým byly v r. 2010 podány 2 dávky P/LAIV s kmenem A/British Columbia/CN-6/2004 H7N3 (kontrolní skupina P/LAIV); ve skupině 4 i ve skupině 5 bylo 20 subjektů, které nebyly dříve imunizovány vakcínou LAIV a dosud se nesetkaly s virem H5. Subjektům ve skupinách 1 až 4 byla podána jedna 45gg dávka inaktivované vakcíny proti pandemické chřipce (P/IIV) s kmenem A/Vietnam/1203/2004, kdežto subjektům ve skupině 5 byly podány 2 dávky v intervalu přibližně 28 dnů.
U subjektů primárně imunizovaných kmenem P/LAIV H5N1 se po následné expozici inaktivované vakcíně H5N1 vytvořila prudká protilátková odpověď na divoký chřipkový virus H5N1, ačkoliv tyto protilátkové odpovědi nebyly u většiny subjektů po 2 primárních dávkách zjistitelné. Subjekty, které byly primárně imunizovány vakcínou P/LAIV obsahující kmen A/Vietnam/1203/2004 nebo vakcínou P/LAIV obsahující kmen A/Hong Kong/213/2003, měly podstatně lepší odpověď na jednu dávku inaktivované vakcíny H5N1 než subjekty, které vakcínou P/LAIV imunizovány nebyly. Protilátková odpověď subjektů primárně imunizovaných vakcínou P/LAIV obsahující kmen A/Vietnam/1203/2004 byla rovněž silnější než odpověď pozorovaná po 2 dávkách inaktivované vakcíny u subjektů neimunizovaných vakcínou P/LAIV (viz tabulka 3).
Tabulka 3 Protilátková odpověď ve dnech 28 a 56 po podání inaktivované vakcíny H5N1 _v testech mikroneutralizace (MN) a inhibice hemaglutinace (HAI)_
|
Studijní skupina |
P/LAIV iniciální dávka |
Počet dávek inaktivované vakcíny Vietnam 2004 |
Počet subjektů |
28 dnů po podání inaktivované vakcínya |
56 dnů po podání inaktivované vakcínya | ||||||
|
Geometrický střední titr |
Subjekty se 4násobným vzestupem protilátek (procenta)b |
Geometrický střední titr |
Subjekty se 4násobným vzestupem protilátek (procenta)b | ||||||||
|
MN |
HAI |
MN |
HAI |
MN |
HAI |
MN |
HAI | ||||
|
1 |
H5N1 Vietnam 2004 |
1 |
11 |
48 |
87 |
73 |
73 |
25 |
66 |
55 |
82 |
|
2 |
H5N1 Hong Kong 2003 |
1 |
10 |
31 |
29 |
60 |
50 |
22 |
21 |
60 |
40 |
|
4 |
žádná |
1 |
20 |
7 |
8 |
10 |
10 |
4 |
8 |
10 |
10 |
|
5 |
žádná |
2 |
20c |
11 |
15 |
30 |
40 |
19 |
21 |
56 |
50 |
Údaje pro skupinu 3, subjekty, kterým byla na počátku podána vakcína H7N3 P/LAIV, nejsou uvedeny.
aDny jsou vypočteny v relaci k jediné dávce P/IIV ve skupinách 1-4 a po prvních 2 dávkách P/IIV ve skupině 5.
bSérologická odpověď definovaná jako > 4násobný vzestup titru protilátek (> 1:20).
cVzorky séra byly dostupné od 7 subjektů ve skupině 3 v den 28 a od 18 subjektů ve skupině 5 v den 56.
Protilátková odpověď se u subjektů primárně imunizovaných vakcínou P/LAIV H5N1 vytvořila rychle. Sedm z 11 (64 %) subjektů ve skupině 1 (kmen A/Vietnam/1204/2004 [H5N1]) mělo > 4násobné zvýšení titru protilátek HAI do 7. dne po podání inaktivované vakcíny, přičemž hodnota geometrického středního titru (GMT) byla 165 a rozmezí titrů byl u reagujících osob 20 až 1280. Jen 10 % subjektů primárně neimunizovaných vakcínou P/LAIV mělo do 7. dne > 4násobné zvýšení. Protilátkové odpovědi byly u subjektů primárně imunizovaných vakcínou P/LAIV H5N1 také širší.
U subjektů primárně imunizovaných vakcínou P/LAIV H5N1 se vytvořila protilátková odpověď, která neutralizovala 2 nebo více typů virů H5N1 z kmene A/Goose/Guangdong/1996 H5N1, kdežto pouze u několika subjektů ze skupiny se 2 dávkami inaktivované vakcíny H5N1 se vytvořily neutralizační protilátky proti zkříženým kmenům. Afinita protilátek proti doméně HA1 subtypu H5 HA u skupin primárně imunizovaných vakcínou P/LAIV H5N1 byla výrazně vyšší než ve skupině se 2 dávkami inaktivované vakcíny, což korelovalo s neutralizací zkřížených kmenů H5N1.
Podobné odpovědi byly pozorovány u subjektů primárně imunizovaných vakcínou P/LAIV H7N7 a H7N9, u nichž se proběhla prudká protilátková odpověď na odpovídající divoké viry po následné expozici inaktivované vakcíně z téhož subtypu. V případě vakcíny P/LAIV H7N7 byla u 9 z 13 osob zjištěna výrazná přítomnost sérových protilátek MN a HAI, přičemž maximálních titrů bylo dosaženo do 14. dne. V případě vakcíny P/LAIV H7N9 se u 8 ze 14 osob, kterým byla podána jedna dávka vakcíny, resp. u 13 z 16 osob, kterým byly podány dvě dávky vakcíny, vznikla silné protilátková odpověď; maximálních titrů bylo opět dosaženo do 14. dne.
5.2 Farmakokinetické vlastnosti
Není relevantní.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané s Vakcínou proti pandemické chřipce H5N1 MedImmune a sezónními vakcínami T/LAIV a Fluenz Tetra na základě konvenčních neklinických studií toxicity po opakovaném podávání, reprodukční a vývojové toxicity, lokální snášenlivosti a neurovirulence neodhalily žádné zvláštní riziko pro člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Sacharosa
Hydrogenfosforečnan draselný Dihydrogenfosforečnan draselný Želatina (prasečí, typ A)
Arginin-hydrochlorid
Monohydrát natrium-hydrogen-glutamátu
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto nesmí být tento léčivý přípravek mísen s jinými léčivými přípravky.
6.3 Doba použitelnosti 18 týdnů
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C ).
Uchovávejte nosní aplikátor v krabičce, aby byl chráněn před světlem.
Před použitím může být vakcína jednou vyjmuta z chladničky na dobu maximálně až 12 hodin při teplotě do 25 °C. Pokud není vakcína v průběhu těchto 12 hodin spotřebována, je nutné ji zlikvidovat.
6.5 Druh obalu a obsah balení
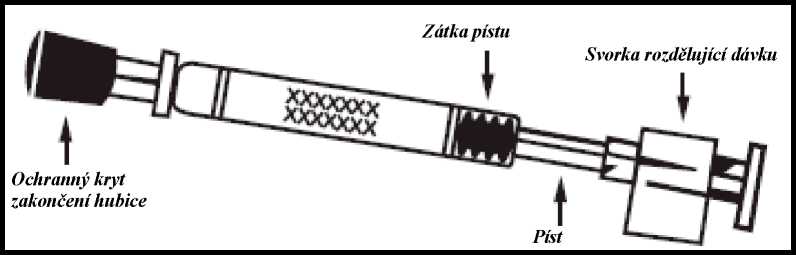
Vakcína proti pandemické chřipce H5N1 MedImmune se dodává jako 0,2 ml suspenze v jednorázovém nosním aplikátoru (sklo třídy I), s hubicí (polypropylen s polyetylenovým přepouštěcím ventilem), ochranným krytem zakončení hubice (syntetická pryž), pístem, zátkou pístu (butylová pryž) a svorkou rozdělující dávku.
Balení po 10.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Podání
Vakcína proti pandemické chřipce H5N1 JE URČENA POUZE PRO NOSNÍ PODÁNÍ.
• NEPOUŽÍVEJTE S JEHLOU. Nepodávejte injekčně.

• Vakcínu proti pandemické chřipce H5N1 MedImmune nepoužívejte po uplynutí doby použitelnosti nebo pokud se rozprašovač jeví jako poškozený, například je-li píst uvolněný nebo je mimo rozprašovač, případně jeví známky netěsnosti.
• Vakcína proti pandemické chřipce H5N1 MedImmune se podává jako rozdělená dávka do obou nosních dírek.
• Po podání poloviny dávky do jedné nosní dírky, podejte ihned nebo krátce poté druhou polovinu dávky do druhé nosní dírky.
• Během podávání vakcíny může pacient normálně dýchat - není potřeba aktivně vdechovat ani popotahovat nosem.
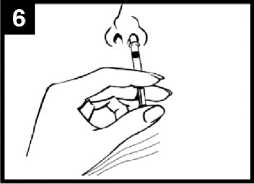
• Pokyny k podání jsou popsány v jednotlivých krocích v diagramu zobrazujícím podání Vakcíny proti pandemické chřipce H5N1 MedImmune (Obrázek 1).
Obrázek 1 Podání Vakcíny proti pandemické chřipce H5N1 MedImmune
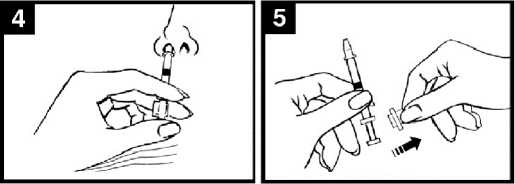
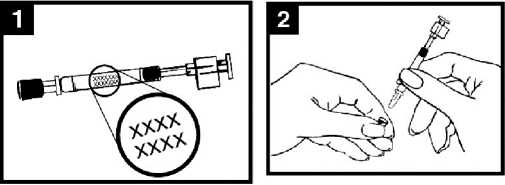
Zkontrolujte datum použitelnosti
Přípravek se musí spotřebovat do data uvedeného na štítku aplikátoru.
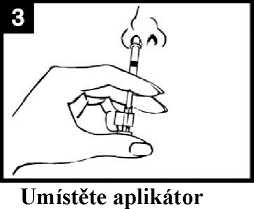
Připravte aplikátor
Sejměte pryžový ochranný kryt zakončení hubice. Neodstraňujte svorku rozdělující dávku na druhém konci aplikátoru.
S pacientem ve vzpřímené poloze umístěte pouze zakončení aplikátoru do nosní dírky tak, aby se zajistilo, že se Vakcína proti pandemické chřipce H5N1 MedImmune dostane do nosu.
Stlačte píst
Jediným pohybem stlačte píst tak rychle, jak je to možné, a až na doraz, dokud Vám to svorka rozdělující dávku dovolí.
Odstraňte svorku rozdělující dávku
Pro podání do druhé nosní dírky uštípněte a odstraňte z pístu svorku rozdělující dávku.
Vstříkněte dávku do druhé nosní dírky
Umístěte pouze zakončení aplikátoru do druhé nosní dírky a jediným pohybem stlačte píst tak rychle, jak je to možné, abyste podal(a) zbylou část vakcíny.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky pro zdravotnický odpad.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
MedImmune, LLC Lagelandseweg 78 6545 CG Nijmegen Nizozemsko (Tel) +31 24 371 7310
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/16/1089/001
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace:
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
A. VÝROBCE BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
E. ZVLÁŠTNÍ POVINNOST USKUTEČNIT POREGISTRAČNÍ OPATŘENÍ PRO PODMÍNĚNOU REGISTRACI PŘÍPRAVKU
A. VÝROBCE BIOLOGICKÉ LÉČIVÉ LÁTKY ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce biologické léčivé látky
MedImmune UK Limited Plot 6, Renaissance Way Boulevard Industry Park Speke,
Liverpool, L24 9JW Velká Británie
Název a adresa výrobce odpovědného za propouštění šarží
MedImmune UK Limited Plot 6, Renaissance Way Boulevard Industry Park Speke,
Liverpool, L24 9JW Velká Británie
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
• Úřední propouštění sarzí
Podle článku 114 směrnice 2001/83/ES bude úřední propouštění šarží provádět některá státní laboratoř nebo laboratoř k tomuto účelu určená.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
Držitel rozhodnutí o registraci předloží první pravidelně aktualizovanou zprávu o bezpečnosti pro tento léčivý přípravek do 6 měsíců od jeho registrace.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
• Další opatření k minimalizaci rizik
Neuplatňuje se.
E. ZVLÁŠTNÍ POVINNOST USKUTEČNIT POREGISTRAČNÍ OPATŘENÍ PRO PODMÍNĚNOU REGISTRACI PŘÍPRAVKU
Tato registrace byla schválena postupem tzv. podmíněného schválení, a proto podle článku 14(7) nařízení (ES) č. 726/2004 držitel rozhodnutí o registraci uskuteční v daném termínu následující opatření:
|
Popis |
Termín splnění |
|
Neintervenční poregistrační studie bezpečnosti (PASS) za účelem dalšího zjištění tolerance Vakcíny proti pandemické chřipce H5N1 MedImmune a odhadu výskytu nežádoucích účinků zvláštního zájmu u dětí a dospívajících. Držitel rozhodnutí o registraci provede observační prospektivní bezpečnostní studii s velkou reprezentativní kohortou dětí a dospívajících ve věku od 12 měsíců do 18 let v průběhu další vyhlášené pandemické situace. Držitel rozhodnutí o registraci předloží závěrečné výsledky této studie. |
Po vyhlášení pandemické situace v EU a po implementaci pandemické vakcíny |
|
K dalšímu potvrzení účinnosti Vakcíny proti pandemické chřipce H5N1 MedImmune držitel rozhodnutí o registraci provede observační studii účinnosti na populaci bydlících dětí a dospívajících ve věku od 12 měsíců do 18 let s laboratorně potvrzenou chřipkou v průběhu další vyhlášené pandemické situace. Držitel rozhodnutí o registraci předloží závěrečné výsledky této studie. |
Po vyhlášení pandemické situace v EU a po implementaci pandemické vakcíny |
|
K dalšímu potvrzení bezpečnosti a reaktogenity Vakcíny proti pandemické chřipce H5N1 MedImmune držitel rozhodnutí o registraci provede otevřenou jednoramennou intervenční studii ke zhodnocení bezpečnosti a imunogenicity P/LAIV u dětí a dospívajících ve věku od 12 měsíců do 18 let v průběhu další vyhlášené pandemické situace. Držitel rozhodnutí o registraci předloží závěrečné výsledky této studie. |
Po vyhlášení pandemické situace v EU a po implementaci pandemické vakcíny |
|
K definování doby použitelnosti Vakcíny proto pandemické chřipce H5N1 MedImmune se specifickým kmenem získá držitel rozhodnutí o registraci stabilitní údaje s aktuálním pandemickým kmenem. Držitel rozhodnutí o registraci předloží závěrečné výsledky této studie. |
V době schválení další pandemické změny |
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
BALENÍ PO 10 JEDNORÁZOVÝCH NOSNÍCH APLIKÁTORECH (V BLISTRU)
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vakcína proti pandemické chřipce H5N1 MedImmune nosní sprej, suspenze
vakcína proti pandemické chřipce (H5N1) (živá atenuovaná, nosní)
|
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK | |
|
Reasortant-virus infuenzae (vivum attenuatum) následujících kmenů: A/Vietnam/1203/2004 (H5N1) | |
|
(A/Vietnam/1203/2004, MEDI 0141000136) v dávce 0,2 ml |
107,°±0,5 FFU |
|
3. SEZNAM POMOCNÝCH LÁTEK | |
Pomocné látky: sacharosa, hydrogenfosforečnan draselný, dihydrogenfosforečnan draselný, želatina (prasečí, typ A), arginin-hydrochlorid, monohydrát natrium-hydrogen-glutamátu, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
nosní sprej, suspenze
10 jednorázových nosních aplikátorů (po 0,2 ml)
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pouze pro nosní podání. Nepodávejte injekčně. Před použitím si přečtěte příbalovou informaci.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9 ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem. Chraňte před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
MedImmune, LLC Lagelandseweg 78 6545 CG Nijmegen Nizozemsko
12. REGISTRAČNÍ CÍSLO/CÍSLA
EU/1/16/1089/001
13. ČÍSLO SARZE
Lot
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
Nevyžaduje se - odůvodnění přijato.
17. JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD
2D čárový kód s jedinečným identifikátorem.
18. JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM
PC:
SN:
NN:
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Vakcína proti pandemické chřipce H5N1 MedImmune nosní sprej, suspenze
vakcína proti pandemické chřipce (živá atenuovaná, nosní)
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
MedImmune, LLC
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
Pouze pro nosní podání. Nepodávejte injekčně.
5 jednorázových nosních aplikátorů (po 0,2 ml)
Uchovávejte v chladničce. Chraňte před mrazem.
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Vakcína proti pandemické chřipce H5N1 MedImmune vakcína proti pandemické chřipce
2 ZPŮSOB PODÁNÍ
Pouze pro nosní podání.
3. POUŽITELNOST
EXP
4 ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
0,2 ml 6 JINÉ
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro uživatele
Vakcína proti pandemické chřipce H5N1 MedImmune, nosní sprej, suspenze
vakcína proti pandemické chřipce (H5N1) (živá atenuovaná, nosní)
'VTento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4.
Přečtěte si pozorně celou příbalovou informaci dříve, než je vakcína podána, protože obsahuje pro Vás nebo pro Vaše dítě důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
- Tato vakcína byla předepsána výhradně Vám nebo Vašemu dítěti. Nedávejte ji žádné další osobě.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, zdravotní sestře nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Vakcína proti pandemické chřipce H5N1 MedImmune a k čemu se používá
2. Čemu musíte věnovat pozornost předtím, než Vám bude Vakcína proti pandemické chřipce H5N1 MedImmune podána
3. Jak se Vakcína proti pandemické chřipce H5N1 MedImmune používá
4. Možné nežádoucí účinky
5 Jak Vakcínu proti pandemické chřipce H5N1 uchovávat
6. Obsah balení a další informace
1. Co je Vakcína proti pandemické chřipce H5N1 MedImmune a k čemu se používá
Vakcína proti pandemické chřipce H5N1 MedImmune je vakcína určená k prevenci chřipky při úředně vyhlášené pandemické situaci. Používá se u dětí a dospívajících od 12 měsíců do méně než 18 let.
Pandemická chřipka je typem chřipky, která se objevuje v časových intervalech, které mohou kolísat od méně než 10 let až po mnoho desetiletí. Šíří se rychle po celém světě. Projevy pandemické chřipky jsou podobné jako u normální sezónní chřipky, ale mohou být závažnější.
Jak Vakcína proti pandemické chřipce H5N1 MedImmune působí
Vakcína proti pandemické chřipce H5N1 MedImmune je podobná jako Fluenz Tetra (nosní vakcína proti chřipce, která obsahuje 4 kmeny), ovšem Vakcína proti pandemické chřipce H5N1 MedImmune poskytuje ochranu proti jednomu kmeni chřipkového viru při úředně potvrzené pandemické situaci.
Pokud člověk dostane vakcínu, imunitní systém (přirozený obranný systém) začne vytvářet svoji vlastní ochranu proti chřipkovému viru. Žádná složka vakcíny nemůže vyvolat chřipku.
Viry obsažené ve Vakcíně proti pandemické chřipce H5N1 MedImmune se množí ve slepičích vejcích. Chřipkový kmen obsažený ve vakcíně je shodný s kmenem doporučeným Světovou zdravotnickou organizací při úředně vyhlášené pandemii chřipky.
2. Čemu musíte věnovat pozornost, než začnete Vakcínu proti pandemické chřipce H5N1 MedImmune používat
- jestliže jste již dříve měl(a) těžkou alergickou reakci (tedy život ohrožující stav) na vejce, vaječné bílkoviny, gentamicin, želatinu nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6 „Obsah balení a další informace“). Známky alergické reakce jsou uvedeny v bodě 4 „Možné nežádoucí účinky“. V pandemické situaci Vám však lékař může doporučit použití vakcíny za předpokladu, že jsou okamžitě k dispozici lékařská opatření pro případ, že se objeví alergická reakce.
Pokud se některý z výše uvedených bodů vztahuje též na Vás, informujte o tom lékaře, zdravotní sestru nebo lékárníka.
Upozornění a opatření
Před použitím vakcíny se poraďte se svým lékařem, zdravotní sestrou nebo lékárníkem:
• jestliže je dítě mladší než 12 měsíců. Děti mladší než 12 měsíců nesmí tuto vakcínu používat kvůli riziku nežádoucích účinků.
• jestliže jste měl(a) alergickou reakci jinou než reakci ohrožující Váš život na vejce, vaječné bílkoviny, gentamicin, želatinu nebo na kteroukoli další složku této vakcíny (uvedené v bodě 6 „Obsah balení a další informace“).
• jestliže již užíváte kyselinu acetylsalicylovou (látku obsaženou v mnoha léčivých přípravcích k léčbě bolesti a snížení horečky). Existuje riziko vzniku velmi vzácného, ale závažného onemocnění (Reyův syndrom).
• jestliže máte poruchu krve nebo nádor ovlivňující imunitní systém.
• jestliže Vám lékař řekl, že máte oslabený imunitní systém jako výsledek probíhající nemoci, podávání léků nebo z jiných příčin.
• jestliže máte astma nebo máte současně sípot.
• jestliže jste v blízkém kontaktu s někým, kdo trpí těžkým oslabením imunitního systému
(např. pacienti po transplantaci kostní dřeně s potřebou izolace).
Pokud se některý bod výše vztahuje též na Vás, informujte o tom svého lékaře, zdravotní sestru nebo lékárníka ještě před podáním vakcíny. Lékař rozhodne, zda je Vakcína proti pandemické chřipce H5N1 MedImmune pro Vás vhodná.
Další léčivé přípravky a Vakcína proti pandemické chřipce H5N1 MedImmune
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které osoba, které má být vakcína podána, užívá, které v nedávné době užíval(a) nebo které možná bude užívat, včetně léčivých přípravků dostupných bez lékařského předpisu.
• Nepodávejte kyselinu acetylsalicylovou (látka obsažená v mnoha léčivých přípravcích k léčbě bolesti a ke snížení horečky) dětem čtyři týdny po podání Vakcíny proti pandemické chřipce H5N1 MedImmune, pokud Vám to neporadí lékař, zdravotní sestra nebo lékárník. Mohl by se objevit Reyův syndrom, velmi vzácné, ale závažné onemocnění, které postihuje mozek a játra.
• Doporučuje se nepodávat Vakcínu proti pandemické chřipce H5N1 MedImmune ve stejnou dobu jako protichřipkové léčivé přípravky obsahující oseltamivir a zanamivir. Je to proto, že vakcína může být méně účinná.
Váš lékař, zdravotní sestra nebo lékárník rozhodnou, zda lze Vakcínu proti pandemické chřipce H5N1 MedImmune podat ve stejnou dobu s jinými vakcínami.
Těhotenství a kojení
• Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem před podáním vakcíny. Lékař rozhodne, zda je Vakcína proti pandemické chřipce H5N1 MedImmune pro Vás vhodná.
• Nedoporučuje se podávat Vakcínu proti pandemické chřipce H5N1 MedImmune kojícím ženám.
Řízení dopravních prostředků a obsluha strojů
Vakcína proti pandemické chřipce H5N1 MedImmune nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
3. Jak se Vakcína proti pandemické chřipce H5N1 MedImmune používá
Vakcína proti pandemické chřipce H5N1 MedImmune se podává pod dohledem lékaře, zdravotní sestry nebo lékárníka.
Vakcína proti pandemické chřipce H5N1 MedImmune se musí podat do nosu jako nosní sprej.
Vakcína proti pandemické chřipce H5N1 MedImmune se nesmí podávat jehlou.
Vakcína proti pandemické chřipce H5N1 MedImmune se podává jako nosní sprej do obou nosních dírek. V průběhu podání Vakcíny proti pandemické chřipce H5N1 MedImmune dýchejte normálně. Není třeba aktivně nadechovat nebo potahovat.
Dávkování
Doporučená dávka pro děti a dospívající je 0,2 ml Vakcíny proti pandemické chřipce H5N1 MedImmune, podaná jako 0,1 ml do každé nosní dírky. Po nejméně 4 týdnech dostanou všechny děti ještě druhou dávku.
Pokud máte další dotazy k této vakcíně, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tato vakcína nežádoucí účinky, které se ale nemusí vyskytnout u každého. Většina nežádoucích účinků byla v průběhu klinického hodnocení této vakcíny mírná a krátkodobá.
Pokud budete chtít vědět více o možných nežádoucích účincích Vakcíny proti pandemické chřipce H5N1 MedImmune, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
Některé nežádoucí účinky mohou být závažné:
Velmi vzácné
(mohou postihnout až 1 z 10000 lidí):
• závažná alergická reakce: známky závažné alergické reakce mohou zahrnovat pocit ztíženého dýchání a otok obličeje nebo jazyka.
Informujte okamžitě lékaře nebo vyhledejte okamžitou lékařskou pomoc, pokus se dostaví účinky uvedené výše.
V klinických studiích u dospělých, kterým byla podávána Vakcína proti pandemické chřipce H5N1 MedImmune byly nejčastěji pozorovanými nežádoucími účinky bolest hlavy a infekce horních cest dýchacích (zánět nosu, krku a vedlejších nosních dutin).
Další nežádoucí účinky Vakcíny proti pandemické chřipce H5N1 MedImmune Velmi časté
(mohoupostihnout více než 1 z 10 lidí):
• výtok z nosu nebo ucpaný nos
snížená chuť k jídlu slabost
Časté
(mohou postihnout až 1 z 10 lidí):
• horečka
• svalové křeče
Méně časté
(mohoupostihnout až 1 z 100 lidí):
• vyrážka
• krvácení z nosu
• alergické reakce
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, zdravotní sestře nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Vakcínu proti pandemické chřipce H5N1 MedImmune uchovávat
Uchovávejte tuto vakcínu mimo dohled a dosah dětí.
Nepoužívejte tuto vakcínu po uplynutí doby použitelnosti uvedené na štítku aplikátoru za EXP. Uchovávejte v chladničce (2 °C - 8 °C). Chraňte před mrazem.
Uchovávejte nosní aplikátor v krabičce, aby byl chráněn před světlem.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co Vakcína proti pandemické chřipce H5N1 MedImmune obsahuje
- Léčivou látkou je:
Reasortant -virus influenzae * (vivum attenuatum) následujícího kmene**:
A/Vietnam/1203/2004 (H5N1) kmen
(A/Vietnam/1203/2004, MEDI 0141000136) 107,0±0,5 FFU***
_v dávce 0,2 ml
* pomnožený v oplodněných slepičích vejcích ze zdravých chovů drůbeže.
** produkovaných v buňkách VERO pomocí technologie reverzní genetiky. Tento přípravek obsahuje geneticky modifikované organizmy (GMO).
*** fluorescenční fokální jednotky.
Tato vakcína vyhovuje doporučení SZO a EU rozhodnutí pro pandemickou chřipku.
Dalšími složkami jsou sacharosa, hydrogenfosforečnan draselný, dihydrogenfosforečnan draselný, želatina (prasečí, typ A), arginin-hydrochlorid, monohydrát natrium-hydrogen-glutamátu, voda na injekci
Tato vakcína se vyrábí jako nosní sprej, suspenze v jednodávkovém aplikátoru (0,2 ml) v balení po 10.
Suspenze je bezbarvá až slabě nažloutlá, čirá až mírně zakalená. Mohou být přítomny malé bílé částečky.
Držitel rozhodnutí o registraci a výrobce
Držitel rozhodnutí o registraci: MedImmune, LLC, Lagelandseweg 78, 6545 CG Nijmegen, Nizozemsko, (Tel) +31 24 371 7310
Výrobce: MedImmune, UK Limited, Plot 6, Renaissance Way, Boulevard Industry Park, Speke, Liverpool, L24 9JW, Velká Británie
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
|
Belgie/Belgique/Belgien AstraZeneca S.A./N.V. Tel: +32 2 370 48 11 |
Lietuva UAB ,AstraZeneca Lietuva Tel: +370 5 2660550 |
|
Eunrapnu Acrpa3eHeKa Etnrapua EOOfl Ten: +359 24455000 |
Luxembourg/Luxemburg AstraZeneca S.A./N.V. Tél/Tel: +32 2 370 48 11 |
|
Česká republika AstraZeneca Czech Republic s.r.o. Tel: +420 222 807 111 |
Magyarország AstraZeneca Kft. Tel.: +36 1 883 6500 |
|
Danmark AstraZeneca A/S Tlf: +45 43 66 64 62 |
Malta Associated Drug Co. Ltd Tel: +356 2277 8000 |
|
Deutschland AstraZeneca GmbH Tel: +49 41 03 7080 |
Nederland AstraZeneca BV Tel: +31 79 363 2222 |
|
Eesti AstraZeneca Tel: +372 6549 600 |
Norge AstraZeneca AS Tlf: +47 21 00 64 00 |
|
EXláSa AstraZeneca A.E. T^: +30 2-10 6871500 |
Osterreich AstraZeneca Osterreich GmbH Tel: +43 1 711 31 0 |
|
Espaňa AstraZeneca Farmacéutica Spain, S.A. Tel: +34 91 301 91 00 |
Polska AstraZeneca Pharma Poland Sp. z o.o. Tel.: +48 22 245 73 00 |
|
France AstraZeneca Tél: +33 1 41 29 40 00 |
Portugal AstraZeneca Produtos Farmaceuticos, Lda. Tel: +351 21 434 61 00 |
|
Hrvatska AstraZeneca d.o.o. Tel: +385 1 4628 000 |
Románia AstraZeneca Pharma SRL Tel: +40 21 317 60 41 |
|
Ireland AstraZeneca Pharmaceuticals (Ireland) Ltd Tel: +353 1609 7100 |
Slovenija AstraZeneca UK Limited Tel: +386 1 51 35 600 |
|
Ísland Vistor hf. Sími: +354 535 7000 |
Slovenská republika AstraZeneca AB, o.z. Tel: +421 2 5737 7777 |
|
Italia AstraZeneca S.p.A. Tel: +39 02 98011 |
Suomi/Finland AstraZeneca Oy Puh/Tel: +358 10 23 010 |
|
Kónpoq A^ÉKxrnp OappaKeouKq AtS T^: +357 22490305 |
Sverige AstraZeneca AB Tel: +46 8 553 26 000 |
|
Latvija SIA AstraZeneca Latvija Tel: +371 67377100 |
United Kingdom AstraZeneca UK Ltd Tel: +44 1582 836 836 |
Tato příbalová informace byla naposledy revidována
Tomuto léčivému přípravku bylo uděleno tzv. podmíněné schválení. Znamená to, že informace o tomto přípravku budou přibývat. Evropská agentura pro léčivé přípravky nejméně jednou za rok vyhodnotí nové informace o tomto léčivém přípravku a tato příbalová informace bude podle potřeby aktualizována.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
Pokyny pro zdravotnické pracovníky
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Vakcína proti pandemické chřipce H5N1 MedImmune je určena pouze pro nosní podání.
• Nepoužívejte s jehlou. Nepodávejte injekčně.

• Vakcínu proti pandemické chřipce H5N1 MedImmune nepoužívejte po uplynutí doby použitelnosti nebo pokud se rozprašovač jeví jako poškozený, například je-li píst uvolněný nebo je mimo rozprašovač, případně jeví známky netěsnosti.
• Vakcína proti pandemické chřipce H5N1 MedImmune se podává jako rozdělená dávka do obou nosních dírek. (Viz též Jak se vakcína proti pandemické chřipce H5N1 MedImmune podává
v bodě 3)
• Po podání poloviny dávky do jedné nosní dírky, podejte ihned nebo krátce poté druhou polovinu dávky do druhé nosní dírky.
• Během podávání vakcíny může pacient normálně dýchat - není potřeba aktivně vdechovat ani popotahovat nosem.
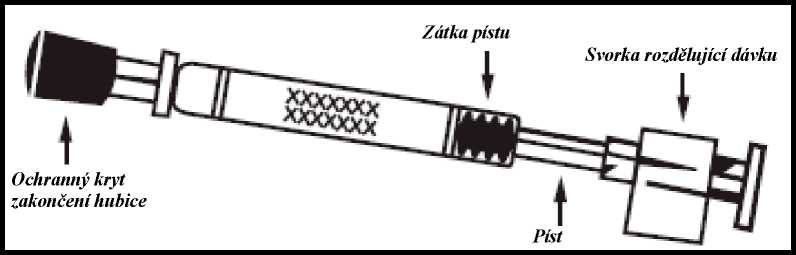
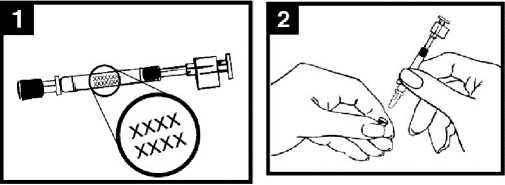
Zkontrolujte datum použitelnosti
Přípravek se musí spotřebovat do data uvedeného na štítku aplikátoru.
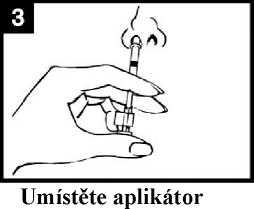
Připravte aplikátor
Sejměte pryžový ochranný kryt zakončení hubice. Neodstraňujte svorku rozdělující dávku na druhém konci aplikátoru.
S pacientem ve vzpřímené poloze umístěte pouze zakončení aplikátoru do nosní dírky tak, aby se zajistilo, že se Vakcína proti pandemické chřipce H5N1 MedImmune dostane do nosu.
Stlačte píst
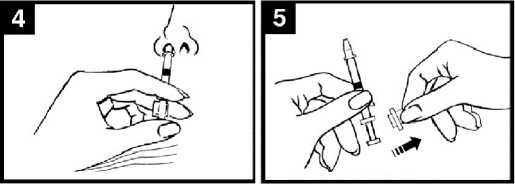
Jediným pohybem stlačte píst tak rychle, jak je to možné, a až na doraz, dokud Vám to svorka rozdělující dávku dovolí.
Odstraňte svorku rozdělující dávku
Pro podání do druhé nosní dírky uštípněte a odstraňte z pístu svorku rozdělující dávku.
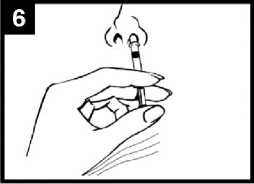
Vstříkněte dávku do druhé nosní dírky
Umístěte pouze zakončení aplikátoru do druhé nosní dírky a jediným pohybem stlačte píst tak rychle, jak je to možné, abyste podal(a) zbylou část vakcíny.
Pokyny ohledně uchovávání a likvidace viz bod 5.
PŘÍLOHA IV
ZÁVĚRY O UDĚLENÍ PODMÍNĚNÉ REGISTRACE PŘÍPRAVKU PŘEDLOŽENÉ EVROPSKOU AGENTUROU PRO LÉČIVÉ PŘÍPRAVKY
Závěry předložené Evropskou agenturou pro léčivé přípravky:
• Podmíněná registrace přípravku
Výbor CHMP posoudil žádost a je toho názoru, že poměr přínosů a rizik je příznivý, a proto doporučuje, aby přípravku byla udělena podmíněná registrace, jak je podrobněji popsáno v Evropské veřejné zprávě o hodnocení.
33