Telmisartan Teva 40 Mg
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Telmisartan Teva 20 mg tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna tableta obsahuje telmisartanum 20 mg
Pomocné látky se známým účinkem:
Jedna tableta obsahuje 21,4 mg sorbitolu (E420)
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Tableta
Bílé až téměř bílé tablety oválného tvaru, na jedné straně tablety je vyraženo číslo “93”. Na druhé straně je vyraženo číslo “7458”.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Hypertenze
Léčba esenciální hypertenze u dospělých pacientů.
Kardiovaskulární prevence
Snížení kardiovaskulární morbidity u dospělých:
• s manifestním aterotrombotickým kardiovaskulárním onemocněním (anamnéza ischemické choroby srdeční nebo cévní mozkové příhody nebo onemocnění periferních tepen) nebo
• s diabetes mellitus typu 2 s prokázaným orgánovým postižením
4.2 Dávkování a způsob podání
Dávkování
Léčba esenciální hypertenze:
Obvyklá účinná dávka je 40 mg jednou denně. U některých pacientů se příznivý výsledek dostavuje již při denní dávce 20 mg. V případech, kdy se nedosáhne požadovaných hodnot krevního tlaku, lze dávku telmisartanu zvýšit až na 80 mg jednou denně. Alternativně lze telmisartan použít v kombinaci diuretiky thiazidového typu, jako např. hydrochlorothiazidem, u kterého bylo prokázáno, že aditivně snižuje krevní tlak pomocí telmisartanu. Pokud se uvažuje o zvyšování dávek, je třeba přihlížet k okolnosti, že maximálního antihypertenzního účinku se obvykle dosáhne čtyři až osm týdnů po zahájení léčby (viz bod 5.1).
Kardiovaskulární prevence
Doporučená dávka je 80 mg jednou denně. Nejsou k dispozici údaje o tom, zda dávky telmisartanu nižší než 80 mg jsou účinné při snižování kardiovaskulární morbidity.
Při zahájení léčby telmisartanem ke snížení kardiovaskulární morbidity se doporučuje pečlivé sledování krevního tlaku. V některých případech může být nezbytné upravit léky snižující krevní tlak.
Pacienti s poruchou _ funkce ledvin
U pacientů se závažnou poruchou funkce ledvin nebo podstupujících hemodialýzu jsou k dispozici jen omezené zkušenosti. U těchto pacientů je doporučena nižší úvodní dávka 20 mg (viz bod 4.4).
U pacientů s mírnou až středně závažnou poruchou funkce ledvin není třeba upravovat dávkování.
Pacienti s poruchou funkce jater
Telmisartan Teva je kontraindikován u pacientů se závažnou poruchou funkce jater (viz bod 4.3). U pacientů s mírnou až středně závažnou poruchou funkce jater by dávka neměla přesáhnout 40 mg jednou denně (viz bod 4.4).
Starší pacienti
Úprava dávkování u starších pacientů není nutná.
Pediatrická populace
Bezpečnost a účinnost přípravku Telmisartan Teva u dětí a dospívajících mladších 18 let nebyla stanovena.
Aktuálně dostupné údaje jsou popsány v bodech 5.1 a 5.2, ale doporučené dávkování stanovit nelze. Způsob podání
Telmisartan tablety se užívají jednou denně perorálně a měly by se podávat s tekutinami, s jídlem nebo bez jídla.
4.3 Kontraindikace
• Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku uvedenou v bodě 6.1
• Druhý a třetí trimestr těhotenství (viz bod 4.4 a 6.4)
• Obstrukce žlučovodů
• Závažná porucha funkce j ater
Současné užívání přípravku Telmisartan Teva s přípravky obsahujícími aliskiren je kontraindikováno u pacientů s diabetes mellitus nebo poruchou funkce ledvin (GFR <60 ml/min/1.73 m2) (viz body 4.5 a 5.1).
4.4 Zvláštní upozornění a opatření pro použití
Léčba pomocí antagonistů receptoru angiotensinu II nesmí být během těhotenství zahájena. Pokud není pokračování v léčbě antagonisty receptoru angiotensinu II považováno za nezbytné, pacientky plánující těhotenství musí být převedeny na jinou léčbu hypertenze, a to takovou, která má ověřený bezpečnostní profil, pokud jde o podávání v těhotenství. Pokud je zjištěno těhotenství, léčba pomocí antagonistů receptoru angiotensinu II musí být ihned ukončena, a pokud je to vhodné, může být zahájena alternativní léčba (viz body 4.3 a 4.6).
Poškození funkce jater
Vzhledem k tomu, že se Telmisartan Teva vylučuje především žlučí, nesmí být podáván pacientům s cholestázou, obstrukcí žlučovodů nebo závažným poškozením jater (viz bod 4.3). U těchto pacientů se předpokládá snížení jaterní clearence telmisartanu. Pacientům s mírným až středně závažným poškozením jater může být Telmisartan Teva podán pouze se zvýšenou opatrností.
Renovaskulární hypertenze
Pacientům s oboustrannou stenózou renální arterie nebo se stenózou arterie zásobující jedinou funkční ledvinu, kteří jsou léčeni přípravky ovlivňujícími renin-angiotenzin-aldosteronový systém, hrozí zvýšené riziko těžké hypotenze a renální nedostatečnost.
Renální poškození a transplantace ledvin
Pokud je přípravek Telmisartan Teva podáván pacientům s poruchou funkce ledvin, je doporučena pravidelná kontrola sérových hladin draslíku a kreatininu v krvi. Nejsou žádné zkušenosti s podáváním přípravku Telmisartan Teva pacientům po transplantaci ledvin.
Intravaskulární hypovolaemie
U pacientů s poklesem objemu nebo koncentrace sodíku v důsledku intenzivní diuretické terapie, omezování soli v dietě, průjmu nebo zvracení se zejména po první dávce přípravku Telmisartan Teva může objevit symptomatická hypotenze. Takové stavy by se měly ještě před podáním přípravku Telmisartan Teva korigovat, stejně jako snížení intravaskulárního objemu nebo deplece sodíku.
Duální blokáda systému renin-angiotenzin-aldosteron (RAAS)
Bylo prokázáno, že současné užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu zvyšuje riziko hypotenze, hyperkalemie a snížení funkce ledvin (včetně akutního selhání ledvin). Duální blokáda RAAS pomocí kombinovaného užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu se proto nedoporučuje (viz body 4.5 a 5.1).
Pokud je duální blokáda považována za naprosto nezbytnou, má k ní docházet pouze pod dohledem specializovaného lékaře a za častého pečlivého sledování funkce ledvin, elektrolytů a krevního tlaku. Inhibitory ACE a blokátory receptorů pro angiotenzin II nemají být používány současně u pacientů s diabetickou nefropatií.
Ostatní stavy provázené stimulací renin-angiotenzin-aldosteronového systému U pacientů, jejichž cévní tonus a renální funkce závisejí převážně na aktivitě renin-angiotenzin-aldosteronového systému (např. u pacientů se závažným městnavým srdečním selháním nebo s průvodním onemocněním ledvin, včetně stenózy renální arterie), byla léčba dalšími přípravky, které ovlivňují tento systém podobně jako telmisartan, spojeny s akutní hypotenzí, hyperazotemií, oligurií nebo vzácněji i s akutním selháním ledvin (viz bod 4.8).
Primární aldosteronismus
Pacienti s primárním aldosteronismem obvykle nereagují na antihypertenziva působící mechanismem inhibice renin-angiotenzin-aldosteronového systému. V těchto případech se léčba telmisartanem nedoporučuje.
Stenóza aortální a mitrální chlopně, obstrukční hypertrofická kardiomyopatie
Stejně jako u ostatních vazodilatancií je třeba věnovat zvlášť zvýšenou pozornost pacientům trpícím
stenózami aortální a mitrální chlopně nebo obstrukční hypertrofickou kardiomyopatií.
Diabetičtí pacienti léčení inzulínem nebo antidiabetiky
U těchto pacientů se může při léčbě telmisartanem objevit hypoglykémie. Proto je u nich
vhodné zvážit sledování hladiny glukózy v krvi; a pokud je indikováno, upravit dávky inzulinu nebo
antidiabetik.
Hyperkalémie
Podávání léčivých přípravků, které ovlivňují renin-angiotenzin-aldosteronový systém, může vést k hyperkalémii.
U starších pacientů, u pacientů s poškozením funkce ledvin, u diabetiků, u pacientů současně léčených jinými přípravky, které mohou zvyšovat hladinu draslíku, a/nebo u pacientů s určitými interkurentními příhodami, může být hyperkalémie fatální.
Před zvažováním současného podávání léčivých přípravků, které ovlivňují renin-angiotenzin-aldosteronový systém, je nutno zhodnotit poměr přínosu a rizika.
Hlavní rizikové faktory hyperkalémie, které je třeba zvažovat:
- Diabetes mellitus, poškozená funkce ledvin, věk (>70 let)
- Kombinace s jedním nebo více léčivými přípravky, které ovlivňují renin-angiotenzin-aldosteronový systém, a/nebo s přípravky doplňujícími draslík. Léčivé přípravky nebo terapeutické třídy léčivých přípravků, které mohou vyvolat hyperkalémii j sou náhražky soli obsahující draslík, draslík šetřící diuretika, ACE inhibitory, antagonisté receptoru angiotenzinu II, nesteroidní protizánětlivé léčivé přípravky (NSAIDs, včetně selektivních COX-2 inhibitorů), heparin, imunosupresiva (cyklosporin nebo takrolismus) a trimethoprim.
- Interkurentní příhody, zejména dehydratace, akutní srdeční dekompenzace, metabolická acidóza, zhoršení renálních funkcí, náhlé zhoršení podmínek pro funkci ledvin (např. infekční onemocnění), rozpad buněk (např. při akutní ischemii končetin, rabdomyolýze, rozsáhlém traumatu).
U rizikových pacientů se doporučuje sledovat sérové hladiny draslíku (viz bod 4.5).
Sorbitol
Tento léčivý přípravek obsahuje sorbitol (E420). Pacienti se vzácnou vrozenou intolerancí fruktosy nesmí Telmisartan Teva užívat.
Etnické odlišnosti
Stejně jako inhibitory enzymu konvertujícího angiotenzin, také telmisartan a další antagonisté receptoru angiotenzinu II zjevně navozují u černošské populace méně výrazné snížení krevního tlaku než u jiných lidských ras, pravděpodobně v souvislosti s vyšší prevalencí stavů s nízkou hladinou reninu v populaci hypertoniků černé pleti.
Další upozornění
Analogicky jako u kterýchkoli jiných antihypertenziv může dojít při nadměrném snížení krevního tlaku u pacientů s ischemickou kardiopatií nebo s ischemickou chorobou srdeční k infarktu myokardu nebo k cévní mozkové příhodě.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Digoxin
Při současném podání telmisartanu s digoxinem bylo pozorováno zvýšení střední hodnoty vrcholové plasmatické koncentrace digoxinu (49%) a minimální koncentrace (20%). Při zahájení, úpravě a ukončení léčby telmisartanem byla monitorována hladina digoxinu proto, aby byla zachována jeho hladina v terapeutickém rozmezí.
Tak jako ostatní léčiva působící na renin-angiotenzin-aldosteronový systém, telmisartan může způsobit hyperkalémii (viz bod 4.4). Riziko se může zvýšit v případě kombinované léčby s dalšími léčivými přípravky, které mohou také vyvolat hyperkalemii (náhražky soli obsahující draslík, draslík šetřící diuretika, ACE inhibitory, antagonisté receptoru angiotenzinu II, nesteroidní protizánětlivé léčivé přípravky (NSAIDs, včetně selektivních COX-2 inhibitorů), heparin, imunosupresiva (cyklosporin nebo takrolismus) a trimethoprim).
Výskyt hyperkalemie závisí na přidružených rizikových faktorech. Riziko se zvyšuje v případě výše uvedených léčebných kombinací. Riziko je zvláště vysoké při kombinaci s kalium šetřícími diuretiky a při kombinaci s náhražkami soli obsahující draslík. Kombinace např. s ACE inhibitory nebo s NSAIDs představují menší riziko za předpokladu, že jsou přesně dodržována opatření při podávání.
Současné podávání se nedoporučuje
Draslík šetřící diuretika a přípravky obsahující draslík
Antagonisté receptoru angiotenzinu II jako telmisartan, zmenšují ztrátu draslíku, navozenou diuretiky. Draslík šetřící diuretika, například spironolakton, eplerenon, triamteren nebo amilorid, přípravky
obsahující draslík nebo náhražky soli obsahující draslík, mohou vést k významnému zvýšení hladiny draslíku v séru. Pokud je indikováno současné podávání z důvodu prokázané hypokalemie, je nutno je podávat opatrně a za častých kontrol hladin draslíku v séru.
Lithium
Při současném podávání lithia spolu s inhibitory angiotenzin konvertujícího enzymu byl hlášen reverzibilní nárůst koncentrací lithia v séru a jeho toxicita, a také při současném podávání lithia a antagonistů receptoru angiotenzinu II včetně telmisartanu. Pokud se ukáže kombinované podávání jako nezbytné, doporučuje se pečlivě monitorovat sérové hladiny lithia.
Současné podávání vyžadující opatrnost
Nesteroidní protizánětlivé léčivé přípravky (NSAIDs)
NSAIDs (např. kyselina acetylosalicylová v protizánětlivých dávkách, inhibitory COX-2 a neselektivní NSAIDs) mohou snižovat antihypertenzivní účinek antagonistů receptoru angiotensinu II. U některých pacientů s oslabenou funkcí ledvin (např. u dehydratovaných pacientů nebo starších pacientů s poruchou funkce ledvin) může mít současné podávání antagonistů receptoru angiotensinu II a přípravků, které blokují cyklooxygenázu, za následek další zhoršení funkce ledvin, včetně možného vzniku akutního selhání ledvin, které je obvykle reverzibilní. Z tohoto důvodu je nutno podávat takovou kombinaci velmi opatrně, zejména u starších pacientů. Pacienti musí být dostatečně hydratováni a je třeba zvážit kontroly funkce ledvin po zahájení, a také v pravidelných intervalech během této kombinované terapie.
V jedné studii vedlo současné podávání telmisartanu a ramiprilu ke 2,5 násobnému zvýšení AUC 0-24 a Cmax ramiprilu a ramiprilátu. Klinický význam tohoto zjištění není znám.
Diuretika (thiazidová nebo kličková diuretika)
Předchozí léčba vysokými dávkami diuretik jako je furosemid (kličkové diuretikum) a hydrochlorothiazid (thiazidové diuretikum) může vést k volumdepleci a k riziku vzniku hypotenze po zahájení léčby telmisartanem.
Současné podávání, které je nutno zvažovat
Jiná antihypertenziva
Účinek telmisartanu na snížení krevního tlaku může být zvýrazněn při současném podávání jiných antihypertenziv.
Data z klinických studií ukázala, že duální blokáda systému renin-angiotenzin-aldosteron (RAAS) pomocí kombinovaného užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu je spojena s vyšší frekvencí nežádoucích účinků, jako je hypotenze, hyperkalemie a snížená funkce ledvin (včetně akutního renálního selhání) ve srovnání s použitím jedné látky ovlivňující RAAS (viz body 4.3, 4.4 a 5.1).
Na základě farmakologických vlastností následně uvedených léků lze očekávat, že tyto léčivé přípravky mohou zvýraznit hypotenzní účinek všech antihypertenziv, včetně telmisartanu: baklofen, amifostin.
Vedle toho může být orthostatická hypotenze potencována alkoholem, barbituráty, narkotiky nebo antidepresivy.
Kortikosteroidy (systémové podání)
Snížení antihypertenzního účinku.
4.6 Fertilita, těhotenství a kojení
Užívání antagonistů receptoru angiotensinu II se nedoporučuje během prvního trimestru těhotenství (viz bod 4.4). Užívání antagonistů receptoru angiotensinu II je kontraindikováno během druhého a třetího trimestru těhotenství (viz body 4.3 a 4.4).
Adekvátní údaje o podávání přípravku Telmisartan Teva těhotným ženám nejsou k dispozici. Studie na zvířatech poukázaly na reprodukční toxicitu (viz bod 5.3).
Epidemiologické důkazy týkající se rizika teratogenicity při podávání ACE inhibitorů během prvního trimestru těhotenství nebyly nezvratné; malý nárůst rizika však nelze vyloučit. I když neexistují žádné kontrolované epidemiologické údaje pokud jde o riziko při podávání antagonistů receptoru angiotenzinu II, pro tuto třídu léčiv může existovat riziko podobné. Pokud pokračování v léčbě antagonisty receptoru angiotenzinu II není považováno za nezbytné, pacientky plánující těhotenství musí být převedeny na jinou léčbu vysokého krevního tlaku, a to takovou, která má ověřený bezpečnostní profil, pokud jde o podávání v těhotenství. Jestliže je těhotenství prokázáno, léčba pomocí antagonistů receptoru angiotenzinu II musí být ihned ukončena, a pokud je to vhodné, je nutné zahájit jiný způsob léčby.
Je známo, že expozice vůči antagonistům receptoru angiotenzinu II během druhého a třetího trimestru těhotenství vede u lidí k fetotoxicitě (pokles funkce ledvin, oligohydramnion, zpoždění osifikace lebky) a k novorozenecké toxicitě (selhání ledvin, hypotenze, hyperkalémie). (Viz bod 5.3).
Pokud by došlo k expozici vůči antagonistům receptoru angiotenzinu II od druhého trimestru těhotenství, doporučuje se sonografická kontrola funkce ledvin a lebky.
Děti, jejichž matky užívaly antagonisty receptoru angiotenzinu II, musí být pečlivě sledovány, pokud jde o hypotenzi (viz body 4.3 a 4.4).
Kojení
Protože nejsou k dispozici žádné údaje ohledně užívání přípravku Telmisartan Teva během kojení, Telmisartan Teva se nedoporučuje, je vhodnější zvolit jinou léčbu s lepším bezpečnostním profilem během kojení, obzvláště během kojení novorozence nebo předčasně narozeného dítěte.
Fertilita:
V předklinických studiích nebyly u telmisartanu pozorovány žádné účinky na samčí nebo samičí plodnost.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Při řízení motorových vozidel nebo obsluze strojních zařízení je však třeba mít na paměti, že léčba antihypertenzivy, jako je Telmisartan Teva může v některých případech způsobovat závratě nebo ospalost.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Vzácně (>1/10 000 až <1/1 000) mohou být pozorovány závažné nežádoucí účinky včetně anafylaktické reakce a angioedému a akutní renální selhání.
V kontrolovaných studiích u pacientů s hypertenzí byla celková frekvence výskytu nežádoucích účinků hlášených pro telmisartan obvykle srovnatelná s placebem (41,4% vs 43,9 %). Výskyt nežádoucích účinků není závislý na dávce ani na pohlaví, věku nebo rase pacientů. Bezpečnostní profil telmisartanu podávaného pacientům ke snížení kardiovaskulární morbidity byl shodný
s bezpečnostním profilem zjištěným u pacientů s hypertenzí.
Následně uvedené nežádoucí účinky byly shromážděny z kontrolovaných klinických studií u pacientů s hypertenzí a z postmarketingových sledování. Dále se vycházelo z hlášení závažných nežádoucích příhod a nežádoucích příhod vedoucích k přerušení léčby v rámci tří dlouhodobých klinických studií s 21642 pacienty, kterým byl podáván telmisartan ke snížení kardiovaskulární morbidity až po dobu šesti let.
Souhrn nežádoucích účinků v tabulce
Nežádoucí účinky jsou podle frekvence výskytu rozděleny za použití následujícího pravidla: velmi časté (>1/10); časté (>1/100 až <1/10); méně časté (>1/1000 až <1/100); vzácné (>1/10000 až <1/1000); velmi vzácné (<1/10000)
V každé skupině četnosti jsou nežádoucí účinky seřazeny podle klesající závažnosti.
Infekce a infestace
Méně časté: Infekce močových cest včetně zánětů močového měchýře,
infekce horních cest dýchacích včetně faryngitidy a sinusitidy Vzácné: Sepse včetně případů vedoucích k úmrtí1
Poruchy krve a lymfatického systému Méně časté: Anémie,
Vzácné: Eosinofilie, trombocytopenie
Poruchy imunitního systému
Vzácné: Přecitlivělost, anafylaktická reakce
Poruchy metabolismu a výživy
Méně časté: Hyperkalémie
Vzácné: Hypoglykémie (u diabetických pacientů)
Psychiatrické poruchy
Méně časté: Insomnie, deprese
Vzácné: Úzkost
Poruchy nervového systému
Méně časté: Synkopa
Vzácné: Somnolence
Poruchy oka Vzácné:
Poruchy ucha a labyrintu Méně časté:
Srdeční poruchy Méně časté: Vzácné:
Cévní poruchy Méně časté:
Poruchy vidění Vertigo
Bradykardie
Respirační, hrudní a mediastinální poruchy
Méně časté: Dyspnoe, kašel
Velmi vzácné: Intersticiální plicní nemoc4
Gastrointestinální poruchy Méně časté:
Bolesti břicha, průjem, dyspepsie, plynatost, zvracení
Poruchy jater a žlučových cest
V zácné: Abnormální j atemí funkce/ poruchy funkce j ater3
Poruchy kůže a podkožní tkáně
Méně časté: Zvýšené pocení, pruritus, kožní vyrážka
Vzácné: Erytém, angioedém (včetně případů vedoucích k úmrtí), ekzém,
kopřivka, polékový exantém, toxoalergický exantém,
Poruchy svalové a kosterní soustavy a pojivové tkáně
Méně časté: Bolesti zad (např. ischias), svalové spasmy, myalgie
Vzácné: Artralgie, bolesti končetin, bolesti šlach (příznaky podobné zánětu
šlach)
Poruchy ledvin a močových cest
Méně časté: Poškození ledvin včetně akutního renálního selhání
Celkové poruchy a reakce v místě aplikace
Méně časté: Bolesti na hrudi, astenie (slabost)
Vzácné: Onemocnění připomínající chřipku
Vyšetření
Méně časté: Zvýšená hladina kreatininu v krvi,
Vzácné: Pokles hemoglobinu, zvýšené hladiny kyseliny močové v krvi,
zvýšení jaterních enzymů, zvýšení kreatinfosfokinázy
1 2,3,4 pro další popis, viz část „Popis vybraných nežádoucích účinků “
Popis vybraných nežádoucích účinků Sepse
Ve studii PRoFESS byl pozorován zvýšený výskyt sepse po telmisartanu ve srovnání s placebem. Příhoda může být náhodný nález nebo může souviset s dosud neznámým mechanismem (viz také bod 5.1).
Tento nežádoucí účinek byl hlášen jako častý u pacientů s upraveným krevním tlakem, kterým byl podáván telmisartan ke snížení kardiovaskulární morbidity nad rámec standardní péče.
Abnormální jaterní funkce/porucha jater
Většina případů abnormální jaterní funkce/poruchy jater z post-marketingových zkušeností se vyskytla u japonských pacientů. U japonských pacientů se tyto nežádoucí účinky vyskytují s větší pravděpodobností.
Intersticiální plicní nemoc
Na základě zkušeností po uvedení přípravku na trh byly hlášeny případy intersticiální plicní nemoci v časové souvislosti s podáním telmisartanu. Příčinná souvislost ale nebyla stanovena
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky,
aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
K dispozici jsou pouze omezené informace týkající se předávkování u člověka.
Příznaky
Nejnápadnějšími projevy předávkování telmisartanem jsou hypotenze a tachykardie; vyskytla se bradykardie, závrať, zvýšení kreatininu v séru a akutní selhání ledvin.
Terapie
Telmisartan nelze odstranit hemodialýzou. Pacient by měl být pečlivě monitorován, léčba by měla být podpůrná a symptomatická. Léčba závisí na časovém úseku, který uplynul od požití a na závažnosti příznaků. Navrhovaná opatření zahrnují navození zvracení a/nebo výplach žaludku. Vhodnou léčbou předávkování může být použití aktivního uhlí. Hladiny elektrolytů a kreatininu v séru je nutno často monitorovat. Pokud dojde k hypotenzi, je nutno pacienta uložit do polohy vleže na zádech a urychleně podat soli a doplnit objem tekutin.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antagonisté angiotensinu II, samotní; ATC kód: C09CA07. Mechanismus účinku
Telmisartan je specifický antagonista receptoru angiotenzinu II (typ ATj) účinný po perorálním podání. S vysokou afinitou vytěsňuje angiotenzin II z jeho vazebného místa na subtypu receptoru ATb který odpovídá za známé působení angiotenzinu II. Telmisartan nemá na receptoru ATj žádnou parciální agonistickou aktivitu a váže se selektivně na tento receptor. Vazba má dlouhodobý charakter. Telmisartan nevykazuje afinitu k ostatním receptorům, včetně AT2 a ostatních méně charakterizovaných AT. Funkční význam těchto receptorů není znám, stejně jako efekt jejich možné zvýšené stimulace angiotenzinem II, jehož hladiny se podáváním telmisartanem zvyšují. Plazmatické hladiny aldosteronu se podáváním telmisartanu snižují. Telmisartan neinhibuje u lidí plazmatický renin ani neblokuje iontové kanály. Telmisartan neinhibuje enzym konvertující angiotenzin (kinázu II), což je enzym, který rovněž rozkládá bradykinin. Proto se nepředpokládá, že by telmisartan potencoval nežádoucí účinky zprostředkované bradykininem.
Dávka telmisartanu 80 mg u člověka téměř zcela inhibuje zvýšení krevního tlaku vyvolané angiotenzinem II. Inhibiční účinek přetrvává déle než 24 hodin a je měřitelný po dobu až 48 hodin.
Klinická účinnost a bezpečnost
Léčba esenciální hypertenze
Po první dávce telmisartanu dojde v průběhu tří hodin postupně k poklesu krevního tlaku. Maximální redukce krevního tlaku se dosáhne obvykle v průběhu 4 až 8 týdnů od zahájení léčby a přetrvává během dlouhodobé terapie.
Antihypertenzní účinek trvá 24 hodin po podání přípravku včetně posledních 4 hodin před podáním následující dávky, jak bylo prokázáno ambulantním monitorováním krevního tlaku. Ve studiích kontrolovaných placebem po dávce 40 a 80 mg telmisartanu je toto potvrzeno poměrem minimálních a maximálních hodnot tlaku krve, který byl konzistentně nad 80 %.
Existuje zjevná závislost mezi podanou dávkou přípravku a časem potřebným k návratu systolického krevního tlaku (STK) na původní hodnoty. Údaje týkající se diastolického krevního tlaku (DTK) nejsou jednotné.
U pacientů s hypertenzí snižuje telmisartan jak systolický, tak i diastolický krevní tlak bez ovlivnění tepové frekvence. Příspěvek diuretického a natriuretického efektu léčivého přípravku k jeho hypotenznímu působení musí být ještě určen.
Antihypertenzní účinnost telmisartanu je srovnatelná se zástupci jiných tříd antihypertenziv (což bylo prokázáno v klinických studiích porovnávajících telmisartan s amlodipinem, atenololem, enalaprilem, hydrochlorothiazidem a lisinoprilem).
Po náhlém přerušení léčby telmisartanem se během několika dnů krevní tlak postupně vrací k hodnotám před léčbou bez vzniku „rebound“ fenoménu.
V klinických studiích přímo srovnávajících dvě antihypertenziva byl výskyt suchého kašle významně nižší u pacientů léčených telmisartanem než u pacientů léčených inhibitory enzymu konvertujícího angiotenzin.
Kardiovaskulární prevence
Klinická studie ONTARGET (z anglického ONgoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial) srovnávala účinky telmisartanu, ramiprilu a kombinace telmisartanu a ramiprilu na kardiovaskulární výsledky u 25620 pacientů ve věku 55 let nebo starších s anamnézou ischemické choroby srdeční, cévní mozkové příhody, tranzitorní ischemické ataky, onemocnění periferních tepen nebo diabetes mellitus 2. typu s prokázaným orgánovým postižením (např. retinopatie, hypertrofie levé srdeční komory, makro- nebo mikroalbuminurie), což je populace s rizikem vzniku kardiovaskulárních příhod.
Pacienti byly náhodně zařazeni do jedné ze 3 následujících léčebných skupin: telmisartan 80 mg (n = 8542), ramipril 10 mg (n = 8576) nebo kombinace telmisartan 80 mg plus ramipril 10 mg (n = 8502) a následně sledováni po dobu průměrně 4,5 roku.
Pokud jde o primární kombinovaný cílový parametr účinnosti klinické studie - snížení úmrtí z kardiovaskulárních příčin, nefatálních srdečních infarktů, nefatálních cévních mozkových příhod nebo hospitalizace z důvodu srdečního selhání, telmisartan ukázal podobný účinek jako ramipril. Výskyt primárního cílového parametru u skupiny užívající telmisartan (16,7%) a ramipril (16,5%) byl podobný. Relativní riziko pro telmisartan ve srovnání s ramiprilem bylo 1,01 (97,5% CI 0,93 - 1,10, p (non-inferiorita) = 0,0019, v rozpětí 1,13). Úmrtnost ze všech příčin byla u pacientů léčených telmisartanem 11,6%, u ramiprilu 11,8%.
Ve dvou velkých randomizovaných, kontrolovaných studiích (ONTARGET (ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) a VA NEPHRON-D (The Veterans Affairs Nephropathy in Diabetes)) bylo hodnoceno podávání kombinace inhibitoru ACE s blokátorem receptorů pro angiotenzin II.
Studie ONTARGET byla vedena u pacientů s anamnézou kardiovaskulárního nebo cerebrovaskulárního onemocnění nebo u pacientů s diabetes mellitus 2. typu se známkami poškození cílových orgánů. Studie VA NEPHRON-D byla vedena u pacientů s diabetes mellitus 2. typu a diabetickou nefropatií.
V těchto studiích nebyl prokázán žádný významně příznivý účinek na renální a/nebo kardiovaskulární ukazatele a na mortalitu, ale v porovnání s monoterapií bylo pozorováno zvýšené riziko hyperkalemie, akutního poškození ledvin a/nebo hypotenze. Vzhledem k podobnosti farmakodynamických vlastností jsou tyto výsledky relevantní rovněž pro další inhibitory ACE a blokátory receptorů pro angiotenzin II. Inhibitory ACE ia blokátory receptorů pro angiotensin II. proto nesmí pacienti s diabetickou nefropatií užívat současně.
Studie ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) byla navržena tak, aby zhodnotila přínos přidání aliskirenu k standardní terapii inhibitorem
ACE nebo blokátorem receptorů pro angiotenzin II u pacientů s diabetes mellitus 2. typu a chronickým onemocněním ledvin, kardiovaskulárním onemocnění, nebo obojím. Studie byla předčasně ukončena z důvodu zvýšení rizika nežádoucích komplikací. Kardiovaskulární úmrtí a cévní mozková příhoda byly numericky častější ve skupině s aliskirenem než ve skupině s placebem a zároveň nežádoucí účinky a sledované závažné nežádoucí účinky (hyperkalemie, hypotenze a renální dysfunkce) byly častěji hlášeny ve skupině s aliskirenem oproti placebové skupině.
Telmisartan byl také podobně účinný jako ramipril, pokud se týká předem stanoveného sekundárního cílového parametru účinnosti - úmrtí z kardiovaskulárních příčin, nefatální infarkty myokardu a nefatální cévní mozkové příhody [0,99 (97,5% CI 0,90 - 1,08, p (non-inferiorita) = 0,0004)], které byly primárním cílovým parametrem účinnosti referenční studie HOPE (z anglického Heart Outcomes Prevention Evaluation), která zkoumala účinek ramiprilu ve srovnání s placebem.
Klinická studie TRANSCEND randomizovala pacienty netolerující ACE-inhibitory, jinak byla vstupní kriteria stejná jako ve studii ONTARGET. Pacienti užívali telmisartan 80 mg (n=2954) nebo placebo (n=2972), obojí nad rámec standardní péče. Průměrná doba sledování byla 4 roky a 8 měsíců.
Nebyl prokázán statisticky významný rozdíl ve výskytu primárního kombinovaného cílového parametru (úmrtí z kardiovaskulárních příčin, nefatální srdeční infarkty, nefatální cévní mozkové příhody nebo hospitalizace z důvodu srdečního selhání) - 15,7% telmisartan, 17,0% placebo s relativním rizikem 0,92 (95% CI 0,81 - 1,05, p = 0,22). Telmisartan byl účinnější než placebo v předem stanoveném sekundárním kombinovaném cílovém parametru - úmrtí z kardiovaskulárních příčin, nefatální srdeční infarkty a nefatální cévní mozkové příhody [0,87 (95% CI 0,76 - 1,00, p = 0,048)]. Prospěch nebyl prokázán u kardiovaskulární mortality (relativní riziko 1,03, 95% CI 0,85 - 1,24).
U pacientů léčených telmisartanem byl méně často hlášen kašel a angioedém než u pacientů, kterým byl podáván ramipril. Naopak v případě telmisartanu byla častěji hlášena hypotenze.
Kombinace telmisartanu s ramiprilem nepřinesla další prospěch ve srovnání se samotným ramiprilem nebo samotným telmisartanem. Výskyt kardiovaskulární mortality a mortality ze všech příčin byl u této kombinace vyšší. Navíc v této skupině došlo k významně vyššímu výskytu hyperkalémie, renálnímu selhání, hypotenze a synkop. U této skupiny pacientů se proto používání kombinace telmisartanu s ramiprilem nedoporučuje.
Ve studii „Účinná sekundární prevence cévních mozkových příhod“ (PRoFESS) u pacientů ve věku 50 let a starších, kteří prodělali cévní mozkovou příhodu, byl zaznamenán zvýšený výskyt sepse po telmisartanu ve srovnání s placebem, 0,70 % vs. 0,49 % [RR 1,43 (95 % interval spolehlivosti 1,00-2,06)]; výskyt fatálních případů sepse byl zvýšen u pacientů léčených telmisartanem (0,33 %) vs. pacienti léčení placebem (0,16 %) [RR 2,07 (95 % interval spolehlivosti 1,14-3,76)]. Pozorovaná zvýšená míra výskytu sepse spojené s podáváním telmisartanu může být náhodný nález nebo může souviset s dosud neznámým mechanismem.
Pediatrická populace
Bezpečnost a účinnost přípravku Telmisartan Teva u dětí a dospívajících mladších 18 let nebyla stanovena.
Hypotenzní účinky dvou dávek telmisartanu byly hodnoceny u 76 pacientů s hypertenzí, převážně s nadváhou ve věku 6 až 18 let (tělesná hmotnost > 20 kg a < 120 kg, průměrně 74,6 kg) po podání telmisartanu v dávce 1 mg/kg (n = 29 léčených pacientů) nebo 2 mg/kg (n = 31 léčených pacientů) po dobu 4 týdnů léčby. Sekundární hypertenze nebyla do hodnocení zahrnuta. U některých sledovaných pacientů byly užité dávky vyšší, než jsou doporučené k léčbě hypertenze u dospělé populace a dosáhly denní dávky srovnatelné se 160 mg, která byla testována u dospělých pacientů. Průměrné změny systolického krevního tlaku oproti výchozímu stavu (primární cíl), upravené s ohledem na věkovou skupinu, byly -14,5 (1,7) mm Hg ve skupině s telmisartanem 2 mg, -9,7 (1,7) mm Hg ve skupině s telmisartanem 1 mg/kg a -6,0 (2,4) mm Hg ve skupině s placebem.
Upravené změny diastolického tlaku oproti výchozímu stavu byly -8,4 (1,5) mm Hg, -4,5 (1,6) mm Hg a -3,5 (2,1) mm Hg. Změna byla závislá na dávce. Údaje o bezpečnosti z této studie u pacientů ve věku 6 až 18 let jsou obecně podobné jako u dospělých. Bezpečnost dlouhodobé léčby telmisartanem u dětí a dospívajících nebyla hodnocena.
Zvýšení eosinofilů hlášené v této skupině pacientů nebylo u dospělých zaznamenáno. Jeho klinický význam a závažnost nejsou známy.
Tyto klinické údaje neumožňují stanovit účinnost a bezpečnost telmisartanu u pediatrické populace s hypertenzí.
5.2 Farmakokinetické vlastnosti
Absorpce
Absorpce telmisartanu je rychlá, i když rozsah jeho vstřebání kolísá. Průměrná hodnota absolutní biologické dostupnosti telmisartanu představuje asi 50 %. Pokud se telmisartan podává spolu s jídlem, pohybuje se redukce plochy pod křivkou závislosti plazmatických koncentrací na čase (AUC-nekonečno) přibližně od 6 % (dávka 40 mg) do 19 % (dávka 160 mg). Od 3 hodin po podání telmisartanu nalačno nebo současně s jídlem se jeho plazmatické koncentrace neliší.
Linearita/nelinearita
Nepředpokládá se, že by menší redukce AUC mohla vést ke snížení terapeutické účinnosti.
Neexistuje lineární závislost mezi dávkami a plazmatickými hladinami. Hodnoty Cmax a v menší míře i AUC rostou nerovnoměrně při dávkách překračujících 40 mg.
Distribuce
Telmisartan se z velké části váže na plazmatické bílkoviny (>99,5 %), především na albumin a alfa-1 kyselý glykoprotein. Distribuční objem v ustáleném stavu (Vdss) dosahuje přibližně 500 l.
Biotransformace
Telmisartan se metabolizuje konjugací na glukuronid výchozí látky. U konjugátu nebyla prokázána žádná farmakologická aktivita.
Eliminace
Telmisartan je charakterizován biexponenciálním poklesem farmakokinetiky s terminálním poločasem eliminace >20 h. Maximální plazmatické koncentrace (Cmax) a v menší míře plocha pod křivkou plazmatických koncentrací v závislosti na čase (AUC) rostou nerovnoměrně s dávkou.
V doporučovaných dávkách nebyla prokázána klinicky významná kumulace telmisartanu. Plazmatické koncentrace byly u žen vyšší než u mužů, avšak bez významného vlivu na účinnost.
Po perorálním (a nitrožilním) podání se telmisartan téměř výhradně vylučuje stolicí, většinou jako nezměněná substance. Kumulativní vylučování močí je menší než 1 % dávky. Celková plazmatická clearance (Cltot) je vysoká (přibližně 1000 ml/min) v porovnání s průtokem krve játry (kolem 1500 ml/min).
Zvláštní skupiny pacientů
Pediatrická populace
Farmakokinetika dvou dávek telmisartanu byla hodnocena jako sekundární cíl u pacientů s hypertenzí (n = 57) ve věku od 6 do 18 let po podání telmisartanu 1 mg/kg nebo 2 mg/kg po dobu 4 týdnů léčby. Farmakokinetické parametry zahrnovaly stanovení ustáleného stavu telmisartanu u dětí a dospívajících a hodnocení rozdílů v závislosti na věku. Přestože studie byla příliš malá pro významné posouzení farmakokinetiky u dětí mladších 12 let, výsledky jsou obecně v souladu s nálezy u dospělých a potvrzují ne-linearitu telmisartanu, zejména pro Cmax.
Pohlaví:
Byly pozorovány rozdíly v plazmatických koncentracích v závislosti na pohlaví, s hodnotami Cmax přibližně třikrát a AUC přibližně dvakrát vyššími u žen než u mužů.
Starší pacienti:
Farmakokinetika telmisartanu se u starších pacientů a pacientů mladších než 65 let neliší.
Porucha funkce ledvin:
U pacientů s mírnou až středně závažnou a závažnou poruchou funkce ledvin byly pozorovány dvojnásobné koncentrace v plazmě, avšak u pacientů s nedostatečností ledvin podstupujících hemodialýzu byly pozorovány nižší plazmatické koncentrace. Telmisartan se u pacientů s ledvinnou nedostatečností do vysoké míry váže na plazmatické bílkoviny a dialýzou jej nelze odstranit. Poločas eliminace se u pacientů s poruchou funkce ledvin nemění.
Porucha funkce jater
Farmakokinetické studie u pacientů s poruchou funkce jater prokázaly zvýšení hodnot absolutní biologické dostupnosti téměř na 100 %. Poločas eliminace se u pacientů s poruchou funkce jater nemění.
5.3 Předklinické údaje vztahující se k bezpečnosti
V předklinických studiích bezpečnosti po podání dávek, které vedly k expozici srovnatelné s klinickým terapeutickým rozmezím, došlo u normotenzních zvířat ke snížení hodnot červeného krevního obrazu (erytrocytů, hemoglobinu, hematokritu), změnám v renální hemodynamice (nárůst dusíku močoviny a kreatininu) a zvýšení hladiny sérového draslíku. U psů byla pozorována dilatace renálních tubulů a jejich atrofie. U potkanů a psů byly rovněž zaznamenány změny žaludeční sliznice (eroze, vředy nebo zánět). Těmto farmakologicky vyvolaným nežádoucím účinkům, známým z předklinického hodnocení jak inhibitorů enzymu konvertujícího angiotenzin, tak antagonistů receptoru angiotenzinu II, bylo možné předejít perorálním podáváním fyziologického roztoku.
U potkanů a psů byly rovněž pozorovány zvýšené hodnoty reninu v plazmě a hypertrofie/hyperplazie ledvinových juxtaglomerulárních buněk. Tyto změny, představující rovněž skupinový účinek inhibitorů enzymu konvertujícího angiotenzin II a antagonistů receptoru angiotenzinu II, zřejmě nemají klinický význam.
Nebyl zjištěn žádný důkaz o teratogenním účinku, avšak podávání telmisartanu v toxických dávkách má vliv na postnatální vývoj jedinců jako je nižší tělesná hmotnost a opožděné otevírání očí.
Testy in vitro neprokázaly mutagenní a významnou klastogenní aktivitu ani nebyl prokázán kancerogenní účinek u potkanů a myší.
6. FARMACEUTICKÉ VLASTNOSTI
6.1 Seznam pomocných látek
Mikrokrystalická celulosa (Avicel PH 102) Sodná sůl karboxymethylškrobu (Typ A) Poloxamer Meglumin
Povidon (PVP K-30)
Sorbitol (E420)
Magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3. Doba použitelnosti
2 roky
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
Al/Al odlupovací perforované jednodávkové blistry a Al/Al perforované jednodávkové blistry. Odlupovací perforované blistry obsahující 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet.
Perforované blistry obsahující 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Teva B.V.
Swensweg 5 2031GA Haarlem Nizozemsko
8. REGISTRAČNÍ ČÍSLO (A)
EU/1/09/610/001
EU/1/09/610/002
EU/1/09/610/003
EU/1/09/610/004
EU/1/09/610/005
EU/1/09/610/006
EU/1/09/610/007
EU/1/09/610/008
EU/1/09/610/009
EU/1/09/610/010
EU/1/09/610/031
Krabička se 14x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 28x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 30x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 40x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 56x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 60x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 84x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 90x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 98x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 100x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 14x1 tabletami v perforovaných jednodávkových Al/Al blistrech
Krabička s 28x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 30x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 40x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 56x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 60x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 84x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 90x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 98x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 100x1 tabletami v perforovaných jednodávkových Al/Al blistrech
EU/1/09/610/032 EU/1/09/610/033 EU/1/09/610/034 EU/1/09/610/035 EU/1/09/610/036 EU/1/09/610/037 EU/1/09/610/038 EU/1/09/610/039 EU/1/09/610/040
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 26. ledna 2010
Datum posledního prodloužení registrace: 19/12/2014
10. DATUM REVIZE TEXTU
Podrobné informace o tomto přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
1. NÁZEV PŘÍPRAVKU
Telmisartan Teva 40 mg tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna tableta obsahuje telmisartanum 40 mg
Pomocné látky se známým účinkem:
Jedna tableta obsahuje 42,8 mg sorbitolu (E420)
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Tablety
Bílé až téměř bílé tablety oválného tvaru, na jedné straně tablety je vyraženo číslo “93”. Na druhé straně je vyraženo číslo “7459”.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Hypertenze
Léčba esenciální hypertenze u dospělých pacientů
Kardiovaskulární prevence
Snížení kardiovaskulární morbidity u dospělých:
• s manifestním aterotrombotickým kardiovaskulárním onemocněním (anamnéza ischemické choroby srdeční nebo cévní mozkové příhody nebo onemocnění periferních tepen) nebo
• s diabetes mellitus typu 2 s prokázaným orgánovým postižením
4.2 Dávkování a způsob podání
Dávkování
Léčba esenciální hypertenze
Obvyklá účinná dávka je 40 mg jednou denně. U některých pacientů se příznivý výsledek dostavuje již při denní dávce 20 mg. V případech, kdy se nedosáhne požadovaných hodnot krevního tlaku, lze dávku telmisartanu zvýšit až na 80 mg jednou denně. Alternativně lze telmisartan použít v kombinaci s diuretiky thiazidového typu, jako např. hydrochlorothiazidem, u kterého bylo prokázáno, že aditivně snižuje krevní tlak pomocí telmisartanu. Pokud se uvažuje o zvyšování dávek, je třeba přihlížet k okolnosti, že maximálního antihypertenzního účinku se obvykle dosáhne čtyři až osm týdnů po zahájení léčby (viz bod 5.1).
Kardiovaskulární prevence
Doporučená dávka je 80 mg jednou denně. Nejsou k dispozici údaje o tom, zda dávky telmisartanu nižší než 80 mg jsou účinné při snižování kardiovaskulární morbidity.
Při zahájení léčby telmisartanem ke snížení kardiovaskulární morbidity se doporučuje pečlivé sledování krevního tlaku. V některých případech může být nezbytné upravit léky snižující krevní tlak.
Pacienti s poruchou _ funkce ledvin
U pacientů se závažnou poruchou funkce ledvin nebo podstupujících hemodialýzu jsou k dispozici jen omezené zkušenosti. U těchto pacientů je doporučena nižší úvodní dávka 20 mg (viz bod 4.4).
U pacientů s mírnou až středně závažnou poruchou funkce ledvin není třeba upravovat dávkování.
Pacienti s poruchou funkce jater
Telmisartan Teva je kontraindikován u pacientů se závažnou poruchou funkce jater (viz bod 4.3). U pacientů s mírnou až středně závažnou poruchou funkce jater by dávka neměla přesáhnout 40 mg jednou denně (viz bod 4.4).
Starší pacienti
Úprava dávkování u starších pacientů není nutná.
Pediatrická populace
Bezpečnost a účinnost přípravku Telmisartan Teva u dětí a dospívajících mladších 18 let nebyla stanovena.
Aktuálně dostupné údaje jsou popsány v bodech 5.1 a 5.2, ale doporučené dávkování stanovit nelze Způsob podání
Telmisartan tablety se užívají jednou denně perorálně a měly by se podávat s tekutinami, s jídlem nebo bez jídla.
4.3 Kontraindikace
• Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku uvedenou v bodě 6.1
• Druhý a třetí trimestr těhotenství (viz bod 4.4 a 6.4)
• Obstrukce žlučovodů
• Závažná porucha funkce jater
Současné užívání přípravku Telmisartan Teva s přípravky obsahujícími aliskiren je kontraindikováno u pacientů s diabetes mellitus nebo poruchou funkce ledvin (GFR <60 ml/min/1.73 m2) (viz body 4.5 a 5.1).
4.4 Zvláštní upozornění a opatření pro použití
Léčba pomocí antagonistů receptoru angiotensinu II nesmí být během těhotenství zahájena. Pokud není pokračování v léčbě antagonisty receptoru angiotensinu II považováno za nezbytné, pacientky plánující těhotenství musí být převedeny na jinou léčbu hypertenze, a to takovou, která má ověřený bezpečnostní profil, pokud jde o podávání v těhotenství. Pokud je zjištěno těhotenství, léčba pomocí antagonistů receptoru angiotensinu II musí být ihned ukončena, a pokud je to vhodné, může být zahájena alternativní léčba (viz body 4.3 a 4.6).
Poškození funkce jater
Vzhledem k tomu, že se Telmisartan Teva vylučuje především žlučí, nesmí být podáván pacientům s cholestázou, obstrukcí žlučovodů nebo závažným poškozením jater (viz bod 4.3). U těchto pacientů se předpokládá snížení jaterní clearence telmisartanu. Pacientům s mírným až středně závažným poškozením jater může být Telmisartan Teva podán pouze se zvýšenou opatrností.
Renovaskulární hypertenze
Pacientům s oboustrannou stenózou renální arterie nebo se stenózou arterie zásobující jedinou funkční ledvinu, kteří jsou léčeni přípravky ovlivňujícími renin-angiotenzin-aldosteronový systém, hrozí zvýšené riziko těžké hypotenze a renální nedostatečnost.
Renální poškození a transplantace ledvin
Pokud je přípravek Telmisartan Teva podáván pacientům s poruchou jater, je doporučena pravidelná kontrola sérových hladin draslíku a kreatininu v krvi. Nejsou žádné zkušenosti s podáváním přípravku Telmisartan Teva pacientům po transplantaci ledvin.
Intravaskulární hypovolaemie
U pacientů s poklesem objemu nebo koncentrace sodíku v důsledku intenzivní diuretické terapie, omezování soli v dietě, průjmu nebo zvracení se zejména po první dávce přípravku Telmisartan Teva může objevit symptomatická hypotenze. Takové stavy by se měly ještě před podáním přípravku Telmisartan Teva korigovat, stejně jako snížení intravaskulárního objemu nebo deplece sodíku.
Duální blokáda systému renin-angiotenzin-aldosteron (RAAS)
Bylo prokázáno, že současné užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu zvyšuje riziko hypotenze, hyperkalemie a snížení funkce ledvin (včetně akutního selhání ledvin). Duální blokáda RAAS pomocí kombinovaného užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu se proto nedoporučuje (viz body 4.5 a 5.1).
Pokud je duální blokáda považována za naprosto nezbytnou, má k ní docházet pouze pod dohledem specializovaného lékaře a za častého pečlivého sledování funkce ledvin, elektrolytů a krevního tlaku. Inhibitory ACE a blokátory receptorů pro angiotenzin II nemají být používány současně u pacientů s diabetickou nefropatií.
Ostatní stavy provázené stimulací renin-angiotenzin-aldosteronového systému U pacientů, jejichž cévní tonus a renální funkce závisejí převážně na aktivitě renin-angiotenzin-aldosteronového systému (např. u pacientů se závažným městnavým srdečním selháním nebo s průvodním onemocněním ledvin, včetně stenózy renální arterie), byla léčba dalšími přípravky, které ovlivňují tento systém podobně jako telmisartan, spojeny s akutní hypotenzí, hyperazotemií, oligurií nebo vzácněji i s akutním selháním ledvin (viz bod 4.8).
Primární aldosteronismus
Pacienti s primárním aldosteronismem obvykle nereagují na antihypertenziva působící mechanismem inhibice renin-angiotenzin-aldosteronového systému. V těchto případech se léčba telmisartanem nedoporučuje.
Stenóza aortální a mitrální chlopně, obstrukční hypertrofická kardiomyopatie
Stejně jako u ostatních vazodilatancií je třeba věnovat zvlášť zvýšenou pozornost pacientům trpícím
stenózami aortální a mitrální chlopně nebo obstrukční hypertrofickou kardiomyopatií.
Diabetičtí pacienti léčení inzulínem nebo antidiabetiky
U těchto pacientů se může při léčbě telmisartanem objevit hypoglykémie. Proto je u nich
vhodné zvážit sledování hladiny glukózy v krvi; a pokud je indikováno, upravit dávky inzulinu nebo
antidiabetik.
Hyperkalémie
Podávání léčivých přípravků, které ovlivňují renin-angiotenzin-aldosteronový systém, může vést k hyperkalémii.
U starších pacientů, u pacientů s poškozením funkce ledvin, u diabetiků, u pacientů současně léčených jinými přípravky, které mohou zvyšovat hladinu draslíku, a/nebo u pacientů s určitými interkurentními příhodami, může být hyperkalémie fatální.
Před zvažováním současného podávání léčivých přípravků, které ovlivňují renin-angiotenzin-aldosteronový systém, je nutno zhodnotit poměr přínosu a rizika.
Hlavní rizikové faktory hyperkalemie, které je třeba zvažovat:
- Diabetes mellitus, poškozená funkce ledvin, věk (>70 let)
- Kombinace s jedním nebo více léčivými přípravky, které ovlivňují renin-angiotenzin-aldosteronový systém, a/nebo s přípravky doplňujícími draslík. Léčivé přípravky nebo terapeutické třídy léčivých přípravků, které mohou vyvolat hyperkalémii jsou náhražky soli obsahující draslík, draslík šetřící diuretika, ACE inhibitory, antagonisté receptoru angiotenzinu II, nesteroidní protizánětlivé léčivé přípravky (NSAIDs, včetně selektivních COX-2 inhibitorů), heparin, imunosupresiva (cyklosporin nebo takrolismus) a trimethoprim.
- Interkurentní příhody, zejména dehydratace, akutní srdeční dekompenzace, metabolická acidóza, zhoršení renálních funkcí, náhlé zhoršení podmínek pro funkci ledvin (např. infekční onemocnění), rozpad buněk (např. při akutní ischemii končetin, rabdomyolýze, rozsáhlém traumatu).
U rizikových pacientů se doporučuje sledovat sérové hladiny draslíku (viz bod 4.5).
Sorbitol
Tento léčivý přípravek obsahuje sorbitol (E420). Pacienti se vzácnou vrozenou intolerancí fruktosy nesmí Telmisartan Teva užívat.
Etnické odlišnosti
Stejně jako inhibitory enzymu konvertujícího angiotenzin, také telmisartan a další antagonisté receptoru angiotenzinu II zjevně navozují u černošské populace méně výrazné snížení krevního tlaku než u jiných lidských ras, pravděpodobně v souvislosti s vyšší prevalencí stavů s nízkou hladinou reninu v populaci hypertoniků černé pleti.
Další upozornění
Analogicky jako u kterýchkoli jiných antihypertenziv může dojít při nadměrném snížení krevního tlaku u pacientů s ischemickou kardiopatií nebo s ischemickou chorobou srdeční k infarktu myokardu nebo k cévní mozkové příhodě.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Digoxin
Při současném podání telmisartanu s digoxinem bylo pozorováno zvýšení střední hodnoty vrcholové plasmatické koncentrace digoxinu (49%) a minimální koncentrace (20%). Při zahájení, úpravě a ukončení léčby telmisartanem byla monitorována hladina digoxinu proto, aby byla zachována jeho hladina v terapeutickém rozmezí.
Tak jako ostatní léčiva působící na renin-angiotenzin-aldosteronový systém, telmisartan může způsobit hyperkalémii (viz bod 4.4). Riziko se může zvýšit v případě kombinované léčby s dalšími léčivými přípravky, které mohou také vyvolat hyperkalémii (náhražky soli obsahující draslík, draslík šetřící diuretika, ACE inhibitory, antagonisté receptoru angiotenzinu II, nesteroidní protizánětlivé léčivé přípravky (NSAIDs, včetně selektivních COX-2 inhibitorů), heparin, imunosupresiva (cyklosporin nebo takrolismus) a trimethoprim).
Výskyt hyperkalémie závisí na přidružených rizikových faktorech. Riziko se zvyšuje v případě výše uvedených léčebných kombinací. Riziko je zvláště vysoké při kombinaci s kalium šetřícími diuretiky a při kombinaci s náhražkami soli obsahujícími draslík. Kombinace např. s ACE inhibitory nebo s NSAIDs představují menší riziko za předpokladu, že jsou přesně dodržována opatření při podávání.
Současné podávání se nedoporučuje
Draslík šetřící diuretika a přípravky obsahující draslík
Antagonisté receptoru angiotenzinu II jako telmisartan, zmenšují ztrátu draslíku, navozenou diuretiky. Draslík šetřící diuretika, například spironolakton, eplerenon, triamteren nebo amilorid, přípravky obsahující draslík nebo náhražky soli obsahující draslík, mohou vést k významnému zvýšení hladiny draslíku v séru. Pokud je indikováno současné podávání z důvodu prokázané hypokalemie, je nutno je podávat opatrně a za častých kontrol hladin draslíku v séru.
Lithium
Při současném podávání lithia spolu s inhibitory angiotenzin konvertujícího enzymu byl hlášen reverzibilní nárůst koncentrací lithia v séru a jeho toxicita, a také při současném podávání lithia a antagonistů receptoru angiotenzinu II včetně telmisartanu. Pokud se ukáže kombinované podávání jako nezbytné, doporučuje se pečlivě monitorovat sérové hladiny lithia.
Současné podávání vyžadující opatrnost
Nesteroidní protizánětlivé léčivé přípravky (NSAIDs)
NSAIDs (např. kyselina acetylosalicylová v protizánětlivých dávkách, inhibitory COX-2 a neselektivní NSAIDs) mohou snižovat antihypertenzivní účinek antagonistů receptoru angiotensinu II. U některých pacientů s oslabenou funkcí ledvin (např. u dehydratovaných pacientů nebo starších pacientů s poruchou funkce ledvin) může mít současné podávání antagonistů receptoru angiotensinu II a přípravků, které blokují cyklooxygenázu, za následek další zhoršení funkce ledvin, včetně možného vzniku akutního selhání ledvin, které je obvykle reverzibilní. Z tohoto důvodu je nutno podávat takovou kombinaci velmi opatrně, zejména u starších pacientů. Pacienti musí být dostatečně hydratováni a je třeba zvážit kontroly funkce ledvin po zahájení, a také v pravidelných intervalech během této kombinované terapie.
V jedné studii vedlo současné podávání telmisartanu a ramiprilu ke 2,5 násobnému zvýšení AUC0-24 a Cmax ramiprilu a ramiprilátu. Klinický význam tohoto zjištění není znám.
Diuretika (thiazidová nebo kličková diuretika)
Předchozí léčba vysokými dávkami diuretik jako je furosemid (kličkové diuretikum) a hydrochlorothiazid (thiazidové diuretikum) může vést k volumdepleci a k riziku vzniku hypotenze po zahájení léčby telmisartanem.
Současné podávání, které je nutno zvažovat
Jiná antihypertenziva
Účinek telmisartanu na snížení krevního tlaku může být zvýrazněn při současném podávání jiných antihypertenziv.
Data z klinických studií ukázala, že duální blokáda systému renin-angiotenzin-aldosteron (RAAS) pomocí kombinovaného užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu je spojena s vyšší frekvencí nežádoucích účinků, jako je hypotenze, hyperkalemie a snížená funkce ledvin (včetně akutního renálního selhání) ve srovnání s použitím jedné látky ovlivňující RAAS (viz body 4.3, 4.4 a 5.1).
Na základě farmakologických vlastností následně uvedených léku lze očekávat, že tyto léčivé přípravky mohou zvýraznit hypotenzní účinek všech antihypertenziv, včetně telmisartanu: baklofem, amifostin.
Vedle toho může být orthostatická hypotenze potencována alkoholem, barbituráty, narkotiky nebo antidepresivy.
Kortikosteroidy (systémové podání)
Snížení antihypertenzního účinku.
4.6 Fertilita, těhotenství a kojení
Užívání antagonistů receptoru angiotensinu II se nedoporučuje během prvního trimestru těhotenství (viz bod 4.4). Užívání antagonistů receptoru angiotensinu II je kontraindikováno během druhého a třetího trimestru těhotenství (viz body 4.3 a 4.4).
Adekvátní údaje o podávání přípravku Telmisartan Teva těhotným ženám nejsou k dispozici. Studie na zvířatech poukázaly na reprodukční toxicitu (viz bod 5.3).
Epidemiologické důkazy týkající se rizika teratogenicity při podáván ACE inhibitorů během prvního trimestru těhotenství nebyly nezvratné; malý nárůst rizika však nelze vyloučit. I když neexistují žádné kontrolované epidemiologické údaje pokud jde o riziko při podávání antagonistů receptoru angiotenzinu II, pro tuto třídu léčiv může existovat riziko podobné. Pokud pokračování v léčbě antagonisty receptoru angiotenzinu II není považováno za nezbytné, pacientky plánující těhotenství musí být převedeny na jinou léčbu vysokého krevního tlaku, a to takovou, která má ověřený bezpečnostní profil, pokud jde o podávání v těhotenství. Jestliže je těhotenství prokázáno, léčba pomocí antagonistů receptoru angiotenzinu II musí být ihned ukončena, a pokud je to vhodné, je nutné zahájit jiný způsob léčby.
Je známo, že expozice vůči antagonistům receptoru angiotenzinu II během druhého a třetího trimestru těhotenství vede u lidí k fetotoxicitě (pokles funkce ledvin, oligohydramnion, zpoždění osifikace lebky) a k novorozenecké toxicitě (selhání ledvin, hypotenze, hyperkalémie). (Viz bod 5.3).
Pokud by došlo k expozici vůči antagonistům receptoru angiotenzinu II od druhého trimestru těhotenství, doporučuje se sonografická kontrola funkce ledvin a lebky.
Děti, jejichž matky užívaly antagonisty receptoru angiotenzinu II, musí být pečlivě sledovány, pokud jde o hypotenzi (viz body 4.3 a 4.4).
Kojení
Protože nejsou k dispozici žádné údaje ohledně užívání přípravku Telmisartan Teva během kojení, Telmisartan Teva se nedoporučuje, je vhodnější zvolit jinou léčbu s lepším bezpečnostním profilem během kojení, obzvláště během kojení novorozence nebo předčasně narozeného dítěte.
Fertilita:
V předklinických studiích nebyly u telmisartanu pozorovány žádné účinky na samčí nebo samičí plodnost.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Při řízení motorových vozidel nebo obsluze strojních zařízení je však třeba mít na paměti, že léčba antihypertenzivy, jako je Telmisartan Teva, může v některých případech způsobovat závratě nebo ospalost.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Vzácně (>1/10 000 až <1/1 000) mohou být pozorovány závažné nežádoucí účinky včetně anafylaktické reakce a angioedému a akutní renální selhání.
V kontrolovaných studiích u pacientů s hypertenzí byla celková frekvence výskytu nežádoucích účinků hlášených pro telmisartan obvykle srovnatelná s placebem (41,4% vs 43,9 %). Výskyt nežádoucích účinků není závislý na dávce ani na pohlaví, věku nebo rase pacientů. Bezpečnostní profil telmisartanu podávaného pacientům ke snížení kardiovaskulární morbidity byl shodný
s bezpečnostním profilem zjištěným u pacientů s hypertenzí.
Následně uvedené nežádoucí účinky byly shromážděny z kontrolovaných studií u pacientů léčených pro hypertenzi a z postmarketingových sledování. Dále se vycházelo z hlášení závažných nežádoucích příhod a nežádoucích příhod vedoucích k přerušení léčby v rámci tří dlouhodobých klinických studií s 21642 pacienty, kterým byl podáván telmisartan ke snížení kardiovaskulární morbidity až po dobu šesti let.
Souhrn nežádoucích účinků v tabulce
Nežádoucí účinky jsou podle frekvence výskytu rozděleny za použití následujícího pravidla: velmi časté (>1/10); časté (>1/100 až <1/10); méně časté (>1/1000 až <1/100; vzácné (>1/10000 až <1/1000); velmi vzácné (<1/10000).
V každé skupině četnosti jsou nežádoucí účinky seřazeny podle klesající závažnosti.
|
Infekce a infestace Méně časté: Vzácné: |
Infekce močových cest včetně zánětů močového měchýře, infekce horních cest dýchacích včetně faryngitidy a sinusitidy Sepse včetně případů vedoucích k úmrtí1 |
Poruchy krve a lymfatického systému Méně časté: Anémie
Vzácné: Eosinofilie, trombocytopenie
Poruchy imunitního systému
Vzácné: Přecitlivělost, anafylaktická reakce
Poruchy metabolismu a výživy
Méně časté: Hyperkalémie
|
Vzácné: |
Hypoglykémie (u diabetických pacientů) |
|
Psychiatrické poruchy Méně časté: Vzácné: |
Insomnie, deprese Úzkost |
|
Poruchy nervového systému Méně časté: Vzácné: |
Synkopa Somnolence |
|
Poruchy oka Vzácné: |
Poruchy vidění |
|
Poruchy ucha a labyrintu Méně časté: | |
|
Srdeční poruchy Méně časté: Vzácné: |
Bradykardie |
|
Cévní poruchy Méně časté: |
Respirační, hrudní a mediastinální poruchy
Méně časté: Dyspnoe, kašel
|
Velmi vzácné: |
Intersticiální plicní nemoc4 |
|
Gastrointestinální poruchy Méně časté: Vzácné: |
Bolesti břicha, průjem, dyspepsie, plynatost, zvracení Sucho v ústech, žaludeční nevolnost, dysgeuzie |
Poruchy jater a žlučových cest
V zácné: Abnormální j atemí funkce/j atemí poruchy3
Poruchy kůže a podkožní tkáně
Méně časté: Zvýšené pocení, pruritus, kožní vyrážka
Vzácné: Erytém, angioedém (včetně případů vedoucích k úmrtí), urticaria,
ekzém, polékový exantém, toxoalergický exantém,
Poruchy svalové a kosterní soustavy a pojivové tkáně
Méně časté: Bolesti zad (například ischias), svalové spasmy, myalgie
Vzácné: Artralgie, bolesti končetin, bolesti šlach (příznaky podobné zánětu
šlach)
Poruchy ledvin a močových cest
Méně časté: Poškození ledvin včetně akutního renálního selhání
Celkové poruchy a reakce v místě aplikace
Méně časté: Bolesti na hrudi, astenie (slabost)
Vzácné: Onemocnění připomínající chřipku
Vyšetření
Méně časté: Zvýšená hladina kreatininu v krvi
Vzácné: Pokles hemoglobinu, zvýšení hladiny kyseliny močové v krvi,
zvýšení jaterních enzymů, zvýšení kreatinfosfokinázy
1, 2,3,4.
pro další popis, viz část „Popis vybraných nežádoucích účinků “
c. Popis vybraných nežádoucích účinků
Sepse
Ve studii PRoFESS byl pozorován zvýšený výskyt sepse po telmisartanu ve srovnání s placebem. Příhoda může být náhodný nález nebo může souviset s dosud neznámým mechanismem (viz také bod 5.1).
Tento nežádoucí účinek byl hlášen jako častý u pacientů s upraveným krevním tlakem, kterým byl podáván telmisartan ke snížení kardiovaskulární morbidity nad rámec standardní péče.
Abnormální jaterní funkce/porucha jater
Většina případů abnormální jaterní funkce/poruchy jater z post-marketingových zkušeností se vyskytla u japonských pacientů. U japonských pacientů se tyto nežádoucí účinky vyskytují s větší pravděpodobností.
Intersticiální plicní nemoc
Na základě zkušeností po uvedení přípravku na trh byly hlášeny případy intersticiální plicní nemoci v časové souvislosti s podáním telmisartanu. Příčinná souvislost ale nebyla stanovena.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
K dispozici jsou pouze omezené informace týkající se předávkování u člověka.
Příznaky
Nejnápadnějšími projevy předávkování telmisartanem jsou hypotenze a tachykardie; vyskytla se bradykardie, závrať, zvýšení kreatininu v séru a akutní selhání ledvin.
Terapie
Telmisartan nelze odstranit hemodialýzou. Pacient by měl být pečlivě monitorován, léčba by měla být podpůrná a symptomatická. Léčba závisí na časovém úseku, který uplynul od požití a na závažnosti příznaků. Navrhovaná opatření zahrnují navození zvracení a/nebo výplach žaludku. Vhodnou léčbou předávkování může být použití aktivního uhlí. Hladiny elektrolytů a kreatininu v séru je nutno často monitorovat. Pokud dojde k hypotenzi, je nutno pacienta uložit do polohy vleže na zádech a urychleně podat soli a doplnit objem tekutin.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antagonisté angiotensinu II, samotní; ATC kód: C09CA07. Mechanismus účinku
Telmisartan je specifický antagonista receptoru angiotenzinu II (typ AT1) účinný po perorálním podání. S vysokou afinitou vytěsňuje angiotenzin II z jeho vazebného místa na subtypu receptoru AT1, který odpovídá za známé působení angiotenzinu II. Telmisartan nemá na receptoru AT1 žádnou parciální agonistickou aktivitu a váže se selektivně na tento receptor. Vazba má dlouhodobý charakter. Telmisartan nevykazuje afinitu k ostatním receptorům, včetně AT2 a ostatních méně charakterizovaných AT. Funkční význam těchto receptorů není znám, stejně jako efekt jejich možné zvýšené stimulace angiotenzinem II, jehož hladiny se podáváním telmisartanem zvyšují. Plazmatické hladiny aldosteronu se podáváním telmisartanu snižují. Telmisartan neinhibuje u lidí plazmatický renin ani neblokuje iontové kanály. Telmisartan neinhibuje enzym konvertující angiotenzin (kinázu II), což je enzym, který rovněž rozkládá bradykinin. Proto se nepředpokládá, že by telmisartan potencoval nežádoucí účinky zprostředkované bradykininem.
Dávka telmisartanu 80 mg u člověka téměř zcela inhibuje zvýšení krevního tlaku vyvolané angiotenzinem II. Inhibiční účinek přetrvává déle než 24 hodin a je měřitelný po dobu až 48 hodin.
Klinická účinnost a bezpečnost
Léčba esenciální hypertenze
Po první dávce telmisartanu dojde v průběhu tří hodin postupně k poklesu krevního tlaku. Maximální redukce krevního tlaku se dosáhne obvykle v průběhu 4 až 8 týdnů od zahájení léčby a přetrvává během dlouhodobé terapie.
Antihypertenzní účinek trvá 24 hodin po podání přípravku včetně posledních 4 hodin před podáním následující dávky, jak bylo prokázáno ambulantním monitorováním krevního tlaku. Ve studiích kontrolovaných placebem po dávce 40 a 80 mg telmisartanu je toto potvrzeno poměrem minimálních a maximálních hodnot tlaku krve, který byl konzistentně nad 80 %.
Existuje zjevná závislost mezi podanou dávkou přípravku a časem potřebným k návratu systolického krevního tlaku (STK) na původní hodnoty. Údaje týkající se diastolického krevního tlaku (DTK) nejsou jednotné.
U pacientů s hypertenzí snižuje telmisartan jak systolický, tak i diastolický krevní tlak bez ovlivnění tepové frekvence. Příspěvek diuretického a natriuretického efektu léčivého přípravku k jeho hypotenznímu působení musí být ještě určen. Antihypertenzní účinnost telmisartanu je srovnatelná se zástupci jiných tříd antihypertenziv (což bylo prokázáno v klinických studiích porovnávajících telmisartan s amlodipinem, atenololem, enalaprilem, hydrochlorothiazidem a lisinoprilem).
Po náhlém přerušení léčby telmisartanem se během několika dnů krevní tlak postupně vrací k hodnotám před léčbou bez vzniku „rebound“ fenoménu.
V klinických studiích přímo srovnávajících dvě antihypertenziva byl výskyt suchého kašle významně nižší u pacientů léčených telmisartanem než u pacientů léčených inhibitory enzymu konvertujícího angiotenzin.
Kardiovaskulární prevence
Klinická studie ONTARGET (z anglického ONgoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial) srovnávala účinky telmisartanu, ramiprilu a kombinace telmisartanu a ramiprilu na kardiovaskulární výsledky u 25620 pacientů ve věku 55 let nebo starších s anamnézou ischemické choroby srdeční, cévní mozkové příhody, tranzitorní ischemické ataky, onemocnění periferních tepen nebo diabetes mellitus 2. typu s prokázaným orgánovým postižením (např. retinopatie, hypertrofie levé srdeční komory, makro- nebo mikroalbuminurie), což je populace s rizikem vzniku kardiovaskulárních příhod.
Pacienti byly náhodně zařazeni do jedné ze 3 následujících léčebných skupin: telmisartan 80 mg (n = 8542), ramipril 10 mg (n = 8576) nebo kombinace telmisartan 80 mg plus ramipril 10 mg (n = 8502) a následně sledováni po dobu průměrně 4,5 roku.
Pokud jde o primární kombinovaný cílový parametr účinnosti klinické studie - snížení úmrtí z kardiovaskulárních příčin, nefatálních srdečních infarktů, nefatálních cévních mozkových příhod nebo hospitalizace z důvodu srdečního selhání, telmisartan ukázal podobný účinek jako ramipril. Výskyt primárního cílového parametru u skupiny užívající telmisartan (16,7%) a ramipril (16,5%) byl podobný. Relativní riziko pro telmisartan ve srovnání s ramiprilem bylo 1,01 (97,5% CI 0,93 - 1,10, p (non-inferiorita) = 0,0019, v rozpětí 1,13). Úmrtnost ze všech příčin byla u pacientů léčených telmisartanem 11,6%, u ramiprilu 11,8%.
Ve dvou velkých randomizovaných, kontrolovaných studiích (ONTARGET (ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) a VA NEPHRON-D (The Veterans Affairs Nephropathy in Diabetes)) bylo hodnoceno podávání kombinace inhibitoru ACE s blokátorem receptorů pro angiotenzin II.
Studie ONTARGET byla vedena u pacientů s anamnézou kardiovaskulárního nebo cerebrovaskulárního onemocnění nebo u pacientů s diabetes mellitus 2. typu se známkami poškození cílových orgánů. Studie VA NEPHRON-D byla vedena u pacientů s diabetes mellitus 2. typu a diabetickou nefropatií.
V těchto studiích nebyl prokázán žádný významně příznivý účinek na renální a/nebo kardiovaskulární ukazatele a na mortalitu, ale v porovnání s monoterapií bylo pozorováno zvýšené riziko hyperkalemie, akutního poškození ledvin a/nebo hypotenze. Vzhledem k podobnosti farmakodynamických vlastností jsou tyto výsledky relevantní rovněž pro další inhibitory ACE a blokátory receptorů pro angiotenzin II. Inhibitory ACE ia blokátory receptorů pro angiotensin II. proto nesmí pacienti s diabetickou nefropatií užívat současně.
Studie ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) byla navržena tak, aby zhodnotila přínos přidání aliskirenu k standardní terapii inhibitorem ACE nebo blokátorem receptorů pro angiotenzin II u pacientů s diabetes mellitus 2. typu a chronickým onemocněním ledvin, kardiovaskulárním onemocnění, nebo obojím. Studie byla předčasně ukončena z důvodu zvýšení rizika nežádoucích komplikací. Kardiovaskulární úmrtí a cévní mozková příhoda byly numericky častější ve skupině s aliskirenem než ve skupině s placebem a zároveň nežádoucí účinky a sledované závažné nežádoucí účinky (hyperkalemie, hypotenze a renální dysfunkce) byly častěji hlášeny ve skupině s aliskirenem oproti placebové skupině.
Telmisartan byl také podobně účinný jako ramipril, pokud se týká předem stanoveného sekundárního cílového parametru účinnosti - úmrtí z kardiovaskulárních příčin, nefatální infarkty myokardu a nefatální cévní mozkové příhody [0,99 (97,5% CI 0,90 - 1,08, p (non-inferiorita) = 0,0004)], které byly primárním cílovým parametrem účinnosti referenční studie HOPE (z anglického Heart Outcomes Prevention Evaluation), která zkoumala účinek ramiprilu ve srovnání s placebem.
Klinická studie TRANSCEND randomizovala pacienty netolerující ACE-inhibitory, jinak byla vstupní kriteria stejná jako ve studii ONTARGET. Pacienti užívali telmisartan 80 mg (n=2954) nebo placebo (n=2972), obojí nad rámec standardní péče. Průměrná doba sledování byla 4 roky a 8 měsíců.
Nebyl prokázán statisticky významný rozdíl ve výskytu primárního kombinovaného cílového parametru (úmrtí z kardiovaskulárních příčin, nefatální srdeční infarkty, nefatální cévní mozkové příhody nebo hospitalizace z důvodu srdečního selhání) - 15,7% telmisartan, 17,0% placebo s relativním rizikem 0,92 (95% CI 0,81 - 1,05, p = 0,22). Telmisartan byl účinnější než placebo v předem stanoveném sekundárním kombinovaném cílovém parametru - úmrtí z kardiovaskulárních příčin, nefatální srdeční infarkty a nefatální cévní mozkové příhody [0,87 (95% CI 0,76 - 1,00, p = 0,048)]. Prospěch nebyl prokázán u kardiovaskulární mortality (relativní riziko 1,03, 95% CI 0,85 - 1,24).
U pacientů léčených telmisartanem byl méně často hlášen kašel a angioedém než u pacientů, kterým byl podáván ramipril. Naopak v případě telmisartanu byla častěji hlášena hypotenze.
Kombinace telmisartanu s ramiprilem nepřinesla další prospěch ve srovnání se samotným ramiprilem nebo samotným telmisartanem. Výskyt kardiovaskulární mortality a mortality ze všech příčin byl u této kombinace vyšší. Navíc v této skupině došlo k významně vyššímu výskytu hyperkalémie, renálnímu selhání, hypotenze a synkop. U této skupiny pacientů se proto používání kombinace telmisartanu s ramiprilem nedoporučuje.
Ve studii „Účinná sekundární prevence cévních mozkových příhod“ (PRoFESS) u pacientů ve věku 50 let a starších, kteří prodělali cévní mozkovou příhodu, byl zaznamenán zvýšený výskyt sepse po telmisartanu ve srovnání s placebem, 0,70 % vs. 0,49 % [RR 1,43 (95 % interval spolehlivosti 1,00-2,06)]; výskyt fatálních případů sepse byl zvýšen u pacientů léčených telmisartanem (0,33 %) vs. pacienti léčení placebem (0,16 %) [RR 2,07 (95 % interval spolehlivosti 1,14-3,76)]. Pozorovaná zvýšená míra výskytu sepse spojené s podáváním telmisartanu může být náhodný nález nebo může souviset s dosud neznámým mechanismem.
Pediatrická populace
Bezpečnost a účinnost přípravku Telmisartan Teva u dětí a dospívajících mladších 18 let nebyla stanovena.
Hypotenzní účinky dvou dávek telmisartanu byly hodnoceny u 76 pacientů s hypertenzí, převážně s nadváhou ve věku 6 až 18 let (tělesná hmotnost > 20 kg a < 120 kg, průměrně 74,6 kg) po podání telmisartanu v dávce 1 mg/kg (n = 29 léčených pacientů) nebo 2 mg/kg (n = 31 léčených pacientů) po dobu 4 týdnů léčby. Sekundární hypertenze nebyla do hodnocení zahrnuta. U některých sledovaných pacientů byly užité dávky vyšší než jsou doporučené k léčbě hypertenze u dospělé populace a dosáhly denní dávky srovnatelné se 160 mg, která byla testována u dospělých pacientů. Průměrné změny systolického krevního tlaku oproti výchozímu stavu (primární cíl), upravené s ohledem na věkovou skupinu, byly -14,5 (1,7) mm Hg ve skupině s telmisartanem 2 mg, -9,7 (1,7) mm Hg ve skupině s telmisartanem 1 mg/kg a -6,0 (2,4) mm Hg ve skupině s placebem. Upravené změny diastolického tlaku oproti výchozímu stavu byly -8,4 (1,5) mm Hg, -4,5 (1,6) mm Hg a -3,5 (2,1) mm Hg. Změna byla závislá na dávce. Údaje o bezpečnosti z této studie u pacientů ve věku 6 až 18 let jsou obecně podobné jako u dospělých. Bezpečnost dlouhodobé léčby telmisartanem u dětí a dospívajících nebyla hodnocena.
Zvýšení eosinofilů hlášené v této skupině pacientů nebylo u dospělých zaznamenáno. Jeho klinický význam a závažnost nejsou známy.
Tyto klinické údaje neumožňují stanovit účinnost a bezpečnost telmisartanu u pediatrické populace
s hypertenzí.
5.2 Farmakokinetické vlastnosti
Absorpce
Absorpce telmisartanu je rychlá, i když rozsah jeho vstřebání kolísá. Průměrná hodnota absolutní biologické dostupnosti telmisartanu představuje asi 50 %. Pokud se telmisartan podává spolu s jídlem, pohybuje se redukce plochy pod křivkou závislosti plazmatických koncentrací na čase (AUC-nekonečno) přibližně od 6 % (dávka 40 mg) do 19 % (dávka 160 mg). Od 3 hodin po podání telmisartanu nalačno nebo současně s jídlem se jeho plazmatické koncentrace neliší.
Linearita/nelinearita
Nepředpokládá se, že by menší redukce AUC mohla vést ke snížení terapeutické účinnosti.
Neexistuje lineární závislost mezi dávkami a plazmatickými hladinami. Hodnoty Cmax a v menší míře i AUC rostou nerovnoměrně při dávkách překračujících 40 mg.
Distribuce
Telmisartan se z velké části váže na plazmatické bílkoviny (>99,5 %), především na albumin a alfa-1 kyselý glykoprotein. Distribuční objem v ustáleném stavu (Vdss) dosahuje přibližně 500 l.
Biotransformace
Telmisartan se metabolizuje konjugací na glukuronid výchozí látky. U konjugátu nebyla prokázána žádná farmakologická aktivita.
Eliminace
Telmisartan je charakterizován biexponenciálním poklesem farmakokinetiky s terminálním poločasem eliminace >20 h. Maximální plazmatické koncentrace (Cmax) a v menší míře plocha pod křivkou plazmatických koncentrací v závislosti na čase (AUC) rostou nerovnoměrně s dávkou.
V doporučovaných dávkách nebyla prokázána klinicky významná kumulace telmisartanu. Plazmatické koncentrace byly u žen vyšší než u mužů, avšak bez významného vlivu na účinnost.
Po perorálním (a nitrožilním) podání se telmisartan téměř výhradně vylučuje stolicí, většinou jako nezměněná substance. Kumulativní vylučování močí je menší než 1 % dávky. Celková plazmatická clearance (Cltot) je vysoká (přibližně 1000 ml/min) v porovnání s průtokem krve játry (kolem 1500 ml/min).
Zvláštní skupiny pacientů
Pediatrická populace
Farmakokinetika dvou dávek telmisartanu byla hodnocena jako sekundární cíl u pacientů s hypertenzí (n = 57) ve věku od 6 do 18 let po podání telmisartanu 1 mg/kg nebo 2 mg/kg po dobu 4 týdnů léčby. Farmakokinetické parametry zahrnovaly stanovení ustáleného stavu telmisartanu u dětí a dospívajících a hodnocení rozdílů v závislosti na věku. Přestože studie byla příliš malá pro významné posouzení farmakokinetiky u dětí mladších 12 let, výsledky jsou obecně v souladu s nálezy u dospělých a potvrzují ne-linearitu telmisartanu, zejména pro Cmax.
Pohlaví:
Byly pozorovány rozdíly v plazmatických koncentracích v závislosti na pohlaví, s hodnotami Cmax přibližně třikrát a AUC přibližně dvakrát vyššími u žen než u mužů.
Starší pacienti:
Farmakokinetika telmisartanu se u starších pacientů a pacientů mladších než 65 let neliší.
Porucha funkce ledvin:
U pacientů s mírnou až středně závažnou a závažnou poruchou funkce ledvin byly pozorovány dvojnásobné koncentrace v plazmě, avšak u pacientů s nedostatečností ledvin podstupujících hemodialýzu byly pozorovány nižší plazmatické koncentrace. Telmisartan se u pacientů s ledvinnou nedostatečností do vysoké míry váže na plazmatické bílkoviny a dialýzou jej nelze odstranit. Poločas eliminace se u pacientů s poruchou funkce ledvin nemění.
Porucha funkce jater
Farmakokinetické studie u pacientů s poruchou funkce jater prokázaly zvýšení hodnot absolutní biologické dostupnosti téměř na 100 %. Poločas eliminace se u pacientů s poruchou funkce jater nemění.
5.3 Předklinické údaje vztahující se k bezpečnosti
V předklinických studiích bezpečnosti po podání dávek, které vedly k expozici srovnatelné s klinickým terapeutickým rozmezím, došlo u normotenzních zvířat ke snížení hodnot červeného krevního obrazu (erytrocytů, hemoglobinu, hematokritu), změnám v renální hemodynamice (nárůst dusíku močoviny a kreatininu) a zvýšení hladiny sérového draslíku. U psů byla pozorována dilatace renálních tubulů a jejich atrofie. U potkanů a psů byly rovněž zaznamenány změny žaludeční sliznice (eroze, vředy nebo zánět). Těmto farmakologicky vyvolaným nežádoucím účinkům, známým z předklinického hodnocení jak inhibitorů enzymu konvertujícího angiotenzin, tak antagonistů receptoru angiotenzinu II, bylo možné předejít perorálním podáváním fyziologického roztoku.
U potkanů a psů byly rovněž pozorovány zvýšené hodnoty reninu v plazmě a hypertrofie/hyperplazie ledvinových juxtaglomerulárních buněk. Tyto změny, představující rovněž skupinový účinek inhibitorů enzymu konvertujícího angiotenzin II a antagonistů receptoru angiotenzinu II, zřejmě nemají klinický význam.
Nebyl zjištěn žádný jasný důkaz o teratogenním účinku, avšak podávání telmisartanu v toxických dávkách má vliv na postnatální vývoj jedinců jako je nižší tělesná hmotnost a opožděné otevírání očí.
Testy in vitro neprokázaly mutagenní a významnou klastogenní aktivitu ani nebyl prokázán kancerogenní účinek u potkanů a myší.
6. FARMACEUTICKÉ VLASTNOSTI
6.1 Seznam pomocných látek
Mikrokrystalická celulosa (Avicel PH 102) Sodná sůl karboxymethylškrobu (Typ A) Poloxamer Meglumin
Povidon (PVP K-30)
Sorbitol (E420)
Magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
2 roky
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
Al/Al odlupovací perforované jednodávkové blistry a Al/Al perforované jednodávkové blistry.
Odlupovací perforované blistry obsahující 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet.
Perforované blistry obsahující 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet. Al/Al blistry obsahující 30 tablet.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Teva B.V.
Swensweg 5 2031GA Haarlem Nizozemsko
8. REGISTRAČNÍ ČÍSLO (A)
EU/1/09/610/011
EU/1/09/610/012
EU/1/09/610/013
EU/1/09/610/014
EU/1/09/610/015
EU/1/09/610/016
EU/1/09/610/017
EU/1/09/610/018
EU/1/09/610/019
EU/1/09/610/020
EU/1/09/610/041
EU/1/09/610/042
EU/1/09/610/043
Krabička se 14x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 28x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 30x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 40x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 56x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 60x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 84x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 90x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 98x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 100x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 14x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 28x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 30x1 tabletami v perforovaných jednodávkových Al/Al blistrech
Krabička se 40x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 56x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 60x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 84x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 90x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 98x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 100x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 30 tabletami v Al/Al blistrech
EU/1/09/610/044
EU/1/09/610/045
EU/1/09/610/046
EU/1/09/610/047
EU/1/09/610/048
EU/1/09/610/049
EU/1/09/610/050
EU/1/09/610/061
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 26. ledna 2010 Datum posledního prodloužení registrace: 19/12/2014
10. DATUM REVIZE TEXTU
Podrobné informace o tomto přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
1. NÁZEV PŘÍPRAVKU
Telmisartan Teva 80 mg tablet
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna tableta obsahuje telmisartanum 80 mg
Pomocné látky se známým účinkem:
Jedna tableta obsahuje 85,6 mg sorbitolu (E420)
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Tablety
Bílé až téměř bílé tablety oválného tvaru, na jedné straně tablety je vyraženo číslo “93”. Na druhé straně je vyraženo číslo “7460”.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Hypertenze
Léčba esenciální hypertenze u dospělých pacientů
Kardiovaskulární prevence
Snížení kardiovaskulární morbidity u dospělých:
• s manifestním aterotrombotickým kardiovaskulárním onemocněním (anamnéza ischemické choroby srdeční nebo cévní mozkové příhody nebo onemocnění periferních tepen) nebo
• s diabetes mellitus typu 2 s prokázaným orgánovým postižením
4.2 Dávkování a způsob podání
Dávkování
Léčba esenciální hypertenze
Obvyklá účinná dávka je 40 mg jednou denně. U některých pacientů se příznivý výsledek dostavuje již při denní dávce 20 mg. V případech, kdy se nedosáhne požadovaných hodnot krevního tlaku, lze dávku telmisartanu zvýšit až na 80 mg jednou denně. Alternativně lze telmisartan použít v kombinaci s diuretiky thiazidového typu, jako např. hydrochlorothiazidem, u kterého bylo prokázáno, že aditivně snižuje krevní tlak pomocí telmisartanu.Pokud se uvažuje o zvyšování dávek, je třeba přihlížet k okolnosti, že maximálního antihypertenzního účinku se obvykle dosáhne čtyři až osm týdnů po zahájení léčby (viz bod 5.1).
Kardiovaskulární _ prevence
Doporučená dávka je 80 mg jednou denně. Nejsou k dispozici údaje o tom, zda dávky telmisartanu nižší než 80 mg jsou účinné při snižování kardiovaskulární morbidity. Při zahájení léčby telmisartanem ke snížení kardiovaskulární morbidity se doporučuje pečlivé sledování krevního tlaku.
V některých případech může být nezbytné upravit léky snižující krevní tlak.
Pacienti s poruchou _ funkce ledvin
U pacientů se závažnou poruchou funkce ledvin nebo podstupujících hemodialýzu jsou k dispozici jen omezené zkušenosti. U těchto pacientů je doporučena nižší úvodní dávka 20 mg (viz bod 4.4).
U pacientů s mírnou až středně závažnou poruchou funkce ledvin není třeba upravovat dávkování.
Pacienti s poruchou funkce jater
Telmisartan Teva je kontraindikován u pacientů se závažnou poruchou funkce jater (viz bod 4.3).
U pacientů s mírnou až středně závažnou poruchou funkce jater by dávka neměla přesáhnout 40 mg jednou denně (viz bod 4.4).
Starší pacienti
Úprava dávkování u starších pacientů není nutná.
Pediatrická populace
Bezpečnost a účinnost přípravku Telmisartan Teva u dětí a dospívajících mladších 18 let nebyla
stanovena.
Aktuálně dostupné údaje jsou popsány v bodech 5.1 a 5.2, ale doporučené dávkování stanovit nelze. Způsob podání
Telmisartan tablety se užívají jednou denně perorálně a měly by se podávat s tekutinami, s jídlem nebo bez jídla.
4.3 Kontraindikace
• Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku uvedenou v bodě 6.1
• Druhý a třetí trimestr těhotenství (viz bod 4.4 a 6.4)
• Obstrukce žlučovodů
• Závažné poškození funkce jater
Současné užívání přípravku Telmisartan Teva s přípravky obsahujícími aliskiren je kontraindikováno u pacientů s diabetes mellitus nebo poruchou funkce ledvin (GFR <60 ml/min/1.73 m2) (viz body 4.5 a 5.1).
4.4 Zvláštní upozornění a opatření pro použití
Léčba pomocí antagonistů receptoru angiotensinu II nesmí být během těhotenství zahájena. Pokud není pokračování v léčbě antagonisty receptoru angiotensinu II považováno za nezbytné, pacientky plánující těhotenství musí být převedeny na jinou léčbu hypertenze, a to takovou, která má ověřený bezpečnostní profil, pokud jde o podávání v těhotenství. Pokud je zjištěno těhotenství, léčba pomocí antagonistů receptoru angiotensinu II musí být ihned ukončena, a pokud je to vhodné, může být zahájena alternativní léčba (viz body 4.3 a 4.6).
Poškození funkce jater
Vzhledem k tomu, že se Telmisartan Teva vylučuje především žlučí, nesmí být podáván pacientům s cholestázou, obstrukcí žlučovodů nebo závažným poškozením jater (viz bod 4.3). U těchto pacientů se předpokládá snížení jaterní clearence telmisartanu. Pacientům s mírným až středně závažným poškozením jater může být Telmisartan Teva podán pouze se zvýšenou opatrností.
Renovaskulámí hypertenze
Pacientům s oboustrannou stenózou renální arterie nebo se stenózou arterie zásobující jedinou funkční ledvinu, kteří jsou léčeni přípravky ovlivňujícími renin-angiotenzin-aldosteronový systém, hrozí zvýšené riziko těžké hypotenze a renální nedostatečnost.
Renální poškození a transplantace ledvin
Pokud je přípravek Telmisartan Teva podáván pacientům s poruchou jater, je doporučena pravidelná kontrola sérových hladin draslíku a kreatininu v krvi. Nejsou žádné zkušenosti s podáváním přípravku Telmisartanu Teva Pharma pacientům po transplantaci ledvin.
Intravaskulární hypovolaemie
U pacientů s poklesem objemu nebo koncentrace sodíku v důsledku intenzivní diuretické terapie, omezování soli v dietě, průjmu nebo zvracení se zejména po první dávce přípravku Telmisartan Teva může objevit symptomatická hypotenze. Takové stavy by se měly ještě před podáním přípravku Telmisartan Teva korigovat, stejně jako snížení intravaskulárního objemu nebo deplece sodíku.
Duální blokáda systému renin-angiotenzin-aldosteron (RAAS)
Bylo prokázáno, že současné užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu zvyšuje riziko hypotenze, hyperkalemie a snížení funkce ledvin (včetně akutního selhání ledvin). Duální blokáda RAAS pomocí kombinovaného užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu se proto nedoporučuje (viz body 4.5 a 5.1).
Pokud je duální blokáda považována za naprosto nezbytnou, má k ní docházet pouze pod dohledem specializovaného lékaře a za častého pečlivého sledování funkce ledvin, elektrolytů a krevního tlaku. Inhibitory ACE a blokátory receptorů pro angiotenzin II nemají být používány současně u pacientů s diabetickou nefropatií.
Ostatní stavy provázené stimulací renin-angiotenzin-aldosteronového systému U pacientů, jejichž cévní tonus a renální funkce závisejí převážně na aktivitě renin-angiotenzin-aldosteronového systému (např. u pacientů se závažným městnavým srdečním selháním nebo s průvodním onemocněním ledvin, včetně stenózy renální arterie), byla léčba dalšími přípravky, které ovlivňují tento systém podobně jako telmisartan, spojeny s akutní hypotenzí, hyperazotemií, oligurií nebo vzácněji i s akutním selháním ledvin (viz bod 4.8).
Primární aldosteronismus
Pacienti s primárním aldosteronismem obvykle nereagují na antihypertenziva působící mechanismem inhibice renin-angiotenzin-aldosteronového systému. V těchto případech se léčba telmisartanem nedoporučuje.
Stenóza aortální a mitrální chlopně, obstrukční hypertrofická kardiomyopatie
Stejně jako u ostatních vazodilatancií je třeba věnovat zvlášť zvýšenou pozornost pacientům trpícím
stenózami aortální a mitrální chlopně nebo obstrukční hypertrofickou kardiomyopatií.
Diabetičtí pacienti léčení inzulínem nebo antidiabetiky
U těchto pacientů se může při léčbě telmisartanem objevit hypoglykémie. Proto je u nich vhodné zvážit sledování hladiny glukózy v krvi; a pokud je indikováno, upravit dávky inzulinu nebo antidiabetik.
Hyperkalémie
Podávání léčivých přípravků, které ovlivňují renin-angiotenzin-aldosteronový systém, může vést k hyperkalémii.
U starších pacientů, u pacientů s poškozením funkce ledvin, u diabetiků, u pacientů současně léčených jinými přípravky, které mohou zvyšovat hladinu draslíku, a/nebo u pacientů s určitými interkurentními příhodami, může být hyperkalémie fatální.
Před zvažováním současného podávání léčivých přípravků, které ovlivňují renin-angiotenzin-aldosteronový systém, je nutno zhodnotit poměr přínosu a rizika.
Hlavní rizikové faktory hyperkalémie, které je třeba zvažovat:
- Diabetes mellitus, poškozená funkce ledvin, věk (>70 let)
- Kombinace s jedním nebo více léčivými přípravky, které ovlivňují renin-angiotenzin-aldosteronový systém, a/nebo s přípravky doplňujícími draslík. Léčivé přípravky nebo terapeutické třídy léčivých přípravků, které mohou vyvolat hyperkalémii jsou náhražky soli obsahující draslík, draslík šetřící diuretika, ACE inhibitory, antagonisté receptoru angiotenzinu II, nesteroidní protizánětlivé léčivé přípravky (NSAIDs, včetně selektivních COX-2 inhibitorů), heparin, imunosupresiva (cyklosporin nebo takrolismus) a trimethoprim.
- Interkurentní příhody, zejména dehydratace, akutní srdeční dekompenzace, metabolická acidóza, zhoršení renálních funkcí, náhlé zhoršení podmínek pro funkci ledvin (např. infekční onemocnění), rozpad buněk (např. při akutní ischemii končetin, rabdomyolýze, rozsáhlém traumatu).
U rizikových pacientů se doporučuje sledovat sérové hladiny draslíku (viz bod 4.5).
Sorbitol
Tento léčivý přípravek obsahuje sorbitol (E420). Pacienti se vzácnou vrozenou intolerancí fruktosy nesmí Telmisartan Teva užívat.
Etnické odlišnosti
Stejně jako inhibitory enzymu konvertujícího angiotenzin, také telmisartan a další antagonisté receptoru angiotenzinu II zjevně navozují u černošské populace méně výrazné snížení krevního tlaku než u jiných lidských ras, pravděpodobně v souvislosti s vyšší prevalencí stavů s nízkou hladinou reninu v populaci hypertoniků černé pleti.
Další upozornění
Analogicky jako u kterýchkoli jiných antihypertenziv může dojít při nadměrném snížení krevního tlaku u pacientů s ischemickou kardiopatií nebo s ischemickou chorobou srdeční k infarktu myokardu nebo k cévní mozkové příhodě.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Digoxin
Při současném podání telmisartanu s digoxinem bylo pozorováno zvýšení střední hodnoty vrcholové plasmatické koncentrace digoxinu (49%) a minimální koncentrace (20%). Při zahájení, úpravě a ukončení léčby telmisartanem byla monitorována hladina digoxinu proto, aby byla zachována jeho hladina v terapeutickém rozmezí.
Tak jako ostatní léčiva působící na renin-angiotenzin-aldosteronový systém, telmisartan může způsobit hyperkalémii (viz bod 4.4). Riziko se může zvýšit v případě kombinované léčby s dalšími léčivými přípravky, které mohou také vyvolat hyperkalemii (náhražky soli obsahující draslík, draslík šetřící diuretika, ACE inhibitory, antagonisté receptoru angiotenzinu II, nesteroidní protizánětlivé léčivé přípravky (NSAIDs, včetně selektivních COX-2 inhibitorů), heparin, imunosupresiva (cyklosporin nebo takrolismus) a trimethoprim).
Výskyt hyperkalémie závisí na přidružených rizikových faktorech. Riziko se zvyšuje v případě výše uvedených léčebných kombinací. Riziko je zvláště vysoké při kombinaci s kalium šetřícími diuretiky a při kombinaci s náhražkami soli obsahující draslík. Kombinace např. s ACE inhibitory nebo s NSAIDs představují menší riziko za předpokladu, že jsou přesně dodržována opatření při podávání.
Současné podávání se nedoporučuje
Draslík šetřící diuretika a přípravky obsahující draslík
Antagonisté receptoru angiotenzinu II jako telmisartan, zmenšují ztrátu draslíku, navozenou diuretiky. Draslík šetřící diuretika, například spironolakton, eplerenon, triamteren nebo amilorid, přípravky obsahující draslík nebo náhražky soli obsahující draslík, mohou vést k významnému zvýšení hladiny draslíku v séru. Pokud je indikováno současné podávání z důvodu prokázané hypokalémie, je nutno je podávat opatrně a za častých kontrol hladin draslíku v séru.
Lithium
Při současném podávání lithia spolu s inhibitory angiotenzin konvertujícího enzymu byl hlášen reverzibilní nárůst koncentrací lithia v séru a jeho toxicita, a také při současném podávání lithia a antagonistů receptoru angiotenzinu II včetně telmisartanu. Pokud se ukáže kombinované podávání jako nezbytné, doporučuje se pečlivě monitorovat sérové hladiny lithia.
Současné podávání vyžadující opatrnost
Nesteroidní protizánětlivé léčivé přípravky (NSAIDs)
NSAIDs (např. kyselina acetylosalicylová v protizánětlivých dávkách, inhibitory COX-2 a neselektivní NSAIDs) mohou snižovat antihypertenzivní účinek antagonistů receptoru angiotensinu II. U některých pacientů s oslabenou funkcí ledvin (např. u dehydratovaných pacientů nebo starších pacientů s poruchou funkce ledvin) může mít současné podávání antagonistů receptoru angiotensinu II a přípravků, které blokují cyklooxygenázu, za následek další zhoršení funkce ledvin, včetně možného vzniku akutního selhání ledvin, které je obvykle reverzibilní. Z tohoto důvodu je nutno podávat takovou kombinaci velmi opatrně, zejména u starších pacientů. Pacienti musí být dostatečně hydratováni a je třeba zvážit kontroly funkce ledvin po zahájení, a také v pravidelných intervalech během této kombinované terapie.
V jedné studii vedlo současné podávání telmisartanu a ramiprilu ke 2,5 násobnému zvýšení AUC0-24 a Cmax ramiprilu a ramiprilátu. Klinický význam tohoto zjištění není znám.
Diuretika (thiazidová nebo kličková diuretika)
Předchozí léčba vysokými dávkami diuretik jako je furosemid (kličkové diuretikum) a hydrochlorothiazid (thiazidové diuretikum) může vést k volumdepleci a k riziku vzniku hypotenze po zahájení léčby telmisartanem.
Současné podávání, které je nutno zvažovat
Jiná antihypertenziva
Účinek telmisartanu na snížení krevního tlaku může být zvýrazněn při současném podávání jiných antihypertenziv.
Data z klinických studií ukázala, že duální blokáda systému renin-angiotenzin-aldosteron (RAAS) pomocí kombinovaného užívání inhibitorů ACE, blokátorů receptorů pro angiotenzin II nebo aliskirenu je spojena s vyšší frekvencí nežádoucích účinků, jako je hypotenze, hyperkalemie a snížená funkce ledvin (včetně akutního renálního selhání) ve srovnání s použitím jedné látky ovlivňující RAAS (viz body 4.3, 4.4 a 5.1).
Na základě farmakologických vlastností následně uvedených léků lze očekávat, že tyto léčivé přípravky mohou zvýraznit hypotenzní účinek všech antihypertenziv, včetně telmisartanu: baklofem, amifostin. Vedle toho může být orthostatická hypotenze potencována alkoholem, barbituráty, narkotiky nebo antidepresivy.
Kortikosteroidy (systémové podání)
Snížení antihypertenzního účinku.
4.6 Fertilita, těhotenství a kojení
Užívání antagonistů receptoru angiotensinu II se nedoporučuje během prvního trimestru těhotenství (viz bod 4.4). Užívání antagonistů receptoru angiotensinu II je kontraindikováno během druhého a třetího trimestru těhotenství (viz body 4.3 a 4.4).
Adekvátní údaje o podávání přípravku Telmisartan Teva těhotným ženám nejsou k dispozici. Studie na zvířatech poukázaly na reprodukční toxicitu (viz bod 5.3).
Epidemiologické důkazy týkající se rizika teratogenicity při podávání ACE inhibitorů během prvního trimestru těhotenství nebyly nezvratné; malý nárůst rizika však nelze vyloučit. I když neexistují žádné kontrolované epidemiologické údaje pokud jde o riziko při podávání antagonistů receptoru angiotenzinu II, pro tuto třídu léčiv může existovat riziko podobné. Pokud pokračování v léčbě antagonisty receptoru angiotenzinu II není považováno za nezbytné, pacientky plánující těhotenství musí být převedeny na jinou léčbu vysokého krevního tlaku, a to takovou, která má ověřený bezpečnostní profil, pokud jde o podávání v těhotenství. Jestliže je těhotenství prokázáno, léčba pomocí antagonistů receptoru angiotenzinu II musí být ihned ukončena, a pokud je to vhodné, je nutné zahájit jiný způsob léčby.
Je známo, že expozice vůči antagonistům receptoru angiotenzinu II během druhého a třetího trimestru těhotenství vede u lidí k fetotoxicitě (pokles funkce ledvin, oligohydramnion, zpoždění osifikace lebky) a k novorozenecké toxicitě (selhání ledvin, hypotenze, hyperkalémie). (Viz bod 5.3).
Pokud by došlo k expozici vůči antagonistům receptoru angiotenzinu II od druhého trimestru těhotenství, doporučuje se sonografická kontrola funkce ledvin a lebky.
Děti, jejichž matky užívaly antagonisty receptoru angiotenzinu II, musí být pečlivě sledovány, pokud jde o hypotenzi (viz body 4.3 a 4.4).
Kojení
Protože nejsou k dispozici žádné údaje ohledně užívání přípravku Telmisartan Teva Pharma během kojení, Telmisartan Teva se nedoporučuje, je vhodnější zvolit jinou léčbu s lepším bezpečnostním profilem během kojení, obzvláště během kojení novorozence nebo předčasně narozeného dítěte.
Fertilita:
V předklinických studiích nebyly u telmisartanu pozorovány žádné účinky na samčí nebo samičí plodnost.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Při řízení motorových vozidel nebo obsluze strojních zařízení je však třeba mít na paměti, že léčba antihypertenzivy, jako je Telmisartan Teva, může v některých případech způsobovat závratě nebo ospalost.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Vzácně ((>1/10,000 až <1/1,000) mohou být pozorovány závažné nežádoucí účinky včetně anafylaktické reakce a angioedému a akutní renální selhání.
V kontrolovaných studiích u pacientů s hypertenzí byla celková frekvence výskytu nežádoucích účinků hlášených pro telmisartan obvykle srovnatelná s placebem (41,4% - 43,9 %). Výskyt nežádoucích účinků není závislý na dávce ani na pohlaví, věku nebo rase pacientů. Bezpečnostní profil telmisartanu podávaného pacientům ke snížení kardiovaskulární morbidity byl shodný s bezpečnostním profilem zjištěným u pacientů s hypertenzí.
Následně uvedené nežádoucí účinky byly shromážděny ze všech kontrolovaných klinických studií u pacientů léčených pro hypertenzi a z postmarketingových sledování. Dále se vycházelo z hlášení závažných nežádoucích příhod a nežádoucích příhod vedoucích k přerušení léčby v rámci tří dlouhodobých klinických studií s 21642 pacienty, kterým byl podáván telmisartan ke snížení kardiovaskulární morbidity až po dobu šesti let.
Souhrn nežádoucích účinků v tabulce
Nežádoucí účinky jsou podle frekvence výskytu rozděleny za použití následujícího pravidla: velmi časté (>1/10); časté (>1/100 až <1/10); méně časté (>1/1000 až <1/100; vzácné (>1/10000 až <1/1000); velmi vzácné (<1/10000).
V každé skupině četnosti jsou nežádoucí účinky seřazeny podle klesající závažnosti.
Infekce a infestace
Méně časté: Infekce močových cest včetně zánětů močového měchýře, infekce
horních cest dýchacích včetně faryngitidy a sinusitidy Vzácné: Sepse včetně případů vedoucích k úmrtí1
Poruchy krve a lymfatického systému Méně časté: Anémie
Vzácné: Eosinofilie, trombocytopenie
Poruchy imunitního systému
Vzácné: Přecitlivělost, anafylaktická reakce
Poruchy metabolismu a výživy
Méně časté: Hyperkalemie
Vzácné: Hypoglykémie (u diabetických pacientů)
Psychiatrické poruchy
Méně časté: Insomnie, deprese
Vzácné: Úzkost
Poruchy nervového systému
Méně časté: Synkopa
Vzácné: Somnolence
Poruchy oka Vzácné:
Poruchy vidění
Poruchy ucha a labyrintu
Méně časté: Vertigo
Bradykardie
Srdeční poruchy Méně časté: Vzácné:
Cévní poruchy Méně časté:
Hypotenze2, ortostatická hypotenze
Respirační, hrudní a mediastinální poruchy
Méně časté: Dyspnoe, kašel
Velmi vzácné: Intersticiální plicní nemoc4
Gastrointestinální poruchy
Méně časté: Bolesti břicha, průjem, dyspepsie, plynatost, zvracení
Vzácné: Sucho v ústech, žaludeční nevolnost, dysgeuzie
Poruchy jater a žlučových cest
V zácné: Abnormální j aterní funkce/j aterní poruchy3
Poruchy kůže a podkožní tkáně
Méně časté: Zvýšené pocení, pruritus, kožní vyrážka
Vzácné: Erytém, angioedém (včetně případů vedoucích k úmrtí), urticaria,
polékový exantém, toxoalergický exantém
Poruchy svalové a kosterní soustavy a pojivové tkáně
Méně časté: Bolesti zad (např. ischias), svalové spasmy, myalgie
Vzácné: Artralgie, bolesti končetin, bolesti šlach (příznaky podobné zánětu
šlach)
Poruchy ledvin a močových cest
Méně časté: Poškození ledvin včetně akutního renálního selhání
Celkové poruchy a reakce v místě aplikace
Méně časté: Bolesti na hrudi, astenie (slabost)
Vzácné: Onemocnění připomínající chřipku
Vyšetření
Méně časté: Zvýšená hladina kreatininu v krvi
Vzácné: Pokles hemoglobinu, zvýšení hladiny kyseliny močové v krvi, zvýšení
jaterních enzymů, zvýšení kreatinfosfokinázy
1 2 3 4: pro další popis, viz část „Popis vybraných nežádoucích účinků “
Popis vybraných nežádoucích účinků
Sepse
Ve studii PRoFESS byl pozorován zvýšený výskyt sepse po telmisartanu ve srovnání s placebem. Příhoda může být náhodný nález nebo může souviset s dosud neznámým mechanismem (viz také bod 5.1).
Tento nežádoucí účinek byl hlášen jako častý u pacientů s upraveným krevním tlakem, kterým byl podáván telmisartan ke snížení kardiovaskulární morbidity nad rámec standardní péče.
Abnormální jaterní funkce/porucha jater
Většina případů abnormální jaterní funkce/poruchy jater z post-marketingových zkušeností se vyskytla u japonských pacientů. U japonských pacientů se tyto nežádoucí účinky vyskytují s větší pravděpodobností.
Intersticiální plicní nemoc
Na základě zkušeností po uvedení přípravku na trh byly hlášeny případy intersticiální plicní nemoci v časové souvislosti s podáním telmisartanu. Příčinná souvislost ale nebyla stanovena.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
K dispozici jsou pouze omezené informace týkající se předávkování u člověka.
Příznaky
Nejnápadnějšími projevy předávkování telmisartanem jsou hypotenze a tachykardie; vyskytla se bradykardie, závrať, zvýšení kreatininu v séru a akutní selhání ledvin.
Terapie
Telmisartan nelze odstranit hemodialýzou. Pacient by měl být pečlivě monitorován, léčba by měla být podpůrná a symptomatická. Léčba závisí na časovém úseku, který uplynul od požití a na závažnosti příznaků. Navrhovaná opatření zahrnují navození zvracení a/nebo výplach žaludku. Vhodnou léčbou předávkování může být použití aktivního uhlí. Hladiny elektrolytů a kreatininu v séru je nutno často monitorovat. Pokud dojde k hypotenzi, je nutno pacienta uložit do polohy vleže na zádech a urychleně podat soli a doplnit objem tekutin.
5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antagonisté angiotensinu II, samotní; ATC kód: C09CA07 Mechanismus účinku
Telmisartan je specifický antagonista receptoru angiotenzinu II (typ AT1) účinný po perorálním podání. S vysokou afinitou vytěsňuje angiotenzin II z jeho vazebného místa na subtypu receptoru AT1, který odpovídá za známé působení angiotenzinu II. Telmisartan nemá na receptoru AT1 žádnou parciální agonistickou aktivitu a váže se selektivně na tento receptor. Vazba má dlouhodobý charakter. Telmisartan nevykazuje afinitu k ostatním receptorům, včetně AT2 a ostatních méně charakterizovaných AT. Funkční význam těchto receptorů není znám, stejně jako efekt jejich možné zvýšené stimulace angiotenzinem II, jehož hladiny se podáváním telmisartanu zvyšují. Plazmatické hladiny aldosteronu se podáváním telmisartanu snižují. Telmisartan neinhibuje u lidí plazmatický renin ani neblokuje iontové kanály. Telmisartan neinhibuje enzym konvertující angiotenzin (kinázu II), což je enzym, který rovněž rozkládá bradykinin. Proto se nepředpokládá, že by telmisartan potencoval nežádoucí účinky zprostředkované bradykininem.
Dávka telmisartanu 80 mg u člověka téměř zcela inhibuje zvýšení krevního tlaku vyvolané angiotenzinem II. Inhibiční účinek přetrvává déle než 24 hodin a je měřitelný po dobu až 48 hodin.
Klinická účinnost a bezpečnost
Léčba esenciální hypertenze
Po první dávce telmisartanu dojde v průběhu tří hodin postupně k poklesu krevního tlaku. Maximální redukce krevního tlaku se dosáhne obvykle v průběhu 4 až 8 týdnů od zahájení léčby a přetrvává během dlouhodobé terapie.
Antihypertenzní účinek trvá 24 hodin po podání přípravku včetně posledních 4 hodin před podáním následující dávky, jak bylo prokázáno ambulantním monitorováním krevního tlaku. Ve studiích kontrolovaných placebem po dávce 40 a 80 mg telmisartanu je toto potvrzeno poměrem minimálních a maximálních hodnot tlaku krve, který byl konzistentně nad 80 %.
Existuje zjevná závislost mezi podanou dávkou přípravku a časem potřebným k návratu systolického krevního tlaku (STK) na původní hodnoty. Údaje týkající se diastolického krevního tlaku (DTK) nejsou jednotné.
U pacientů s hypertenzí snižuje telmisartan jak systolický, tak i diastolický krevní tlak bez ovlivnění tepové frekvence. Příspěvek diuretického a natriuretického efektu léčivého přípravku k jeho hypotenznímu působení musí být ještě určen. Antihypertenzní účinnost telmisartanu je srovnatelná se zástupci jiných tříd antihypertenziv (což bylo prokázáno v klinických studiích porovnávajících telmisartan s amlodipinem, atenololem, enalaprilem, hydrochlorothiazidem a lisinoprilem).
Po náhlém přerušení léčby telmisartanem se během několika dnů krevní tlak postupně vrací k hodnotám před léčbou bez vzniku „rebound“ fenoménu.
V klinických studiích přímo srovnávajících dvě antihypertenziva byl výskyt suchého kašle významně nižší u pacientů léčených telmisartanem než u pacientů léčených inhibitory enzymu konvertujícího angiotenzin.
Kardiovaskulární prevence
Klinická studie ONTARGET (z anglického ONgoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial) srovnávala účinky telmisartanu, ramiprilu a kombinace telmisartanu a ramiprilu na kardiovaskulární výsledky u 25620 pacientů ve věku 55 let nebo starších s anamnézou ischemické choroby srdeční, cévní mozkové příhody, tranzitorní ischemické ataky, onemocnění periferních tepen nebo diabetes mellitus 2. typu s prokázaným orgánovým postižením (např. retinopatie, hypertrofie levé srdeční komory, makro- nebo mikroalbuminurie), což je populace s rizikem vzniku kardiovaskulárních příhod.
Pacienti byly náhodně zařazeni do jedné ze 3 následujících léčebných skupin: telmisartan 80 mg (n = 8542), ramipril 10 mg (n = 8576) nebo kombinace telmisartan 80 mg plus ramipril 10 mg (n = 8502) a následně sledováni po dobu průměrně 4,5 roku.
Pokud jde o primární kombinovaný cílový parametr účinnosti klinické studie - snížení úmrtí z kardiovaskulárních příčin, nefatálních srdečních infarktů, nefatálních cévních mozkových příhod nebo hospitalizace z důvodu srdečního selhání, telmisartan ukázal podobný účinek jako ramipril. Výskyt primárního cílového parametru u skupiny užívající telmisartan (16,7%) a ramipril (16,5%) byl podobný. Relativní riziko pro telmisartan ve srovnání s ramiprilem bylo 1,01 (97,5% CI 0,93 - 1,10, p (non-inferiorita) = 0,0019, v rozpětí 1,13). Úmrtnost ze všech příčin byla u pacientů léčených telmisartanem 11,6%, u ramiprilu 11,8%.
Ve dvou velkých randomizovaných, kontrolovaných studiích (ONTARGET (ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) a VA NEPHRON-D (The Veterans Affairs Nephropathy in Diabetes)) bylo hodnoceno podávání kombinace inhibitoru ACE s blokátorem receptorů pro angiotenzin II.
Studie ONTARGET byla vedena u pacientů s anamnézou kardiovaskulárního nebo cerebrovaskulárního onemocnění nebo u pacientů s diabetes mellitus 2. typu se známkami poškození cílových orgánů. Studie VA NEPHRON-D byla vedena u pacientů s diabetes mellitus 2. typu a diabetickou nefropatií.
V těchto studiích nebyl prokázán žádný významně příznivý účinek na renální a/nebo kardiovaskulární ukazatele a na mortalitu, ale v porovnání s monoterapií bylo pozorováno zvýšené riziko hyperkalemie, akutního poškození ledvin a/nebo hypotenze. Vzhledem k podobnosti farmakodynamických vlastností jsou tyto výsledky relevantní rovněž pro další inhibitory ACE a blokátory receptorů pro angiotenzin II. Inhibitory ACE ia blokátory receptorů pro angiotensin II. proto nesmí pacienti s diabetickou nefropatií užívat současně.
Studie ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) byla navržena tak, aby zhodnotila přínos přidání aliskirenu k standardní terapii inhibitorem ACE nebo blokátorem receptorů pro angiotenzin II u pacientů s diabetes mellitus 2. typu a chronickým onemocněním ledvin, kardiovaskulárním onemocnění, nebo obojím. Studie byla předčasně ukončena z důvodu zvýšení rizika nežádoucích komplikací. Kardiovaskulární úmrtí a cévní mozková příhoda byly numericky častější ve skupině s aliskirenem než ve skupině s placebem a zároveň nežádoucí účinky a sledované závažné nežádoucí účinky (hyperkalemie, hypotenze a renální dysfunkce) byly častěji hlášeny ve skupině s aliskirenem oproti placebové skupině.
Telmisartan byl také podobně účinný jako ramipril, pokud se týká předem stanoveného sekundárního cílového parametru účinnosti - úmrtí z kardiovaskulárních příčin, nefatální infarkty myokardu a nefatální cévní mozkové příhody [0,99 (97,5% CI 0,90 - 1,08, p (non-inferiorita) = 0,0004)], které byly primárním cílovým parametrem účinnosti referenční studie HOPE (z anglického Heart Outcomes Prevention Evaluation), která zkoumala účinek ramiprilu ve srovnání s placebem.
Klinická studie TRANSCEND randomizovala pacienty netolerující ACE-inhibitory, jinak byla vstupní kriteria stejná jako ve studii ONTARGET. Pacienti užívali telmisartan 80 mg (n=2954) nebo placebo (n=2972), obojí nad rámec standardní péče. Průměrná doba sledování byla 4 roky a 8 měsíců.
Nebyl prokázán statisticky významný rozdíl ve výskytu primárního kombinovaného cílového parametru (úmrtí z kardiovaskulárních příčin, nefatální srdeční infarkty, nefatální cévní mozkové příhody nebo hospitalizace z důvodu srdečního selhání) - 15,7% telmisartan, 17,0% placebo s relativním rizikem 0,92 (95% CI 0,81 - 1,05, p = 0,22). Telmisartan byl účinnější než placebo v předem stanoveném sekundárním kombinovaném cílovém parametru - úmrtí z kardiovaskulárních příčin, nefatální srdeční infarkty a nefatální cévní mozkové příhody [0,87 (95% CI 0,76 - 1,00, p = 0,048)]. Prospěch nebyl prokázán u kardiovaskulární mortality (relativní riziko 1,03, 95% CI 0,85 - 1,24).
U pacientů léčených telmisartanem byl méně často hlášen kašel a angioedém než u pacientů, kterým byl podáván ramipril. Naopak v případě telmisartanu byla častěji hlášena hypotenze.
Kombinace telmisartanu s ramiprilem nepřinesla další prospěch ve srovnání se samotným ramiprilem nebo samotným telmisartanem. Výskyt kardiovaskulární mortality a mortality ze všech příčin byl u této kombinace vyšší. Navíc v této skupině došlo k významně vyššímu výskytu hyperkalémie, renálnímu selhání, hypotenze a synkop. U této skupiny pacientů se proto používání kombinace telmisartanu s ramiprilem nedoporučuje.
Ve studii „Účinná sekundární prevence cévních mozkových příhod“ (PRoFESS) u pacientů ve věku 50 let a starších, kteří prodělali cévní mozkovou příhodu, byl zaznamenán zvýšený výskyt sepse po telmisartanu ve srovnání s placebem, 0,70 % vs. 0,49 % [RR 1,43 (95 % interval spolehlivosti 1,00 - 2,06)]; výskyt fatálních případů sepse byl zvýšen u pacientů léčených telmisartanem (0,33 %) vs. pacienti léčení placebem (0,16 %) [RR 2,07 (95 % interval spolehlivosti 1,14 - 3,76)]. Pozorovaná zvýšená míra výskytu sepse spojené s podáváním telmisartanu může být náhodný nález nebo může souviset s dosud neznámým mechanismem.
Pediatrická populace
Bezpečnost a účinnost přípravku Telmisartan Teva u dětí a dospívajících mladších 18 let nebyla stanovena.
Hypotenzní účinky dvou dávek telmisartanu byly hodnoceny u 76 pacientů s hypertenzí, převážně s nadváhou ve věku 6 až 18 let (tělesná hmotnost > 20 kg a < 120 kg, průměrně 74,6 kg) po podání telmisartanu v dávce 1 mg/kg (n = 29 léčených pacientů) nebo 2 mg/kg (n = 31 léčených pacientů) po dobu 4 týdnů léčby. Sekundární hypertenze nebyla do hodnocení zahrnuta. U některých sledovaných pacientů byly užité dávky vyšší než jsou doporučené k léčbě hypertenze u dospělé populace a dosáhly denní dávky srovnatelné se 160 mg, která byla testována u dospělých pacientů. Průměrné změny systolického krevního tlaku oproti výchozímu stavu (primární cíl), upravené s ohledem na věkovou skupinu, byly -14,5 (1,7) mm Hg ve skupině s telmisartanem 2 mg, -9,7 (1,7) mm Hg ve skupině s telmisartanem 1 mg/kg a -6,0 (2,4) mm Hg ve skupině s placebem. Upravené změny diastolického tlaku oproti výchozímu stavu byly -8,4 (1,5) mm Hg, -4,5 (1,6) mm Hg a -3,5 (2,1) mm Hg. Změna byla závislá na dávce. Údaje o bezpečnosti z této studie u pacientů ve věku 6 až 18 let jsou obecně podobné jako u dospělých. Bezpečnost dlouhodobé léčby telmisartanem u dětí a dospívajících nebyla hodnocena.
Zvýšení eosinofilů hlášené v této skupině pacientů nebylo u dospělých zaznamenáno. Jeho klinický význam a závažnost nejsou známy.
Tyto klinické údaje neumožňují stanovit účinnost a bezpečnost telmisartanu u pediatrické populace s hypertenzí.
5.2 Farmakokinetické vlastnosti
Absorpce
Absorpce telmisartanu je rychlá, i když rozsah jeho vstřebání kolísá. Průměrná hodnota absolutní biologické dostupnosti telmisartanu představuje asi 50 %. Pokud se telmisartan podává spolu s jídlem, pohybuje se redukce plochy pod křivkou závislosti plazmatických koncentrací na čase (AUC-nekonečno) přibližně od 6 % (dávka 40 mg) do 19 % (dávka 160 mg). Od 3 hodin po podání telmisartanu nalačno nebo současně s jídlem se jeho plazmatické koncentrace neliší.
Linearita/nelinearita
Nepředpokládá se, že by menší redukce AUC mohla vést ke snížení terapeutické účinnosti.
Neexistuje lineární závislost mezi dávkami a plazmatickými hladinami. Hodnoty Cmax a v menší míře i AUC rostou nerovnoměrně při dávkách překračujících 40 mg.
Distribuce
Telmisartan se z velké části váže na plazmatické bílkoviny (>99,5 %), především na albumin a alfa-1 kyselý glykoprotein. Distribuční objem v ustáleném stavu (Vdss) dosahuje přibližně 500 l.
Biotransformace
Telmisartan se metabolizuje konjugací na glukuronid výchozí látky. U konjugátu nebyla prokázána žádná farmakologická aktivita.
Eliminace
Telmisartan je charakterizován biexponenciálním poklesem farmakokinetiky s terminálním poločasem eliminace >20 h. Maximální plazmatické koncentrace (Cmax) a v menší míře plocha pod křivkou plazmatických koncentrací v závislosti na čase (AUC) rostou nerovnoměrně s dávkou.
V doporučovaných dávkách nebyla prokázána klinicky významná kumulace telmisartanu. Plazmatické koncentrace byly u žen vyšší než u mužů, avšak bez významného vlivu na účinnost.
Po perorálním (a nitrožilním) podání se telmisartan téměř výhradně vylučuje stolicí, většinou jako nezměněná substance. Kumulativní vylučování močí je menší než 1 % dávky. Celková plazmatická clearance (Cltot) je vysoká (přibližně 1000 ml/min) v porovnání s průtokem krve játry (kolem 1500 ml/min).
Zvláštní skupiny pacientů
Pediatrická populace
Farmakokinetika dvou dávek telmisartanu byla hodnocena jako sekundární cíl u pacientů s hypertenzí (n = 57) ve věku od 6 do 18 let po podání telmisartanu 1 mg/kg nebo 2 mg/kg po dobu 4 týdnů léčby. Farmakokinetické parametry zahrnovaly stanovení ustáleného stavu telmisartanu u dětí a dospívajících a hodnocení rozdílů v závislosti na věku. Přestože studie byla příliš malá pro významné posouzení farmakokinetiky u dětí mladších 12 let, výsledky jsou obecně v souladu s nálezy u dospělých a potvrzují ne-linearitu telmisartanu, zejména pro Cmax.
Pohlaví:
Byly pozorovány rozdíly v plazmatických koncentracích v závislosti na pohlaví, s hodnotami Cmax přibližně třikrát a AUC přibližně dvakrát vyššími u žen než u mužů.
Starší pacienti:
Farmakokinetika telmisartanu se u starších pacientů a pacientů mladších než 65 let neliší.
Porucha funkce ledvin:
U pacientů s mírnou až středně závažnou a závažnou poruchou funkce ledvin byly pozorovány dvojnásobné koncentrace v plazmě, avšak u pacientů s nedostatečností ledvin podstupujících hemodialýzu byly pozorovány nižší plazmatické koncentrace. Telmisartan se u pacientů s ledvinnou nedostatečností do vysoké míry váže na plazmatické bílkoviny a dialýzou jej nelze odstranit. Poločas eliminace se u pacientů s poškozením funkce ledvin nemění.
Porucha funkce jater
Farmakokinetické studie u pacientů s poruchou funkce jater prokázaly zvýšení hodnot absolutní biologické dostupnosti téměř na 100 %. Poločas eliminace se u pacientů s poruchou funkce jater nemění.
5.3 Předklinické údaje vztahující se k bezpečnosti
V předklinických studiích bezpečnosti po podání dávek, které vedly k expozici srovnatelné s klinickým terapeutickým rozmezím, došlo u normotenzních zvířat ke snížení hodnot červeného krevního obrazu (erytrocytů, hemoglobinu, hematokritu), změnám v renální hemodynamice (nárůst dusíku močoviny a kreatininu) a zvýšení hladiny sérového draslíku. U psů byla pozorována dilatace renálních tubulů a jejich atrofie. U potkanů a psů byly rovněž zaznamenány změny žaludeční sliznice (eroze, vředy nebo zánět). Těmto farmakologicky vyvolaným nežádoucím účinkům, známým z předklinického hodnocení jak inhibitorů enzymu konvertujícího angiotenzin, tak antagonistů receptoru angiotenzinu II, bylo možné předejít perorálním podáváním fyziologického roztoku.
U potkanů a psů byly rovněž pozorovány zvýšené hodnoty reninu v plazmě a hypertrofie/hyperplazie ledvinových juxtaglomerulárních buněk. Tyto změny představují rovněž skupinový účinek inhibitorů enzymu konvertujícího angiotenzin II a antagonistů receptoru angiotenzinu II, zřejmě nemají klinický význam.
Nebyl zjištěn žádný jasný důkaz o teratogenním účinku, avšak podávání telmisartanu v toxických dávkách má vliv na postnatální vývoj jedinců jako je nižší tělesná hmotnost a opožděné otevírání očí.
Testy in vitro neprokázaly mutagenní a významnou klastogenní aktivitu ani nebyl prokázán kancerogenní účinek u potkanů a myší.
6. FARMACEUTICKÉ VLASTNOSTI 6.1 Seznam pomocných látek
Mikrokrystalická celulosa (Avicel PH 102) Sodná sůl karboxymethylškrobu (Typ A) Poloxamer Meglumin
Povidon (PVP K-30)
Sorbitol (E420)
Magnesium-stearát
6.5 Inkompatibility
Neuplatňuje se.
6.3. Doba použitelnosti
2 roky
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
Al/Al odlupovací perforované jednodávkové blistry a Al/Al perforované jednodávkové blistry. Odlupovací perforované blistry obsahující 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet.
Perforované blistry obsahující 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet. Al/Al blistry obsahující 30 tablet.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Teva B.V.
Swensweg 5 2031GA Haarlem Nizozemsko
8. REGISTRAČNÍ ČÍSLO (A)
EU/1/09/610/021
EU/1/09/610/022
EU/1/09/610/023
EU/1/09/610/024
EU/1/09/610/025
EU/1/09/610/026
EU/1/09/610/027
EU/1/09/610/028
EU/1/09/610/029
EU/1/09/610/030
EU/1/09/610/051
EU/1/09/610/052
Krabička se 14x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 28x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 30x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 40x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 56x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 60x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 84x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 90x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička s 98x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 100x1 tabletami v odlupovacích perforovaných jednodávkových Al/Al blistrech
Krabička se 14x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 28x1 tabletami v perforovaných jednodávkových Al/Al blistrech
Krabička se 30x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 40x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 56x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 60x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 84x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 90x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 98x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička se 100x1 tabletami v perforovaných jednodávkových Al/Al blistrech Krabička s 30 tabletami v Al/Al blistrech
EU/1/09/610/053 EU/1/09/610/054 EU/1/09/610/055 EU/1/09/610/056 EU/1/09/610/057 EU/1/09/610/058 EU/1/09/610/059 EU/1/09/610/060 EU/1/09/610/062
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 26. ledna 2010
Datum posledního prodloužení registrace: 19/12/2014
10. DATUM REVIZE TEXTU
Podrobné informace o tomto přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
PŘÍLOHA II
A. VÝROBCE/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
Název a adresa výrobců odpovědných za propouštění šarží
Teva Pharmaceutical Works Private Limited Company
Pallagi út 13, 4042 Debrecen
Maďarsko
TEVA Pharmaceutical Works Private Limited Company
H-2100 Godollo, Táncsics Mihály út 82
Maďarsko (Headquarters: 4042 Debrecen, Pallagi út 13)
TEVA UK Ltd
Brampton Road, Hampden Park, Eastbourne, East Sussex, BN22 9AG Velká Británie
Pharmachemie B.V.
Swensweg 5,
2031 GA Haarlem Nizozemsko
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propouštění dané šarže.
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
Pravidelně aktualizované zprávy o bezpečnosti
Držitel rozhodnutí o registraci předkládá pravidelně aktualizované zprávy o bezpečnosti pro tento léčivý přípravek v souladu s požadavky uvedenými v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a zveřejněném na evropském webovém portálu pro léčivé přípravky.
Systém farmakovigilance
Držitel rozhodnutí o registraci musí zajistit, aby byl zaveden funkční systém farmakovigilance uvedený v modulu 1.8.1 schválené registrace předtím, než bude léčivý přípravek uveden na trh, a dále po celou dobu, kdy bude léčivý přípravek na trhu.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ TOHOTO LÉČIVÉHO PŘÍPRAVKU
Plán řízení rizik (RMP)
Neuplatňuje se.
PŘÍLOHA III
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Telmisartan Teva 20 mg tablety telmisartanum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jedna tableta obsahuje telmisartanum 20 mg
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje sorbitol (E420). Další informace naleznete v příbalové informaci.
4. LÉKOVÁ FORMA A OBSAH
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
5. ZPŮSOB A CESTA PODÁNÍ
Perorální podání.
Před užitím čtěte příbalovou informaci
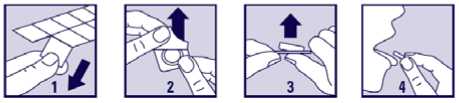
1. Oddělte jednotlivý článek blistru od jeho zbytku jemným odtržením podél ražení
2. Pečlivě sloupněte vrchní papírovou vrstvu
3. Vytlačte tabletu skrz obrácenou folii
4. Vložte tabletu do úst a polkněte spolu s vodou nebo jinou vhodnou tekutinou
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V. Swensweg 5 2031GA Haarlem Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
EU/1/09/610/001
EU/1/09/610/002
EU/1/09/610/003
EU/1/09/610/004
EU/1/09/610/005
EU/1/09/610/006
EU/1/09/610/007
EU/1/09/610/008
EU/1/09/610/009
EU/1/09/610/010
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
16. BRAILLOVO PÍSMO
Telmisartan Teva 20 mg
Telmisartan Teva 20 mg tablety telmisartanum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jedna tableta obsahuje telmisartanum 20 mg
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje sorbitol (E420). Další informace naleznete v příbalové informaci.
4. LÉKOVÁ FORMA A OBSAH
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
5. ZPŮSOB A CESTA PODÁNÍ
Perorální podání.
Před užitím čtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V. Swensweg 5 2031GA Haarlem Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
EU/1/09/610/031
EU/1/09/610/032
EU/1/09/610/033
EU/1/09/610/034
EU/1/09/610/035
EU/1/09/610/036
EU/1/09/610/037
EU/1/09/610/038
EU/1/09/610/039
EU/1/09/610/040
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. BRAILLOVO PÍSMO
Telmisartan Teva 20 mg
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Telmisartan Teva 40 mg tablety telmisartanum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jedna tableta obsahuje telmisartanum 40 mg
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje sorbitol (E420). Další informace naleznete v příbalové informaci.
4. LÉKOVÁ FORMA A OBSAH
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
5. ZPŮSOB A CESTA PODÁNÍ
Perorální podání.
Před užitím čtěte příbalovou informaci

1. Oddělte jednotlivý článek blistru od jeho zbytku jemným odtržením podél ražení
2. Pečlivě sloupněte vrchní papírovou vrstvu
3. Vytlačte tabletu skrz obrácenou folii
4. Vložte tabletu do úst a polkněte spolu s vodou nebo jinou vhodnou tekutinou
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V. Swensweg 5 2031GA Haarlem Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
EU/1/09/610/011
EU/1/09/610/012
EU/1/09/610/013
EU/1/09/610/014
EU/1/09/610/015
EU/1/09/610/016
EU/1/09/610/017
EU/1/09/610/018
EU/1/09/610/019
EU/1/09/610/020
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
16. BRAILLOVO PÍSMO
Telmisartan Teva 40 mg

Telmisartan Teva 40 mg tablety telmisartanum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jedna tableta obsahuje telmisartanum 40 mg
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje sorbitol (E420). Další informace naleznete v příbalové informaci.
4. LÉKOVÁ FORMA A OBSAH
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet 30 tablet
5. ZPŮSOB A CESTA PODÁNÍ
Perorální podání.
Před užitím čtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V. Swensweg 5 2031GA Haarlem Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet 30 tablet
EU/1/09/610/041
EU/1/09/610/042
EU/1/09/610/043
EU/1/09/610/044
EU/1/09/610/045
EU/1/09/610/046
EU/1/09/610/047
EU/1/09/610/048
EU/1/09/610/049
EU/1/09/610/050
EU/1/09/610/061
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. BRAILLOVO PÍSMO
Telmisartan Teva 40 mg
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Telmisartan Teva 80 mg tablety telmisartanum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jedna tableta obsahuje telmisartanum 80 mg
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje sorbitol (E420). Další informace naleznete v příbalové informaci.
4. LÉKOVÁ FORMA A OBSAH
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
5. ZPŮSOB A CESTA PODÁNÍ
Perorální podání.
Před užitím čtěte příbalovou informaci

1. Oddělte jednotlivý článek blistru od jeho zbytku jemným odtržením podél ražení
2. Pečlivě sloupněte vrchní papírovou vrstvu
3. Vytlačte tabletu skrz obrácenou folii
4. Vložte tabletu do úst a polkněte spolu s vodou nebo jinou vhodnou tekutinou
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V. Swensweg 5 2031GA Haarlem Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet
EU/1/09/610/021
EU/1/09/610/022
EU/1/09/610/023
EU/1/09/610/024
EU/1/09/610/025
EU/1/09/610/026
EU/1/09/610/027
EU/1/09/610/028
EU/1/09/610/029
EU/1/09/610/030
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
16. BRAILLOVO PÍSMO
Telmisartan Teva 80 mg

Telmisartan Teva 80 mg tablety telmisartanum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jedna tableta obsahuje telmisartanum 80 mg
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje sorbitol (E420). Další informace naleznete v příbalové informaci.
4. LÉKOVÁ FORMA A OBSAH
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet 30 tablet
5. ZPŮSOB A CESTA PODÁNÍ
Perorální podání.
Před užitím čtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V. Swensweg 5 2031GA Haarlem Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
14x1 tablet 28x1 tablet 30x1 tablet 40x1 tablet 56x1 tablet 60x1 tablet 84x1 tablet 90x1 tablet 98x1 tablet 100x1 tablet 30 tablet
EU/1/09/610/051
EU/1/09/610/052
EU/1/09/610/053
EU/1/09/610/054
EU/1/09/610/055
EU/1/09/610/056
EU/1/09/610/057
EU/1/09/610/058
EU/1/09/610/059
EU/1/09/610/060
EU/1/09/610/062
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. BRAILLOVO PÍSMO
Telmisartan Teva 80 mg
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Telmisartan Teva 20 mg tablety Telmisartanum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI_
Teva B. V.
3. POUŽITELNOST_
EXP:
4. ČÍSLO ŠARŽE_
č.š.:
5. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Telmisartan Teva 40 mg tablety Telmisartanum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI_
Teva B. V.
3. POUŽITELNOST_
EXP:
4. ČÍSLO ŠARŽE_
č.š.:
5. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Telmisartan Teva 80 mg tablety Telmisartanum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI_
Teva B. V.
3. POUŽITELNOST_
EXP:
4. ČÍSLO ŠARŽE_
č.š.:
5. JINÉ
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro uživatele
Telmisartan Teva 20 mg tablety
Telmisartanum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li případně další otázky, zeptejte se, prosím, svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Telmisartan Teva a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Telmisartan Teva používat
3. Jak se Telmisartan Teva používá
4. Možné nežádoucí účinky
5. Jak Telmisartan Teva uchovávat
6. Obsah balení a další informace
1. Co je Telmisartan Teva a k čemu se používá
Telmisartan Teva patří ke skupině léků, které jsou známy jako blokátory (antagonisté) receptoru angiotenzinu II. Angiotenzin II je látka, která vzniká v těle. Jejím účinkem dochází k zúžení cév, čímž se zvyšuje krevní tlak. Telmisartan Teva blokuje účinek angiotenzinu II, takže dochází k roztažení cév, a tím ke snížení krevního tlaku.
Přípravek Telmisartan Teva se užívá k léčbě esenciální hypertenze (vysoký krevní tlak) u dospělých. „Esenciální“ znamená, že vysoký krevní tlak není způsoben žádnými jinými okolnostmi.
Pokud není vysoký krevní tlak léčen, může poškozovat krevní cévy v řadě orgánů, což může někdy vést k srdečnímu infarktu, k selhání srdce nebo ledvin, k cévní mozkové příhodě (mrtvici), nebo ke slepotě. V době před vznikem poškození zvýšený krevní tlak obvykle nemá žádné příznaky. Proto je velmi důležité pravidelným měřením ověřovat, zda jsou hodnoty krevního tlaku v normálním rozmezí.
Telmisartan Teva se také používá u dospělých pacientů ke snížení výskytu srdečně-cévních příhod (např. srdeční infarkt nebo cévní mozková příhoda), kterými jsou ohroženi pacienti s nedostatečným krevním zásobením srdce nebo dolních končetin nebo pacienti, kteří prodělali cévní mozkovou příhodu nebo vysoce rizikoví pacienti s cukrovkou. Lékař Vám sdělí, zda máte vysoké riziko těchto příhod.
2. Čemu musíte věnovat pozornost, než začnete Telmisartan Teva používat Neužívejte přípravek Telmisartan Teva
- jestliže j ste alergický/á na telmisartan nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže jste více než 3 měsíce těhotná. (Také je lepší vyhnout se přípravku Telmisartan Teva v časném těhotenství - viz bod Těhotenství.)
- jestliže máte závažné jatemí onemocnění, jako je cholestáza nebo obstrukce žlučových cest (problémy s odváděním žluči z jater a ze žlučníku) nebo jakékoliv jiné závažné jatemí onemocnění.
- jestliže máte cukrovku (diabetes) nebo poruchu funkce ledvin nebo jste léčen(a) přípravkem ke snížení krevního tlaku obsahujícím aliskiren.
Jestliže se Vás cokoliv z výše uvedeného týká, oznamte to svému lékaři nebo lékárníkovi před tím, než začnete přípravek Telmisartan Teva užívat.
Upozornění a opatření
Oznamte svému lékaři, jestliže trpíte nebo jste trpěl(a) některým z následujících stavů nebo onemocnění:
- Onemocnění ledvin nebo prodělaná transplantace ledvin
- Stenóza renální artérie (zúžení tepny, která přivádí krev do jedné nebo do obou ledvin)
- Onemocnění jater
- Problémy se srdcem
- Zvýšená hladina hormonu aldosteronu (zadržování vody a solí v těle spolu s kolísáním různých krevních minerálů)
- Nízký krevní tlak (hypotenze), který s vyšší pravděpodobností může nastat v případě dehydratace organismu (tj. při nadměrné ztrátě vody z těla) nebo při nedostatku soli v těle, způsobeným močopudnou (diuretickou) terapií (tj. „tabletami na odvodnění", tzv. diuretiky), při stravě s nízkým obsahem soli, při průjmech nebo zvracení
- Zvýšená hladina draslíku v krvi
- Cukrovka
Než začnete užívat přípravek Telmisartan Teva poraďte se svým lékařem:
• jestliže užíváte digoxin
• pokud užíváte některý z následujících přípravků používaných k léčbě vysokého krevního tlaku:
- inhibitor ACE (například enalapril, lisinopril, ramipril), a to zejména pokud máte problémy s ledvinami související s diabetem.
- aliskiren
Váš lékař může v pravidelných intervalech kontrolovat funkci ledvin, krevní tlak a množství elektrolytů (např. draslíku) v krvi.
Viz také informace v bodě: “Neužívejte přípravek Telmisartan Teva“
Musíte sdělit svému lékaři, pokud se domníváte, že jste (nebo můžete být) těhotná. Podávání přípravku Telmisartan Teva se nedoporučuje v časném těhotenství a nesmí se užívat, jestliže jste těhotná déle než 3 měsíce, protože může způsobit závažné poškození dítěte, pokud se užívá v tomto období (viz bod Těhotenství).
V případě operace nebo narkózy je nutno sdělit lékaři, že užíváte přípravek Telmisartan Teva.
Telmisartan Teva může být méně účinný při snižování krevního tlaku u pacientů černošské rasy.
Děti a dospívající
Použití přípravku Telmisartan Teva u dětí a dospívajících ve věku do 18 let se nedoporučuje.
Další léčivé přípravky a Telmisartan Teva
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Váš lékař může dospět k závěru, že je třeba změnit dávkování některých jiných léčivých přípravků, které užíváte, nebo že je nutno přijmout další opatření.
V některých případech možná budete muset užívání některého léku ukončit. To se týká zejména léků uvedených níže, pokud se užívají současně s přípravkem Telmisartan Teva:
• Pokud užíváte inhibitory ACE nebo aliskiren (viz také informace v bodě "Neužívejte přípravek Telmisartan Teva" a "Upozornění a opatření“).
• Léky obsahující lithium, užívané k léčbě některých typů deprese.
• Léky, které mohou zvýšit hladinu draslíku v krvi, jako jsou náhražky soli obsahující draslík, draslík šetřící močopudné léky (draslík šetřící diuretika tzv. „tablety na odvodnění“), ACE inhibitory, blokátory receptoru angiotenzinu II, NSAIDs (nesteroidní protizánětlivé léky, například kyselina acetylsalicylová nebo ibuprofen), heparin, imunosupresiva (například cyklosporin nebo takrolimus) a antibiotikum trimetoprim.
• Diuretika (močopudné léky, „tablety na odvodnění") mohou vést k nadměrným ztrátám vody z těla a k nízkému krevnímu tlaku (hypotenzi), zejména jsou-li užívány ve vysokých dávkách současně s přípravkem Telmisartan Teva.
• Digoxin
Účinek přípravku Telmisartan Teva může být oslaben současným užíváním léků ze skupiny NSAIDs (nesteroidních protizánětlivých léků, například kyseliny acetylsalicylové nebo ibuprofenu) nebo kortikosteroidy.
Telmisartan Teva může zesilovat účinek jiných léků, které jsou užívány k léčbě vysokého krevního tlaku a krevní tlak snižují.
Pokud trpíte onemocněním nazývaným orthostatická hypotenze (pokles krevního tlaku při změně polohy ze sedu nebo lehu do stoje, který způsobuje závrať nebo mdlobu), Váš stav se může zhoršit pokud užíváte Telmisartan Teva v kombinaci s:
• jinými přípravky k léčbě krevního tlaku
• Baklofenem (přípravek na uvolnění svalů)
• Amifostinem (podpůrný přípravek užívaný během ozařování při léčbě nádorů)
• Alkoholem
• Barbituráty (přípravky na spaní)
• Narkotickými léky proti bolesti
• Antidepresivy
Těhotenství a kojení Těhotenství
Musíte sdělit svému lékaři, pokud se domníváte, že jste (nebo můžete být) těhotná. Lékař Vám obvykle poradí přestat s užíváním přípravku Telmisartan Teva dříve než otěhotníte nebo jakmile zjistíte, že jste těhotná a doporučí užívat jiný lék místo přípravku Telmisartan Teva. Přípravek Telmisartan Teva se nedoporučuje v časném těhotenství a nesmí se užívat, jestliže jste těhotná déle než 3 měsíce, protože může v období po třetím měsíci těhotenství způsobit při užívání závažné poškození dítěte.
Kojení
Poraďte se s lékařem, pokud kojíte nebo začínáte s kojením. Telmisartan Teva se nedoporučuje u kojících matek a lékař Vám zřejmě zvolí jinou léčbu, pokud si budete přát kojit, zejména u novorozenců nebo předčasně narozených dětí.
Řízení dopravních prostředků a obsluha strojů
Někteří lidé mohou při užívání přípravku Telmisartan Teva cítit závrať nebo únavu. Pokud pociťujete závrať nebo únavu, neřiďte dopravní prostředky a neobsluhujte stroje.
Telmisartan Teva
Jestliže trpíte nesnášenlivostí některých cukrů, poraďte se před užíváním přípravku Telmisartan Teva s lékařem.
3. Jak se Telmisartan Teva užívá
Přípravek Telmisartan Teva vždy užívejte přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka přípravku Telmisartan Teva je jedna tableta denně. Snažte se užívat tablety každý den ve stejnou dobu. Telmisartan Teva můžete užívat s jídlem nebo bez něj. Tablety je třeba spolknout a zapít vodou nebo nějakým jiným nealkoholickým nápojem. Pokud Vám lékař neřekne jinak, je důležité, abyste užívali přípravek Telmisartan Teva každý den. Pokud se domníváte, že je účinek přípravku Telmisartan Teva příliš silný nebo slabý, poraďte se se svým lékařem nebo lékárníkem.
Při léčbě vysokého krevního tlaku je obvyklá dávka přípravku Telmisartan Teva pro většinu pacientů jedna 40 mg tableta denně, která Váš krevní tlak udržuje pod kontrolou 24 hodin. Váš lékař Vám doporučenou dávku snížil na 20 mg denně, což představuje užití jedné tablety denně. Eventuálně lze přípravek Telmisartan Teva užívat v kombinaci s diuretiky („tablety na odvodnění“) jako je hydrochlorothiazid, u něhož bylo prokázáno, že zesiluje účinek přípravku Telmisartan Teva na snížení krevního tlaku.
Ke snížení výskytu srdečně-cévních příhod je obvyklá dávka přípravku Telmisartan Teva jedna tableta 80 mg jednou denně. Při zahájení preventivní léčby přípravkem Telmisartan Teva 80 mg by měl být často měřen krevní tlak.
Pokud trpíte poruchou činnosti jater, pak by obvyklá dávka neměla přesáhnout 40 mg jednou denně. Jestliže jste užil(a) více přípravku Telmisartan Teva, než jste měl(a)
Jestliže jste nedopatřením užil(a) příliš mnoho tablet, poraďte se ihned se svým lékařem, lékárníkem, nebo na pohotovostním oddělení nejbližší nemocnice.
Jestliže jste zapomněl(a) užít přípravek Telmisartan Teva
Jestliže jste zapomněl(a) užít dávku přípravku Telmisartan Teva, nedělejte si starosti. Vezměte ji, jakmile si vzpomenete, a poté pokračujte jako dříve. Jestliže tabletu jeden den nevezmete, vezměte si normální dávku následující den. Nezdvojujte následující dávku, abyste nahradil(a) vynechanou dávku.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento léčivý přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Některé nežádoucí účinky mohou být závažné a vyžadují okamžitou lékařskou pomoc:
Musíte okamžitě navštívit lékaře, pokud zaznamenáte některý z následujících příznaků:
Sepse (často nazývaná "otrava krve", je závažná infekce se zánětlivou odpovědí celého těla obvykle spojená s vysokými horečkami, horkostí, zarudlou kůží, zvýšenou srdeční frekvencí, zrychleným dýcháním, změnami mentálního stavu, otoky a nízkým krevním tlakem), rychlý otok kůže a sliznic (angioedém); tyto nežádoucí účinky jsou vzácné (mohou se vyskytnout u 1 pacienta z 1000), ale jsou extrémně závažné a pacienti by měli tento přípravek přestat užívat a okamžitě navštívit lékaře. Pokud se tyto nežádoucí účinky neléčí, mohou vést k úmrtí.
Další možné nežádoucí účinky telmisartanu:
Časté nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 10):
Nízký krevní tlak (hypotenze) u pacientů užívajících přípravek ke snížení výskytu srdečně-cévních příhod.
Méně časté nežádoucí účinky (mohou se vyskytnout u 1 pacienta ze 100):
Infekce močových cest, infekce horních cest dýchacích (například bolesti v krku, zánět vedlejších nosních dutin - sinusitida, běžné nachlazení), nedostatek červených krvinek (anémie), vysoká hladina draslíku, potíže při usínání, pocity smutku (deprese), mdloba (synkopa), pocit točení hlavy (závrať), zpomalení srdeční činnosti (bradykardie), nízký krevní tlak (hypotenze) u pacientů léčených pro vysoký krevní tlak, závrať po postavení (ortostatická hypotenze), zkrácený dech (dušnost), kašel, bolesti břicha, průjem, pocit nepohody v břiše (břišní diskomfort), otok, zvracení, svědění, zvýšené pocení, poléková vyrážka, bolesti zad, svalové křeče, bolesti svalů (myalgie), zhoršení funkce ledvin včetně náhlého selhání ledvin, bolesti na hrudi, pocity slabosti a zvýšená hladina kreatininu v krvi.
Vzácné nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 1000):
Zvýšení určitého druhu bílých krvinek (eozinofílie), pokles počtu krevních destiček (trombocytopenie), závažné alergické reakce (anafylaktická reakce), alergické reakce (například vyrážka, svědění, potíže s dechem, sípání, otok tváře nebo nízký krevní tlak), nízká hladina krevního cukru (u diabetických pacientů), pocity úzkosti, ospalost, poruchy zraku, zrychlená srdeční činnost (tachykardie), sucho v ústech, žaludeční nevolnost, poruchy vnímání chuti (dysgeuzie), abnormální funkce jater (tento nežádoucí účinek se vyskytuje s větší pravděpodobností u japonských pacientů), ekzém (porucha kůže), zarudnutí kůže, kopřivka (urticaria), závažná poléková vyrážka, bolesti kloubů (artralgie), bolesti končetin, bolesti šlach, onemocnění připomínající chřipku, pokles hemoglobinu (krevní bílkovina), zvýšená hladina kyseliny močové, jaterních enzymů nebo kreatinfosfokinázy v krvi.
Velmi vzácné nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 10 000):
Progresivní zjizvení plicní tkáně (intersticiální plicní nemoc).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Telmisartan Teva uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Tento léčivý přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na krabičce a blistru za „Použitelné do:“ Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co Telmisartan Teva obsahuje
- Léčivou látkou je telmisartan. Jedna tableta přípravku Telmisartan Teva obsahuje telmisartanum 20 mg.
- Pomocnými látkami jsou mikrokrystalická celulosa (Avicel PH 102), sodná sůl karboxymethylškrobu (Typ A), poloxamer, meglumin, povidon, sorbitol (E420) a magnesium-stearát.
Jak Telmisartan Teva vypadá a co obsahuje toto balení
Telmisartan Teva 20 mg jsou bílé až téměř bílé, oválné tablety s vyraženým číslem „93“ na jedné straně a s číslem „7458“ na straně druhé.
Telmisartan Teva je dodáván v odloupnutelných perforovaných jednodávkových Al/Al blistrech nebo perforovaných jednodávkových Al/Al blistrech, obsahujících 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet.
Na trhu nemusí být všechny velikosti balení.
Přečtěte si, prosím, návod jak vyjmout tabletu z blistru, který je umístěn na krabičce s odloupnutelnými blistry.
Držitel rozhodnutí o registraci
Teva B.V.
Swensweg 5 2031GA Haarlem Nizozemsko
Výrobce
TEVA Pharmaceutical Works Private Limited Company Pallagi út 13,
4042 Debrecen,
Maďarsko
nebo
TEVA Pharmaceutical Works Private Limited Company H-2100 Godollo,
Táncsics Mihály út 82 Maďarsko
nebo
TEVA UK Ltd Brampton Road,
Hampden Park,
Eastbourne,
East Sussex,
BN22 9AG Velká Británie
nebo
Pharmachemie B.V. Swensweg 5,
2031 GA, Haarlem, Nizozemsko
|
Další informace o tomto přípravku získáte |
u místního zástupce držitele rozhodnutí o registraci |
|
Belgie/Belgique/Belgien Teva Pharma Belgium N.V./S.A. Tel/Tél: +32 3 820 73 73 |
Luxembourg/Luxemburg Teva Pharma Belgium S.A. Belgien/Belgique Tél/Tel: +32 3 820 73 73 |
|
Btarapna TeBa OapMacroTHKtac Etarapna EOOfl Tea: +359 2 489 95 82 |
Magyarország Teva Gyógyszergyár Zrt. (TPW) Tel.: +36 1 288 64 00 |
|
Česká republika Teva Pharmaceuticals CR, s.r.o. Tel: +420 251 007 111 |
Malta Teva Pharmaceuticals Ireland Tel: +353 51 321740 L-Irlanda |
|
Danmark Teva Denmark A/S Tlf: +45 44 98 55 11 |
Nederland Teva Nederland B.V. Tel: +31 (0) 800 0228400 |
|
Deutschland Teva GmbH Tel: (49) 731 40208 |
Norge Teva Norway AS Tlf: +47 66 77 55 90 |
|
Eesti Teva Eesti esindus UAB Sicor Biotech Eesti filiaal Tel: +372 661 0801 |
Osterreich Ratiopharm Arzneimittel Vertriebs-GmbH Tel: +43 1 97 00 7 |
|
EkXáSa Teva ETAág A.E. Tqk +30 210 72 79 099 |
Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel.: +(48) 22 345 93 00 |
|
Espaňa Teva Pharma, S.L.U Tél: +(34) 91 387 32 80 |
Portugal Teva Pharma - Produtos Farmaceuticos Lda Tel: (351) 214 235 910 |
|
France Teva Santé Tél: +(33) 1 55 91 7800 Hrvatska Pliva Hrvatska d.o.o Tel: + 385 1 37 20 000 |
Románia Teva Pharmaceuticals S.R.L Tel: +4021 230 65 24 |
|
Ireland Teva Pharmaceuticals Ireland |
Slovenija Pliva Ljubljana d.o.o. |
Island
ratiopharm Oy Finnland
Sími: +358 9 180 452 5900 Italia
Teva Italia S.r.l.
Tel: +(39) 028917981
Kórcpog
Teva Ekkág A.E.
Ekká5a
Tpk: +30 210 72 79 099 Latvija
UAB Sicor Biotech filiale Latvija Tel: +371 67 784 980
Lietuva
UAB “Sicor Biotech”
Tel: +370 5 266 02 03
Slovenská republika
Teva Pharmaceuticals Slovakia s.r.o. Tel: +(421) 2 5726 7911
Suomi/Finland
ratiopharm Oy Puh/Tel: +358 20 180 5900
Sverige
Teva Sweden AB Tel: +(46) 42 12 11 00
United Kingdom
Teva UK Limited Tel: +(44) 1977 628 500
Tato příbalová informace byla naposledy revidována:
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
Příbalová informace: informace pro uživatele
Telmisartan Teva 40 mg tablety
Telmisartanum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li případně další otázky, zeptejte se, prosím, svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Telmisartan Teva a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Telmisartan Teva používat
3. Jak se Telmisartan Teva používá
4. Možné nežádoucí účinky
5. Jak Telmisartan Teva uchovávat
6. Obsah balení a další informace
1. Co je Telmisartan Teva a k čemu se používá
Telmisartan Teva patří ke skupině léků, které jsou známy jako blokátory (antagonisté) receptoru angiotenzinu II. Angiotenzin II je látka, která vzniká v těle. Jejím účinkem dochází k zúžení cév, čímž se zvyšuje krevní tlak. Telmisartan Teva blokuje účinek angiotenzinu II, takže dochází k roztažení cév, a tím ke snížení krevního tlaku.
Přípravek Telmisartan Teva se užívá k léčbě esenciální hypertenze (vysoký krevní tlak) u dospělých. „Esenciální“ znamená, že vysoký krevní tlak není způsoben žádnými jinými okolnostmi.
Pokud není vysoký krevní tlak léčen, může poškozovat krevní cévy v řadě orgánů, což může někdy vést k srdečnímu infarktu, k selhání srdce nebo ledvin, k cévní mozkové příhodě (mrtvici), nebo ke slepotě. V době před vznikem poškození zvýšený krevní tlak obvykle nemá žádné příznaky. Proto je velmi důležité pravidelným měřením ověřovat, zda jsou hodnoty krevního tlaku v normálním rozmezí.
Telmisartan Teva se také používá u dospělých pacientů ke snížení výskytu srdečně-cévních příhod (např. srdeční infarkt nebo cévní mozková příhoda), kterými jsou ohroženi pacienti s nedostatečným krevním zásobením srdce nebo dolních končetin nebo pacienti, kteří prodělali cévní mozkovou příhodu nebo vysoce rizikoví pacienti s cukrovkou. Lékař Vám sdělí, zda máte vysoké riziko těchto příhod.
2. Čemu musíte věnovat pozornost, než začnete Telmisartan Teva užívat Neužívejte přípravek Telmisartan Teva
- jestliže j ste alergický/á na telmisartan nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže jste více než 3 měsíce těhotná. (Také je lepší vyhnout se přípravku Telmisartan Teva v časném těhotenství - viz bod Těhotenství.)
- jestliže máte závažné jatemí onemocnění, jako je cholestáza nebo obstrukce žlučových cest (problémy s odváděním žluči z jater a ze žlučníku) nebo jakékoliv jiné závažné jatemí onemocnění.
- jestliže máte cukrovku (diabetes) nebo poruchu funkce ledvin nebo jste léčen(a) přípravkem ke snížení krevního tlaku obsahujícím aliskiren.
Jestliže se Vás cokoliv z výše uvedeného týká, oznamte to svému lékaři nebo lékárníkovi před tím, než začnete přípravek Telmisartan Teva užívat.
Upozornění a opatření
Oznamte svému lékaři, jestliže trpíte nebo jste trpěl(a) některým z následujících stavů nebo onemocnění:
- Onemocnění ledvin nebo prodělaná transplantace ledvin
- Stenóza renální artérie (zúžení tepny, která přivádí krev do jedné nebo do obou ledvin)
- Onemocnění jater
- Problémy se srdcem
- Zvýšená hladina hormonu aldosteronu (zadržování vody a solí v těle spolu s kolísáním různých krevních minerálů)
- Nízký krevní tlak (hypotenze), který s vyšší pravděpodobností může nastat v případě dehydratace organismu (tj. při nadměrné ztrátě vody z těla) nebo při nedostatku soli v těle, způsobeným močopudnou (diuretickou) terapií (tj. „tabletami na odvodnění", tzv. diuretiky), při stravě s nízkým obsahem soli, při průjmech nebo zvracení
- Zvýšená hladina draslíku v krvi
- Cukrovka
Než začnete užívat přípravek Telmisartan Teva poraďte se svým lékařem:
• jestliže užíváte digoxin
• pokud užíváte některý z následujících přípravků používaných k léčbě vysokého krevního tlaku:
- inhibitor ACE (například enalapril, lisinopril, ramipril), a to zejména pokud máte problémy s ledvinami související s diabetem.
- aliskiren
Váš lékař může v pravidelných intervalech kontrolovat funkci ledvin, krevní tlak a množství elektrolytů (např. draslíku) v krvi.
Viz také informace v bodě: “Neužívejte přípravek Telmisartan Teva“.
Musíte sdělit svému lékaři, pokud se domníváte, že jste (nebo můžete být) těhotná. Podávání přípravku Telmisartan Teva se nedoporučuje v časném těhotenství a nesmí se užívat, jestliže jste těhotná déle než 3 měsíce, protože může způsobit závažné poškození dítěte, pokud se užívá v tomto období (viz bod Těhotenství).
V případě operace nebo narkózy je nutno sdělit lékaři, že užíváte přípravek Telmisartan Teva. Telmisartan Teva může být méně účinný při snižování krevního tlaku u pacientů černošské rasy.
Děti a dospívající
Použití přípravku Telmisartan Teva u dětí a dospívajících ve věku do 18 let se nedoporučuje.
Další léčivé přípravky a Telmisartan Teva
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Váš lékař může dospět k závěru, že je třeba změnit dávkování některých jiných léčivých přípravků, které užíváte, nebo že je nutno přijmout další opatření.
V některých případech možná budete muset užívání některého léku ukončit. To se týká zejména léků uvedených níže, pokud se užívají současně s přípravkem Telmisartan Teva:
• Pokud užíváte inhibitory ACE nebo aliskiren (viz také informace v bodě "Neužívejte přípravek Telmisartan Teva" a "Upozornění a opatření").
• Léky obsahující lithium, užívané k léčbě některých typů deprese.
• Léky, které mohou zvýšit hladinu draslíku v krvi, jako jsou náhražky soli obsahující draslík, draslík šetřící močopudné léky (draslík šetřící diuretika tzv. „tablety na odvodnění“), ACE inhibitory, blokátory receptoru angiotenzinu II, NSAIDs (nesteroidní protizánětlivé léky, například kyselina acetylsalicylová nebo ibuprofen), heparin, imunosupresiva (například cyklosporin nebo takrolimus) a antibiotikum trimetoprim.
• Diuretika (močopudné léky, „tablety na odvodnění") mohou vést k nadměrným ztrátám vody z těla a k nízkému krevnímu tlaku (hypotenzi), zejména jsou-li užívány ve vysokých dávkách současně s přípravkem Telmisartan Teva.
• Digoxin
Účinek přípravku Telmisartan Teva může být oslaben současným užíváním léků ze skupiny NSAIDs (nesteroidních protizánětlivých léků, například kyseliny acetylsalicylové nebo ibuprofenu) nebo kortikosteroidy.
Telmisartan Teva může zesilovat účinek jiných léků, které jsou užívány k léčbě vysokého krevního tlaku a krevní tlak snižují.
Pokud trpíte onemocněním nazývaným orthostatická hypotenze (pokles krevního tlaku při změně polohy ze sedu nebo lehu do stoje, který způsobuje závrať nebo mdlobu), Váš stav se může zhoršit pokud užíváte Telmisartan Teva v kombinaci s:
• jinými přípravky k léčbě krevního tlaku
• Baklofenem (přípravek na uvolnění svalů)
• Amifostinem (podpůrný přípravek užívaný během ozařování při léčbě nádorů)
• Alkoholem
• Barbituráty (přípravky na spaní)
• Narkotickými léky proti bolesti
• Antidepresivy
Těhotenství a kojení Těhotenství
Musíte sdělit svému lékaři, pokud se domníváte, že jste (nebo můžete být) těhotná. Lékař Vám obvykle poradí přestat s užíváním přípravku Telmisartan Teva dříve než otěhotníte nebo jakmile zjistíte, že jste těhotná a doporučí užívat jiný lék místo přípravku Telmisartan Teva. Přípravek Telmisartan Teva se nedoporučuje v časném těhotenství a nesmí se užívat, jestliže jste těhotná déle než 3 měsíce, protože může v období po třetím měsíci těhotenství způsobit při užívání závažné poškození dítěte.
Kojení
Poraďte se s lékařem, pokud kojíte nebo začínáte s kojením. Telmisartan Teva se nedoporučuje u kojících matek a lékař Vám zřejmě zvolí jinou léčbu, pokud si budete přát kojit, zejména u novorozenců nebo předčasně narozených dětí.
Řízení dopravních prostředků a obsluha strojů
Někteří lidé mohou při užívání přípravku Telmisartan Teva cítit závrať nebo únavu. Pokud pociťujete závrať nebo únavu, neřiďte dopravní prostředky a neobsluhujte stroje.
Telmisartan Teva obsahuje sorbitol.
Jestliže trpíte nesnášenlivostí některých cukrů, poraďte se před užíváním přípravku Telmisartan Teva s lékařem.
Jak se Telmisartan Teva užívá
3.
Přípravek Telmisartan Teva vždy užívejte přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka přípravku Telmisartan Teva je jedna tableta denně. Snažte se užívat tablety každý den ve stejnou dobu. Telmisartan Teva můžete užívat s jídlem nebo bez něj. Tablety je třeba spolknout a zapít vodou nebo něj akým j iným nealkoholickým nápoj em. Pokud V ám lékař neřekne j inak, j e důležité, abyste užívali přípravek Telmisartan Teva každý den. Pokud se domníváte, že je účinek přípravku Telmisartan Teva příliš silný nebo slabý, poraďte se se svým lékařem nebo lékárníkem.
Při léčbě vysokého krevního tlaku je obvyklá dávka přípravku Telmisartan Teva pro většinu pacientů jedna 40 mg tableta denně, která Váš krevní tlak udržuje pod kontrolou 24 hodin. V některých případech však lékař může doporučit snížení dávky na 20 mg, nebo naopak zvýšení dávky na 80 mg. Eventuálně lze přípravek Telmisartan Teva užívat v kombinaci s diuretiky („tablety na odvodnění“) jako hydrochlorothiazid, u něhož bylo prokázáno, že zesiluje účinek přípravku Telmisartan Teva na snížení krevního tlaku.
Ke snížení výskytu srdečně-cévních příhod je obvyklá dávka přípravku Telmisartan Teva jedna tableta 80 mg jednou denně. Při zahájení preventivní léčby přípravkem Telmisartan Teva 80 mg by měl být často měřen krevní tlak.
Pokud trpíte poruchou činnosti jater, pak by obvyklá dávka neměla přesáhnout 40 mg jednou denně. Jestliže jste užil(a) více přípravku Telmisartan Teva, než jste měl(a)
Jestliže jste nedopatřením užil(a) příliš mnoho tablet, poraďte se ihned se svým lékařem, lékárníkem, nebo na pohotovostním oddělení nejbližší nemocnice.
Jestliže jste zapomněl(a) užít přípravek Telmisartan Teva
Jestliže jste zapomněl(a) užít dávku přípravku Telmisartan Teva, nedělejte si starosti. Vezměte ji, jakmile si vzpomenete, a poté pokračujte jako dříve. Jestliže tabletu jeden den nevezmete, vezměte si normální dávku následující den. Nezdvojujte následující dávku, abyste nahradil(a) vynechanou dávku.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento léčivý přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Některé nežádoucí účinky mohou být závažné a vyžadují okamžitou lékařskou pomoc:
Musíte okamžitě navštívit lékaře, pokud zaznamenáte některý z následujících příznaků:
Sepse (často nazývaná "otrava krve", je závažná infekce se zánětlivou odpovědí celého těla obvykle spojená s vysokými horečkami, horkostí, zarudlou kůží, zvýšenou srdeční frekvencí, zrychleným dýcháním, změnami mentálního stavu, otoky a nízkým krevním tlakem), rychlý otok kůže a sliznic (angioedém); tyto nežádoucí účinky jsou vzácné (mohou se vyskytnout u 1 pacienta z 1000), ale jsou extrémně závažné a pacienti by měli tento přípravek přestat užívat a okamžitě navštívit lékaře. Pokud se tyto nežádoucí účinky neléčí, mohou vést k úmrtí.
Další možné nežádoucí účinky telmisartanu:
Časté nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 10):
Nízký krevní tlak (hypotenze) u pacientů užívajících přípravek ke snížení výskytu srdečně-cévních příhod.
Méně časté nežádoucí účinky (mohou se vyskytnout u 1 pacienta ze 100):
Infekce močových cest, infekce horních cest dýchacích (například bolesti v krku, zánět vedlejších nosních dutin - sinusitida, běžné nachlazení), nedostatek červených krvinek (anémie), vysoká hladina draslíku, potíže při usínání, pocity smutku (deprese), mdloba (synkopa), pocit točení hlavy (závrať), zpomalení srdeční činnosti (bradykardie), nízký krevní tlak (hypotenze) u pacientů léčených pro vysoký krevní tlak, závrať po postavení (ortostatická hypotenze), zkrácený dech (dušnost), kašel, bolesti břicha, průjem, pocit nepohody v břiše (břišní diskomfort), otok, zvracení, svědění, zvýšené pocení, poléková vyrážka, bolesti zad, svalové křeče, bolesti svalů (myalgie), zhoršení funkce ledvin včetně náhlého selhání ledvin, bolesti na hrudi, pocity slabosti a zvýšená hladina kreatininu v krvi.
Vzácné nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 1000):
Zvýšení určitého druhu bílých krvinek (eozinofílie), pokles počtu krevních destiček (trombocytopenie), závažné alergické reakce (anafylaktická reakce), alergické reakce (například vyrážka, svědění, potíže s dechem, sípání, otok tváře nebo nízký krevní tlak), nízká hladina krevního cukru (u diabetických pacientů), pocity úzkosti, ospalost, poruchy zraku, zrychlená srdeční činnost (tachykardie), sucho v ústech, žaludeční nevolnost, poruchy vnímání chuti (dysgeuzie), abnormální funkce jater (tento nežádoucí účinek se vyskytuje s větší pravděpodobností u japonských pacientů), ekzém (porucha kůže), zarudnutí kůže, kopřivka (urticaria), závažná poléková vyrážka, bolesti kloubů (artralgie), bolesti končetin, bolesti šlach, onemocnění připomínající chřipku, pokles hemoglobinu (krevní bílkovina), zvýšená hladina kyseliny močové, jaterních enzymů nebo kreatinfosfokinázy v krvi.
Velmi vzácné nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 10 000):
Progresivní zjizvení plicní tkáně (intersticiální plicní nemoc).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Telmisartan Teva uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Tento léčivý přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na krabičce a blistru za „Použitelné do:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co Telmisartan Teva obsahuje
- Léčivou látkou je telmisartan. Jedna tableta přípravku Telmisartan Teva obsahuje telmisartanum 40 mg.
- Pomocnými látkami jsou mikrokrystalická celulosa (Avicel PH 102), sodná sůl karboxymethylškrobu (Typ A), poloxamer, meglumin, povidon, sorbitol (E420) a magnesium-stearát.
Jak Telmisartan Teva vypadá a co obsahuje toto balení
Telmisartan Teva 40 mg jsou bílé až téměř bílé, oválné tablety s vyraženým číslem „93“ na jedné straně a s číslem „7459“ na straně druhé.
Telmisartan Teva je dodáván v odloupnutelných perforovaných jednodávkových Al/Al blistrech nebo perforovaných jednodávkových Al/Al blistrech, obsahujících 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet.
Telmisartan Teva je dodáván také v Al/Al blistrech obsahujících 30 tablet.
Na trhu nemusí být všechny velikosti balení.
Přečtěte si, prosím, návod jak vyjmout tabletu z blistru, který je umístěn na krabičce s odloupnutelnými blistry.
Držitel rozhodnutí o registraci
Teva B.V.
Swensweg 5 2031GA Haarlem Nizozemsko
Výrobce
TEVA Pharmaceutical Works Private Limited Company Pallagi út 13,
4042 Debrecen,
Maďarsko
nebo
TEVA Pharmaceutical Works Private Limited Company H-2100 Godollo,
Táncsics Mihály út 82 Maďarsko
nebo
TEVA UK Ltd Brampton Road,
Hampden Park,
Eastbourne,
East Sussex,
BN22 9AG Velká Británie
nebo
Pharmachemie B.V Swensweg 5, 2031 GA, Haarlem.
Nizozemsko
|
Další informace o tomto přípravku získáte |
u místního zástupce držitele rozhodnutí o registraci |
|
Belgie/Belgique/Belgien Teva Pharma Belgium N.V./S.A. Tel/Tél: +32 3 820 73 73 |
Luxembourg/Luxemburg Teva Pharma Belgium S.A. Belgien/Belgique Tél/Tel: +32 3 820 73 73 |
|
Btarapna TeBa OapMacroTHKMC Etarapna EOOfl Tea: +359 2 489 95 82 |
Magyarország Teva Gyógyszergyár Zrt. (TPW) Tel.: +36 1 288 64 00 |
|
Česká republika Teva Pharmaceuticals CR, s.r.o. Tel: +420 251 007 111 |
Malta Teva Pharmaceuticals Ireland L-Irlanda Tel: +353 51 321740 |
|
Danmark Teva Denmark A/S Tlf: +45 44 98 55 11 |
Nederland Teva Nederland B.V. Tel: +31 (0) 800 0228400 |
|
Deutschland Teva GmbH Tel: (49) 731 40208 |
Norge Teva Norway AS Tlf: +47 66 77 55 90 |
|
Eesti Teva Eesti esindus UAB Sicor Biotech Eesti filiaal Tel: +372 611 0801 |
Osterreich ratiopharm Arzneimittel Vertriebs-GmbH Tel: +43 1 97 00 7 |
|
EkXáSa Teva EAAág A.E. Tqk +30 210 72 79 099 |
Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel.: +(48) 22 345 93 00 |
|
Espaňa Teva Pharma, S.L.U Tél: +(34) 91 387 32 80 |
Portugal Teva Pharma - Produtos Farmaceuticos Lda Tel: (351) 214 235 910 |
|
France Teva Santé Tél: +(33) 1 55 91 7800 |
Románia Teva Pharmaceuticals S.R.L Tel: +4021 230 65 24 |
|
Hrvatska Pliva Hrvatska d.o.o Tel: + 385 1 37 20 000 Ireland Teva Pharmaceuticals Ireland Tel: +353 (0)51 321 740 |
Slovenija Pliva Ljubljana d.o.o. Tel: +386 1 58 90 390 |
|
Ísland ratiopharm Oy Finnland |
Slovenská republika Teva Pharmaceuticals Slovakia s.r.o. Tel: +(421) 2 5726 7911 |
Sími: +358 9 180 452 5900
Suomi/Finland
ratiopharm Oy Puh/Tel: +358 20 180 5900
Sverige
Teva Sweden AB Tel: +(46) 42 12 11 00
United Kingdom
Teva UK Limited Tel: +(44) 1977 628 500
Italia
Teva Italia S.r.l.
Tel: +(39) 028917981
Kúrcpog
Teva EXkáq A.E.
Ekká5a
Tnk: +30 210 72 79 099 Latvija
UAB Sicor Biotech filiale Latvija Tel: +371 67 784 980
Lietuva
UAB “Sicor Biotech”
Tel: +370 5 266 02 03
Tato příbalová informace byla naposledy revidována:
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Příbalová informace: informace pro uživatele
Telmisartan Teva 80 mg tablety
Telmisartanum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li případně další otázky, zeptejte se, prosím, svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Telmisartan Teva a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Telmisartan Teva používat
3. Jak se Telmisartan Teva používá
4. Možné nežádoucí účinky
5. Jak Telmisartan Teva uchovávat
6. Obsah balení a další informace
1. Co je Telmisartan Teva a k čemu se používá
Telmisartan Teva patří ke skupině léků, které jsou známy jako blokátory (antagonisté) receptoru angiotenzinu II. Angiotenzin II je látka, která vzniká v těle. Jejím účinkem dochází k zúžení cév, čímž se zvyšuje krevní tlak. Telmisartan Teva blokuje účinek angiotenzinu II, takže dochází k roztažení cév, a tím ke snížení krevního tlaku.
Přípravek Telmisartan Teva se užívá k léčbě esenciální hypertenze (vysoký krevní tlak) u dospělých. „Esenciální“ znamená, že vysoký krevní tlak není způsoben žádnými jinými okolnostmi.
Pokud není vysoký krevní tlak léčen, může poškozovat krevní cévy v řadě orgánů, což může někdy vést k srdečnímu infarktu, k selhání srdce nebo ledvin, k cévní mozkové příhodě (mrtvici), nebo ke slepotě. V době před vznikem poškození zvýšený krevní tlak obvykle nemá žádné příznaky. Proto je velmi důležité pravidelným měřením ověřovat, zda jsou hodnoty krevního tlaku v normálním rozmezí.
Telmisartan Teva se také používá u dospělých pacientů ke snížení výskytu srdečně-cévních příhod (např. srdeční infarkt nebo cévní mozková příhoda), kterými jsou ohroženi pacienti s nedostatečným krevním zásobením srdce nebo dolních končetin nebo pacienti, kteří prodělali cévní mozkovou příhodu nebo vysoce rizikoví pacienti s cukrovkou. Lékař Vám sdělí, zda máte vysoké riziko těchto příhod
2. Čemu musíte věnovat pozornost, než začnete Telmisartan Teva užívat Neužívejte přípravek Telmisartan Teva
- jestliže j ste alergický/á na telmisartan nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže jste více než 3 měsíce těhotná. (Také je lepší vyhnout se přípravku Telmisartan Teva v časném těhotenství - viz bod Těhotenství.)
- jestliže máte závažné jatemí onemocnění, jako je cholestáza nebo obstrukce žlučových cest (problémy s odváděním žluči z jater a ze žlučníku) nebo jakékoliv jiné závažné jatemí onemocnění.
- jestliže máte cukrovku (diabetes) nebo poruchu funkce ledvin nebo jste léčen(a) přípravkem ke snížení krevního tlaku obsahujícím aliskiren.
Jestliže se Vás cokoliv z výše uvedeného týká, oznamte to svému lékaři nebo lékárníkovi před tím, než začnete přípravek Telmisartan Teva užívat.
Upozornění a opatření
Oznamte svému lékaři, jestliže trpíte nebo jste trpěl(a) některým z následujících stavů nebo onemocnění:
- Onemocnění ledvin nebo prodělaná transplantace ledvin
- Stenóza renální artérie (zúžení tepny, která přivádí krev do jedné nebo do obou ledvin)
- Onemocnění jater
- Problémy se srdcem
- Zvýšená hladina hormonu aldosteronu (zadržování vody a solí v těle spolu s kolísáním různých krevních minerálů)
- Nízký krevní tlak (hypotenze), který s vyšší pravděpodobností může nastat v případě dehydratace organismu (tj. při nadměrné ztrátě vody z těla) nebo při nedostatku soli v těle, způsobeným močopudnou (diuretickou) terapií (tj. „tabletami na odvodnění", tzv. diuretiky), při stravě s nízkým obsahem soli, při průjmech nebo zvracení
- Zvýšená hladina draslíku v krvi
- Cukrovka
Než začnete užívat přípravek Telmisartan Teva poraďte se svým lékařem:
• jestliže užíváte digoxin
• pokud užíváte některý z následujících přípravků používaných k léčbě vysokého krevního tlaku:
- inhibitor ACE (například enalapril, lisinopril, ramipril), a to zejména pokud máte problémy s ledvinami související s diabetem.
- aliskiren
Váš lékař může v pravidelných intervalech kontrolovat funkci ledvin, krevní tlak a množství elektrolytů (např. draslíku) v krvi.
Viz také informace v bodě: “Neužívejte přípravek Telmisartan Teva“
Musíte sdělit svému lékaři, pokud se domníváte, že jste (nebo můžete být) těhotná. Podávání přípravku Telmisartan Teva se nedoporučuje v časném těhotenství a nesmí se užívat, jestliže j ste těhotná déle než 3 měsíce, protože může způsobit závažné poškození dítěte, pokud se užívá v tomto období (viz bod Těhotenství).
V případě operace nebo narkózy je nutno sdělit lékaři, že užíváte přípravek Telmisartan Teva. Telmisartan Teva může být méně účinný při snižování krevního tlaku u pacientů černošské rasy.
Děti a dospívající
Použití přípravku Telmisartan Teva u dětí a dospívajících ve věku do 18 let se nedoporučuje.
Další léčivé přípravky a Telmisartan Teva
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Váš lékař může dospět k závěru, že je třeba změnit dávkování některých jiných léčivých přípravků, které užíváte, nebo že je nutno přijmout další opatření.
V některých případech možná budete muset užívání některého léku ukončit. To se týká zejména léků uvedených níže, pokud se užívají současně s přípravkem Telmisartan Teva:
• Pokud užíváte inhibitory ACE nebo aliskiren (viz také informace v bodě "Neužívejte přípravek Telmisartan Teva" a "Upozornění a opatření").
• Léky obsahující lithium, užívané k léčbě některých typů deprese.
• Léky, které mohou zvýšit hladinu draslíku v krvi, jako jsou náhražky soli obsahující draslík, draslík šetřící močopudné léky (draslík šetřící diuretika tzv. „tablety na odvodnění“), ACE inhibitory, blokátory receptoru angiotenzinu II, NSAIDs (nesteroidní protizánětlivé léky, například kyselina acetylsalicylová nebo ibuprofen), heparin, imunosupresiva (například cyklosporin nebo takrolimus) a antibiotikum trimetoprim.
• Diuretika (močopudné léky, „tablety na odvodnění") mohou vést k nadměrným ztrátám vody z těla a k nízkému krevnímu tlaku (hypotenzi), zejména jsou-li užívány ve vysokých dávkách současně s přípravkem Telmisartan Teva.
• Digoxin
Účinek přípravku Telmisartan Teva může být oslaben oslaben současným užíváním léků ze skupiny NSAIDs (nesteroidních protizánětlivých léků, například kyseliny acetylsalicylové nebo ibuprofenu) nebo kortikosteroidy.
Telmisartan Teva může zesilovat účinek jiných léků, které jsou užívány k léčbě vysokého krevního tlaku a krevní tlak snižují.
Pokud trpíte onemocněním nazývaným orthostatická hypotenze (pokles krevního tlaku při změně polohy ze sedu nebo lehu do stoje, který způsobuje závrať nebo mdlobu), Váš stav se může zhoršit pokud užíváte Telmisartan Teva v kombinaci s:
• jinými přípravky k léčbě krevního tlaku
• Baklofenem (přípravek na uvolnění svalů)
• Amifostinem (podpůrný přípravek užívaný během ozařování při léčbě nádorů)
• Alkoholem
• Barbituráty (přípravky na spaní)
• Narkotickými léky proti bolesti
• Antidepresivy
Těhotenství a kojení Těhotenství
Musíte sdělit svému lékaři, pokud se domníváte, že jste (nebo můžete být) těhotná. Lékař Vám obvykle poradí přestat s užíváním přípravku Telmisartan Teva dříve než otěhotníte nebo jakmile zjistíte, že jste těhotná a doporučí užívat jiný lék místo přípravku Telmisartan Teva. Přípravek Telmisartan Teva se nedoporučuje v časném těhotenství a nesmí se užívat, jestliže jste těhotná déle než 3 měsíce, protože může v období po třetím měsíci těhotenství způsobit při užívání závažné poškození dítěte.
Kojení
Poraďte se s lékařem, pokud kojíte nebo začínáte s kojením. Telmisartan Teva se nedoporučuje u kojících matek a lékař Vám zřejmě zvolí jinou léčbu, pokud si budete přát kojit, zejména u novorozenců nebo předčasně narozených dětí.
Řízení dopravních prostředků a obsluha strojů
Někteří lidé mohou při užívání přípravku Telmisartan Teva cítit závrať nebo únavu. Pokud pociťujete závrať nebo únavu, neřiďte dopravní prostředky a neobsluhujte stroje.
Telmisartan Teva obsahuje sorbitol.
Jestliže trpíte nesnášenlivostí některých cukrů, poraďte se před užíváním přípravku Telmisartan Teva s lékařem.
3. Jak se Telmisartan Teva užívá
Přípravek Telmisartan Teva vždy užívejte přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka přípravku Telmisartan Teva je jedna tableta denně. Snažte se užívat tablety každý den ve stejnou dobu. Telmisartan Teva můžete užívat s jídlem nebo bez něj. Tablety je třeba spolknout a zapít vodou nebo něj akým j iným nealkoholickým nápoj em. Pokud V ám lékař neřekne j inak, j e důležité, abyste užívali přípravek Telmisartan Teva každý den. Pokud se domníváte, že je účinek přípravku Telmisartan Teva příliš silný nebo slabý, poraďte se se svým lékařem nebo lékárníkem.
Při léčbě vysokého krevního tlaku je obvyklá dávka přípravku Telmisartan Teva pro většinu pacientů jedna 40 mg tableta denně, která Váš krevní tlak udržuje pod kontrolou 24 hodin. Váš lékař Vám doporučil dávku zvýšit na 80 mg denně. Eventuálně lze přípravek Telmisartan Teva užívat v kombinaci s diuretiky („tablety na odvodnění“) jako je hydrochlorothiazid, u něhož bylo prokázáno, že zesiluje účinek přípravku Telmisartan Teva na snížení krevního tlaku.
Ke snížení výskytu srdečně-cévních příhod je obvyklá dávka přípravku Telmisartan Teva jedna tableta 80 mg jednou denně. Při zahájení preventivní léčby přípravkem Telmisartan Teva 80 mg by měl být často měřen krevní tlak.
Pokud trpíte poruchou činnosti jater, pak by obvyklá dávka neměla přesáhnout 40 mg jednou denně. Jestliže jste užil(a) více přípravku Telmisartan Teva, než jste měl(a)
Jestliže jste nedopatřením užil(a) příliš mnoho tablet, poraďte se ihned se svým lékařem, lékárníkem, nebo na pohotovostním oddělení nejbližší nemocnice.
Jestliže jste zapomněl(a) užít přípravek Telmisartan Teva
Jestliže jste zapomněl(a) užít dávku přípravku Telmisartan Teva, nedělejte si starosti. Vezměte ji, jakmile si vzpomenete, a poté pokračujte jako dříve. Jestliže tabletu jeden den nevezmete, vezměte si normální dávku následující den. Nezdvojujte následující dávku, abyste nahradil(a) vynechanou dávku.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento léčivý přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Některé nežádoucí účinky mohou být závažné a vyžadují okamžitou lékařskou pomoc:
Musíte okamžitě navštívit lékaře, pokud zaznamenáte některý z následujících příznaků:
Sepse (často nazývaná "otrava krve", je závažná infekce se zánětlivou odpovědí celého těla obvykle spojená s vysokými horečkami, horkostí, zarudlou kůží, zvýšenou srdeční frekvencí, zrychleným dýcháním, změnami mentálního stavu, otoky a nízkým krevním tlakem), rychlý otok kůže a sliznic (angioedém); tyto nežádoucí účinky jsou vzácné (mohou se vyskytnout u 1 pacienta z 1000), ale jsou extrémně závažné a pacienti by měli tento přípravek přestat užívat a okamžitě navštívit lékaře. Pokud se tyto nežádoucí účinky neléčí, mohou vést k úmrtí.
Další možné nežádoucí účinky telmisartanu:
Časté nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 10):
Nízký krevní tlak (hypotenze) u pacientů užívajících přípravek ke snížení výskytu srdečně-cévních příhod.
Méně časté nežádoucí účinky (mohou se vyskytnout u 1 pacienta ze 100):
Infekce močových cest, infekce horních cest dýchacích (například bolesti v krku, zánět vedlejších nosních dutin - sinusitida, běžné nachlazení), nedostatek červených krvinek (anémie), vysoká hladina draslíku, potíže při usínání, pocity smutku (deprese), mdloba (synkopa), pocit točení hlavy (závrať), zpomalení srdeční činnosti (bradykardie), nízký krevní tlak (hypotenze) u pacientů léčených pro vysoký krevní tlak, závrať po postavení (ortostatická hypotenze), zkrácený dech (dušnost), kašel, bolesti břicha, průjem, pocit nepohody v břiše (břišní diskomfort), otok, zvracení, svědění, zvýšené pocení, poléková vyrážka, bolesti zad, svalové křeče, bolesti svalů (myalgie), zhoršení funkce ledvin včetně náhlého selhání ledvin, bolesti na hrudi, pocity slabosti a zvýšená hladina kreatininu v krvi.
Vzácné nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 1000):
Zvýšení určitého druhu bílých krvinek (eozinofílie), pokles počtu krevních destiček (trombocytopenie), závažné alergické reakce (anafylaktická reakce), alergické reakce (například vyrážka, svědění, potíže s dechem, sípání, otok tváře nebo nízký krevní tlak), nízká hladina krevního cukru (u diabetických pacientů), pocity úzkosti, ospalost, poruchy zraku, zrychlená srdeční činnost (tachykardie), sucho v ústech, žaludeční nevolnost, poruchy vnímání chuti (dysgeuzie), abnormální funkce jater (tento nežádoucí účinek se vyskytuje s větší pravděpodobností u japonských pacientů), ekzém (porucha kůže), zarudnutí kůže, kopřivka (urticaria), závažná poléková vyrážka, bolesti kloubů (artralgie), bolesti končetin, bolesti šlach, onemocnění připomínající chřipku, pokles hemoglobinu (krevní bílkovina), zvýšená hladina kyseliny močové, jaterních enzymů nebo kreatinfosfokinázy v krvi.
Velmi vzácné nežádoucí účinky (mohou se vyskytnout u 1 pacienta z 10 000):
Progresivní zjizvení plicní tkáně (intersticiální plicní nemoc).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Telmisartan Teva uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Tento léčivý přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na krabičce a blistru za „Použitelné do:“ Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co Telmisartan Teva obsahuje
- Léčivou látkou je telmisartan. Jedna tableta přípravku Telmisartan Teva obsahuje 80 mg telmisartanum.
- Pomocnými látkami jsou mikrokrystalická celulosa (Avicel PH 102), sodná sůl karboxymethylškrobu (Typ A), poloxamer, meglumin, povidon (PVP K-30), sorbitol (E420) a magnesium-stearát.
Jak Telmisartan Teva vypadá a co obsahuje toto balení
Telmisartan Teva 80 mg jsou bílé až téměř bílé, oválné tablety s vyraženým číslem „93“ na jedné straně a s číslem „7460“ na straně druhé.
Telmisartan Teva je dodáván v odloupnutelných perforovaných jednodávkových Al/Al blistrech nebo perforovaných jednodávkových Al/Al blistrech, obsahujících 14x1, 28x1, 30x1, 40x1, 56x1, 60x1, 84x1, 90x1, 98x1, 100x1 tablet.
Telmisartan Teva je dodáván také v Al/Al blistrech obsahujících 30 tablet.
Na trhu nemusí být všechny velikosti balení.
Přečtěte si, prosím, návod jak vyjmout tabletu z blistru, který je umístěn na krabičce s odloupnutelnými blistry.
Držitel rozhodnutí o registraci
Teva B.V.
Swensweg 5 2031GA Haarlem Nizozemsko
Výrobce
TEVA Pharmaceutical Works Private Limited Company Pallagi út 13,
4042 Debrecen,
Maďarsko
nebo
TEVA Pharmaceutical Works Private Limited Company H-2100 Godollo,
Táncsics Mihály út 82 Maďarsko
nebo
TEVA UK Ltd Brampton Road,
Hampden Park,
Eastbourne,
East Sussex,
BN22 9AG Velká Británie
nebo
Pharmachemie B.V. Swensweg 5,
2031 GA, Haarlem, Nizozemsko
|
Další informace o tomto přípravku získáte |
u místního zástupce držitele rozhodnutí o registraci |
|
Belgie/Belgique/Belgien Teva Pharma Belgium N.V./S.A. Tel/Tél: +32 3 820 73 73 |
Luxembourg/Luxemburg Teva Pharma Belgium S.A. Belgien/Belgique Tél/Tel: +32 3 820 73 73 |
|
Btarapna TeBa OapMacmTHKtnc Etnrapua EOOfl Ten: +359 2 489 95 82 |
Magyarország Teva Gyógyszergyár Zrt. (TPW) Tel.: +36 1 288 64 00 |
|
Česká republika Teva Pharmaceuticals CR, s.r.o. Tel: +420 251 007 111 |
Malta Teva Pharmaceuticals Ireland L-Irlanda Tel: +355 51 321740 |
|
Danmark Teva Denmark A/S Tlf: +45 44 98 55 11 |
Nederland Teva Nederland B.V. Tel: +31 (0) 800 0228400 |
|
Deutschland Teva GmbH Tel: (49) 731 40208 |
Norge Teva Norway AS Tlf: +47 66 77 55 90 |
|
Eesti Teva Eesti esindus UAB Sicor Biotech Eesti filiaal Tel: +372 661 0801 |
Osterreich ratiopharm Arzneimittel Vertriebs-GmbH Tel: +43 1 97 00 7 |
|
EkXáSa Teva EAAág A.E. Tq^: +30 210 72 79 099 |
Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel.: +(48) 22 345 93 00 |
|
Espaňa Teva Pharma, S.L.U Tél: +(34) 91 387 32 80 |
Portugal Teva Pharma - Produtos Farmaceuticos Lda Tel: (351) 214 235 910 |
|
France Teva Santé Tél: +(33) 1 55 91 7800 |
Románia Teva Pharmaceuticals S.R.L Tel: +4021 230 65 24 |
|
Hrvatska Pliva Hrvatska d.o.o Tel: + 385 1 37 20 000 Ireland Teva Pharmaceuticals Ireland Tel: +353 (0)51 321 740 |
Slovenija Pliva Ljubljana d.o.o. Tel: +386 1 58 90 390 |
|
Ísland Ratiopharm Oy Finnland |
Slovenská republika Teva Pharmaceuticals Slovakia s.r.o. Tel: +(421) 2 5726 7911 |
Sími: +358 9 180 452 5900
Suomi/Finland
ratiopharm Oy Puh/Tel: +358 20 180 5900
Sverige
Teva Sweden AB Tel: +(46) 42 12 11 00
United Kingdom
Teva UK Limited Tel: +(44) 1977 628 500
Italia
Teva Italia S.r.l.
Tel: +(39) 028917981
Kúrcpog
Teva EXkáq A.E.
Ekká5a
Tnk: +30 210 72 79 099 Latvija
UAB Sicor Biotech filiale Latvija Tel: +371 67 784 980
Lietuva
UAB “Sicor Biotech”
Tel: +370 5 266 02 03
Tato příbalová informace byla naposledy revidována:
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
93