Simbrinza 10 Mg/Ml + 2 Mg/Ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
SIMBRINZA 10 mg/ml + 2 mg/ml oční kapky, suspenze
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje brinzolamidum 10 mg a brimonidini tartras 2 mg, což odpovídá brimonidinum
1,3 mg.
Pomocná látka se známým účinkem:
Jeden ml suspenze obsahuje 0,03 mg benzalkonium-chloridu.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Oční kapky, suspenze (oční kapky).
Bílá až krémově bílá homogenní suspenze, pH 6,5 (přibližně).
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Snížení zvýšeného nitroočního tlaku (NOT) u dospělých pacientů s glaukomem s otevřeným úhlem nebo oční hypertenzí, u nichž monoterapie nevede k dostatečnému snížení NOT (viz bod 5.1).
4.2 Dávkování a způsob podání
Dávkování
Použití u dospělých včetně starších osob
Doporučená dávka je jedna kapka přípravku SIMBRINZA do postiženého oka (očí) dvakrát denně.
Porucha _ funkce _ jater a/nebo ledvin
Přípravek SIMBRINZA nebyl hodnocen u pacientů s poruchou funkce jater, a proto se u této populace doporučuje postupovat opatrně (viz bod 4.4).
Přípravek SIMBRINZA nebyl hodnocen u pacientů s těžkou poruchou funkce ledvin (clearance kreatininu [CrCl] < 30 ml/min) ani u pacientů s hyperchloremickou acidózou. Jelikož brinzolamid, který je složkou přípravku SIMBRINZA, a jeho metabolity jsou vylučovány převážně ledvinami, je přípravek SIMBRINZA u těchto pacientů kontraindikován (viz bod 4.3).
Pediatrická _ populace
Bezpečnost a účinnost přípravku SIMBRINZA u dětí a dospívajících ve věku od 2 do 17 let nebyla stanovena. Nejsou dostupné žádné údaje. Přípravek SIMBRINZA se nedoporučuje u dětí a dospívajících (viz bod 4.4).
Přípravek SIMBRINZA se nesmí používat u novorozenců, kojenců a batolat ve věku do 2 let z důvodu bezpečnostních rizik (viz bod 4.3).
Způsob podání Oční podání.
Pacienty je třeba poučit, aby lahvičku před použitím dobře protřepali.
Při použití nazolakrimální okluze a uzavření očního víčka na dobu 2 minut se systémová absorpce snižuje.
To může vést ke snížení systémových nežádoucích účinků a ke zvýšení lokálního působení (viz bod 4.4).
Aby se zabránilo kontaminaci hrotu kapátka a roztoku, je třeba dbát na to, aby se hrot kapátka lahvičky nedotkl očního víčka, okolních tkání nebo jiných povrchů. Pacienty je třeba poučit, aby v době, kdy přípravek nepoužívají, uchovávali lahvičku pevně uzavřenou.
Přípravek SIMBRINZA lze používat souběžně s jinými topickými oftalmologickými léčivými přípravky ke snížení nitroočního tlaku. Při použití více než jednoho lokálního oftalmologika se musí léčivé přípravky podávat s odstupem nejméně 5 minut.
Při vynechání dávky se má v léčbě pokračovat další plánovanou dávkou. Dávka nemá přesáhnout 1 kapku do postiženého oka (očí) 2krát denně.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku(y) nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1 nebo na sulfonamidy (viz bod 4.4).
Pacienti léčení inhibitorem monoaminooxidázy (MAO) (viz bod 4.5).
Pacienti užívající antidepresiva, která ovlivňují noradrenergní přenos (např. tricyklická antidepresiva a mianserin) (viz bod 4.5).
Pacienti s těžkou poruchou funkce ledvin (viz bod 4.4).
Pacienti s hyperchloremickou acidózou.
Novorozenci, kojenci a batolata ve věku do 2 let (viz bod 4.4).
4.4 Zvláštní upozornění a opatření pro použití
Tento léčivý přípravek se nesmí podávat injekčně. Pacienty je třeba poučit, aby přípravek SIMBRINZA nepolykali.
Účinky na oko
Přípravek SIMBRINZA nebyl hodnocen u pacientů s glaukomem s úzkým úhlem a jeho použití u těchto pacientů se nedoporučuje.
Možný účinek brinzolamidu na funkci endotelu rohovky nebyl zkoumán u pacientů s poškozením rohovky (zejména u pacientů s nízkým počtem endoteliálních buněk). Přípravek nebyl hodnocen konkrétně u pacientů používajících kontaktní čočky. Doporučuje se tyto pacienty při používání brinzolamidu pečlivě sledovat, neboť inhibitory karboanhydrázy mohou ovlivňovat hydrataci rohovky a nošení kontaktních čoček by mohlo zvýšit riziko poškození rohovky. Doporučuje se pečlivě sledovat pacienty s poškozením rohovky, jako jsou pacienti s diabetem mellitem nebo dystrofií rohovky. Přípravek SIMBRINZA lze u pacientů používajících kontaktní čočky používat za podmínky pečlivého sledování (viz níže v bodu „Benzalkonium-chlorid“).
Brimonidin-tartarát může způsobovat oční alergické reakce. Při výskytu alergických reakcí je nutné léčbu ukončit. Při používání brimonidin-tartarátu byly hlášeny opožděné hypersenzitivní reakce očí, z nichž některé byly spojeny se zvýšením NOT.
Potenciální účinky po ukončení léčby přípravkem SIMBRINZA nebyly hodnoceny. Přestože nebyla hodnocena doba trvání účinků přípravku SIMBRINZA na snížení NOT, očekává se, že účinek brinzolamidu na snížení NOT bude trvat 5-7 dní. Účinek brimonidinu na snížení NOT může trvat i déle.
Systémové účinky
Přípravek SIMBRINZA obsahuje brinzolamid, sulfonamidový inhibitor karboanhydrázy, a přestože je podáván lokálně, vstřebává se systémově. Při lokálním podání se mohou vyskytnout stejné typy nežádoucích reakcí, jaké lze přisuzovat sulfonamidům. Objeví-li se známky závažných reakcí nebo hypersenzitivity, je nutné podávání tohoto léčivého přípravku ukončit.
Srdeční poruchy
Po podání přípravku SIMBRINZA byly u některých pacientů pozorovány malé poklesy krevního tlaku. Doporučuje se postupovat opatrně při souběžném používání přípravku SIMBRINZA s určitými léčivými přípravky, jako jsou antihypertenziva a/nebo srdeční glykosidy, nebo v případě pacientů se závažným nebo nestabilním a nekontrolovaným kardiovaskulárním onemocněním (viz bod 4.5).
Přípravek SIMBRINZA se má používat s opatrností u pacientů s depresí, cerebrální nebo koronární insuficiencí, Raynaudovým fenoménem, ortostatickou hypotenzí nebo obliterující trombangiitidou.
Poruchy acidobazické rovnováhy
Poruchy acidobazické rovnováhy byly hlášeny u perorálních inhibitorů karboanhydrázy. Přípravek SIMBRINZA obsahuje brinzolamid, inhibitor karboanhydrázy a vstřebává se systémově, přestože je podáván lokálně. Při lokálním podání se mohou vyskytnout stejné typy nežádoucích reakcí, jaké lze přisuzovat perorálním inhibitorům karboanhydrázy (tj. poruchy acidobazické rovnováhy) (viz bod 4.5).
Opatrnosti je třeba při použití u pacientů s rizikem poruchy funkce ledvin z důvodu možného rizika metabolické acidózy. Přípravek SIMBRINZA je kontraindikován u pacientů s těžkou poruchou funkce ledvin (viz bod 4.3).
Porucha funkce jater
Přípravek SIMBRINZA nebyl hodnocen u pacientů s poruchou funkce jater, a proto je třeba při léčbě těchto pacientů postupovat opatrně (viz bod 4.2).
Duševní bdělost
Perorální inhibitory karboanhydrázy mohou negativně ovlivnit schopnost vykonávat úkoly vyžadující duševní bdělost a/nebo tělesnou koordinaci u starších pacientů. Přípravek SIMBRINZA se vstřebává systémově, a proto může při lokálním podání dojít k systémové absorpci (viz bod. 4.7).
Benzalkonium-chlorid
Přípravek SIMBRINZA obsahuje benzalkonium-chlorid, který může způsobit podráždění oka a je o něm známo, že zabarvuje měkké kontaktní čočky. Je potřebné se vyhnout kontaktu s měkkými kontaktními čočkami. Pacienti musí být poučeni, aby si před aplikací přípravku SIMBRINZA vyjmuli kontaktní čočky a vyčkali 15 minut před opětovným nasazením kontaktních čoček do očí.
Bylo rovněž hlášeno, že benzalkonium-chlorid způsobil keratopathia punctata a/nebo toxickou ulcerózní keratopatii. Při častém nebo dlouhodobém používání je třeba pacienta pečlivě sledovat.
Pediatrická populace
Bezpečnost a účinnost přípravku SIMBRINZA u dětí a dospívajících ve věku od 2 do 17 let nebyla stanovena. Příznaky předávkování brimonidinem (včetně ztráty vědomí, hypotenze, hypotonie, bradykardie, hypotermie, cyanózy a apnoe) byly hlášeny u novorozenců, kojenců a batolat používajících oční kapky s brimonidinem v rámci léčby vrozeného glaukomu. Přípravek SIMBRINZA je proto kontraindikován u dětí ve věku do 2 let (viz bod 4.3).
Léčba dětí ve věku od 2 let (především dětí ve věku 2-7 let a/nebo s tělesnou hmotností < 20 kg) se nedoporučuje vzhledem k možnému riziku nežádoucích účinků souvisejících s centrálním nervovým systémem (viz bod. 4.9).
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Nebyly provedeny žádné specifické studie interakcí s přípravkem SIMBRINZA.
Přípravek SIMBRINZA je kontraindikován u pacientů užívajících inhibitory monoaminooxidázy a u pacientů léčených antidepresivy, která ovlivňují noradrenergní přenos (např. tricyklická antidepresiva a mianserin) (viz bod 4.3). Tricyklická antidepresiva mohou zastínit hypotenzní reakci oka na léčbu přípravkem SIMBRINZA.
V případě užívání látek tlumících centrální nervový systém (např. alkoholu, barbiturátů, opiátů, sedativ nebo anestetik) se doporučuje postupovat opatrně z důvodu možného aditivního či potencujícího účinku.
Nejsou k dispozici žádné údaje o hladině katecholaminů v oběhovém systému po podání přípravku SIMBRINZA. Doporučuje se však postupovat opatrně u pacientů užívajících léčivé přípravky, které mohou ovlivnit metabolismus a vychytávání cirkulujících aminů (např. inhibitory zpětného vychytávání chlorpromazinu, methylfenidátu, reserpinu, serotonin-noradrenalinu).
Přípravky ze třídy a-adrenergních agonistů (např. brimonidin-tartarát) mohou snížit pulz a krevní tlak. Po podání přípravku SIMBRINZA byly u některých pacientů pozorovány mírné poklesy krevního tlaku. Doporučuje se postupovat opatrně při souběžném používání takových léčivých přípravků, jako j sou antihypertenziva a/nebo srdeční glykosidy, s přípravkem SIMBRINZA.
Doporučuje se postupovat opatrně při zahajování (nebo změně dávkování) souběžné léčby systémovými léčivými přípravky (bez ohledu na jejich lékovou formu), které mohou interagovat s a-adrenergními agonisty nebo ovlivnit jejich účinek, tj. agonisty nebo antagonisty adrenergních receptorů (např. izoprenalinem, prazosinem).
Brinzolamid je inhibitor karboanhydrázy a vstřebává se systémově, přestože je podáván lokálně. Poruchy acidobazické rovnováhy byly hlášeny u perorálních inhibitorů karboanhydrázy. U pacientů používajících přípravek SIMBRINZA je nutné vzít v úvahu možnost interakcí.
U pacientů, kteří užívají perorálně inhibitor karboanhydrázy a topický brinzolamid, existuje potenciál k rozšíření známých systémových účinků inhibice karboanhydrázy. Souběžné podávání přípravku SIMBRINZA a perorálních inhibitorů karboanhydrázy se nedoporučuje.
Izoenzymy cytochromu P-450 zodpovědné za metabolismus brinzolamidu zahrnují enzymy CYP3A4 (hlavní), CYP2A6, CYP2B6, CYP2C8 a CYP2C9. Předpokládá se, že inhibitory enzymu CYP3A4, jako je ketokonazol, itrakonazol, klotrimazol, ritonavir a troleandomycin, budou prostřednictvím CYP3A4 inhibovat metabolismus brinzolamidu. Při souběžném podávání inhibitorů CYP3A4 se doporučuje postupovat opatrně. Kumulace brinzolamidu je však nepravděpodobná, neboť je vylučován převážně ledvinami. Brinzolamid není inhibitorem izoenzymů cytochromu P-450.
4.6 Fertilita, těhotenství a kojení
Údaje o podávání přípravku SIMBRINZA těhotným ženám jsou omezené nebo nejsou k dispozici. Brinzolamid byl po systémovém podání teratogenní u potkanů, ne však u králíků. Studie reprodukční toxicity na zvířatech nenaznačují přímé škodlivé účinky. Ve studiích na zvířatech prostupoval brimonidin placentou a v omezené míře vstupoval do fetálního oběhu. Podávání přípravku SIMBRINZA se v těhotenství a u žen ve fertilním věku, které nepoužívají antikoncepci, nedoporučuje
Kojení
Není známo, zda se lokální přípravek SIMBRINZA vylučuje do lidského mateřského mléka. Dostupné farmakodynamické/toxikologické údaje u zvířat prokázaly, že se brinzolamid po perorálním podání vylučuje do mateřského mléka v minimální míře. Perorálně podávaný brimonidin se vylučuje do mateřského mléka. Přípravek SIMBRINZA se nemá u kojících žen používat.
Fertilita
Neklinické údaje neprokazují žádné účinky brinzolamidu nebo brimonidinu na fertilitu. O účinku přípravku SIMBRINZA na fertilitu u lidí po lokálním očním podání nejsou k dispozici žádné údaje.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Přípravek SIMBRINZA má středně závažný vliv na schopnost řídit nebo obsluhovat stroje.
Přípravek SIMBRINZA může způsobit závrať, únavu a/nebo ospalost, což může negativně ovlivnit schopnost řídit nebo obsluhovat stroje.
Přechodně rozmazané vidění nebo jiné poruchy vidění mohou ovlivnit schopnost řídit nebo obsluhovat stroje. Pokud se po nakapání přípravku objeví rozmazané vidění, musí pacient vyčkat, dokud se vidění neprojasní, a teprve potom může řídit nebo obsluhovat stroje.
Perorální inhibitory karboanhydrázy mohou u pacientů pokročilejšího věku negativně ovlivnit schopnost vykonávat úkoly vyžadující duševní bdělost a/nebo tělesnou koordinaci (viz bod 4.4).
4.8 Nežádoucí účinky
Shrnutí bezpečnostního profilu
V klinických hodnoceních s přípravkem SIMBRINZA v dávkování dvakrát denně byly nej častějšími nežádoucími účinky oční hyperemie a oční alergická reakce, které se vyskytly přibližně u 6-7 % pacientů, a dysgeuzie (hořká nebo neobvyklá chuť v ústech po nakapání přípravku), která se vyskytla přibližně u 3 % pacientů. Bezpečnostní profil přípravku SIMBRINZA byl obdobný jako u jeho jednotlivých složek (brinzolamidu 10 mg/ml a brimonidinu 2 mg/ml).
Tabulkový přehled nežádoucích účinků
Následující nežádoucí účinky byly hlášeny během klinických studií s přípravkem SIMBRINZA v dávkování dvakrát denně a během klinických studií s jednotlivými složkami, brinzolamidem a brimonidinem, a po jejich uvedení na trh. Nežádoucí účinky jsou seřazeny podle následující konvence: velmi časté (> 1/10), časté (> 1/100 až < 1/10), méně časté (> 1/1000 až < 1/100), vzácné (> 1/10 000 až < 1/1000), velmi vzácné (<1/10 000, nebo není známo (podle dostupných údajů nelze odhadnout). V každé skupině četností jsou nežádoucí účinky seřazeny podle klesající závažnosti.
|
Třída orgánového systému |
Nežádoucí účinky |
|
Infekce a infestace |
Méně časté: nazofaryngitida2, faryngitida2, sinusitida2 Není známo: rinitida2 |
|
Poruchy krve a lymfatického systému |
Méně časté: snížený počet erytrocytů2, zvýšená hladina chloridů v krvi2 |
|
Poruchy imunitního systému |
Méně časté: hypersenzitivita3 |
|
Psychiatrické poruchy |
Méně časté: apatie2, deprese2,3, depresivní nálada2, insomnie1, snížené libido2, noční můry2, nervozita2 |
|
Poruchy nervového systému |
Časté: somnolence1, závrať3, dysgeuzie1 Méně časté: bolest hlavy1, motorická dysfunkce2, amnézie2, poruchy paměti2, parestezie2 Velmi vzácné: synkopa3 Není známo: tremor2, hypestezie2, ageuzie2 |
|
Poruchy oka |
Časté: oční alergie , keratitida , bolest oka , oční diskomfort, rozmazané vidění1, abnormální vidění3, oční hyperemie1, zblednutí spojivek3 Méně časté: eroze rohovky1, edém rohovky2, blefaritida1, rohovková depozita (rohovkové precipitáty) 1, onemocnění spojivky (papily) 1, fotofobie1, fotopsie2, otok oka2, edém očního víčka1, edém spojivky1, suché oko1, sekrece z oka1, snížená zraková ostrost2, zvýšené slzení1, pterygium2, erytém očního víčka1, meibomianitida2, diplopie2, oslnění 2, hypestezie oka2, sklerální pigmentace2, subkonjunktivální cysta2, abnormální pocit v oku1, astenopie1 Velmi vzácné: uveitida3, mióza3 Není známo: poruchy vidění2, madaróza2 |
|
Poruchy ucha a labyrintu |
Méně časté: vertigo1, tinitus2 |
|
Srdeční poruchy |
Méně časté: kardiorespirační tíseň2, angina pectoris2, arytmie3, |
|
Třída orgánového systému |
Nežádoucí účinky |
|
palpitace , , nepravidelná srdeční frekvence , bradykardie , , tachykardie3 | |
|
Cévní poruchy |
Méně časté: hypotenze1 Velmi vzácné: hypertenze3 |
|
Respirační, hrudní a mediastinální poruchy |
Méně časté: dyspnoe2, bronchiální hyperaktivita2, faryngolaryngeální bolest2, suché hrdlo1, kašel2, epistaxe2, překrvení horních cest dýchacích2, nazální překrvení1, rinorea2, podráždění hrdla2, sucho v nose1, postnazální zatékání hlenu1, kýchání2 Není známo: astma2 |
|
Gastrointestinální poruchy |
V 1 Časté: sucho v ústech Méně časté: dyspepsie1, ezofagitida2, břišní diskomfort1, průjem2, zvracení2, nauzea2, častá stolice2, flatulence2, orální hypestezie2, orální parestezie 1 |
|
Poruchy jater a žlučových cest |
Není známo: abnormální test funkce jater 2 |
|
Poruchy kůže a podkožní tkáně |
Méně časté: kontaktní dermatitida1, kopřivka2, vyrážka2, makulopapulózní vyrážka2, generalizovaný pruritus2, alopecie2, napětí kůže2 Není známo: edém obličeje , dermatitida , , erytém , |
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Méně časté: bolest zad2, svalové spasmy2, myalgie2 Není známo: artralgie2, bolest končetin2 |
|
Poruchy ledvin a močových cest |
Méně časté: renální bolest2 Není známo: polakisurie2 |
|
Poruchy reprodukčního systému a prsu |
Méně časté: erektilní dysfunkce2 |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté: bolest2, hrudní diskomfort2, abnormální pocit2, pocit nervozity2, podrážděnost2, reziduum léku1 Není známo: bolest na hrudi2, periferní edém2,3 |
1 nežádoucí účinek pozorovaný u přípravku SIMBRINZA
2 další nežádoucí účinek pozorovaný při monoterapii brinzolamidem
3 další nežádoucí účinek pozorovaný při monoterapii brimonidinem
Popis vybraných nežádoucích účinků
Dysgeuzie byla nejčastější systémovou nežádoucí reakcí spojenou s používáním přípravku SIMBRINZA (3,4 %). Dysgeuzie je pravděpodobně způsobena průtokem očních kapek do nazofaryngu slzným kanálkem a je převážně přisuzována brinzolamidové složce přípravku SIMBRINZA. Nazolakrimální okluze nebo jemné zavření očního víčka po nakapání přípravku přispívá ke snížení výskytu tohoto účinku (viz bod 4.2).
Přípravek SIMBRINZA obsahuje brinzolamid, který je sulfonamidovým inhibitorem karboanhydrázy se systémovou absorpcí. Hematologické účinky a účinky na gastrointestinální trakt, nervový systém, ledviny a metabolismus jsou obecně spojeny se systémovými inhibitory karboanhydrázy. Při lokálním podání se mohou vyskytnout stejné typy nežádoucích reakcí, jaké lze přisuzovat perorálním inhibitorům karboanhydrázy.
Nežádoucí účinky často spojené s brimonidinovou složkou přípravku SIMBRINZA zahrnují rozvoj očních reakcí alergického typu, únavu a/nebo ospalost a sucho v ústech. Použití brimonidinu bylo spojeno s minimálními poklesy krevního tlaku. Někteří pacienti, kteří používali přípravek SIMBRINZA, zaznamenali obdobné poklesy krevního tlaku, jaké byly pozorovány při použití brimonidinu v monoterapii.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Při předávkování přípravkem SIMBRINZA je nutná symptomatická a podpůrná léčba. U pacienta je potřeba udržovat dýchací cesty průchodné.
V důsledku brinzolamidové složky přípravku SIMBRINZA může dojít k elektrolytové nerovnováze, rozvoji acidotického stavu a možným účinkům na nervový systém. Musí se sledovat sérové hladiny elektrolytů (především draslíku) a hladiny pH krve.
Informace o náhodném požití brimonidinové složky přípravku SIMBRINZA u dospělých pacientů jsou velmi omezené. Jedinou dosud hlášenou nežádoucí příhodou byla hypotenze. Bylo hlášeno, že po hypotenzní epizodě následovala hypertenze po náhlém přerušení léčby.
Bylo hlášeno, že při předávkování po perorálním podání jiných a-2-agonistů se objevily příznaky, jako jsou hypotenze, astenie, zvracení, letargie, sedace, bradykardie, arytmie, mióza, apnoe, hypotonie, hypotermie, respirační deprese a záchvat.
Pediatrická populace
U pediatrických subjektů byly hlášeny závažné nežádoucí účinky po neúmyslném požití brimonidinové složky přípravku SIMBRINZA. Subjekty zaznamenaly příznaky deprese centrálního nervového systému, obvykle dočasné kóma nebo nízkou úroveň vědomí, letargii, somnolenci, hypotonii, bradykardii, hypotermie, bledost, respirační depresi a apnoi, a vyžadovaly přijetí na jednotku intenzivní péče s intubací, pokud byla indikována. U všech subjektů bylo hlášeno úplné vyléčení, obvykle do 6-24 hodin.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Oftalmologika, Antiglaukomatika a miotika ATC kód: S01EC54 Mechanismus účinku
Přípravek SIMBRINZA obsahuje dvě léčivé látky: brinzolamid a brimonidin-tartarát. Tyto dvě složky potlačují produkci komorové vody z řasnatého tělíska v oku, čímž u pacientů s glaukomem s otevřeným úhlem a oční hypertenzí snižují nitrooční tlak (NOT). Přestože jak brinzolamid, tak i brimonidin snižují NOT tím, že potlačují tvorbu komorové vody, mají odlišný mechanismus účinku.
Brinzolamid působí prostřednictvím inhibice enzymu karboanhydrázy (CA-II) v epitelu řasnatého tělíska, který snižuje produkci hydrogenuhličitanových iontů, s následným omezením transportu sodíku a tekutiny přes epitel řasnatého tělíska, což vede ke snížené produkci komorové vody. Brimonidin je a-2-adrenergní agonista, který inhibuje enzym adenylátcyklázu a potlačuje tvorbu komorové vody závislou na c-AMP. Kromě toho podání brimonidinu vede ke zvýšení odtoku uveosklerální cestou.
Farmakodynamické účinky
Klinická účinnost a bezpečnost
Šestiměsíční kontrolovaná klinická studie sledující příspěvek jednotlivých složek přípravku zahrnovala 560 pacientů s glaukomem s otevřeným úhlem (včetně pseudoexfoliace nebo pigmentové disperze) a/nebo oční hypertenzí, u nichž bylo podle názoru zkoušejícího onemocnění nedostatečně kontrolováno monoterapií nebo již bylo léčeno několika léčivými přípravky na snížení nitroočního tlaku a kteří měli na počátku studie střední hodnotu denního NOT 26 mmHg. U těchto pacientů byl účinek na snížení průměrné hodnoty denního NOT při léčbě přípravkem SIMBRINZA s dávkováním dvakrát denně přibližně 8 mmHg. U přípravku SIMBRINZA byla pozorována statisticky superiorní snížení průměrné hodnoty denního NOT v porovnání s brinzolamidem 10 mg/ml nebo brimonidinem 2 mg/ml v dávkování dvakrát denně při všech návštěvách v průběhu celé studie (obrázek č. 1).
Obrázek č. 1 Změna průměrné hodnotya denního (9:00, +2 hod., +7 hod.) NOT oproti hodnotě na počátku studie (mmHg) - studie účinku složek přípravku
□ SIMBRINZA Brinzolamide □ Brtmomdine
Týden 2
n=191 n=191 n=174
Týden 6
n=188 n=189 n=172
Měsíc 3
n=176 n=182 n=161
Měsíc 6
11=160 n=178 n=145
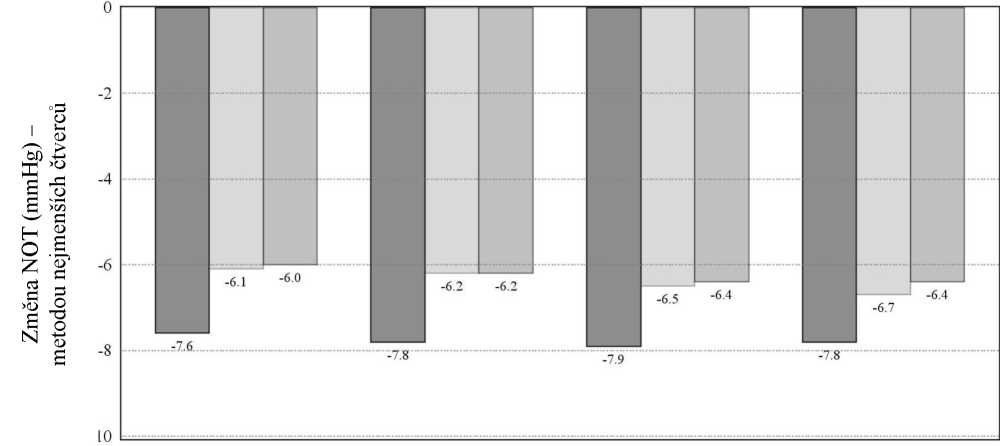
a Průměrné hodnoty dosažené metodou nejmenších čtverců odvozené ze statistického modelu platného pro pracoviště studie, úrovně NOT v 9:00 na počátku studie a korelovaných měření NOT u jednotlivých pacientů.
Všechny rozdíly v léčbě (přípravek SIMBRINZA versus jednotlivé složky přípravku) byly statisticky významné s p = 0,0001 nebo nižší.
Průměrné snížení NOT v každém časovém bodě při každé návštěvě oproti hodnotě na počátku studie bylo u přípravku SIMBRINZA vyšší (6 až 9 mmHg) než u monoterapie brinzolamidem (5 až 7 mmHg) nebo brimonidinem (4 až 7 mmHg). Průměrné procentní snížení NOT od počátku studie se u přípravku SIMBRINZA pohybovala od 23 do 34 %. Procentní podíly pacientů s naměřenými hodnotami NOT méně než 18 mmHg byly vyšší ve skupině léčené přípravkem SIMBRINZA než ve skupině léčené brinzolamidem při 9 z 12 vyšetření až do 6. měsíce a byly vyšší ve skupině léčené přípravkem SIMBRINZA než ve skupině léčené brimonidinem při všech 12 vyšetřeních až do 6. měsíce. V časovém bodě +2 hod. (doba odpovídající rannímu maximu účinnosti) pro návštěvu hodnotící primární parametr účinnosti ve 3. měsíci byl procentní podíl pacientů s NOT nižším než 18 mmHg 61,7 % ve skupině léčené přípravkem SIMBRINZA, 40,1 % ve skupině léčené brinzolamidem a 40 % ve skupině léčené brimonidinem.
Šestiměsíční kontrolovaná klinická studie non-inferiority zahrnovala 890 pacientů s glaukomem s otevřeným úhlem (včetně pseudoexfoliace nebo pigmentové disperze) a/nebo oční hypertenzí, u nichž bylo podle názoru zkoušejícího onemocnění nedostatečně kontrolováno monoterapií nebo již bylo léčeno několika léčivými přípravky na snížení nitroočního tlaku a kteří měli na počátku studie střední hodnotu denního NOT 26 až 27 mmHg. U těchto pacientů byla při všech návštěvách v průběhu celé studie prokázána non-inferiorita přípravku SIMBRINZA s ohledem na snížení střední hodnoty denního NOT oproti hodnotě na počátku studie v porovnání se souběžným podáváním brinzolamidu 10 mg/ml + brimonidinem 2 mg/ml (tabulka č. 1).
Tabulka č. 1. Porovnání změny průměrné hodnoty denního NOT (mmHg) oproti hodnotě na počátku studie studie non-inferiority
|
Návštěva |
SIMBRINZA, Průměr3 |
Brinzolamid + brimonidin, Průmět |
Rozdíl, Průměr (95% IS) |
|
Týden 2 |
-8,4 (n = 394) |
-8,4 (n = 384) |
-0,0 (-0,4; 0,3) |
|
Týden 6 |
-8,5 (n = 384) |
-8,4 (n = 377) |
-0,1 (-0,4; 0,2) |
|
Měsíc 3 |
-8,5 (n = 384) |
-8,3 (n = 373) |
-0,1 (-0,5; 0,2) |
|
Měsíc 6 |
-8,1 (n = 346) |
-8,2 (n = 330) |
0,1 (-0,3; 0,4) |
a Průměrné hodnoty dosažené metodou nejmenších čtverců odvozené ze statistického modelu platného pro pracoviště studie, úrovně NOT v 9:00 na počátku studie a korelovaných měření NOT u jednotlivých pacientů.
Průměrné snížení NOT v každém časovém bodě při každé návštěvě oproti hodnotě na počátku studie byla u přípravku SIMBRINZA i u jednotlivých složek podávaných souběžně obdobná (7 až 10 mmHg). Průměrné procentní snížení NOT od počátku studie se u přípravku SIMBRINZA pohybovala od 25 do 37 %. Procentní podíly pacientů s naměřenými hodnotami NOT méně než 18 mmHg byly v jednotlivých časových bodech při všech návštěvách ve studii až do 6. měsíce obdobné ve skupině léčené přípravkem SIMBRINZA i ve skupině léčené brinzolamidem + brimonidinem. V časovém bodě +2 hod. (doba odpovídající rannímu maximu účinnosti) pro návštěvu hodnotící primární parametr účinnosti ve 3. měsíci byl procentní podíl pacientů s NOT nižším než 18 mmHg 65,6% ve skupině léčené přípravkem SIMBRINZA a 63,7 % ve skupině léčené brinzolamidem + brimonidinem.
Pediatrická populace
Evropská agentura pro léčivé přípravky udělila výjimku z povinnosti předložit výsledky studií s přípravkem SIMBRINZA u všech podskupin pediatrické populace v indikaci léčby glaukomu a oční hypertenze (informace o použití v pediatrické populaci viz bod 4.2).
5.2 Farmakokinetické vlastnosti
Absorpce
Brinzolamid se po lokálním očním podání absorbuje rohovkou. Je rovněž absorbován do systémového oběhu, kde dochází k silné vazbě na karboanhydrázu v erytrocytech. Jeho plazmatické koncentrace jsou velmi nízké. Poločas eliminace z plné krve je u člověka delší (> 100 dní) v důsledku vazby na karboanhydrázu v erytrocytech.
Brimonidin se po lokálním podání rychle vstřebává do oka. U králíků bylo maximálních koncentrací v oku ve většině případů dosaženo za méně než jednu hodinu. Maximální plazmatické koncentrace u člověka jsou < 1 ng/ml a jsou dosahovány do < 1 hodinu. Plazmatické hladiny klesají s poločasem přibližně 2-3 hodiny. Při dlouhodobém podávání nedochází k žádné akumulaci.
V klinické studii při očním podání porovnávající systémovou farmakokinetiku přípravku SIMBRINZA podávaného dvakrát nebo třikrát denně s brinzolamidem a brimonidinem podávanými samostatně ve stejných dvou dávkovacích schématech byla farmakokinetika brinzolamidu a N-desethylbrinzolamidu při ustálených hladinách v plné krvi obdobná u kombinovaného přípravku i brinzolamidu samotného. Podobně byla farmakokinetika brimonidinu z kombinovaného přípravku při ustálených plazmatických hladinách obdobná jako u brimonidinu podávaného samostatně s výjimkou léčebné skupiny používající přípravek SIMBRINZA dvakrát denně, kde byla střední hodnota AUC0-12 hod. přibližně o 25 % nižší než při podávání samotného brimonidinu dvakrát denně.
Distribuce
Studie na králících prokázaly maximální koncentrace brinzolamidu v oku po lokálním podání ve tkáních předních segmentů, jako j sou rohovka, spojivka, komorová voda, duhovka a řasnaté tělísko. V očních tkáních zůstává po delší dobu v důsledku vazby na karboanhydrázu. Brinzolamid se středně váže (přibližně ze 60 %) na humánní plazmatické proteiny.
Brimonidin vykazuje afinitu k pigmentovým očním tkáním, především duhovce a řasnatému tělísku, v důsledku jeho známé schopnosti vázat se na melanin. Klinické i neklinické údaje o bezpečnosti však ukazují, že při dlouhodobém podávání je brimonidin dobře snášen a je bezpečný.
Biotransformace
Brinzolamid se metabolizuje prostřednictvím izoenzymů jaterního cytochromu P-450, konkrétně CYP3A4, CYP2A6, CYP2B6, CYP2C8 a CYP2C9. Primárním metabolitem je N-desethylbrinzolamid následovaný N-desmethoxypropyl a O-desmethyl metabolitem, jakož i analogem kyseliny N-propionové, který vzniká oxidací N-propylového bočního řetězce O-desmethyl-brinzolamidu. Brinzolamid a N-desethylbrinzolamid neinhibují izoenzymy cytochromu P-450 při koncentracích nejméně 100násobně vyšších než jsou maximální hladiny v systémovém oběhu.
Brimonidin je výrazně metabolizován jaterní aldehydoxidázou, přičemž vznikají 2-oxobrimonidin, 3-oxobrimonidin a 2,3-dioxobrimonidin, které jsou jeho nejdůležitějšími metabolity. Bylo rovněž pozorováno oxidativní štěpení imidazolinového kruhu na 5-bromo-6-guanidinochinoxalin.
Eliminace
Brinzolamid je primárně eliminován močí v nezměněné formě. U člověka odpovídá brinzolamid v moči přibližně 60 % dávky a N-desethylbrinzolamid přibližně 6 % dávky. Údaje o potkanech prokázaly částečné vylučování žlučí (přibližně 30 %), především ve formě metabolitů.
Brimonidin je primárně eliminován močí ve formě metabolitů. U potkanů a opic dosahovaly metabolity v moči 60 až 75 % perorální nebo intravenózní dávky.
Linearita/nelinearita
Farmakokinetika brinzolamidu je ve své podstatě nelineární v důsledku saturabilní vazby na karboanhydrázu v plné krvi a různých tkáních. Expozice v ustáleném stavu se nezvyšuje úměrně dávce.
Naopak brimonidin vykazuje lineární farmakokinetiku v celém rozsahu klinických terapeutických dávek.
Farmakokinetický/farmakodynamický vztah
Přípravek SIMBRINZA je určen k lokálnímu působení uvnitř oka. Vyhodnocení expozice u člověka při očním podání účinných dávek není možné uskutečnit. Farmakokinetický/farmakodynamický vztah u člověka pro snížení NOT nebyl stanoven.
Další zvláštní populace
Studie s přípravkem SIMBRINZA zaměřené na stanovení efektu věku, rasy a poruchy funkce ledvin nebo jater nebyly provedeny. Studie brinzolamidu s japonskými a nejaponskými subjekty prokázala, že systémová farmakokinetika byla v obou skupinách obdobná. Ve studii brinzolamidu se subjekty s poruchou funkce ledvin byl prokázán 1,6násobný až 2,8násobný nárůst systémové expozice u brinzolamidu a N-desethylbrinzolamidu mezi subjekty s normální funkcí ledvin a subjekty se středně těžkou poruchou funkce ledvin. Toto zvýšení ustálených koncentrací látek souvisejících s lékem v erytrocytech neinhibovalo aktivitu karboanhydrázy erytrocytech v míře, která je spojena se systémovými nežádoucími účinky. Kombinovaný přípravek se však nedoporučuje u pacientů s těžkou poruchou funkce ledvin (clearance kreatininu < 30 ml/min).
Hodnoty Cmax, AUC a eliminační poločas brimonidinu jsou u subjektů pokročilejšího věku (> 65 let) obdobné jako u mladých dospělých. Vliv poruchy funkce ledvin a jater na systémovou farmakokinetiku brimonidinu nebyl hodnocen. Vzhledem k nízké systémové expozici brimonidinu po lokálním očním podání se předpokládá, že změny plazmatické expozice nebudou klinicky relevantní.
Pediatrická populace
Systémová farmakokinetika brinzolamidu a brimonidinu podávaných samostatně nebo v kombinaci pediatrickým pacientům nebyla hodnocena.
5.3 Předklinické údaje vztahující se k bezpečnosti
Brinzolamid
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a hodnocení karcinogenního potenciálu neodhalily žádné zvláštní riziko pro člověka.
Účinky v neklinických studiích reprodukční a vývojové toxicity byly pozorovány pouze po expozicích dostatečně převyšujících maximální expozici u člověka, což svědčí o malém významu při klinickém použití. U králíků neodhalily perorální, pro matku toxické dávky brinzolamidu ve výši až 6 mg/kg/den (261násobek doporučené denní klinické dávky 23 pg/kg/den) žádný účinek na vývoj plodu. U potkanů vedly dávky 18 mg/kg/den (783násobek doporučené denní klinické dávky), nikoli však dávky 6 mg/kg/den, k mírně omezené osifikaci lebky a hrudní kosti plodů. Tato zjištění byla spojena s metabolickou acidózou se sníženým přírůstkem tělesné hmotnosti u samic a sníženou hmotností plodů. S dávkou související poklesy hmotnosti plodů byly pozorovány u potomků samic, kterým byla podávána dávka 2 až 18 mg/kg/den. Během laktace byla dávka, při níž nedocházelo k žádným nežádoucím účinkům u potomků, 5 mg/kg/den.
Brimonidin
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity, hodnocení karcinogenního potenciálu, reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Benzalkonium-chlorid
Propylenglykol
Karbomer 974 P
Kyselina boritá
Mannitol
Chlorid sodný
Tyloxapol
Kyselina chlorovodíková a/nebo hydroxid sodný (pro úpravu pH)
Čištěná voda
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
2 roky.
4 týdny po prvním otevření.
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
8ml oválné lahvičky z neprůhledného polyethylenu s nízkou hustotou (LDPE) s kapátkem z LDPE a bílým polypropylenovým šroubovacím uzávěrem (Drop-Tainer) obsahující 5 ml suspenze.
Krabička obsahuje 1 nebo 3 lahvičky.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Žádné zvláštní požadavky na likvidaci.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Alcon Laboratories (UK) Ltd Frimley Business Park Frimley, Camberley Surrey GU16 7SR Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/14/933/001-002
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace:
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
A. VÝROBCE ODPOVĚDNÝ /VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE ODPOVĚDNÝ /VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce odpovědného/výrobců odpovědných za propouštění šarží
Alcon-Couvreur N.V.
Rijksweg 14 BE-2870 Puurs Belgie
nebo
Alcon Cusí SA Camil Fabra 58 08320 El Masnou (Barcelona)
Španělsko
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
• Pravidelně aktualizované zprávy o bezpečnosti
Držitel rozhodnutí o registraci předloží první pravidelně aktualizovanou zprávu o bezpečnosti pro tento léčivý přípravek do 6 měsíců od jeho registrace. Držitel rozhodnutí o registraci dále předkládá pravidelně aktualizované zprávy o bezpečnosti pro tento léčivý přípravek v souladu s požadavky uvedenými v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a zveřejněném na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
Pokud se shodují data předložení aktualizované zprávy o bezpečnosti (PSUR) a aktualizovaného RMP, je možné je předložit současně.
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
SIMBRINZA 10 mg/ml + 2 mg/ml oční kapky, suspenze brinzolamidum/brimonidini tartras
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
1 ml suspenze obsahuje brinzolamidum 10 mg a brimonidini tartras 2 mg.
3. SEZNAM POMOCNÝCH LÁTEK
Benzalkonium-chlorid, propylenglykol, karbomer 974 P, kyselina boritá, mannitol, chlorid sodný, tyloxapol, kyselina chlorovodíková a/nebo hydroxid sodný (pro úpravu pH) a čištěná voda.
Pro více informací si přečtěte příbalovou informaci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Oční kapky, suspenze 1x 5 ml 3x 5 ml
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím dobře protřepejte.
Před použitím si přečtěte příbalovou informaci. Oční podání
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
Zlikvidujte 4 týdny po prvním otevření. Otevřeno:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Alcon Laboratories (UK) Ltd. Frimley Business Park Frimley, Camberley Surrey GU16 7SR Velká Británie
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/14/933/001 1x 5 ml
EU/1/14/933/002 3x 5 ml
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
simbrinza
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
SIMBRINZA 10 mg/ml + 2 mg/ml oční kapky brinzolamidum/brimonidini tartras
Oční podání
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
5 ml
6. JINÉ
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro uživatele
SIMBRINZA 10 mg/ml + 2 mg/ml oční kapky, suspenze
brinzolamidum/brimonidini tartras
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, optometristy (optika) nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek SIMBRINZA a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek SIMBRINZA používat
3. Jak se přípravek SIMBRINZA používá
4. Možné nežádoucí účinky
5. Jak přípravek SIMBRINZA uchovávat
6. Obsah balení a další informace
1. Co je přípravek SIMBRINZA a k čemu se používá
Přípravek SIMBRINZA obsahuje dvě léčivé látky: brinzolamid a brimonidin-tartarát. Brinzolamid patří do skupiny léků označovaných „inhibitory karboanhydrázy“ a brimonidin-tartarát patří do skupiny léků označovaných „agonisté a-2-adrenergních receptorů“. Obě látky společně způsobí snížení nitroočního tlaku.
Přípravek SIMBRINZA se používá ke snížení nitroočního tlaku u dospělých pacientů (starších 18 let věku), kteří mají tzv. glaukom nebo oční hypertenzi, a u nichž nelze vysoký tlak v očích účinně léčit pomocí jednoho samostatného léku.
2. Čemu musíte věnovat pozornost, než začnete přípravek SIMBRINZA používat Nepoužívejte přípravek SIMBRINZA:
- jestliže jste alergický(á) na brinzolamid nebo brimonidin-tartarát nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6)
- jestliže jste alergický(á) na sulfonamidy (například léky používané k léčbě cukrovky a infekcí a dále diuretika (léky na odvodnění))
- jestliže užíváte inhibitory monoaminooxidázy (MAO) (například léky k léčbě deprese) nebo Parkinsonovy choroby) nebo určitá antidepresiva. Musíte informovat svého lékaře, jestliže užíváte jakákoli antidepresiva
- jestliže máte závažné potíže s ledvinami
- jestliže máte příliš vysokou hladinu kyselin v krvi (stav zvaný hyperchloremická acidóza)
- u dětí ve věku do 2 let.
Upozornění a opatření
Před použitím přípravku SIMBRINZA se poraďte se svým lékařem, optometristou (optikem) nebo lékárníkem, jestliže v současnosti máte nebo jste v minulosti měl(a):
- problémy s játry
- typ vysokého nitroočního tlaku, kterému se říká glaukom s úzkým úhlem
- suché oči nebo problémy s rohovkou
- onemocnění věnčitých srdečních tepen (příznaky mohou zahrnovat bolest nebo tíseň na hrudi, dušnost nebo dušení), srdeční selhání, vysoký nebo nízký krevní tlak
- depresi
- poruchu krevního oběhu nebo slabý krevní oběh (například Raynaudovu nemoc, Raynaudův syndrom nebo mozkovou nedostatečnost).
Jestliže nosíte měkké kontaktní čočky, nepoužívejte kapky, pokud máte nasazené čočky (viz níže bod Používání kontaktních čoček - přípravek SIMBRINZA obsahuje benzalkonium-chlorid).
Děti a dospívající
Přípravek SIMBRINZA se nedoporučuje u dětí a dospívajících ve věku do 18 let. Aby tento přípravek nebyl použit u dětí je důležité především ve věku do 2 let (viz bod Nepoužívejte přípravek SIMBRINZA). Přípravek SIMBRINZA se nemá používat u dětí z důvodu možných závažných nežádoucích účinků (viz bod
3).
Další léčivé přípravky a přípravek SIMBRINZA
Informujte svého lékaře, optometristu (optika) nebo lékárníka o všech lécích, které používáte, které jste v nedávné době používal(a) nebo které možná budete používat.
Přípravek SIMBRINZA může ovlivnit nebo může být ovlivněn dalšími léky, které používáte, včetně jiných očních kapek k léčbě glaukomu.
Informujte svého lékaře, jestliže užíváte nebo chcete užívat kterékoli z následujících léků:
- léky na snížení krevního tlaku
- léky na onemocnění srdce včetně digoxinu (používaného k léčbě srdečních onemocnění)
- jiné léky k léčbě glaukomu, které rovněž léčí výškovou nemoc, známé jako acetazolamid, methazolamid a dorzolamid
- léky, které mohou ovlivnit metabolismus, jako jsou chlorpromazin, methylfenidát a reserpin
- antivirové léky, antiretrovirové léky (používané k léčbě onemocnění virem HIV) nebo antibiotika
- léky proti kvasinkám nebo plísním
- inhibitory monoaminooxidázy (MAO) nebo antidepresiva, včetně amitriptylinu, nortriptylinu, klomipraminu, mianserinu, venlafaxinu a duloxetinu
- anestetika
- sedativa, opiáty nebo barbituráty
- nebo při změně dávky kteréhokoli, v současné době užívaného léku.
Přípravek SIMBRINZA s alkoholem
Jestliže konzumujete alkohol pravidelně, poraďte se se svým lékařem, optometristou (optikem) nebo lékárníkem dříve, než začnete tento přípravek užívat. Alkohol může ovlivnit účinek přípravku SIMBRINZA.
Těhotenství a kojení
Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem, optometristou (optikem) nebo lékárníkem dříve, než začnete tento přípravek používat. Ženám, které mohou otěhotnět, se doporučuje během léčby přípravkem SIMBRINZA používat účinnou antikoncepci. Podávání přípravku SIMBRINZA se v těhotenství nedoporučuje. Přípravek SIMBRINZA používejte pouze tehdy, když Vám to jasně nařídil lékař.
Jestliže kojíte, může přípravek SIMBRINZA přecházet do Vašeho mateřského mléka. Podávání přípravku SIMBRINZA se během kojení nedoporučuje.
Řízení dopravních prostředků a obsluha strojů
Můžete zjistit, že Vaše vidění je po použití přípravku SIMBRINZA po určitou dobu rozmazané nebo abnormální. Přípravek SIMBRINZA může u některých pacientů způsobit také závrať, ospalost nebo únava.
Neřiďte ani neobsluhujte stroje, dokud tyto příznaky neodezní.
Používání kontaktních čoček - přípravek SIMBRINZA obsahuje benzalkonium-chlorid
Přípravek SIMBRINZA obsahuje konzervační látku (benzalkonium-chlorid), která může způsobit podráždění oka a je známo, že zabarvuje měkké kontaktní čočky. Vyhněte se kontaktu s měkkými kontaktními čočkami. Před aplikací přípravku SIMBRINZA si kontaktní čočky vyjměte a po jeho použití vyčkejte alespoň 15 minut, než si kontaktní čočky opět nasadíte.
3. Jak se přípravek SIMBRINZA používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře, optometristy (optika) nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem, optometristou (optikem) nebo lékárníkem.
Přípravek SIMBRINZA používejte pouze k nakapání do očí. Přípravek nepolykejte ani neaplikujte injekčně.
Doporučená dávka je jedna kapka do postiženého oka nebo očí dvakrát denně. Používejte vždy ve stejnou denní dobu.
Návod k použití
Nejprve si umyjte ruce.

1
Před použitím dobře protřepejte.
Odšroubujte uzávěr lahvičky. Pokud je po sejmutí víčka bezpečnostní kroužek uvolněný, před použitím přípravku jej odstraňte.
Při otvírání a zavírání lahvičky se prsty nedotýkejte kapátka. Mohlo by dojít ke kontaminaci kapek.
Držte lahvičku mezi palcem a prsty dnem vzhůru.
Zakloňte hlavu.
Čistým prstem si stáhněte dolní oční víčko tak, aby se mezi očním víčkem a okem vytvořila „kapsa“, do níž umístíte kapku (obrázek č. 1).
Přiložte hrot kapátka lahvičky k oku. Použijte zrcadlo, pokud Vám to pomůže.
Nedotýkejte se kapátkem oka ani očního víčka, okolních oblastí či jiných povrchů. Mohlo by dojít ke kontaminaci kapek.
Lehce stlačte spodní část lahvičky, aby se uvolnila právě jedna kapka přípravku SIMBRINZA Lahvičku nemačkejte - je navržena tak, aby stačil jemný tlak na dno lahvičky (obrázek č. 2).
Po použití očních kapek zavřete oko a prstem jemně stiskněte koutek oka u nosu po dobu alespoň 2 minut, čímž omezíte množství přípravku, které se dostane do ostatních částí těla.
Jestliže používáte kapky do obou očí, opakujte postup u druhého oka. Při použití kapek pro druhé oko není potřeba lahvičku zavřít a protřepat. Ihned po použití lahvičku pevně uzavřete.
Jestliže používáte ještě jiné oční kapky, vyčkejte mezi aplikací přípravku SIMBRINZA a dalších kapek nejméně pět minut.
Jestliže kapka nedopadne do oka, zkuste to znovu.
Jestliže jste použil(a) více přípravku SIMBRINZA, než jste měl(a)
Vypláchněte si oko teplou vodou. Nepodávejte žádné další kapky, dokud nenastane doba pro Vaši další pravidelnou dávku.
Dospělí, kteří nedopatřením pozřeli léky obsahující brimonidin, zaznamenali sníženou srdeční frekvenci, snížený krevní tlak, po němž může následovat zvýšení krevního tlaku, srdeční selhání, dýchací obtíže a účinky na nervový systém. Pokud toto nastane, kontaktujte ihned svého lékaře.
U dětí, které nedopatřením pozřely léky obsahující brimonidin, byly hlášeny závažné nežádoucí účinky. Jejich známky zahrnovaly ospalost, ochablost, nízká tělesná teplota, bledost a dýchací obtíže. V takovém případě ihned kontaktujte svého lékaře.
V případě náhodného požití přípravku SIMBRINZA je nutné ihned kontaktovat lékaře.
Jestliže jste zapomněl(a) použít přípravek SIMBRINZA
Pokračujte další plánovanou dávkou. Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku. Nikdy nepodávejte více než jednu kapku do postiženého oka (očí) dvakrát denně.
Jestliže jste přestal(a) používat přípravek SIMBRINZA
Než přestanete používat přípravek SIMBRINZA, nejprve se poraďte se svým lékařem. Jestliže přestanete používat přípravek SIMBRINZA, nebude Váš nitrooční tlak pod kontrolou, což by mohlo vést ke ztrátě zraku.
Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře, optometristy (optika) nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Jestliže zaznamenáte jakékoli z následujících nežádoucích účinků, přestaňte tento lék používat a ihned vyhledejte lékařskou péči, neboť by se mohlo jednat o známky reakce na lék. Četnost výskytu alergické reakce způsobené tímto lékem není známa (frekvenci z dostupných údajů nelze určit).
• závažné kožní reakce, včetně vyrážky nebo zarudnutí, nebo svědění těla nebo očí;
• obtíže s dýcháním;
• bolest na hrudi, nepravidelný srdeční rytmus.
Pokud se u Vás objeví extrémní únava nebo závratě, ihned se obraťte na svého lékaře.
Následující nežádoucí účinky byly pozorovány při léčbě přípravkem SIMBRINZA a jinými léky, které obsahují samotný brinzolamid nebo brimonidin.
Časté nežádoucí účinky (mohou postihnout až 1 osobu z 10)
- Účinky na oko: alergický zánět spojivek (oční alergie), zánět povrchu oka, bolest oka, nepříjemný pocit v oku, rozmazané nebo abnormální vidění, zarudnutí oka
- Celkové nežádoucí účinky: ospalost, závrať, nepříjemná chuť v ústech, sucho v ústech Méně časté nežádoucí účinky (mohou postihnout až 1 osobu ze 100)
- Účinky na oko: poškození povrchu oka s úbytkem buněk, zánět očního víčka, depozita na povrchu oka, citlivost na světlo, otok oka (postihující rohovku nebo oční víčko), suché oko, výtok z oka, slzící oko, zarudnutí očního víčka, abnormální pocit nebo snížený cit v oku, unavené oko, zhoršené vidění, dvojité vidění, částice léku v oku
- Celkové nežádoucí účinky: snížený krevní tlak, bolest na hrudi, nepravidelný tlukot srdce, pomalý nebo rychlý srdeční puls, bušení srdce, problémy se spaním (insomnie), noční můry, deprese, celková slabost, bolest hlavy, závrať, nervozita, podrážděnost, obecné cítění se špatně, ztráta paměti, dušnost, astma, krvácení z nosu, příznaky nachlazení, sucho v nose nebo v krku, bolest v krku, podráždění v krku, kašel, nosní sekrece, pocit ucpaného nosu, kýchání, zánět vedlejších nosních dutin, překrvení v oblasti dolních dýchacích cest, ušní šelest, porucha trávení, plynatost nebo bolest břicha, pocit na zvracení, průjem, zvracení, abnormální pocit v ústech, zvýšené alergické příznaky na kůži, vyrážka, abnormální citlivost kůže, vypadávání vlasů, svědění kůže celého těla, zvýšené hladiny chloru v krvi nebo snížený počet červených krvinek podle krevního testu, bolest, bolest zad, bolest nebo křeče svalů, bolest od ledvin (například bolest v dolní části zad), snížené libido, sexuální problémy u mužů
Velmi vzácné (mohou postihnout až 1 osobu z 10 000)
- Účinky na oko: zmenšená zornice
- Celkové nežádoucí účinky: mdloby, zvýšený krevní tlak Není známo (četnost nelze z dostupných údajů určit)
- Účinky na oko: snížený růst očních řas
- Celkové nežádoucí účinky: třes, snížená citlivost, ztráta chuti, abnormální hodnoty jaterní funkce podle krevního testu, otok obličeje, bolest kloubů, časté močení, bolest na hrudi, otok končetin
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek SIMBRINZA uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na lahvičce a na krabičce za EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Lahvičku zlikvidujte 4 týdny po prvním otevření z důvodu rizika kontaminace a použijte novou lahvičku. Datum otevření zapište na vyhrazené místo na krabičce.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého optometristy (optika) nebo lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek SIMBRINZA obsahuje
- Léčivými látkami jsou brinzolamidum a brimonidini tartras. Jeden ml suspenze obsahuje brinzolamidum 10 mg a brimonidini tartras 2 mg, odpovídající brimonidinum 1,3 mg.
- Dalšími složkami jsou benzalkonium-chlorid (viz bod 2 Používání kontaktních čoček - přípravek SIMBRINZA obsahuje benzalkonium-chlorid), propylenglykol, karbomer 974 P, kyselinu boritou, mannitol, chlorid sodný, tyloxapol, kyselina chlorovodíková a/nebo hydroxid sodný a čištěnou vodu.
Přípravek dále obsahuje malé množství kyseliny chlorovodíkové a/nebo hydroxidu sodného za účelem udržení normální kyselosti (hodnoty pH).
Jak přípravek SIMBRINZA vypadá a co obsahuje toto balení
Přípravek SIMBRINZA oční kapky, suspenze je tekutina (bílá až krémově bílá suspenze), která se prodává v balení obsahujícím jednu nebo tři 5ml plastové lahvičky se šroubovacím uzávěrem. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci
Alcon Laboratories (UK) Ltd.
Frimley Business Park Frimley, Camberley Surrey GU16 7SR Velká Británie
Výrobce
Alcon-Couvreur N.V. Rijksweg 14 B-2870 Puurs Belgie
Výrobce
Alcon Cusí, S.A. Camil Fabra 58 08320 El Masnou Španělsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Belgie/Belgique/Belgien Latvija
Luxembourg/Luxemburg Alcon Pharmaceuticals Ltd
Alcon NV ® + 371 67 321 121
@ + 32 (0)2 754 32 10 (Belgie/Belgique/Belgien)
BtnrapHH Lietuva
Aukoh Euarapna EOOfl Alcon Pharmaceuticals Ltd. atstovybé
® + 359 2 950 15 65 ® + 370 5 2 314 756
Česká republika
Alcon Pharmaceuticals (Czech Republic) s.r.o. ® + 420 225 775 111
Danmark
Island
Norge
Suomi/Finland
Sverige
Alcon Nordic A/S ® + 45 3636 4300
Deutschland
Alcon Pharma GmbH ® + 49 (0) 761 1304-0
Magyarország
Alcon Hungária Gyógyszerkereskedelmi Kft. ® + 36 1 463 9080
Nederland
Alcon Nederland BV ® + 31 (0) 183 654 321
|
Eesti Alcon Pharmaceuticals Ltd. Eesti filiaal ® + 372 6 313 214 |
Osterreich Alcon Ophthalmika GmbH ® + 43 (0)1 596 69 70 |
|
EkXúba Kúrcpog A^kov Aapnopáxoprg EMá; AEBE ® + 30 210 68 78 300 (EUáSa) |
Polska Alcon Polska Sp. z.o.o. ® + 48 22 820 3450 |
|
Espaňa Alcon Cusí, S.A. ® + 34 93 497 7000 |
Portugal Alcon Portugal - Produtos e Equipamentos Oftalmológicos, Lda. ® + 351 214 400 300 |
|
France Laboratoires Alcon ® + 33 (0)1 47 10 47 10 |
Románia S.C. Alcon Romania S.R.L. ® + 40 21 203 93 24 |
|
Hrvatska Alcon Farmaceutika d.o.o. ® + 385 1 4611 988 |
Slovenija Alcon d.o.o. ® + 386 1 422 5280 |
|
Ireland Malta United Kingdom Alcon Laboratories (UK) Ltd. ® + 44 (0) 345 266 9363 (United Kingdom) Italia Alcon Italia S.p.A. ® +39 02 81 80 31 |
Slovenská republika Novartis Slovakia s.r.o. Alcon Division ® + 421 2 5441 0378 |
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
28