Novomix 70 Flexpen 100 Jednotek/Ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
NovoMix 30 Penfill 100 jednotek/ml injekční suspenze v zásobní vložce
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje 100 jednotek Insulinům aspartum solubile*/Insulinum aspartum protaminatum cristallinum* v poměru 30/70 (což odpovídá 3,5 mg). 1 zásobní vložka obsahuje 3 ml, což odpovídá 300 jednotkám.
* Insulin aspart je vyrobený rekombinantní DNA technologií na Saccharomyces cerevisiae.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční suspenze Zakalená, bílá vodná suspenze.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
NovoMix 30 je indikován k léčbě diabetes mellitus u dospělých, dospívajících a dětí ve věku od 10 let.
4.2 Dávkování a způsob podání
Dávkování
Účinnost inzulinových analogů, včetně inzulinu aspart, se vyjadřuje v jednotkách, zatímco účinnost humánních inzulinů se vyjadřuje v mezinárodních jednotkách.
Dávkování přípravku NovoMix 30 je individuální a je stanoveno v souladu s pacientovými potřebami. Pro dosažení optimální kontroly glykemie je doporučeno monitorování glukózy v krvi a úpravy dávky inzulinu.
U pacientů s diabetem 2. typu lze NovoMix 30 podávat jako monoterapii. NovoMix 30 může být také podáván v kombinaci s perorálními antidiabetiky, pokud je hladina glukózy v krvi nedostatečně kontrolována podáváním těchto perorálních antidiabetik samotných. Pro pacienty s diabetem 2. typu je doporučená počáteční dávka přípravku NovoMix 30 6 jednotek při snídani a 6 jednotek při večeři (večerním jídle). Používání přípravku NovoMix 30 může být také zahájeno podáním 12 jednotek jedenkrát denně při večeři (večerním jídle). Pokud je NovoMix 30 podáván jednou denně a jestliže již bylo dosaženo 30 jednotek, je obecně doporučeno přejít na dávkování dvakrát denně rozdělením dávky na dvě stejné dávky při snídani a při večeři. Jestliže při podávání přípravku NovoMix 30 dvakrát denně dochází k opakovaným hypoglykemickým příhodám během dne, může být ranní dávka rozdělena do ranní dávky a dávky při obědě (dávkování 3krát denně).
Pro úpravu dávky je doporučen následující titrační postup.
Hladiny glukózy v krvi před jídlem
Úprava dávky přípravku NovoMix 30
|
< 4,4 mmol/l |
< 80 mg/dl |
- 2 jednotky |
|
4,4 - 6,1 mmol/l |
80 - 110 mg/dl |
0 |
|
6,2 - 7,8 mmol/l |
111 - 140 mg/dl |
+ 2 jednotky |
|
7,9 - 10 mmol/l |
141 - 180 mg/dl |
+ 4 jednotky |
|
> 10 mmol/l |
> 180 mg/dl |
+ 6 jednotek |
Použity by měly být nejnižší hladiny glukózy v krvi před jídlem naměřené během tří předchozích dní. Dávka by neměla být zvyšována, jestliže během těchto dní došlo k hypoglykemické příhodě. Dávka může být upravována jednou týdně až do dosažení cílové hodnoty HbAic. K vyhodnocení přiměřenosti předchozí dávky by měly být užity hladiny glukózy v krvi naměřené před jídlem.
Individuální inzulinová potřeba pacientů s diabetem 1. typu je obvykle mezi 0,5 a 1,0 jednotkou/kg/den. NovoMix 30 může plně nebo částečně tuto potřebu zajistit.
Úprava dávky může být nutná, pokud pacient podstupuje zvýšenou tělesnou námahu, mění svou obvyklou dietu nebo během současně probíhajícího jiného onemocnění.
Zvláštní skupiny pacientů
Starší pacienti (> 65 let)
NovoMix 30 může být používán staršími pacienty, avšak zkušenost s užíváním přípravku NovoMix 30 v kombinaci s perorálními antidiabetiky u pacientů starších 75 let je omezená.
Monitorování glukózy u starších pacientů by mělo být intenzivnější a dávkování inzulinu aspart by mělo být upraveno individuálně.
Poškození ledvin a jater
Poškození ledvin nebo jater může snížit pacientovu potřebu inzulinu.
Monitorování glukózy u pacientů s poškozením ledvin nebo jater by mělo být intenzivnější a dávkování inzulinu aspart by mělo být upraveno individuálně.
Pediatrická populace
NovoMix 30 může být používán u dospívajících a dětí ve věku od 10 let, pokud je preferován premixovaný inzulin. Pro děti ve věku od 6 - 9 let existují s přípravkem NovoMix 30 omezené klinické zkušenosti (viz bod 5.1).
Pro použití přípravku NovoMix 30 u dětí ve věku do 6 let nejsou dostupné žádné údaje Přechod z jiných inzulínových přípravků
Při převodu pacienta z bifázického humánního inzulinu na NovoMix 30 začněte se stejnou dávkou a ve stejném režimu. Poté titrujte podle individuálních potřeb pacienta (viz výše doporučený titrační postup).
Během přechodu a několik týdnů poté je doporučeno pečlivé monitorování glukózy (viz bod 4.4). Způsob podání
NovoMix 30 je bifázická suspenze inzulinového analogu inzulin aspart. Suspenze obsahuje rychle působící a střednědobě působící inzulin aspart v poměru 30/70.
NovoMix 30 je určen pouze pro subkutánní podání.
NovoMix 30 je podáván subkutánně do stehna nebo břišní stěny. Pokud je to přijatelné, je možné ho aplikovat do oblasti hýždí nebo deltoidní oblasti. Injekční místa ve stejné oblasti je vždy třeba měnit rotačním způsobem, aby se snížilo riziko lipodystrofie. Vliv různých míst vpichu na absorpci přípravku NovoMix 30 nebyl sledován. Trvání účinku se mění podle dávky, místa vpichu, prokrvení,
teploty a fyzické aktivity.
NovoMix 30 má rychlejší nástup účinku než humánní bifázický inzulin a měl by být tedy obecně podáván bezprostředně před jídlem. Pokud je to nutné, může být NovoMix 30 podán i brzy po jídle.
Podání s inzulínovými aplikátory
NovoMix 30 Penfill je určen k použití spolu s aplikátory Novo Nordisk a jehlami NovoFine nebo NovoTwist.
K přípravku NovoMix 30 Penfill je přiložena příbalová informace s podrobným návodem k použití, který by měl být dodržován.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
NovoMix 30 nesmí být podáván intravenózně, neboť to může vést k těžké hypoglykemii. Vyvarujte se intramuskulárního podání. NovoMix 30 není určen pro použití v inzulinových infuzních pumpách.
Před cestou mezi různými časovými pásmy by se pacient měl poradit s lékařem. Cestování mezi různými časovými pásmy může totiž znamenat, že pacient bude muset užívat inzulin a přijímat jídla v odlišných časech.
Hyperglykemie
Nedostatečné dávkování nebo přerušovaná léčba, zejména u diabetu 1. typu, může vést k hyperglykemii a diabetické ketoacidóze. První symptomy hyperglykemie se obvykle v průběhu hodin nebo dní stupňují. Mezi ně patří žízeň, zvýšená frekvence močení, nauzea, zvracení, ospalost, zarudlá suchá kůže, sucho v ústech, ztráta chuti k jídlu či acetonový zápach dechu. U diabetu 1. typu mohou vést neléčené hyperglykemické stavy až k diabetické ketoacidóze, která je potenciálně letální.
Hypoglykemie
Vynechání jídla nebo neplánovaná namáhavá fyzická aktivita mohou vést k hypoglykemii.
Hypoglykemie se může objevit, pokud je dávka inzulinu příliš vysoká ve vztahu k potřebě inzulinu.
V případě hypoglykemie či podezření na hypoglykemii nesmí být NovoMix podáván. Poté co u pacienta dojde ke stabilizaci hladiny glukózy, měla by být zvážena úprava dávky (viz body 4.2, 4.8 a 4.9).
Ve srovnání s bifázickým humánním inzulinem může mít NovoMix 30 výraznější účinek na snížení hladiny glukózy až 6 hodin po aplikaci. Toto je třeba u jednotlivých pacientů kompenzovat úpravou dávky inzulinu a/nebo příjmu jídla.
Pacienti, u kterých se kontrola diabetu výrazně zlepšila, např. při intenzifikované inzulinové terapii, mohou zaznamenat změnu obvyklých varovných příznaků hypoglykemie, a měli by být patřičně poučeni. U pacientů s dlouholetým diabetem mohou běžné varovné symptomy vymizet.
Přísnější kontrola hladiny glukózy může zvyšovat možnost vzniku hypoglykemických příhod, a proto je během intenzifikace dávky vyžadována speciální pozornost (viz bod 4.2).
Protože NovoMix 30 má být aplikován v těsné závislosti na jídle, je třeba zvážit rychlý nástup účinku u pacientů s doprovodnými nemocemi nebo při léčbě, během níž může být očekávána zpožděná absorpce jídla.
Přidružené onemocnění, zejména infekce a horečnaté stavy, obvykle zvyšují pacientovu potřebu inzulinu. Přidružené onemocnění ledvin, jater či onemocnění ovlivňující nadledviny, podvěsek mozkový nebo štítnou žlázu může vyžadovat změny v dávce inzulinu.
Pokud je pacient převeden na jiný typ inzulinových přípravků, může dojít ke změně či potlačení časných varovných příznaků hypoglykemie oproti těm, které se u pacienta projevovaly u předchozího inzulinu.
Převedení z jiných inzulínových přípravků
Převod pacienta na jiný typ nebo značku inzulinu by měl probíhat pod přísným lékařským dozorem. Změny v síle, značce (výrobce), typu, původu (zvířecí inzulin, humánní inzulin nebo analog inzulinu) a/nebo metodě výroby (rekombinantní DNA versus inzulin ze zvířecích zdrojů) mohou vést k potřebě změnit dávkování. Pacienti převádění na přípravek NovoMix 30 z jiných typů inzulinu mohou vyžadovat vyšší počet injekcí denně nebo změnu dávkování oproti jejich obvyklým inzulinovým léčivým přípravkům. Pokud je potřeba přizpůsobit dávkování, může k tomu dojít při první dávce nebo během prvních týdnů či měsíců.
Reakce v místě vpichu
Tak jako při každé léčbě inzulinem se mohou objevit reakce v místě vpichu, které se projevují bolestivostí, zarudnutím, kopřivkou, zánětem, podlitinami, otoky a svěděním. Pravidelné obměňování injekčního místa v rámci jedné oblasti snižuje riziko vzniku těchto reakcí. Reakce obvykle vymizí do několika dnů nebo týdnů. Ve vzácných případech si mohou reakce v místě vpichu vyžádat vysazení přípravku NovoMix 30.
Kombinace přípravku NovoMix s pioglitazonem
Pokud byl pioglitazon užíván v kombinaci s inzulinem, byly hlášeny případy srdečního selhání a to zvláště u pacientů s rizikovými faktory pro vznik srdečního selhání. Tuto skutečnost je nutno vzít v úvahu, pokud je zvažována léčba pioglitazonem v kombinaci s přípravkem NovoMix. Pokud je tato kombinace použita, měli by být pacienti sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení hmotnosti a edém. Pioglitazon by měl být vysazen, pokud se objeví jakékoliv zhoršení srdečních příznaků.
Protilátky proti inzulinu
Podávání inzulinu může vyvolat tvorbu protilátek proti inzulinu. Ve vzácných případech může přítomnost těchto protilátek vyžadovat úpravu dávky inzulinu, aby se usměrnila tendence k hyper- či hypoglykemii.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
U řady léčivých přípravků je známa interakce s glukózovým metabolismem.
Následující látky mohou snižovat pacientovu potřebu inzulinu:
Perorální antidiabetika, inhibitory monoaminoxidázy (IMAO), beta-blokátory, angiotensin konvertujícího enzymu (ACE) inhibitory, salicyláty, anabolické steroidy a sulfonamidy.
Následující látky mohou zvyšovat pacientovu potřebu inzulinu:
Perorální kontraceptiva, thiazidy, glukokortikoidy, thyreoidální hormony, sympatomimetika, růstový hormon a danazol.
Beta-blokátory mohou zakrývat příznaky hypoglykemie.
Oktreotid/lanreotid mohou buď zvýšit, nebo snížit potřebu inzulínu. Alkohol může zesílit nebo snížit hypoglykemický účinek inzulinu.
4.6 Fertilita, těhotenství a kojení Těhotenství
Klinické zkušenosti s užíváním přípravku NovoMix 30 v těhotenství jsou omezené.
Reprodukční studie na zvířatech neukázaly žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče embryotoxicity nebo teratogenity.
Obecně platí, že v průběhu celého těhotenství a při jeho plánování se doporučují intenzifikované kontroly hladin glukózy v krvi a monitorování těhotných diabetiček. Potřeba inzulinu obvykle v průběhu prvního trimestru klesne a následně se zvyšuje ve druhém a třetím trimestru. Po porodu se potřeba inzulinu rychle vrací na úroveň před těhotenstvím.
Kojení
Léčba přípravkem NovoMix 30 při kojení není omezena. Léčba kojících matek inzulinem nepředstavuje pro dítě žádné riziko. Dávkování přípravku NovoMix 30 však může vyžadovat úpravu.
Fertilita
Reprodukční studie se zvířaty neodhalily žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče fertility.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Pacientova schopnost koncentrace a reakce se může v důsledku hypoglykemie zhoršit. To může představovat riziko v situacích, kde jsou tyto schopnosti zvláště důležité (např. řízení vozu nebo obsluha strojů).
Pacienti by měli být poučeni o opatřeních, jak se vyvarovat vzniku hypoglykemie během řízení či během obsluhy strojů. Je to důležité zvláště u pacientů, kteří mají slabé nebo žádné varovné příznaky hypoglykemie nebo kteří mají časté epizody hypoglykemie. V těchto případech je třeba vhodnost řízení či obsluhy strojů zvážit.
4.8 Nežádoucí účinky
a. Souhrn bezpečnostního profilu
Nežádoucí účinky pozorované u pacientů užívajících NovoMix jsou převážně způsobeny farmakologickým efektem inzulinu aspart.
Nejčastěji hlášeným nežádoucím účinkem během léčby je hypoglykemie. Frekvence výskytu hypoglykemie se mění s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly, viz bod c níže.
Na počátku inzulinové léčby se mohou vyskytnout poruchy refrakce, edém a reakce v místě vpichu (bolest, zarudnutí, kopřivka, zánět, podlitiny, otoky a svědění v místě vpichu). Tyto reakce jsou obvykle přechodné povahy. Rychlé zlepšení hladiny glukózy v krvi může být spojeno s akutní bolestivou neuropatií, která je obvykle reverzibilní. Intenzifikace inzulinové terapie s prudkým zlepšením glykemické kontroly může být spojena s přechodným zhoršením diabetické retinopatie, zatímco dlouhodobé zlepšení glykemické kontroly snižuje riziko progrese diabetické retinopatie.
b. Seznam nežádoucích účinků v tabulce
Nežádoucí účinky uvedené níže jsou založeny na údajích z klinických studií a jsou klasifikovány podle MedDRA frekvence výskytu a třídy orgánových systémů. Frekvence výskytu jsou definovány podle následující konvence: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000), velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
|
Poruchy imunitního systému |
Méně časté - Kopřivka, vyrážky, erupce |
|
Velmi vzácné - Anafylaktické reakce* | |
|
Poruchy metabolismu a výživy |
Velmi časté - Hypoglykemie* |
|
Poruchy nervového systému |
Vzácné - Periferní neuropatie (bolestivá neuropatie) |
|
Poruchy oka |
Méně časté - Poruchy refrakce |
|
Méně časté - Diabetická retinopatie | |
|
Poruchy kůže a podkožní tkáně |
Méně časté - Lipodystrofie* |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté - Otoky |
|
Méně časté - Reakce v místě vpichu |
viz bod c.
c. Popis vybraných nežádoucích účinků Anafylaktické reakce:
Vznik generalizovaných hypersenzitivních reakcí (zahrnujících generalizované kožní vyrážky, svědění, pocení, gastrointestinální obtíže, angioneurotický edém, obtížné dýchání, palpitace a pokles krevního tlaku) je velmi vzácný, avšak může být potenciálně život ohrožující.
Hypoglykemie:
Nejčastěji hlášeným nežádoucím účinkem je hypoglykemie. Může nastat v případě, kdy je dávka inzulinu příliš vysoká vzhledem k inzulinové potřebě. Těžká hypoglykemie může vést k bezvědomí a/nebo křečím a může vyústit v přechodné nebo trvalé poškození mozkových funkcí nebo dokonce vést ke smrti. Příznaky hypoglykemie se obvykle objevují náhle. Mohou zahrnovat studený pot, chladnou bledou pokožku, únavu, nervozitu nebo třes, úzkost, neobvyklou vyčerpanost nebo slabost, zmatenost, potíže s koncentrací, ospalost, velký hlad, změny vidění, bolest hlavy, nauzeu a palpitaci.
V klinických studiích se frekvence výskytu hypoglykemií měnila s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly. Během klinických studií se celkový výskyt hypoglykemií nelišil u pacientů léčených inzulinem aspart ve srovnání s humánním inzulinem.
Lipodystrofie:
V místě vpichu může vzniknout lipodystrofie (zahrnující lipohypertrofii, lipoatrofii). Průběžná cyklická změna místa vpichu v dané oblasti snižuje riziko vzniku takovýchto reakcí.
d. Pediatrická populace
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u pediatrické populace, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
e. Další populační specifika
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u starších pacientů a u pacientů s poškozením ledvin či jater, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
f. Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Specifické předávkování inzulinem nelze definovat, ovšem v následných stádiích se může vyvinout hypoglykemie, pokud jsou pacientovi podány dávky, které jsou vzhledem k jeho potřebě inzulinu příliš vysoké:
• Mírné hypoglykemické příhody mohou být léčeny perorálním podáním glukózy nebo potravin obsahujících cukr. Proto se diabetikům doporučuje, aby s sebou vždy nosili potraviny s obsahem cukru.
• Těžké hypoglykemické příhody, při kterých pacient upadl do bezvědomí, mohou být léčeny intramuskulárním nebo subkutánním podáním glukagonu (0,5 až 1 mg) zaškolenou osobou nebo intravenózní aplikací glukózy zdravotnickým pracovníkem. Glukózu je nutno podat intravenózně i v případě, jestliže pacient nereaguje na glukagon do 10 až 15 minut. Po návratu pacienta k vědomí se doporučuje podat mu perorálně sacharidy jako prevenci relapsu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antidiabetika. Inzuliny a analogy střednědobě nebo dlouze působící v kombinaci s rychle působícími, k injekční aplikaci. ATC kód: A10AD05.
NovoMix 30 je bifázická suspenze 30 % rozpustného inzulinu aspart (rychle působícího analogu humánního inzulinu) a 70 % krystalického protaminového inzulinu aspart (střednědobě působícího analogu humánního inzulinu).
Mechanismus účinku a farmakodynamické účinky
Účinek inzulinu aspart na pokles hladiny glukózy v krvi je důsledkem usnadněného vychytávání glukózy a následné vazby inzulinu na receptory ve svalových a tukových buňkách a současné inhibice uvolňování glukózy z jater.
NovoMix 30 je bifázický inzulin, který obsahuje 30 % rozpustného inzulinu aspart. Tento má rychlý nástup účinku, takže dovoluje podání v těsnější závislosti na jídle (rozmezí 0 až 10 minut od jídla) ve srovnání s rozpustným humánním inzulinem. Krystalická část (70 %) je tvořena krystalickým protaminovým inzulinem aspart, jehož profil účinku se podobá profilu humánního NPH inzulinu.
Je-li NovoMix 30 aplikován subkutánně, nástup účinku nastává v průběhu 10 až 20 minut po injekci. Maximálního účinku je dosaženo za 1 až 4 hodiny po injekci. Účinek trvá až 24 hodin (obrázek 1).
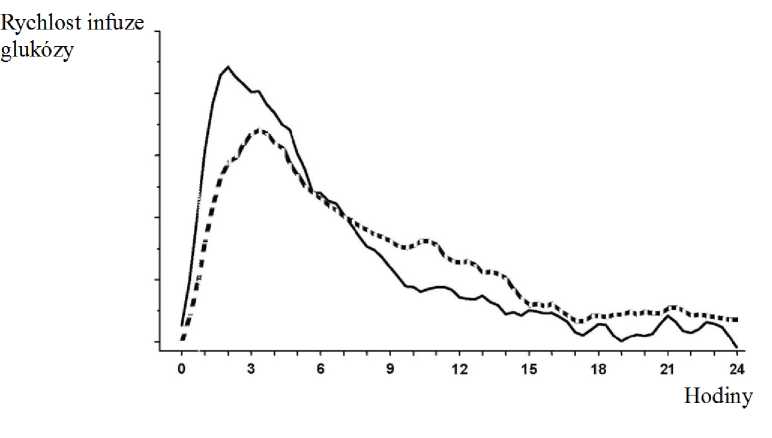
Obrázek 1: Profil aktivity přípravku NovoMix 30 (—) a bifázického humánního inzulínu 30 (---) u zdravých subjektů.
Klinická účinnost a bezpečnost
V 3 měsíční klinické studii u pacientů s diabetem 1. a 2. typu byla kontrola glykosylovaného hemoglobinu při léčbě přípravkem NovoMix 30 stejná, jako při léčbě bifázickým humánním inzulinem 30. Inzulin aspart je ekvipotentní s humánním inzulinem na molární bázi. V porovnání
s bifázickým humánním inzulinem 30 vedlo podávání přípravku NovoMix 30 před snídaní a večeří k nižší postprandiální hladině glukózy v krvi po obou jídlech (snídaně a večeře).
Meta-analýza zahrnující devět studií s pacienty s diabetem 1. typu i s diabetem 2. typu prokázala, že hladina glukózy v krvi nalačno byla vyšší u pacientů léčených přípravkem NovoMix 30 než u pacientů léčených bifázickým humánním inzulinem 30.
V jedné klinické studii bylo 341 pacientů s diabetem 2. typu randomizováno buď pouze s přípravkem NovoMix 30 nebo v kombinaci s metforminem nebo v kombinaci metformin společně se sulfonylureou. Primární účinnost - HbA1c po 16 týdnech léčby se nelišila mezi pacienty léčenými přípravkem NovoMix 30 v kombinaci s metforminem a pacienty léčenými metforminem a sulfonylureou. V této studii mělo 57 % pacientů výchozí hodnotu HbA1c nad 9 %; u pacientů léčených přípravkem NovoMix 30 v kombinaci s metforminem došlo k významnému snížení hodnoty HbA1c ve srovnání s pacienty léčenými kombinací metformin a sulfonylurea.
V jedné klinické studii byli pacienti s diabetem 2. typu, kteří nebyli dostatečně kompenzováni samotnými perorálními antidiabetiky, randomizováni v jedné větvi s přípravkem NovoMix 30 podávaným 2x denně (117 pacientů) a ve druhé větvi s inzulinem glargin podávaným 1x denně (116 pacientů). Po 28 týdnech léčby při dodržování dávkovacího postupu popsaného v bodě 4.2 bylo průměrné snížení HbA1c u přípravku NovoMix 30 rovno 2,8 % (průměrná výchozí hodnota = 9,7 %).
U přípravku NovoMix 30 dosáhlo 66 % a 42 % pacientů úrovně HbA1c pod 7 % respektive 6,5 % a průměrná hodnota FPG byla snížena přibližně o 7 mmol/l (z výchozí hodnoty 14,0 mmol/l na
7,1 mmol/l).
U pacientů s diabetem 2. typu meta-analýza prokázala snížené riziko celkových nočních hypoglykemických příhod a závažných hypoglykémií u přípravku NovoMix 30 ve srovnání s bifázickým humánním inzulinem 30. Riziko celkových hypoglykemických příhod v denní době bylo u pacientů léčených přípravkem NovoMix 30 zvýšené.
Byla prováděna 16týdenní klinická studie, která srovnávala kompenzaci postprandiální glykémie přípravkem NovoMix 30 s kompenzací humánním inzulinem/bifázickým humánním inzulinem 30 v obou případech podávanými ve vztahu k příjmu jídla a v kombinaci s inzulinem NPH podávaným před spaním, a to u 167 pacientů ve věku 10 až 18 let. Průměrná hodnota HbAJc zůstala během studie u obou léčených skupin podobná jako základní hodnota a v počtu hypoglykemií nebylo rozdílu mezi přípravkem NovoMix 30 nebo bifázickým humánním inzulinem 30.
V menší a mladší skupině (54 pacientů, věkové rozmezí 6 - 12 let) léčené ve dvojitě zaslepené zkřížené klinické studii (12 týdnů trvání každé léčby) byly počet hypoglykemických epizod i zvýšení hladiny postprandiální glykémie významně nižší u přípravku NovoMix 30 ve srovnání s bifázickým humánním inzulinem 30. Konečná hodnota HbAJc byla ve skupině léčené bifázickým humánním inzulinem 30 významně nižší v porovnání s přípravkem NovoMix 30.
5.2 Farmakokinetické vlastnosti
Absorpce, distribuce a eliminace
Substituce aminokyseliny prolinu kyselinou asparagovou v inzulinu aspart na pozici B28 snižuje tendenci ke tvorbě hexamerů tak, jak to bylo pozorováno u rozpustného humánního inzulinu. Inzulin aspart v rozpustné fázi přípravku Novo Mix 30 tvoří 30 % celkového inzulinu, který se ze subkutánní vrstvy vstřebává rychleji, než rozpustná složka bifázického humánního inzulinu. Zbývajících 70 % tvoří krystalická forma krystalický protaminový inzulin aspart, který má prodloužený absorpční profil podobný humánnímu NPH inzulinu.
Maximální koncentrace inzulinu v séru je u přípravku NovoMix 30 v průměru o 50 % vyšší než u bifázického humánního inzulinu 30. Čas potřebný k dosažení maximální koncentrace je v průměru poloviční než u bifázického humánního inzulinu 30. U zdravých dobrovolníků bylo dosaženo průměrné maximální koncentrace v séru 140 ± 32 pmol/l asi 60 minut po subkutánní aplikaci dávky 0,20 jednotky/kg tělesné hmotnosti. Průměrný poločas (t./2) přípravku NovoMix 30, odrážející absorpční rychlost frakce vázané na protamin, byl asi 8 - 9 hodin. Hladina inzulinu v séru se vrátila na bazální hodnotu za 15 - 18 hodin po subkutánní dávce. U pacientů s diabetem 2. typu bylo maximální koncentrace dosaženo za 95 minut po aplikaci dávky a nejméně za 14 hodin po aplikaci dávky byly koncentrace v séru měřitelné.
Zvláštní skupiny pacientů
Farmakokinetika přípravku NovoMix 30 nebyla sledována u starších pacientů ani u pacientů s poškozením ledvin nebo jater.
Pediatrická populace
Farmakokinetika přípravku NovoMix 30 nebyla u dětí nebo dospívajících sledována. Avšak u dětí (6 - 12 let) a dospívajících (13 - 17 let) s diabetem 1. typu byly sledovány farmakokinetické a farmakodynamické vlastnosti rozpustného inzulinu aspart. V obou věkových skupinách byl inzulin aspart rychle absorbován s podobným tmax jako u dospělých. Nicméně Cmax se v jednotlivých věkových skupinách odlišovala, s důrazem na důležitost individuální titrace inzulinu aspart.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
Při zkouškách in vitro, včetně vazby na inzulinová a IGF-1 receptorová místa a účinků na buněčný
růst, se inzulin aspart choval podobně jako humánní inzulin. Studie také ukazují, že disociace inzulínu aspart z vazby na inzulinových receptorech je ekvivalentní humánnímu inzulinu.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Glycerol Fenol Metakresol Chlorid zinečnatý
Dihydrát hydrogenfosforečnanu sodného
Chlorid sodný
Protamin-sulfát
Kyselina chlorovodíková (pro úpravu pH)
Hydroxid sodný (pro úpravu pH)
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nej sou k dispozici, a proto tento léčivý přípravek nesmí být mísen s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
Před otevřením: 2 roky.
Během používání nebo pokud NovoMix nosíte jako zásobní: přípravek smí být uchováván maximálně 4 týdny.
6.4 Zvláštní opatření pro uchovávání
Před otevřením: uchovávejte v chladničce (2 °C - 8 °C). Neuchovávejte v blízkosti chladicího zařízení. Chraňte před mrazem.
Během používání nebo pokud NovoMix nosíte jako zásobní: uchovávejte při teplotě do 30 °C. Chraňte před chladem. Chraňte před mrazem.
Uchovávejte zásobní vložku v krabičce, aby byl přípravek chráněn před světlem.
6.5 Druh obalu a obsah balení
3 ml suspenze v zásobní vložce (sklo typu 1), s pístem (bromobutyl) a pryžovým uzávěrem (bromobutyl/polyisopren). V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání.
Velikosti balení jsou 5 a 10 zásobních vložek. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Jehly a NovoMix 30 Penfill nesmí být s nikým sdíleny. Zásobní vložka se nesmí znovu plnit.
Po vyjmutí přípravku NovoMix 30 Penfill z chladničky je před promícháním inzulinu dle instrukcí pro první použití doporučeno nechat NovoMix 30 Penfill ohřát na pokojovou teplotu.
Tento léčivý přípravek nepoužívejte, pokud si všimnete, že po promíchání tekutina není vodná, stejnoměrně bílá a zakalená.
Pacientovi je třeba zdůraznit, že těsně před použitím je nutné suspenzi přípravku NovoMix 30 promíchat.
NovoMix 30, který zmrzl, nesmí být použit.
Pacient musí být poučen o tom, že po každé aplikaci musí použitou jehlu vyhodit.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
8. REGISTRAČNÍ ČÍSLA
EU/1/00/142/004
EU/1/00/142/005
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 1. srpna 2000
Datum posledního prodloužení registrace: 2. července 2010
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské lékové agentury http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
NovoMix 50 Penfill 100 jednotek/ml injekční suspenze v zásobní vložce
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje 100 jednotek Insulinům aspartum solubile*/Insulinum aspartum protaminatum cristallinum* v poměru 50/50 (což odpovídá 3,5 mg). 1 zásobní vložka obsahuje 3 ml, což odpovídá 300 jednotkám.
* Insulin aspart je vyrobený rekombinantní DNA technologií na Saccharomyces cerevisiae.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční suspenze Zakalená, bílá vodná suspenze.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
NovoMix 50 je indikován k léčbě diabetes mellitus u dospělých.
4.2 Dávkování a způsob podání
Dávkování
Účinnost inzulinových analogů, včetně inzulinu aspart, se vyjadřuje v jednotkách, zatímco účinnost humánních inzulinů se vyjadřuje v mezinárodních jednotkách.
Dávkování přípravku NovoMix 50 je individuální a je stanoveno v souladu s pacientovými potřebami. Pro dosažení optimální kontroly glykemie je doporučeno monitorování glukózy v krvi a úpravy dávky inzulinu.
Individuální inzulinová potřeba je obvykle mezi 0,5 a 1,0 jednotkou/kg/den. NovoMix 50 může plně nebo částečně tuto potřebu zajistit.
U pacientů s diabetem 2. typu lze NovoMix 50 podávat jako monoterapii nebo v kombinaci s metforminem, pokud je hladina glukózy v krvi nedostatečně kontrolována podáváním metforminu samotného.
Úprava dávky může být nutná, pokud pacient podstupuje zvýšenou tělesnou námahu, mění svou obvyklou dietu nebo během současně probíhajícího jiného onemocnění.
Zvláštní skupiny pacientů
V případě starších pacientů (> 65 let) a pacientů s poškozením jater či ledvin by mělo být monitorování glukózy intenzifikováno a dávka inzulinu aspart by měla být upravena individuálně.
Poškození ledvin nebo jater může snížit pacientovu potřebu inzulinu.
Bezpečnost a účinnost přípravku NovoMix 50 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
Přechod z jiných inzulínových přípravků
Přechod na NovoMix 50 z jiných inzulínových přípravků může vyžadovat úpravu dávky a času podání. Během přechodu a několik týdnů poté je doporučeno pečlivé monitorování glukózy (viz bod 4.4).
Způsob podání
NovoMix 50 je bifázická suspenze inzulinového analogu inzulin aspart. Suspenze obsahuje rychle působící a střednědobě působící inzulin aspart v poměru 50/50.
NovoMix 50 je určen pouze pro subkutánní podání.
NovoMix 50 je podáván subkutánně do stehna nebo břišní stěny. Pokud je to přijatelné, je možné ho aplikovat do oblasti hýždí nebo deltoidní oblasti. Injekční místa ve stejné oblasti je vždy třeba měnit rotačním způsobem, aby se snížilo riziko lipodystrofie. Vliv různých míst vpichu na absorpci přípravku NovoMix 50 nebyl sledován. Trvání účinku se mění podle dávky, místa vpichu, prokrvení, teploty a fyzické aktivity.
NovoMix 50 má rychlejší nástup účinku než humánní bifázický inzulin a měl by být tedy obecně podáván bezprostředně před jídlem. Pokud je to nutné, může být NovoMix 50 podán i brzy po jídle.
Podání s inzulínovými aplikátory
NovoMix 50 Penfill je určen k použití spolu s aplikátory Novo Nordisk a jehlami NovoFine nebo NovoTwist.
K přípravku NovoMix 50 Penfill je přiložena příbalová informace s podrobným návodem k použití, který by měl být dodržován.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
NovoMix 50 nesmí být podáván intravenózně, neboť to může vést k těžké hypoglykemii. Vyvarujte se intramuskulárního podání. NovoMix 50 není určen pro použití v inzulinových infuzních pumpách.
Před cestou mezi různými časovými pásmy by se pacient měl poradit s lékařem. Cestování mezi různými časovými pásmy může totiž znamenat, že pacient bude muset užívat inzulin a přijímat jídla v odlišných časech.
Hyperglykemie
Nedostatečné dávkování nebo přerušovaná léčba, zejména u diabetu 1. typu, může vést k hyperglykemii a diabetické ketoacidóze. První symptomy hyperglykemie se obvykle v průběhu hodin nebo dní stupňují. Mezi ně patří žízeň, zvýšená frekvence močení, nauzea, zvracení, ospalost, zarudlá suchá kůže, sucho v ústech, ztráta chuti k jídlu či acetonový zápach dechu. U diabetu 1. typu mohou vést neléčené hyperglykemické stavy až k diabetické ketoacidóze, která je potenciálně letální.
Hypoglykemie
Vynechání jídla nebo neplánovaná namáhavá fyzická aktivita mohou vést k hypoglykemii.
Hypoglykemie se může objevit, pokud je dávka inzulinu příliš vysoká ve vztahu k potřebě inzulinu.
V případě hypoglykemie či podezření na hypoglykemii nesmí být NovoMix podáván. Poté co u pacienta dojde ke stabilizaci hladiny glukózy, měla by být zvážena úprava dávky (viz body 4.2, 4.8 a 4.9).
Pacienti, u kterých se kontrola diabetu výrazně zlepšila, např. při intenzifikované inzulinové terapii, mohou zaznamenat změnu obvyklých varovných příznaků hypoglykemie a měli by být patřičně poučeni. U pacientů s dlouholetým diabetem mohou běžné varovné symptomy vymizet.
Protože NovoMix 50 má být aplikován v těsné závislosti na jídle, je třeba zvážit rychlý nástup účinku u pacientů s doprovodnými nemocemi nebo při léčbě, během níž může být očekávána zpožděná absorpce jídla.
Přidružené onemocnění, zejména infekce a horečnaté stavy, obvykle zvyšují pacientovu potřebu inzulinu. Přidružené onemocnění ledvin, jater či onemocnění ovlivňující nadledviny, podvěsek mozkový nebo štítnou žlázu může vyžadovat změny v dávce inzulinu.
Pokud je pacient převeden na jiný typ inzulinových přípravků, může dojít ke změně či potlačení časných varovných příznaků hypoglykemie oproti těm, které se u pacienta projevovaly u předchozího inzulinu.
Převedení z jiných inzulínových přípravků
Převod pacienta na jiný typ nebo značku inzulinu by měl probíhat pod přísným lékařským dozorem. Změny v síle, značce (výrobce), typu, původu (zvířecí inzulin, humánní inzulin nebo analog inzulinu) a/nebo metodě výroby (rekombinantní DNA versus inzulin ze zvířecích zdrojů) mohou vést k potřebě změnit dávkování. Pacienti převádění na přípravek NovoMix 50 z jiných typů inzulinu mohou vyžadovat vyšší počet injekcí denně nebo změnu dávkování oproti jejich obvyklým inzulinovým léčivým přípravkům. Pokud je potřeba přizpůsobit dávkování, může k tomu dojít při první dávce nebo během prvních týdnů či měsíců.
Reakce v místě vpichu
Tak jako při každé léčbě inzulinem se mohou objevit reakce v místě vpichu, které se projevují bolestivostí, zarudnutím, kopřivkou, zánětem, podlitinami, otoky a svěděním. Pravidelné obměňování injekčního místa v rámci jedné oblasti snižuje riziko vzniku těchto reakcí. Reakce obvykle vymizí do několika dnů nebo týdnů. Ve vzácných případech si mohou reakce v místě vpichu vyžádat vysazení přípravku NovoMix 50.
Kombinace přípravku NovoMix s pioglitazonem
Pokud byl pioglitazon užíván v kombinaci s inzulinem, byly hlášeny případy srdečního selhání a to zvláště u pacientů s rizikovými faktory pro vznik srdečního selhání. Tuto skutečnost je nutno vzít v úvahu, pokud je zvažována léčba pioglitazonem v kombinaci s přípravkem NovoMix. Pokud je tato kombinace použita, měli by být pacienti sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení hmotnosti a edém. Pioglitazon by měl být vysazen, pokud se objeví jakékoliv zhoršení srdečních příznaků.
Protilátky proti inzulinu
Podávání inzulínu může vyvolat tvorbu protilátek proti inzulínu. Ve vzácných případech může přítomnost těchto protilátek vyžadovat úpravu dávky inzulinu, aby se usměrnila tendence k hyper- či hypoglykemii.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
U řady léčivých přípravků je známa interakce s glukózovým metabolismem.
Následující látky mohou snižovat pacientovu potřebu inzulinu:
Perorální antidiabetika, inhibitory monoaminoxidázy (IMAO), beta-blokátory, angiotensin konvertujícího enzymu (ACE) inhibitory, salicyláty, anabolické steroidy a sulfonamidy.
Následující látky mohou zvyšovat pacientovu potřebu inzulinu:
Perorální kontraceptiva, thiazidy, glukokortikoidy, thyreoidální hormony, sympatomimetika, růstový hormon a danazol.
Beta-blokátory mohou zakrývat příznaky hypoglykemie.
Oktreotid/lanreotid mohou buď zvýšit nebo snížit potřebu inzulinu.
Alkohol může zesílit nebo snížit hypoglykemický účinek inzulinu.
4.6 Fertilita, těhotenství a kojení Těhotenství
Klinické zkušenosti s užíváním přípravku NovoMix 50 v těhotenství jsou omezené.
Reprodukční studie na zvířatech neukázaly žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče embryotoxicity nebo teratogenity.
Obecně platí, že v průběhu celého těhotenství a při jeho plánování se doporučují intenzifikované kontroly hladin glukózy v krvi a monitorování těhotných diabetiček. Potřeba inzulinu obvykle v průběhu prvního trimestru klesne a následně se zvyšuje ve druhém a třetím trimestru. Po porodu se potřeba inzulinu rychle vrací na úroveň před těhotenstvím.
Kojení
Léčba přípravkem NovoMix 50 při kojení není omezena. Léčba kojících matek inzulinem nepředstavuje pro dítě žádné riziko. Dávkování přípravku NovoMix 50 však může vyžadovat úpravu.
Fertilita
Reprodukční studie se zvířaty neodhalily žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče fertility.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Pacientova schopnost koncentrace a reakce se může v důsledku hypoglykemie zhoršit. To může představovat riziko v situacích, kde jsou tyto schopnosti zvláště důležité (např. řízení vozu nebo obsluha strojů).
Pacienti by měli být poučeni o opatřeních, jak se vyvarovat vzniku hypoglykemie během řízení či během obsluhy strojů. Je to důležité zvláště u pacientů, kteří mají slabé nebo žádné varovné příznaky hypoglykemie nebo kteří mají časté epizody hypoglykemie. V těchto případech je třeba vhodnost řízení či obsluhy strojů zvážit.
4.8 Nežádoucí účinky
a. Souhrn bezpečnostního profilu
Nežádoucí účinky pozorované u pacientů užívajících NovoMix jsou převážně způsobeny farmakologickým efektem inzulinu aspart.
Nejčastěji hlášeným nežádoucím účinkem během léčby je hypoglykemie. Frekvence výskytu hypoglykemie se mění s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly, viz bod c níže.
Na počátku inzulinové léčby se mohou vyskytnout poruchy refrakce, edém a reakce v místě vpichu (bolest, zarudnutí, kopřivka, zánět, podlitiny, otoky a svědění v místě vpichu). Tyto reakce jsou obvykle přechodné povahy. Rychlé zlepšení hladiny glukózy v krvi může být spojeno s akutní bolestivou neuropatií, která je obvykle reverzibilní. Intenzifikace inzulinové terapie s prudkým zlepšením glykemické kontroly může být spojena s přechodným zhoršením diabetické retinopatie, zatímco dlouhodobé zlepšení glykemické kontroly snižuje riziko progrese diabetické retinopatie.
b. Seznam nežádoucích účinků v tabulce
Nežádoucí účinky uvedené níže jsou založeny na údajích z klinických studií a jsou klasifikovány podle MedDRA frekvence výskytu a třídy orgánových systémů. Frekvence výskytu jsou definovány podle následující konvence: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000), velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
|
Poruchy imunitního systému |
Méně časté - Kopřivka, vyrážky, erupce |
|
Velmi vzácné - Anafylaktické reakce* | |
|
Poruchy metabolismu a výživy |
Velmi časté - Hypoglykemie* |
|
Poruchy nervového systému |
Vzácné - Periferní neuropatie (bolestivá neuropatie) |
|
Poruchy oka |
Méně časté - Poruchy refrakce |
|
Méně časté - Diabetická retinopatie | |
|
Poruchy kůže a podkožní tkáně |
Méně časté - Lipodystrofie* |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté - Otoky |
|
Méně časté - Reakce v místě vpichu |
viz bod c.
c. Popis vybraných nežádoucích účinků Anafylaktické reakce:
Vznik generalizovaných hypersenzitivních reakcí (zahrnujících generalizované kožní vyrážky, svědění, pocení, gastrointestinální obtíže, angioneurotický edém, obtížné dýchání, palpitace a pokles krevního tlaku) je velmi vzácný, avšak může být potenciálně život ohrožující.
Hypoglykemie:
Nejčastěji hlášeným nežádoucím účinkem je hypoglykemie. Může nastat v případě, kdy je dávka inzulínu příliš vysoká vzhledem k inzulínové potřebě. Těžká hypoglykemie může vést k bezvědomí a/nebo křečím a může vyústit v přechodné nebo trvalé poškození mozkových funkcí nebo dokonce vést ke smrti. Příznaky hypoglykemie se obvykle objevují náhle. Mohou zahrnovat studený pot, chladnou bledou pokožku, únavu, nervozitu nebo třes, úzkost, neobvyklou vyčerpanost nebo slabost, zmatenost, potíže s koncentrací, ospalost, velký hlad, změny vidění, bolest hlavy, nauzeu a palpitaci.
V klinických studiích se frekvence výskytu hypoglykemií měnila s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly. Během klinických studií se celkový výskyt hypoglykemií nelišil u pacientů léčených inzulinem aspart ve srovnání s humánním inzulinem.
Lipodystrofie:
V místě vpichu může vzniknout lipodystrofie (zahrnující lipohypertrofii, lipoatrofii). Průběžná cyklická změna místa vpichu v dané oblasti snižuje riziko vzniku takovýchto reakcí.
d. Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 50 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
e. Další populační specifika
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u starších pacientů a u pacientů s poškozením ledvin či jater, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
f. Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Specifické předávkování inzulinem nelze definovat, ovšem v následných stádiích se může vyvinout hypoglykemie, pokud jsou pacientovi podány dávky, které jsou vzhledem k jeho potřebě inzulinu příliš vysoké:
• Mírné hypoglykemické příhody mohou být léčeny perorálním podáním glukózy nebo potravin obsahujících cukr. Proto se diabetikům doporučuje, aby s sebou vždy nosili potraviny s obsahem cukru.
• Těžké hypoglykemické příhody, při kterých pacient upadl do bezvědomí, mohou být léčeny intramuskulárním nebo subkutánním podáním glukagonu (0,5 až 1 mg) zaškolenou osobou nebo intravenózní aplikací glukózy zdravotnickým pracovníkem. Glukózu je nutno podat intravenózně i v případě, jestliže pacient nereaguje na glukagon do 10 až 15 minut. Po návratu pacienta k vědomí se doporučuje podat mu perorálně sacharidy jako prevenci relapsu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antidiabetika. Inzuliny a analogy střednědobě nebo dlouze působící v kombinaci s rychle působícími, k injekční aplikaci. ATC kód: A10AD05.
NovoMix 50 je bifázická suspenze 50 % rozpustného inzulínu aspart (rychle působícího analogu humánního inzulinu) a 50 % krystalického protaminového inzulinu aspart (střednědobě působícího analogu humánního inzulinu).
Mechanismus účinku a farmakodynamické účinky
Účinek inzulinu aspart na pokles hladiny glukózy v krvi je důsledkem usnadněného vychytávání glukózy a následné vazby inzulinu na receptory ve svalových a tukových buňkách a současné inhibice uvolňování glukózy z jater.
NovoMix 50 je bifázický inzulin, který obsahuje 50 % rozpustného inzulinu aspart. Tento má rychlý nástup účinku, takže dovoluje podání v těsnější závislosti na jídle (rozmezí 0 až 10 minut od jídla) ve srovnání s rozpustným humánním inzulinem. Krystalická část (50 %) je tvořena krystalickým protaminovým inzulinem aspart, jehož profil účinku se podobá profilu humánního NPH inzulinu.
Je-li NovoMix 50 aplikován subkutánně, nástup účinku nastává v průběhu 10 až 20 minut po injekci. Maximálního účinku je dosaženo za 1 až 4 hodiny po injekci. Účinek trvá 14 až 24 hodin (obrázek 1).
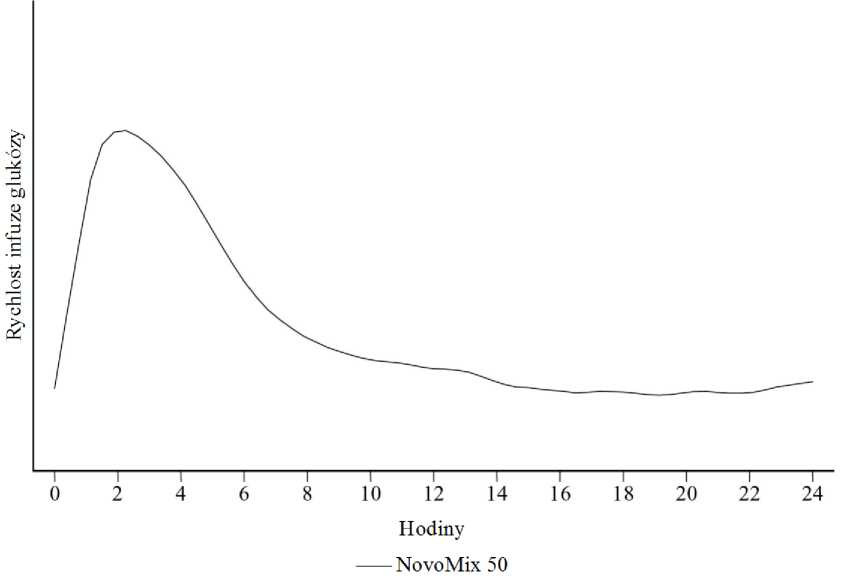
Obrázek 1: Profil aktivity přípravku NovoMix 50 u zdravých bělošských subjektů.
Inzulin aspart je ekvipotentní s humánním inzulinem na molární bázi.
5.2 Farmakokinetické vlastnosti Absorpce, distribuce a eliminace
Substituce aminokyseliny prolinu kyselinou asparagovou v inzulinu aspart na pozici B28 snižuje tendenci ke tvorbě hexamerů tak, jak to bylo pozorováno u rozpustného humánního inzulinu. Inzulin aspart v rozpustné fázi přípravku Novo Mix 50 tvoří 50 % celkového inzulinu, který se ze subkutánní vrstvy vstřebává rychleji, než rozpustná složka bifázického humánního inzulinu. Zbývajících 50 % tvoří krystalická forma krystalický protaminový inzulin aspart, který má prodloužený absorpční profil podobný humánnímu NPH inzulinu.
U zdravých dobrovolníků bylo průměrné maximální koncentrace v séru 445 ± 135 pmol/l dosaženo přibližně za 60 minut po subkutánním podání dávky 0,30 jednotky/kg tělesné hmotnosti. U pacientů s diabetem 2. typu bylo maximální koncentrace dosaženo přibližně po 95 minutách od podání.
Zvláštní skupiny pacientů
Farmakokinetika přípravku NovoMix 50 nebyla sledována u dětí, starších pacientů ani u pacientů s poškozením ledvin nebo jater.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
Při zkouškách in vitro, včetně vazby na inzulinová a IGF-1 receptorová místa a účinků na buněčný růst, se inzulin aspart choval podobně jako humánní inzulin. Studie také ukazují, že disociace inzulinu aspart z vazby na inzulinových receptorech je ekvivalentní humánnímu inzulinu.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Glycerol Fenol Metakresol Chlorid zinečnatý
Dihydrát hydrogenfosforečnanu sodného
Chlorid sodný
Protamin-sulfát
Kyselina chlorovodíková (pro úpravu pH)
Hydroxid sodný (pro úpravu pH)
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto tento léčivý přípravek nesmí být mísen s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
Před otevřením: 2 roky.
Během používání nebo pokud NovoMix nosíte jako zásobní: přípravek smí být uchováván maximálně 4 týdny.
6.4 Zvláštní opatření pro uchovávání
Před otevřením: uchovávejte v chladničce (2 °C - 8 °C). Neuchovávejte v blízkosti chladicího zařízení. Chraňte před mrazem.
Během používání nebo pokud NovoMix nosíte jako zásobní: uchovávejte při teplotě do 30 °C. Chraňte před chladem. Chraňte před mrazem.
Uchovávejte zásobní vložku v krabičce, aby byl přípravek chráněn před světlem.
3 ml suspenze v zásobní vložce (sklo typu 1), s pístem (bromobutyl) a pryžovým uzávěrem (bromobutyl/polyisopren). V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání.
Velikosti balení jsou 1, 5 a 10 zásobních vložek. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Jehly a NovoMix 50 Penfill nesmí být s nikým sdíleny. Zásobní vložka se nesmí znovu plnit.
Po vyjmutí přípravku NovoMix 50 Penfill z chladničky je před promícháním inzulinu dle instrukcí pro první použití doporučeno nechat NovoMix 50 Penfill ohřát na pokojovou teplotu.
Tento léčivý přípravek nepoužívejte, pokud si všimnete, že po promíchání tekutina není vodná, stejnoměrně bílá a zakalená.
Pacientovi je třeba zdůraznit, že těsně před použitím je nutné suspenzi přípravku NovoMix 50 promíchat.
NovoMix 50, který zmrzl, nesmí být použit.
Pacient musí být poučen o tom, že po každé aplikaci musí použitou jehlu vyhodit.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
8. REGISTRAČNÍ ČÍSLA
EU/1/00/142/011
EU/1/00/142/012
EU/1/00/142/013
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 1. srpna 2000
Datum posledního prodloužení registrace: 2. července 2010
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské lékové agentury http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
NovoMix 70 Penfill 100 jednotek/ml injekční suspenze v zásobní vložce
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile*/Insulinum aspartum protaminatum cristallinum* v poměru 70/30 (což odpovídá 3,5 mg). 1 zásobní vložka obsahuje 3 ml, což odpovídá 300 jednotkám.
* Insulin aspart je vyrobený rekombinantní DNA technologií na Saccharomyces cerevisiae.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční suspenze Zakalená, bílá vodná suspenze.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
NovoMix 70 je indikován k léčbě diabetes mellitus u dospělých.
4.2 Dávkování a způsob podání
Dávkování
Účinnost inzulinových analogů, včetně inzulinu aspart, se vyjadřuje v jednotkách, zatímco účinnost humánních inzulinů se vyjadřuje v mezinárodních jednotkách.
Dávkování přípravku NovoMix 70 je individuální a je stanoveno v souladu s pacientovými potřebami. Pro dosažení optimální kontroly glykemie je doporučeno monitorování glukózy v krvi a úpravy dávky inzulinu.
Individuální inzulinová potřeba je obvykle mezi 0,5 a 1,0 jednotkou/kg/den. NovoMix 70 může plně nebo částečně tuto potřebu zajistit.
U pacientů s diabetem 2. typu lze NovoMix 70 podávat jako monoterapii nebo v kombinaci s metforminem, pokud je hladina glukózy v krvi nedostatečně kontrolována podáváním metforminu samotného.
Úprava dávky může být nutná, pokud pacient podstupuje zvýšenou tělesnou námahu, mění svou obvyklou dietu nebo během současně probíhajícího jiného onemocnění.
Zvláštní skupiny pacientů
V případě starších pacientů (> 65 let) a pacientů s poškozením jater či ledvin by mělo být monitorování glukózy intenzifikováno a dávka inzulinu aspart by měla být upravena individuálně.
Poškození ledvin nebo jater může snížit pacientovu potřebu inzulinu.
Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 70 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
Přechod z jiných inzulínových přípravků
Přechod na NovoMix 70 z jiných inzulinových přípravků může vyžadovat úpravu dávky a času podání. Během přechodu a několik týdnů poté je doporučeno pečlivé monitorování glukózy (viz bod 4.4).
Způsob podání
NovoMix 70 je bifázická suspenze inzulinového analogu inzulin aspart. Suspenze obsahuje rychle působící a střednědobě působící inzulin aspart v poměru 70/30.
NovoMix 70 je určen pouze pro subkutánní podání.
NovoMix 70 je podáván subkutánně do stehna nebo břišní stěny. Pokud je to přijatelné, je možné ho aplikovat do oblasti hýždí nebo deltoidní oblasti. Injekční místa ve stejné oblasti je vždy třeba měnit rotačním způsobem, aby se snížilo riziko lipodystrofie. Vliv různých míst vpichu na absorpci přípravku NovoMix 70 nebyl sledován. Trvání účinku se mění podle dávky, místa vpichu, prokrvení, teploty a fyzické aktivity.
NovoMix 70 má rychlejší nástup účinku než humánní bifázický inzulin a měl by být tedy obecně podáván bezprostředně před jídlem. Pokud je to nutné, může být NovoMix 70 podán i brzy po jídle.
Podání s inzulínovými aplikátory
NovoMix 70 Penfill je určen k použití spolu s aplikátory Novo Nordisk a jehlami NovoFine nebo NovoTwist.
K přípravku NovoMix 70 Penfill je přiložena příbalová informace s podrobným návodem k použití, který by měl být dodržován.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
NovoMix 70 nesmí být podáván intravenózně, neboť to může vést k těžké hypoglykemii. Vyvarujte se intramuskulárního podání. NovoMix 70 není určen pro použití v inzulinových infuzních pumpách.
Před cestou mezi různými časovými pásmy by se pacient měl poradit s lékařem. Cestování mezi různými časovými pásmy může totiž znamenat, že pacient bude muset užívat inzulin a přijímat jídla v odlišných časech.
Hyperglykemie
Nedostatečné dávkování nebo přerušovaná léčba, zejména u diabetu 1. typu, může vést k hyperglykemii a diabetické ketoacidóze. První symptomy hyperglykemie se obvykle v průběhu hodin nebo dní stupňují. Mezi ně patří žízeň, zvýšená frekvence močení, nauzea, zvracení, ospalost, zarudlá suchá kůže, sucho v ústech, ztráta chuti k jídlu či acetonový zápach dechu. U diabetu 1. typu mohou vést neléčené hyperglykemické stavy až k diabetické ketoacidóze, která je potenciálně letální.
Hypoglykemie
Vynechání jídla nebo neplánovaná namáhavá fyzická aktivita mohou vést k hypoglykemii.
Hypoglykemie se může objevit, pokud je dávka inzulinu příliš vysoká ve vztahu k potřebě inzulinu.
V případě hypoglykemie či podezření na hypoglykemii nesmí být NovoMix podáván. Poté co u pacienta dojde ke stabilizaci hladiny glukózy, měla by být zvážena úprava dávky (viz body 4.2, 4.8 a 4.9).
Pacienti, u kterých se kontrola diabetu výrazně zlepšila, např. při intenzifikované inzulinové terapii, mohou zaznamenat změnu obvyklých varovných příznaků hypoglykemie a měli by být patřičně poučeni. U pacientů s dlouholetým diabetem mohou běžné varovné symptomy vymizet.
Protože NovoMix 70 má být aplikován v těsné závislosti na jídle, je třeba zvážit rychlý nástup účinku u pacientů s doprovodnými nemocemi nebo při léčbě, během níž může být očekávána zpožděná absorpce jídla.
Přidružené onemocnění, zejména infekce a horečnaté stavy, obvykle zvyšují pacientovu potřebu inzulinu. Přidružené onemocnění ledvin, jater či onemocnění ovlivňující nadledviny, podvěsek mozkový nebo štítnou žlázu může vyžadovat změny v dávce inzulinu.
Pokud je pacient převeden na jiný typ inzulinových přípravků, může dojít ke změně či potlačení časných varovných příznaků hypoglykemie oproti těm, které se u pacienta projevovaly u předchozího inzulinu.
Převedení z jiných inzulínových přípravků
Převod pacienta na jiný typ nebo značku inzulinu by měl probíhat pod přísným lékařským dozorem. Změny v síle, značce (výrobce), typu, původu (zvířecí inzulin, humánní inzulin nebo analog inzulinu) a/nebo metodě výroby (rekombinantní DNA versus inzulin ze zvířecích zdrojů) mohou vést k potřebě změnit dávkování. Pacienti převádění na přípravek NovoMix 70 z jiných typů inzulinu mohou vyžadovat vyšší počet injekcí denně nebo změnu dávkování oproti jejich obvyklým inzulinovým léčivým přípravkům. Pokud je potřeba přizpůsobit dávkování, může k tomu dojít při první dávce nebo během prvních týdnů či měsíců.
Reakce v místě vpichu
Tak jako při každé léčbě inzulinem se mohou objevit reakce v místě vpichu, které se projevují bolestivostí, zarudnutím, kopřivkou, zánětem, podlitinami, otoky a svěděním. Pravidelné obměňování injekčního místa v rámci jedné oblasti snižuje riziko vzniku těchto reakcí. Reakce obvykle vymizí do několika dnů nebo týdnů. Ve vzácných případech si mohou reakce v místě vpichu vyžádat vysazení přípravku NovoMix 70.
Kombinace přípravku NovoMix s pioglitazonem
Pokud byl pioglitazon užíván v kombinaci s inzulinem, byly hlášeny případy srdečního selhání a to zvláště u pacientů s rizikovými faktory pro vznik srdečního selhání. Tuto skutečnost je nutno vzít v úvahu, pokud je zvažována léčba pioglitazonem v kombinaci s přípravkem NovoMix. Pokud je tato kombinace použita, měli by být pacienti sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení hmotnosti a edém. Pioglitazon by měl být vysazen, pokud se objeví jakékoliv zhoršení srdečních příznaků.
Protilátky proti inzulinu
Podávání inzulínu může vyvolat tvorbu protilátek proti inzulínu. Ve vzácných případech může přítomnost těchto protilátek vyžadovat úpravu dávky inzulinu, aby se usměrnila tendence k hyper- či hypoglykemii.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
U řady léčivých přípravků je známa interakce s glukózovým metabolismem.
Následující látky mohou snižovat pacientovu potřebu inzulinu:
Perorální antidiabetika, inhibitory monoaminoxidázy (IMAO), beta-blokátory, angiotensin konvertujícího enzymu (ACE) inhibitory, salicyláty, anabolické steroidy a sulfonamidy.
Následující látky mohou zvyšovat pacientovu potřebu inzulinu:
Perorální kontraceptiva, thiazidy, glukokortikoidy, thyreoidální hormony, sympatomimetika, růstový hormon a danazol.
Beta-blokátory mohou zakrývat příznaky hypoglykemie.
Oktreotid/lanreotid mohou buď zvýšit nebo snížit potřebu inzulinu.
Alkohol může zesílit nebo snížit hypoglykemický účinek inzulinu.
4.6 Fertilita, těhotenství a kojení Těhotenství
Klinické zkušenosti s užíváním přípravku NovoMix 70 v těhotenství jsou omezené.
Reprodukční studie na zvířatech neukázaly žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče embryotoxicity nebo teratogenity.
Obecně platí, že v průběhu celého těhotenství a při jeho plánování se doporučují intenzifikované kontroly hladin glukózy v krvi a monitorování těhotných diabetiček. Potřeba inzulinu obvykle v průběhu prvního trimestru klesne a následně se zvyšuje ve druhém a třetím trimestru. Po porodu se potřeba inzulinu rychle vrací na úroveň před těhotenstvím.
Kojení
Léčba přípravkem NovoMix 70 při kojení není omezena. Léčba kojících matek inzulinem nepředstavuje pro dítě žádné riziko. Dávkování přípravku NovoMix 70 však může vyžadovat úpravu.
Fertilita
Reprodukční studie se zvířaty neodhalily žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče fertility.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Pacientova schopnost koncentrace a reakce se může v důsledku hypoglykemie zhoršit. To může představovat riziko v situacích, kde jsou tyto schopnosti zvláště důležité (např. řízení vozu nebo obsluha strojů).
Pacienti by měli být poučeni o opatřeních, jak se vyvarovat vzniku hypoglykemie během řízení či během obsluhy strojů. Je to důležité zvláště u pacientů, kteří mají slabé nebo žádné varovné příznaky hypoglykemie nebo kteří mají časté epizody hypoglykemie. V těchto případech je třeba vhodnost řízení či obsluhy strojů zvážit.
4.8 Nežádoucí účinky
a. Souhrn bezpečnostního profilu
Nežádoucí účinky pozorované u pacientů užívajících NovoMix jsou převážně způsobeny farmakologickým efektem inzulinu aspart.
Nejčastěji hlášeným nežádoucím účinkem během léčby je hypoglykemie. Frekvence výskytu hypoglykemie se mění s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly, viz bod c níže.
Na počátku inzulinové léčby se mohou vyskytnout poruchy refrakce, edém a reakce v místě vpichu (bolest, zarudnutí, kopřivka, zánět, podlitiny, otoky a svědění v místě vpichu). Tyto reakce jsou obvykle přechodné povahy. Rychlé zlepšení hladiny glukózy v krvi může být spojeno s akutní bolestivou neuropatií, která je obvykle reverzibilní. Intenzifikace inzulinové terapie s prudkým zlepšením glykemické kontroly může být spojena s přechodným zhoršením diabetické retinopatie, zatímco dlouhodobé zlepšení glykemické kontroly snižuje riziko progrese diabetické retinopatie.
b. Seznam nežádoucích účinků v tabulce
Nežádoucí účinky uvedené níže jsou založeny na údajích z klinických studií a jsou klasifikovány podle MedDRA frekvence výskytu a třídy orgánových systémů. Frekvence výskytu jsou definovány podle následující konvence: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000), velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
|
Poruchy imunitního systému |
Méně časté - Kopřivka, vyrážky, erupce |
|
Velmi vzácné - Anafylaktické reakce* | |
|
Poruchy metabolismu a výživy |
Velmi časté - Hypoglykemie* |
|
Poruchy nervového systému |
Vzácné - Periferní neuropatie (bolestivá neuropatie) |
|
Poruchy oka |
Méně časté - Poruchy refrakce |
|
Méně časté - Diabetická retinopatie | |
|
Poruchy kůže a podkožní tkáně |
Méně časté - Lipodystrofie* |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté - Otoky |
|
Méně časté - Reakce v místě vpichu |
viz bod c.
c. Popis vybraných nežádoucích účinků Anafylaktické reakce:
Vznik generalizovaných hypersenzitivních reakcí (zahrnujících generalizované kožní vyrážky, svědění, pocení, gastrointestinální obtíže, angioneurotický edém, obtížné dýchání, palpitace a pokles krevního tlaku) je velmi vzácný, avšak může být potenciálně život ohrožující.
Hypoglykemie:
Nejčastěji hlášeným nežádoucím účinkem je hypoglykemie. Může nastat v případě, kdy je dávka inzulínu příliš vysoká vzhledem k inzulínové potřebě. Těžká hypoglykemie může vést k bezvědomí a/nebo křečím a může vyústit v přechodné nebo trvalé poškození mozkových funkcí nebo dokonce vést ke smrti. Příznaky hypoglykemie se obvykle objevují náhle. Mohou zahrnovat studený pot, chladnou bledou pokožku, únavu, nervozitu nebo třes, úzkost, neobvyklou vyčerpanost nebo slabost, zmatenost, potíže s koncentrací, ospalost, velký hlad, změny vidění, bolest hlavy, nauzeu a palpitaci.
V klinických studiích se frekvence výskytu hypoglykemií měnila s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly. Během klinických studií se celkový výskyt hypoglykemií nelišil u pacientů léčených inzulinem aspart ve srovnání s humánním inzulinem.
Lipodystrofie:
V místě vpichu může vzniknout lipodystrofie (zahrnující lipohypertrofii, lipoatrofii). Průběžná cyklická změna místa vpichu v dané oblasti snižuje riziko vzniku takovýchto reakcí.
d. Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 70 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
e. Další populační specifika
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u starších pacientů a u pacientů s poškozením ledvin či jater, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
f. Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Specifické předávkování inzulinem nelze definovat, ovšem v následných stádiích se může vyvinout hypoglykemie, pokud jsou pacientovi podány dávky, které jsou vzhledem k jeho potřebě inzulinu příliš vysoké:
• Mírné hypoglykemické příhody mohou být léčeny perorálním podáním glukózy nebo potravin obsahujících cukr. Proto se diabetikům doporučuje, aby s sebou vždy nosili potraviny s obsahem cukru.
• Těžké hypoglykemické příhody, při kterých pacient upadl do bezvědomí, mohou být léčeny intramuskulárním nebo subkutánním podáním glukagonu (0,5 až 1 mg) zaškolenou osobou nebo intravenózní aplikací glukózy zdravotnickým pracovníkem. Glukózu je nutno podat intravenózně i v případě, jestliže pacient nereaguje na glukagon do 10 až 15 minut. Po návratu pacienta k vědomí se doporučuje podat mu perorálně sacharidy jako prevenci relapsu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antidiabetika. Inzuliny a analogy střednědobě nebo dlouze působící v kombinaci s rychle působícími, k injekční aplikaci. ATC kód: A10AD05.
NovoMix 70 je bifázická suspenze 70 % rozpustného inzulínu aspart (rychle působícího analogu humánního inzulinu) a 30 % krystalického protaminového inzulinu aspart (střednědobě působícího analogu humánního inzulinu).
Mechanismus účinku a farmakodynamické účinky
Účinek inzulinu aspart na pokles hladiny glukózy v krvi je důsledkem usnadněného vychytávání glukózy a následné vazby inzulinu na receptory ve svalových a tukových buňkách a současné inhibice uvolňování glukózy z jater.
NovoMix 70 je bifázický inzulin, který obsahuje 70 % rozpustného inzulinu aspart. Tento má rychlý nástup účinku, takže dovoluje podání v těsnější závislosti na jídle (rozmezí 0 až 10 minut od jídla) ve srovnání s rozpustným humánním inzulinem. Krystalická část (30 %) je tvořena krystalickým protaminovým inzulinem aspart, jehož profil účinku se podobá profilu humánního NPH inzulinu.
Je-li NovoMix 70 aplikován subkutánně, nástup účinku nastává v průběhu 10 až 20 minut po injekci. Maximálního účinku je dosaženo za 1 až 4 hodiny po injekci. Účinek trvá 14 až 24 hodin (obrázek 1).
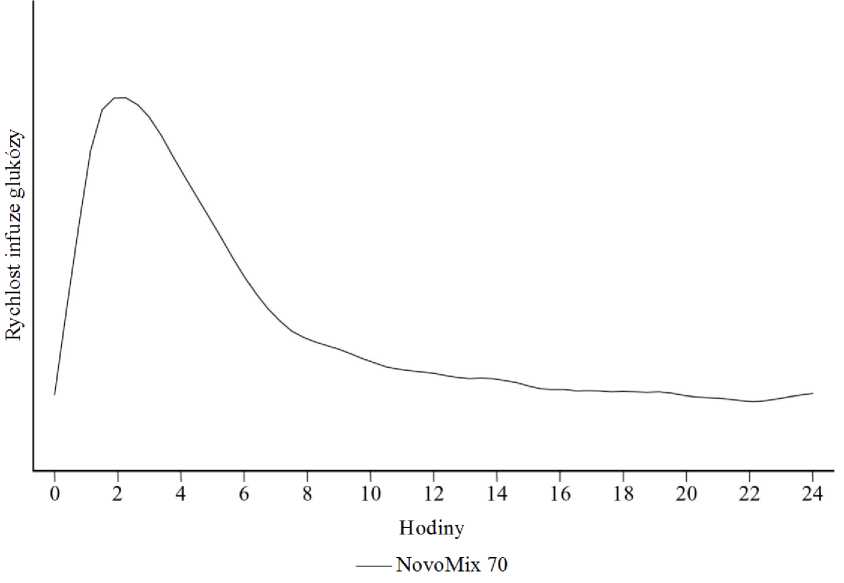
Obrázek 1: Profil aktivity přípravku NovoMix 70 u zdravých bělošských subjektů.
Inzulin aspart je ekvipotentní s humánním inzulinem na molární bázi.
5.2 Farmakokinetické vlastnosti Absorpce, distribuce a eliminace
Substituce aminokyseliny prolinu kyselinou asparagovou v inzulinu aspart na pozici B28 snižuje tendenci ke tvorbě hexamerů tak, jak to bylo pozorováno u rozpustného humánního inzulinu. Inzulin aspart v rozpustné fázi přípravku Novo Mix 70 tvoří 70 % celkového inzulinu, který se ze subkutánní vrstvy vstřebává rychleji, než rozpustná složka bifázického humánního inzulinu. Zbývajících 30 % tvoří krystalická forma krystalický protaminový inzulin aspart, který má prodloužený absorpční profil podobný humánnímu NPH inzulinu.
U zdravých dobrovolníků bylo průměrné maximální koncentrace v séru 645 ± 185 pmol/l dosaženo přibližně za 60 minut po subkutánním podání dávky 0,30 jednotky/kg tělesné hmotnosti. U pacientů s diabetem 2. typu bylo maximální koncentrace dosaženo přibližně po 75 minutách od podání.
U pacientů s diabetem 1. typu byla průměrná maximální koncentrace v séru 721 ± 184 pmol/l dosažena za cca 60 minut od subkutánního podání dávky 0,30 jednotky/kg tělesné hmotnosti.
Zvláštní skupiny pacientů
Farmakokinetika přípravku NovoMix 70 nebyla sledována u dětí, starších pacientů ani u pacientů s poškozením ledvin nebo jater.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
Při zkouškách in vitro, včetně vazby na inzulinová a IGF-1 receptorová místa a účinků na buněčný růst, se inzulin aspart choval podobně jako humánní inzulin. Studie také ukazují, že disociace inzulinu aspart z vazby na inzulinových receptorech je ekvivalentní humánnímu inzulinu.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Glycerol Fenol Metakresol Chlorid zinečnatý
Dihydrát hydrogenfosforečnanu sodného
Chlorid sodný
Protamin-sulfát
Kyselina chlorovodíková (pro úpravu pH)
Hydroxid sodný (pro úpravu pH)
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto tento léčivý přípravek nesmí být mísen s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
Před otevřením: 2 roky.
Během používání nebo pokud NovoMix nosíte jako zásobní: přípravek smí být uchováván maximálně 4 týdny.
6.4 Zvláštní opatření pro uchovávání
Před otevřením: uchovávejte v chladničce (2 °C - 8 °C). Neuchovávejte v blízkosti chladicího zařízení. Chraňte před mrazem.
Během používání nebo pokud NovoMix nosíte jako zásobní: uchovávejte při teplotě do 30 °C.
Chraňte před chladem. Chraňte před mrazem.
Uchovávejte zásobní vložku v krabičce, aby byl přípravek chráněn před světlem.
6.5 Druh obalu a obsah balení
3 ml suspenze v zásobní vložce (sklo typu 1), s pístem (bromobutyl) a pryžovým uzávěrem (bromobutyl/polyisopren). V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání.
Velikosti balení jsou 1, 5 a 10 zásobních vložek. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Jehly a NovoMix 70 Penfill nesmí být s nikým sdíleny. Zásobní vložka se nesmí znovu plnit.
Po vyjmutí přípravku NovoMix 70 Penfill z chladničky je před promícháním inzulinu dle instrukcí pro první použití doporučeno nechat NovoMix 70 Penfill ohřát na pokojovou teplotu.
Tento léčivý přípravek nepoužívejte, pokud si všimnete, že po promíchání tekutina není vodná, stejnoměrně bílá a zakalená.
Pacientovi je třeba zdůraznit, že těsně před použitím je nutné suspenzi přípravku NovoMix 70 promíchat.
NovoMix 70, který zmrzl, nesmí být použit.
Pacient musí být poučen o tom, že po každé aplikaci musí použitou jehlu vyhodit.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
8. REGISTRAČNÍ ČÍSLA
EU/1/00/142/017
EU/1/00/142/018
EU/1/00/142/019
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 1. srpna 2000
Datum posledního prodloužení registrace: 2. července 2010
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské lékové agentury http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
NovoMix 30 FlexPen 100 jednotek/ml injekční suspenze v předplněném peru
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile*/Insulinum aspartum protaminatum cristallinum* v poměru 30/70 (což odpovídá 3,5 mg). 1 předplněné pero obsahuje 3 ml, což odpovídá 300 jednotkám.
* Insulin aspart je vyrobený rekombinantní DNA technologií na Saccharomyces cerevisiae.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční suspenze Zakalená, bílá vodná suspenze.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
NovoMix 30 je indikován k léčbě diabetes mellitus u dospělých, dospívajících a dětí ve věku od 10 let.
4.2 Dávkování a způsob podání
Dávkování
Účinnost inzulinových analogů, včetně inzulinu aspart, se vyjadřuje v jednotkách, zatímco účinnost humánních inzulinů se vyjadřuje v mezinárodních jednotkách.
Dávkování přípravku NovoMix 30 je individuální a je stanoveno v souladu s pacientovými potřebami. Pro dosažení optimální kontroly glykemie je doporučeno monitorování glukózy v krvi a úpravy dávky inzulinu.
U pacientů s diabetem 2. typu lze NovoMix 30 podávat jako monoterapii. NovoMix 30 může být také podáván v kombinaci s perorálními antidiabetiky, pokud je hladina glukózy v krvi nedostatečně kontrolována podáváním těchto perorálních antidiabetik samotných. Pro pacienty s diabetem 2. typu je doporučená počáteční dávka přípravku NovoMix 30 6 jednotek při snídani a 6 jednotek při večeři (večerním jídle). Používání přípravku NovoMix 30 může být také zahájeno podáním 12 jednotek jedenkrát denně při večeři (večerním jídle). Pokud je NovoMix 30 podáván jednou denně a jestliže již bylo dosaženo 30 jednotek, je obecně doporučeno přejít na dávkování dvakrát denně rozdělením dávky na dvě stejné dávky při snídani a při večeři. Jestliže při podávání přípravku NovoMix 30 dvakrát denně dochází k opakovaným hypoglykemickým příhodám během dne, může být ranní dávka rozdělena do ranní dávky a dávky při obědě (dávkování 3krát denně).
Pro úpravu dávky je doporučen následující titrační postup.
Hladiny glukózy v krvi před jídlem
Úprava dávky přípravku NovoMix 30
|
< 4,4 mmol/l |
< 80 mg/dl |
- 2 jednotky |
|
4,4 - 6,1 mmol/l |
80 - 110 mg/dl |
0 |
|
6,2 - 7,8 mmol/l |
111 - 140 mg/dl |
+ 2 jednotky |
|
7,9 - 10 mmol/l |
141 - 180 mg/dl |
+ 4 jednotky |
|
> 10 mmol/l |
> 180 mg/dl |
+ 6 jednotek |
Použity by měly být nejnižší hladiny glukózy v krvi před jídlem naměřené během tří předchozích dní. Dávka by neměla být zvyšována, jestliže během těchto dní došlo k hypoglykemické příhodě. Dávka může být upravována jednou týdně až do dosažení cílové hodnoty HbAic. K vyhodnocení přiměřenosti předchozí dávky by měly být užity hladiny glukózy v krvi naměřené před jídlem.
Individuální inzulinová potřeba pacientů s diabetem 1. typu je obvykle mezi 0,5 a 1,0 jednotkou/kg/den. NovoMix 30 může plně nebo částečně tuto potřebu zajistit.
Úprava dávky může být nutná, pokud pacient podstupuje zvýšenou tělesnou námahu, mění svou obvyklou dietu nebo během současně probíhajícího jiného onemocnění.
Zvláštní skupiny pacientů
Starší_pacienti (>65 let)
NovoMix 30 může být používán staršími pacienty, avšak zkušenost s užíváním přípravku NovoMix 30 v kombinaci s perorálními antidiabetiky u pacientů starších 75 let je omezená.
Monitorování glukózy u starších pacientů by mělo být intenzivnější a dávkování inzulinu aspart by mělo být upraveno individuálně.
Poškození ledvin a _jater
Poškození ledvin nebo jater může snížit pacientovu potřebu inzulinu.
Monitorování glukózy u pacientů s poškozením ledvin nebo jater by mělo být intenzivnější a dávkování inzulinu aspart by mělo být upraveno individuálně.
Pediatrická populace
NovoMix 30 může být používán u dospívajících a dětí ve věku od 10 let, pokud je preferován premixovaný inzulin. Pro děti ve věku od 6 do 9 let existují s přípravkem NovoMix 30 omezené klinické zkušenosti (viz bod 5.1).
Pro použití přípravku NovoMix 30 u dětí ve věku do 6 let nejsou dostupné žádné údaje Přechod z jiných inzulínových přípravků
Při převodu pacienta z bifázického humánního inzulinu na NovoMix 30 začněte se stejnou dávkou a ve stejném režimu. Poté titrujte podle individuálních potřeb pacienta (viz výše doporučený titrační postup).
Během přechodu a několik týdnů poté je doporučeno pečlivé monitorování glukózy (viz bod 4.4). Způsob podání
NovoMix 30 je bifázická suspenze inzulinového analogu inzulin aspart. Suspenze obsahuje rychle působící a střednědobě působící inzulin aspart v poměru 30/70.
NovoMix 30 je určen pouze pro subkutánní podání.
NovoMix 30 je podáván subkutánně do stehna nebo břišní stěny. Pokud je to přijatelné, je možné ho aplikovat do oblasti hýždí nebo deltoidní oblasti. Injekční místa ve stejné oblasti je vždy třeba měnit rotačním způsobem, aby se snížilo riziko lipodystrofie. Vliv různých míst vpichu na absorpci přípravku NovoMix 30 nebyl sledován. Trvání účinku se mění podle dávky, místa vpichu, prokrvení,
teploty a fyzické aktivity.
NovoMix 30 má rychlejší nástup účinku než humánní bifázický inzulin a měl by být tedy obecně podáván bezprostředně před jídlem. Pokud je to nutné, může být NovoMix 30 podán i brzy po jídle.
Podání pomocí pera FlexPen
NovoMix 30 FlexPen je předplněné pero, které je určeno k použití spolu jehlami NovoFine nebo NovoTwist. Dávky lze nastavit od 1 do 60 jednotek v přírůstcích po 1 jednotce.
NovoMix 30 FlexPen je barevně kódován a je k němu přiložena příbalová informace s podrobným návodem k použití, jenž by měl být dodržován.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
NovoMix 30 nesmí být podáván intravenózně, neboť to může vést k těžké hypoglykemii. Vyvarujte se intramuskulárního podání. NovoMix 30 není určen pro použití v inzulinových infuzních pumpách.
Před cestou mezi různými časovými pásmy by se pacient měl poradit s lékařem. Cestování mezi různými časovými pásmy může totiž znamenat, že pacient bude muset užívat inzulin a přijímat jídla v odlišných časech.
Hyperglykemie
Nedostatečné dávkování nebo přerušovaná léčba, zejména u diabetu 1. typu, může vést k hyperglykemii a diabetické ketoacidóze. První symptomy hyperglykemie se obvykle v průběhu hodin nebo dní stupňují. Mezi ně patří žízeň, zvýšená frekvence močení, nauzea, zvracení, ospalost, zarudlá suchá kůže, sucho v ústech, ztráta chuti k jídlu či acetonový zápach dechu. U diabetu 1. typu mohou vést neléčené hyperglykemické stavy až k diabetické ketoacidóze, která je potenciálně letální.
Hypoglykemie
Vynechání jídla nebo neplánovaná namáhavá fyzická aktivita mohou vést k hypoglykemii.
Hypoglykemie se může objevit, pokud je dávka inzulinu příliš vysoká ve vztahu k potřebě inzulinu.
V případě hypoglykemie či podezření na hypoglykemii nesmí být NovoMix podáván. Poté co u pacienta dojde ke stabilizaci hladiny glukózy, měla by být zvážena úprava dávky (viz body 4.2, 4.8 a 4.9).
Ve srovnání s bifázickým humánním inzulinem může mít NovoMix 30 výraznější účinek na snížení hladiny glukózy až 6 hodin po aplikaci. Toto je třeba u jednotlivých pacientů kompenzovat úpravou dávky inzulinu a/nebo příjmu jídla.
Pacienti, u kterých se kontrola diabetu výrazně zlepšila, např. při intenzifikované inzulinové terapii, mohou zaznamenat změnu obvyklých varovných příznaků hypoglykemie, a měli by být patřičně poučeni. U pacientů s dlouholetým diabetem mohou běžné varovné symptomy vymizet.
Přísnější kontrola hladiny glukózy může zvyšovat možnost vzniku hypoglykemických příhod, a proto je během intenzifikace dávky vyžadována speciální pozornost (viz bod 4.2).
Protože NovoMix 30 má být aplikován v těsné závislosti na jídle, je třeba zvážit rychlý nástup účinku u pacientů s doprovodnými nemocemi nebo při léčbě, během níž může být očekávána zpožděná absorpce jídla.
Přidružené onemocnění, zejména infekce a horečnaté stavy, obvykle zvyšují pacientovu potřebu inzulinu. Přidružené onemocnění ledvin, jater či onemocnění ovlivňující nadledviny, podvěsek mozkový nebo štítnou žlázu může vyžadovat změny v dávce inzulinu.
Pokud je pacient převeden na jiný typ inzulinových přípravků, může dojít ke změně či potlačení časných varovných příznaků hypoglykemie oproti těm, které se u pacienta projevovaly u předchozího inzulinu.
Převedení z jiných inzulínových přípravků
Převod pacienta na jiný typ nebo značku inzulinu by měl probíhat pod přísným lékařským dozorem. Změny v síle, značce (výrobce), typu, původu (zvířecí inzulin, humánní inzulin nebo analog inzulinu) a/nebo metodě výroby (rekombinantní DNA versus inzulin ze zvířecích zdrojů) mohou vést k potřebě změnit dávkování. Pacienti převádění na přípravek NovoMix 30 z jiných typů inzulinu mohou vyžadovat vyšší počet injekcí denně nebo změnu dávkování oproti jejich obvyklým inzulinovým léčivým přípravkům. Pokud je potřeba přizpůsobit dávkování, může k tomu dojít při první dávce nebo během prvních týdnů či měsíců.
Reakce v místě vpichu
Tak jako při každé léčbě inzulinem se mohou objevit reakce v místě vpichu, které se projevují bolestivostí, zarudnutím, kopřivkou, zánětem, podlitinami, otoky a svěděním. Pravidelné obměňování injekčního místa v rámci jedné oblasti snižuje riziko vzniku těchto reakcí. Reakce obvykle vymizí do několika dnů nebo týdnů. Ve vzácných případech si mohou reakce v místě vpichu vyžádat vysazení přípravku NovoMix 30.
Kombinace přípravku NovoMix s pioglitazonem
Pokud byl pioglitazon užíván v kombinaci s inzulinem, byly hlášeny případy srdečního selhání a to zvláště u pacientů s rizikovými faktory pro vznik srdečního selhání. Tuto skutečnost je nutno vzít v úvahu, pokud je zvažována léčba pioglitazonem v kombinaci s přípravkem NovoMix. Pokud je tato kombinace použita, měli by být pacienti sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení hmotnosti a edém. Pioglitazon by měl být vysazen, pokud se objeví jakékoliv zhoršení srdečních příznaků.
Protilátky proti inzulinu
Podávání inzulinu může vyvolat tvorbu protilátek proti inzulinu. Ve vzácných případech může přítomnost těchto protilátek vyžadovat úpravu dávky inzulinu, aby se usměrnila tendence k hyper- či hypoglykemii.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
U řady léčivých přípravků je známa interakce s glukózovým metabolismem.
Následující látky mohou snižovat pacientovu potřebu inzulinu:
Perorální antidiabetika, inhibitory monoaminoxidázy (IMAO), beta-blokátory, angiotensin konvertujícího enzymu (ACE) inhibitory, salicyláty, anabolické steroidy a sulfonamidy.
Následující látky mohou zvyšovat pacientovu potřebu inzulinu:
Perorální kontraceptiva, thiazidy, glukokortikoidy, thyreoidální hormony, sympatomimetika, růstový hormon a danazol.
Beta-blokátory mohou zakrývat příznaky hypoglykemie.
Oktreotid/lanreotid mohou buď zvýšit nebo snížit potřebu inzulínu. Alkohol může zesílit nebo snížit hypoglykemický účinek inzulinu.
4.6 Fertilita, těhotenství a kojení Těhotenství
Klinické zkušenosti s užíváním přípravku NovoMix 30 v těhotenství jsou omezené.
Reprodukční studie na zvířatech neukázaly žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče embryotoxicity nebo teratogenity.
Obecně platí, že v průběhu celého těhotenství a při jeho plánování se doporučují intenzifikované kontroly hladin glukózy v krvi a monitorování těhotných diabetiček. Potřeba inzulinu obvykle v průběhu prvního trimestru klesne a následně se zvyšuje ve druhém a třetím trimestru. Po porodu se potřeba inzulinu rychle vrací na úroveň před těhotenstvím.
Kojení
Léčba přípravkem NovoMix 30 při kojení není omezena. Léčba kojících matek inzulinem nepředstavuje pro dítě žádné riziko. Dávkování přípravku NovoMix 30 však může vyžadovat úpravu.
Fertilita
Reprodukční studie se zvířaty neodhalily žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče fertility.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Pacientova schopnost koncentrace a reakce se může v důsledku hypoglykemie zhoršit. To může představovat riziko v situacích, kde jsou tyto schopnosti zvláště důležité (např. řízení vozu nebo obsluha strojů).
Pacienti by měli být poučeni o opatřeních, jak se vyvarovat vzniku hypoglykemie během řízení či během obsluhy strojů. Je to důležité zvláště u pacientů, kteří mají slabé nebo žádné varovné příznaky hypoglykemie nebo kteří mají časté epizody hypoglykemie. V těchto případech je třeba vhodnost řízení či obsluhy strojů zvážit.
4.8 Nežádoucí účinky
a. Souhrn bezpečnostního profilu
Nežádoucí účinky pozorované u pacientů užívajících NovoMix jsou převážně způsobeny farmakologickým efektem inzulinu aspart.
Nejčastěji hlášeným nežádoucím účinkem během léčby je hypoglykemie. Frekvence výskytu hypoglykemie se mění s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly, viz bod c níže.
Na počátku inzulinové léčby se mohou vyskytnout poruchy refrakce, edém a reakce v místě vpichu (bolest, zarudnutí, kopřivka, zánět, podlitiny, otoky a svědění v místě vpichu). Tyto reakce jsou obvykle přechodné povahy. Rychlé zlepšení hladiny glukózy v krvi může být spojeno s akutní bolestivou neuropatií, která je obvykle reverzibilní. Intenzifikace inzulinové terapie s prudkým zlepšením glykemické kontroly může být spojena s přechodným zhoršením diabetické retinopatie, zatímco dlouhodobé zlepšení glykemické kontroly snižuje riziko progrese diabetické retinopatie.
b. Seznam nežádoucích účinků v tabulce
Nežádoucí účinky uvedené níže jsou založeny na údajích z klinických studií a jsou klasifikovány podle MedDRA frekvence výskytu a třídy orgánových systémů. Frekvence výskytu jsou definovány podle následující konvence: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000), velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
|
Poruchy imunitního systému |
Méně časté - Kopřivka, vyrážky, erupce |
|
Velmi vzácné - Anafylaktické reakce* | |
|
Poruchy metabolismu a výživy |
Velmi časté - Hypoglykemie* |
|
Poruchy nervového systému |
Vzácné - Periferní neuropatie (bolestivá neuropatie) |
|
Poruchy oka |
Méně časté - Poruchy refrakce |
|
Méně časté - Diabetická retinopatie | |
|
Poruchy kůže a podkožní tkáně |
Méně časté - Lipodystrofie* |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté - Otoky |
|
Méně časté - Reakce v místě vpichu |
viz bod c.
c. Popis vybraných nežádoucích účinků Anafylaktické reakce:
Vznik generalizovaných hypersenzitivních reakcí (zahrnujících generalizované kožní vyrážky, svědění, pocení, gastrointestinální obtíže, angioneurotický edém, obtížné dýchání, palpitace a pokles krevního tlaku) je velmi vzácný, avšak může být potenciálně život ohrožující.
Hypoglykemie:
Nejčastěji hlášeným nežádoucím účinkem je hypoglykemie. Může nastat v případě, kdy je dávka inzulinu příliš vysoká vzhledem k inzulinové potřebě. Těžká hypoglykemie může vést k bezvědomí a/nebo křečím a může vyústit v přechodné nebo trvalé poškození mozkových funkcí nebo dokonce vést ke smrti. Příznaky hypoglykemie se obvykle objevují náhle. Mohou zahrnovat studený pot, chladnou bledou pokožku, únavu, nervozitu nebo třes, úzkost, neobvyklou vyčerpanost nebo slabost, zmatenost, potíže s koncentrací, ospalost, velký hlad, změny vidění, bolest hlavy, nauzeu a palpitaci.
V klinických studiích se frekvence výskytu hypoglykemií měnila s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly. Během klinických studií se celkový výskyt hypoglykemií nelišil u pacientů léčených inzulinem aspart ve srovnání s humánním inzulinem.
Lipodystrofie:
V místě vpichu může vzniknout lipodystrofie (zahrnující lipohypertrofii, lipoatrofii). Průběžná cyklická změna místa vpichu v dané oblasti snižuje riziko vzniku takovýchto reakcí.
d. Pediatrická populace
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u pediatrické populace, jakékoliv rozdíly oproti širším
zkušenostem v obecné populaci.
e. Další populační specifika
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u starších pacientů a u pacientů s poškozením ledvin či jater, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
f. Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Specifické předávkování inzulinem nelze definovat, ovšem v následných stádiích se může vyvinout hypoglykemie, pokud jsou pacientovi podány dávky, které jsou vzhledem k jeho potřebě inzulinu příliš vysoké:
• Mírné hypoglykemické příhody mohou být léčeny perorálním podáním glukózy nebo potravin obsahujících cukr. Proto se diabetikům doporučuje, aby s sebou vždy nosili potraviny s obsahem cukru.
• Těžké hypoglykemické příhody, při kterých pacient upadl do bezvědomí, mohou být léčeny intramuskulárním nebo subkutánním podáním glukagonu (0,5 až 1 mg) zaškolenou osobou nebo intravenózní aplikací glukózy zdravotnickým pracovníkem. Glukózu je nutno podat intravenózně i v případě, jestliže pacient nereaguje na glukagon do 10 až 15 minut. Po návratu pacienta k vědomí se doporučuje podat mu perorálně sacharidy jako prevenci relapsu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antidiabetika. Inzuliny a analogy střednědobě nebo dlouze působící v kombinaci s rychle působícími, k injekční aplikaci. ATC kód: A10AD05.
NovoMix 30 je bifázická suspenze 30 % rozpustného inzulinu aspart (rychle působícího analogu humánního inzulinu) a 70 % krystalického protaminového inzulinu aspart (střednědobě působícího analogu humánního inzulinu).
Mechanismus účinku a farmakodynamické účinky
Účinek inzulinu aspart na pokles hladiny glukózy v krvi je důsledkem usnadněného vychytávání glukózy a následné vazby inzulinu na receptory ve svalových a tukových buňkách a současné inhibice uvolňování glukózy z jater.
NovoMix 30 je bifázický inzulin, který obsahuje 30 % rozpustného inzulinu aspart. Tento má rychlý nástup účinku, takže dovoluje podání v těsnější závislosti na jídle (rozmezí 0 až 10 minut od jídla) ve srovnání s rozpustným humánním inzulinem. Krystalická část (70 %) je tvořena krystalickým protaminovým inzulinem aspart, jehož profil účinku se podobá profilu humánního NPH inzulinu.
Je-li NovoMix 30 aplikován subkutánně, nástup účinku nastává v průběhu 10 až 20 minut po injekci. Maximálního účinku je dosaženo za 1 až 4 hodiny po injekci. Účinek trvá až 24 hodin (obrázek 1) .
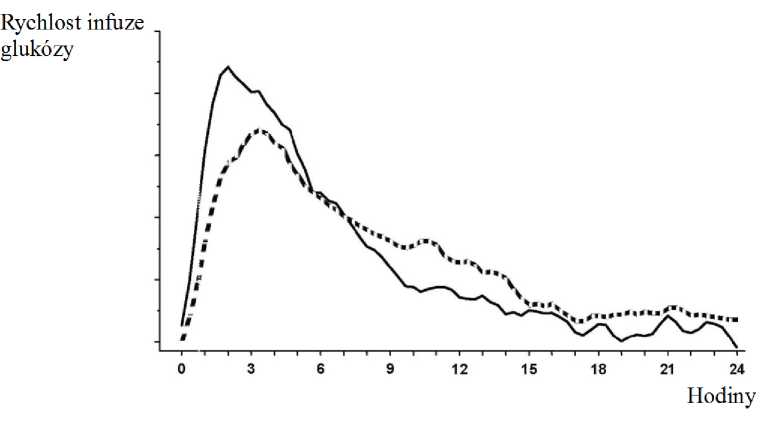
Obrázek 1: Profil aktivity přípravku NovoMix 30 (—) a bifázického humánního inzulínu 30 (---) u zdravých subjektů.
Klinická účinnost a bezpečnost
V 3 měsíční klinické studii u pacientů s diabetem 1. a 2. typu byla kontrola glykosylovaného hemoglobinu při léčbě přípravkem NovoMix 30 stejná, jako při léčbě bifázickým humánním inzulinem 30. Inzulin aspart je ekvipotentní s humánním inzulinem na molární bázi. V porovnání
s bifázickým humánním inzulinem 30 vedlo podávání přípravku NovoMix 30 před snídaní a večeří k nižší postprandiální hladině glukózy v krvi po obou jídlech (snídaně a večeře).
Meta-analýza zahrnující devět studií s pacienty s diabetem 1. typu i s diabetem 2. typu prokázala, že hladina glukózy v krvi nalačno byla vyšší u pacientů léčených přípravkem NovoMix 30 než u pacientů léčených bifázickým humánním inzulinem 30.
V jedné klinické studii bylo 341 pacientů s diabetem 2. typu randomizováno buď pouze s přípravkem NovoMix 30 nebo v kombinaci s metforminem nebo v kombinaci metformin společně se sulfonylureou. Primární účinnost - HbA1c po 16 týdnech léčby se nelišila mezi pacienty léčenými přípravkem NovoMix 30 v kombinaci s metforminem a pacienty léčenými metforminem a sulfonylureou. V této studii mělo 57 % pacientů výchozí hodnotu HbA1c nad 9 %; u pacientů léčených přípravkem NovoMix 30 v kombinaci s metforminem došlo k významnému snížení hodnoty HbA1c ve srovnání s pacienty léčenými kombinací metformin a sulfonylurea.
V jedné klinické studii byli pacienti s diabetem 2. typu, kteří nebyli dostatečně kompenzováni samotnými perorálními antidiabetiky, randomizováni v jedné větvi s přípravkem NovoMix 30 podávaným 2x denně (117 pacientů) a ve druhé větvi s inzulinem glargin podávaným 1x denně (116 pacientů). Po 28 týdnech léčby při dodržování dávkovacího postupu popsaného v bodě 4.2 bylo průměrné snížení HbA1c u přípravku NovoMix 30 rovno 2,8 % (průměrná výchozí hodnota = 9,7 %).
U přípravku NovoMix 30 dosáhlo 66 % a 42 % pacientů úrovně HbA1c pod 7 % respektive 6,5 % a průměrná hodnota FPG byla snížena přibližně o 7 mmol/l (z výchozí hodnoty 14,0 mmol/l na
7,1 mmol/l).
U pacientů s diabetem 2. typu meta-analýza prokázala snížené riziko celkových nočních hypoglykemických příhod a závažných hypoglykémií u přípravku NovoMix 30 ve srovnání s bifázickým humánním inzulinem 30. Riziko celkových hypoglykemických příhod v denní době bylo u pacientů léčených přípravkem NovoMix 30 zvýšené.
Pediatrická populace
Byla prováděna 16týdenní klinická studie, která srovnávala kompenzaci postprandiální glykémie přípravkem NovoMix 30 s kompenzací humánním inzulinem/bifázickým humánním inzulínem 30 v obou případech podávanými ve vztahu k příjmu jídla a v kombinaci s inzulinem NPH podávaným před spaním, a to u 167 pacientů ve věku 10 až 18 let. Průměrná hodnota HbAJc zůstala během studie u obou léčených skupin podobná jako základní hodnota a v počtu hypoglykemií nebylo rozdílu mezi přípravkem NovoMix 30 nebo bifázickým humánním inzulinem 30.
V menší a mladší skupině (54 pacientů, věkové rozmezí 6 - 12 let) léčené ve dvojitě zaslepené zkřížené klinické studii (12 týdnů trvání každé léčby) byly počet hypoglykemických epizod i zvýšení hladiny postprandiální glykémie významně nižší u přípravku NovoMix 30 ve srovnání s bifázickým humánním inzulinem 30. Konečná hodnota HbAJc byla ve skupině léčené bifázickým humánním inzulinem 30 významně nižší v porovnání s přípravkem NovoMix 30.
5.2 Farmakokinetické vlastnosti
Absorpce, distribuce a eliminace
Substituce aminokyseliny prolinu kyselinou asparagovou v inzulinu aspart na pozici B28 snižuje tendenci ke tvorbě hexamerů tak, jak to bylo pozorováno u rozpustného humánního inzulinu. Inzulin aspart v rozpustné fázi přípravku Novo Mix 30 tvoří 30 % celkového inzulinu, který se ze subkutánní vrstvy vstřebává rychleji, než rozpustná složka bifázického humánního inzulinu. Zbývajících 70 % tvoří krystalická forma krystalický protaminový inzulin aspart, který má prodloužený absorpční profil podobný humánnímu NPH inzulinu.
Maximální koncentrace inzulinu v séru je u přípravku NovoMix 30 v průměru o 50 % vyšší než u bifázického humánního inzulinu 30. Čas potřebný k dosažení maximální koncentrace je v průměru poloviční než u bifázického humánního inzulinu 30. U zdravých dobrovolníků bylo dosaženo průměrné maximální koncentrace v séru 140 ± 32 pmol/l asi 60 minut po subkutánní aplikaci dávky 0,20 jednotky/kg tělesné hmotnosti. Průměrný poločas (t./2) přípravku NovoMix 30, odrážející absorpční rychlost frakce vázané na protamin, byl asi 8 - 9 hodin. Hladina inzulinu v séru se vrátila na bazální hodnotu za 15 - 18 hodin po subkutánní dávce. U pacientů s diabetem 2. typu bylo maximální koncentrace dosaženo za 95 minut po aplikaci dávky a nejméně za 14 hodin po aplikaci dávky byly koncentrace v séru měřitelné.
Zvláštní skupiny pacientů
Farmakokinetika přípravku NovoMix 30 nebyla sledována u starších pacientů ani u pacientů s poškozením ledvin nebo jater.
Pediatrická populace
Farmakokinetika přípravku NovoMix 30 nebyla u dětí nebo dospívajících sledována. Avšak u dětí (6 - 12 let) a dospívajících (13 - 17 let) s diabetem 1. typu byly sledovány farmakokinetické a farmakodynamické vlastnosti rozpustného inzulinu aspart. V obou věkových skupinách byl inzulin aspart rychle absorbován s podobným tnax jako u dospělých. Nicméně Cmax se v jednotlivých věkových skupinách odlišovala, s důrazem na důležitost individuální titrace inzulinu aspart.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
Při zkouškách in vitro, včetně vazby na inzulinová a IGF-1 receptorová místa a účinků na buněčný růst, se inzulin aspart choval podobně jako humánní inzulin. Studie také ukazují, že disociace inzulinu aspart z vazby na inzulinových receptorech je ekvivalentní humánnímu inzulinu.
FARMACEUTICKÉ ÚDAJE
6.
6.1 Seznam pomocných látek
Glycerol Fenol Metakresol Chlorid zinečnatý
Dihydrát hydrogenfosforečnanu sodného
Chlorid sodný
Protamin-sulfát
Kyselina chlorovodíková (pro úpravu pH)
Hydroxid sodný (pro úpravu pH)
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nej sou k dispozici, a proto tento léčivý přípravek nesmí být mísen s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
Před otevřením: 2 roky.
Během používání nebo pokud NovoMix nosíte jako zásobní: přípravek smí být uchováván maximálně 4 týdny.
6.4 Zvláštní opatření pro uchovávání
Před otevřením: uchovávejte v chladničce (2 °C - 8 °C). Neuchovávejte v blízkosti chladicího zařízení. Chraňte před mrazem.
Během používání nebo pokud NovoMix nosíte jako zásobní: uchovávejte při teplotě do 30 °C. Chraňte před chladem. Chraňte před mrazem.
FlexPen uchovávejte s nasazeným krytem, aby byl přípravek chráněn před světlem.
6.5 Druh obalu a obsah balení
3 ml suspenze v zásobní vložce (sklo typu 1), s pístem (bromobutyl) a pryžovým uzávěrem (bromobutyl/polyisopren) v jednorázovém vícedávkovém předplněném peru zhotoveném z polypropylenu. V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání.
Velikosti balení jsou 1 (včetně jehel nebo bez jehel), 5 (bez jehel) a 10 (bez jehel) předplněných per. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Jehly a NovoMix 30 FlexPen nesmí být s nikým sdíleny. Zásobní vložka se nesmí znovu plnit.
Po vyjmutí přípravku NovoMix 30 FlexPen z chladničky je před promícháním inzulinu dle instrukcí pro první použití doporučeno nechat NovoMix 30 FlexPen ohřát na pokojovou teplotu.
Tento léčivý přípravek nepoužívejte, pokud si všimnete, že po promíchání tekutina není vodná, stejnoměrně bílá a zakalená.
Pacientovi je třeba zdůraznit, že těsně před použitím je nutné suspenzi přípravku NovoMix 30 promíchat.
NovoMix 30, který zmrzl, nesmí být použit.
Pacient musí být poučen o tom, že po každé aplikaci musí použitou jehlu vyhodit.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
8. REGISTRAČNÍ ČÍSLA
EU/1/00/142/009
EU/1/00/142/010
EU/1/00/142/023
EU/1/00/142/024
EU/1/00/142/025
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 1. srpna 2000
Datum posledního prodloužení registrace: 2. července 2010
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské lékové agentury http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
NovoMix 50 FlexPen 100 jednotek/ml injekční suspenze v předplněném peru
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile*/Insulinum aspartum protaminatum cristallinum* v poměru 50/50 (což odpovídá 3,5 mg). 1 předplněné pero obsahuje 3 ml, což odpovídá 300 jednotkám.
* Insulin aspart je vyrobený rekombinantní DNA technologií na Saccharomyces cerevisiae.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční suspenze Zakalená, bílá vodná suspenze.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
NovoMix 50 je indikován k léčbě diabetes mellitus u dospělých.
4.2 Dávkování a způsob podání
Dávkování
Účinnost inzulinových analogů, včetně inzulinu aspart, se vyjadřuje v jednotkách, zatímco účinnost humánních inzulinů se vyjadřuje v mezinárodních jednotkách.
Dávkování přípravku NovoMix 50 je individuální a je stanoveno v souladu s pacientovými potřebami. Pro dosažení optimální kontroly glykemie je doporučeno monitorování glukózy v krvi a úpravy dávky inzulinu.
Individuální inzulinová potřeba je obvykle mezi 0,5 a 1,0 jednotkou/kg/den. NovoMix 50 může plně nebo částečně tuto potřebu zajistit.
U pacientů s diabetem 2. typu lze NovoMix 50 podávat jako monoterapii nebo v kombinaci s metforminem, pokud je hladina glukózy v krvi nedostatečně kontrolována podáváním metforminu samotného.
Úprava dávky může být nutná, pokud pacient podstupuje zvýšenou tělesnou námahu, mění svou obvyklou dietu nebo během současně probíhajícího jiného onemocnění.
Zvláštní skupiny pacientů
V případě starších pacientů (> 65 let) a pacientů s poškozením jater či ledvin by mělo být monitorování glukózy intenzifikováno a dávka inzulinu aspart by měla být upravena individuálně.
Poškození ledvin nebo jater může snížit pacientovu potřebu inzulinu.
Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 50 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
Přechod z jiných inzulínových přípravků
Přechod na NovoMix 50 z jiných inzulínových přípravků může vyžadovat úpravu dávky a času podání. Během přechodu a několik týdnů poté je doporučeno pečlivé monitorování glukózy (viz bod 4.4).
Způsob podání
NovoMix 50 je bifázická suspenze inzulinového analogu inzulin aspart. Suspenze obsahuje rychle působící a střednědobě působící inzulin aspart v poměru 50/50.
NovoMix 50 je určen pouze pro subkutánní podání.
NovoMix 50 je podáván subkutánně do stehna nebo břišní stěny. Pokud je to přijatelné, je možné ho aplikovat do oblasti hýždí nebo deltoidní oblasti. Injekční místa ve stejné oblasti je vždy třeba měnit rotačním způsobem, aby se snížilo riziko lipodystrofie. Vliv různých míst vpichu na absorpci přípravku NovoMix 50 nebyl sledován. Trvání účinku se mění podle dávky, místa vpichu, prokrvení, teploty a fyzické aktivity.
NovoMix 50 má rychlejší nástup účinku než humánní bifázický inzulin a měl by být tedy obecně podáván bezprostředně před jídlem. Pokud je to nutné, může být NovoMix 50 podán i brzy po jídle.
Podání pomocí pera FlexPen
NovoMix 50 FlexPen je předplněné pero, které je určeno k použití spolu jehlami NovoFine nebo NovoTwist. Dávky lze nastavit od 1 do 60 jednotek v přírůstcích po 1 jednotce.
NovoMix 50 FlexPen je barevně kódován a je k němu přiložena příbalová informace s podrobným návodem k použití, jenž by měl být dodržován.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
NovoMix 50 nesmí být podáván intravenózně, neboť to může vést k těžké hypoglykemii. Vyvarujte se intramuskulárního podání. NovoMix 50 není určen pro použití v inzulinových infuzních pumpách.
Před cestou mezi různými časovými pásmy by se pacient měl poradit s lékařem. Cestování mezi různými časovými pásmy může totiž znamenat, že pacient bude muset užívat inzulin a přijímat jídla v odlišných časech.
Hyperglykemie
Nedostatečné dávkování nebo přerušovaná léčba, zejména u diabetu 1. typu, může vést k hyperglykemii a diabetické ketoacidóze. První symptomy hyperglykemie se obvykle v průběhu hodin nebo dní stupňují. Mezi ně patří žízeň, zvýšená frekvence močení, nauzea, zvracení, ospalost, zarudlá suchá kůže, sucho v ústech, ztráta chuti k jídlu či acetonový zápach dechu. U diabetu 1. typu mohou vést neléčené hyperglykemické stavy až k diabetické ketoacidóze, která je potenciálně letální.
Hypoglykemie
Vynechání jídla nebo neplánovaná namáhavá fyzická aktivita mohou vést k hypoglykemii.
Hypoglykemie se může objevit, pokud je dávka inzulinu příliš vysoká ve vztahu k potřebě inzulinu.
V případě hypoglykemie či podezření na hypoglykemii nesmí být NovoMix podáván. Poté co u pacienta dojde ke stabilizaci hladiny glukózy, měla by být zvážena úprava dávky (viz body 4.2, 4.8 a 4.9).
Pacienti, u kterých se kontrola diabetu výrazně zlepšila, např. při intenzifikované inzulinové terapii, mohou zaznamenat změnu obvyklých varovných příznaků hypoglykemie a měli by být patřičně poučeni. U pacientů s dlouholetým diabetem mohou běžné varovné symptomy vymizet.
Protože NovoMix 50 má být aplikován v těsné závislosti na jídle, je třeba zvážit rychlý nástup účinku u pacientů s doprovodnými nemocemi nebo při léčbě, během níž může být očekávána zpožděná absorpce jídla.
Přidružené onemocnění, zejména infekce a horečnaté stavy, obvykle zvyšují pacientovu potřebu inzulinu. Přidružené onemocnění ledvin, jater či onemocnění ovlivňující nadledviny, podvěsek mozkový nebo štítnou žlázu může vyžadovat změny v dávce inzulinu.
Pokud je pacient převeden na jiný typ inzulinových přípravků, může dojít ke změně či potlačení časných varovných příznaků hypoglykemie oproti těm, které se u pacienta projevovaly u předchozího inzulinu.
Převedení z jiných inzulínových přípravků
Převod pacienta na jiný typ nebo značku inzulinu by měl probíhat pod přísným lékařským dozorem. Změny v síle, značce (výrobce), typu, původu (zvířecí inzulin, humánní inzulin nebo analog inzulinu) a/nebo metodě výroby (rekombinantní DNA versus inzulin ze zvířecích zdrojů) mohou vést k potřebě změnit dávkování. Pacienti převádění na přípravek NovoMix 50 z jiných typů inzulinu mohou vyžadovat vyšší počet injekcí denně nebo změnu dávkování oproti jejich obvyklým inzulinovým léčivým přípravkům. Pokud je potřeba přizpůsobit dávkování, může k tomu dojít při první dávce nebo během prvních týdnů či měsíců.
Reakce v místě vpichu
Tak jako při každé léčbě inzulinem se mohou objevit reakce v místě vpichu, které se projevují bolestivostí, zarudnutím, kopřivkou, zánětem, podlitinami, otoky a svěděním. Pravidelné obměňování injekčního místa v rámci jedné oblasti snižuje riziko vzniku těchto reakcí. Reakce obvykle vymizí do několika dnů nebo týdnů. Ve vzácných případech si mohou reakce v místě vpichu vyžádat vysazení přípravku NovoMix 50.
Kombinace přípravku NovoMix s pioglitazonem
Pokud byl pioglitazon užíván v kombinaci s inzulinem, byly hlášeny případy srdečního selhání a to zvláště u pacientů s rizikovými faktory pro vznik srdečního selhání. Tuto skutečnost je nutno vzít v úvahu, pokud je zvažována léčba pioglitazonem v kombinaci s přípravkem NovoMix. Pokud je tato kombinace použita, měli by být pacienti sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení hmotnosti a edém. Pioglitazon by měl být vysazen, pokud se objeví jakékoliv zhoršení srdečních příznaků.
Protilátky proti inzulinu
Podávání inzulínu může vyvolat tvorbu protilátek proti inzulínu. Ve vzácných případech může přítomnost těchto protilátek vyžadovat úpravu dávky inzulinu, aby se usměrnila tendence k hyper- či hypoglykemii.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
U řady léčivých přípravků je známa interakce s glukózovým metabolismem.
Následující látky mohou snižovat pacientovu potřebu inzulinu:
Perorální antidiabetika, inhibitory monoaminoxidázy (IMAO), beta-blokátory, angiotensin konvertujícího enzymu (ACE) inhibitory, salicyláty, anabolické steroidy a sulfonamidy.
Následující látky mohou zvyšovat pacientovu potřebu inzulinu:
Perorální kontraceptiva, thiazidy, glukokortikoidy, thyreoidální hormony, sympatomimetika, růstový hormon a danazol.
Beta-blokátory mohou zakrývat příznaky hypoglykemie.
Oktreotid/lanreotid mohou buď zvýšit nebo snížit potřebu inzulinu.
Alkohol může zesílit nebo snížit hypoglykemický účinek inzulinu.
4.6 Fertilita, těhotenství a kojení Těhotenství
Klinické zkušenosti s užíváním přípravku NovoMix 50 v těhotenství jsou omezené.
Reprodukční studie na zvířatech neukázaly žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče embryotoxicity nebo teratogenity.
Obecně platí, že v průběhu celého těhotenství a při jeho plánování se doporučují intenzifikované kontroly hladin glukózy v krvi a monitorování těhotných diabetiček. Potřeba inzulinu obvykle v průběhu prvního trimestru klesne a následně se zvyšuje ve druhém a třetím trimestru. Po porodu se potřeba inzulinu rychle vrací na úroveň před těhotenstvím.
Kojení
Léčba přípravkem NovoMix 50 při kojení není omezena. Léčba kojících matek inzulinem nepředstavuje pro dítě žádné riziko. Dávkování přípravku NovoMix 50 však může vyžadovat úpravu.
Fertilita
Reprodukční studie se zvířaty neodhalily žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče fertility.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Pacientova schopnost koncentrace a reakce se může v důsledku hypoglykemie zhoršit. To může představovat riziko v situacích, kde jsou tyto schopnosti zvláště důležité (např. řízení vozu nebo obsluha strojů).
Pacienti by měli být poučeni o opatřeních, jak se vyvarovat vzniku hypoglykemie během řízení či během obsluhy strojů. Je to důležité zvláště u pacientů, kteří mají slabé nebo žádné varovné příznaky hypoglykemie nebo kteří mají časté epizody hypoglykemie. V těchto případech je třeba vhodnost řízení či obsluhy strojů zvážit.
4.8 Nežádoucí účinky
a. Souhrn bezpečnostního profilu
Nežádoucí účinky pozorované u pacientů užívajících NovoMix jsou převážně způsobeny farmakologickým efektem inzulinu aspart.
Nejčastěji hlášeným nežádoucím účinkem během léčby je hypoglykemie. Frekvence výskytu hypoglykemie se mění s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly, viz bod c níže.
Na počátku inzulinové léčby se mohou vyskytnout poruchy refrakce, edém a reakce v místě vpichu (bolest, zarudnutí, kopřivka, zánět, podlitiny, otoky a svědění v místě vpichu). Tyto reakce jsou obvykle přechodné povahy. Rychlé zlepšení hladiny glukózy v krvi může být spojeno s akutní bolestivou neuropatií, která je obvykle reverzibilní. Intenzifikace inzulinové terapie s prudkým zlepšením glykemické kontroly může být spojena s přechodným zhoršením diabetické retinopatie, zatímco dlouhodobé zlepšení glykemické kontroly snižuje riziko progrese diabetické retinopatie.
b. Seznam nežádoucích účinků v tabulce
Nežádoucí účinky uvedené níže jsou založeny na údajích z klinických studií a jsou klasifikovány podle MedDRA frekvence výskytu a třídy orgánových systémů. Frekvence výskytu jsou definovány podle následující konvence: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000), velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
|
Poruchy imunitního systému |
Méně časté - Kopřivka, vyrážky, erupce |
|
Velmi vzácné - Anafylaktické reakce* | |
|
Poruchy metabolismu a výživy |
Velmi časté - Hypoglykemie* |
|
Poruchy nervového systému |
Vzácné - Periferní neuropatie (bolestivá neuropatie) |
|
Poruchy oka |
Méně časté - Poruchy refrakce |
|
Méně časté - Diabetická retinopatie | |
|
Poruchy kůže a podkožní tkáně |
Méně časté - Lipodystrofie* |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté - Otoky |
|
Méně časté - Reakce v místě vpichu |
viz bod c.
c. Popis vybraných nežádoucích účinků Anafylaktické reakce:
Vznik generalizovaných hypersenzitivních reakcí (zahrnujících generalizované kožní vyrážky, svědění, pocení, gastrointestinální obtíže, angioneurotický edém, obtížné dýchání, palpitace a pokles krevního tlaku) je velmi vzácný, avšak může být potenciálně život ohrožující.
Hypoglykemie:
Nejčastěji hlášeným nežádoucím účinkem je hypoglykemie. Může nastat v případě, kdy je dávka inzulínu příliš vysoká vzhledem k inzulínové potřebě. Těžká hypoglykemie může vést k bezvědomí a/nebo křečím a může vyústit v přechodné nebo trvalé poškození mozkových funkcí nebo dokonce vést ke smrti. Příznaky hypoglykemie se obvykle objevují náhle. Mohou zahrnovat studený pot, chladnou bledou pokožku, únavu, nervozitu nebo třes, úzkost, neobvyklou vyčerpanost nebo slabost, zmatenost, potíže s koncentrací, ospalost, velký hlad, změny vidění, bolest hlavy, nauzeu a palpitaci.
V klinických studiích se frekvence výskytu hypoglykemií měnila s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly. Během klinických studií se celkový výskyt hypoglykemií nelišil u pacientů léčených inzulinem aspart ve srovnání s humánním inzulinem.
Lipodystrofie:
V místě vpichu může vzniknout lipodystrofie (zahrnující lipohypertrofii, lipoatrofii). Průběžná cyklická změna místa vpichu v dané oblasti snižuje riziko vzniku takovýchto reakcí.
d. Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 50 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
e. Další populační specifika
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u starších pacientů a u pacientů s poškozením ledvin či jater, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
f. Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Specifické předávkování inzulinem nelze definovat, ovšem v následných stádiích se může vyvinout hypoglykemie, pokud jsou pacientovi podány dávky, které jsou vzhledem k jeho potřebě inzulinu příliš vysoké:
• Mírné hypoglykemické příhody mohou být léčeny perorálním podáním glukózy nebo potravin obsahujících cukr. Proto se diabetikům doporučuje, aby s sebou vždy nosili potraviny s obsahem cukru.
• Těžké hypoglykemické příhody, při kterých pacient upadl do bezvědomí, mohou být léčeny intramuskulárním nebo subkutánním podáním glukagonu (0,5 až 1 mg) zaškolenou osobou nebo intravenózní aplikací glukózy zdravotnickým pracovníkem. Glukózu je nutno podat intravenózně i v případě, jestliže pacient nereaguje na glukagon do 10 až 15 minut. Po návratu pacienta k vědomí se doporučuje podat mu perorálně sacharidy jako prevenci relapsu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antidiabetika. Inzuliny a analogy střednědobě nebo dlouze působící v kombinaci s rychle působícími, k injekční aplikaci. ATC kód: A10AD05.
NovoMix 50 je bifázická suspenze 50 % rozpustného inzulínu aspart (rychle působícího analogu humánního inzulinu) a 50 % krystalického protaminového inzulinu aspart (střednědobě působícího analogu humánního inzulinu).
Mechanismus účinku a farmakodynamické účinky
Účinek inzulinu aspart na pokles hladiny glukózy v krvi je důsledkem usnadněného vychytávání glukózy a následné vazby inzulinu na receptory ve svalových a tukových buňkách a současné inhibice uvolňování glukózy z jater.
NovoMix 50 je bifázický inzulin, který obsahuje 50 % rozpustného inzulinu aspart. Tento má rychlý nástup účinku, takže dovoluje podání v těsnější závislosti na jídle (rozmezí 0 až 10 minut od jídla) ve srovnání s rozpustným humánním inzulinem. Krystalická část (50 %) je tvořena krystalickým protaminovým inzulinem aspart, jehož profil účinku se podobá profilu humánního NPH inzulinu.
Je-li NovoMix 50 aplikován subkutánně, nástup účinku nastává v průběhu 10 až 20 minut po injekci. Maximálního účinku je dosaženo za 1 až 4 hodiny po injekci. Účinek trvá 14 až 24 hodin (obrázek 1).
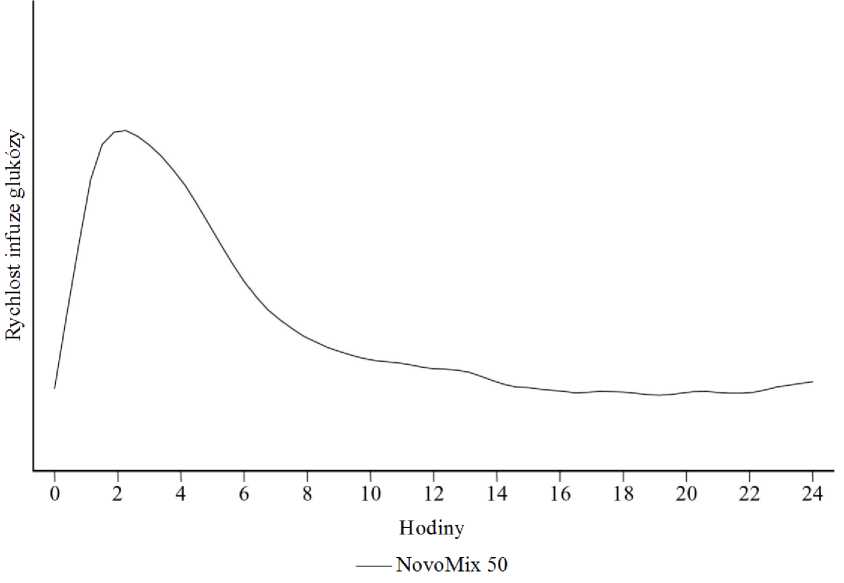
Obrázek 1: Profil aktivity přípravku NovoMix 50 u zdravých bělošských subjektů.
Inzulin aspart je ekvipotentní s humánním inzulinem na molární bázi.
5.2 Farmakokinetické vlastnosti Absorpce, distribuce a eliminace
Substituce aminokyseliny prolinu kyselinou asparagovou v inzulinu aspart na pozici B28 snižuje tendenci ke tvorbě hexamerů tak, jak to bylo pozorováno u rozpustného humánního inzulinu. Inzulin aspart v rozpustné fázi přípravku Novo Mix 50 tvoří 50 % celkového inzulinu, který se ze subkutánní vrstvy vstřebává rychleji, než rozpustná složka bifázického humánního inzulinu. Zbývajících 50 % tvoří krystalická forma krystalický protaminový inzulin aspart, který má prodloužený absorpční profil podobný humánnímu NPH inzulinu.
U zdravých dobrovolníků bylo průměrné maximální koncentrace v séru 445 ± 135 pmol/l dosaženo přibližně za 60 minut po subkutánním podání dávky 0,30 jednotky/kg tělesné hmotnosti. U pacientů s diabetem 2. typu bylo maximální koncentrace dosaženo přibližně po 95 minutách od podání.
Zvláštní skupiny pacientů
Farmakokinetika přípravku NovoMix 50 nebyla sledována u dětí, starších pacientů ani u pacientů s poškozením ledvin nebo jater.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
Při zkouškách in vitro, včetně vazby na inzulinová a IGF-1 receptorová místa a účinků na buněčný růst, se inzulin aspart choval podobně jako humánní inzulin. Studie také ukazují, že disociace inzulinu aspart z vazby na inzulinových receptorech je ekvivalentní humánnímu inzulinu.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Glycerol Fenol Metakresol Chlorid zinečnatý
Dihydrát hydrogenfosforečnanu sodného
Chlorid sodný
Protamin-sulfát
Kyselina chlorovodíková (pro úpravu pH)
Hydroxid sodný (pro úpravu pH)
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto tento léčivý přípravek nesmí být mísen s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
Před otevřením: 2 roky.
Během používání nebo pokud NovoMix nosíte jako zásobní: přípravek smí být uchováván maximálně 4 týdny.
6.4 Zvláštní opatření pro uchovávání
Před otevřením: uchovávejte v chladničce (2 °C - 8 °C). Neuchovávejte v blízkosti chladicího zařízení. Chraňte před mrazem.
Během používání nebo pokud NovoMix nosíte jako zásobní: uchovávejte při teplotě do 30 °C. Chraňte před chladem. Chraňte před mrazem.
FlexPen uchovávejte s nasazeným krytem, aby byl přípravek chráněn před světlem.
3 ml suspenze v zásobní vložce (sklo typu 1), s pístem (bromobutyl) a pryžovým uzávěrem (bromobutyl/polyisopren) v jednorázovém vícedávkovém předplněném peru zhotoveném z polypropylenu. V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání.
Velikosti balení jsou 1, 5 a 10 předplněných per. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Jehly a NovoMix 50 FlexPen nesmí být s nikým sdíleny. Zásobní vložka se nesmí znovu plnit.
Po vyjmutí přípravku NovoMix 50 FlexPen z chladničky je před promícháním inzulinu dle instrukcí pro první použití doporučeno nechat NovoMix 50 FlexPen ohřát na pokojovou teplotu.
Tento léčivý přípravek nepoužívejte, pokud si všimnete, že po promíchání tekutina není vodná, stejnoměrně bílá a zakalená.
Pacientovi je třeba zdůraznit, že těsně před použitím je nutné suspenzi přípravku NovoMix 50 promíchat.
NovoMix 50, který zmrzl, nesmí být použit.
Pacient musí být poučen o tom, že po každé aplikaci musí použitou jehlu vyhodit.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
8. REGISTRAČNÍ ČÍSLA
EU/1/00/142/014
EU/1/00/142/015
EU/1/00/142/016
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 1. srpna 2000
Datum posledního prodloužení registrace: 2. července 2010
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské lékové agentury http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
NovoMix 70 FlexPen 100 jednotek/ml injekční suspenze v předplněném peru
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile*/Insulinum aspartum protaminatum cristallinum* v poměru 70/30 (což odpovídá 3,5 mg). 1 předplněné pero obsahuje 3 ml, což odpovídá 300 jednotkám.
* Insulin aspart je vyrobený rekombinantní DNA technologií na Saccharomyces cerevisiae.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční suspenze Zakalená, bílá vodná suspenze.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
NovoMix 70 je indikován k léčbě diabetes mellitus u dospělých.
4.2 Dávkování a způsob podání
Dávkování
Účinnost inzulinových analogů, včetně inzulinu aspart, se vyjadřuje v jednotkách, zatímco účinnost humánních inzulinů se vyjadřuje v mezinárodních jednotkách.
Dávkování přípravku NovoMix 70 je individuální a je stanoveno v souladu s pacientovými potřebami. Pro dosažení optimální kontroly glykemie je doporučeno monitorování glukózy v krvi a úpravy dávky inzulinu.
Individuální inzulinová potřeba je obvykle mezi 0,5 a 1,0 jednotkou/kg/den. NovoMix 70 může plně nebo částečně tuto potřebu zajistit.
U pacientů s diabetem 2. typu lze NovoMix 70 podávat jako monoterapii nebo v kombinaci s metforminem, pokud je hladina glukózy v krvi nedostatečně kontrolována podáváním metforminu samotného.
Úprava dávky může být nutná, pokud pacient podstupuje zvýšenou tělesnou námahu, mění svou obvyklou dietu nebo během současně probíhajícího jiného onemocnění.
Zvláštní skupiny pacientů
V případě starších pacientů (> 65 let) a pacientů s poškozením jater či ledvin by mělo být monitorování glukózy intenzifikováno a dávka inzulinu aspart by měla být upravena individuálně.
Poškození ledvin nebo jater může snížit pacientovu potřebu inzulinu.
Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 70 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
Přechod z jiných inzulínových přípravků
Přechod na NovoMix 70 z jiných inzulinových přípravků může vyžadovat úpravu dávky a času podání. Během přechodu a několik týdnů poté je doporučeno pečlivé monitorování glukózy (viz bod 4.4).
Způsob podání
NovoMix 70 je bifázická suspenze inzulinového analogu inzulin aspart. Suspenze obsahuje rychle působící a střednědobě působící inzulin aspart v poměru 70/30.
NovoMix 70 je určen pouze pro subkutánní podání.
NovoMix 70 je podáván subkutánně do stehna nebo břišní stěny. Pokud je to přijatelné, je možné ho aplikovat do oblasti hýždí nebo deltoidní oblasti. Injekční místa ve stejné oblasti je vždy třeba měnit rotačním způsobem, aby se snížilo riziko lipodystrofie. Vliv různých míst vpichu na absorpci přípravku NovoMix 70 nebyl sledován. Trvání účinku se mění podle dávky, místa vpichu, prokrvení, teploty a fyzické aktivity.
NovoMix 70 má rychlejší nástup účinku než humánní bifázický inzulin a měl by být tedy obecně podáván bezprostředně před jídlem. Pokud je to nutné, může být NovoMix 70 podán i brzy po jídle.
Podání pomocí pera FlexPen
NovoMix 70 FlexPen je předplněné pero, které je určeno k použití spolu jehlami NovoFine nebo NovoTwist. Dávky lze nastavit od 1 do 60 jednotek v přírůstcích po 1 jednotce.
NovoMix 70 FlexPen je barevně kódován a je k němu přiložena příbalová informace s podrobným návodem k použití, jenž by měl být dodržován.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
NovoMix 70 nesmí být podáván intravenózně, neboť to může vést k těžké hypoglykemii. Vyvarujte se intramuskulárního podání. NovoMix 70 není určen pro použití v inzulinových infuzních pumpách.
Před cestou mezi různými časovými pásmy by se pacient měl poradit s lékařem. Cestování mezi různými časovými pásmy může totiž znamenat, že pacient bude muset užívat inzulin a přijímat jídla v odlišných časech.
Hyperglykemie
Nedostatečné dávkování nebo přerušovaná léčba, zejména u diabetu 1. typu, může vést k hyperglykemii a diabetické ketoacidóze. První symptomy hyperglykemie se obvykle v průběhu hodin nebo dní stupňují. Mezi ně patří žízeň, zvýšená frekvence močení, nauzea, zvracení, ospalost, zarudlá suchá kůže, sucho v ústech, ztráta chuti k jídlu či acetonový zápach dechu. U diabetu 1. typu mohou vést neléčené hyperglykemické stavy až k diabetické ketoacidóze, která je potenciálně letální.
Hypoglykemie
Vynechání jídla nebo neplánovaná namáhavá fyzická aktivita mohou vést k hypoglykemii.
Hypoglykemie se může objevit, pokud je dávka inzulínu příliš vysoká ve vztahu k potřebě inzulínu.
V případě hypoglykemie či podezření na hypoglykemii nesmí být NovoMix podáván. Poté co u pacienta dojde ke stabilizaci hladiny glukózy, měla by být zvážena úprava dávky (viz body 4.2, 4.8 a 4.9).
Pacienti, u kterých se kontrola diabetu výrazně zlepšila, např. při intenzifikované inzulinové terapii, mohou zaznamenat změnu obvyklých varovných příznaků hypoglykemie a měli by být patřičně poučeni. U pacientů s dlouholetým diabetem mohou běžné varovné symptomy vymizet.
Protože NovoMix 70 má být aplikován v těsné závislosti na jídle, je třeba zvážit rychlý nástup účinku u pacientů s doprovodnými nemocemi nebo při léčbě, během níž může být očekávána zpožděná absorpce jídla.
Přidružené onemocnění, zejména infekce a horečnaté stavy, obvykle zvyšují pacientovu potřebu inzulinu. Přidružené onemocnění ledvin, jater či onemocnění ovlivňující nadledviny, podvěsek mozkový nebo štítnou žlázu může vyžadovat změny v dávce inzulinu.
Pokud je pacient převeden na jiný typ inzulinových přípravků, může dojít ke změně či potlačení časných varovných příznaků hypoglykemie oproti těm, které se u pacienta projevovaly u předchozího inzulinu.
Převedení z jiných inzulinových přípravků
Převod pacienta na jiný typ nebo značku inzulinu by měl probíhat pod přísným lékařským dozorem. Změny v síle, značce (výrobce), typu, původu (zvířecí inzulin, humánní inzulin nebo analog inzulinu) a/nebo metodě výroby (rekombinantní DNA versus inzulin ze zvířecích zdrojů) mohou vést k potřebě změnit dávkování. Pacienti převádění na přípravek NovoMix 70 z jiných typů inzulinu mohou vyžadovat vyšší počet injekcí denně nebo změnu dávkování oproti jejich obvyklým inzulinovým léčivým přípravkům. Pokud je potřeba přizpůsobit dávkování, může k tomu dojít při první dávce nebo během prvních týdnů či měsíců.
Reakce v místě vpichu
Tak jako při každé léčbě inzulinem se mohou objevit reakce v místě vpichu, které se projevují bolestivostí, zarudnutím, kopřivkou, zánětem, podlitinami, otoky a svěděním. Pravidelné obměňování injekčního místa v rámci jedné oblasti snižuje riziko vzniku těchto reakcí. Reakce obvykle vymizí do několika dnů nebo týdnů. Ve vzácných případech si mohou reakce v místě vpichu vyžádat vysazení přípravku NovoMix 70.
Kombinace přípravku NovoMix s pioglitazonem
Pokud byl pioglitazon užíván v kombinaci s inzulinem, byly hlášeny případy srdečního selhání a to zvláště u pacientů s rizikovými faktory pro vznik srdečního selhání. Tuto skutečnost je nutno vzít v úvahu, pokud je zvažována léčba pioglitazonem v kombinaci s přípravkem NovoMix. Pokud je tato kombinace použita, měli by být pacienti sledováni s ohledem na známky a příznaky srdečního selhání, zvýšení hmotnosti a edém. Pioglitazon by měl být vysazen, pokud se objeví jakékoliv zhoršení srdečních příznaků.
Protilátky proti inzulinu
Podávání inzulínu může vyvolat tvorbu protilátek proti inzulínu. Ve vzácných případech může přítomnost těchto protilátek vyžadovat úpravu dávky inzulinu, aby se usměrnila tendence k hyper- či hypoglykemii.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
U řady léčivých přípravků je známa interakce s glukózovým metabolismem.
Následující látky mohou snižovat pacientovu potřebu inzulinu:
Perorální antidiabetika, inhibitory monoaminoxidázy (IMAO), beta-blokátory, angiotensin konvertujícího enzymu (ACE) inhibitory, salicyláty, anabolické steroidy a sulfonamidy.
Následující látky mohou zvyšovat pacientovu potřebu inzulinu:
Perorální kontraceptiva, thiazidy, glukokortikoidy, thyreoidální hormony, sympatomimetika, růstový hormon a danazol.
Beta-blokátory mohou zakrývat příznaky hypoglykemie.
Oktreotid/lanreotid mohou buď zvýšit nebo snížit potřebu inzulinu.
Alkohol může zesílit nebo snížit hypoglykemický účinek inzulinu.
4.6 Fertilita, těhotenství a kojení Těhotenství
Klinické zkušenosti s užíváním přípravku NovoMix 70 v těhotenství jsou omezené.
Reprodukční studie na zvířatech neukázaly žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče embryotoxicity nebo teratogenity.
Obecně platí, že v průběhu celého těhotenství a při jeho plánování se doporučují intenzifikované kontroly hladin glukózy v krvi a monitorování těhotných diabetiček. Potřeba inzulinu obvykle v průběhu prvního trimestru klesne a následně se zvyšuje ve druhém a třetím trimestru. Po porodu se potřeba inzulinu rychle vrací na úroveň před těhotenstvím.
Kojení
Léčba přípravkem NovoMix 70 při kojení není omezena. Léčba kojících matek inzulinem nepředstavuje pro dítě žádné riziko. Dávkování přípravku NovoMix 70 však může vyžadovat úpravu.
Fertilita
Reprodukční studie se zvířaty neodhalily žádné rozdíly mezi inzulinem aspart a humánním inzulinem, co se týče fertility.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Pacientova schopnost koncentrace a reakce se může v důsledku hypoglykemie zhoršit. To může představovat riziko v situacích, kde jsou tyto schopnosti zvláště důležité (např. řízení vozu nebo obsluha strojů).
Pacienti by měli být poučeni o opatřeních, jak se vyvarovat vzniku hypoglykemie během řízení či během obsluhy strojů. Je to důležité zvláště u pacientů, kteří mají slabé nebo žádné varovné příznaky hypoglykemie nebo kteří mají časté epizody hypoglykemie. V těchto případech je třeba vhodnost řízení či obsluhy strojů zvážit.
4.8 Nežádoucí účinky
a. Souhrn bezpečnostního profilu
Nežádoucí účinky pozorované u pacientů užívajících NovoMix jsou převážně způsobeny farmakologickým efektem inzulinu aspart.
Nejčastěji hlášeným nežádoucím účinkem během léčby je hypoglykemie. Frekvence výskytu hypoglykemie se mění s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly, viz bod c níže.
Na počátku inzulinové léčby se mohou vyskytnout poruchy refrakce, edém a reakce v místě vpichu (bolest, zarudnutí, kopřivka, zánět, podlitiny, otoky a svědění v místě vpichu). Tyto reakce jsou obvykle přechodné povahy. Rychlé zlepšení hladiny glukózy v krvi může být spojeno s akutní bolestivou neuropatií, která je obvykle reverzibilní. Intenzifikace inzulinové terapie s prudkým zlepšením glykemické kontroly může být spojena s přechodným zhoršením diabetické retinopatie, zatímco dlouhodobé zlepšení glykemické kontroly snižuje riziko progrese diabetické retinopatie.
b. Seznam nežádoucích účinků v tabulce
Nežádoucí účinky uvedené níže jsou založeny na údajích z klinických studií a jsou klasifikovány podle MedDRA frekvence výskytu a třídy orgánových systémů. Frekvence výskytu jsou definovány podle následující konvence: Velmi časté (>1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000), velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
|
Poruchy imunitního systému |
Méně časté - Kopřivka, vyrážky, erupce |
|
Velmi vzácné - Anafylaktické reakce* | |
|
Poruchy metabolismu a výživy |
Velmi časté - Hypoglykemie* |
|
Poruchy nervového systému |
Vzácné - Periferní neuropatie (bolestivá neuropatie) |
|
Poruchy oka |
Méně časté - Poruchy refrakce |
|
Méně časté - Diabetická retinopatie | |
|
Poruchy kůže a podkožní tkáně |
Méně časté - Lipodystrofie* |
|
Celkové poruchy a reakce v místě aplikace |
Méně časté - Otoky |
|
Méně časté - Reakce v místě vpichu |
viz bod c.
c. Popis vybraných nežádoucích účinků Anafylaktické reakce:
Vznik generalizovaných hypersenzitivních reakcí (zahrnujících generalizované kožní vyrážky, svědění, pocení, gastrointestinální obtíže, angioneurotický edém, obtížné dýchání, palpitace a pokles krevního tlaku) je velmi vzácný, avšak může být potenciálně život ohrožující.
Hypoglykemie:
Nejčastěji hlášeným nežádoucím účinkem je hypoglykemie. Může nastat v případě, kdy je dávka inzulínu příliš vysoká vzhledem k inzulínové potřebě. Těžká hypoglykemie může vést k bezvědomí a/nebo křečím a může vyústit v přechodné nebo trvalé poškození mozkových funkcí nebo dokonce vést ke smrti. Příznaky hypoglykemie se obvykle objevují náhle. Mohou zahrnovat studený pot, chladnou bledou pokožku, únavu, nervozitu nebo třes, úzkost, neobvyklou vyčerpanost nebo slabost, zmatenost, potíže s koncentrací, ospalost, velký hlad, změny vidění, bolest hlavy, nauzeu a palpitaci.
V klinických studiích se frekvence výskytu hypoglykemií měnila s populací pacientů, dávkovacím režimem a úrovní glykemické kontroly. Během klinických studií se celkový výskyt hypoglykemií nelišil u pacientů léčených inzulinem aspart ve srovnání s humánním inzulinem.
Lipodystrofie:
V místě vpichu může vzniknout lipodystrofie (zahrnující lipohypertrofii, lipoatrofii). Průběžná cyklická změna místa vpichu v dané oblasti snižuje riziko vzniku takovýchto reakcí.
d. Pediatrická populace
Bezpečnost a účinnost přípravku NovoMix 70 u dětí ve věku do 18 let nebyla stanovena.
Nejsou dostupné žádné údaje.
e. Další populační specifika
Na základě zdrojů z postmarketingového sledování a z klinických studií nenaznačují frekvence, typ a závažnost nežádoucích účinků, pozorovaných u starších pacientů a u pacientů s poškozením ledvin či jater, jakékoliv rozdíly oproti širším zkušenostem v obecné populaci.
f. Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Specifické předávkování inzulinem nelze definovat, ovšem v následných stádiích se může vyvinout hypoglykemie, pokud jsou pacientovi podány dávky, které jsou vzhledem k jeho potřebě inzulinu příliš vysoké:
• Mírné hypoglykemické příhody mohou být léčeny perorálním podáním glukózy nebo potravin obsahujících cukr. Proto se diabetikům doporučuje, aby s sebou vždy nosili potraviny s obsahem cukru.
• Těžké hypoglykemické příhody, při kterých pacient upadl do bezvědomí, mohou být léčeny intramuskulárním nebo subkutánním podáním glukagonu (0,5 až 1 mg) zaškolenou osobou nebo intravenózní aplikací glukózy zdravotnickým pracovníkem. Glukózu je nutno podat intravenózně i v případě, jestliže pacient nereaguje na glukagon do 10 až 15 minut. Po návratu pacienta k vědomí se doporučuje podat mu perorálně sacharidy jako prevenci relapsu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antidiabetika. Inzuliny a analogy střednědobě nebo dlouze působící v kombinaci s rychle působícími, k injekční aplikaci. ATC kód: A10AD05.
NovoMix 70 je bifázická suspenze 70 % rozpustného inzulínu aspart (rychle působícího analogu humánního inzulinu) a 30 % krystalického protaminového inzulinu aspart (střednědobě působícího analogu humánního inzulinu).
Mechanismus účinku a farmakodynamické účinky
Účinek inzulinu aspart na pokles hladiny glukózy v krvi je důsledkem usnadněného vychytávání glukózy a následné vazby inzulinu na receptory ve svalových a tukových buňkách a současné inhibice uvolňování glukózy z jater.
NovoMix 70 je bifázický inzulin, který obsahuje 70 % rozpustného inzulinu aspart. Tento má rychlý nástup účinku, takže dovoluje podání v těsnější závislosti na jídle (rozmezí 0 až 10 minut od jídla) ve srovnání s rozpustným humánním inzulinem. Krystalická část (30 %) je tvořena krystalickým protaminovým inzulinem aspart, jehož profil účinku se podobá profilu humánního NPH inzulinu.
Je-li NovoMix 70 aplikován subkutánně, nástup účinku nastává v průběhu 10 až 20 minut po injekci. Maximálního účinku je dosaženo za 1 až 4 hodiny po injekci. Účinek trvá 14 až 24 hodin (obrázek 1).
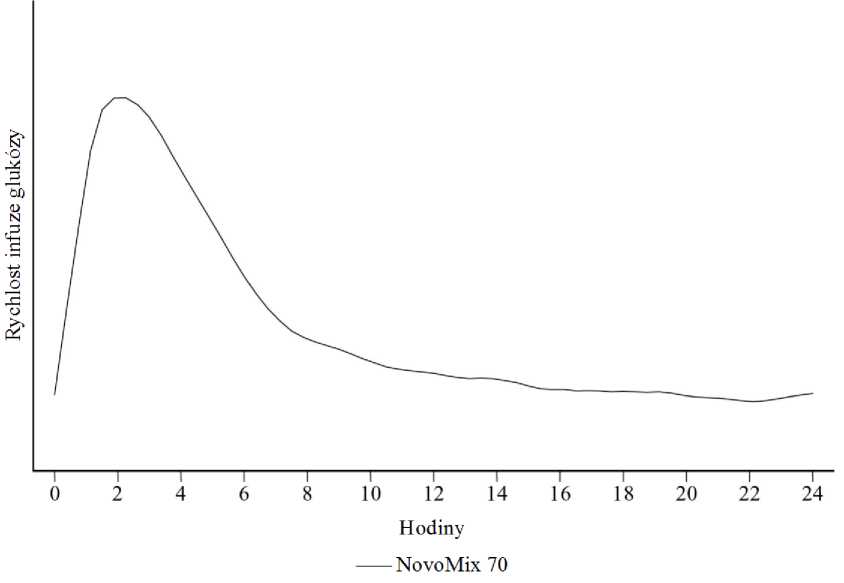
Obrázek 1: Profil aktivity přípravku NovoMix 70 u zdravých bělošských subjektů.
Inzulin aspart je ekvipotentní s humánním inzulinem na molární bázi.
5.2 Farmakokinetické vlastnosti Absorpce, distribuce a eliminace
Substituce aminokyseliny prolinu kyselinou asparagovou v inzulinu aspart na pozici B28 snižuje tendenci ke tvorbě hexamerů tak, jak to bylo pozorováno u rozpustného humánního inzulinu. Inzulin aspart v rozpustné fázi přípravku Novo Mix 70 tvoří 70 % celkového inzulinu, který se ze subkutánní vrstvy vstřebává rychleji, než rozpustná složka bifázického humánního inzulinu. Zbývajících 30 % tvoří krystalická forma krystalický protaminový inzulin aspart, který má prodloužený absorpční profil podobný humánnímu NPH inzulinu.
U zdravých dobrovolníků bylo průměrné maximální koncentrace v séru 645 ± 185 pmol/l dosaženo přibližně za 60 minut po subkutánním podání dávky 0,30 jednotky/kg tělesné hmotnosti. U pacientů s diabetem 2. typu bylo maximální koncentrace dosaženo přibližně po 75 minutách od podání.
U pacientů s diabetem 1. typu byla průměrná maximální koncentrace v séru 721 ± 184 pmol/l dosažena za cca 60 minut od subkutánního podání dávky 0,30 jednotky/kg tělesné hmotnosti.
Zvláštní skupiny pacientů
Farmakokinetika přípravku NovoMix 70 nebyla sledována u dětí, starších pacientů ani u pacientů s poškozením ledvin nebo jater.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a reprodukční a vývojové toxicity neodhalily žádné zvláštní riziko pro člověka.
Při zkouškách in vitro, včetně vazby na inzulinová a IGF-1 receptorová místa a účinků na buněčný růst, se inzulin aspart choval podobně jako humánní inzulin. Studie také ukazují, že disociace inzulinu aspart z vazby na inzulinových receptorech je ekvivalentní humánnímu inzulinu.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Glycerol Fenol Metakresol Chlorid zinečnatý
Dihydrát hydrogenfosforečnanu sodného
Chlorid sodný
Protamin-sulfát
Kyselina chlorovodíková (pro úpravu pH)
Hydroxid sodný (pro úpravu pH)
Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto tento léčivý přípravek nesmí být mísen s žádnými dalšími léčivými přípravky.
6.3 Doba použitelnosti
Před otevřením: 2 roky.
Během používání nebo pokud NovoMix nosíte jako zásobní: přípravek smí být uchováván maximálně 4 týdny.
6.4 Zvláštní opatření pro uchovávání
Před otevřením: uchovávejte v chladničce (2 °C - 8 °C). Neuchovávejte v blízkosti chladicího zařízení. Chraňte před mrazem.
Během používání nebo pokud NovoMix nosíte jako zásobní: uchovávejte při teplotě do 30 °C.
Chraňte před chladem. Chraňte před mrazem.
FlexPen uchovávejte s nasazeným krytem, aby byl přípravek chráněn před světlem.
6.5 Druh obalu a obsah balení
3 ml suspenze v zásobní vložce (sklo typu 1), s pístem (bromobutyl) a pryžovým uzávěrem (bromobutyl/polyisopren) v jednorázovém vícedávkovém předplněném peru zhotoveném z polypropylenu. V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání.
Velikosti balení jsou 1, 5 a 10 předplněných per. Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Jehly a NovoMix 70 FlexPen nesmí být s nikým sdíleny. Zásobní vložka se nesmí znovu plnit.
Po vyjmutí přípravku NovoMix 70 FlexPen z chladničky je před promícháním inzulinu dle instrukcí pro první použití doporučeno nechat NovoMix 70 FlexPen ohřát na pokojovou teplotu.
Tento léčivý přípravek nepoužívejte, pokud si všimnete, že po promíchání tekutina není vodná, stejnoměrně bílá a zakalená.
Pacientovi je třeba zdůraznit, že těsně před použitím je nutné suspenzi přípravku NovoMix 70 promíchat.
NovoMix 70, který zmrzl, nesmí být použit.
Pacient musí být poučen o tom, že po každé aplikaci musí použitou jehlu vyhodit.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
8. REGISTRAČNÍ ČÍSLA
EU/1/00/142/020
EU/1/00/142/021
EU/1/00/142/022
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 1. srpna 2000
Datum posledního prodloužení registrace: 2. července 2010
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské lékové agentury http://www.ema.europa.eu/
A. VÝROBCI BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCI BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce biologické léčivé látky
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
Novo Nordisk A/S Hallas Allé DK-4400 Kalundborg Dánsko
Název a adresa výrobců odpovědných za propouštění šarží
NovoMix 30 Penfill a NovoMix 30 FlexPen:
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
Novo Nordisk Production SAS 45, Avenue d’Orléans F-28000 Chartres Francie
NovoMix 50 Penfill a NovoMix 50 FlexPen:
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
NovoMix 70 Penfill a NovoMix 70 FlexPen:
Novo Nordisk A/S Novo Allé DK-2880 Bagsv^rd Dánsko
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propouštění dané šarže
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Držitel rozhodnutí o registraci předkládá pravidelně aktualizované zprávy o bezpečnosti pro tento
léčivý přípravek v souladu s požadavky uvedenými v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a zveřejněném na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
Pokud se shodují data předložení aktualizované zprávy o bezpečnosti (PSUR) a aktualizovaného RMP, je možné je předložit současně.
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
NovoMix 30 Penfill 100 jednotek/ml Injekční suspenze v zásobní vložce
30 % Insulinům aspartum solubile a 70 % Insulinům aspartum protaminatum cristallinum
2. OBSAH LÉČIVÉ LÁTKY
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile/Insulinum aspartum protaminatum cristallmum v poměru 30/70 (odpovídá 3,5 mg). 1 zásobní vložka obsahuje 3 ml odpovídající 300 jednotkám,
3. SEZNAM POMOCNÝCH LÁTEK
glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselinu chlorovodíkovou/hydroxid sodný pro úpravu pH a vodu na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční suspenze
5 x 3 ml zásobní vložky 10 x 3 ml zásobní vložky
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Subkutánní podání
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Promíchejte dle instrukcí.
Používejte pouze tehdy, pokud je suspenze po promíchání vodná, stejnoměrně bílá a zakalená. Pro použití pouze jednou osobou.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Před otevřením: uchovávejte v chladničce (2 °C až 8 °C).
Během používání: chraňte před chladem. Uchovávejte při teplotě do 30 °C. Chraňte před mrazem.
Uchovávejte zásobní vložku v krabičce, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Po každé injekci odstraňte jehlu.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
12. REGISTRAČNÍ ČÍSLA
EU/1/00/142/004 5 zásobních vložek po 3 ml EU/1/00/142/005 10 zásobních vložek po 3 ml
13. ČÍSLO ŠARŽE
č.S.
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
NovoMix 30 Penfill
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA PODÁNÍ
NovoMix 30 Penfill 100 jednotek/ml Injekční suspenze
30 % Insulinům aspartum solubile a 70 % Insulinům aspartum protaminatum cristallinum Subkutánní podání
2. ZPŮSOB PODÁNÍ
Promíchejte dle instrukcí. Penfill
3. POUŽITELNOST
Použitelné do
4. ČÍSLO ŠARŽE
č.S.
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
3 ml
6. JINÉ
Novo Nordisk A/S
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
NovoMix 50 Penfill 100 jednotek/ml Injekční suspenze v zásobní vložce
50 % Insulinům aspartum solubile a 50 % Insulinům aspartum protaminatum cristallinum
2. OBSAH LÉČIVÉ LÁTKY
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile/Insulinum aspartum protaminatum cristallmum v poměru 50/50 (odpovídá 3,5 mg). 1 zásobní vložka obsahuje 3 ml odpovídající 300 jednotkám,
3. SEZNAM POMOCNÝCH LÁTEK
glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselinu chlorovodíkovou/hydroxid sodný pro úpravu pH a vodu na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční suspenze.
1 x 3 ml zásobní vložka 5 x 3 ml zásobní vložky 10 x 3 ml zásobní vložky
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Subkutánní podání
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Promíchejte dle instrukcí.
Používejte pouze tehdy, pokud je suspenze po promíchání vodná, stejnoměrně bílá a zakalená. Pro použití pouze jednou osobou.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Před otevřením: uchovávejte v chladničce (2 °C až 8 °C).
Během používání: chraňte před chladem. Uchovávejte při teplotě do 30 °C. Chraňte před mrazem.
Uchovávejte zásobní vložku v krabičce, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Po každé injekci odstraňte jehlu.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
12. REGISTRAČNÍ ČÍSLA
EU/1/00/142/011 1 zásobní vložka po 3 ml EU/1/00/142/012 5 zásobních vložek po 3 ml EU/1/00/142/013 10 zásobních vložek po 3 ml
13. ČÍSLO ŠARŽE
č.S.
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
NovoMix 50 Penfill
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA PODÁNÍ
NovoMix 50 Penfill 100 jednotek/ml Injekční suspenze
50 % Insulinům aspartum solubile a 50 % Insulinům aspartum protaminatum cristallinum Subkutánní podání
2. ZPŮSOB PODÁNÍ
Promíchejte dle instrukcí. Penfill
3. POUŽITELNOST
Použitelné do
4. ČÍSLO ŠARŽE
č.S.
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
3 ml
6. JINÉ
Novo Nordisk A/S
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
NovoMix 70 Penfill 100 jednotek/ml Injekční suspenze v zásobní vložce
70 % Insulinům aspartum solubile a 30 % Insulinům aspartum protaminatum cristallinum
2. OBSAH LÉČIVÉ LÁTKY
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile/Insulinum aspartum protaminatum cristallmum v poměru 70/30 (odpovídá 3,5 mg). 1 zásobní vložka obsahuje 3 ml odpovídající 300 jednotkám,
3. SEZNAM POMOCNÝCH LÁTEK
glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselinu chlorovodíkovou/hydroxid sodný pro úpravu pH a vodu na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční suspenze
1 x 3 ml zásobní vložka 5 x 3 ml zásobní vložky 10 x 3 ml zásobní vložky
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Subkutánní podání
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Promíchejte dle instrukcí.
Používejte pouze tehdy, pokud je suspenze po promíchání vodná, stejnoměrně bílá a zakalená. Pro použití pouze jednou osobou.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Před otevřením: uchovávejte v chladničce (2 °C až 8 °C).
Během používání: chraňte před chladem. Uchovávejte při teplotě do 30 °C. Chraňte před mrazem.
Uchovávejte zásobní vložku v krabičce, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Po každé injekci odstraňte jehlu.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
12. REGISTRAČNÍ ČÍSLA
EU/1/00/142/017 1 zásobní vložka po 3 ml EU/1/00/142/018 5 zásobních vložek po 3 ml EU/1/00/142/019 10 zásobních vložek po 3 ml
13. ČÍSLO ŠARŽE
č.S.
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
NovoMix 70 Penfill
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA PODÁNÍ
NovoMix 70 Penfill 100 jednotek/ml Injekční suspenze
70 % Insulinům aspartum solubile a 30 % Insulinům aspartum protaminatum cristallinum Subkutánní podání
2. ZPŮSOB PODÁNÍ
Promíchejte dle instrukcí. Penfill
3. POUŽITELNOST
Použitelné do
4. ČÍSLO ŠARŽE
č.S.
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
3 ml
6. JINÉ
Novo Nordisk A/S
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
NovoMix 30 FlexPen 100 jednotek/ml Injekční suspenze v předplněném peru
30 % Insulinum aspartum solubile a 70 % Insulinum aspartum protaminatum cristallinum
2. OBSAH LÉČIVÉ LÁTKY
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile/Insulinum aspartum protaminatum cristallinum v poměru 30/70 (odpovídá 3,5 mg). 1 předplněné pero obsahuje 3 ml odpovídající 300 jednotkám,
3. SEZNAM POMOCNÝCH LÁTEK
glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselinu chlorovodíkovou/hydroxid sodný pro úpravu pH a vodu na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční suspenze
1 x 3 ml předplněné pero 5 x 3 ml předplněná pera 10 x 3 ml předplněná pera 1 x 3 ml předplněné pero + 7 jehel NovoFine 1 x 3 ml předplněné pero + 7 jehel NovoTwist
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci.
Subkutánní podání
Jehly nejsou součástí balení.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Promíchejte dle instrukcí.
Používejte pouze tehdy, pokud je suspenze po promíchání vodná, stejnoměrně bílá a zakalená. Pro použití pouze jednou osobou.
Určeno pro použití s jednorázovými jehlami NovoFine nebo NovoTwist o délce do 8 mm.
8. POUŽITELNOST
Použitelné do
Během používání: spotřebujte do 4 týdnů.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Před otevřením: uchovávejte v chladničce (2 °C až 8 °C).
Během používání: chraňte před chladem. Uchovávejte při teplotě do 30 °C. Chraňte před mrazem.
Mějte na peru nasazen kryt, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Po každé injekci odstraňte jehlu.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
12. REGISTRAČNÍ ČÍSLA
EU/1/00/142/023
EU/1/00/142/009
EU/1/00/142/010
EU/1/00/142/024
EU/1/00/142/025
1 pero o obsahu 3 ml 5 per po 3 ml 10 per po 3 ml
1 pero o obsahu 3 ml a 7 jehel NovoFine 1 pero o obsahu 3 ml a 7 jehel NovoTwist
13. ČÍSLO ŠARŽE
č.S.
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
NovoMix 30 FlexPen
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA PODÁNÍ
NovoMix 30 FlexPen 100 jednotek/ml Injekční suspenze
30 % Insulinům aspartum solubile a 70 % Insulinům aspartum protaminatum cristallinum Subkutánní podání
2. ZPŮSOB PODÁNÍ
Promíchejte dle instrukcí. FlexPen
3. POUŽITELNOST
Použitelné do
4. ČÍSLO ŠARŽE
č.S.
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
3 ml
6. JINÉ
Novo Nordisk A/S
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
NovoMix 50 FlexPen 100 jednotek/ml Injekční suspenze v předplněném peru
50 % Insulinum aspartum solubile a 50 % Insulinum aspartum protaminatum cristallinum
2. OBSAH LÉČIVÉ LÁTKY
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile/Insulinum aspartum protaminatum cristallinum v poměru 50/50 (odpovídá 3,5 mg). 1 předplněné pero obsahuje 3 ml odpovídající 300 jednotkám,
3. SEZNAM POMOCNÝCH LÁTEK
glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselinu chlorovodíkovou/hydroxid sodný pro úpravu pH a vodu na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční suspenze
1 x 3 ml předplněné pero 5 x 3 ml předplněná pera 10 x 3 ml předplněná pera
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci.
Subkutánní podání
Jehly nejsou součástí balení.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Promíchejte dle instrukcí.
Používejte pouze tehdy, pokud je suspenze po promíchání vodná, stejnoměrně bílá a zakalená. Pro použití pouze jednou osobou.
Určeno pro použití s jednorázovými jehlami NovoFine nebo NovoTwist o délce do 8 mm.
Použitelné do
Během používání: spotřebujte do 4 týdnů.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Před otevřením: uchovávejte v chladničce (2 °C až 8 °C).
Během používání: chraňte před chladem. Uchovávejte při teplotě do 30 °C. Chraňte před mrazem.
Mějte na peru nasazen kryt, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Po každé injekci odstraňte jehlu.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
12. REGISTRAČNÍ ČÍSLA
EU/1/00/142/014 1 pero po3 ml EU/1/00/142/015 5 per po 3 ml EU/1/00/142/016 10 per po 3 ml
13. ČÍSLO ŠARŽE
č.S.
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
NovoMix 50 FlexPen
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA PODÁNÍ
NovoMix 50 FlexPen 100 jednotek/ml Injekční suspenze
50 % Insulinům aspartum solubile a 50 % Insulinům aspartum protaminatum cristallinum Subkutánní podání
2. ZPŮSOB PODÁNÍ
Promíchejte dle instrukcí. FlexPen
3. POUŽITELNOST
Použitelné do
4. ČÍSLO ŠARŽE
č.S.
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
3 ml
6. JINÉ
Novo Nordisk A/S
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
NovoMix 70 FlexPen 100 jednotek/ml Injekční suspenze v předplněném peru
70 % Insulinum aspartum solubile a 30 % Insulinum aspartum protaminatum cristallinum
2. OBSAH LÉČIVÉ LÁTKY
1 ml suspenze obsahuje 100 jednotek Insulinum aspartum solubile/Insulinum aspartum protaminatum cristallinum v poměru 70/30 (odpovídá 3,5 mg). 1 předplněné pero obsahuje 3 ml odpovídající 300 jednotkám,
3. SEZNAM POMOCNÝCH LÁTEK
glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselinu chlorovodíkovou/hydroxid sodný pro úpravu pH a vodu na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční suspenze
1 x 3 ml předplněné pero 5 x 3 ml předplněná pera 10 x 3 ml předplněná pera
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci.
Subkutánní podání
Jehly nejsou součástí balení.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Promíchejte dle instrukcí.
Používejte pouze tehdy, pokud je suspenze po promíchání vodná, stejnoměrně bílá a zakalená. Pro použití pouze jednou osobou.
Určeno pro použití s jednorázovými jehlami NovoFine nebo NovoTwist o délce do 8 mm.
Použitelné do
Během používání: spotřebujte do 4 týdnů.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Před otevřením: uchovávejte v chladničce (2 °C až 8 °C).
Během používání: chraňte před chladem. Uchovávejte při teplotě do 30 °C. Chraňte před mrazem.
Mějte na peru nasazen kryt, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Po každé injekci odstraňte jehlu.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
12. REGISTRAČNÍ ČÍSLA
EU/1/00/142/020 1 pero po 3 ml EU/1/00/142/021 5 per po 3 ml EU/1/00/142/022 10 per po 3 ml
13. ČÍSLO ŠARŽE
č.S.
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
NovoMix 70 FlexPen
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA PODÁNÍ
NovoMix 70 FlexPen 100 jednotek/ml Injekční suspenze
70 % Insulinům aspartum solubile a 30 % Insulinům aspartum protaminatum cristallinum Subkutánní podání
2. ZPŮSOB PODÁNÍ
Promíchejte dle instrukcí. FlexPen
3. POUŽITELNOST
Použitelné do
4. ČÍSLO ŠARŽE
č.S.
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
3 ml
6. JINÉ
Novo Nordisk A/S
B. PŘÍBALOVÁ INFORMACE
NovoMix 30 Penfill 100 jednotek/ml injekční suspenze v zásobní vložce
30 % Insulinům aspartum solubile a 70 % Insulinům aspartum protaminatum cristallinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí
ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek NovoMix 30 a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 30 používat
3. Jak se přípravek NovoMix 30 používá
4. Možné nežádoucí účinky
5. Jak přípravek NovoMix 30 uchovávat
6. Obsah balení a další informace
1. Co je přípravek NovoMix 30 a k čemu se používá
NovoMix 30 je moderní inzulin (analog inzulinu) s krátkodobě i střednědobě působícím účinkem v poměru 30/70. Moderní inzulinové přípravky jsou zdokonalené verze lidského inzulinu.
NovoMix 30 je používán ke snižování vysoké hladiny cukru v krvi u dospělých, dospívajících a dětí ve věku 10 let a více s diabetes mellitus (cukrovkou). Diabetes je onemocnění, při němž tělo neprodukuje dostatek inzulinu ke kontrole hladiny cukru v krvi. NovoMix 30 může být používán v kombinaci s tabletami na léčbu diabetu.
NovoMix 30 začne snižovat hladinu krevního cukru za 10 - 20 minut po podání, maximálního účinku dosahuje za 1 až 4 hodiny po podání a jeho účinek přetrvává až 24 hodin.
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 30 používat
Nepoužívejte NovoMix 30
► Jestliže jste alergický(á) na inzulin aspart nebo na kteroukoli další složku tohoto přípravku (viz bod 6, Obsah balení a další informace).
► Jestliže máte podezření, že nastupuje hypoglykemie (nízká hladina krevního cukru) (viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4).
► V inzulinových infuzních pumpách
► Pokud zásobní vložka nebo aplikátor obsahující zásobní vložku upadly, jsou poškozené nebo promáčklé.
► Jestliže inzulin nebyl správně skladován nebo byl zmražen, viz bod 5, Jak přípravek NovoMix 30 uchovávat.
► Jestliže po promíchání inzulin není vodný, stejnoměrně bílý a zakalený.
► Jestliže po promíchání obsahuje shluky nebo pevné bílé částice usazené na dně nebo stěně zásobní vložky.
Pokud platí něco z výše uvedeného, NovoMix 30 neužívejte. Požádejte o radu lékaře, zdravotní sestru nebo lékárníka.
Před užitím přípravku NovoMix 30
► Podle informací na štítku se ujistěte, že se jedná o správný typ inzulínu.
► Vždy zkontrolujte zásobní vložku včetně gumového pístu na spodní straně zásobní vložky. Nepoužívejte ji, pokud je viditelné jakékoliv poškození nebo pokud byl gumový píst vytažen nad bílý kódovací proužek na spodní straně zásobní vložky. Může to být důsledek úniku inzulinu. Máte-li podezření, že je zásobní vložka poškozena, vraťte ji svému dodavateli. Další pokyny najdete ve své příručce k používání injekčního pera.
► Pro každou aplikaci použijte vždy novou jehlu, aby se zabránilo kontaminaci.
► Jehly a NovoMix 30 Penfill nesmíte nikomu půjčovat.
Upozornění a opatření
Některé stavy a činnosti mohou ovlivnit vaši potřebu inzulinu. Poraďte se s lékařem:
► jestliže máte obtíže s ledvinami nebo játry či nadledvinami, podvěskem mozkovým nebo štítnou žlázou
► jestliže vykonáváte větší fyzickou aktivitu než obvykle nebo pokud chcete učinit změnu ve své běžné dietě, neboť to může ovlivnit hladinu cukru v krvi
► pokud jste nemocný(á), pokračujte v inzulinové léčbě a poraďte se s lékařem
► pokud cestujete do ciziny, cestování přes různá časová pásma může ovlivnit Vaši potřebu inzulinu a časování injekcí.
Děti a dospívající
• NovoMix 30 může být používán u dospívajících a dětí ve věku od 10 let.
• Pro děti ve věku od 6 - 9 let existují s přípravkem NovoMix 30 omezené klinické zkušenosti.
• Pro použití přípravku NovoMix 30 u dětí ve věku do 6 let nejsou dostupné žádné údaje.
Další léčivé přípravky a přípravek NovoMix 30
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Některé léčivé přípravky ovlivňují hladinu krevního cukru, což může znamenat, že vaše dávka inzulinu musí být změněna. Seznam nejběžnějších léčivých přípravků, které mohou ovlivnit vaši léčbu inzulinem, je uveden níže.
Vaše hladina krevního cukru může být snížena (hypoglykemie), pokud užíváte:
• jiné přípravky na léčbu cukrovky
• inhibitory monoaminooxidázy (IMAO) (používané k léčbě deprese)
• beta-blokátory (používané k léčbě vysokého krevního tlaku)
• inhibitory angiotensin konvertujícího enzymu (ACE) (používané k léčbě některých srdečních onemocnění nebo vysokého krevního tlaku)
• salicyláty (používané k úlevě od bolesti nebo ke snížení horečky)
• anabolické steroidy (jako například testosteron)
• sulfonamidy (používané k léčbě infekcí).
Vaše hladina krevního cukru může být zvýšena (hyperglykemie), pokud užíváte:
• perorální antikoncepci (používaná ke kontrole početí)
• thiazidy (používané k léčbě vysokého krevního tlaku nebo nadměrného zadržování tekutin)
• glukokortikoidy (jako například „kortison“ používaný k léčbě zánětů)
• hormony štítné žlázy (používané k léčbě poruch štítné žlázy)
• sympatomimetika (jako například epinefrin [adrenalin], salbutamol nebo terbutalin používané k léčbě astmatu)
• růstový hormon (lék ke stimulaci skeletálního a somatického růstu a mající vliv na metabolické procesy v těle)
• danazol (lék ovlivňující ovulaci).
Oktreotid a lanreotid (používané k léčbě akromegalie - vzácné hormonální poruchy, která se obvykle objevuje u dospělých středního věku a je způsobena nadměrnou produkcí růstového hormonu podvěskem mozkovým) mohou hladinu cukru v krvi buď zvyšovat nebo snižovat.
Beta-blokátory (používané k léčbě vysokého krevního tlaku) mohou oslabit nebo zcela potlačit první varovné příznaky umožňující rozpoznat nízkou hladinu cukru v krvi.
Pioglitazon (tablety používané k léčbě diabetu 2. typu)
U některých pacientů s dlouhodobým onemocněním diabetem 2. typu a srdečním onemocněním či prodělanou cévní mozkovou příhodou, kteří byli léčeni pioglitazonem a inzulinem, došlo k rozvoji srdečního selhání. Informujte ošetřujícího lékaře, jakmile to bude možné, pokud pocítíte příznaky srdečního selhání jako jsou neobvyklá dušnost nebo rychlý nárůst hmotnosti či lokalizovaný otok (edém).
Pokud užíváte kterýkoli ze zde zmíněných léků, sdělte to lékaři, zdravotní sestře nebo lékárníkovi. Přípravek NovoMix 30 s alkoholem
► Pokud pijete alkohol, může se vaše potřeba inzulinu změnit, protože hladina cukru v krvi se může jak zvýšit, tak snížit. Je doporučena pečlivá kontrola.
Těhotenství a kojení
► Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat. Klinické zkušenosti s inzulinem aspart v těhotenství jsou omezené. Vaše dávka inzulinu může během těhotenství a po porodu vyžadovat změnu. Pečlivá kompenzace cukrovky a zvlášť prevence hypoglykemie je důležitá pro zdraví vašeho dítěte.
► Během kojení není léčba přípravkem NovoMix 30 omezena.
Pokud jste těhotná či kojíte, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
► Zeptejte se, prosím, svého lékaře, zda můžete řídit auto nebo obsluhovat stroje, pokud:
• máte časté hypoglykemie
• je pro vás obtížné hypoglykemii rozeznat.
Pokud máte hladinu krevního cukru příliš nízkou nebo vysokou, může to ovlivnit vaše soustředění a schopnost reagovat a tím také vaši schopnost řídit nebo obsluhovat stroje. Mějte na paměti, že byste mohl(a) ohrozit sebe nebo ostatní.
Důležitá informace o některých pomocných látkách přípravku NovoMix 30
NovoMix 30 obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. v podstatě je „bez sodíku“.
3. Jak se přípravek NovoMix 30 používá Dávkování inzulinu a kdy inzulin užívat
Vždy užívejte inzulin a upravujte svoji dávku přesně tak, jak vám ošetřující lékař řekl. Pokud si nejste jistý(á), poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
NovoMix 30 má být obecně podáván bezprostředně před jídlem. Do 10 minut po podání injekce snězte jídlo nebo svačinu, abyste předešel(předešla) nízké hladině cukru v krvi. Pokud je to nutné, může být NovoMix 30 podán i brzy po jídle. Další informace viz níže Jak a kam aplikovat injekci.
Používáte-li NovoMix 30 v kombinaci s tabletami na léčbu diabetu, mělo by být upraveno dávkování.
Svůj inzulin neměňte, pokud vám to lékař neřekne. Pokud vám lékař změnil typ nebo druh inzulinu, je možné, že vám bude muset upravit také jeho dávkování.
Použití u dětí a dospívajících
NovoMix 30 může být používán u dospívajících a dětí ve věku od 10 let, pokud je preferován premixovaný inzulin. Pro děti ve věku 6 - 9 let existují omezená klinická data. Pro použití přípravku NovoMix 30 u dětí ve věku do 6 let nejsou dostupné žádné údaje.
Použití u zvláštních skupin pacientů
Máte-li sníženou funkci ledvin nebo jater, či pokud je vám více než 65 let, bude u vás nutno sledovat hladinu cukru v krvi intenzivněj i a konzultovat změny v dávkování inzulinu s lékařem.
Jak a kam si aplikovat injekci
NovoMix 30 je určen pro aplikaci pod kůži (subkutánně). Nikdy neaplikujte inzulin přímo do žíly (intravenózně) nebo svalu (intramuskulárně).
Při každé injekci střídejte místa vpichu v rámci té oblasti, kterou právě k aplikaci používáte. To může snižovat riziko tvorby bouliček nebo důlků v kůži (viz bod 4, Možné nežádoucí účinky). Nejlepšími místy pro aplikaci injekce jsou: přední strana břicha, hýždě, přední strana stehen nebo horní části paží. Inzulin bude mít rychlejší účinek, pokud jej aplikujete do oblasti kolem pasu. Vždy byste si měl(a) pravidelně měřit obsah cukru v krvi.
► Nenaplňujte znovu zásobní vložku.
► Zásobní vložky NovoMix 30 Penfill jsou navrženy k použití s aplikátory Novo Nordisk a jehlami NovoFine nebo NovoTwist.
► Jestliže jste léčen(a) přípravkem NovoMix 30 Penfill a zároveň jiným inzulinem v zásobních vložkách Penfill, měl(a) byste používat dva aplikátory, pro každý typ inzulinu jeden.
► Vždy noste náhradní zásobní vložku Penfill pro případ, že byste tu, kterou právě používáte, ztratil(a) nebo by došlo k jejímu poškození.
Promíchání přípravku NovoMix 30
Vždy se ujistěte, že v zásobní vložce zbývá dostatek inzulinu (alespoň 12 jednotek), aby ho vůbec bylo možno promíchat. Pokud v zásobní vložce nezbylo dost inzulinu, použijte novou. Další instrukce najdete v příručce k injekčnímu peru.
► Pokaždé, když začínáte používat nový NovoMix 30 Penfill (před vložením zásobní vložky do aplikátoru)
• Než inzulin použijete, nechte ho ohřát na pokojovou teplotu. To umožní snadnější promíchání.
• Převalujte zásobní vložku mezi dlaněmi 10krát - je důležité držet zásobní vložku v horizontální (vodorovné) poloze (viz obrázek A).
• Pohybujte zásobní vložkou nahoru a dolů mezi pozicemi a a b (viz obrázek B) 10krát tak, aby se skleněná kulička pohybovala z jednoho konce zásobní vložky na druhý.
• Opakujte převalování a promíchávání (viz obrázky A a B) tak dlouho, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Zásobní vložku nepoužívejte, pokud inzulin není po promíchání vodný, stejnoměrně bílý a zakalený.
• Dokončete ostatní kroky injekční aplikace bez dalšího zdržení
► Před každou další injekcí
Pohybujte aplikátorem s vloženou zásobní vložkou nahoru a dolů mezi polohami a a b (viz obrázek B) nejméně 10krát, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Zásobní vložku nepoužívejte, pokud inzulin není po promíchání vodný, stejnoměrně bílý a zakalený. Dokončete ostatní kroky injekční aplikace bez dalšího zdržení.

Obrázek B

Jak si aplikovat injekci přípravku NovoMix 30
► Aplikujte inzulin pod kůži. Používejte injekční techniku, kterou vám doporučil váš lékař nebo zdravotní sestra a popsanou v příručce k vašemu injekčnímu peru.
► Nechte jehlu pod kůží po dobu alespoň 6 vteřin. Dávkovací tlačítko držte zcela stlačené, dokud jehlu nevytáhnete z kůže. To zaručí podání správné dávky a omezí možné proniknutí krve do jehly nebo inzulinové zásobní vložky.
► Po každé aplikaci se ujistěte, že jste odstranil(a) a vyhodil(a) jehlu a že skladujete NovoMix 30 bez nasazené jehly. Jinak by mohla unikat tekutina, což může způsobit nepřesné dávkování.
Jestliže jste užil(a) více inzulínu, než jste měl(a)
Pokud jste užil(a) příliš inzulinu, vaše hladina cukru v krvi se může příliš snížit (hypoglykemie). Viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4.
Jestliže jste zapomněl(a) užít inzulin
Jestliže jste zapomněl(a) užít inzulin, vaše hladina krevního cukru může stoupnout příliš vysoko (hyperglykemie). Viz část c) Důsledky diabetu v bodě 4.
Jestliže jste přestal(a) užívat inzulin
Inzulin nepřestávejte užívat bez porady s lékařem, který vám poradí, co je třeba dělat. Mohlo by to vést k velmi vysoké hladině krevního cukru (těžké hyperglykemii) a ketoacidóze. Viz část c) Důsledky diabetu v bodě 4.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
a) Souhrn závažných a velmi častých nežádoucích účinků
Nízká hladina cukru v krvi (hypoglykemie) je velmi častý nežádoucí účinek. Může se projevit u více než 1 pacienta z 10.
Nízká hladina cukru může nastat, pokud:
• si aplikujete příliš mnoho inzulinu
• jíte příliš málo nebo vynecháte-li jídlo
• cvičíte více než obvykle
• pijete alkohol (viz bod 2, Přípravek NovoMix 30 s alkoholem).
Příznaky nízké hladiny cukru v krvi: studený pot, chladná bledá pokožka, bolest hlavy, rychlý srdeční tep, pocit nevolnosti, pocit velkého hladu, dočasné změny vidění, ospalost, neobvyklá vyčerpanost a slabost, nervozita nebo třes, pocit úzkosti, pocit zmatenosti, potíže s koncentrací.
Velmi nízká hladina cukru v krvi může vést k bezvědomí. Pokud déle trvající nízká hladina cukru v krvi není léčena, může způsobit poškození mozku (dočasné nebo trvalé) a dokonce úmrtí. Z bezvědomí se můžete zotavit rychleji, pokud vám někdo, kdo ví, jak jej použít, aplikuje hormon glukagon. Pokud dostanete glukagon, budete potřebovat glukózu nebo sladkou přesnídávku ihned poté, co nabudete vědomí. Pokud nereagujete na léčbu glukagonem, budete muset být léčen(a) v nemocnici.
Co dělat, pokud pocítíte příznaky nízké hladiny cukru v krvi:
► Pokud pocítíte příznaky nízké hladiny cukru v krvi, vezměte si glukózové tablety nebo jinou přesnídávku s vysokým obsahem cukru (např. sladkosti, sušenky, ovocnou šťávu). Pokud je to možné, změřte si hladinu cukru v krvi a odpočívejte. Vždy s sebou pro případ potřeby noste glukózové tablety nebo sladkosti s vysokým obsahem cukru.
► Poté, co příznaky nízké hladiny cukru v krvi ustoupí nebo se u vás stabilizuje hladina cukru v krvi, pokračujte s inzulinovou léčbou jako obvykle.
► Míváte-li tak nízkou hladinu cukru v krvi, že omdlíváte, pokud jste potřeboval(a) aplikovat glukagon nebo pokud míváte nízkou hladinu cukru v krvi často, pohovořte si se svým lékařem. Možná bude potřeba upravit množství nebo časové intervaly podání inzulinu, jídla nebo cvičení.
Řekněte lidem ve svém okolí, že máte diabetes, a seznamte je s jeho důsledky včetně rizika, že omdlíte (upadnete do bezvědomí) z důvodu nízké hladiny cukru v krvi. Řekněte jim, že pokud omdlíte, musí vás položit na bok a okamžitě zajistit lékařskou pomoc. Nesmějí vám dávat najíst ani napít, protože byste se mohl(a) zadusit.
Závažné alergické reakce na NovoMix 30 nebo na některou z jeho pomocných látek (tzv. systémová alergická reakce) je velmi vzácný nežádoucí účinek. Může být však potenciálně život ohrožující. Může se projevit u méně než 1 pacienta z 10 000.
Vyhledejte ihned lékařskou pomoc:
• Pokud se příznaky alergie rozšíří na další části těla.
• Pokud se náhle necítíte dobře a začnete se potit, pociťujete nevolnost (zvracení), máte dýchací potíže, zrychlený tep a točí se vám hlava.
► Pokud zaznamenáte některé z těchto příznaků, okamžitě vyhledejte lékařskou pomoc.
b) Souhrn ostatních nežádoucích účinků
Méně časté nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta ze 100.
Příznaky alergie: v místě vpichu se mohou objevit různé příznaky místní alergické reakce (bolest, zarudnutí, kopřivka, zánět, podlitiny, otok a svědění). Obvykle vymizí po několika týdnech inzulinové léčby. Pokud nevymizí, navštivte svého lékaře.
Poruchy vidění: na počátku léčby inzulinem může dojít k poruchám vidění, tyto poruchy jsou však obvykle přechodného rázu.
Změny v místě vpichu (lipodystrofie): tuková tkáň pod kůží se může v místě vpichu ztenčit (lipoatrofie) nebo zesílit (lipohypertrofie). Obměňování míst vpichu při každé injekci snižuje riziko takových změn kůže. Pokud zjistíte, že vaše kůže má v místě vpichu dolíčky nebo zesílení, informujte svého lékaře nebo zdravotní sestru. Tyto reakce se totiž mohou zhoršit nebo mohou změnit absorbci inzulinu, pokud si do tohoto místa inzulin aplikujete.
Otoky kloubů: na začátku inzulinové léčby může dojít k zadržování vody v oblasti kotníků a dalších kloubů. Obvykle tato reakce brzy odezní. Pokud ne, kontaktujte lékaře.
Diabetická retinopatie (oční onemocnění spojené s cukrovkou, které může vést ke ztrátě zraku): jestliže trpíte diabetickou retinopatií a hladina vašeho krevního cukru se velmi rychle zlepší, může dojít ke zhoršení retinopatie. Poraďte se o tom se svým lékařem.
Vzácné nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta z 1 000.
Bolestivá neuropatie (bolest způsobená poškozením nervů): jestliže se hladina vašeho krevního cukru velmi rychle zlepší, může se dostavit bolest nervového původu. Tento stav se nazývá akutní bolestivá neuropatie a obvykle se jedná o přechodný stav.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
c) Důsledky diabetu
Vysoká hladina cukru v krvi (hyperglykemie)
Vysoká hladina cukru může nastat, pokud:
• j ste si neaplikoval(a) dostatečné množství inzulinu
• zapomněl(a) jste si aplikovat inzulin nebo jste ho přestal(a) užívat
• opakovaně užíváte menší dávky inzulinu, než je třeba
• máte infekci a/nebo horečku
• jíte více než obvykle
• cvičíte méně než obvykle.
Varovné příznaky vysoké hladiny cukru v krvi:
Varovné příznaky se objevují postupně. Zahrnují: častější močení, pocit žízně, ztrátu chuti k jídlu, pocit nevolnosti (pocit na zvracení nebo zvracení), pocit ospalosti nebo únavy, zarudlou, suchou pokožku, sucho v ústech a ovocný (acetonový) zápach dechu.
Co dělat, pokud pocítíte příznaky vysoké hladiny cukru v krvi:
► Pokud zaznamenáte některé z výše uvedených příznaků: zkontrolujte si hladinu krevního cukru, otestuje si moč na ketony, máte-li možnost, a potom ihned vyhledejte lékařskou pomoc.
► Mohou to být příznaky velmi závažného stavu nazývaného diabetická ketoacidóza (hromadění kyseliny v krvi, protože tělo odbourává místo cukru tuk). Pokud jej neléčíte, může vést až k diabetickému kómatu a případně ke smrti.
5. Jak přípravek NovoMix 30 uchovávat
Uchovávejte tento přípravek mimo dohled a dosah a dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku zásobní vložky a krabičce za „Použitelné do”. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Pokud zásobní vložku právě nepoužíváte, uchovávejte ji vždy v krabičce, aby byl přípravek chráněn před světlem. NovoMix 30 musí být chráněn před vysokými teplotami a světlem.
Před otevřením: NovoMix 30 Penfill, který není používán, musí být uchováván v chladničce (2 °C až 8 °C), mimo chladicí zařízení. Chraňte před mrazem.
Před použitím vyjměte NovoMix 30 Penfill z chladničky. Pokaždé, když začínáte používat nový NovoMix 30 Penfill, je doporučeno promíchat inzulin dle instrukcí pro promíchání v bodě 3, část Promíchání přípravku NovoMix 30.
Během používání či pohotovostně nošený: NovoMix 30 Penfill, který používáte nebo nosíte jako náhradní, by neměl být uchováván v chladničce. Můžete jej nosit s sebou a uchovávat při pokojové teplotě (do 30 °C) až po dobu 4 týdnů.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co NovoMix 30 obsahuje
• Léčivou látkou je inzulin aspart. NovoMix 30 je směs složená z 30 % rozpustného inzulinu aspart a 70 % krystalického protaminového inzulinu aspart. 1 ml obsahuje 100 jednotek inzulinu aspart. Jedna zásobní vložka obsahuje 300 jednotek inzulinu aspart ve 3 ml injekční suspenze.
• Pomocnými látkami j sou glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselina chlorovodíková, hydroxid sodný a voda na injekci.
Jak NovoMix 30 vypadá a co obsahuje toto balení
NovoMix 30 je dodáván jako injekční suspenze. V zásobní vložce je umístěna skleněná kulička, která
usnadňuje promíchávání. Po promíchání by kapalina měla být vodná, stejnoměrně bílá a zakalená.
Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, nepoužívejte ho.
Velikosti balení jsou 5 a 10 zásobních vložek po 3 ml. Na trhu nemusí být všechny velikosti balení.
Zakalená, bílá vodná suspenze.
Držitel rozhodnutí o registraci a výrobce
Držitel rozhodnutí o registraci
Novo Nordisk A/S
Novo Allé
DK-2880 Bagsv^rd, Dánsko
Výrobce
Výrobce může být identifikován pomocí čísla šarže vytištěného na záložce krabičky a na štítku:
• Jsou-li druhý a třetí znak, S6, P5, K7, R7, VG, FG nebo ZF, pak je výrobcem Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
• Jsou-li druhý a třetí znak H7 nebo T6, pak je výrobcem Novo Nordisk Production SAS, 45 Avenue ďOrléans F-28000 Chartres, Francie
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky: http://www.ema.europa.eu/
NovoMix 50 Penfill 100 jednotek/ml injekční suspenze v zásobní vložce
50 % Insulinům aspartum solubile a 50 % Insulinům aspartum protaminatum cristallinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek NovoMix 50 a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 50 používat
3. Jak se přípravek NovoMix 50 používá
4. Možné nežádoucí účinky
5. Jak přípravek NovoMix 50 uchovávat
6. Obsah balení a další informace
1. Co je přípravek NovoMix 50 a k čemu se používá
NovoMix 50 je moderní inzulin (analog inzulinu) s krátkodobě i střednědobě působícím účinkem v poměru 50/50. Moderní inzulinové přípravky jsou zdokonalené verze lidského inzulinu.
NovoMix 50 je používán ke snižování vysoké hladiny cukru v krvi u pacientů s diabetes mellitus (cukrovkou). Diabetes je onemocnění, při němž tělo neprodukuje dostatek inzulinu ke kontrole hladiny cukru v krvi. NovoMix 50 může být používán v kombinaci s metforminem.
NovoMix 50 začne snižovat hladinu krevního cukru za 10 - 20 minut po podání, maximálního účinku dosahuje za 1 až 4 hodiny po podání a jeho účinek přetrvává až po dobu 14 - 24 hodin.
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 50 používat
Nepoužívejte NovoMix 50
► Jestliže jste alergický(á) na inzulin aspart nebo na kteroukoli další složku tohoto přípravku (viz bod 6, Obsah balení a další informace).
► Jestliže máte podezření, že nastupuje hypoglykemie (nízká hladina krevního cukru) (viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4).
► V inzulinových infuzních pumpách
► Pokud zásobní vložka nebo aplikátor obsahující zásobní vložku upadly, jsou poškozené nebo promáčklé.
► Jestliže inzulin nebyl správně skladován nebo byl zmražen, viz bod 5, Jak přípravek NovoMix 50 uchovávat.
► Jestliže po promíchání inzulin není vodný, stejnoměrně bílý a zakalený
► Jestliže po promíchání obsahuje shluky nebo pevné bílé částice usazené na dně nebo stěně zásobní vložky.
Pokud platí něco z výše uvedeného, NovoMix 50 neužívejte. Požádejte o radu lékaře, zdravotní sestru
nebo lékárníka.
► Podle informací na štítku se ujistěte, že se jedná o správný typ inzulínu.
► Vždy zkontrolujte zásobní vložku včetně gumového pístu na spodní straně zásobní vložky. Nepoužívejte ji, pokud je viditelné jakékoliv poškození nebo pokud byl gumový píst vytažen nad bílý kódovací proužek na spodní straně zásobní vložky. Může to být důsledek úniku inzulinu. Máte-li podezření, že je zásobní vložka poškozena, vraťte ji svému dodavateli. Další pokyny najdete ve své příručce k používání injekčního pera.
► Pro každou aplikaci použijte vždy novou jehlu, aby se zabránilo kontaminaci.
► Jehly a NovoMix 50 Penfill nesmíte nikomu půjčovat.
Upozornění a opatření
Některé stavy a činnosti mohou ovlivnit vaši potřebu inzulinu. Poraďte se s lékařem:
► jestliže máte obtíže s ledvinami nebo játry či nadledvinami, podvěskem mozkovým nebo štítnou žlázou
► jestliže vykonáváte větší fyzickou aktivitu než obvykle nebo pokud chcete učinit změnu ve své běžné dietě, neboť to může ovlivnit hladinu cukru v krvi
► pokud jste nemocný(á), pokračujte v inzulinové léčbě a poraďte se s lékařem
► pokud cestujete do ciziny, cestování přes různá časová pásma může ovlivnit Vaši potřebu inzulinu a časování injekcí.
Další léčivé přípravky a přípravek NovoMix 50
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Některé léčivé přípravky ovlivňují hladinu krevního cukru, což může znamenat, že vaše dávka inzulinu musí být změněna. Seznam nejběžnějších léčivých přípravků, které mohou ovlivnit vaši léčbu inzulinem, je uveden níže.
Vaše hladina krevního cukru může být snížena (hypoglykemie), pokud užíváte:
• jiné přípravky na léčbu cukrovky
• inhibitory monoaminooxidázy (IMAO) (používané k léčbě deprese)
• beta-blokátory (používané k léčbě vysokého krevního tlaku)
• inhibitory angiotensin konvertujícího enzymu (ACE) (používané k léčbě některých srdečních onemocnění nebo vysokého krevního tlaku)
• salicyláty (používané k úlevě od bolesti nebo ke snížení horečky)
• anabolické steroidy (jako například testosteron)
• sulfonamidy (používané k léčbě infekcí).
Vaše hladina krevního cukru může být zvýšena (hyperglykemie), pokud užíváte:
• perorální antikoncepci (používaná ke kontrole početí)
• thiazidy (používané k léčbě vysokého krevního tlaku nebo nadměrného zadržování tekutin)
• glukokortikoidy (jako například „kortison“ používaný k léčbě zánětů)
• hormony štítné žlázy (používané k léčbě poruch štítné žlázy)
• sympatomimetika (jako například epinefrin [adrenalin], salbutamol nebo terbutalin používané k léčbě astmatu)
• růstový hormon (lék ke stimulaci skeletálního a somatického růstu a mající vliv na metabolické procesy v těle)
• danazol (lék ovlivňující ovulaci).
Oktreotid a lanreotid (používané k léčbě akromegalie - vzácné hormonální poruchy, která se obvykle objevuje u dospělých středního věku a je způsobena nadměrnou produkcí růstového hormonu podvěskem mozkovým) mohou hladinu cukru v krvi buď zvyšovat nebo snižovat.
Beta-blokátory (používané k léčbě vysokého krevního tlaku) mohou oslabit nebo zcela potlačit první varovné příznaky umožňující rozpoznat nízkou hladinu cukru v krvi.
Pioglitazon (tablety používané k léčbě diabetu 2. typu)
U některých pacientů s dlouhodobým onemocněním diabetem 2. typu a srdečním onemocněním či prodělanou cévní mozkovou příhodou, kteří byli léčeni pioglitazonem a inzulinem, došlo k rozvoji srdečního selhání. Informujte ošetřujícího lékaře, jakmile to bude možné, pokud pocítíte příznaky srdečního selhání jako jsou neobvyklá dušnost nebo rychlý nárůst hmotnosti či lokalizovaný otok (edém).
Pokud užíváte kterýkoli ze zde zmíněných léků, sdělte to lékaři, zdravotní sestře nebo lékárníkovi. Přípravek NovoMix 50 s alkoholem
► Pokud pijete alkohol, může se vaše potřeba inzulinu změnit, protože hladina cukru v krvi se může jak zvýšit, tak snížit. Je doporučena pečlivá kontrola.
Těhotenství a kojení
► Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat. Klinické zkušenosti s inzulinem aspart v těhotenství jsou omezené. Vaše dávka inzulinu může během těhotenství a po porodu vyžadovat změnu. Pečlivá kompenzace cukrovky a zvlášť prevence hypoglykemie je důležitá pro zdraví vašeho dítěte.
► Během kojení není léčba přípravkem NovoMix 50 omezena.
Pokud jste těhotná či kojíte, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
► Zeptejte se, prosím, svého lékaře, zda můžete řídit auto nebo obsluhovat stroje, pokud:
• máte časté hypoglykemie
• je pro vás obtížné hypoglykemii rozeznat.
Pokud máte hladinu krevního cukru příliš nízkou nebo vysokou, může to ovlivnit vaše soustředění a schopnost reagovat a tím také vaši schopnost řídit nebo obsluhovat stroje. Mějte na paměti, že byste mohl(a) ohrozit sebe nebo ostatní.
Důležitá informace o některých pomocných látkách přípravku NovoMix 50
NovoMix 50 obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. v podstatě je „bez sodíku“.
3. Jak se přípravek NovoMix 50 používá Dávkování inzulinu a kdy inzulin užívat
Vždy užívejte inzulin a upravujte svoji dávku přesně tak, jak vám ošetřující lékař řekl. Pokud si nejste jistý(á), poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
NovoMix 50 má být obecně podáván bezprostředně před jídlem. Do 10 minut po podání injekce snězte jídlo nebo svačinu, abyste předešel(předešla) nízké hladině cukru v krvi. Pokud je to nutné, může být NovoMix 50 podán i brzy po jídle. Další informace viz níže Jak a kam aplikovat injekci.
Používáte-li NovoMix 50 v kombinaci s metforminem, mělo by být upraveno dávkování.
Svůj inzulin neměňte, pokud vám to lékař neřekne. Pokud vám lékař změnil typ nebo druh inzulínu, je možné, že vám bude muset upravit také jeho dávkování.
Použití u dětí a dospívajících
Nebyly prováděny klinické studie s používáním přípravku NovoMix 50 dětmi a dospívajícími ve věku do 18 let.
Použití u zvláštních skupin pacientů
Máte-li sníženou funkci ledvin nebo jater či, pokud je vám více než 65 let, bude u vás nutno sledovat hladinu cukru v krvi intenzivněj i a konzultovat změny v dávkování inzulinu s lékařem.
Jak a kam si aplikovat injekci
NovoMix 50 je určen pro aplikaci pod kůži (subkutánně). Nikdy neaplikujte inzulin přímo do žíly (intravenózně) nebo svalu (intramuskulárně).
Při každé injekci střídejte místa vpichu v rámci té oblasti, kterou právě k aplikaci používáte. To může snižovat riziko tvorby bouliček nebo důlků v kůži (viz bod 4, Možné nežádoucí účinky). Nejlepšími místy pro aplikaci injekce jsou: přední strana břicha, hýždě, přední strana stehen nebo horní části paží. Inzulin bude mít rychlejší účinek, pokud jej aplikujete do oblasti kolem pasu. Vždy byste si měl(a) pravidelně měřit obsah cukru v krvi.
► Nenaplňujte znovu zásobní vložku.
► Zásobní vložky NovoMix 50 Penfill jsou navrženy k použití s aplikátory Novo Nordisk a jehlami NovoFine nebo NovoTwist.
► Jestliže jste léčen(a) přípravkem NovoMix 50Penfill a zároveň jiným inzulinem v zásobních vložkách Penfill, měl(a) byste používat dva aplikátory, pro každý typ inzulinu jeden.
► Vždy noste náhradní zásobní vložku Penfill pro případ, že byste tu, kterou právě používáte, ztratil(a) nebo by došlo k jejímu poškození.
Promíchání přípravku NovoMix 50
Vždy se ujistěte, že v zásobní vložce zbývá dostatek inzulinu (alespoň 12 jednotek), aby ho vůbec bylo možno promíchat. Pokud v zásobní vložce nezbylo dost inzulinu, použijte novou. Další instrukce najdete v příručce k injekčnímu peru.
► Pokaždé, když začínáte používat nový NovoMix 50 Penfill (před vložením zásobní vložky do aplikátoru)
• Než inzulin použijete, nechte ho ohřát na pokojovou teplotu. To umožní snadnější promíchání.
• Převalujte zásobní vložku mezi dlaněmi 10krát - je důležité držet zásobní vložku v horizontální (vodorovné) poloze (viz obrázek A).
• Pohybujte zásobní vložkou nahoru a dolů mezi pozicemi a a b (viz obrázek B) 10krát tak, aby se skleněná kulička pohybovala z jednoho konce zásobní vložky na druhý.
• Opakujte převalování a promíchávání (viz obrázky A a B) tak dlouho, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Zásobní vložku nepoužívejte, pokud inzulin není po promíchání vodný, stejnoměrně bílý a zakalený.
• Dokončete ostatní kroky injekční aplikace bez dalšího zdržení
► Před každou další injekcí
• Pohybujte aplikátorem s vloženou zásobní vložkou nahoru a dolů mezi polohami a a b (viz obrázek B) nejméně 10krát, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Zásobní vložku nepoužívejte, pokud inzulin není po promíchání vodný stejnoměrně bílý a zakalený.
• Pokud tento postup samotný nestačí k tomu, aby vznikla vodná, stejnoměrně bílá a zakalená tekutina, opakujte převalování a promíchávání popsané výše tak dlouho, dokud tekutina nemá vodný, stejnoměrně bílý a zakalený vzhled.
• Dokončete ostatní kroky injekční aplikace bez dalšího zdržení.

Obrázek B

Jak si aplikovat injekci přípravku NovoMix 50
► Aplikujte inzulin pod kůži. Používejte injekční techniku, kterou vám doporučil váš lékař nebo zdravotní sestra a popsanou v příručce k vašemu injekčnímu peru.
► Nechte jehlu pod kůží po dobu alespoň 6 vteřin. Dávkovací tlačítko držte zcela stlačené, dokud jehlu nevytáhnete z kůže. To zaručí podání správné dávky a omezí možné proniknutí krve do jehly nebo inzulinové zásobní vložky.
► Po každé aplikaci se ujistěte, že jste odstranil(a) a vyhodil(a) jehlu a že skladujete NovoMix 50 bez nasazené jehly. Jinak by mohla unikat tekutina, což může způsobit nepřesné dávkování.
Jestliže jste užil(a) více inzulínu, než jste měl(a)
Pokud jste užil(a) příliš inzulinu, vaše hladina cukru v krvi se může příliš snížit (hypoglykemie). Viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4.
Jestliže jste zapomněl(a) užít inzulin
Jestliže jste zapomněl(a) užít inzulin, vaše hladina krevního cukru může stoupnout příliš vysoko (hyperglykemie). Viz část c) Důsledky diabetu v bodě 4.
Jestliže jste přestal(a) užívat inzulin
Inzulin nepřestávejte užívat bez porady s lékařem, který vám poradí, co je třeba dělat. Mohlo by to vést k velmi vysoké hladině krevního cukru (těžké hyperglykemii) a ketoacidóze. Viz část c) Důsledky diabetu v bodě 4.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
a) Souhrn závažných a velmi častých nežádoucích účinků
Nízká hladina cukru v krvi (hypoglykemie) je velmi častý nežádoucí účinek. Může se projevit u více než 1 pacienta z 10.
Nízká hladina cukru může nastat, pokud:
• si aplikujete příliš mnoho inzulinu
• jíte příliš málo nebo vynecháte-li jídlo
• cvičíte více než obvykle
• pijete alkohol (viz bod 2, Přípravek NovoMix 50 s alkoholem).
Příznaky nízké hladiny cukru v krvi: studený pot, chladná bledá pokožka, bolest hlavy, rychlý srdeční tep, pocit nevolnosti, pocit velkého hladu, dočasné změny vidění, ospalost, neobvyklá vyčerpanost a slabost, nervozita nebo třes, pocit úzkosti, pocit zmatenosti, potíže s koncentrací.
Velmi nízká hladina cukru v krvi může vést k bezvědomí. Pokud déle trvající nízká hladina cukru v krvi není léčena, může způsobit poškození mozku (dočasné nebo trvalé) a dokonce úmrtí. Z bezvědomí se můžete zotavit rychleji, pokud vám někdo, kdo ví, jak jej použít, aplikuje hormon glukagon. Pokud dostanete glukagon, budete potřebovat glukózu nebo sladkou přesnídávku ihned poté, co nabudete vědomí. Pokud nereagujete na léčbu glukagonem, budete muset být léčen(a) v nemocnici.
Co dělat, pokud pocítíte příznaky nízké hladiny cukru v krvi:
► Pokud pocítíte příznaky nízké hladiny cukru v krvi, vezměte si glukózové tablety nebo jinou přesnídávku s vysokým obsahem cukru (např. sladkosti, sušenky, ovocnou šťávu). Pokud je to možné, změřte si hladinu cukru v krvi a odpočívejte. Vždy s sebou pro případ potřeby noste glukózové tablety nebo sladkosti s vysokým obsahem cukru.
► Poté, co příznaky nízké hladiny cukru v krvi ustoupí nebo se u vás stabilizuje hladina cukru v krvi, pokračujte s inzulinovou léčbou jako obvykle.
► Míváte-li tak nízkou hladinu cukru v krvi, že omdlíváte, pokud jste potřeboval(a) aplikovat glukagon nebo pokud míváte nízkou hladinu cukru v krvi často, pohovořte si se svým lékařem. Možná bude potřeba upravit množství nebo časové intervaly podání inzulinu, jídla nebo cvičení.
Řekněte lidem ve svém okolí, že máte diabetes, a seznamte je s jeho důsledky včetně rizika, že omdlíte (upadnete do bezvědomí) z důvodu nízké hladiny cukru v krvi. Řekněte jim, že pokud omdlíte, musí vás položit na bok a okamžitě zajistit lékařskou pomoc. Nesmějí vám dávat najíst ani napít, protože byste se mohl(a) zadusit.
Závažné alergické reakce na NovoMix 50 nebo na některou z jeho pomocných látek (tzv. systémová alergická reakce) je velmi vzácný nežádoucí účinek. Může být však potenciálně život ohrožující. Může se projevit u méně než 1 pacienta z 10 000.
Vyhledejte ihned lékařskou pomoc:
• Pokud se příznaky alergie rozšíří na další části těla.
• Pokud se náhle necítíte dobře a začnete se potit, pociťujete nevolnost (zvracení), máte dýchací potíže, zrychlený tep a točí se vám hlava.
► Pokud zaznamenáte některé z těchto příznaků, okamžitě vyhledejte lékařskou pomoc.
b) Souhrn ostatních nežádoucích účinků
Méně časté nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta ze 100.
Příznaky alergie: v místě vpichu se mohou objevit různé příznaky místní alergické reakce (bolest,
zarudnutí, kopřivka, zánět, podlitiny, otok a svědění). Obvykle vymizí po několika týdnech inzulinové léčby. Pokud nevymizí, navštivte svého lékaře.
Poruchy vidění: na počátku léčby inzulinem může dojít k poruchám vidění, tyto poruchy jsou však obvykle přechodného rázu.
Změny v místě vpichu (lipodystrofie): tuková tkáň pod kůží se může v místě vpichu ztenčit (lipoatrofie) nebo zesílit (lipohypertrofie). Obměňování míst vpichu při každé injekci snižuje riziko takových změn kůže. Pokud zjistíte, že vaše kůže má v místě vpichu dolíčky nebo zesílení, informujte svého lékaře nebo zdravotní sestru. Tyto reakce se totiž mohou zhoršit nebo mohou změnit absorbci inzulinu, pokud si do tohoto místa inzulin aplikujete.
Otoky kloubů: na začátku inzulinové léčby může dojít k zadržování vody v oblasti kotníků a dalších kloubů. Obvykle tato reakce brzy odezní. Pokud ne, kontaktujte lékaře.
Diabetická retinopatie (oční onemocnění spojené s cukrovkou, které může vést ke ztrátě zraku): jestliže trpíte diabetickou retinopatií a hladina vašeho krevního cukru se velmi rychle zlepší, může dojít ke zhoršení retinopatie. Poraďte se o tom se svým lékařem.
Vzácné nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta z 1 000.
Bolestivá neuropatie (bolest způsobená poškozením nervů): jestliže se hladina vašeho krevního cukru velmi rychle zlepší, může se dostavit bolest nervového původu. Tento stav se nazývá akutní bolestivá neuropatie a obvykle se jedná o přechodný stav.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
c) Důsledky diabetu
Vysoká hladina cukru v krvi (hyperglykemie)
Vysoká hladina cukru může nastat, pokud:
• j ste si neaplikoval(a) dostatečné množství inzulinu
• zapomněl(a) jste si aplikovat inzulin nebo jste ho přestal(a) užívat
• opakovaně užíváte menší dávky inzulinu, než je třeba
• máte infekci a/nebo horečku
• jíte více než obvykle
• cvičíte méně než obvykle.
Varovné příznaky vysoké hladiny cukru v krvi:
Varovné příznaky se objevují postupně. Zahrnují: častější močení, pocit žízně, ztrátu chuti k jídlu, pocit nevolnosti (pocit na zvracení nebo zvracení), pocit ospalosti nebo únavy, zarudlou, suchou pokožku, sucho v ústech a ovocný (acetonový) zápach dechu.
Co dělat, pokud pocítíte příznaky vysoké hladiny cukru v krvi:
► Pokud zaznamenáte některé z výše uvedených příznaků: zkontrolujte si hladinu krevního cukru, otestuje si moč na ketony, máte-li možnost, a potom ihned vyhledejte lékařskou pomoc.
► Mohou to být příznaky velmi závažného stavu nazývaného diabetická ketoacidóza (hromadění kyseliny v krvi, protože tělo odbourává místo cukru tuk). Pokud jej neléčíte, může vést až k diabetickému kómatu a případně ke smrti.
Uchovávejte tento přípravek mimo dohled a dosah a dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku zásobní vložky a krabičce za „Použitelné do”. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Pokud zásobní vložku právě nepoužíváte, uchovávejte ji vždy v krabičce, aby byl přípravek chráněn před světlem. NovoMix 50 musí být chráněn před vysokými teplotami a světlem.
Před otevřením: NovoMix 50 Penfill, který není používán, musí být uchováván v chladničce (2 °C až 8 °C), mimo chladicí zařízení. Chraňte před mrazem.
Před použitím vyjměte NovoMix 50 Penfill z chladničky. Pokaždé, když začínáte používat nový NovoMix 50 Penfill, je doporučeno promíchat inzulin dle instrukcí pro promíchání v bodě 3, část Promíchání přípravku NovoMix 50.
Během používání či pohotovostně nošený: NovoMix 50 Penfill, který používáte nebo nosíte jako náhradní, by neměl být uchováván v chladničce. Můžete jej nosit s sebou a uchovávat při pokojové teplotě (do 30 °C) až po dobu 4 týdnů.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co NovoMix 50 obsahuje
• Léčivou látkou je inzulin aspart. NovoMix 50 je směs složená z 50 % rozpustného inzulinu aspart a 50 % krystalického protaminového inzulinu aspart. 1 ml obsahuje 100 jednotek inzulinu aspart. Jedna zásobní vložka obsahuje 300 jednotek inzulinu aspart ve 3 ml injekční suspenze.
• Pomocnými látkami jsou glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselina chlorovodíková, hydroxid sodný a voda na injekci.
Jak NovoMix 50 vypadá a co obsahuje toto balení
NovoMix 50 je dodáván jako injekční suspenze. V zásobní vložce je umístěna skleněná kulička, která
usnadňuje promíchávání. Po promíchání by kapalina měla být vodná, stejnoměrně bílá a zakalená.
Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, nepoužívejte ho.
Velikosti balení jsou 1, 5 a 10 zásobních vložek po 3 ml. Na trhu nemusí být všechny velikosti balení.
Zakalená, bílá vodná suspenze.
Držitel rozhodnutí o registraci a výrobce
Novo Nordisk A/S
Novo Allé
DK-2880 Bagsv^rd, Dánsko
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky: http://www.ema.europa.eu//
NovoMix 70 Penfill 100 jednotek/ml injekční suspenze v zásobní vložce
70 % Insulinům aspartum solubile a 30 % Insulinům aspartum protaminatum cristallinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek NovoMix 70 a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 70 používat
3. Jak se přípravek NovoMix 70 používá
4. Možné nežádoucí účinky
5. Jak přípravek NovoMix 70 uchovávat
6. Obsah balení a další informace
1. Co je přípravek NovoMix 70 a k čemu se používá
NovoMix 70 je moderní inzulin (analog inzulinu) s krátkodobě i střednědobě působícím účinkem v poměru 70/30. Moderní inzulinové přípravky jsou zdokonalené verze lidského inzulinu.
NovoMix 70 je používán ke snižování vysoké hladiny cukru v krvi u pacientů s diabetes mellitus (cukrovkou). Diabetes je onemocnění, při němž tělo neprodukuje dostatek inzulinu ke kontrole hladiny cukru v krvi. NovoMix 70 může být používán v kombinaci s metforminem.
NovoMix 70 začne snižovat hladinu krevního cukru za 10 - 20 minut po podání, maximálního účinku dosahuje za 1 až 4 hodiny po podání a jeho účinek přetrvává až po dobu 14 - 24 hodin.
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 70 používat
Nepoužívejte NovoMix 70
► Jestliže jste alergický(á) na inzulin aspart nebo na kteroukoli další složku tohoto přípravku (viz bod 6, Obsah balení a další informace).
► Jestliže máte podezření, že nastupuje hypoglykemie (nízká hladina krevního cukru) (viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4).
► V inzulinových infuzních pumpách
► Pokud zásobní vložka nebo aplikátor obsahující zásobní vložku upadly, jsou poškozené nebo promáčklé.
► Jestliže inzulin nebyl správně skladován nebo byl zmražen, viz bod 5, Jak přípravek NovoMix 70 uchovávat.
► Jestliže po promíchání inzulin není vodný, stejnoměrně bílý a zakalený
► Jestliže po promíchání obsahuje shluky nebo pevné bílé částice usazené na dně nebo stěně zásobní vložky.
Pokud platí něco z výše uvedeného, NovoMix 70 neužívejte. Požádejte o radu lékaře, zdravotní sestru
nebo lékárníka.
► Podle informací na štítku se ujistěte, že se jedná o správný typ inzulínu.
► Vždy zkontrolujte zásobní vložku včetně gumového pístu na spodní straně zásobní vložky. Nepoužívejte ji, pokud je viditelné jakékoliv poškození nebo pokud byl gumový píst vytažen nad bílý kódovací proužek na spodní straně zásobní vložky. Může to být důsledek úniku inzulinu. Máte-li podezření, že je zásobní vložka poškozena, vraťte ji svému dodavateli. Další pokyny najdete ve své příručce k používání injekčního pera.
► Pro každou aplikaci použijte vždy novou jehlu, aby se zabránilo kontaminaci.
► Jehly a NovoMix 70 Penfill nesmíte nikomu půjčovat.
Upozornění a opatření
Některé stavy a činnosti mohou ovlivnit vaši potřebu inzulinu. Poraďte se s lékařem:
► jestliže máte obtíže s ledvinami nebo játry či nadledvinami, podvěskem mozkovým nebo štítnou žlázou
► jestliže vykonáváte větší fyzickou aktivitu než obvykle nebo pokud chcete učinit změnu ve své běžné dietě, neboť to může ovlivnit hladinu cukru v krvi
► pokud jste nemocný(á), pokračujte v inzulinové léčbě a poraďte se s lékařem
► pokud cestujete do ciziny, cestování přes různá časová pásma může ovlivnit Vaši potřebu inzulinu a časování injekcí.
Další léčivé přípravky a přípravek NovoMix 70
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Některé léčivé přípravky ovlivňují hladinu krevního cukru, což může znamenat, že vaše dávka inzulinu musí být změněna. Seznam nejběžnějších léčivých přípravků, které mohou ovlivnit vaši léčbu inzulinem, je uveden níže.
Vaše hladina krevního cukru může být snížena (hypoglykemie), pokud užíváte:
• jiné přípravky na léčbu cukrovky
• inhibitory monoaminooxidázy (IMAO) (používané k léčbě deprese)
• beta-blokátory (používané k léčbě vysokého krevního tlaku)
• inhibitory angiotensin konvertujícího enzymu (ACE) (používané k léčbě některých srdečních onemocnění nebo vysokého krevního tlaku)
• salicyláty (používané k úlevě od bolesti nebo ke snížení horečky)
• anabolické steroidy (jako například testosteron)
• sulfonamidy (používané k léčbě infekcí).
Vaše hladina krevního cukru může být zvýšena (hyperglykemie), pokud užíváte:
• perorální antikoncepci (používaná ke kontrole početí)
• thiazidy (používané k léčbě vysokého krevního tlaku nebo nadměrného zadržování tekutin)
• glukokortikoidy (jako například „kortison“ používaný k léčbě zánětů)
• hormony štítné žlázy (používané k léčbě poruch štítné žlázy)
• sympatomimetika (jako například epinefrin [adrenalin], salbutamol nebo terbutalin používané k léčbě astmatu)
• růstový hormon (lék ke stimulaci skeletálního a somatického růstu a mající vliv na metabolické procesy v těle)
• danazol (lék ovlivňující ovulaci).
Oktreotid a lanreotid (používané k léčbě akromegalie - vzácné hormonální poruchy, která se obvykle objevuje u dospělých středního věku a je způsobena nadměrnou produkcí růstového hormonu podvěskem mozkovým) mohou hladinu cukru v krvi buď zvyšovat nebo snižovat.
Beta-blokátory (používané k léčbě vysokého krevního tlaku) mohou oslabit nebo zcela potlačit první varovné příznaky umožňující rozpoznat nízkou hladinu cukru v krvi.
Pioglitazon (tablety používané k léčbě diabetu 2. typu)
U některých pacientů s dlouhodobým onemocněním diabetem 2. typu a srdečním onemocněním či prodělanou cévní mozkovou příhodou, kteří byli léčeni pioglitazonem a inzulinem, došlo k rozvoji srdečního selhání. Informujte ošetřujícího lékaře, jakmile to bude možné, pokud pocítíte příznaky srdečního selhání jako jsou neobvyklá dušnost nebo rychlý nárůst hmotnosti či lokalizovaný otok (edém).
Pokud užíváte kterýkoli ze zde zmíněných léků, sdělte to lékaři, zdravotní sestře nebo lékárníkovi. Přípravek NovoMix 70 s alkoholem
► Pokud pijete alkohol, může se vaše potřeba inzulinu změnit, protože hladina cukru v krvi se může jak zvýšit, tak snížit. Je doporučena pečlivá kontrola.
Těhotenství a kojení
► Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat. Klinické zkušenosti s inzulinem aspart v těhotenství jsou omezené. Vaše dávka inzulinu může během těhotenství a po porodu vyžadovat změnu. Pečlivá kompenzace cukrovky a zvlášť prevence hypoglykemie je důležitá pro zdraví vašeho dítěte.
► Během kojení není léčba přípravkem NovoMix 70 omezena.
Pokud jste těhotná či kojíte, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
► Zeptejte se, prosím, svého lékaře, zda můžete řídit auto nebo obsluhovat stroje, pokud:
• máte časté hypoglykemie
• je pro vás obtížné hypoglykemii rozeznat.
Pokud máte hladinu krevního cukru příliš nízkou nebo vysokou, může to ovlivnit vaše soustředění a schopnost reagovat a tím také vaši schopnost řídit nebo obsluhovat stroje. Mějte na paměti, že byste mohl(a) ohrozit sebe nebo ostatní.
Důležitá informace o některých pomocných látkách přípravku NovoMix 70
NovoMix 70 obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. v podstatě je „bez sodíku“.
3. Jak se přípravek NovoMix 70 používá Dávkování inzulinu a kdy inzulin užívat
Vždy užívejte inzulin a upravujte svoji dávku přesně tak, jak vám ošetřující lékař řekl. Pokud si nejste jistý(á), poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
NovoMix 70 má být obecně podáván bezprostředně před jídlem. Do 10 minut po podání injekce snězte jídlo nebo svačinu, abyste předešel(předešla) nízké hladině cukru v krvi. Pokud je to nutné, může být NovoMix 70 podán i brzy po jídle. Další informace viz níže Jak a kam aplikovat injekci.
Používáte-li NovoMix 70 v kombinaci s metforminem, mělo by být upraveno dávkování.
Svůj inzulin neměňte, pokud vám to lékař neřekne. Pokud vám lékař změnil typ nebo druh inzulínu, je možné, že vám bude muset upravit také jeho dávkování.
Použití u dětí a dospívajících
Nebyly prováděny klinické studie s používáním přípravku NovoMix 70 dětmi a dospívajícími ve věku do 18 let.
Použití u zvláštních skupin pacientů
Máte-li sníženou funkci ledvin nebo jater či, pokud je vám více než 65 let, bude u vás nutno sledovat hladinu cukru v krvi intenzivněj i a konzultovat změny v dávkování inzulinu s lékařem.
Jak a kam si aplikovat injekci
NovoMix 70 je určen pro aplikaci pod kůži (subkutánně). Nikdy neaplikujte inzulin přímo do žíly (intravenózně) nebo svalu (intramuskulárně).
Při každé injekci střídejte místa vpichu v rámci té oblasti, kterou právě k aplikaci používáte. To může snižovat riziko tvorby bouliček nebo důlků v kůži (viz bod 4, Možné nežádoucí účinky). Nejlepšími místy pro aplikaci injekce jsou: přední strana břicha, hýždě, přední strana stehen nebo horní části paží. Inzulin bude mít rychlejší účinek, pokud jej aplikujete do oblasti kolem pasu. Vždy byste si měl(a) pravidelně měřit obsah cukru v krvi.
► Nenaplňujte znovu zásobní vložku.
► Zásobní vložky NovoMix 70 Penfill jsou navrženy k použití s aplikátory Novo Nordisk a jehlami NovoFine nebo NovoTwist.
► Jestliže jste léčen(a) přípravkem NovoMix 70 Penfill a zároveň jiným inzulinem v zásobních vložkách Penfill, měl(a) byste používat dva aplikátory, pro každý typ inzulinu jeden.
► Vždy noste náhradní zásobní vložku Penfill pro případ, že byste tu, kterou právě používáte, ztratil(a) nebo by došlo k jejímu poškození.
Promíchání přípravku NovoMix 70
Vždy se ujistěte, že v zásobní vložce zbývá dostatek inzulinu (alespoň 12 jednotek), aby ho vůbec bylo možno promíchat. Pokud v zásobní vložce nezbylo dost inzulinu, použijte novou. Další instrukce najdete v příručce k injekčnímu peru.
► Pokaždé, když začínáte používat nový NovoMix 70 Penfill (před vložením zásobní vložky do aplikátoru)
• Než inzulin použijete, nechte ho ohřát na pokojovou teplotu. To umožní snadnější promíchání.
• Převalujte zásobní vložku mezi dlaněmi 10krát - je důležité držet zásobní vložku v horizontální (vodorovné) poloze (viz obrázek A).
• Pohybujte zásobní vložkou nahoru a dolů mezi pozicemi a a b (viz obrázek B) 10krát tak, aby se skleněná kulička pohybovala z jednoho konce zásobní vložky na druhý.
• Opakujte převalování a promíchávání (viz obrázky A a B) tak dlouho, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Zásobní vložku nepoužívejte, pokud inzulin není po promíchání vodný, stejnoměrně bílý a zakalený.
• Dokončete ostatní kroky injekční aplikace bez dalšího zdržení
► Před každou další injekcí
• Pohybujte aplikátorem s vloženou zásobní vložkou nahoru a dolů mezi polohami a a b (viz obrázek B) nejméně 10krát, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Zásobní vložku nepoužívejte, pokud inzulin není po promíchání vodný, stejnoměrně bílý a zakalený.
• Pokud tento postup samotný nestačí k tomu, aby vznikla vodná, stejnoměrně bílá a zakalená tekutina, opakujte převalování a promíchávání popsané výše tak dlouho, dokud tekutina nemá vodný, stejnoměrně bílý a zakalený vzhled.
• Dokončete ostatní kroky injekční aplikace bez dalšího zdržení.

Obrázek B

Jak si aplikovat injekci přípravku NovoMix 70
► Aplikujte inzulin pod kůži. Používejte injekční techniku, kterou vám doporučil váš lékař nebo zdravotní sestra a popsanou v příručce k vašemu injekčnímu peru.
► Nechte jehlu pod kůží po dobu alespoň 6 vteřin. Dávkovací tlačítko držte zcela stlačené, dokud jehlu nevytáhnete z kůže. To zaručí podání správné dávky a omezí možné proniknutí krve do jehly nebo inzulinové zásobní vložky.
► Po každé aplikaci se ujistěte, že jste odstranil(a) a vyhodil(a) jehlu a že skladujete NovoMix 70 bez nasazené jehly. Jinak by mohla unikat tekutina, což může způsobit nepřesné dávkování.
Jestliže jste užil(a) více inzulínu, než jste měl(a)
Pokud jste užil(a) příliš inzulinu, vaše hladina cukru v krvi se může příliš snížit (hypoglykemie). Viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4.
Jestliže jste zapomněl(a) užít inzulin
Jestliže jste zapomněl(a) užít inzulin, vaše hladina krevního cukru může stoupnout příliš vysoko (hyperglykemie). Viz část c) Důsledky diabetu v bodě 4.
Jestliže jste přestal(a) užívat inzulin
Inzulin nepřestávejte užívat bez porady s lékařem, který vám poradí, co je třeba dělat. Mohlo by to vést k velmi vysoké hladině krevního cukru (těžké hyperglykemii) a ketoacidóze. Viz část c) Důsledky diabetu v bodě 4.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
a) Souhrn závažných a velmi častých nežádoucích účinků
Nízká hladina cukru v krvi (hypoglykemie) je velmi častý nežádoucí účinek. Může se projevit u více než 1 pacienta z 10.
Nízká hladina cukru může nastat, pokud:
• si aplikujete příliš mnoho inzulinu
• jíte příliš málo nebo vynecháte-li jídlo
• cvičíte více než obvykle
• pijete alkohol (viz bod 2, Pití alkoholu a užívání přípravku NovoMix 70).
Příznaky nízké hladiny cukru v krvi: studený pot, chladná bledá pokožka, bolest hlavy, rychlý srdeční tep, pocit nevolnosti, pocit velkého hladu, dočasné změny vidění, ospalost, neobvyklá vyčerpanost a slabost, nervozita nebo třes, pocit úzkosti, pocit zmatenosti, potíže s koncentrací.
Velmi nízká hladina cukru v krvi může vést k bezvědomí. Pokud déle trvající nízká hladina cukru v krvi není léčena, může způsobit poškození mozku (dočasné nebo trvalé) a dokonce úmrtí. Z bezvědomí se můžete zotavit rychleji, pokud vám někdo, kdo ví, jak jej použít, aplikuje hormon glukagon. Pokud dostanete glukagon, budete potřebovat glukózu nebo sladkou přesnídávku ihned poté, co nabudete vědomí. Pokud nereagujete na léčbu glukagonem, budete muset být léčen(a) v nemocnici.
Co dělat, pokud pocítíte příznaky nízké hladiny cukru v krvi:
► Pokud pocítíte příznaky nízké hladiny cukru v krvi, vezměte si glukózové tablety nebo jinou přesnídávku s vysokým obsahem cukru (např. sladkosti, sušenky, ovocnou šťávu). Pokud je to možné, změřte si hladinu cukru v krvi a odpočívejte. Vždy s sebou pro případ potřeby noste glukózové tablety nebo sladkosti s vysokým obsahem cukru.
► Poté, co příznaky nízké hladiny cukru v krvi ustoupí nebo se u vás stabilizuje hladina cukru v krvi, pokračujte s inzulinovou léčbou jako obvykle.
► Míváte-li tak nízkou hladinu cukru v krvi, že omdlíváte, pokud jste potřeboval(a) aplikovat glukagon nebo pokud míváte nízkou hladinu cukru v krvi často, pohovořte si se svým lékařem. Možná bude potřeba upravit množství nebo časové intervaly podání inzulinu, jídla nebo cvičení.
Řekněte lidem ve svém okolí, že máte diabetes, a seznamte je s jeho důsledky včetně rizika, že omdlíte (upadnete do bezvědomí) z důvodu nízké hladiny cukru v krvi. Řekněte jim, že pokud omdlíte, musí vás položit na bok a okamžitě zajistit lékařskou pomoc. Nesmějí vám dávat najíst ani napít, protože byste se mohl(a) zadusit.
Závažné alergické reakce na NovoMix 70 nebo na některou z jeho pomocných látek (tzv. systémová alergická reakce) je velmi vzácný nežádoucí účinek. Může být však potenciálně život ohrožující. Může se projevit u méně než 1 pacienta z 10 000.
Vyhledejte ihned lékařskou pomoc:
• Pokud se příznaky alergie rozšíří na další části těla.
• Pokud se náhle necítíte dobře a začnete se potit, pociťujete nevolnost (zvracení), máte dýchací potíže, zrychlený tep a točí se vám hlava.
► Pokud zaznamenáte některé z těchto příznaků, okamžitě vyhledejte lékařskou pomoc.
b) Souhrn ostatních nežádoucích účinků
Méně časté nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta ze 100.
Příznaky alergie: v místě vpichu se mohou objevit různé příznaky místní alergické reakce (bolest,
zarudnutí, kopřivka, zánět, podlitiny, otok a svědění). Obvykle vymizí po několika týdnech inzulinové léčby. Pokud nevymizí, navštivte svého lékaře.
Poruchy vidění: na počátku léčby inzulinem může dojít k poruchám vidění, tyto poruchy jsou však obvykle přechodného rázu.
Změny v místě vpichu (lipodystrofie): tuková tkáň pod kůží se může v místě vpichu ztenčit (lipoatrofie) nebo zesílit (lipohypertrofie). Obměňování míst vpichu při každé injekci snižuje riziko takových změn kůže. Pokud zjistíte, že vaše kůže má v místě vpichu dolíčky nebo zesílení, informujte svého lékaře nebo zdravotní sestru. Tyto reakce se totiž mohou zhoršit nebo mohou změnit absorbci inzulinu, pokud si do tohoto místa inzulin aplikujete.
Otoky kloubů: na začátku inzulinové léčby může dojít k zadržování vody v oblasti kotníků a dalších kloubů. Obvykle tato reakce brzy odezní. Pokud ne, kontaktujte lékaře.
Diabetická retinopatie (oční onemocnění spojené s cukrovkou, které může vést ke ztrátě zraku): jestliže trpíte diabetickou retinopatií a hladina vašeho krevního cukru se velmi rychle zlepší, může dojít ke zhoršení retinopatie. Poraďte se o tom se svým lékařem.
Vzácné nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta z 1 000.
Bolestivá neuropatie (bolest způsobená poškozením nervů): jestliže se hladina vašeho krevního cukru velmi rychle zlepší, může se dostavit bolest nervového původu. Tento stav se nazývá akutní bolestivá neuropatie a obvykle se jedná o přechodný stav.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
c) Důsledky diabetu
Vysoká hladina cukru v krvi (hyperglykemie)
Vysoká hladina cukru může nastat, pokud:
• j ste si neaplikoval(a) dostatečné množství inzulinu
• zapomněl(a) jste si aplikovat inzulin nebo jste ho přestal(a) užívat
• opakovaně užíváte menší dávky inzulinu, než je třeba
• máte infekci a/nebo horečku
• jíte více než obvykle
• cvičíte méně než obvykle.
Varovné příznaky vysoké hladiny cukru v krvi:
Varovné příznaky se objevují postupně. Zahrnují: častější močení, pocit žízně, ztrátu chuti k jídlu, pocit nevolnosti (pocit na zvracení nebo zvracení), pocit ospalosti nebo únavy, zarudlou, suchou pokožku, sucho v ústech a ovocný (acetonový) zápach dechu.
Co dělat, pokud pocítíte příznaky vysoké hladiny cukru v krvi:
► Pokud zaznamenáte některé z výše uvedených příznaků: zkontrolujte si hladinu krevního cukru, otestuje si moč na ketony, máte-li možnost, a potom ihned vyhledejte lékařskou pomoc.
► Mohou to být příznaky velmi závažného stavu nazývaného diabetická ketoacidóza (hromadění kyseliny v krvi, protože tělo odbourává místo cukru tuk). Pokud jej neléčíte, může vést až k diabetickému kómatu a případně ke smrti.
5. Jak přípravek NovoMix 70 uchovávat
Uchovávejte tento přípravek mimo dohled a dosah a dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku zásobní vložky a krabičce za „Použitelné do”. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Pokud zásobní vložku právě nepoužíváte, uchovávejte ji vždy v krabičce, aby byl přípravek chráněn před světlem. NovoMix 70 musí být chráněn před vysokými teplotami a světlem.
Před otevřením: NovoMix 70 Penfill, který není používán, musí být uchováván v chladničce (2 °C až 8 °C), mimo chladicí zařízení. Chraňte před mrazem.
Před použitím vyjměte NovoMix 70 Penfill z chladničky. Pokaždé, když začínáte používat nový NovoMix 70 Penfill, je doporučeno promíchat inzulin dle instrukcí pro promíchání v bodě 3, část Promíchání přípravku NovoMix 70.
Během používání či pohotovostně nošený: NovoMix 70 Penfill, který používáte nebo nosíte jako náhradní, by neměl být uchováván v chladničce. Můžete jej nosit s sebou a uchovávat při pokojové teplotě (do 30 °C) až po dobu 4 týdnů.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co NovoMix 70 obsahuje
• Léčivou látkou je inzulin aspart. NovoMix 70 je směs složená ze 70 % rozpustného inzulinu aspart a 30 % krystalického protaminového inzulinu aspart. 1 ml obsahuje 100 jednotek inzulinu aspart. Jedna zásobní vložka obsahuje 300 jednotek inzulinu aspart ve 3 ml injekční suspenze.
• Pomocnými látkami j sou glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselina chlorovodíková, hydroxid sodný a voda na injekci.
Jak NovoMix 70 vypadá a co obsahuje toto balení
NovoMix 70 je dodáván jako injekční suspenze. V zásobní vložce je umístěna skleněná kulička, která
usnadňuje promíchávání. Po promíchání by kapalina měla být vodná, stejnoměrně bílá a zakalená.
Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, nepoužívejte ho.
Velikosti balení jsou 1, 5 a 10 zásobních vložek po 3 ml. Na trhu nemusí být všechny velikosti balení.
Zakalená, bílá vodná suspenze.
Držitel rozhodnutí o registraci a výrobce
Novo Nordisk A/S Novo Allé
DK-2880 Bagsv^rd, Dánsko
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky: http://www.ema.europa.eu/
NovoMix 30 FlexPen 100 jednotek/ml injekční suspenze v předplněném peru
30 % Insulinům aspartum solubile a 70 % Insulinům aspartum protaminatum cristallinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek NovoMix 30 a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 30 používat
3. Jak se přípravek NovoMix 30 používá
4. Možné nežádoucí účinky
5. Jak přípravek NovoMix 30 uchovávat
6. Obsah balení a další informace
1. Co je přípravek NovoMix 30 a k čemu se používá
NovoMix 30 je moderní inzulin (analog inzulinu) s krátkodobě i střednědobě působícím účinkem v poměru 30/70. Moderní inzulinové přípravky jsou zdokonalené verze lidského inzulinu.
NovoMix 30 je používán ke snižování vysoké hladiny cukru v krvi u dospělých, dospívajících a dětí ve věku 10 let a více s diabetes mellitus (cukrovkou). Diabetes je onemocnění, při němž tělo neprodukuje dostatek inzulinu ke kontrole hladiny cukru v krvi. NovoMix 30 může být používán v kombinaci s tabletami na léčbu diabetu.
NovoMix 30 začne snižovat hladinu krevního cukru za 10 - 20 minut po podání, maximálního účinku dosahuje za 1 až 4 hodiny po podání a jeho účinek přetrvává až 24 hodin.
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 30 používat
Nepoužívejte NovoMix 30
► Jestliže jste alergický(á) na inzulin aspart nebo na kteroukoli další složku tohoto přípravku (viz bod 6, Obsah balení a další informace).
► Jestliže máte podezření, že nastupuje hypoglykemie (nízká hladina krevního cukru) (viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4).
► V inzulinových infuzních pumpách
► Pokud FlexPen upadl, je poškozený nebo promáčklý.
► Jestliže inzulin nebyl správně skladován nebo byl zmražen, viz bod 5, Jak přípravek NovoMix 30 uchovávat.
► Jestliže po promíchání inzulin není vodný, stejnoměrně bílý a zakalený.
► Jestliže po promíchání obsahuje shluky nebo pevné bílé částice usazené na dně nebo stěně zásobní vložky.
Pokud platí něco z výše uvedeného, NovoMix 30 neužívejte. Požádejte o radu lékaře, zdravotní sestru nebo lékárníka.
Před užitím přípravku NovoMix 30
► Podle informací na štítku se ujistěte, že se jedná o správný typ inzulínu.
► Pro každou aplikaci použijte vždy novou jehlu, aby se zabránilo kontaminaci.
► Jehly a NovoMix 30 FlexPen nesmíte nikomu půjčovat.
Upozornění a opatření
Některé stavy a činnosti mohou ovlivnit vaši potřebu inzulinu. Poraďte se s lékařem:
► jestliže máte obtíže s ledvinami nebo játry či nadledvinami, podvěskem mozkovým nebo štítnou žlázou
► jestliže vykonáváte větší fyzickou aktivitu než obvykle nebo pokud chcete učinit změnu ve své běžné dietě, neboť to může ovlivnit hladinu cukru v krvi
► pokud jste nemocný(á), pokračujte v inzulinové léčbě a poraďte se s lékařem
► pokud cestujete do ciziny, cestování přes různá časová pásma může ovlivnit Vaši potřebu inzulinu a časování injekcí.
Děti a dospívající
• NovoMix 30 může být používán u dospívajících a dětí ve věku od 10 let.
• Pro děti ve věku od 6 - 9 let existují s přípravkem NovoMix 30 omezené klinické zkušenosti.
• Pro použití přípravku NovoMix 30 u dětí ve věku do 6 let nejsou dostupné žádné údaje.
Další léčivé přípravky a přípravek NovoMix 30
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Některé léčivé přípravky ovlivňují hladinu krevního cukru, což může znamenat, že vaše dávka inzulinu musí být změněna. Seznam nejběžnějších léčivých přípravků, které mohou ovlivnit vaši léčbu inzulinem, je uveden níže.
Vaše hladina krevního cukru může být snížena (hypoglykemie), pokud užíváte:
• jiné přípravky na léčbu cukrovky
• inhibitory monoaminooxidázy (IMAO) (používané k léčbě deprese)
• beta-blokátory (používané k léčbě vysokého krevního tlaku)
• inhibitory angiotensin konvertujícího enzymu (ACE) (používané k léčbě některých srdečních onemocnění nebo vysokého krevního tlaku)
• salicyláty (používané k úlevě od bolesti nebo ke snížení horečky)
• anabolické steroidy (jako například testosteron)
• sulfonamidy (používané k léčbě infekcí).
Vaše hladina krevního cukru může být zvýšena (hyperglykemie), pokud užíváte:
• perorální antikoncepci (používaná ke kontrole početí)
• thiazidy (používané k léčbě vysokého krevního tlaku nebo nadměrného zadržování tekutin)
• glukokortikoidy (jako například „kortison“ používaný k léčbě zánětů)
• hormony štítné žlázy (používané k léčbě poruch štítné žlázy)
• sympatomimetika (jako například epinefrin [adrenalin], salbutamol nebo terbutalin používané k léčbě astmatu)
• růstový hormon (lék ke stimulaci skeletálního a somatického růstu a mající vliv na metabolické procesy v těle)
• danazol (lék ovlivňující ovulaci).
Oktreotid a lanreotid (používané k léčbě akromegalie - vzácné hormonální poruchy, která se obvykle objevuje u dospělých středního věku a je způsobena nadměrnou produkcí růstového hormonu podvěskem mozkovým) mohou hladinu cukru v krvi buď zvyšovat nebo snižovat.
Beta-blokátory (používané k léčbě vysokého krevního tlaku) mohou oslabit nebo zcela potlačit první varovné příznaky umožňující rozpoznat nízkou hladinu cukru v krvi.
Pioglitazon (tablety používané k léčbě diabetu 2. typu)
U některých pacientů s dlouhodobým onemocněním diabetem 2. typu a srdečním onemocněním či prodělanou cévní mozkovou příhodou, kteří byli léčeni pioglitazonem a inzulinem, došlo k rozvoji srdečního selhání. Informujte ošetřujícího lékaře, jakmile to bude možné, pokud pocítíte příznaky srdečního selhání jako jsou neobvyklá dušnost nebo rychlý nárůst hmotnosti či lokalizovaný otok (edém).
Pokud užíváte kterýkoli ze zde zmíněných léků, sdělte to lékaři, zdravotní sestře nebo lékárníkovi. Přípravek NovoMix 30 s alkoholem
► Pokud pijete alkohol, může se vaše potřeba inzulinu změnit, protože hladina cukru v krvi se může jak zvýšit, tak snížit. Je doporučena pečlivá kontrola.
Těhotenství a kojení
► Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat. Klinické zkušenosti s inzulinem aspart v těhotenství jsou omezené. Vaše dávka inzulinu může během těhotenství a po porodu vyžadovat změnu. Pečlivá kompenzace cukrovky a zvlášť prevence hypoglykemie je důležitá pro zdraví vašeho dítěte.
► Během kojení není léčba přípravkem NovoMix 30 omezena.
Pokud jste těhotná či kojíte, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
► Zeptejte se, prosím, svého lékaře, zda můžete řídit auto nebo obsluhovat stroje, pokud:
• máte časté hypoglykemie
• je pro vás obtížné hypoglykemii rozeznat.
Pokud máte hladinu krevního cukru příliš nízkou nebo vysokou, může to ovlivnit vaše soustředění a schopnost reagovat a tím také vaši schopnost řídit nebo obsluhovat stroje. Mějte na paměti, že byste mohl(a) ohrozit sebe nebo ostatní.
Důležitá informace o některých pomocných látkách přípravku NovoMix 30
NovoMix 30 obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. v podstatě je „bez sodíku“.
3. Jak se přípravek NovoMix 30 používá Dávkování inzulinu a kdy inzulin užívat
Vždy užívejte inzulin a upravujte svoji dávku přesně tak, jak vám ošetřující lékař řekl. Pokud si nejste jistý(á), poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
NovoMix 30 má být obecně podáván bezprostředně před jídlem. Do 10 minut po podání injekce snězte jídlo nebo svačinu, abyste předešel(předešla) nízké hladině cukru v krvi. Pokud je to nutné, může být NovoMix 30 podán i brzy po jídle. Další informace viz níže Jak a kam aplikovat injekci.
Používáte-li NovoMix 30 v kombinaci s tabletami na léčbu diabetů, mělo by být upraveno dávkování.
Svůj inzulin neměňte, pokud vám to lékař neřekne. Pokud vám lékař změnil typ nebo druh inzulínu, je možné, že vám bude muset upravit také jeho dávkování.
Použití u dětí a dospívajících
NovoMix 30 může být používán u dospívajících a dětí ve věku od 10 let, pokud je preferován premixovaný inzulin. Pro děti ve věku 6 - 9 let existují omezená klinická data. Pro použití přípravku NovoMix 30 u dětí ve věku do 6 let nejsou dostupné žádné údaje.
Použití u zvláštních skupin pacientů
Máte-li sníženou funkci ledvin nebo jater či, pokud je vám více než 65 let, bude u vás nutno sledovat hladinu cukru v krvi intenzivněji a konzultovat změny v dávkování inzulinu s lékařem.
Jak a kam si aplikovat injekci
NovoMix 30 je určen pro aplikaci pod kůži (subkutánně). Nikdy neaplikujte inzulin přímo do žíly (intravenózně) nebo svalu (intramuskulárně).
Při každé injekci střídejte místa vpichu v rámci té oblasti, kterou právě k aplikaci používáte. To může snižovat riziko tvorby bouliček nebo důlků v kůži (viz bod 4, Možné nežádoucí účinky). Nejlepšími místy pro aplikaci injekce jsou: přední strana břicha, hýždě, přední strana stehen nebo horní části paží. Inzulin bude mít rychlejší účinek, pokud jej aplikujete do oblasti kolem pasu. Vždy byste si měl(a) pravidelně měřit obsah cukru v krvi.
Jak zacházet s přípravkem NovoMix 30 FlexPen
NovoMix 30 FlexPen je předplněné barevně označené pero na jedno použití obsahující směs rychle a střednědobě působícího inzulinu aspart v poměru 30/70.
Přečtěte si pečlivě instrukce pro použití, které jsou součástí této příbalové informace. Pero musíte používat tak, jak je uvedeno v Instrukcích pro použití.
Před každou aplikací inzulinu se vždy ujistěte, že používáte správné pero.
Jestliže jste užil(a) více inzulinu, než jste měl(a)
Pokud jste užil(a) příliš inzulinu, vaše hladina cukru v krvi se může příliš snížit (hypoglykemie). Viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4.
Jestliže jste zapomněl(a) užít inzulin
Jestliže jste zapomněl(a) užít inzulin, vaše hladina krevního cukru může stoupnout příliš vysoko (hyperglykemie). Viz část c) Důsledky diabetu v bodě 4.
Jestliže jste přestal(a) užívat inzulin
Inzulin nepřestávejte užívat bez porady s lékařem, který vám poradí, co je třeba dělat. Mohlo by to vést k velmi vysoké hladině krevního cukru (těžké hyperglykemii) a ketoacidóze. Viz část c) Důsledky diabetu v bodě 4.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, zdravotní zdravotní sestry nebo lékárníka.
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
a) Souhrn závažných a velmi častých nežádoucích účinků
Nízká hladina cukru v krvi (hypoglykemie) je velmi častý nežádoucí účinek. Může se projevit u více než 1 pacienta z 10.
Nízká hladina cukru může nastat, pokud:
• si aplikujete příliš mnoho inzulinu
• jíte příliš málo nebo vynecháte-li jídlo
• cvičíte více než obvykle
• pijete alkohol (viz bod 2, Přípravek NovoMix 30 s alkoholem).
Příznaky nízké hladiny cukru v krvi: studený pot, chladná bledá pokožka, bolest hlavy, rychlý srdeční tep, pocit nevolnosti, pocit velkého hladu, dočasné změny vidění, ospalost, neobvyklá vyčerpanost a slabost, nervozita nebo třes, pocit úzkosti, pocit zmatenosti, potíže s koncentrací.
Velmi nízká hladina cukru v krvi může vést k bezvědomí. Pokud déle trvající nízká hladina cukru v krvi není léčena, může způsobit poškození mozku (dočasné nebo trvalé) a dokonce úmrtí. Z bezvědomí se můžete zotavit rychleji, pokud vám někdo, kdo ví, jak jej použít, aplikuje hormon glukagon. Pokud dostanete glukagon, budete potřebovat glukózu nebo sladkou přesnídávku ihned poté, co nabudete vědomí. Pokud nereagujete na léčbu glukagonem, budete muset být léčen(a) v nemocnici.
Co dělat, pokud pocítíte příznaky nízké hladiny cukru v krvi:
► Pokud pocítíte příznaky nízké hladiny cukru v krvi, vezměte si glukózové tablety nebo jinou přesnídávku s vysokým obsahem cukru (např. sladkosti, sušenky, ovocnou šťávu). Pokud je to možné, změřte si hladinu cukru v krvi a odpočívejte. Vždy s sebou pro případ potřeby noste glukózové tablety nebo sladkosti s vysokým obsahem cukru.
► Poté, co příznaky nízké hladiny cukru v krvi ustoupí nebo se u vás stabilizuje hladina cukru v krvi, pokračujte s inzulinovou léčbou jako obvykle.
► Míváte-li tak nízkou hladinu cukru v krvi, že omdlíváte, pokud jste potřeboval(a) aplikovat glukagon nebo pokud míváte nízkou hladinu cukru v krvi často, pohovořte si se svým lékařem. Možná bude potřeba upravit množství nebo časové intervaly podání inzulinu, jídla nebo cvičení.
Řekněte lidem ve svém okolí, že máte diabetes, a seznamte je s jeho důsledky včetně rizika, že omdlíte (upadnete do bezvědomí) z důvodu nízké hladiny cukru v krvi. Řekněte jim, že pokud omdlíte, musí vás položit na bok a okamžitě zajistit lékařskou pomoc. Nesmějí vám dávat najíst ani napít, protože byste se mohl(a) zadusit.
Závažné alergické reakce na NovoMix 30 nebo na některou z jeho pomocných látek (tzv. systémová alergická reakce) je velmi vzácný nežádoucí účinek. Může být však potenciálně život ohrožující. Může se projevit u méně než 1 pacienta z 10 000.
Vyhledejte ihned lékařskou pomoc:
• Pokud se příznaky alergie rozšíří na další části těla.
• Pokud se náhle necítíte dobře a začnete se potit, pociťujete nevolnost (zvracení), máte dýchací potíže, zrychlený tep a točí se vám hlava.
► Pokud zaznamenáte některé z těchto příznaků, okamžitě vyhledejte lékařskou pomoc.
b) Souhrn ostatních nežádoucích účinků
Příznaky alergie: v místě vpichu se mohou objevit různé příznaky místní alergické reakce (bolest, zarudnutí, kopřivka, zánět, podlitiny, otok a svědění). Obvykle vymizí po několika týdnech inzulinové léčby. Pokud nevymizí, navštivte svého lékaře.
Poruchy vidění: na počátku léčby inzulinem může dojít k poruchám vidění, tyto poruchy jsou však obvykle přechodného rázu.
Změny v místě vpichu (lipodystrofie): tuková tkáň pod kůží se může v místě vpichu ztenčit (lipoatrofie) nebo zesílit (lipohypertrofie). Obměňování míst vpichu při každé injekci snižuje riziko takových změn kůže. Pokud zjistíte, že vaše kůže má v místě vpichu dolíčky nebo zesílení, informujte svého lékaře nebo zdravotní sestru. Tyto reakce se totiž mohou zhoršit nebo mohou změnit absorbci inzulinu, pokud si do tohoto místa inzulin aplikujete.
Otoky kloubů: na začátku inzulinové léčby může dojít k zadržování vody v oblasti kotníků a dalších kloubů. Obvykle tato reakce brzy odezní. Pokud ne, kontaktujte lékaře.
Diabetická retinopatie (oční onemocnění spojené s cukrovkou, které může vést ke ztrátě zraku): jestliže trpíte diabetickou retinopatií a hladina vašeho krevního cukru se velmi rychle zlepší, může dojít ke zhoršení retinopatie. Poraďte se o tom se svým lékařem.
Vzácné nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta z 1 000.
Bolestivá neuropatie (bolest způsobená poškozením nervů): jestliže se hladina vašeho krevního cukru velmi rychle zlepší, může se dostavit bolest nervového původu. Tento stav se nazývá akutní bolestivá neuropatie a obvykle se jedná o přechodný stav.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
c) Důsledky diabetu
Vysoká hladina cukru v krvi (hyperglykemie)
Vysoká hladina cukru může nastat, pokud:
• j ste si neaplikoval(a) dostatečné množství inzulinu
• zapomněl(a) jste si aplikovat inzulin nebo jste ho přestal(a) užívat
• opakovaně užíváte menší dávky inzulinu, než je třeba
• máte infekci a/nebo horečku
• jíte více než obvykle
• cvičíte méně než obvykle.
Varovné příznaky vysoké hladiny cukru v krvi:
Varovné příznaky se objevují postupně. Zahrnují: častější močení, pocit žízně, ztrátu chuti k jídlu, pocit nevolnosti (pocit na zvracení nebo zvracení), pocit ospalosti nebo únavy, zarudlou, suchou pokožku, sucho v ústech a ovocný (acetonový) zápach dechu.
Co dělat, pokud pocítíte příznaky vysoké hladiny cukru v krvi:
► Pokud zaznamenáte některé z výše uvedených příznaků: zkontrolujte si hladinu krevního cukru, otestuje si moč na ketony, máte-li možnost, a potom ihned vyhledejte lékařskou pomoc.
► Mohou to být příznaky velmi závažného stavu nazývaného diabetická ketoacidóza (hromadění kyseliny v krvi, protože tělo odbourává místo cukru tuk). Pokud jej neléčíte, může vést až k diabetickému kómatu a případně ke smrti.
5. Jak přípravek NovoMix 30 uchovávat
Uchovávejte tento přípravek mimo dohled a dosah a dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku pera FlexPen a krabičce za „Použitelné do”. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Mějte pero FlexPen vždy, když je nepoužíváte, opatřené krytem pera, aby byl přípravek chráněn před světlem. NovoMix 30 musí být chráněn před vysokými teplotami a světlem.
Před otevřením: NovoMix 30 FlexPen, který není používán, musí být uchováván v chladničce (2 °C až 8 °C), mimo chladicí zařízení. Chraňte před mrazem.
Před použitím vyjměte NovoMix 30 FlexPen z chladničky. Pokaždé, když začínáte používat nové pero, je doporučeno promíchat inzulin dle instrukcí. Viz Instrukce pro použití.
Během používání či pohotovostně nošený: NovoMix 30 FlexPen, který používáte nebo nosíte jako náhradní, by neměl být uchováván v chladničce. Můžete jej nosit s sebou a uchovávat při pokojové teplotě (do 30 °C) až po dobu 4 týdnů.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co NovoMix 30 obsahuje
• Léčivou látkou je inzulin aspart. NovoMix 30 je směs složená z 30 % rozpustného inzulinu aspart a 70 % krystalického protaminového inzulinu aspart. 1 ml obsahuje 100 jednotek inzulinu aspart. Jedno předplněné pero obsahuje 300 jednotek inzulinu aspart ve 3 ml injekční suspenze.
• Pomocnými látkami j sou glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselina chlorovodíková, hydroxid sodný a voda na injekci.
Jak NovoMix 30 vypadá a co obsahuje toto balení
NovoMix 30 je dodáván jako injekční suspenze v předplněném peru. V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání. Po promíchání by kapalina měla být vodná, stejnoměrně bílá a zakalená. Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, nepoužívejte ho.
Velikosti balení jsou 1 (včetně jehel nebo bez jehel), 5 (bez jehel) a 10 (bez jehel) předplněných per po 3 ml. Na trhu nemusí být všechny velikosti balení.
Zakalená, bílá vodná suspenze.
Držitel rozhodnutí o registraci a výrobce
Držitel rozhodnutí o registraci
Novo Nordisk A/S Novo Allé
DK-2880 Bagsv^rd, Dánsko Výrobce
Výrobce může být identifikován pomocí čísla šarže vytištěného na záložce krabičky a na štítku:
• Jsou-li druhý a třetí znak S6, P5, K7, R7, VG, FG nebo ZF, pak je výrobcem Novo Nordisk A/S, Novo Allé, DK-2880 Bagsv^rd, Dánsko
• Jsou-li druhý a třetí znak H7 nebo T6, pak je výrobcem Novo Nordisk Production SAS, 45 Avenue ďOrléans F-28000 Chartres, Francie
Nyní si na druhé straně přečtěte informace o použití pera FlexPen.
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky: http://www.ema.europa.eu/
Instrukce pro použití NovoMix 30 injekční suspenze v peru FlexPen.
Před použitím pera FlexPen si pečlivě přečtěte dále uvedené pokyny. Pokud nebudete tyto pokyny pečlivě dodržovat, můžete si aplikovat inzulínu příliš málo nebo příliš mnoho, což může vést k příliš vysoké či příliš nízké hladině cukru v krvi.
FlexPen je předplněné inzulinové pero s možností nastavení dávky.
► Dávky lze nastavit od 1 do 60 jednotek v přírůstcích po 1 jednotce.
► FlexPen je určen pro použití s jednorázovými jehlami NovoFine nebo NovoTwist o délce do 8 mm.
► Vždy při sobě noste náhradní inzulinový aplikátor pro případ, že pero FlexPen ztratíte nebo bude poškozeno.
NovoMix 30 FlexPen Skleněná Zásobní kulička vložka
Uzávěr pera


Stupnice ukazatele zbývajícího množství inzulinu
Volič Dávkovači Jehla (příklad)
dávky tlačítko
Ukazatel dávky | Velký vnější Vnitřní Jehla
kryt j ehly kryt j ehly
Papírový
kryt
Péče o pero
► Pero FlexPen vyžaduje opatrné zacházení. Jestliže spadlo, bylo poškozeno nebo bylo vystaveno nárazu, vzniká riziko úniku inzulinu. To může způsobit nepřesné dávkování, což může vést
k příliš vysoké nebo příliš nízké hladině cukru v krvi.
► Vnější povrch pera FlexPen můžete očistit otřením desinfekčním tamponem. Nenamáčejte jej, neomývejte jej ani jej nemažte, protože byste ho tím mohl(a) poškodit.
► FlexPen znovu nenaplňujte.
Promíchání inzulinu
A
Zkontrolujte název a barvu na štítku pera, abyste se ujistil(a), že obsahuje správný typ inzulinu. To je obzvlášť důležité, pokud užíváte více než jeden typ inzulinu. Pokud si aplikujete špatný typ inzulinu, může Vám hladina cukru v krvi příliš stoupnout nebo příliš klesnout.
Pokaždé, když používáte nové pero.
Než inzulin použijete, nechte ho ohřát na pokojovou teplotu. To usnadní jeho promíchání.
Sejměte uzávěr pera.

B
Před první injekcí novým perem FlexPen musíte inzulin promíchat:
Převalujte pero mezi dlaněmi 10krát - je důležité držet pero v horizontální (vodorovné) poloze.

C
Potom 10krát pohybujte perem nahoru a dolů mezi dvěma polohami (viz obrázek) tak, aby se skleněná kulička pohybovala z jednoho konce zásobní vložky na druhý.
Převalování a protřepávání opakujte, dokud není tekutina vodná, stejnoměrně bílá a zakalená.
Před každou další injekcí
Pohybujte perem nahoru a dolů mezi dvěma polohami alespoň 10krát, dokud není tekutina vodná, stejnoměrně bílá a zakalená.
► Před každou injekcí se ujistěte, že jste inzulin promíchal(a). Promíchání sníží riziko příliš vysoké nebo příliš nízké hladiny cukru v krvi. Po promíchání inzulinu dokončete neprodleně všechny další kroky k aplikaci injekce.

A Vždy zkontrolujte, zda v zásobní vložce zbývá ještě alespoň 12 jednotek inzulinu, abyste ho mohl(a) rovnoměrně promíchat. Je-li v ní méně než 12 jednotek, použijte nový FlexPen.
12 jednotek je vyznačeno na stupnici ukazatele zbývajícího množství inzulinu (viz velký obrázek na začátku této instrukce).
A Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, pero nepoužívejte. Nasazení jehly D
Vezměte si novou jehlu a odtrhněte papírový kryt.
Našroubujte jehlu rovně a pevně na FlexPen.

E
Sejměte z jehly velký vnější kryt a uchovejte ho pro pozdější potřebu.

Sejměte z jehly vnitřní kryt a vyhoďte ho.
Nikdy se nepokoušejte vnitřní kryt jehly opět nasadit na jehlu. Mohl(a) byste se o jehlu píchnout.

A Pro každou aplikaci použijte vždy novou jehlu. Tím se sníží riziko kontaminace, infekce, úniku inzulinu, ucpání jehel a nepřesného dávkování.
A Dbejte, abyste jehlu před použitím neohnul(a) nebo jinak nepoškodil(a).
Ověření funkčnosti
Před každou injekcí se během normálního používání může v zásobní vložce nahromadit malé množství vzduchu. Abyste zabránil(a) vpíchnutí vzduchu a zajistil(a) správné dávkování, postupujte dle dále uvedených pokynů:
G
Otočte voličem dávky tak, abyste nastavil(a) 2 jednotky.

H
Držte FlexPen jehlou směrem nahoru a jemně na zásobní vložku několikrát poklepte prstem, aby se v horní části zásobní vložky nahromadily případné vzduchové bubliny.

Držte jehlu stále směrem vzhůru a stlačte úplně dávkovací tlačítko. Volič dávky se vrátí na nulu.
Na hrotu jehly se musí objevit kapka inzulinu. Jestliže se neobjeví, vyměňte jehlu a celý postup zopakujte, nejvíce však 6krát.
Jestliže se kapka inzulinu ani potom neobjeví, je pero vadné a musíte použít jiné.

A Vždy před podáním injekce zkontrolujte, zda se na špičce jehly objeví kapka. Tím se ujistíte, že inzulin protéká perem. Pokud se neobjeví žádná kapka, neaplikoval(a) byste si žádný inzulin, i když by se volič dávky pohyboval. Může to znamenat, že je jehla ucpaná nebo poškozená.
A Před aplikací vždy ověřte průtok. Pokud průtok neověříte, můžete si aplikovat inzulinu příliš málo, nebo si neaplikujete inzulin vůbec žádný. Může to vést k příliš vysoké hladině cukru v krvi.
Nastavení dávky
Zkontrolujte, zda je volič dávky nastaven na nule.
J
Otáčením voliče dávky nastavte požadovaný počet jednotek.
Dávku lze zmenšit nebo zvětšit otáčením voliče dávky příslušným směrem tak, aby správná dávka
byla proti značce v okénku ukazatele dávky. Při otáčení voličem dávky dbejte na to, abyste nestiskl(a)
dávkovací tlačítko, protože by inzulin unikal z pera.
Nemůžete nastavit vyšší dávku, než je počet jednotek zbývajících v zásobní vložce.

A Před aplikací inzulinu vždy pomocí voliče dávky a ukazatele dávky zkontrolujte, kolik jednotek jste zvolil(a).
A Nepočítejte cvakání pera. Pokud si zvolíte a aplikujete nesprávnou dávku, může Vám hladina cukru v krvi příliš stoupnout nebo příliš klesnout. Nepoužívejte stupnici ukazatele zbývajícího množství inzulinu - ukazuje pouze přibližné množství inzulinu zbývající ve vašem peru.
Aplikace injekce
Vpíchněte jehlu do kůže. Použijte injekční techniku, kterou vám doporučil váš lékař nebo
zdravotní sestra.
K
Dávku si vpíchněte stlačením dávkovacího tlačítka zcela dolů, až se v okénku ukazatele dávky objeví
proti značce nula. Dávejte pozor, abyste při vpichování injekce stiskl(a) pouze dávkovací tlačítko.
Otočením voliče dávky k aplikaci inzulinu nedojde.

L
► Držte dávkovači tlačítko zcela stlačené a nechte jehlu pod kůží alespoň po dobu 6 sekund.
Zajistíte tak, že bude podána celá dávka.
► Vytáhněte jehlu z kůže a potom uvolněte dávkovací tlačítko.
► Po aplikaci se vždy ujistěte, že se volič dávky vrátil na 0. Pokud se volič dávky zastaví dříve, než se vrátí na 0, nebyla aplikována celá dávka. To může mít za následek příliš vysokou hladinu cukru v krvi.

M
Jehlu zasuňte do velkého vnějšího krytu jehly, aniž byste se ho dotkl(a). Jakmile je jehla uvnitř, opatrně velký vnější kryt jehly zcela dotlačte a poté odšroubujte jehlu.
Opatrně ji vyhoďte a na pero FlexPen nasaďte zpět uzávěr pera.

A Po každé injekci jehlu vždy odstraňte a FlexPen skladujte bez nasazené jehly. Tím se sníží riziko kontaminace, infekce, úniku inzulinu, ucpání jehel a nepřesného dávkování.
Další důležité informace
A Pečující osoby musí být při manipulaci s použitými jehlami velice opatrné, aby se snížilo riziko poranění jehlou a přenesení infekce.
A Použitý FlexPen opatrně zlikvidujte bez připojené jehly.
A Pero ani jehly s nikým nesdílejte. Může to vést k přenosu infekce.
A Nikdy pero nesdílejte s dalšími osobami. Váš lék může jejich zdraví poškodit.
A Pero a jehly vždy uchovávejte mimo dohled a dosah ostatních, hlavně dětí.
NovoMix 50 FlexPen 100 jednotek/ml injekční suspenze v předplněném peru
50 % Insulinům aspartum solubile a 50 % Insulinům aspartum protaminatum cristallinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek NovoMix 50 a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 50 používat
3. Jak se přípravek NovoMix 50 používá
4. Možné nežádoucí účinky
5. Jak přípravek NovoMix 50 uchovávat
6. Obsah balení a další informace
1. Co je přípravek NovoMix 50 a k čemu se používá
NovoMix 50 je moderní inzulin (analog inzulinu) s krátkodobě i střednědobě působícím účinkem v poměru 50/50. Moderní inzulinové přípravky jsou zdokonalené verze lidského inzulinu.
NovoMix 50 je používán ke snižování vysoké hladiny cukru v krvi u pacientů s diabetes mellitus (cukrovkou). Diabetes je onemocnění, při němž tělo neprodukuje dostatek inzulinu ke kontrole hladiny cukru v krvi. NovoMix 50 může být používán v kombinaci s metforminem.
NovoMix 50 začne snižovat hladinu krevního cukru za 10 - 20 minut po podání, maximálního účinku dosahuje za 1 až 4 hodiny po podání a jeho účinek přetrvává až po dobu 14 - 24 hodin.
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 50 používat
Nepoužívejte NovoMix 50
► Jestliže jste alergický(á) na inzulin aspart nebo na kteroukoli další složku tohoto přípravku (viz bod 6, Obsah balení a další informace).
► Jestliže máte podezření, že nastupuje hypoglykemie (nízká hladina krevního cukru) (viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4).
► V inzulinových infuzních pumpách
► Pokud FlexPen upadl, je poškozený nebo promáčklý.
► Jestliže inzulin nebyl správně skladován nebo byl zmražen, viz bod 5, Jak přípravek NovoMix 50 uchovávat.
► Jestliže po promíchání inzulin není vodný, stejnoměrně bílý a zakalený.
► Jestliže po promíchání obsahuje shluky nebo pevné bílé částice usazené na dně nebo stěně zásobní vložky.
Pokud platí něco z výše uvedeného, NovoMix 50 neužívejte. Požádejte o radu lékaře, zdravotní sestru
nebo lékárníka.
Před užitím přípravku NovoMix 50
► Podle informací na štítku se ujistěte, že se jedná o správný typ inzulínu.
► Pro každou aplikaci použijte vždy novou jehlu, aby se zabránilo kontaminaci.
► Jehly a NovoMix 50 FlexPen nesmíte nikomu půjčovat.
Upozornění a opatření
Některé stavy a činnosti mohou ovlivnit vaši potřebu inzulinu. Poraďte se s lékařem:
► jestliže máte obtíže s ledvinami nebo játry či nadledvinami, podvěskem mozkovým nebo štítnou žlázou
► jestliže vykonáváte větší fyzickou aktivitu než obvykle nebo pokud chcete učinit změnu ve své běžné dietě, neboť to může ovlivnit hladinu cukru v krvi
► pokud jste nemocný(á), pokračujte v inzulinové léčbě a poraďte se s lékařem
► pokud cestujete do ciziny, cestování přes různá časová pásma může ovlivnit Vaši potřebu inzulinu a časování injekcí.
Další léčivé přípravky a přípravek NovoMix 50
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Některé léčivé přípravky ovlivňují hladinu krevního cukru, což může znamenat, že vaše dávka inzulinu musí být změněna. Seznam nejběžnějších léčivých přípravků, které mohou ovlivnit vaši léčbu inzulinem, je uveden níže.
Vaše hladina krevního cukru může být snížena (hypoglykemie), pokud užíváte:
• jiné přípravky na léčbu cukrovky
• inhibitory monoaminooxidázy (IMAO) (používané k léčbě deprese)
• beta-blokátory (používané k léčbě vysokého krevního tlaku)
• inhibitory angiotensin konvertujícího enzymu (ACE) (používané k léčbě některých srdečních onemocnění nebo vysokého krevního tlaku)
• salicyláty (používané k úlevě od bolesti nebo ke snížení horečky)
• anabolické steroidy (jako například testosteron)
• sulfonamidy (používané k léčbě infekcí).
Vaše hladina krevního cukru může být zvýšena (hyperglykemie), pokud užíváte:
• perorální antikoncepci (používaná ke kontrole početí)
• thiazidy (používané k léčbě vysokého krevního tlaku nebo nadměrného zadržování tekutin)
• glukokortikoidy (jako například „kortison“ používaný k léčbě zánětů)
• hormony štítné žlázy (používané k léčbě poruch štítné žlázy)
• sympatomimetika (jako například epinefrin [adrenalin], salbutamol nebo terbutalin používané k léčbě astmatu)
• růstový hormon (lék ke stimulaci skeletálního a somatického růstu a mající vliv na metabolické procesy v těle)
• danazol (lék ovlivňující ovulaci).
Oktreotid a lanreotid (používané k léčbě akromegalie - vzácné hormonální poruchy, která se obvykle objevuje u dospělých středního věku a je způsobena nadměrnou produkcí růstového hormonu podvěskem mozkovým) mohou hladinu cukru v krvi buď zvyšovat nebo snižovat.
Beta-blokátory (používané k léčbě vysokého krevního tlaku) mohou oslabit nebo zcela potlačit první varovné příznaky umožňující rozpoznat nízkou hladinu cukru v krvi.
Pioglitazon (tablety používané k léčbě diabetu 2. typu)
U některých pacientů s dlouhodobým onemocněním diabetem 2. typu a srdečním onemocněním či prodělanou cévní mozkovou příhodou, kteří byli léčeni pioglitazonem a inzulinem, došlo k rozvoji
srdečního selhání. Informujte ošetřujícího lékaře, jakmile to bude možné, pokud pocítíte příznaky srdečního selhání jako jsou neobvyklá dušnost nebo rychlý nárůst hmotnosti či lokalizovaný otok (edém).
Pokud užíváte kterýkoli ze zde zmíněných léků, sdělte to lékaři, zdravotní sestře nebo lékárníkovi. Přípravek NovoMix 50 s alkoholem
► Pokud pijete alkohol, může se vaše potřeba inzulinu změnit, protože hladina cukru v krvi se může jak zvýšit, tak snížit. Je doporučena pečlivá kontrola.
Těhotenství a kojení
► Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat. Klinické zkušenosti s inzulinem aspart v těhotenství jsou omezené. Vaše dávka inzulinu může během těhotenství a po porodu vyžadovat změnu. Pečlivá kompenzace cukrovky a zvlášť prevence hypoglykemie je důležitá pro zdraví vašeho dítěte.
► Během kojení není léčba přípravkem NovoMix 50 omezena.
Pokud jste těhotná či kojíte, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
► Zeptejte se, prosím, svého lékaře, zda můžete řídit auto nebo obsluhovat stroje, pokud:
• máte časté hypoglykemie
• je pro vás obtížné hypoglykemii rozeznat.
Pokud máte hladinu krevního cukru příliš nízkou nebo vysokou, může to ovlivnit vaše soustředění a schopnost reagovat a tím také vaši schopnost řídit nebo obsluhovat stroje. Mějte na paměti, že byste mohl(a) ohrozit sebe nebo ostatní.
Důležitá informace o některých pomocných látkách přípravku NovoMix 50
NovoMix 50 obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. v podstatě je „bez sodíku“.
3. Jak se přípravek NovoMix 50 používá Dávkování inzulinu a kdy inzulin užívat
Vždy užívejte inzulin a upravujte svoji dávku přesně tak, jak vám ošetřující lékař řekl. Pokud si nejste jistý(á), poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
NovoMix 50 má být obecně podáván bezprostředně před jídlem. Do 10 minut po podání injekce snězte jídlo nebo svačinu, abyste předešel(předešla) nízké hladině cukru v krvi. Pokud je to nutné, může být NovoMix 50 podán i brzy po jídle. Další informace viz níže Jak a kam aplikovat injekci.
Používáte-li NovoMix 50 v kombinaci s metforminem, mělo by být upraveno dávkování.
Svůj inzulin neměňte, pokud vám to lékař neřekne. Pokud vám lékař změnil typ nebo druh inzulinu, je možné, že vám bude muset upravit také jeho dávkování.
Použití u dětí a dospívajících
Nebyly prováděny klinické studie s používáním přípravku NovoMix 50 dětmi a dospívajícími ve věku do 18 let.
Použití u zvláštních skupin pacientů
Máte-li sníženou funkci ledvin nebo jater či, pokud je vám více než 65 let, bude u vás nutno sledovat hladinu cukru v krvi intenzivněji a konzultovat změny v dávkování inzulinu s lékařem.
Jak a kam si aplikovat injekci
NovoMix 50 je určen pro aplikaci pod kůži (subkutánně). Nikdy neaplikujte inzulin přímo do žíly (intravenózně) nebo svalu (intramuskulárně).
Při každé injekci střídejte místa vpichu v rámci té oblasti, kterou právě k aplikaci používáte. To může snižovat riziko tvorby bouliček nebo důlků v kůži (viz bod 4, Možné nežádoucí účinky). Nejlepšími místy pro aplikaci injekce jsou: přední strana břicha, hýždě, přední strana stehen nebo horní části paží. Inzulin bude mít rychlejší účinek, pokud jej aplikujete do oblasti kolem pasu. Vždy byste si měl(a) pravidelně měřit obsah cukru v krvi.
Jak zacházet s přípravkem NovoMix 50 FlexPen
NovoMix 50 FlexPen je předplněné barevně označené pero na jedno použití obsahující směs rychle a střednědobě působícího inzulinu aspart v poměru 50/50.
Přečtěte si pečlivě instrukce pro použití, které jsou součástí této příbalové informace. Pero musíte používat tak, jak je uvedeno v Instrukcích pro použití.
Před každou aplikací inzulinu se vždy ujistěte, že používáte správné pero.
Jestliže jste užil(a) více inzulinu, než jste měl(a)
Pokud jste užil(a) příliš inzulinu, vaše hladina cukru v krvi se může příliš snížit (hypoglykemie). Viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4.
Jestliže jste zapomněl(a) užít inzulin
Jestliže jste zapomněl(a) užít inzulin, vaše hladina krevního cukru může stoupnout příliš vysoko (hyperglykemie). Viz část c) Důsledky diabetu v bodě 4.
Jestliže jste přestal(a) užívat inzulin
Inzulin nepřestávejte užívat bez porady s lékařem, který vám poradí, co je třeba dělat. Mohlo by to vést k velmi vysoké hladině krevního cukru (těžké hyperglykemii) a ketoacidóze. Viz část c) Důsledky diabetu v bodě 4.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, zdravotní zdravotní sestry nebo lékárníka.
Jak zacházet s přípravkem NovoMix 50 FlexPen
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
a) Souhrn závažných a velmi častých nežádoucích účinků
Nízká hladina cukru v krvi (hypoglykemie) je velmi častý nežádoucí účinek. Může se projevit u více než 1 pacienta z 10.
Nízká hladina cukru může nastat, pokud:
• si aplikujete příliš mnoho inzulinu
• jíte příliš málo nebo vynecháte-li jídlo
• cvičíte více než obvykle
• pijete alkohol (viz bod 2, Přípravek NovoMix 50 s alkoholem).
Příznaky nízké hladiny cukru v krvi: studený pot, chladná bledá pokožka, bolest hlavy, rychlý srdeční tep, pocit nevolnosti, pocit velkého hladu, dočasné změny vidění, ospalost, neobvyklá vyčerpanost a slabost, nervozita nebo třes, pocit úzkosti, pocit zmatenosti, potíže s koncentrací.
Velmi nízká hladina cukru v krvi může vést k bezvědomí. Pokud déle trvající nízká hladina cukru v krvi není léčena, může způsobit poškození mozku (dočasné nebo trvalé) a dokonce úmrtí. Z bezvědomí se můžete zotavit rychleji, pokud vám někdo, kdo ví, jak jej použít, aplikuje hormon glukagon. Pokud dostanete glukagon, budete potřebovat glukózu nebo sladkou přesnídávku ihned poté, co nabudete vědomí. Pokud nereagujete na léčbu glukagonem, budete muset být léčen(a) v nemocnici.
Co dělat, pokud pocítíte příznaky nízké hladiny cukru v krvi:
► Pokud pocítíte příznaky nízké hladiny cukru v krvi, vezměte si glukózové tablety nebo jinou přesnídávku s vysokým obsahem cukru (např. sladkosti, sušenky, ovocnou šťávu). Pokud je to možné, změřte si hladinu cukru v krvi a odpočívejte. Vždy s sebou pro případ potřeby noste glukózové tablety nebo sladkosti s vysokým obsahem cukru.
► Poté, co příznaky nízké hladiny cukru v krvi ustoupí nebo se u vás stabilizuje hladina cukru v krvi, pokračujte s inzulinovou léčbou jako obvykle.
► Míváte-li tak nízkou hladinu cukru v krvi, že omdlíváte, pokud jste potřeboval(a) aplikovat glukagon nebo pokud míváte nízkou hladinu cukru v krvi často, pohovořte si se svým lékařem. Možná bude potřeba upravit množství nebo časové intervaly podání inzulinu, jídla nebo cvičení.
Řekněte lidem ve svém okolí, že máte diabetes, a seznamte je s jeho důsledky včetně rizika, že omdlíte (upadnete do bezvědomí) z důvodu nízké hladiny cukru v krvi. Řekněte jim, že pokud omdlíte, musí vás položit na bok a okamžitě zajistit lékařskou pomoc. Nesmějí vám dávat najíst ani napít, protože byste se mohl(a) zadusit.
Závažné alergické reakce na NovoMix 50 nebo na některou z jeho pomocných látek (tzv. systémová alergická reakce) je velmi vzácný nežádoucí účinek. Může být však potenciálně život ohrožující.
Může se projevit u méně než 1 pacienta z 10 000.
Vyhledejte ihned lékařskou pomoc:
• Pokud se příznaky alergie rozšíří na další části těla.
• Pokud se náhle necítíte dobře a začnete se potit, pociťujete nevolnost (zvracení), máte dýchací potíže, zrychlený tep a točí se vám hlava.
► Pokud zaznamenáte některé z těchto příznaků, okamžitě vyhledejte lékařskou pomoc.
b) Souhrn ostatních nežádoucích účinků
Méně časté nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta ze 100.
Příznaky alergie: v místě vpichu se mohou objevit různé příznaky místní alergické reakce (bolest, zarudnutí, kopřivka, zánět, podlitiny, otok a svědění). Obvykle vymizí po několika týdnech inzulinové léčby. Pokud nevymizí, navštivte svého lékaře.
Poruchy vidění: na počátku léčby inzulínem může dojít k poruchám vidění, tyto poruchy jsou však obvykle přechodného rázu.
Změny v místě vpichu (lipodystrofie): tuková tkáň pod kůží se může v místě vpichu ztenčit (lipoatrofie) nebo zesílit (lipohypertrofie). Obměňování míst vpichu při každé injekci snižuje riziko takových změn kůže. Pokud zjistíte, že vaše kůže má v místě vpichu dolíčky nebo zesílení, informujte svého lékaře nebo zdravotní sestru. Tyto reakce se totiž mohou zhoršit nebo mohou změnit absorbci inzulinu, pokud si do tohoto místa inzulin aplikujete.
Otoky kloubů: na začátku inzulinové léčby může dojít k zadržování vody v oblasti kotníků a dalších kloubů. Obvykle tato reakce brzy odezní. Pokud ne, kontaktujte lékaře.
Diabetická retinopatie (oční onemocnění spojené s cukrovkou, které může vést ke ztrátě zraku): jestliže trpíte diabetickou retinopatií a hladina vašeho krevního cukru se velmi rychle zlepší, může dojít ke zhoršení retinopatie. Poraďte se o tom se svým lékařem.
Vzácné nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta z 1 000.
Bolestivá neuropatie (bolest způsobená poškozením nervů): jestliže se hladina vašeho krevního cukru velmi rychle zlepší, může se dostavit bolest nervového původu. Tento stav se nazývá akutní bolestivá neuropatie a obvykle se jedná o přechodný stav.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
c) Důsledky diabetu
Vysoká hladina cukru v krvi (hyperglykemie)
Vysoká hladina cukru může nastat, pokud:
• j ste si neaplikoval(a) dostatečné množství inzulinu
• zapomněl(a) jste si aplikovat inzulin nebo jste ho přestal(a) užívat
• opakovaně užíváte menší dávky inzulinu, než je třeba
• máte infekci a/nebo horečku
• jíte více než obvykle
• cvičíte méně než obvykle.
Varovné příznaky vysoké hladiny cukru v krvi:
Varovné příznaky se objevují postupně. Zahrnují: častější močení, pocit žízně, ztrátu chuti k jídlu, pocit nevolnosti (pocit na zvracení nebo zvracení), pocit ospalosti nebo únavy, zarudlou, suchou pokožku, sucho v ústech a ovocný (acetonový) zápach dechu.
Co dělat, pokud pocítíte příznaky vysoké hladiny cukru v krvi:
► Pokud zaznamenáte některé z výše uvedených příznaků: zkontrolujte si hladinu krevního cukru, otestuje si moč na ketony, máte-li možnost, a potom ihned vyhledejte lékařskou pomoc.
► Mohou to být příznaky velmi závažného stavu nazývaného diabetická ketoacidóza (hromadění kyseliny v krvi, protože tělo odbourává místo cukru tuk). Pokud jej neléčíte, může vést až k diabetickému kómatu a případně ke smrti.
Jak přípravek NovoMix 50 uchovávat
5.
Uchovávejte tento přípravek mimo dohled a dosah a dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku pera FlexPen a krabičce za „Použitelné do”. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Mějte pero FlexPen vždy, když jej nepoužíváte, opatřené krytem pera, aby byl přípravek chráněn před světlem. NovoMix 50 musí být chráněn před vysokými teplotami a světlem.
Před otevřením: NovoMix 50 FlexPen, který není používán, musí být uchováván v chladničce (2 °C až 8 °C), mimo chladicí zařízení. Chraňte před mrazem.
Před použitím vyjměte NovoMix 50 FlexPen z chladničky. Pokaždé, když začínáte používat nové pero, je doporučeno promíchat inzulin dle instrukcí. Viz Instrukce pro použití.
Během používání či pohotovostně nošený: NovoMix 50 FlexPen, který používáte nebo nosíte jako náhradní, by neměl být uchováván v chladničce. Můžete ho nosit s sebou a uchovávat při pokojové teplotě (do 30 °C) až po dobu 4 týdnů.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co NovoMix 50 obsahuje
• Léčivou látkou je inzulin aspart. NovoMix 50 je směs složená z 50 % rozpustného inzulinu aspart a 50 % krystalického protaminového inzulinu aspart. 1 ml obsahuje 100 jednotek inzulinu aspart. Jedno předplněné pero obsahuje 300 jednotek inzulinu aspart ve 3 ml injekční suspenze.
• Pomocnými látkami jsou glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselina chlorovodíková, hydroxid sodný a voda na injekci.
Jak NovoMix 50 vypadá a co obsahuje toto balení
NovoMix 50 je dodáván jako injekční suspenze v předplněném peru. V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání. Po promíchání by kapalina měla být vodná, stejnoměrně bílá a zakalená. Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, nepoužívejte ho.
Velikosti balení jsou 1, 5 a 10 předplněných per po 3 ml. Na trhu nemusí být všechny velikosti balení.
Zakalená, bílá vodná suspenze.
Držitel rozhodnutí o registraci a výrobce
Novo Nordisk A/S Novo Allé
DK-2880 Bagsv^rd, Dánsko
Nyní si na druhé straně přečtěte informace o použití pera FlexPen. Tato příbalová informace byla naposledy revidována
Další zdroje informací
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky: http://www.ema.europa.eu/
Instrukce pro použití přípravku NovoMix 50 injekční suspenze v peru FlexPen.
Před použitím pera FlexPen si pečlivě přečtěte dále uvedené pokyny. Pokud nebudete tyto pokyny pečlivě dodržovat, můžete si aplikovat inzulínu příliš málo nebo příliš mnoho, což může vést k příliš vysoké či příliš nízké hladině cukru v krvi.
FlexPen je předplněné inzulinové pero s možností nastavení dávky.
► Dávky lze nastavit od 1 do 60 jednotek v přírůstcích po 1 jednotce.
► FlexPen je určen pro použití s jednorázovými jehlami NovoFine nebo NovoTwist o délce do 8 mm.
► Vždy při sobě noste náhradní inzulinový aplikátor pro případ, že pero FlexPen ztratíte nebo bude poškozeno.
NovoMix 50 FlexPen

Stupnice ukazatele zbývajícího množství inzulinu
Uzávěr pera

Volič Dávkovači (priklftd)
Ukazatel dávky tlačítko „ „ , ....
dávky | Velký vnejsi Vnitřní
kryt jehly kryt jehly
Jehla
Papírový
kryt
Péče o pero
► Pero FlexPen vyžaduje opatrné zacházení. Jestliže spadlo, bylo poškozeno nebo bylo vystaveno nárazu, vzniká riziko úniku inzulinu. To může způsobit nepřesné dávkování, což může vést
k příliš vysoké nebo příliš nízké hladině cukru v krvi.
► Vnější povrch pera FlexPen můžete očistit otřením desinfekčním tamponem. Nenamáčejte jej, neomývejte jej ani jej nemažte, protože byste ho tím mohl(a) poškodit.
► FlexPen znovu nenaplňujte.
Promíchání inzulinu
A
Zkontrolujte název a barvu na štítku pera, abyste se ujistil(a), že obsahuje správný typ inzulinu. To je obzvlášť důležité, pokud užíváte více než jeden typ inzulinu. Pokud si aplikujete špatný typ inzulinu, může Vám hladina cukru v krvi příliš stoupnout nebo příliš klesnout.
Pokaždé, když začínáte používat nové pero.
Než inzulin použijete, nechte ho ohřát na pokojovou teplotu. To usnadní jeho promíchání.
Sejměte uzávěr pera.

B
Před první injekcí novým perem FlexPen musíte inzulin promíchat:
Převalujte pero mezi dlaněmi 10krát - je důležité držet pero v horizontální (vodorovné) poloze.

C
Potom 10krát pohybujte perem nahoru a dolů mezi dvěma polohami (viz obrázek) tak, aby se skleněná kulička pohybovala z jednoho konce zásobní vložky na druhý.
Převalování a protřepávání opakujte, dokud není tekutina vodná, stejnoměrně bílá a zakalená.
Před každou další injekcí
Pohybujte perem nahoru a dolů mezi dvěma polohami alespoň 10krát, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Pokud tento postup samotný nestačí k tomu, aby vznikla vodná, stejnoměrně bílá a zakalená tekutina, opakujte převalování a promíchávání (viz obrázky B a C) tak dlouho, dokud tekutina nemá vodný, stejnoměrně bílý a zakalený vzhled.
► Před každou injekcí se ujistěte, že jste inzulin promíchal(a). Promíchání sníží riziko příliš vysoké nebo příliš nízké hladiny cukru v krvi. Po promíchání inzulinu dokončete neprodleně všechny další kroky k aplikaci injekce.

A Vždy zkontrolujte, zda v zásobní vložce zbývá ještě alespoň 12 jednotek inzulinu, abyste ho mohl(a) rovnoměrně promíchat. Je-li v ní méně než 12 jednotek, použijte nový FlexPen.
12 jednotek je vyznačeno na stupnici ukazatele zbývajícího množství inzulinu (viz velký obrázek na začátku této instrukce).
A Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, pero nepoužívejte.
Nasazení jehly D
Vezměte si novou jehlu a odtrhněte papírový kryt. Našroubujte jehlu rovně a pevně na FlexPen.

Sejměte z jehly velký vnější kryt a uchovejte ho pro pozdější potřebu.

Sejměte z jehly vnitřní kryt a vyhoďte ho.
Nikdy se nepokoušejte vnitřní kryt jehly opět nasadit na jehlu. Mohl(a) byste se o jehlu píchnout.

A Pro každou aplikaci použijte vždy novou jehlu. Tím se sníží riziko kontaminace, infekce, úniku inzulinu, ucpání jehel a nepřesného dávkování.
A Dbejte, abyste jehlu před použitím neohnul(a) nebo jinak nepoškodil(a).
Ověření funkčnosti
Před každou injekcí se během normálního používání může v zásobní vložce nahromadit malé množství vzduchu. Abyste zabránil(a) vpíchnutí vzduchu a zajistil(a) správné dávkování, postupujte dle dále uvedených pokynů:
G
Otočte voličem dávky tak, abyste nastavil(a) 2 jednotky.

H
Držte FlexPen jehlou směrem nahoru a jemně na zásobní vložku několikrát poklepte prstem, aby se v horní části zásobní vložky nahromadily případné vzduchové bubliny.

I
Držte jehlu stále směrem vzhůru a stlačte úplně dávkovací tlačítko. Volič dávky se vrátí na nulu.
Na hrotu jehly se musí objevit kapka inzulinu. Jestliže se neobjeví, vyměňte jehlu a celý postup zopakujte, nejvíce však 6krát.
Jestliže se kapka inzulinu ani potom neobjeví, je pero vadné a musíte použít jiné.

A Vždy před podáním injekce zkontrolujte, zda se na špičce jehly objeví kapka. Tím se ujistíte, že inzulin protéká perem. Pokud se neobjeví žádná kapka, neaplikoval(a) byste si žádný inzulin, i když by se volič dávky pohyboval. Může to znamenat, že je jehla ucpaná nebo poškozená.
A Před aplikací vždy ověřte průtok. Pokud průtok neověříte, můžete si aplikovat inzulinu příliš málo, nebo si neaplikujete inzulin vůbec žádný. Může to vést k příliš vysoké hladině cukru v krvi.
Nastavení dávky
Zkontrolujte, zda je volič dávky nastaven na nule.
J
Otáčením voliče dávky nastavte požadovaný počet jednotek.
Dávku lze zmenšit nebo zvětšit otáčením voliče dávky příslušným směrem tak, aby správná dávka
byla proti značce v okénku ukazatele dávky. Při otáčení voličem dávky dbejte na to, abyste nestiskl(a)
dávkovací tlačítko, protože by inzulin unikal z pera.
Nemůžete nastavit vyšší dávku, než je počet jednotek zbývajících v zásobní vložce.

A Před aplikací inzulinu vždy pomocí voliče dávky a ukazatele dávky zkontrolujte, kolik jednotek jste zvolil(a).
A Nepočítejte cvakání pera. Pokud si zvolíte a aplikujete nesprávnou dávku, může Vám hladina cukru v krvi příliš stoupnout nebo příliš klesnout. Nepoužívejte stupnici ukazatele zbývajícího množství inzulinu - ukazuje pouze přibližné množství inzulinu zbývající ve vašem peru.
Aplikace injekce
Vpíchněte jehlu do kůže. Použijte injekční techniku, kterou vám doporučil váš lékař nebo
zdravotní sestra.
K
Dávku si vpíchněte stlačením dávkovacího tlačítka zcela dolů, až se v okénku ukazatele dávky objeví proti značce nula. Dávejte pozor, abyste při vpichování injekce stiskl(a) pouze dávkovací tlačítko.
Otočením voliče dávky k aplikaci inzulínu nedojde.

L
► Držte dávkovači tlačítko zcela stlačené a nechte jehlu pod kůží alespoň po dobu 6 sekund.
Zajistíte tak, že bude podána celá dávka.
► Vytáhněte jehlu z kůže a potom uvolněte dávkovací tlačítko.
► Po aplikaci se vždy ujistěte, že se volič dávky vrátil na 0. Pokud se volič dávky zastaví dříve, než se vrátí na 0, nebyla aplikována celá dávka. To může mít za následek příliš vysokou hladinu cukru v krvi.

M
Jehlu zasuňte do velkého vnějšího krytu jehly, aniž byste se ho dotkl(a). Jakmile je jehla uvnitř, opatrně velký vnější kryt jehly zcela dotlačte a poté odšroubujte jehlu.
Opatrně ji vyhoďte a na pero FlexPen nasaďte zpět uzávěr pera.

A Po každé injekci jehlu vždy odstraňte a FlexPen skladujte bez nasazené jehly. Tím se sníží riziko kontaminace, infekce, úniku inzulinu, ucpání jehel a nepřesného dávkování.
Další důležité informace
A Pečující osoby musí být při manipulaci s použitými jehlami velice opatrné, aby se snížilo riziko poranění jehlou a přenesení infekce.
A Použitý FlexPen opatrně zlikvidujte bez připojené jehly.
A Pero ani jehly s nikým nesdílejte. Může to vést k přenosu infekce.
A Nikdy pero nesdílejte s dalšími osobami. Váš lék může jejich zdraví poškodit.
A Pero a jehly vždy uchovávejte mimo dohled a dosah ostatních, hlavně dětí.
NovoMix 70 FlexPen 100 jednotek/ml injekční suspenze v předplněném peru
70 % Insulinům aspartum solubile a 30 % Insulinům aspartum protaminatum cristallinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, zdravotní sestry nebo lékárníka.
• Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek NovoMix 70 a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 70 používat
3. Jak se přípravek NovoMix 70 používá
4. Možné nežádoucí účinky
5. Jak přípravek NovoMix 70 uchovávat
6. Obsah balení a další informace
1. Co je přípravek NovoMix 70 a k čemu se používá
NovoMix 70 je moderní inzulin (analog inzulinu) s krátkodobě i střednědobě působícím účinkem v poměru 70/30. Moderní inzulinové přípravky jsou zdokonalené verze lidského inzulinu.
NovoMix 70 je používán ke snižování vysoké hladiny cukru v krvi u pacientů s diabetes mellitus (cukrovkou). Diabetes je onemocnění, při němž tělo neprodukuje dostatek inzulinu ke kontrole hladiny cukru v krvi. NovoMix 70 může být používán v kombinaci s metforminem.
NovoMix 70 začne snižovat hladinu krevního cukru za 10 - 20 minut po podání, maximálního účinku dosahuje za 1 až 4 hodiny po podání a jeho účinek přetrvává až po dobu 14 - 24 hodin.
2. Čemu musíte věnovat pozornost, než začnete přípravek NovoMix 70 používat
Nepoužívejte NovoMix 70
► Jestliže jste alergický(á) na inzulin aspart nebo na kteroukoli další složku tohoto přípravku (viz bod 6, Obsah balení a další informace).
► Jestliže máte podezření, že nastupuje hypoglykemie (nízká hladina krevního cukru) (viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4).
► V inzulinových infuzních pumpách
► Pokud FlexPen upadl, je poškozený nebo promáčklý.
► Jestliže inzulin nebyl správně skladován nebo byl zmražen, viz bod 5, Jak přípravek NovoMix 70 uchovávat.
► Jestliže po promíchání inzulin není vodný, stejnoměrně bílý a zakalený.
► Jestliže po promíchání obsahuje shluky nebo pevné bílé částice usazené na dně nebo stěně zásobní vložky.
Pokud platí něco z výše uvedeného, NovoMix 70 neužívejte. Požádejte o radu lékaře, zdravotní sestru
nebo lékárníka.
► Podle informací na štítku se ujistěte, že se jedná o správný typ inzulínu.
► Pro každou aplikaci použijte vždy novou jehlu, aby se zabránilo kontaminaci.
► Jehly a NovoMix 70 FlexPen nesmíte nikomu půjčovat.
Upozornění a opatření
Některé stavy a činnosti mohou ovlivnit vaši potřebu inzulinu. Poraďte se s lékařem:
► jestliže máte obtíže s ledvinami nebo játry či nadledvinami, podvěskem mozkovým nebo štítnou žlázou
► jestliže vykonáváte větší fyzickou aktivitu než obvykle nebo pokud chcete učinit změnu ve své běžné dietě, neboť to může ovlivnit hladinu cukru v krvi
► pokud jste nemocný(á), pokračujte v inzulinové léčbě a poraďte se s lékařem
► pokud cestujete do ciziny, cestování přes různá časová pásma může ovlivnit Vaši potřebu inzulinu a časování injekcí.
Další léčivé přípravky a přípravek NovoMix 70
Informujte svého lékaře, zdravotní sestru nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Některé léčivé přípravky ovlivňují hladinu krevního cukru, což může znamenat, že vaše dávka inzulinu musí být změněna. Seznam nejběžnějších léčivých přípravků, které mohou ovlivnit vaši léčbu inzulinem, je uveden níže.
Vaše hladina krevního cukru může být snížena (hypoglykemie), pokud užíváte:
• jiné přípravky na léčbu cukrovky
• inhibitory monoaminooxidázy (IMAO) (používané k léčbě deprese)
• beta-blokátory (používané k léčbě vysokého krevního tlaku)
• inhibitory angiotensin konvertujícího enzymu (ACE) (používané k léčbě některých srdečních onemocnění nebo vysokého krevního tlaku)
• salicyláty (používané k úlevě od bolesti nebo ke snížení horečky)
• anabolické steroidy (jako například testosteron)
• sulfonamidy (používané k léčbě infekcí).
Vaše hladina krevního cukru může být zvýšena (hyperglykemie), pokud užíváte:
• perorální antikoncepci (používaná ke kontrole početí)
• thiazidy (používané k léčbě vysokého krevního tlaku nebo nadměrného zadržování tekutin)
• glukokortikoidy (jako například „kortison“ používaný k léčbě zánětů)
• hormony štítné žlázy (používané k léčbě poruch štítné žlázy)
• sympatomimetika (jako například epinefrin [adrenalin], salbutamol nebo terbutalin používané k léčbě astmatu)
• růstový hormon (lék ke stimulaci skeletálního a somatického růstu a mající vliv na metabolické procesy v těle)
• danazol (lék ovlivňující ovulaci).
Oktreotid a lanreotid (používané k léčbě akromegalie - vzácné hormonální poruchy, která se obvykle objevuje u dospělých středního věku a je způsobena nadměrnou produkcí růstového hormonu podvěskem mozkovým) mohou hladinu cukru v krvi buď zvyšovat nebo snižovat.
Beta-blokátory (používané k léčbě vysokého krevního tlaku) mohou oslabit nebo zcela potlačit první varovné příznaky umožňující rozpoznat nízkou hladinu cukru v krvi.
Pioglitazon (tablety používané k léčbě diabetu 2. typu)
U některých pacientů s dlouhodobým onemocněním diabetem 2. typu a srdečním onemocněním či prodělanou cévní mozkovou příhodou, kteří byli léčeni pioglitazonem a inzulinem, došlo k rozvoji
srdečního selhání. Informujte ošetřujícího lékaře, jakmile to bude možné, pokud pocítíte příznaky srdečního selhání jako jsou neobvyklá dušnost nebo rychlý nárůst hmotnosti či lokalizovaný otok (edém).
Pokud užíváte kterýkoli ze zde zmíněných léků, sdělte to lékaři, zdravotní sestře nebo lékárníkovi. Přípravek NovoMix 70 s alkoholem
► Pokud pijete alkohol, může se vaše potřeba inzulinu změnit, protože hladina cukru v krvi se může jak zvýšit, tak snížit. Je doporučena pečlivá kontrola.
Těhotenství a kojení
► Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat. Klinické zkušenosti s inzulinem aspart v těhotenství jsou omezené. Vaše dávka inzulinu může během těhotenství a po porodu vyžadovat změnu. Pečlivá kompenzace cukrovky a zvlášť prevence hypoglykemie je důležitá pro zdraví vašeho dítěte.
► Během kojení není léčba přípravkem NovoMix 70 omezena.
Pokud jste těhotná či kojíte, poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem dříve, než začnete užívat jakýkoliv lék.
Řízení dopravních prostředků a obsluha strojů
► Zeptejte se, prosím, svého lékaře, zda můžete řídit auto nebo obsluhovat stroje, pokud:
• máte časté hypoglykemie
• je pro vás obtížné hypoglykemii rozeznat.
Pokud máte hladinu krevního cukru příliš nízkou nebo vysokou, může to ovlivnit vaše soustředění a schopnost reagovat a tím také vaši schopnost řídit nebo obsluhovat stroje. Mějte na paměti, že byste mohl(a) ohrozit sebe nebo ostatní.
Důležitá informace o některých pomocných látkách přípravku NovoMix 70
NovoMix 70 obsahuje méně než 1 mmol (23 mg) sodíku v jedné dávce, tj. v podstatě je „bez sodíku“.
3. Jak se přípravek NovoMix 70 používá Dávkování inzulinu a kdy inzulin užívat
Vždy užívejte inzulin a upravujte svoji dávku přesně tak, jak vám ošetřující lékař řekl. Pokud si nejste jistý(á), poraďte se se svým lékařem, zdravotní sestrou nebo lékárníkem.
NovoMix 70 má být obecně podáván bezprostředně před jídlem. Do 10 minut po podání injekce snězte jídlo nebo svačinu, abyste předešel(předešla) nízké hladině cukru v krvi. Pokud je to nutné, může být NovoMix 70 podán i brzy po jídle. Další informace viz níže Jak a kam aplikovat injekci.
Používáte-li NovoMix 70 v kombinaci s metforminem, mělo by být upraveno dávkování.
Svůj inzulin neměňte, pokud vám to lékař neřekne. Pokud vám lékař změnil typ nebo druh inzulinu, je možné, že vám bude muset upravit také jeho dávkování.
Použití u dětí a dospívajících
Nebyly prováděny klinické studie s používáním přípravku NovoMix 70 dětmi a dospívajícími ve věku do 18 let.
Použití u zvláštních skupin pacientů
Máte-li sníženou funkci ledvin nebo jater či, pokud je vám více než 65 let, bude u vás nutno sledovat hladinu cukru v krvi intenzivněji a konzultovat změny v dávkování inzulinu s lékařem.
Jak a kam si aplikovat injekci
NovoMix 70 je určen pro aplikaci pod kůži (subkutánně). Nikdy neaplikujte inzulin přímo do žíly (intravenózně) nebo svalu (intramuskulárně).
Při každé injekci střídejte místa vpichu v rámci té oblasti, kterou právě k aplikaci používáte. To může snižovat riziko tvorby bouliček nebo důlků v kůži (viz bod 4, Možné nežádoucí účinky). Nejlepšími místy pro aplikaci injekce jsou: přední strana břicha, hýždě, přední strana stehen nebo horní části paží. Inzulin bude mít rychlejší účinek, pokud jej aplikujete do oblasti kolem pasu. Vždy byste si měl(a) pravidelně měřit obsah cukru v krvi.
Jak zacházet s přípravkem NovoMix 70 FlexPen
NovoMix 70 FlexPen je předplněné barevně označené pero na jedno použití obsahující směs rychle a střednědobě působícího inzulinu aspart v poměru 70/30.
Přečtěte si pečlivě instrukce pro použití, které jsou součástí této příbalové informace. Pero musíte používat tak, jak je uvedeno v Instrukcích pro použití.
Před každou aplikací inzulinu se vždy ujistěte, že používáte správné pero.
Jestliže jste užil(a) více inzulinu, než jste měl(a)
Pokud jste užil(a) příliš inzulinu, vaše hladina cukru v krvi se může příliš snížit (hypoglykemie). Viz část a) Souhrn závažných a velmi častých nežádoucích účinků v bodě 4.
Jestliže jste zapomněl(a) užít inzulin
Jestliže jste zapomněl(a) užít inzulin, vaše hladina krevního cukru může stoupnout příliš vysoko (hyperglykemie). Viz část c) Důsledky diabetu v bodě 4.
Jestliže jste přestal(a) užívat inzulin
Inzulin nepřestávejte užívat bez porady s lékařem, který vám poradí, co je třeba dělat. Mohlo by to vést k velmi vysoké hladině krevního cukru (těžké hyperglykemii) a ketoacidóze. Viz část c) Důsledky diabetu v bodě 4.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře, zdravotní zdravotní sestry nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
a) Souhrn závažných a velmi častých nežádoucích účinků
Nízká hladina cukru v krvi (hypoglykemie) je velmi častý nežádoucí účinek. Může se projevit u více než 1 pacienta z 10.
Nízká hladina cukru může nastat, pokud:
• si aplikujete příliš mnoho inzulinu
• jíte příliš málo nebo vynecháte-li jídlo
• cvičíte více než obvykle
• pijete alkohol (viz bod 2, Přípravek NovoMix 70 s alkoholem).
Příznaky nízké hladiny cukru v krvi: studený pot, chladná bledá pokožka, bolest hlavy, rychlý srdeční tep, pocit nevolnosti, pocit velkého hladu, dočasné změny vidění, ospalost, neobvyklá vyčerpanost a slabost, nervozita nebo třes, pocit úzkosti, pocit zmatenosti, potíže s koncentrací.
Velmi nízká hladina cukru v krvi může vést k bezvědomí. Pokud déle trvající nízká hladina cukru v krvi není léčena, může způsobit poškození mozku (dočasné nebo trvalé) a dokonce úmrtí. Z bezvědomí se můžete zotavit rychleji, pokud vám někdo, kdo ví, jak jej použít, aplikuje hormon glukagon. Pokud dostanete glukagon, budete potřebovat glukózu nebo sladkou přesnídávku ihned poté, co nabudete vědomí. Pokud nereagujete na léčbu glukagonem, budete muset být léčen(a) v nemocnici.
Co dělat, pokud pocítíte příznaky nízké hladiny cukru v krvi:
► Pokud pocítíte příznaky nízké hladiny cukru v krvi, vezměte si glukózové tablety nebo jinou přesnídávku s vysokým obsahem cukru (např. sladkosti, sušenky, ovocnou šťávu). Pokud je to možné, změřte si hladinu cukru v krvi a odpočívejte. Vždy s sebou pro případ potřeby noste glukózové tablety nebo sladkosti s vysokým obsahem cukru.
► Poté, co příznaky nízké hladiny cukru v krvi ustoupí nebo se u vás stabilizuje hladina cukru v krvi, pokračujte s inzulinovou léčbou jako obvykle.
► Míváte-li tak nízkou hladinu cukru v krvi, že omdlíváte, pokud jste potřeboval(a) aplikovat glukagon nebo pokud míváte nízkou hladinu cukru v krvi často, pohovořte si se svým lékařem. Možná bude potřeba upravit množství nebo časové intervaly podání inzulinu, jídla nebo cvičení.
Řekněte lidem ve svém okolí, že máte diabetes, a seznamte je s jeho důsledky včetně rizika, že omdlíte (upadnete do bezvědomí) z důvodu nízké hladiny cukru v krvi. Řekněte jim, že pokud omdlíte, musí vás položit na bok a okamžitě zajistit lékařskou pomoc. Nesmějí vám dávat najíst ani napít, protože byste se mohl(a) zadusit.
Závažné alergické reakce na NovoMix 70 nebo na některou z jeho pomocných látek (tzv. systémová alergická reakce) je velmi vzácný nežádoucí účinek. Může být však potenciálně život ohrožující.
Může se projevit u méně než 1 pacienta z 10 000.
Vyhledejte ihned lékařskou pomoc:
• Pokud se příznaky alergie rozšíří na další části těla.
• Pokud se náhle necítíte dobře a začnete se potit, pociťujete nevolnost (zvracení), máte dýchací potíže, zrychlený tep a točí se vám hlava.
► Pokud zaznamenáte některé z těchto příznaků, okamžitě vyhledejte lékařskou pomoc.
b) Souhrn ostatních nežádoucích účinků
Méně časté nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta ze 100.
Příznaky alergie: v místě vpichu se mohou objevit různé příznaky místní alergické reakce (bolest, zarudnutí, kopřivka, zánět, podlitiny, otok a svědění). Obvykle vymizí po několika týdnech inzulinové léčby. Pokud nevymizí, navštivte svého lékaře.
Poruchy vidění: na počátku léčby inzulinem může dojít k poruchám vidění, tyto poruchy jsou však
obvykle přechodného rázu.
Změny v místě vpichu (lipodystrofie): tuková tkáň pod kůží se může v místě vpichu ztenčit (lipoatrofie) nebo zesílit (lipohypertrofie). Obměňování míst vpichu při každé injekci snižuje riziko takových změn kůže. Pokud zjistíte, že vaše kůže má v místě vpichu dolíčky nebo zesílení, informujte svého lékaře nebo zdravotní sestru. Tyto reakce se totiž mohou zhoršit nebo mohou změnit absorbci inzulinu, pokud si do tohoto místa inzulin aplikujete.
Otoky kloubů: na začátku inzulinové léčby může dojít k zadržování vody v oblasti kotníků a dalších kloubů. Obvykle tato reakce brzy odezní. Pokud ne, kontaktujte lékaře.
Diabetická retinopatie (oční onemocnění spojené s cukrovkou, které může vést ke ztrátě zraku): jestliže trpíte diabetickou retinopatií a hladina vašeho krevního cukru se velmi rychle zlepší, může dojít ke zhoršení retinopatie. Poraďte se o tom se svým lékařem.
Vzácné nežádoucí účinky
Mohou se_projevit u méně než 1 pacienta z 1 000.
Bolestivá neuropatie (bolest způsobená poškozením nervů): jestliže se hladina vašeho krevního cukru velmi rychle zlepší, může se dostavit bolest nervového původu. Tento stav se nazývá akutní bolestivá neuropatie a obvykle se jedná o přechodný stav.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
c) Důsledky diabetu
Vysoká hladina cukru v krvi (hyperglykemie)
Vysoká hladina cukru může nastat, pokud:
• j ste si neaplikoval(a) dostatečné množství inzulinu
• zapomněl(a) jste si aplikovat inzulin nebo jste ho přestal(a) užívat
• opakovaně užíváte menší dávky inzulinu, než je třeba
• máte infekci a/nebo horečku
• jíte více než obvykle
• cvičíte méně než obvykle.
Varovné příznaky vysoké hladiny cukru v krvi:
Varovné příznaky se objevují postupně. Zahrnují: častější močení, pocit žízně, ztrátu chuti k jídlu, pocit nevolnosti (pocit na zvracení nebo zvracení), pocit ospalosti nebo únavy, zarudlou, suchou pokožku, sucho v ústech a ovocný (acetonový) zápach dechu.
Co dělat, pokud pocítíte příznaky vysoké hladiny cukru v krvi:
► Pokud zaznamenáte některé z výše uvedených příznaků: zkontrolujte si hladinu krevního cukru, otestuje si moč na ketony, máte-li možnost, a potom ihned vyhledejte lékařskou pomoc.
► Mohou to být příznaky velmi závažného stavu nazývaného diabetická ketoacidóza (hromadění kyseliny v krvi, protože tělo odbourává místo cukru tuk). Pokud jej neléčíte, může vést až k diabetickému kómatu a případně ke smrti.
5. Jak přípravek NovoMix 70 uchovávat
Uchovávejte tento přípravek mimo dohled a dosah a dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na štítku pera FlexPen a krabičce za „Použitelné do”. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Mějte pero FlexPen vždy, když jej nepoužíváte, opatřené krytem pera, aby byl přípravek chráněn před světlem. NovoMix 70 musí být chráněn před vysokými teplotami a světlem.
Před otevřením: NovoMix 70 FlexPen, který není používán, musí být uchováván v chladničce (2 °C až 8 °C), mimo chladicí zařízení. Chraňte před mrazem.
Před použitím vyjměte NovoMix 70 FlexPen z chladničky. Pokaždé, když začínáte používat nové pero, je doporučeno promíchat inzulin dle instrukcí. Viz Instrukce pro použití.
Během používání či pohotovostně nošený: NovoMix 70 FlexPen, který používáte nebo nosíte jako náhradní, by neměl být uchováván v chladničce. Můžete ho nosit s sebou a uchovávat při pokojové teplotě (do 30 °C) až po dobu 4 týdnů.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co NovoMix 70 obsahuje
• Léčivou látkou je inzulin aspart. NovoMix 70 je směs složená ze 70 % rozpustného inzulinu aspart a 30 % krystalického protaminového inzulinu aspart. 1 ml obsahuje 100 jednotek inzulinu aspart. Jedno předplněné pero obsahuje 300 jednotek inzulinu aspart ve 3 ml injekční suspenze.
• Pomocnými látkami jsou glycerol, fenol, metakresol, chlorid zinečnatý, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, protamin-sulfát, kyselina chlorovodíková, hydroxid sodný a voda na injekci.
Jak NovoMix 70 vypadá a co obsahuje toto balení
NovoMix 70 je dodáván jako injekční suspenze v předplněném peru. V zásobní vložce je umístěna skleněná kulička, která usnadňuje promíchávání. Po promíchání by kapalina měla být vodná, stejnoměrně bílá a zakalená. Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, nepoužívejte ho.
Velikosti balení jsou 1, 5 a 10 předplněných per po 3 ml. Na trhu nemusí být všechny velikosti balení.
Zakalená, bílá vodná suspenze.
Držitel rozhodnutí o registraci a výrobce
Novo Nordisk A/S Novo Allé
DK-2880 Bagsv^rd, Dánsko
Nyní si na druhé straně přečtěte informace o použití pera FlexPen. Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku j sou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky: http://www.ema.europa.eu/
Instrukce pro použití přípravku NovoMix 70 injekční suspenze v peru FlexPen.
Před použitím pera FlexPen si pečlivě přečtěte dále uvedené pokyny. Pokud nebudete tyto pokyny pečlivě dodržovat, můžete si aplikovat inzulínu příliš málo nebo příliš mnoho, což může vést k příliš vysoké či příliš nízké hladině cukru v krvi.
FlexPen je předplněné inzulinové pero s možností nastavení dávky.
► Dávky lze nastavit od 1 do 60 jednotek v přírůstcích po 1 jednotce.
► FlexPen je určen pro použití s jednorázovými jehlami NovoFine nebo NovoTwist o délce do 8 mm.
► Vždy při sobě noste náhradní inzulinový aplikátor pro případ, že pero FlexPen ztratíte nebo bude poškozeno.
NovoMix 70 FlexPen
Uzávěr pera
Skleněná Zásobní kulička vložka
Volič Dávkovači Jehla (příklad)
Ukazatel dávky tlačítko
Velký vnější Vnitřní kryt j ehly kryt j ehly

12 jednotek Stupnice ukazatele zbývajícího množství inzulinu
Jehla
Papírový
kryt

Péče o pero
► Pero FlexPen vyžaduje opatrné zacházení. Jestliže spadlo, bylo poškozeno nebo bylo vystaveno nárazu, vzniká riziko úniku inzulinu. To může způsobit nepřesné dávkování, což může vést
k příliš vysoké nebo příliš nízké hladině cukru v krvi.
► Vnější povrch pera FlexPen můžete očistit otřením desinfekčním tamponem. Nenamáčejte jej, neomývejte jej ani jej nemažte, protože byste ho tím mohl(a) poškodit.
► FlexPen znovu nenaplňujte.
Promíchání inzulinu
A
Zkontrolujte název a barvu na štítku pera, abyste se ujistil(a), že obsahuje správný typ inzulinu. To je obzvlášť důležité, pokud užíváte více než jeden typ inzulinu. Pokud si aplikujete špatný typ inzulinu, může Vám hladina cukru v krvi příliš stoupnout nebo příliš klesnout.
Pokaždé, když začínáte používat nové pero.
Než inzulin použijete, nechte ho ohřát na pokojovou teplotu. To usnadní jeho promíchání.
Sejměte uzávěr pera.

B
Před první injekcí novým perem FlexPen musíte inzulin promíchat:
Převalujte pero mezi dlaněmi 10krát - je důležité držet pero v horizontální (vodorovné) poloze.

C
Potom 10krát pohybujte perem nahoru a dolů mezi dvěma polohami (viz obrázek) tak, aby se skleněná kulička pohybovala z jednoho konce zásobní vložky na druhý.
Převalování a protřepávání opakujte, dokud není tekutina vodná, stejnoměrně bílá a zakalená.
Před každou další injekcí
Pohybujte perem nahoru a dolů mezi dvěma polohami alespoň 10krát, dokud není tekutina vodná, stejnoměrně bílá a zakalená. Pokud tento postup samotný nestačí k tomu, aby vznikla vodná, stejnoměrně bílá a zakalená tekutina, opakujte převalování a promíchávání (viz obrázky B a C) tak dlouho, dokud tekutina nemá vodný, stejnoměrně bílý a zakalený vzhled.
► Před každou injekcí se ujistěte, že jste inzulin promíchal(a). Promíchání sníží riziko příliš vysoké nebo příliš nízké hladiny cukru v krvi. Po promíchání inzulinu dokončete neprodleně všechny další kroky k aplikaci injekce.

A Vždy zkontrolujte, zda v zásobní vložce zbývá ještě alespoň 12 jednotek inzulinu, abyste ho mohl(a) rovnoměrně promíchat. Je-li v ní méně než 12 jednotek, použijte nový FlexPen.
12 jednotek je vyznačeno na stupnici ukazatele zbývajícího množství inzulinu (viz velký obrázek na začátku této instrukce).
A Jestliže inzulin po promíchání není vodný, stejnoměrně bílý a zakalený, pero nepoužívejte. Nasazení jehly D
Vezměte si novou jehlu a odtrhněte papírový kryt.
Našroubujte jehlu rovně a pevně na FlexPen.

E
Sejměte z jehly velký vnější kryt a uchovejte ho pro pozdější potřebu.

F
Sejměte z jehly vnitřní kryt a vyhoďte ho.
Nikdy se nepokoušejte vnitřní kryt jehly opět nasadit na jehlu. Mohl(a) byste se o jehlu píchnout.

A Pro každou aplikaci použijte vždy novou jehlu. Tím se sníží riziko kontaminace, infekce, úniku inzulinu, ucpání jehel a nepřesného dávkování.
A Dbejte, abyste jehlu před použitím neohnul(a) nebo jinak nepoškodil(a).
Ověření funkčnosti
Před každou injekcí se během normálního používání může v zásobní vložce nahromadit malé množství vzduchu. Abyste zabránil(a) vpíchnutí vzduchu a zajistil(a) správné dávkování, postupujte dle dále uvedených pokynů:
G
Otočte voličem dávky tak, abyste nastavil(a) 2 jednotky.

H
Držte FlexPen jehlou směrem nahoru a jemně na zásobní vložku několikrát poklepte prstem, aby se v horní části zásobní vložky nahromadily případné vzduchové bubliny.

I
Držte jehlu stále směrem vzhůru a stlačte úplně dávkovací tlačítko. Volič dávky se vrátí na nulu.
Na hrotu jehly se musí objevit kapka inzulinu. Jestliže se neobjeví, vyměňte jehlu a celý postup zopakujte, nejvíce však 6krát.
Jestliže se kapka inzulinu ani potom neobjeví, je pero vadné a musíte použít jiné.

A Vždy před podáním injekce zkontrolujte, zda se na špičce jehly objeví kapka. Tím se ujistíte, že inzulin protéká perem. Pokud se neobjeví žádná kapka, neaplikoval(a) byste si žádný inzulin, i když by se volič dávky pohyboval. Může to znamenat, že je jehla ucpaná nebo poškozená.
A Před aplikací vždy ověřte průtok. Pokud průtok neověříte, můžete si aplikovat inzulinu příliš málo, nebo si neaplikujete inzulin vůbec žádný. Může to vést k příliš vysoké hladině cukru v krvi.
Nastavení dávky
Zkontrolujte, zda je volič dávky nastaven na nule.
J
Otáčením voliče dávky nastavte požadovaný počet jednotek.
Dávku lze zmenšit nebo zvětšit otáčením voliče dávky příslušným směrem tak, aby správná dávka
byla proti značce v okénku ukazatele dávky. Při otáčení voličem dávky dbejte na to, abyste nestiskl(a)
dávkovací tlačítko, protože by inzulin unikal z pera.
Nemůžete nastavit vyšší dávku, než je počet jednotek zbývajících v zásobní vložce.

A Před aplikací inzulinu vždy pomocí voliče dávky a ukazatele dávky zkontrolujte, kolik jednotek jste zvolil(a).
A Nepočítejte cvakání pera. Pokud si zvolíte a aplikujete nesprávnou dávku, může Vám hladina cukru v krvi příliš stoupnout nebo příliš klesnout. Nepoužívejte stupnici ukazatele zbývajícího množství inzulinu - ukazuje pouze přibližné množství inzulinu zbývající ve vašem peru.
Aplikace injekce
Vpíchněte jehlu do kůže. Použijte injekční techniku, kterou vám doporučil váš lékař nebo
zdravotní sestra.
K
Dávku si vpíchněte stlačením dávkovacího tlačítka zcela dolů, až se v okénku ukazatele dávky objeví
proti značce nula. Dávejte pozor, abyste při vpichování injekce stiskl(a) pouze dávkovací tlačítko.
Otočením voliče dávky k aplikaci inzulínu nedojde.

L
► Držte dávkovači tlačítko zcela stlačené a nechte jehlu pod kůží alespoň po dobu 6 sekund.
Zajistíte tak, že bude podána celá dávka.
► Vytáhněte jehlu z kůže a potom uvolněte dávkovací tlačítko.
► Po aplikaci se vždy ujistěte, že se volič dávky vrátil na 0. Pokud se volič dávky zastaví dříve, než se vrátí na 0, nebyla aplikována celá dávka. To může mít za následek příliš vysokou hladinu cukru v krvi.

Jehlu zasuňte do velkého vnějšího krytu jehly, aniž byste se ho dotkl(a). Jakmile je jehla uvnitř, opatrně velký vnější kryt jehly zcela dotlačte a poté odšroubujte jehlu.
Opatrně ji vyhoďte a na pero FlexPen nasaďte zpět uzávěr pera.

A Po každé injekci jehlu vždy odstraňte a FlexPen skladujte bez nasazené jehly. Tím se sníží riziko kontaminace, infekce, úniku inzulinu, ucpání jehel a nepřesného dávkování.
Další důležité informace
A Pečující osoby musí být při manipulaci s použitými jehlami velice opatrné, aby se snížilo riziko poranění jehlou a přenesení infekce.
A Použitý FlexPen opatrně zlikvidujte bez připojené jehly.
A Pero ani jehly s nikým nesdílejte. Může to vést k přenosu infekce.
A Nikdy pero nesdílejte s dalšími osobami. Váš lék může jejich zdraví poškodit.
A Pero a jehly vždy uchovávejte mimo dohled a dosah ostatních, hlavně dětí.
151