Mirena
Jeden sterilní intrauterinm inzert obsahuje 52 mg levonorgestrelum
Pomocné látky: dimetikonový elastomer, dimetikonová trubička, polyethylen (obsahuje 20-24 % síranu
_barnatého), polyethylen pigmentovaný oxidem železitým a hydroxidem železa_
4. LÉKOVÁ FORMA A VELIKOST BALENÍ
Intrauterinní inzert
K zavedení do dělohy, zavedení musí provést lékař.
Před použitím si přečtěte přiloženou příbalovou informaci a pokyny pro zavádění.
Uchovávejte mimo dohled a dosah dětí.
Upozornění: Text na blistru je v rumunštině. Na blistru je přelepka s českým ekvivalentem textu.
Použitelné do:
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
Nepoužitelné léčivo vraťte do lékárny.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Držitel rozhodnutí o registraci referenčního přípravku v ČR:
Bayer OY, 20210 Turku, Finsko
Souběžný dovozce:
GlucoPharma s.r.o., Tvrdého 47, 199 00 Praha 9, Česká republika
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
17/372/97-C/PI/001/13
13. ČÍSLO ŠARŽE
Č. šarže:_
14. KLASIFIKACE PRO VÝDEJ
Výdej léku je vázaný na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
Mirena
Obrázek inzertu s textem: skutečná velikost Mireny
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Mirena 20 mikrogramů /24 hodin, sterilní intrauterinní inzert Levonorgestrelum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jeden sterilní intrauterinní inzert obsahuje 52 mg levonorgestrelum.
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: polyethylen, síran barnatý, hnědý oxid železitý, dimetikon.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
intrauterinní inzert
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
K zavedení do dělohy, zavedení musí provést lékař.
Tělísko je sterilní, pokud není pouzdro poškozené nebo otevřené.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Upozornění pro lékaře, který přípravek zavádí
> Tento systém nelze zasunovat opakovaně.
> Před zavedením si pečlivě přečtěte pokyny pro zavádění.
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
Nepoužitelné léčivo vraťte do lékárny.
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Bayer OY
20210 Turku, Finsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
17/372/97-C/PI/001/13
13. ČÍSLO ŠARŽE <, KÓD DÁRCE A KÓD LÉČIVÉHO PŘÍPRAVKU>
č.s.:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
Součástí balení je kartička s důležitými údaji pro pacientku (volně vložená v krabičce).
|
Jméno pacientky | |
|
C_) | |
|
Datum zavedení |
Nejpozdější datum vyjmutí |
|
C J C 3 | |
|
Kontaktní údaje lékaře | |
|
r | |
|
v |
razítko lékaře^/ |
POKYNY PRO ZAVÁDĚNÍ Mirena
20 ^g /24 hodin, intrauterinní inzert
Zavádění smí provádět pouze lékař za použití aseptické techniky.
Mirena je dodávána se zavaděčem ve sterilním balení, které se smí otevřít až těsně před zavedením. Znovu nesterilizujte. Mirena je určena pouze pro jednorázové použití. Nepoužívejte, pokud je vnitřní obal poškozený nebo otevřený. Nezavádějte po uplynutí doby použitelnosti (měsíc a rok) uvedené na štítku.
Informace o tom, kdy je možné zavádět Mirenu viz příbalová informace.
Příprava k zavedení
Proveďte vyšetření pacientky, abyste určili velikost a polohu dělohy a zjistili jakékoli příznaky akutní genitální infekce nebo jiné kontraindikace pro zavedení Mireny a vyloučili těhotenství.
Zastavte čípek do zrcadel a poté důkladně dezinfikujte čípek i pochvu vhodným antiseptickým roztokem.
Podle potřeby využijte asistenta
Přední okraj čípku uchopte vhodným držákem nebo kleštěmi a stabilizujte dělohu. Pokud je děloha zakloněna dozadu, může být vhodnější uchopit zadní okraj čípku. Jemným tahem za kleště napřímíte cervikální kanál. Kleště by měly zůstat ve stejné pozici a v průběhu zavádění udržovat jemný protitah za děložní hrdlo.
Postupujte děložní sondou přes kanál děložního hrdla až k fundu, abyste změřili hloubku a určili směr děložní dutiny a vyloučili přítomnost intrauterinních abnormalit (např. septum, submukózní fibroid) nebo již dříve zavedeného nitroděložního antikoncepčního přípravku, který nebyl vyjmutý. Pokud se vyskytnou problémy, zvažte dilataci děložního hrdla. Pokud je potřeba dilatace děložního hrdla, zvažte použití analgetik a/nebo paracervikálního bloku.
Zavedení
1. Nejdříve zcela otevřete sterilní obal (obrázek 1). Potom použijte sterilní techniku a sterilní rukavice.
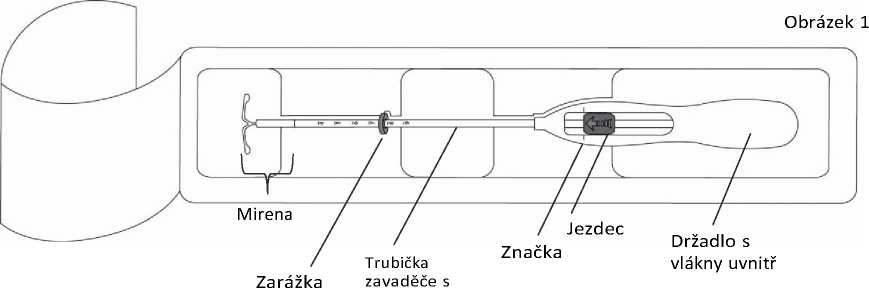
pístem a stupnicí
Obrázek 2

2. Posuňte jezdec dopředu ve směru šipky do nejvzdálenější polohy, abyste zasunuli Mirenu do trubičky zavaděče (obrázek 2).
DŮLEŽITÉ! Netahejte jezdec dolů, neboť by se takto mohla Mirena předčasně uvolnit. Jakmile se Mirena jednou uvolní, již ji nelze do trubičky znovu zasunout.
3. Držte jezdec v nejvzdálenější poloze, nastavte horní okraj zarážky tak, aby odpovídala odměřené
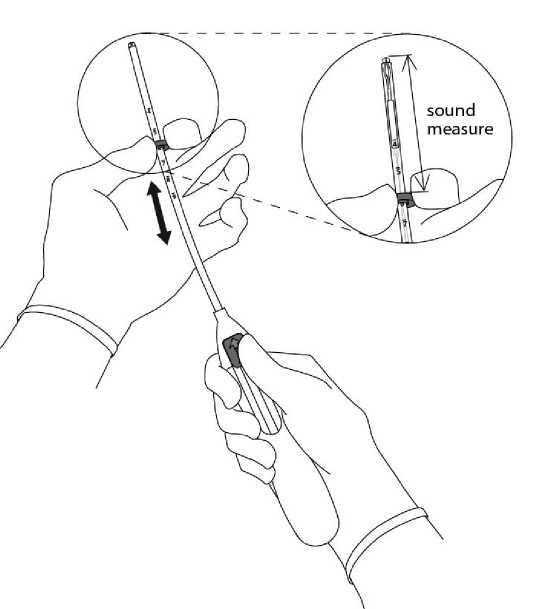
odměření sondou
Obrázek 4

vzdálenosti hloubky dělohy (obrázek 3).
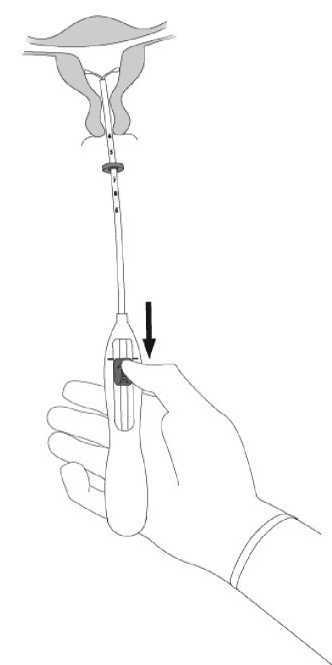
4. Zatímco držíte jezdec v nejvzdálenější poloze, zasunujte zavaděč přes děložní hrdlo, až bude zarážka ve vzdálenosti zhruba 1,5-2,0 cm od děložního hrdla (obrázek 4).
POZOR! Netlačte na zavaděč silou. Je-li nutné, dilatujte cervikální kanál.
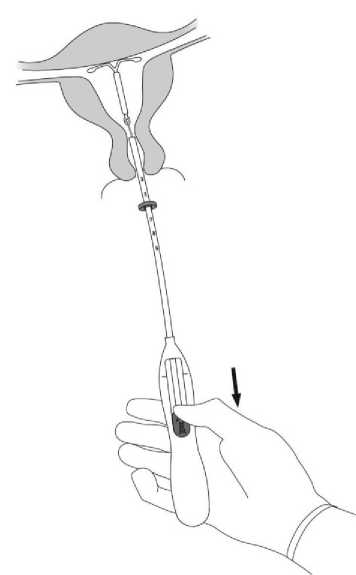
5. Zatímco držíte zavaděč na místě, uvolněte horizontální raménka Mireny přitažením jezdce zpět až ke značce (obrázek 5). Čekejte 5 až 10 vteřin, až se horizontální raménka zcela rozvinou.
Obrázek 6

6. Šetrně vtlačte zavaděč směrem k fundu dělohy, až se zarážka dotkne hrdla.
Nyní je Mirena ve fundu (obrázek 6).
7. Držte zavaděč na místě a uvolněte Mirenu úplným posunutím jezdce zpět dolů (obrázek 7). Zatímco držíte jezdec co nejníže, vytažením jemně vyjměte zavaděč. Vlákna zkraťte tak, aby 2 - 3 cm zůstaly viditelné vně děložního hrdla.
DŮLEŽITÉ! Pokud byste se domnívali, že systém není ve správné poloze, zkontrolujte jeho polohu (například ultrazvukem). Systém vyjměte, jestliže není správně umístěn v děložní dutině. Vyjmutý systém nesmí být znovu zaveden.
Vyjmutí/ výměna
Pro informace o vyjmutí/výměně si prosím přečtěte příbalovou informaci přiloženou k Mířené.
Obrázek 8
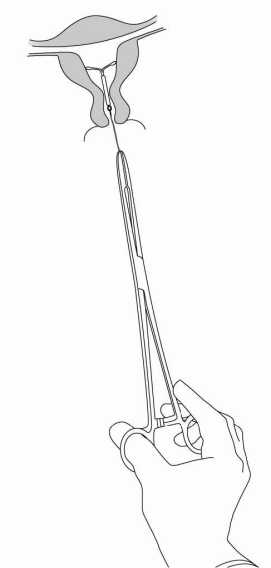
Mířenu můžete vyjmout peánem tažením za vlákna (obrázek 8).
Ihned po vyjmutí můžete zavést novou Mířenu.
VÝROBCE:
Bayer Oy, Pansíontíe 47,20210 Turku, Finsko SOUBĚŽNÝ DOVOZCE:
GlucoPharma s.r.o., Tvrdého 47, 199 00 Praha 9, Česká republika
DATUM REVIZE TEXTU: 18.5.2016
11