Mabthera 100 Mg
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
MabThera 100 mg koncentrát pro infuzní roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden ml obsahuje 10 mg rituximabum.
Jedna injekční lahvička obsahuje 100 mg rituximabum.
Rituximab je genetickým inženýrstvím získaná chimérická myší/lidská monoklonální protilátka. Jde o glykosylovaný imunoglobulin s lidskou IgG1 konstantní částí, zatímco variabilní části lehkých a těžkých řetězců jsou myšího původu. Protilátka je produkována suspenzí uměle kultivovaných savčích buněk (ovariální buňky čínských křečků) a je purifikována afinitní chromatografií a iontoměničem. Případně přítomné viry jsou v průběhu výroby odstraněny a inaktivovány.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Koncentrát pro infuzní roztok.
Čirý, bezbarvý roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek MabThera se používá k léčbě dospělých pacientů v následujících indikacích:
Nehodgkinské lymfomy (NHL)
Přípravek MabThera je indikován k léčbě dosud neléčených nemocných s folikulárním lymfomem III. a IV. klinického stádia v kombinaci s chemoterapií.
Udržovací léčba přípravkem MabThera je indikována k léčbě pacientů s folikulárním lymfomem, kteří odpovídají na indukční léčbu.
Přípravek MabThera v monoterapii je indikován k léčbě pacientů s folikulárním lymfomem III.- IV. klinického stádia, kteří se nacházejí ve druhém či dalším relapsu po chemoterapii nebo jejichž nádor je chemorezistentní.
Přípravek MabThera je v kombinaci s chemoterapií CHOP (cyklofosfamid, doxorubicin, vinkristin, prednizolon) indikován k léčbě nemocných s CD20 pozitivním difúzním velkobuněčným nehodgkinským maligním lymfomem z B buněk.
Chronická lymfocytární leukemie (CLL)
Přípravek MabThera je indikován v kombinaci s chemoterapií k léčbě pacientů s dříve neléčenou a relabující/refrakterní CLL. K dispozici jsou pouze omezené údaje týkající se účinnosti a bezpečnosti u pacientů dříve léčených monoklonálními protilátkami včetně přípravku MabThera nebo u pacientů nereagujících na předchozí léčbu přípravkem MabThera a chemoterapií.
Viz bod 5.1 pro další informace.
Revmatoidní artritida
Přípravek MabThera je v kombinaci s metotrexátem indikován k léčbě dospělých pacientů s těžkou aktivní revmatoidní artritidou, kteří na léčbu dalšími nemoc modifikujícími protirevmatickými léčivými přípravky (DMARD, disease-modifying anti-rheumatic drugs), včetně jedné či více terapií inhibitory tumor nekrotizujícího faktoru (TNF, tumour necrosis factor), odpovídali nedostatečně nebo léčbu netolerovali.
Bylo prokázáno, že přípravek MabThera, pokud se podává v kombinaci s metotrexátem, snižuje rychlost progrese kloubního poškození, měřeného pomocí RTG vyšetření, a zlepšuje fyzické funkce.
Granulomatóza s polyangiitidou a mikroskopická polyangiitida
Přípravek MabThera je v kombinaci s glukokortikoidy indikován k indukci remise u dospělých pacientů se závažnou aktivní granulomatózou s polyangiitidou (Wegenerova granulomatóza) (GPA) a mikroskopickou polyangiitidou (MPA).
4.2 Dávkování a způsob podání
Přípravek MabThera má být podáván pod pečlivým dohledem zkušeného zdravotnického pracovníka a v prostředí, kde je okamžitě dostupné úplné vybavení pro resuscitaci (viz bod 4.4).
Před každým podáním přípravku MabThera je vždy třeba podat premedikaci, kterou tvoří antipyretikum a antihistaminikum, např. paracetamol a difenhydramin.
U pacientů s nehodgkinským lymfomem a chronickou lymfocytární leukemií má být zvážena premedikace glukokortikoidy, pokud není přípravek MabThera podáván v kombinaci s chemoterapeutickým režimem obsahujícím glukokortikoidy.
U pacientů s revmatoidní artritidou je třeba ke snížení incidence a závažnosti reakcí souvisejících s infuzí podat premedikaci 100 mg methylprednisolonu intravenózně 30 minut před podáním infuze přípravku MabThera.
U pacientů s granulomatózou s polyangiitidou (Wegenerova granulomatóza) nebo mikroskopickou polyangiitidou se doporučuje intravenózní podání methylprednisolonu po dobu 1 až 3 dnů v dávce 1000 mg denně před podáním první infuze přípravku MabThera (poslední dávku methylprednisolonu lze podat ve stejný den jako první infuzi přípravku MabThera). Na intravenózní léčbu má navazovat perorální léčba prednisonem v dávce 1 mg/kg/den (celková denní dávka nesmí přesáhnout 80 mg a snižuje se tak rychle, jak je to na základě klinického stavu možné) a to v průběhu léčby přípravkem MabThera i po jejím ukončení.
Dávkování
Je důležité zkontrolovat označení přípravku a ujistit se, že je podáván správný přípravek (pro intravenózní nebo subkutánní podání), který byl pacientovi předepsán.
Nehodskinské lymfomy
Folikulární lymfom Kombinovaná léčba
Doporučená dávka přípravku MabThera v kombinaci s chemoterapií v rámci indukční léčby pacientů s dosud neléčeným nebo relabujícím/refrakterním folikulárním lymfomem je: 375 mg/m2 tělesného povrchu v každém cyklu, až do celkového počtu 8 cyklů.
Přípravek MabThera má být podáván v den 1 každého cyklu chemoterapie, po nitrožilním podání glukokortikoidu, pokud je součástí chemoterapeutického režimu.
Udržovací léčba
• Dosud neléčený folikulární lymfom
Doporučená dávka přípravku MabThera v udržovací léčbě pacientů s dosud neléčeným folikulárním lymfomem, kteří odpověděli na indukční léčbu, je: 375 mg/m2 tělesného povrchu jednou za 2 měsíce (zahájení udržovací léčby 2 měsíce po poslední dávce indukční léčby) do progrese nemoci či nejdéle po dobu dvou let.
• Relabující/refrakterní folikulární lymfom
Doporučená dávka přípravku MabThera v udržovací léčbě pacientů s relabujícím/refrakterním folikulárním lymfomem, kteří odpověděli na indukční léčbu, je: 375 mg/m2 tělesného povrchu jednou za 3 měsíce (zahájení udržovací léčby 3 měsíce po poslední dávce indukční léčby) do progrese nemoci či nejdéle po dobu dvou let.
Monoterapie
• Relabující/refrakterní folikulární lymfom
Doporučená dávka přípravku MabThera v monoterapii při indukční léčbě dospělých pacientů s folikulárním lymfomem stádia III-IV, jejichž nádor je chemorezistentní, či kteří se nacházejí v druhém či dalším relapsu po předchozí chemoterapii, je: 375 mg/m2 tělesného povrchu, podávaná jako nitrožilní infuze jednou týdně po dobu čtyř týdnů.
Pro opakovanou léčbu přípravkem MabThera v monoterapii u pacientů, kteří odpověděli na předchozí léčbu relabujícího/refrakterního folikulárního lymfomu monoterapií přípravkem MabThera, je doporučená dávka: 375 mg/m2 tělesného povrchu, podávaná jako nitrožilní infuze jednou týdně po dobu čtyř týdnů (viz bod 5.1).
Difúzní velkobuněčný nehodgkinský lymfom z B buněk
Přípravek MabThera by měl být použit v kombinaci s chemoterapií CHOP. Doporučená dávka přípravku, 375 mg/m2 tělesného povrchu, se podává 1. den každého z 8 chemoterapeutických cyklů po intravenózní aplikaci glukokortikoidu, který je součástí režimu CHOP. Bezpečnost a účinnost přípravku MabThera v kombinaci s jinými chemoterapeutickými režimy v léčbě difúzního B-velkobuněčného lymfomu nebyly dosud stanoveny.
Úprava dávkování v průběhu léčby
Redukce dávkování přípravku MabThera není doporučena. Při kombinaci přípravku MabThera s chemoterapií CHOP mohou být chemoterapeutika redukována podle standardních pravidel.
Chronická lymfocytární leukemie
K omezení rizika syndromu z rozpadu nádoru je u pacientů s CLL doporučována profylaxe s dostatečnou hydratací a podáním antiuratik zahájená 48 hodin před zahájením léčby. U pacientů s CLL s počtem lymfocytů vyšším než 25 x 109/l je doporučováno podání prednisonu/prednisolonu v dávce 100 mg intravenózně krátce před infuzí přípravku MabThera, aby se snížil výskyt a závažnost akutní reakce na infuzi a/nebo syndromu z uvolnění cytokinů.
Doporučená dávka přípravku MabThera v kombinaci s chemoterapií u dříve neléčených a relabujících/refrakterních pacientů je 375 mg/m2 tělesného povrchu v den 0 prvního cyklu léčby následovaná dávkou 500 mg/m2 tělesného povrchu podávanou v den 1 každého z následujících celkem 6 cyklů léčby. Chemoterapie by měla být podávána po infuzi přípravku MabThera.
Revmatoidní artritida
Pacientům léčeným přípravkem MabThera musí být při každé infuzi předána Karta pro pacienta.
Cyklus léčby spočívá v podání dvou intravenózních infuzí 1000 mg přípravku MabThera. Doporučená dávka 1000 mg přípravku MabThera podaná intravenózní infuzí je následována druhou intravenózní infuzí 1000 mg o dva týdny později.
Nutnost dalších cyklů léčby je třeba zhodnotit za 24 týdnů po předchozím cyklu. Opakovanou léčbu je třeba zahájit tehdy, pokud reziduální aktivita onemocnění přetrvává, v opačném případě je třeba opakování léčby odložit až do návratu aktivity onemocnění.
Dostupné údaje naznačují, že klinické odpovědi se obvykle dosáhne během 16 - 24 týdnů úvodního léčebného cyklu. U pacientů, kteří v průběhu tohoto období nevykazují žádné známky prospěchu z léčby, je třeba pokračování v léčbě pečlivě zvážit.
Granulomatóza s polyangiitidou a mikroskopická polyangiitida
Pacientům léčeným přípravkem MabThera musí být při každé infuzi předána Karta pro pacienta.
Doporučené dávkování přípravku MabThera při indukci remise v léčbě granulomatózy s polyangiitidou a mikroskopické polyangiitidy je 375 mg/m2 plochy tělesného povrchu podávané ve formě intravenózní infuze jednou týdně po dobu 4 týdnů (celkem 4 infuze).
U pacientů s granulomatózou s polyangiitidou nebo mikroskopickou polyangiitidou se během léčby přípravkem MabThera a po jejím ukončení (podle potřeby) doporučuje profylaxe pneumonie způsobené Pneumocystis jirovecii (PCP).
Zvláštní _ populace
Pediatrická populace
Účinnost a bezpečnost léčby přípravkem MabThera u dětí mladších 18 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
Starší pacienti
U starších pacientů (ve věku > 65 let) není zapotřebí žádná úprava dávkování.
Způsob podání
Připravený roztok MabThera má být podáván ve formě nitrožilní infuze samostatnou infuzní hadičkou. Neaplikujte připravený infuzní roztok jako nitrožilní injekci nebo bolus.
Pacienti by měli být pečlivě monitorováni s ohledem na možnost rozvoje syndromu z uvolnění cytokinů (viz bod 4.4). Pacientům, u nichž dojde k rozvoji těžkých reakcí, především těžké dušnosti, bronchospazmu nebo hypoxie, musí být infuze okamžitě zastavena. U pacientů s nehodgkinským lymfomem by měla být posouzena možnost vzniku syndromu z rozpadu tumoru, měly by být provedeny příslušné laboratorní testy a rentgenové vyšetření plic k průkazu možné plicní infiltrace. Podání infuzní terapie by u žádného pacienta nemělo být obnoveno dříve, než dojde k úplnému vymizení nežádoucích příznaků a k normalizaci laboratorních hodnot a RTG nálezu. Rychlost podání infuze přitom musí být poloviční nebo nižší než původní rychlost infuze. Pokud se znovu objeví stejné těžké nežádoucí účinky, mělo by být individuálně zváženo ukončení léčby.
Mírné až středně závažné nežádoucí účinky vznikající v důsledku podávání infuze (viz bod 4.8) obvykle odpovídají na snížení rychlosti infuze. Rychlost infuze může být po úpravě symptomů opět zvýšena.
První infuze
Doporučená úvodní rychlost infuze je 50 mg/hod; po prvních 30 minutách může být postupně zvyšována o 50 mg/hod, a takto lze postupně pokračovat vždy po 30 minutách až do maximální rychlosti 400 mg/hod.
Následné infuze
Všechny indikace
Následné dávky přípravku MabThera mohou být podávány úvodní rychlostí 100 mg/hod, a v 30minutových intervalech zvyšovány o 100 mg/hod až k nejvyšší rychlosti 400 mg/hod.
Informace týkající se pouze revmatoidní artritidy
Další možnost následného, zrychleného režimu infuze
Pacientům, u kterých se nevyskytly závažné nežádoucí účinky související s infuzí při podání první nebo následné infuze v dávce 1000 mg přípravku MabThera v rámci stanoveného plánu podávání, mohou být druhá a další následné infuze podány ve zrychleném režimu při použití stejné koncentrace jako u předchozích infuzí (4 mg/ml v objemu 250 ml). Počáteční rychlost infuze je 250 mg/hod prvních 30 minut a pak 600 mg/hod následujících 90 minut. Pokud je zrychlený režim infuze dobře snášen, tento režim infuze může být použit při podání následujících infuzí.
Pacientům, kteří mají klinicky významné kardiovaskulární onemocnění, včetně arytmie, nebo kteří prodělali závažné reakce na infuzi jakékoli dřívější biologické léčby nebo na rituximab, nesmí být zrychlený režim infuze podán.
4.3 Kontraindikace
Kontraindikace použití u nehodgkinských lymfomů a chronické lymfocytární leukemie
Hypersenzitivita na léčivou látku nebo na myší bílkoviny nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Aktivní, závažné infekce (viz bod 4.4).
Pacienti se závažným útlumem imunitního systému.
Kontraindikace použití u revmatoidní artritidy, granulomatózy s polyangiitidou a mikroskopické polvangiitidv
Hypersenzitivita na léčivou látku nebo na myší bílkoviny nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Aktivní, závažné infekce (viz bod 4.4).
Pacienti se závažným útlumem imunitního systému.
Těžké selhání srdce (třída IV dle New York Heart Association) nebo těžké, léčbou neupravené onemocnění srdce (další kardiovaskulární onemocnění, viz bod 4.4).
4.4 Zvláštní upozornění a opatření pro použití
Z důvodu snadnější zpětné zjistitelnosti biologických léčivých přípravků má být obchodní název a číslo šarže podávaného přípravku zřetelně zaznamenáno (nebo vyznačeno) v pacientově dokumentaci.
Progresivní multifokální leukoencefalopatie
Všem pacientům léčeným přípravkem MabThera z důvodu revmatoidní artritidy, granulomatózy s polyangiitidou a mikroskopické polyangiitidy musí být při každé infuzi předána Karta pro pacienta. Karta pro pacienta obsahuje důležité bezpečnostní informace pro pacienty týkající se možného zvýšení rizika infekcí, včetně progresivní multifokální leukoencefalopatie (PML).
Ve velmi vzácných případech byla po užití přípravku MabThera hlášena PML končící úmrtím.
Pacienti musí být v pravidelných intervalech sledováni pro jakékoli nové nebo zhoršující se neurologické symptomy nebo příznaky, které by mohly naznačovat PML. V případě podezření na PML musí být další podávání přípravku pozastaveno, dokud není diagnóza PML vyloučena. Lékař by měl vyhodnotit stav pacienta, aby bylo možno určit, zda příznaky ukazují na neurologickou dysfunkci, a v kladném případě, zda příznaky ukazují na PML. Dle klinické indikace by měla být zvážena konzultace s neurologem.
Při jakýchkoli pochybnostech by měla být zvážena další vyšetření včetně magnetické rezonance, přednostně s kontrastem, vyšetření mozkomíšního moku na JC virovou DNA a opakované neurologické vyšetření.
Lékař by měl věnovat zvláštní pozornost symptomům, které naznačují PML, ale kterých si pacient nemusí všimnout (např. kognitivní, neurologické nebo psychiatrické symptomy). Nemocnému by mělo být doporučeno, aby o léčbě informoval svého partnera nebo osobu, která o něho pečuje, protože ti si mohou všimnout příznaků, které sám nemocný nezaznamená.
Pokud dojde ke vniku PML, podávání přípravku MabThera musí být trvale ukončeno.
Po rekonstituci imunitního sytému u imunosuprimovaných nemocných s PML bylo možno pozorovat stabilizaci nebo zlepšení. Nadále není známo, zda časná detekce PML a ukončení léčby přípravkem MabThera může vést k podobné stabilizaci či zlepšení.
Nehodgkinské lymfomy a chronická lymfocytární leukemie
Reakce související s infuzí
Podání přípravku MabThera je spojeno s reakcemi souvisejícími s infuzí, které mohou souviset s uvolněním cytokinů a/nebo dalších chemických mediátorů. Syndrom z uvolnění cytokinů může být klinicky nerozeznatelný od akutních hypersenzitivních reakcí.
Tento soubor reakcí, které zahrnují syndrom z uvolnění cytokinů, syndrom nádorového rozpadu a anafylaktické či hypersenzitivní reakce, je popsán níže. Reakce nejsou specificky spojené s cestou podání přípravku MabThera a lze je pozorovat u obou forem.
Po uvedení přípravku na trh byly hlášeny závažné reakce související s infuzí, které končily úmrtím, při použití přípravku MabThera pro intravenózní podání s nástupem během 30 minut až 2 hodin po zahájení první intravenózní infuze přípravkem MabThera. Ty byly charakterizovány plicními příhodami a v některých případech zahrnovaly rychlý rozpad nádoru s rysy syndromu nádorového rozpadu, navíc horečku, zimnici, třesavku, hypotenzi, kopřivku, angioedém a další symptomy (viz bod 4.8).
Těžký syndrom z uvolnění cytokinů je charakterizován těžkou dušností, často doprovázenou bronchospazmem a hypoxií, dále horečkou, zimnicí, třesavkou, urtikou a angioedémem. Tento syndrom může být spojen s některými příznaky syndromu z rozpadu tumoru, jako jsou hyperurikémie, hyperkalémie, hypokalcémie, hyperfosfatémie, akutní renální selhání, zvýšení laktát dehydrogenázy (LDH), a může být spojen s akutním respiračním selháním a úmrtím pacienta. Akutní respirační selhání může být provázeno plicní intersticiální infiltrací nebo edémem plic, viditelným na rentgenovém vyšetření. Tento syndrom se často objevuje v průběhu jedné až dvou hodin po zahájení první infuze. U pacientů s anamnézou plicní insuficience nebo u pacientů s nádorovou infiltrací plic je větší nebezpečí nepříznivého průběhu, a proto by tito pacienti měli být léčeni se zvýšenou opatrností.
U pacientů, u kterých dojde k rozvoji těžkého syndromu z uvolnění cytokinů, musí být infuze okamžitě zastavena (viz bod 4.2) a musí u nich být zahájena intenzivní symptomatická léčba. Vzhledem k tomu, že počáteční zlepšení klinických příznaků může být následováno opětovným zhoršením celkového stavu, měli by být pacienti pečlivě monitorováni až do doby, kdy projevy syndromu z rozpadu tumoru a plicní infiltrace vymizí nebo tento syndrom je vyloučen. Další pokračování léčby po úplném vymizení příznaků vedlo vzácně k opakování těžkého syndromu z uvolnění cytokinů.
Pacienti s velkou nádorovou zátěží nebo s vysokým počtem (> 25 x 109/l) cirkulujících maligních buněk, jako jsou pacienti s CLL, u kterých může být zvýšené riziko zejména těžkého syndromu z uvolnění cytokinů, mají být léčeni s nejvyšší opatrností. Tito pacienti mají být velmi pečlivě monitorováni v průběhu první infuze. U těchto pacientů je třeba zvážit snížení rychlosti při podávání první infuze nebo rozdělení dávky v prvním a jakémkoli následujícím cyklu léčby do dvou dnů, pokud je počet lymfocytů stále >25 x 109/l.
Nežádoucí reakce všech typů vznikající v souvislosti s podáním infuze byly pozorovány u 77 % pacientů léčených přípravkem MabThera (včetně syndromu z uvolnění cytokinů doprovázeného hypotenzí a bronchospazmem u 10 % pacientů),viz bod 4.8. Tyto symptomy jsou obvykle reverzibilní po přerušení infuze přípravku a po podání antipyretik, antihistaminik, a podle potřeby po podání kyslíku, infuze fyziologického roztoku nebo bronchodilatancií a glukokortikoidů. Těžké reakce při syndromu z uvolnění cytokinů - viz výše.
Po intravenózním podání bílkovin pacientům byly hlášeny anafylaktické nebo jiné hypersenzitivní reakce. Na rozdíl od syndromu z uvolnění cytokinů se skutečná hypersenzitivní reakce objevuje typicky během několika minut po zahájení infuze. Pro případ rozvoje alergické reakce v průběhu podávání přípravku MabThera, musí být léčiva užívaná k léčbě hypersenzitivní reakce, např. epinefrin (adrenalin), antihistaminika a glukokortikoidy, ihned k dispozici. Klinické příznaky anafylaktické reakce mohou být podobné klinickým příznakům syndromu z uvolnění cytokinů (viz výše). Reakce z přecitlivělosti byly hlášeny méně často než reakce vznikající v souvislosti s uvolněním cytokinů.
Dalšími reakcemi hlášenými v některých případech byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie.
Vzhledem k tomu, že se v průběhu podání přípravku MabThera může objevit hypotenze, mělo by být zváženo přechodné vysazení antihypertenziv 12 hodin před infuzí přípravku MabThera.
Srdeční poruchy
U pacientů léčených přípravkem MabThera se objevily angina pectoris, srdeční arytmie typu fibrilace či flutter síní, srdeční selhání a/nebo infarkt myokardu. Pacienti s anamnézou srdečního onemocnění a/nebo kardiotoxickou chemoterapií mají proto být pečlivě monitorováni.
Hematologická toxicita
Přestože MabThera v monoterapii nepůsobí myelosupresivně, je u nemocných s počtem neutrofilů < 1,5 x 109/l a/nebo trombocytů < 75 x 109/l potřeba opatrnosti, vzhledem k tomu, že u této skupiny nemocných jsou jen malé zkušenosti s podáním přípravku MabThera. Přípravek MabThera byl podán 21 nemocným, kteří podstoupili autologní transplantaci kostní dřeně nebo jinak rizikovým nemocným s předpokládanou redukovanou funkcí kostní dřeně, aniž by byla vyvolána myelotoxicita.
Během léčby přípravkem MabThera je třeba pravidelně kontrolovat kompletní krevní obraz, včetně počtu neutrofilů a trombocytů.
Infekce
Během léčby přípravkem MabThera se mohou objevit závažná infekční onemocnění, včetně onemocnění vedoucích k úmrtí (viz bod 4.8) Přípravek MabThera by neměl být podáván pacientům s aktivním, závažným infekčním onemocněním (např. tuberkulózou, sepsí a oportunními infekcemi, viz bod 4.3).
Lékaři by měli pečlivě zvážit použití přípravku MabThera u pacientů s anamnézou opakovaných či chronických infekčních onemocnění či u pacientů s průvodními chorobami, které by mohly u pacientů dále přispět k náchylnosti k závažným infekčním chorobám (viz bod 4.8).
U pacientů léčených přípravkem MabThera byly popsány případy reaktivace hepatitidy B, včetně hlášení fulminantní hepatitidy s následným úmrtím. Většina těchto pacientů byla rovněž léčena cytotoxickou chemoterapií. Omezené množství informací z jedné studie s pacienty trpícími relabující/refrakterní CLL naznačuje, že léčba přípravkem MabThera by mohla také zhoršit primární infekci hepatitidou B. U všech pacientů má být před zahájením léčby přípravkem MabThera proveden screening na virus hepatitidy B (HBV). Screening má minimálně zahrnovat vyšetření HBsAg-statusu a HBcAb-statusu. Tato vyšetření mohou být doplněna dalšími vhodnými vyšetřeními v souladu s lokálními postupy. Pacienti s aktivním onemocněním hepatitidy B nemají být léčeni přípravkem MabThera. Pacienti se sérologicky pozitivní hepatitidou B (buď HBsAg nebo HBcAb) mají být před zahájením léčby odesláni na odborné vyšetření ke specialistovi na jaterní onemocnění, v průběhu léčby mají být tito pacienti pečlivě sledováni a léčeni v souladu s lokálními medicínskými postupy k prevenci reaktivace hepatitidy B.
U pacientů s NHL a CLL byly po uvedení přípravku MabThera na trh velmi vzácně hlášeny případy progresivní multifokální leukoencefalopatie (PML) (viz bod 4.8). Většina z pacientů dostávala přípravek MabThera v kombinaci s chemoterapií nebo jako součást transplantace krvetvorných kmenových buněk.
Očkování
Bezpečnost očkování živými virovými vakcínami po léčbě přípravkem MabThera nebyla u pacientů s NHL a CLL studována a očkování živými virovými vakcínami není doporučeno. Pacienti léčení přípravkem MabThera mohou podstoupit očkování neživými vakcínami. Účinnost očkování neživými vakcínami však může být nižší. V nerandomizované studii měli pacienti s relapsem nízce maligního NHL léčení monoterapií přípravkem MabThera ve srovnání se zdravými kontrolami nižší odpověď na přeočkování tetanem (16 % vs. 81 %) a očkování látkou Keyhole Limpet Haemocyanin (KLH) (4 % vs. 76 % při zjišťování dvojnásobného vzestupu titru protilátek). U pacientů s CLL je možné vzhledem k podobnosti obou chorob očekávat podobné výsledky, ale nebylo to dosud ověřeno v klinických studiích.
Průměrné hodnoty titrů protilátek proti panelu antigenů (Streptococcus pneumoniae, chřipka A, příušnice, zarděnky, plané neštovice) byly udrženy nejméně 6 měsíců po léčbě přípravkem MabThera.
Kožní reakce
Byly popsány závažné kožní reakce, jako je například toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím (viz bod 4.8). V případě výskytu takovéto příhody, s podezřením na souvislost s podáním přípravku MabThera, má být léčba trvale přerušena.
Revmatoidní artritida, granulomatóza s polyangiitidou a mikroskopická polyangiitida
Populace pacientů s revmatoidní artritidou, která dosud nebyla léčena metotrexátem (MTX)
Užití přípravku MabThera není doporučeno u pacientů, kteří dosud nebyli léčeni MTX, protože u nich nebylo potvrzeno, zda prospěch z léčby převáží její rizika.
Reakce související s infuzí
Podání přípravku MabThera je spojeno s reakcemi souvisejícími s infuzí (IRR, infusion related reaction), které mohou souviset s uvolněním cytokinů a/nebo dalších chemických mediátorů. Před každou infuzí přípravku MabThera je vždy třeba podat premedikaci, kterou tvoří analgetikum/antipyretikum a antihistaminikum. Ke snížení četnosti a závažnosti reakcí souvisejících s infuzí je třeba u pacientů s revmatoidní artritidou před každou infuzí přípravku MabThera rovněž provést premedikaci glukokortikoidy (viz bod 4.2 a bod 4.8).
U pacientů s revmatoidní artritidou byly po uvedení přípravku na trh hlášeny závažné reakce související s infuzí, které končily úmrtím. Většina příhod souvisejících s infuzí u pacientů s revmatoidní artritidou, které byly hlášeny v klinických studiích, byla mírné až střední závažnosti. Nejčastějšími příznaky byly alergické reakce jako bolest hlavy, svědění, podráždění v krku, návaly horka, vyrážka, kopřivka, hypertenze a pyrexie. Obecně byl podíl pacientů, u kterých se objevila jakákoli infuzní reakce, vyšší po první infuzi než po druhé infuzi jakéhokoli cyklu léčby. Incidence IRR klesala s následujícími cykly léčby (viz bod 4.8). Hlášené reakce byly obvykle reverzibilní po snížení rychlosti infuze nebo po přerušení infuze přípravku MabThera a po podání antipyretik a antihistaminik, podle potřeby po podání kyslíku, infuze fyziologického roztoku nebo bronchodilatancií a glukokortikoidů. Pacienty s preexistujícím kardiálním onemocněním a pacienty s anamnézou kardiopulmonálních nežádoucích účinků je nutné pečlivě sledovat. V závislosti na závažnosti reakce související s infuzí a požadovaném zásahu, je nutné dočasně nebo trvale ukončit léčbu přípravkem MabThera. V mnoha případech mohla být infuze obnovena při 50 % snížení rychlosti (např. ze 100 mg/h na 50 mg/h) po úplném vymizení nežádoucích příznaků.
Pro případ rozvoje alergické reakce v průběhu podávání přípravku MabThera musí být ihned k dispozici léčiva užívaná k léčbě hypersenzitivní reakce, např. epinefrin (adrenalin), antihistaminika a glukokortikoidy.
O bezpečnosti přípravku MabThera u pacientů se středně závažným srdečním selháním (třída III dle NYHA) nebo se závažným nekontrolovaným onemocněním srdce nejsou k dispozici žádné údaje. U pacientů léčených přípravkem MabThera, u nichž se současně vyskytovalo preexistující ischemické onemocnění srdce jako angina pectoris, infarkt myokardu a fibrilace či flutter síní, došlo k symptomatickému výskytu tohoto onemocnění. U pacientů s anamnézou srdečního onemocnění a pacientů s anamnézou kardiopulmonálních nežádoucích účinků má proto být před podáním přípravku MabThera zváženo riziko kardiovaskulárních komplikací způsobených infuzní reakcí a pacienti mají být během podávání infuze pečlivě monitorováni. Vzhledem k tomu, že se v průběhu podání infuze přípravku MabThera může objevit hypotenze, mělo by být zváženo přechodné vysazení antihypertenziv 12 hodin před infuzí přípravku MabThera.
Reakce související s infuzí byly u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou podobné reakcím pozorovaným v klinických studiích u pacientů s revmatoidní artritidou (viz bod 4.8).
Srdeční poruchy
U pacientů léčených přípravkem MabThera se objevily angina pectoris, srdeční arytmie typu fibrilace či flutter síní, srdeční selhání a/nebo infarkt myokardu. Pacienti s anamnézou srdečního onemocnění mají proto být pečlivě monitorováni (viz výše Reakce související s infuzí).
Infekce
Na základě mechanismu účinku přípravku MabThera a znalosti, že B-buňky hrají důležitou roli v udržování normální imunitní odpovědi, může u pacientů po léčbě přípravkem MabThera dojít ke zvýšení rizika infekce (viz bod 5.1). Během terapie přípravkem MabThera se mohou vyskytnout závažné infekce, včetně případů s fatálním průběhem (viz bod 4.8). Přípravek MabThera by neměl být podáván pacientům s akutní závažnou infekcí (např. tuberkulóza, sepse a oportunní infekce, viz bod 4.3) nebo pacientům se sníženou funkcí imunitního systému (např. při velmi nízkém počtu CD4 a CD8). Lékaři musí pečlivě zvážit použití přípravku MabThera u pacientů s anamnézou chronických infekcí nebo v podmínkách, které mohou zvýšit náchylnost pacientů k vážným infekcím, např. hypogamaglobulinémii (viz bod 4.8). Před zahájením léčby přípravkem MabThera se doporučuje stanovit hladiny imunoglobulinů.
Pacienti vykazující známky a symptomy infekce po léčbě přípravkem MabThera by měli být okamžitě vyšetřeni a vhodně léčeni. Před podáním dalšího cyklu léčby přípravkem MabThera by u pacientů mělo být znovu posouzeno potenciální riziko infekce.
Po podávání přípravku MabThera k léčbě revmatoidní artritidy a autoimunitních onemocnění, včetně systémového lupus erytematodes (SLE) a vaskulitidy, byly velmi vzácně zaznamenány případy fatální progresivní multifokální leukoencefalopatie (PML).
Infekce hepatitidy B
U pacientů s revmatoidní artritidou, granulomatózou s polyangiitidou a mikroskopickou polyangiitidou léčených přípravkem MabThera byly hlášeny případy reaktivace hepatitidy B, včetně těch, které končily úmrtím.
U všech pacientů má být před zahájením léčby přípravkem MabThera proveden screening na virus hepatitidy B (HBV). Screening má minimálně zahrnovat vyšetření HBsAg-statusu a HBcAb-statusu. Tato vyšetření mohou být doplněna dalšími vhodnými vyšetřeními v souladu s lokálními postupy. Pacienti s aktivním onemocněním hepatitidy B nemají být léčeni přípravkem MabThera. Pacienti se sérologicky pozitivní hepatitidou B (buď HBsAg nebo HBcAb) mají být před zahájením léčby odesláni na odborné vyšetření ke specialistovi na jaterní onemocnění, v průběhu léčby mají být tito pacienti pečlivě sledováni a léčeni v souladu s lokálními medicínskými postupy k prevenci reaktivace hepatitidy B.
Pozdní neutropenie
Je třeba měření neutrofilů v krvi před každým cyklem léčby přípravkem MabThera a pravidelně až po dobu 6 měsíců po ukončení léčby a při známkách nebo příznacích infekce (viz bod 4.8).
Kožní reakce
Byly popsány závažné kožní reakce, jako je například toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím (viz bod 4.8). V případě výskytu takovéto příhody, s podezřením na souvislost s podáním přípravku MabThera, má být léčba trvale přerušena.
Očkování
Lékaři by před zahájením léčby přípravkem MabThera měli posoudit stav očkování pacienta a držet se stávajících očkovacích doporučení. Očkování by mělo být dokončeno nejméně 4 týdny před prvním podáním přípravku MabThera.
Bezpečnost očkování živými virovými vakcínami po léčbě přípravkem MabThera nebyla studována. Proto není doporučeno očkování živými virovými vakcínami během léčby přípravkem MabThera a po dobu deplece B-lymfocytů v periferní krvi.
Pacienti léčení přípravkem MabThera mohou podstoupit očkování neživými vakcínami. Účinnost očkování neživými vakcínami však může být nižší. V randomizované studii měli pacienti s revmatoidní artritidou léčení přípravkem MabThera a metotrexátem ve srovnání s pacienty léčenými pouze metotrexátem srovnatelnou odpověď na přeočkování tetanem (39 % vs. 42 %), nižší četnost odpovědí na pneumokokovou polysacharidovou vakcínu (43 % vs. 82 % na alespoň 2 sérotypy pneumokokových protilátek) a očkování antigenem KLH (47 % vs. 93 %) pokud byly podávány 6 měsíců po léčbě přípravkem MabThera. Pokud je potřeba během léčby přípravkem MabThera provést očkování neživou vakcínou, toto očkování by mělo být dokončeno alespoň 4 týdny před dalším cyklem léčby přípravkem MabThera.
Celkově byl u revmatoidní artritidy po opakované léčbě přípravkem MabThera po dobu delší než 1 rok podíl pacientů s pozitivními titry protilátek proti S. pneumoniae, chřipce, spalničkám, zarděnkám, planým neštovicím a tetanovému anatoxinu v zásadě podobný s podíly při zahájení léčby.
Současné/následné užívání jiných DMARD u pacientů s revmatoidní artritidou
Současné užívání přípravku MabThera a protirevmatických terapií jiných, než jsou ty uvedené pod
indikací revmatoidní artritida, se nedoporučuje.
Jsou pouze omezené údaje z klinických studií, které by umožnily plně zhodnotit bezpečnost následného použití DMARDs (včetně inhibitorů TNF a jiných biologických látek) po léčbě přípravkem MabThera (viz bod 4.5). Dostupná data naznačují, že výskyt klinicky významné infekce se při této léčbě u pacientů dříve léčených přípravkem MabThera nemění, pokud jsou však pacienti po léčbě přípravkem MabThera léčeni biologickými léky a/nebo DMARDs, měli by být pečlivě sledováni kvůli příznakům infekce.
Maligní onemocnění
Imunomodulační látky mohou zvyšovat riziko vzniku malignit. Na základě omezených zkušeností s podáváním přípravku MabThera pacientům s revmatoidní artritidou (viz bod 4.8) se nezdá, že by dostupné údaje nasvědčovaly jakémukoli zvýšení rizika vzniku malignit. Možné riziko rozvoje solidních tumorů však nelze v současné době vyloučit.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
V současné době jsou k dispozici pouze omezené údaje o možných lékových interakcích s přípravkem MabThera.
U pacientů s CLL, kterým byl spolu s přípravkem MabThera podáván fludarabin nebo cyklofosfamid, nebyl pozorován žádný účinek na jejich farmakokinetiku. Kromě toho nebyl pozorován žádný zjevný účinek fludarabinu a cyklofosfamidu na farmakokinetiku přípravku MabThera.
U pacientů s revmatoidní artritidou nemělo současné podávání metotrexátu žádný vliv na farmakokinetiku přípravku MabThera.
Nemocní s protilátkami proti myším bílkovinám (HAMA) nebo s protilátkami proti chimérickým protilátkám (HACA) mohou mít hypersenzitivní nebo alergické reakce při podání jiných diagnostických nebo léčebných monoklonálních protilátek.
283 pacientů s revmatoidní artritidou dostávalo po léčbě přípravkem MabThera následnou léčbu DMARD. U těchto pacientů byl výskyt klinicky významných infekcí během léčby přípravkem MabThera 6,01 na 100 paciento-roků ve srovnání s 4,97 na 100 paciento-roků během léčby biologickým DMARD.
4.6 Fertilita, těhotenství a kojení
Antikoncepce u mužů a žen
Vzhledem k tomu, že rituximab zůstává v těle pacientů s deplecí B buněk po delší dobu, musí ženy ve fertilním věku během léčby přípravkem MabThera a 12 měsíců po jejím ukončení používat efektivní antikoncepční metody.
Je známo, že imunoglobuliny IgG přecházejí přes placentární bariéru.
Počet B lymfocytů u lidských novorozenců po podání přípravku MabThera matce nebylo v klinických hodnoceních studováno. Neexistují žádné dostatečné a dobře kontrolované údaje ze studií u těhotných žen, avšak u některých dětí narozených matkám vystaveným v průběhu těhotenství přípravku MabThera byly hlášeny přechodná deplece B buněk a lymfocytopenie. Podobné účinky byly pozorovány ve studiích na zvířatech (viz bod 5.3). Z těchto důvodů by neměla být MabThera podávána těhotným ženám s výjimkou situace, kdy možný prospěch převáží potencionální riziko.
Kojení
Není známo, zda je rituximab vylučován do lidského mléka. Vzhledem k tomu, že mateřské IgG vylučováno je, a u kojících opic byl rituximab v mléku detekován, neměly by ženy léčené přípravkem MabThera kojit během léčby a 12 měsíců po léčbě přípravkem MabThera.
Fertilita
Studie na zvířatech neprokázaly škodlivé účinky rituximabu na reprodukční orgány.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly prováděny žádné studie hodnotící účinky přípravku MabThera na schopnost řídit a obsluhovat stroje, nicméně farmakologická aktivita a dosud hlášené nežádoucí účinky ukazují, že přípravek MabThera nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Zkušenosti u nehodgkinských lymfomů a chronické lymfocytární leukemie
Shrnutí bezpečnostního _profilu
Celkový bezpečností profil přípravku MabThera je u nehodgkinských lymfomů a chronické lymfocytární leukemie založen na údajích pacientů z klinických studií a postmarketingového pozorování. Tito pacienti byli léčeni buď přípravkem MabThera v monoterapii (jako indukční léčbou nebo udržovací léčbou po indukční léčbě) nebo v kombinaci s chemoterapií.
Nej častěji pozorovanými nežádoucími účinky na lék u pacientů, kteří dostávali přípravek MabThera, byly reakce související s podáním infuze, které se u většiny pacientů objevily v průběhu první infuze. Incidence příznaků souvisejících s podáním infuze se významně snižuje u následujících infuzí a po osmi dávkách přípravku MabThera je nižší než 1 %.
K infekčním příhodám (zejména bakteriálním a virovým) došlo u přibližně 30-55 % pacientů v průběhu klinických studií u pacientů s nehodgkinskými lymfomy a u 30-50 % pacientů v klinických studiích u pacientů s CLL.
Nejčastějšími závažnými nežádoucími účinky na lék byly:
• Reakce související s podáním infuze (včetně syndromu z uvolnění cytokinů, syndromu z rozpadu tumoru), viz bod 4.4.
• Infekce, viz bod 4.4.
• Kardiovaskulární události, viz bod 4.4.
Dalšími závažnými hlášenými nežádoucími účinky na lék byly reaktivace hepatitidy B a PML (viz bod 4.4.)
Shrnutí nežádoucích účinků do tabulky
Četnosti nežádoucích účinků léčivého přípravku (NÚ), které byly hlášeny v souvislosti s podáním samotného přípravku MabThera nebo v kombinaci s chemoterapií, jsou shrnuty v Tabulce 1. Ve všech skupinách četností jsou NÚ prezentovány v pořadí podle klesající závažnosti. Četnost je definována jako velmi častá (>1/10), častá (>1/100 až <1/10), méně častá (>1/1000 až <1/100), vzácná (>1/10000 až <1/1000), velmi vzácná (<1/10000) a není známo (z dostupných údajů nelze určit).
Nežádoucí účinky, které byly zjištěny pouze v postmarketingových pozorováních a u nichž nelze určit četnost, jsou uvedeny jako „není známo“.
v postmarketingovém pozorování u pacientů s nehodgkinským lymfomem léčených přípravkem MabThera monoterapií/udržovací léčbou nebo v kombinaci s chemoterapií ___
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Infekce a infestace |
bakteriální infekce, virové infekce, +bronchitida |
sepse, +pneumonie, +febrilní infekce, +herpes zoster, +infekce dechových cest, plísňové infekce, infekce neznámého původu, +akutní bronchitida, +sinusitida, hepatitida B1 |
závažné virové infekce2 Pmeumocystis jirovecii |
PML | ||
|
Poruchy krve a lymfatického systému |
neutropenie, leukopenie, +febrilní neutropenie +trombocytopenie |
+pancytopenie, +granulocytopenie |
poruchy srážlivosti, přechodná aplastická anémie, hemolytická lymfadenopatie |
přechodný vzestup hladin sérových IgM3 |
pozdní neutropenie3 | |
|
Poruchy imunitního systému |
rekace spojené s podáním, angioedém |
hypersensitivita |
anafylaxe |
syndrom rozpadu nádoru, syndrom z uvolnění cytokinů4, sérová nemoc |
akutní reverzibilní trombocyto- penie související s podáním infuze4 | |
|
Poruchy metabolismu a výživy |
hyperglykémie, pokles hmotnosti, periferní edém, otok obličeje, vzestup LDH, hypokalcémie | |||||
|
Psychiatrické poruchy | ||||||
|
Poruchy nervového systému |
parestézie, hypestézie, agitovanost, vasodilatace, závratě, úzkost |
porucha vnímání chuti |
periferní neuropatie, paresa lícního nervu5 |
kraniální neuropatie, jiné smyslové poruchy5 | ||
|
Poruchy oka |
poruchy slzení, konjunktivitida |
závažná porucha zraku5 | ||||
|
Poruchy ucha a labyrintu |
tinnitus, bolest uší |
porucha sluchu5 | ||||
|
Srdeční poruchy |
+infarkt myokardu4 a 6, arytmie, +fibrilace síní, tachykardie, +srdeční porucha |
+levostranné srdeční selhání, +supraventrikulární tachykardie, +komorová tachykardie, +angina pectoris, +ischemie myokardu, bradykardie |
závažné kardiální poruchy4 a 6 |
srdeční selhání4 a 6 | ||
|
Cévní poruchy |
hypertenze, ortostatická |
vaskulitida (zejména kožní), leuko-cytoklastická vaskulitida |
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Respirační, hrudní a mediastinální poruchy |
Broncho spasmus4, dechové choroby, bolest na hrudi, dušnost, zhoršení kašle, rýma |
astma, obliterující bronchiolitida, plicní poruchy, hypoxie |
intersticiální plicní 7 onemocnění |
respirační selhání4 |
plicní infiltrace | |
|
Gastrointesti-nální poruchy |
zvracení, průjem, bolesti břicha, dysfágie, stomatitida, zácpa, dyspepsie, nechutenství, podráždění hltanu |
zduření břicha |
gastrointesti- nální perforace7 | |||
|
Poruchy kůže a podkožní tkáně |
kopřivka, pocení, noční poty, +kožní onemocnění |
závažné bulózní kožní reakce, Stevens- Johnsonův syndrom, toxická epidermální nekrolýza (Lyellův syndrom)7 | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
hypertonie, myalgie, bolesti kloubů, bolesti zad, bolesti krku, bolest | |||||
|
Poruchy ledvin a močových cest |
renální selhání4 | |||||
|
Celkové poruchy a reakce v místě aplikace |
bolest nádoru, zrudnutí, únava, příznaky nachlazení, +multiorgánové selhání4 |
bolest v místě infuze | ||||
|
Vyšetření |
pokles hladin IgG | |||||
|
Pro každý příznak byla četnost stanovena na základě výskytu reakcí všech stupňů (lehké až závažné) s výjimkou příznaků označených "+", u kterých byla četnost stanovena na základě závažných reakcí (stupeň > 3 dle obecných kritérií toxicity NCI). Jsou uvedeny pouze nejvyšší četnosti ve studiích. 1 zahrnuje reaktivaci a primární infekce; frekvence je založena na R-FC režimu u relabující/refrakterní CLL 2 viz též níže uvedený odstavec infekce 3 viz též níže uvedený odstavec hematologické nežádoucí reakce 4 viz též níže uvedený odstavec účinky spojené s podáním infuze. Vzácně byly hlášeny fatální případy 5 příznaky kraniální neuropatie. Objevily se v různou dobu nejvýše za několik měsíců po ukončení léčby přípravkem MabThera 6 pozorováno zejména u pacientů s předchozím kardiálním onemocněním a/nebo kardiotoxickou chemoterapií a byly většinou spjaty s účinky spojenými s podáním infuze 7 včetně fatálních případů | ||||||
Následující pojmy byly uváděny jako nežádoucí příhody v průběhu klinických studií, jejich četnost však byla ve skupinách pacientů s přípravkem MabThera podobná nebo nižší než v kontrolních skupinách: hematotoxicita, neutropenické infekce, infekce močových cest, poruchy čití, horečka.
U více než 50 % pacientů v klinických studiích byly hlášeny příznaky, které byly suspektní jako účinky spojené s podáním infuze a byly zejména pozorovány v průběhu první infuze, většinou v první nebo v prvých dvou hodinách. Tyto příznaky byly většinou horečka, zimnice a ztuhlost. Mezi další příznaky patří zrudnutí, angioedém, bronchospasmus, zvracení, nevolnost, kopřivka/vyrážka, únava, bolest hlavy, podráždění hltanu, rýma, svědění, bolest, tachykardie, hypertenze, hypotenze, dušnost, dyspepsie, slabost a známky syndrome rozpadu nádoru. Závažné účinky spojené s podáním infuze (například bronchospasmus, hypotense) se vyskytly až u 12 % případů. Další reakce, které byly v několika případech hlášeny, byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie. S nižší nebo neznámou četností byly hlášeny exacerbace již existujících kardiálních onemocnění, jako jsou angina pectoris nebo městnavé srdeční selhání nebo závažné kardiální poruchy (srdeční selhání, infarkt myokardu, fibrilace síní), edém plic, multiorgánové selhání, příznak rozpadu tumoru, příznak uvolnění cytokinů, renální selhání a respirační selhání. Incidence účinků spojených s podáním infuze se významně snížila u následujících infuzí a je <1 % pacientů při osmém cyklu léčby obsahující přípravek MabThera.
Popis vybraných nežádoucích účinků
Infekce
I když přípravek MabThera způsobuje depleci B-lymfocytů u 70 % až 80 % pacientů, snížení sérových koncentrací imunoglobulinů se vyskytuje jen u malého počtu pacientů.
V randomizovaných studiích byly v ramenech obsahujících přípravek MabThera s vyšší četností hlášeny lokalizované infekce kandidou a herpes zoster. Závažné infekce byly hlášeny u asi 4 % pacientů léčených přípravkem MabThera v monoterapii. V průběhu udržovací léčby přípravkem MabThera až po dobu dvou let byly pozorovány vyšší četnosti infekcí celkové, včetně infekcí stupně 3 a 4 ve srovnání s obdobím observace. Po dobu dvouletého léčebného období nebyla hlášena žádná kumulativní toxicita z hlediska infekce. Dále byly hlášeny při léčbě přípravkem MabThera jiné závažné virové infekce buď nové, reaktivované nebo exacerbované, z nichž některé byly fatální. Většina pacientů dostávala přípravek MabThera v kombinaci s chemoterapií nebo jako součást transplantace hematopoetických kmenových buněk. Příklady těchto závažných virových infekcí jsou infekce způsobené herpetickými viry (cytomegalovirem, virem varicella zoster a herpes simplex virem), JC virem (progresivní multifokální leukoencefalopatie (PML)) a virem hepatitidy C.
V klinických studiích byly rovněž zaznamenány případy fatální PML, které se objevily po progresi onemocnění a jeho opakované léčbě. Byly hlášeny případy reaktivace hepatitidy B, z nichž většina byla u pacientů, kteří dostávali přípravek MabThera v kombinaci s cytotoxickou chemoterapií. U pacientů s relabující/refrakterní CLL byla incidence infekce 3/4. stupně hepatitidy B (reaktivace a primární infekce) 2 % u R-FC oproti 0 % u FC. Byla pozorována progrese Kaposiho sarkomu u pacientů vystavených přípravku MabThera, kteří již dříve trpěli Kaposiho sarkomem. Tyto případy se vyskytly u neschválených indikací a většina pacientů byla HIV pozitivní.
Hematologické nežádoucí účinky
V klinických studiích s monoterapií přípravkem MabThera podávaným po dobu 4 týdnů se u malého počtu pacientů vyskytly hematologické abnormality a byly většinou mírné a reverzibilní. Závažné (stupně 3/4) neutropenie byly hlášeny u 4,2 %, anémie u 1,1 % a trombocytopenie u 1,7 % pacientů. V průběhu udržovací léčby přípravkem MabThera po dobu až dvou let byly hlášeny leukopenie (5 % oproti 2 %, stupně 3/4) a neutropenie (10 % oproti.4 %, stupně 3/4) s vyšší incidencí oproti pouhému sledování. Incidence trombocytopenie byla nízká (<1 %, stupně 3/4) a nelišila se mezi jednotlivými léčebnými rameny. V průběhu léčebného cyklu ve studiích s přípravkem MabThera v kombinaci s chemoterapií byly hlášeny leukopenie stupně 3/4 (R-CHOP 88 % oproti CHOP 79 %, R-FC 23 % oproti FC 12 %), neutropenie (R-CVP 24 % oproti CVP 14 %; R-CHOP 97 % oproti CHOP 88 %, R-FC 30 % oproti FC 19 % u doposud neléčené CLL), pancytopenie (R-FC 3 % oproti FC 1 % u doposud neléčené CLL) s obvykle vyšší četností v porovnání se samotnou chemoterapií. Vyšší incidence neutropenie u pacientů léčených přípravkem MabThera a chemoterapií však nebyla spojena s vyšší incidencí infekcí a infestací v porovnání s pacienty léčenými samotnou chemoterapií. Studie u dosud neléčené a relabující/refrakterní CLL ukázaly, že až u 25 % pacientů léčených s R-FC byla neutropenie po léčbě přípravkem MabThera plus FC prolongovaná (definováno jako počet neutrofilů zůstávajících pod hodnotou 1x109/l mezi dnem 24 a 42 po poslední dávce) nebo se projevila opožděně (definováno jako počet neutrofilů pod hodnotou 1x109/l později než 42 dnů po poslední dávce u pacientů, u kterých se dříve prolongovaná neutropenie neprojevila nebo u těch, u kterých došlo ke znovuobjevení před dnem 42). Nebyly hlášeny žádné rozdíly v incidenci anémie. Některé případy pozdní neutropenie se objevily více než 4 týdny po poslední infuzi přípravku MabThera. Ve studii u pacientů s CLL ve stádiu C podle Bineta, kterým byl přípravek podáván jako lék první linie léčby, bylo zaznamenáno více nežádoucích účinků ve skupině R-FC v porovnání se skupinou FC (R-FC
83 % vs. FC 71 %). Ve studii s relabující/refrakterní CLL byla trombocytopenie stupně 3/4 zaznamenána u 11 % pacientů v R-FC skupině v porovnání s 9 % pacientů v FC skupině.
Ve studiích s přípravkem MabThera u pacientů s Waldenstromovou makroglobulinemií byly pozorovány přechodné vzestupy hladin sérových IgM po zahájení léčby, které mohou být spojeny s hyperviskozitou a souvisejícími příznaky. Přechodný vzestup IgM se většinou vrátil minimálně k hladině při zahájení v rozmezí 4 měsíců.
Kardiovaskulární nežádoucí účinky
V průběhu klinických studií s monoterapií přípravkem MabThera byly hlášeny kardiovaskulární příhody u 18,8 % pacientů, přičemž nejčastěji hlášenými událostmi byly hypotenze a hypertenze.
V průběhu infuze byly hlášeny případy arytmie stupně 3 nebo 4 (včetně ventrikulární a supraventrikulární tachykardie). V průběhu udržovací léčby byla incidence kardiálních onemocnění stupně 3/4 srovnatelná u pacientů léčených přípravkem MabThera a u pacientů pouze sledovaných. Jako závažné nežádoucí události (včetně fibrilace síní, infarktu myokardu, levostranného komorového selhání a myokardiální ischémie) byly hlášeny kardiální události u 3 % pacientů léčených přípravkem MabThera ve srovnání s <1 % u sledování. Ve studiích hodnotících přípravek MabThera v kombinaci
s chemoterapií byla incidence kardiálních arytmií stupně 3 a 4, především supraventrikulárních arytmií jako je tachykardie a síňový flutter/fibrilace vyšší ve skupině R-CHOP (14 pacientů, 6,9 %) ve srovnání se skupinou CHOP (3 pacienti, 1,5 %). Všechny tyto arytmie se buď vyskytly v souvislosti s infuzí přípravku MabThera nebo souvisely s predisponujícími podmínkami, jako byly horečka, infekce, akutní infarkt myokardu nebo již existujících respiračních a kardiovaskulárních onemocnění. Nebyly pozorovány žádné rozdíly mezi skupinami R-CHOP a CHOP v incidenci jiných kardiálních událostí stupně 3 a 4 včetně srdečního selhání, infarktu myokardu a manifestace onemocnění koronárních tepen. U CLL byl celkový výskyt srdečních chorob stupně 3 nebo 4 nízký jak ve studii s první linií léčby (4 % R-FC, 3 % FC), tak ve studii s relabující/refrakterní CLL (R-FC 4 %, FC 4 %).
Respirační systém
Byly hlášeny případy intersticiálního plicního onemocnění, některé s fatálním zakončením.
Neurologické poruchy
V průběhu léčebného období (indukční fáze léčby zahrnující R-CHOP pro maximálně 8 cyklů), čtyři pacienti (2 %) léčení ve skupině R-CHOP všichni s kardiovaskulárními rizikovými faktory, prodělali během prvního léčebného cyklu tromboembolickou cerebrovaskulární příhodu. Ve výskytu dalších tromboembolických příhod nebyl mezi skupinami žádný rozdíl. Naopak, tři pacienti (1,5 %) v rameni CHOP měli cerebrovaskulární příhodu, u všech se objevila v období následného pozorování. U CLL byl celkový výskyt poruch nervového systému stupně 3 nebo 4 nízký jak ve studii s první linií léčby (4 % R-FC, 4 % FC), tak ve studii s relabující/refrakterní CLL (R-FC 3 %, FC 3%).
Byly hlášeny případy syndromu posteriorní reverzibilní encefalopatie (PRES)/syndromu reverzibilní posteriorní leukoencefalopatie (RPLS). Známky a příznaky zahrnovaly zrakové poruchy, bolest hlavy, křeče a psychické poruchy, s nebo bez průvodní hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovacím vyšetřením mozku. U hlášených případů byly zaznamenány rizikové faktory PRES/RPLS, které zahrnují průvodní onemocnění pacienta, hypertenzi, imunosupresivní léčbu a/nebo chemoterapii.
Gastrointestinální onemocnění
Gastrointestinální perforace v některých případech vedoucí k úmrtí byly pozorovány u pacientů, kteří dostávali přípravek MabThera v léčbě nehodgkinského lymfomu. Ve většině těchto případů byla MabThera podávána s chemoterapií.
Hladiny IgG
V klinických studiích hodnotících udržovací léčbu přípravkem MabThera u relabujícího/refrakterního folikulárního lymfomu byly po indukční léčbě střední hladiny IgG pod dolní hranicí normy (LLN)
(< 7 g/l) v rameni s pouhým sledováním i v rameni s přípravkem MabThera. V rameni se sledováním došlo následně k vzestupu střední hladiny IgG nad LLN, ale v rameni s přípravkem MabThera zůstaly nezměněny. Podíl pacientů se střední hladinou IgG pod LNN byl v rameni s přípravkem MabThera přibližně 60 % po celou dobu 2letého léčebného období, zatímco v rameni se sledováním tento podíl poklesl (36 % po 2 letech).
Nízký počet spontánních a v literatuře popsaných případů hypogamaglobulinemie byl pozorován u pediatrických pacientů léčených přípravkem MabThera, v některých případech závažných a vyžadujících dlouhodobou substituční terapii imunoglobuliny. Následky dlouhodobé deplece B buněk u pediatrických pacientů nejsou známy.
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Vybrané skupiny pacientů - Monoterapie přípravkem MabThera Starší pacienti (> 65 let):
Incidence nežádoucích reakcí na lék všech stupňů a stupně 3/ 4 byla obdobná ve skupině starších v porovnání s mladšími pacienty (<65 let).
Pacienti s objemným (bulky) onemocněním
U pacientů s objemným onemocněním byla zjištěna vyšší incidence nežádoucích reakcí na lék stupně 3/4 ve srovnání s pacienty bez rozsáhlého nádorového postižení (25,6 % versus 15,4 %). Incidence jakéhokoli stupně nežádoucích reakcí na lék byla mezi oběma skupinami obdobná.
Opakovaná léčba
Procento pacientů hlásících nežádoucí reakci na lék po opětovném zahájení léčby dalšími cykly přípravku MabThera bylo podobné jako procento pacientů uvádějící nežádoucí reakci na lék po prvním podání přípravku (jakýkoliv stupeň a stupeň 3/4 nežádoucích reakcí na lék).
Vybrané skupiny pacientů - kombinovaná terapie přípravkem MabThera Starší pacienti (> 65 let)
Incidence 3/4. stupně nežádoucích účinků týkajících se krve a lymfatického systému byla u starších pacientů vyšší v porovnání s mladšími pacienty (<65 let) s dříve neléčenou nebo relabující/refrakterní CLL.
Zkušenosti u revmatoidní artritidy
Shrnutí bezpečnostního profilu
Celkový bezpečnostní profil přípravku MabThera u revmatoidní artritidy je založen na údajích od pacientů zařazených do klinických studií a na údajích ze sledování přípravku po uvedení na trh.
Bezpečnostní profil přípravku MabThera u pacientů s těžkou revmatoidní artritidou (RA) je shrnutý v bodech níže. V klinických studiích podstoupilo více než 3100 pacientů nejméně jeden léčebný cyklus a bylo sledováno po dobu v rozsahu 6 měsíců až více než 5 let; přibližně 2400 pacientů podstoupilo dva nebo více cyklů léčby, z nichž přes 1000 pacientů podstoupilo více než 5 cyklů léčby. Informace o bezpečnosti shromážděné z údajů po uvedení přípravku na trh odrážejí očekávaný profil nežádoucích účinků, jak byl pozorován v klinických studiích s přípravkem MabThera (viz bod 4.4).
Pacientům bylo podáno 2 x 1000 mg přípravku MabThera v odstupu dvou týdnů a dále metotrexát (10-25 mg/týden). Infuze přípravku MabThera byly podávány po nitrožilní infuzi 100 mg metylprednizolonu; pacientům byl prednizon podáván také perorálně po dobu 15 dní.
Shrnutí nežádoucích účinků do tabulky
Nežádoucí účinky jsou shrnuty v Tabulce 2. Četnost je uvedena jako velmi častá (>1/10), častá (>1/100 až <1/10), méně častá (>1/1000 až <1/100) a velmi vzácná (<1/10000). V každé skupině četností jsou nežádoucí účinky řazeny podle klesající závažnosti.
Nejčastějším nežádoucím účinkem, který byl považován za účinek související s podáním přípravku MabThera, byly reakce související s infuzí. Celková incidence IRR v klinických studiích byla 23 % po
první infuzi a klesala s dalšími infuzemi. Závažné IRR byly méně časté (0,5 % pacientů) a byly pozorovány převážně v průběhu úvodního cyklu léčby. Kromě nežádoucích reakcí zaznamenaných v klinických studiích s přípravkem MabThera při RA, byly v průběhu postmarketingového sledování hlášeny případy progresivní multifokální leukoencefalopatie (PML) (viz bod 4.4) a reakce podobné sérové nemoci.
Tabulka 2 Souhrn NÚ, které byly hlášeny u pacientů s revmatoidní artritidou léčených _přípravkem MabThera v klinických studií a po uvedení přípravku na trh
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
|
Infekce a infestace |
infekce horních cest dýchacích, močové infekce |
bronchitida, sinusitida, gastroenteritida, tinea pedis |
PML, reaktivace viru hepatitidy B | ||
|
Poruchy krve a lymfatického systému |
neutropenie1 |
pozdní neutropenie2 |
Reakce podobná sérové nemoci | ||
|
Srdeční poruchy |
Angina pectoris, fibrilace síní, srdeční selhání, infarkt myokardu |
Flutter síní | |||
|
Poruchy imunitního systému |
3reakce související s podáním infuze (hypertenze, nauzea, vyrážka, pyrexie, pruritus, kopřivka, podráždění hrdla, návaly horka, hypotenze, rýma, ztuhlost, tachykardie, únava, orofaryngeální bolest, periferní otok, erytém) |
*3reakce související s podáním infuze (generalizovaný otok, bronchospazmus, dušnost, otok laryngu, angioneurotický edém, generalizovaný pruritus, anafylaxe, anafylaktoidní reakce) | |||
|
Celkové poruchy a reakce v místě aplikace | |||||
|
Poruchy metabolismu a výživy |
hypercholesterolémie | ||||
|
Poruchy nervového systému |
parestézie migréna, závrať, ischias | ||||
|
Poruchy kůže a podkožní tkáně |
alopecie |
toxická epidermální nekrolýza (Lyellův syndrom), Stevens-Johnsonův syndrom5 | |||
|
Psychiatrické poruchy | |||||
|
Gastrointestinální poruchy |
dyspepsie, průjem, gastroezofageální reflux, ulcerace v ústech, bolest v horní části břicha | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
bolesti kloubů / muskuloskeletální bolest, artróza, bursitida | ||||
|
Vyšetření |
snížení IgM hladin4 |
snížení IgG hladin4 | |||
|
1 Kategorie četnosti odvozeny z laboratorních hodnot shromážděných z běžných laboratorních měření v klinických studiích. 2 Kategorie četnosti odvozeny z údajů po uvedení přípravku na trh. 3 Reakce, které se objeví do 24 hodin po infuzi. Viz též reakce související s infuzí uvedené níže. Reakce související s infuzí mohou být následkem hypersenzitivity a/nebo mechanismu účinku. 4 Včetně pozorování shromážděných z běžných laboratorních měření. 5 Včetně případů končících úmrtím. | |||||
Opakované léčebné cykly
Aplikace opakovaných léčebných cyklů je spojena s podobným profilem NÚ, jaké byly pozorovány po první expozici. Četnost všech NÚ, které následovaly po první expozici přípravku MabThera, byla vyšší v průběhu prvních 6 měsíců a poté klesala. Toto je z větší části přičítáno reakcím souvisejícím s infuzí (které jsou nejčastější v průběhu prvního cyklu léčby), zhoršení RA a infekcím. Všechny tyto reakce byly nej častější právě v průběhu prvních 6 měsíců léčby.
Reakce související s infuzí
Nej častějšími NÚ, které následovaly po podání přípravku MabThera v klinických studiích, byly reakce související s infuzí (IRR) (viz Tabulka 2). Mezi 3189 pacienty léčenými přípravkem MabThera prodělalo 1135 (36 %) pacientů nejméně jednu IRR, přičemž 733/3189 (23 %) pacientů prodělalo IRR po první infuzi při první expozici přípravku MabThera. Incidence IRR klesala u všech následujících infuzí. V klinických studiích prodělalo těžkou IRR méně než 1 % pacientů (174/3189). V souvislosti s IRR nebyly v klinických studiích zaznamenány žádné CTC (obecná kritéria toxicity, common toxicity criteria) stupně 4 ani úmrtí. Procento příhod CTC stupně 3 a procento IRR, které vedlo k ukončení léčby, klesalo v průběhu následujících cyklů a od 3. cyklu byly tyto příhody vzácné. Premedikace intravenózními glukokortikoidy významně snížila incidenci a závažnost IRR (viz body 4.2 a 4.4). Po uvedení přípravku na trh byly hlášeny závažné reakce související s infuzí, které končily úmrtím.
Ve studii zaměřené na vyhodnocení bezpečnosti zrychlené infuze přípravku MabThera u pacientů s revmatoidní artritidou bylo pacientům se středně těžkou až závažnou aktivní RA, u kterých se nevyskytly závažné reakce související s infuzí v průběhu nebo do 24 h od jejich první infuze, umožněno přijímat 2hodinovou infuzi přípravku MabThera intravenózně. Pacienti s anamnézou závažné reakce na infuzi biologickou léčbou RA nesměli být zařazeni. Počet případů, typy a závažnost reakcí souvisejících s infuzí jsou v souladu s dříve pozorovanými údaji. Nebyly pozorovány žádné závažné reakce související s infuzí.
Popis vybraných nežádoucích účinků
Infekce
U pacientů léčených přípravkem MabThera byla celková četnost výskytu infekcí přibližně 94 na 100 paciento-roků. Většinou se jednalo o mírné a středně těžké infekce horních dýchacích cest a infekce močových cest. Incidence těžkých infekcí, nebo infekcí, které vyžadovaly i.v. podání antibiotik, byla přibližně 4 na 100 paciento-roků. Během opakovaných cyklů léčby přípravkem MabThera nedocházelo k žádnému významnému zvýšení četností těžkých infekcí. V průběhu klinických studií byly zaznamenány infekce dolních cest dýchacích (včetně pneumonie), které měly podobnou incidenci v rameni s léčbou přípravkem MabThera ve srovnání s ramenem kontrolním.
Po podávání přípravku MabThera k léčbě autoimunitních onemocnění byly zaznamenány případy progresivní multifokální leukoencefalopatie s fatálním zakončením. Autoimunitní onemocnění zahrnovala revmatoidní artritidu a další nespecifikovaná autoimunitní onemocnění, včetně systémového lupus erytematodes (SLE) a vaskulitidy.
U pacientů s nehodgkinskými lymfomy, kteří jsou léčeni přípravkem MabThera v kombinaci s cytotoxickou chemoterapií, byly hlášeny případy reaktivace viru hepatitidy B (vizNehodgkinské lymfomy).
Případ reaktivace infekce virem hepatitidy B byl také velmi vzácně hlášen u pacientů s RA léčených přípravkem MabThera (viz bod 4.4).
Kardiovaskulární nežádoucí účinky
U pacientů léčených přípravkem MabThera byly těžké kardiální účinky zaznamenány s četností 1,3 na 100 paciento-roků ve srovnání s 1,3 na 100 paciento-roků ve skupině pacientů dostávajících placebo. Procento pacientů, kteří prodělali srdeční nežádoucí účinky (všechny nebo těžké) se v průběhu opakovaných cyklů léčby nezvyšovalo.
Neurologické příhody
Byly hlášeny případy syndromu posteriomí reverzibilní encefalopatie (PRES - posterior reversible encephalopathy syndrome) / syndromu reverzibilní posteriomí leukoencefalopatie (RPLS - reversible posterior leukoencephalopathy). Známky a příznaky zahrnovaly zrakové poruchy, bolesti hlavy, záchvaty a poruchy vědomí, s přítomností nebo bez přítomnosti hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovací vyšetřovací metodou mozku. U nahlášených případů byly zjištěny rizikové faktory PRES/RPLS, mezi které patří základní onemocnění pacienta, hypertenze, imunosupresivní léčba a/nebo chemoterapie.
Neutropenie
Výskyt příhod neutropenie byl pozorován při léčbě přípravkem MabThera, z nichž většina byla přechodná a mírné nebo střední závažnosti. Neutropenie se může objevit několik měsíců po podání přípravku MabThera (viz bod 4.4).
V placebem kontrolovaných obdobích klinických studií se u 0,94 % (13/1382) pacientů léčených přípravkem MabThera a u 0,27 % (2/731) pacientů s placebem rozvinula závažná neutropenie.
Neutropenické příhody, včetně závažného pozdějšího nástupu a přetrvávající neutropenie, byly vzácně hlášeny po uvedení přípravku na trh, některé z nich byly spojeny s infekcemi končícími úmrtím.
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Laboratorní odchylky
Hypogamaglobulinemie (IgG nebo IgM pod dolní hranicí normy) byla pozorována u pacientů s RA léčených přípravkem MabThera. Po rozvoji nízkých IgG nebo IgM nebyla míra celkových infekcí nebo závažných infekcí zvýšena (viz bod 4.4).
Nízký počet spontánních a v literatuře popsaných případů hypogamaglobulinemie byl pozorován u pediatrických pacientů léčených přípravkem MabThera, v některých případech závažných a vyžadujících dlouhodobou substituční terapii imunoglobuliny. Následky dlouhodobé deplece B buněk u pediatrických pacientů nejsou známy.
Zkušenosti s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou
V klinické studii u granulomatózy s polyangiitidou a mikroskopické polyangiitidy bylo 99 pacientů léčeno přípravkem MabThera (375 mg/m2, jednou týdně po dobu 4 týdnů) a glukokortikoidy (viz bod 5.1).
Shrnutí nežádoucích účinků do tabulky
Nežádoucí účinky uvedené v Tabulce 3 byly všechny nežádoucí účinky, které se objevily s incidencí > 5 % ve skupině léčené přípravkem MabThera.
Tabulka 3 Nežádoucí účinky, které se v klíčové klinické studii v 6 měsících vyskytly u > 5 %
pacientů léčených přípravkem MabThera a s vyšší četností než u druhé srovnávací skupiny
|
Tělesný systém |
Rituximab |
|
Nežádoucí účinek |
(n=99) |
|
Poruchy krve | |
|
a lymfatického systému | |
|
T rombocytopenie |
7 % |
|
Gastrointestinální | |
|
poruchy | |
|
18 % | |
|
6 % | |
|
Zácpa |
5 % |
|
Celkové poruchy a | |
|
reakce v místě aplikace | |
|
Periferní edém |
16 % |
|
Poruchy imunitního systému | |
|
Syndrom uvolňování |
5 % |
|
cytokinů | |
|
Infekce a infestace | |
|
Infekce močových cest |
7 % |
|
Bronchitida |
5 % |
|
5 % | |
|
Nazofaryngitida |
5 % |
|
Vyšetření | |
|
Pokles hemoglobinu |
6 % |
|
Poruchy metabolismu a výživy | |
|
Hyperkalemie |
5 % |
|
Poruchy svalové a kosterní | |
|
soustavy a pojivové tkáně | |
|
Svalové spasmy |
18 % |
|
Artralgie |
15 % |
|
Tělesný systém |
Rituximab |
|
Nežádoucí účinek |
(n=99) |
|
10 % | |
|
Svalová slabost |
5 % |
|
Muskuloskeletální bolest |
5 % |
|
Bolest končetin |
5 % |
|
Poruchy nervového systému | |
|
Závratě |
10 % |
|
Tremor |
10 % |
|
Psychiatrické poruchy | |
|
Insomnie |
14 % |
|
Respirační, hrudní a mediastinální poruchy | |
|
12 % | |
|
11 % | |
|
Epistaxe |
11 % |
|
Nazální překrvení |
6 % |
|
Poruchy kůže a podkožní tkáně | |
|
Akné |
7 % |
|
Cévní poruchy | |
|
Hypertenze |
12 % |
|
5 % | |
Vybrané nežádoucí účinky Reakce související s infuzí
Reakce související s infuzí byly v klinické studii s GPA a MPA definovány jako jakýkoli nežádoucí účinek, který se objevil v průběhu 24 hodin po podání infuze a který byl zkoušejícím považován za nežádoucí účinek související s infuzí u populace hodnocené z důvodu bezpečnosti. Přípravkem MabThera bylo léčeno 99 pacientů a 12 % z nich zaznamenalo alespoň jeden nežádoucí účinek související s infuzí. Všechny nežádoucí účinky související s infuzí byly stupně 1 nebo 2 podle CTC. Nejčastější nežádoucí účinky související s infuzí zahrnovaly syndrom uvolňování cytokinů, návaly horka, podráždění v krku a tremor. Přípravek MabThera byl podáván v kombinaci s intravenózními glukokortikoidy, které mohou incidenci a závažnost těchto nežádoucích účinků snižovat.
Infekce
U 99 pacientů léčených přípravkem MabThera byl celkový výskyt infekce přibližně 237 na 100 pacientoroků (95% interval spolehlivosti 197 - 285) u šestiměsíčního primárního cílového parametru. Infekce byly převážně mírné až středně závažné a byly zastoupeny většinou infekcemi horních cest dýchacích, herpes zoster a infekcemi močových cest. Výskyt závažných infekcí byl přibližně 25 na 100 pacientoroků. Nejčastěji hlášenou závažnou infekcí ve skupině léčené přípravkem MabThera byla pneumonie s četností 4 %.
Malignity
Incidence malignit u pacientů léčených přípravkem MabThera v klinické studii s GPA a MPA byla 2,00 na 100 pacientoroků při běžném uzavření dat ze studie (kdy poslední pacient dokončil období následného sledování). Na základě poměrů standardizované incidence se zdá incidence maligních onemocnění podobná incidenci, která byla dříve zaznamenaná u pacientů s ANCA-asociovanou vaskulitidou.
Kardiovaskulární nežádoucí účinky
Kardiální příhody se vyskytovaly s četností přibližně 273 na 100 pacientoroků (95% interval spolehlivosti 149 - 470) u šestiměsíčního primárního cílového parametru. Výskyt závažných kardiálních příhod byl 2,1 na 100 pacientoroků (95% interval spolehlivosti 3 - 15). Nejčastěji hlášenými příhodami byly tachykardie (4 %) a fibrilace síní (3 %) (viz bod 4.4).
Neurologické příhody
Byly hlášeny případy syndromu posteriorní reverzibilní encefalopatie (PRES - posterior reversible encephalopathy syndrome) / syndromu reverzibilní posteriorní leukoencefalopatie (RPLS - reversible posterior leukoencephalopathy). Známky a příznaky zahrnovaly zrakové poruchy, bolesti hlavy, záchvaty a poruchy vědomí, s přítomností nebo bez přítomnosti hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovací vyšetřovací metodou mozku. U nahlášených případů byly zjištěny rizikové faktory PRES/RPLS, mezi které patří základní onemocnění pacienta, hypertenze, imunosupresivní léčba a/nebo chemoterapie.
Reaktivace hepatitidy B
Po uvedení přípravku na trh byl u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou léčených přípravkem MabThera hlášen malý počet případů reaktivace hepatitidy B, z nichž některé končily úmrtím.
Hypogamaglobulinemie
U pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou, kteří byli léčeni přípravkem MabThera, byla pozorována hypogamaglobulinemie (IgA, IgG nebo IgM pod dolní hranicí normálních hodnot). V randomizované, dvojitě zaslepené, multicentrické studii s aktivním komparátorem hodnotící non-inferioritu přípravku mělo ve skupině léčené přípravkem MabThera v 6. měsíci 27 %, 58 % resp. 51 % pacientů s původně normálními hladinami imunoglobulinů nízké hladiny IgA, IgG resp. IgM ve srovnání s 25 %, 50 % resp. 46 % pacientů ve skupině s cyklofosfamidem. Celkový výskyt infekcí nebo závažných infekcí u pacientů s nízkou hladinou IgA, IgG nebo IgM nebyl zvýšen.
Neutropenie
V randomizované, dvojitě zaslepené, multicentrické studii s aktivním komparátorem hodnotící non-inferioritu přípravku MabThera u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou se u 24 % pacientů ve skupině léčené přípravkem MabThera (jeden cyklus) a 23 % pacientů ve skupině s cyklofosfamidem objevila neutropenie stupně 3 nebo vyšší dle CTC. Neutropenie nebyla spojena s pozorovaným zvýšením závažných infekcí u pacientů léčených přípravkem MabThera. Vliv opakovaných cyklů přípravku MabThera na rozvoj neutropenie u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou nebyl v klinických studiích hodnocen.
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Z klinických studií u lidí jsou dostupné omezené zkušenosti s podáním dávek vyšších než je schválená dávka intravenózního přípravku MabThera. Dosud nejvyšší intravenózní dávka přípravku MabThera testovaná u lidí je 5000 mg (2250 mg/m2), testovaná ve studii se zvyšováním dávek u pacientů s chronickou lymfocytární leukemií. Nebyly zjištěny žádné další bezpečnostní signály.
U pacientů, u kterých se vyskytne předávkování, má být okamžitě přerušena infuze a mají být pečlivě sledováni.
Po uvedení přípravku na trh bylo hlášeno pět případů předávkování přípravkem MabThera. Ve třech případech nebyly hlášeny žádné nežádoucí účinky. Dva nežádoucí účinky, které byly hlášeny, byly chřipkovité (flu-like) příznaky při dávce 1,8 g rituximabu a fatální respirační selhání při dávce 2 g rituximabu.
5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: protinádorové látky, monoklonální protilátky, ATC kód: L01XC02
Rituximab se specificky váže na transmembránový antigen CD20, což je neglykosylovaný fosfoprotein vyskytující se na pre-B a zralých B-lymfocytech. Tento antigen je exprimován > 95 % všech nehodgkinských lymfomů původem z B buněk.
CD20 se nachází na normálních i maligních B-lymfocytech, není přítomen na hematopoetických kmenových buňkách, pro-B-buňkách, normálních plazmatických buňkách ani na jiných normálních tkáních. Antigen se po navázání protilátky neinternalizuje a není také uvolňován z povrchu buňky. CD20 necirkuluje v plazmě jako volný antigen a tedy nevzniká kompetice o navázání protilátek.
Rituximab se svým Fab fragmentem naváže na CD20 antigen na povrchu B-lymfocytů a prostřednictvím Fc domény může být zahájena efektorová imunitní reakce, která vede k lýze B-lymfocytů. Možné mechanizmy, kterými je lýza B-lymfocytů zprostředkována, zahrnují jednak cytotoxickou reakci vyvolanou účinkem komplementu (CDC), jejímž prvním krokem je vazba C1q a jednak protilátkami zprostředkovanou buněčnou cytotoxicitu (ADCC), která závisí na aktivaci jednoho či více Fcy receptorů na povrchu granulocytů, makrofágů a NK buněk. Rovněž bylo prokázáno, že vazba rituximabu na antigen CD 20 přítomný na B lymfocytech vyvolává buněčnou smrt navozením apoptózy.
Počet B-lymfocytů v periferní krvi se snižuje pod normu po podání první dávky přípravku MabThera. U pacientů léčených z důvodu hematologických malignit se objevila nová populace B buněk během 6 měsíců po léčbě a obvykle byl jejich normální počet obnoven během 12 měsíců po ukončení terapie, ačkoli u některých pacientů to může trvat déle (se střední dobou do znovuobjevení lymfocytů až 23 měsíců po indukční léčbě). U pacientů s revmatoidní artritidou byla po podání dvou infuzí 1000 mg přípravku MabThera v odstupu 14 dní pozorována bezprostřední deplece B lymfocytů v periferní krvi. Počet B lymfocytů v periferní krvi začal stoupat od 24. týdne a u většiny pacientů bylo pozorováno obnovení populace do 40. týdne, ať byl přípravek MabThera podáván jako monoterapie nebo v kombinaci s metotrexátem. U malého procenta pacientů došlo po poslední dávce přípravku MabThera k prolongované depleci periferních B-buněk trvající 2 roky nebo déle. U pacientů s granulomatózou s polyangiitidou nebo mikroskopickou polyangiitidou se počet periferních B-buněk snížil na <10 buněk/pl po dvoutýdenním podávání infuzí rituximabu 375 mg/m2 a na této úrovni zůstal u většiny pacientů po dobu dalších 6 měsíců. U většiny pacientů (81 %) se po 12 měsících prokázaly známky návratu B-buněk s počtem >10 buněk/pl, po 18 měsících se počet zvýšil u 87 % pacientů.
Klinické zkušenosti v léčbě nehodgkinských lymfomů a chronické lymfocytární leukemie
Folikulární lymfomy Monoterapie
Úvodní terapie 4 dávky jednou týdně
V klíčové studii bylo léčeno 166 pacientů s relabujícím nebo chemorezistentním nízce maligním nebo folikulárním B nehodgkinským lymfomem. Nemocní dostávali dávku 375 mg/m2 přípravku MabThera podávaného ve formě intravenózní infuze jednou týdně po dobu čtyř po sobě jdoucích týdnů. Celkový výskyt odpovědí na léčbu (ORR) byl v populaci "intent-to-treat" (ITT) zaznamenán ve 48 % (CI95%
41 % - 56 %) případů, přičemž v 6 % případů se jednalo o odpověď úplnou (CR), v 42 % o odpověď částečnou (PR). Medián doby do progrese onemocnění (TTP) byl u pacientů s léčebnou odpovědí stanoven na 13,0 měsíců. Multivariantní analýza prokázala lepší terapeutickou odpověď u pacientů, jejichž onemocnění bylo řazeno dle IWF (International Working Formulation) do skupiny B, C a D histologických podtypů v porovnání se skupinou A (58 % vs. 12 %), dále u nemocných jejichž největší zjistitelná nádorová léze ve svém nejdelším rozměru měřila < 5 cm v porovnání s těmi, u kterých byl průměr tumoru > 7 cm (53 % vs. 38 %). Na léčbu lépe odpovídala onemocnění v chemosenzitivním než v chemorezistentním relapsu (definovaném jako trvání odpovědí < 3 měsíce) (50 % vs. 22 %). Odpověď na léčbu u nemocných, kteří prodělali autologní transplantaci kostní dřeně (ABMT), nastala v 78 % případů oproti 43 % u pacientů bez ABMT. Odpověď na léčbu neovlivňovaly následující faktory: věk, pohlaví, histologický grading, iniciální diagnóza, bulky onemocnění, normální nebo vyšší hodnota LDH či extranodální onemocnění (statisticky hodnoceno Fisherovým exaktním testem). Naopak statisticky signifikantní korelace (p=0,0186) byla zjištěna u nemocných s infiltrací kostní dřeně (KD) - léčebná odpověď u pacientů s postižením KD byla zaznamenána ve 40 %, u nemocných bez infiltrace v 59 %. Tato korelace ale nebyla potvrzena v regresní analýze, ze které jako prognosticky významné vycházejí tyto faktory: histologický typ, bcl-2 pozitivita při zahájení léčby, rezistence na poslední chemoterapii a bulky onemocnění.
Úvodní terapie 8 dávek jednou týdně
V multicentrické jednoramenné studii bylo celkem 37 pacientů s relabujícím nebo resistentním lymfomem nízkého stupně malignity nebo s folikulárním B buněčným NHL léčeno přípravkem MabThera v dávce 375 mg/m2 povrchu těla, podávané v intravenózní infuzi jednou týdně po dobu osmi po sobě jdoucích týdnů. ORR byla 57 % (95% interval spolehlivosti (CI): 41 % - 73 %; CR 14 %, PR 43 %), předpokládaná střední doba do progrese u pacientů odpovídajících na léčbu byla 19,4 měsíce (rozmezí 5,3-38,9 měsíce).
Úvodní terapie, bulky onemocnění, 4 dávky jednou týdně
Byla hodnocena souhrnná data ze tří různých studií, kde bylo léčeno 39 pacientů s relabujícím nebo chemorezistentním bulky onemocněním (rozměr jedné léze > 10 cm v průměru), s nízkomaligními lymfomy nebo s folikulárními B-NHL. Pacienti byli léčeni přípravkem MabThera v dávce 375 mg/m2 povrchu těla, podávané v intravenózní infuzi jednou týdně po dobu čtyř po sobě jdoucích týdnů. ORR byla 36 % (CI95% 21 %-51 %; CR 3 %, PR 33 %), předpokládaná střední doba do progrese u pacientů odpovídajících na léčbu byla 9,6 měsíce (rozmezí 4,5-26,8 měsíce).
Opakovaná léčba 4 dávky jednou týdně
V multicentrické jednoramenné studii bylo zařazeno 58 pacientů s relabujícím nebo chemorezistentním nízkomaligním lymfomem nebo folikulárním B-buněčným NHL s prokazatelnou odpovědí na první terapii přípravkem MabThera. Dávkování při léčbě relapsu bylo 375 mg/m2 povrchu těla, podávané v intravenózní infuzi jednou týdně po dobu čtyř po sobě jdoucích týdnů. Tři pacienti byli zařazeni po aplikaci dvou cyklů přípravku MabThera, byli tedy ve třetím cyklu. Dva pacienti byli zařazeni do studie dvakrát. Celkem tedy bylo hodnoceno 60 opakovaných léčebných cyklů, ORR byla 38 % (CI95% 26 %-51 %; 10 % CR, 28 % PR) s předpokládaným mediánem TTP pro pacienty s léčebnou odpovědí 17,8 měsíce (rozmezí 5,4-26,6). Srovnání s TTP pacientů léčených přípravkem MabThera poprvé (TTP 12,4 měsíce) vychází příznivěji pro opakovanou léčbu.
Iniciální léčba v kombinaci s chemoterapií
V otevřené randomizované studii bylo randomizováno celkem 322 nemocných s dříve neléčeným folikulárním lymfomem do skupiny léčené chemoterapií CVP (cyklofosfamid 750 mg/m2, vinkristin 1,4 mg/m2 do celkové dávky maximálně 2 mg v den 1, prednisolon 40 mg/m2/den ve dnech 1-5) opakující se každé 3 týdny do celkového počtu 8 dávek nebo do skupiny léčené přípravkem MabThera (375 mg/m2) v kombinaci s CVP (R-CVP). MabThera byla podávána prvý den každého léčebného cyklu. Celkem bylo léčeno a z pohledu účinnosti analyzováno 321 nemocných (162 R-CVP a 159 CVP). Medián sledování byl 53 měsíce. Léčba R-CVP vedla proti CVP k signifikantnímu zlepšení primárního cíle studie - doby do selhání léčby (27 měsíců proti 6,6 měsícům, p< 0,0001, log-rank test). Ve R-CVP skupině byla zaznamenána signifikantně (p< 0,0001, chí kvadrát test) vyšší odpověď lymfomu na léčbu (CR, Cru, PR) proti skupině CVP (80,9 % proti 57,2 %). Léčba kombinací R-CVP ve srovnání s CVP významně prodloužila dobu do progrese choroby či úmrtí, 33,6 měsíce oproti 14,7 měsíce (p < 0.0001, log-rank test). Medián trvání odpovědi byl ve skupině R-CVP 37,7 měsíce, ve skupině CVP byl 13,5 měsíce (p< 0,0001, log rank test).
Srovnání celkového přežití mezi léčebnými skupinami ukázalo významný klinický rozdíl: (p=0.029, log-rank test stratifikovaný dle center): četnost přežití po 53 měsících byla u pacientů v rameni R-CVP
80,9 %, zatímco u pacientů v rameni CVP to bylo 71,1 %.
Výsledky tří dalších randomizovaných studií, které použily přípravek MabThera/Rituxan v kombinací s jiným chemoterapeutickým režimem než CVP (CHOP, MCP, CHVP-INF) také prokázaly významné zlepšení četnosti odpovědí, na čase závislých parametrů, včetně celkového přežití. Klíčové výsledky všech 4 studií jsou shrnuty v Tabulce 4.
přípravku MabThera s různými chemoterapeutickými režimy u folikulárního lymfomu. _____
|
Studie |
Léčba Počet pacientů |
Střední doba sledování, měsíce |
ORR % |
CR % |
Střední doba TTF/PFS/ EFS měsíce |
OS % |
|
M39021 |
CVP, 159 R-CVP, 162 |
53 |
57 81 |
10 41 |
Medián TTP: 14,7 33,6 P<0,0001 |
53 měsíce 71,1 80,9 p=0,029 |
|
GLSG’00 |
CHOP, 205 R-CHOP, 223 |
18 |
90 96 |
17 20 |
Medián TTF: 2,6 roků Nedosažen p < 0,001 |
18 měsíců 90 95 p = 0,016 |
|
OSHO-39 |
MCP, 96 R-MCP, 105 |
47 |
75 92 |
25 50 |
Medián PFS: 28,8 Nedosažen p < 0,0001 |
48 měsíců 74 87 p = 0,0096 |
|
FL2000 |
CHVP-IFN, 183 R-CHVP-IFN, 175 |
42 |
85 94 |
49 76 |
Medián EFS: 36 Nedosažen p < 0,0001 |
42 měsíce 84 91 p = 0,029 |
EFS - Přežití bez události TTP - Doba do progrese či úmrtí PFS - Přežití bez progrese TTF - Doba do selhání léčby OS - Přežití v době analýzy
Udržovací terapie
Dosud neléčený folikulární lymfom
V prospektivní, otevřené, mezinárodní, multicentrické studii fáze III 1193 pacientů s dosud neléčeným pokročilým folikulárním lymfomem podstoupilo indukční léčbu R-CHOP (n=881), R-CVP (n=268) nebo R-FCM (n=44) dle volby zkoušejícího. Celkem 1078 pacientů odpovědělo na indukční léčbu, 1018 z nich bylo randomizováno k udržovací léčbě přípravkem MabThera (n=505) nebo ke sledování (n=513). Tyto dvě léčebné skupiny byly dobře vyváženy vzhledem k výchozím charakteristikám a rozsahu onemocnění. Udržovací léčba přípravkem MabThera spočívala v jedné infuzi přípravku MabThera v dávce 375 mg/m2 tělesného povrchu, která byla podávána každé 2 měsíce do progrese onemocnění či nejdéle po dobu 2 let.
Při střední době sledování 25 měsíců od randomizace vedla udržovací léčba přípravkem MabThera ve srovnání se samotným sledováním u dosud neléčených pacientů s folikulárním lymfomem ke klinicky důležitému a statisticky významnému zlepšení v primárním cílovém parametru účinnosti, kterým bylo přežití bez progrese (PFS) hodnocené zkoušejícím (Tabulka 5).
Významný přínos udržovací léčby přípravkem MabThera byl zaznamenán také u sekundárních cílových parametrů studie, kterými byly přežití bez příhody (EFS), doba do další protilymfomové léčby (TNLT), doba do další chemoterapie (TNCT) a celkový výskyt odpovědí (ORR) (Tabulka 5). Výsledky primární analýzy byly potvrzeny na základě delší doby sledování (střední doba sledování:
48 měsíců a 73 měsíců), a aktuální výsledky pak byly vloženy do tabulky 5 pro srovnání 25, 48 a 73 měsíčního období sledování.
střední době sledování 73 měsíců (porovnáno s výsledky primární analýzy založené na střední době sledování 25 měsíců a aktuální analýzy založené na střední době sledování 48 měsíců)____
|
Sledování N=513 |
MabThera N=505 |
Log-rank P hodnota |
Snížení rizika | ||
|
Primární parametr | |||||
|
účinnosti | |||||
|
PFS (medián) |
48,5 měsíce |
NR |
<0,0001 |
42 % | |
|
[48,4 měsíce] |
[NR] |
[<0,0001 ] |
[45 %] | ||
|
(NR) |
(NR) |
(<0,0001) |
(50 %) | ||
|
Sekundární parametry | |||||
|
účinnosti | |||||
|
EFS (medián) |
48,4 měsíce |
NR |
<0,0001 |
39 % | |
|
[47,6 měsíce] |
[NR] |
[<0,0001 ] |
[42 %] | ||
|
(37,8 měsíce) |
(NR) |
(< 0,0001) |
(46 %) | ||
|
OS (medián) |
NR |
NR |
0,8959 |
-2 % | |
|
[NR] |
[NR] |
[0,9298] |
[-2 %] | ||
|
(NR) |
(NR) |
(0,7246) |
(11 %) | ||
|
TNLT (medián) |
71,0 měsíce |
NR |
<0,0001 |
37 % | |
|
[60,2 měsíce] |
[NR] |
[< 0,0001] |
[39 %] | ||
|
(NR) |
(NR) |
(0,0003) |
(39 %) | ||
|
TNCT (medián) |
85,1 měsíce |
NR |
0,0006 |
30 % | |
|
[NR] |
[NR] |
[0,0006] |
[34 %] | ||
|
(NR) |
(NR) |
(0,0011) |
(40 %) | ||
|
ORR* |
60,7 % |
79,0 % |
<0,0001# |
OR = 2,43 | |
|
[60,7 %] |
[79,0 %] |
[<0,0001#] |
[OR = 2,43] | ||
|
(55,0 %) |
(74,0 %) |
(< 0,0001#) |
(OR = 2,33) | ||
|
Četnost kompletních |
52,7 % |
66,8 % |
<0,0001 |
OR = 2,34 | |
|
remisí (CR/CRu)* |
[52,7 %] |
[72,2 %] |
[<0,0001 ] |
[OR = 2,34] | |
|
(47,7 %) |
(66,8 %) |
(< 0,0001) |
(OR = 2,21) | ||
*Na konci udržovací léčby/sledování; # p hodnota chí-kvadrát testu.
Hodnoty na prvních řádcích odpovídají 73 měsícům střední doby sledování, hodnoty v závorkách psané kurzívou odpovídají 48 měsícům střední doby sledování a hodnoty v závorkách odpovídají 25 měsícům střední doby sledování (primární analýza). PFS: přežití bez progrese; EFS: přežití bez příhody; OS: celkové přežití; TNLT: doba do další protilymfomové léčby;
TNCT: doba do další chemoterapie; ORR: celkový výskyt odpovědí; NR: nebylo možno dosáhnout v době klinické uzávěrky; OR: poměr šancí.
Udržovací léčba přípravkem MabThera poskytla konzistentní přínos pro všechny předdefinované hodnocené podskupiny: pohlaví (muži, ženy), věk (do 60 let, nad 60 let včetně), hodnota FLIPI (<=1,
2 nebo >=3), indukční léčba (R-CHOP, R-CVP nebo R-FCM) a bez ohledu na kvalitu léčebné odpovědi na indukční léčbu (CR, CRu nebo PR). Exploratorní analýzy prospěchu udržovací léčby prokázaly méně výrazný účinek u starších pacientů (> 70 let), hodnocený vzorek však byl malý.
Relabující/refrakterní folikulární lymfom
V prospektivní, otevřené, mezinárodní, multicentrické klinické studii fáze III bylo v prvním kroku indukční terapie randomizováno 465 pacientů s relabujícím/refrakterním folikulárním lymfomem do skupiny podstupující CHOP (cyklofosfamid, doxorubicin, vinkristin, prednisolon; n=231) nebo do skupiny léčené přípravkem MabThera plus CHOP (R-CHOP, n=234). Dvě léčebné skupiny byly vyvážené z hlediska vstupních charakteristik a stavu onemocnění. Celkem 334 pacientů, kteří po indukční terapii dosáhli kompletní nebo částečné remise, bylo randomizováno v druhém kroku do skupiny s udržovací terapií přípravkem MabThera (n=167) nebo do skupiny podstupující pouze observaci (n=167). Udržovací léčba přípravkem MabThera spočívala v aplikaci jedné infuze přípravku MabThera v dávce 375 mg/m2 plochy povrchu těla, která byla podávána jedenkrát za 3 měsíce až do doby progrese choroby nebo nejvýše po dobu dvou let.
Závěrečná analýza účinnosti zahrnovala všechny pacienty, kteří byli randomizováni v obou částech studie. Po době observace, která byla u pacientů randomizovaných do indukční fáze průměrně 31
měsíců, se stav pacientů s relabujícím/refraktemím folikulámím lymfomem, kteří podstoupili terapii R-CHOP v porovnání s CHOP, signifikantně zlepšil (viz Tabulka 6).
Tabulka 6 Indukční fáze: přehled výsledků účinnosti CHOP vs. R-CHOP (střední doba
_sledování 31 měsíců)_
|
CHOP |
R-CHOP |
Hodnota p |
Snížení rizika^ | |
|
Primární účinnost orr2) |
74 % |
87 % |
0,0003 |
NA |
|
cr2) |
16 % |
29 % |
0,0005 |
NA |
|
pr2) |
58 % |
58 % |
0,9449 |
NA |
1J Odhady vypočítány na základě poměrů rizik
2) Poslední protinádorová odpověď stanovená zkoušejícím. "Primární" statistické testy pro "odpověď" byly vyjádřeny jako trend testu CR versus PR versus nulová odpověď (p < 0,0001)
Vysvětlivky: NA: nedostupná data; ORR: celkový výskyt odpovědí; CR: kompletní odpověď; PR: částečná odpověď
U pacientů randomizovaných do udržovací fáze klinické studie byl medián doby observace 28 měsíců od randomizace. Udržovací léčba přípravkem MabThera vedla ke klinicky relevantnímu a statisticky významnému zlepšení z hlediska primárního cíle, PFS (doba od randomizace do udržovací fáze do relapsu, progrese choroby nebo úmrtí) při srovnání s observační skupinou (bez léčby) (p< 0,0001, log-rank test). Dosažený medián PFS byl 42,2 měsíce ve skupině s udržovací léčbou přípravkem MabThera v porovnání s 14,3 měsíce ve skupině bez léčby. Použití regresní analýzy (Coxův model) ukázalo, že v důsledku udržovací léčby přípravkem MabThera je riziko progrese nebo úmrtí sníženo o 61 % ve srovnání se skupinou bez léčby (95 % CI; 45 %-72 %). Odhad počtu odpovědí bez progrese vycházející z Kaplan-Meierových křivek po 12 měsících léčby byl 78 % ve skupině s udržovací léčbou přípravkem MabThera oproti 57 % ve skupině bez léčby. Analýza celkového přežití potvrdila signifikantní výhodnost udržovací léčby přípravkem MabThera oproti observační skupině (p=0,0039 log-rank test). V důsledku udržovací léčby přípravkem MabThera bylo riziko úmrtí sníženo o 56 % (95 % CI; 22 %-75 %).
Tabulka 7 Udržovací fáze: přehled výsledků účinnosti ve skupině léčené přípravkem
|
Parametr účinnosti |
Určení mediánu doby (měsíce) |
Snížení | ||
|
k dosažení stanoveného parametru |
rizika | |||
|
metodou Kaplan-Meier | ||||
|
Observace |
MabThera |
Log-Rank | ||
|
(N = 167) |
(N=167) |
hodnota p | ||
|
Doba přežití bez progrese (PFS) |
14,3 |
42,2 |
<0,0001 |
61 % |
|
Celkové přežití |
NR |
NR |
0,0039 |
56 % |
|
Doba do nové léčby lymfomu |
20,1 |
38,8 |
<0,0001 |
50 % |
|
Doba přežití bez známek onemocnění3 |
16,5 |
53,7 |
0,0003 |
67 % |
|
Analýza podskupin PFS | ||||
|
CHOP |
11,6 |
37,5 |
<0,0001 |
71 % |
|
R-CHOP |
22,1 |
51,9 |
0,0071 |
46 % |
|
CR |
14,3 |
52,8 |
0,0008 |
64 % |
|
PR |
14,3 |
37,8 |
<0,0001 |
54 % |
|
OS | ||||
|
CHOP |
NR |
NR |
0,0348 |
55 % |
|
R-CHOP |
NR |
NR |
0,0482 |
56 % |
NR: nedosaženo; a: relevantní pouze u pacientů, kteří dosáhli kompletní odpovědi
Výhodnost udržovací léčby přípravkem MabThera byla potvrzena ve všech analyzovaných podskupinách bez ohledu na indukční režim (CHOP nebo R-CHOP) nebo kvalitu odpovědi v rámci indukční léčby (CR nebo PR) (viz Tabulka 7). V důsledku udržovací léčby přípravkem MabThera byl významně prodloužen medián PFS u pacientů odpovídajících na indukční terapii CHOP (medián PFS 37,5 měsíce vs. 11,6 měsíce, p< 0,0001), stejně jako u pacientů odpovídajících na indukční léčbu R-CHOP (medián PFS 51,9 měsíce vs. 22,1 měsíce, p=0,0071). Přestože se jednalo o malé podskupiny, ukázala se udržovací léčba přípravkem MabThera signifikantně výhodnou i z hlediska celkového přežití, a to jak u pacientů odpovídajících na CHOP, tak u pacientů odpovídajících na R-CHOP, ačkoli pro potvrzení tohoto zjištění je zapotřebí delší doba sledování po léčbě.
Difúzní velkobuněčný nehodgkinský lymfom z B buněk
399 dosud neléčených starších pacientů (věk 60 až 80 let) s diagnostikovaným difúzním velkobuněčným B-nehodgkinským lymfomem bylo v rámci randomizované, otevřené studie léčeno osmi cykly standardní chemoterapie CHOP (cyklofosfamid 750 mg/m2 den 1, doxorubicin 50 mg/m2 den 1, vinkristin 1,4 mg/m2 den 1 do maximální dávky 2 mg a prednison 40 mg/m2/den podávaný ve dnech 1-5) aplikované v intervalu 3 týdnů po osm cyklů nebo přípravkem MabThera s chemoterapií CHOP (R-CHOP). Přípravek MabThera byl podáván první den každého léčebného cyklu.
Závěrečná analýza účinnosti byla provedena u všech randomizovaných pacientů (197 CHOP, 202 R-CHOP) a střední hodnota trvání následného sledování byla přibližně 31 měsíců. Obě skupiny byly vyrovnané s ohledem na charakteristiku a pokročilost onemocnění na počátku léčby. Závěrečná analýza potvrdila, že léčebný režim R-CHOP byl spojen s klinicky relevantním a statisticky významným prodloužením přežití bez výskytu nežádoucích příhod (což byl hlavní parametr účinnosti, kde příhodou bylo úmrtí, relaps nebo progrese lymfomu, nebo zahájení nové léčby lymfomu) (p=0,0001). Střední hodnota trvání bezpříznakového období stanovená metodou Kaplan-Meier byla 35 měsíců ve skupině léčené režimem R-CHOP, ve srovnání s 13 měsíci ve skupině léčené režimem CHOP, což představuje snížení rizika o 41 %. Celkové přežití ve 24. měsíci bylo 68,2 % ve skupině léčené R-CHOP ve srovnání s 57,4 % ve skupině léčené režimem CHOP. Následná analýza celkového přežití, provedená po 60 měsících následného sledování, potvrdila větší prospěšnost R-CHOP než CHOP (p=0,0071), což představuje snížení rizika o 32 %.
Analýza všech sekundárních parametrů (četnost odezvy na léčbu, přežití bez známek progrese, přežití bez známek nemoci, trvání odpovědi) ověřila léčebný účinek R-CHOP ve srovnání s CHOP. Celková četnost odezvy na léčbu po 8 cyklech byla 76,2 % ve skupině léčené R-CHOP a 62,4 % ve skupině léčené CHOP (p=0,0028). Riziko progrese nemoci se snížilo o 46 % a riziko relapsu o 51 %. Ve všech podskupinách pacientů (pohlaví, věk, IPI korigovaný na věk, stádium nemoci dle Ann Arbor, ECOG, B2 2 mikroglobulin, LDH, albumin, B-symptomy, bulky disease, mimouzlinová manifestace, postižení kostní dřeně) byly poměry rizik pro asymptomatické přežití a celkové přežití (R-CHOP oproti CHOP) nižší než 0,83 a 0,95. Režim R-CHOP byl spojen se zlepšeným výsledkem léčby u vysoce a nízkorizikových pacientů podle IPI korigovaného na věk.
Klinické laboratorní nálezy
U 67 nemocných vyšetřovaných pro přítomnost HAMA (protilátky proti myším antigenům) nebyla zaznamenána žádná odpověď. Z 356 nemocných vyšetřovaných pro přítomnost HACA (human anti-chimeric antibody) bylo 1,1 % pozitivních (4 pacienti).
Chronická lymfocytární leukemie
Ve dvou otevřených, randomizovaných studiích bylo celkem 817 dosud neléčených pacientů a 552 pacientů s relabující/refrakterní CLL randomizováno k léčbě buď chemoterapií FC (fludarabin 25 mg/m2, cyklofosfamid 250 mg/m2, dny 1-3) podávané každé 4 týdny v 6 cyklech nebo k léčbě přípravkem MabThera v kombinaci s chemoterapií FC (R-FC). Přípravek MabThera byl podáván v dávce 375 mg/m2 během prvního dne prvního cyklu před chemoterapií a v dávce 500 mg/m2 v den 1 následných léčebných cyklů. Ze studie s relabující/refrakterní CLL byli vyloučeni pacienti, kteří byli dříve léčeni monoklonálními protilátkami nebo kteří nereagovali (definováno jako selhání dosažení částečné remise na dobu alespoň 6 měsíců) na léčbu fludarabinem nebo jakýmkoliv nukleosidovým analogem. Analýza účinnosti byla provedena u 810 pacientů (403 R-FC, 407 FC) ze studie s první linií léčby (viz Tabulka 8a a Tabulka 8b) a u 552 pacientů (276 R-FC, 276 FC) ze studie relabující/refrakterní CLL (viz Tabulka 9).
Ve studii s první linií léčby při střední době sledování 48,1 měsíce byla střední hodnota přežití bez progrese ve skupině R-FC 55 měsíců a ve skupině FC 33 měsíce (p < 0,0001, log-rank test). Analýza celkového přežití nadále prokazuje významný přínos léčby R-FC oproti samotné chemoterapii FC (p = 0,0319, log-rank test) (Tabulka 8a). Přínos ve smyslu prodloužení PFS byl konzistentně pozorován ve většině podskupin pacientů analyzovaných na základě vstupního rizika choroby (tj.pro stádia choroby dle Bineta A-C) (Tabulka 8b).
Tabulka 8a Léčba chronické lymfocytární leukemie v první linii
Přehled výsledků účinnosti pro kombinaci MabThera plus FC vs. samotné FC -
|
střední doba slet |
ování 48,1 měsíce | |||
|
Parametr účinnosti |
Odhad střední doby do události dle |
Snížení | ||
|
Kaplan-Meiera (měsíce) |
rizika | |||
|
FC |
R-FC |
Log-Rank | ||
|
(N = 409) |
(N=408) |
p hodnota | ||
|
Přežití bez progrese (PFS) |
32,8 |
55,3 |
<0,0001 |
45 % |
|
Celkové přežití |
NR |
NR |
0,0319 |
27 % |
|
Přežití bez události |
31,3 |
51,8 |
<0,0001 |
44 % |
|
Léčebná odpověď (CR, nPR, či |
72,6 % |
85,8 % |
<0,0001 |
n.a. |
|
PR) | ||||
|
Četnost CR |
16,9 % |
36,0 % |
<0,0001 |
n.a. |
|
Trvání odpovědi* |
36,2 |
57,3 |
<0,0001 |
44 % |
|
Přežití bez známek choroby |
48,9 |
60,3 |
0,0520 |
31 % |
|
(DFS)** | ||||
|
Doba do další léčby |
47,2 |
69,7 |
<0,0001 |
42 % |
Analýza léčebné odpovědi a četnosti CR pomocí Chí-kvadrátového testu. NR: nedosaženo; n.a.: není použitelné *: týká se pouze pacientů, kteří dosáhli CR, nPR, PR **: týká se pouze pacientů, kteří dosáhli CR
Tabulka 8b První linie léčby chronické lymfocytární leukemie
Poměry rizik pro přežití bez progrese podle stádia dle Bineta (ITT) - střední doba sledování 48,1 měsíce_
|
Přežití bez progrese (PFS) |
Počet pacientů |
Poměr rizik (95% CI) |
p-hodnota (Wald test, neadjustovaný) | |
|
FC |
R-FC | |||
|
Stádium A dle Bineta |
22 |
18 |
0,39 (0,15; 0,98) |
0,0442 |
|
Stádium B dle Bineta |
259 |
263 |
0,52 (0,41; 0,66) |
<0,0001 |
|
Stádium C dle Bineta |
126 |
126 |
0,68 (0,49; 0,95) |
0,0224 |
CI: Interval spolehlivosti
Ve studii s relabující/refrakterní CLL bylo přežití bez progrese (primární cílový parametr) 30,6 měsíců ve skupině R-FC a 20,6 měsíců ve skupině FC (p=0,0002, log-rank test). Prospěch PFS byl pozorován u téměř všech pacientů analyzovaných subskupin podle rizika onemocnění na začátku studie. Mírné, ale ne významné zlepšení v celkovém přežití bylo zaznamenáno v rameni R-FC v porovnání s FC.
Tabulka 9 Léčba relabující/refrakterní chronické lymfocytární leukemie - shrnutí výsledků
účinnosti přípravku MabThera s FC v porovnání s FC samotným (střední doba _sledování 25,3 měsíců)._
|
Parametr účinnosti |
Odhad střední doby do události dle Kaplan-Meiera (měsíce) |
Snížení rizika | ||
|
FC (N = 276) |
R-FC (N=276) |
Log-Rank p hodnota | ||
|
Přežití bez progrese (PFS) |
20,6 |
30,6 |
0,0002 |
35 % |
|
Celkové přežití |
51,9 |
NR |
0,2874 |
17 % |
|
Přežití bez události |
19,3 |
28,7 |
0,0002 |
36 % |
|
Léčebná odpověď (CR, nPR, či PR) |
58,0% |
69,9% |
0,0034 |
n.a. |
|
Četnost CR |
13,0% |
24,3% |
0,0007 |
n.a. |
|
Trvání odpovědi * |
27,6 |
39,6 |
0,0252 |
3 1% |
|
Přežití bez známek choroby (DFS)** |
42,2 |
39,6 |
0,8842 |
-6 % |
|
Doba do další léčby |
34,2 |
NR |
0,0024 |
35 % |
Analýza léčebné odpovědi a četnosti CR pomocí Chí-kvadrátového testu.
*: týká se pouze pacientů, kteří dosáhli CR, nPR, PR; NR: nedosaženo n.a. není použitelné **: týká se pouze pacientů, kteří dosáhli CR;
Výsledky z dalších podpůrných studií, které využívaly v léčbě CLL přípravek MabThera v kombinaci s jinými chemoterapeutickými režimy u dříve neléčených a/nebo relabujících/refrakterních pacientů s CLL (zahrnující CHOP, FCM, PC, PCM, bendamustin a kladribin) také ukázaly vysokou četnost kompletních léčebných odpovědí s prospěchem v PFS, i když s mírně vyšší toxicitou (zvláště myelotoxicitou). Tyto studie podporují užití přípravku MabThera s jakoukoli chemoterapií.
Údaje od přibližně 180 pacientů již v minulosti léčených přípravkem MabThera prokázaly klinický přínos (včetně CR) a podporují opakovanou léčbu přípravkem MabThera.
Pediatrická populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem MabThera u všech podskupin pediatrické populace s folikulárním lymfomem a chronickou lymfocytární leukemií. Informace o použití u dětí viz bod 4.2.
Klinické zkušenosti v léčbě revmatoidní artritidy
Bezpečnost a účinnost přípravku MabThera z hlediska zmírnění příznaků a známek revmatoidní artritidy u pacientů s nedostatečnou odpovědí na léčbu inhibitory tumor nekrotizujícího faktoru (TNF) byla demonstrována v klíčové randomizované, kontrolované, dvojitě zaslepené, multicentrické studii (Studie 1).
Studie 1 hodnotila 517 pacientů, kteří vykazovali nedostatečné odpovědi nebo nesnášenlivost na jednu či více terapií inhibitory TNF. Pacienti, kteří byli vybráni do studií, měli aktivní revmatoidní artritidu, diagnostikovanou v souladu s kritérii Amerického sdružení pro revmatologii (ACR, American College of Rheumatology). Přípravek MabThera byl podán ve formě dvou i.v. infuzí s odstupem 15 dnů. Pacienti dostávali 2 x 1000 mg přípravku MabThera i.v. infuzí nebo placebo v kombinaci s MTX. Všichni pacienti dostávali souběžnou léčbu 60 mg perorálního prednisonu ve dnech 2 - 7 a 30 mg ve dnech 8 - 14 po první infuzi. Primárním cílovým parametrem byl podíl pacientů, kteří dosáhli ve 24. týdnu odpovědi ACR20. Pacienti byli dále sledováni i po týdnu 24 z hlediska dlouhodobých cílů, což zahrnovalo i radiologické vyšetření po 56 týdnech a 104 týdnech. Během této doby dostalo mezi týdny 24 a 56 přípravek MabThera v rámci prodloužené otevřené klinické studie 81 % pacientů ze skupiny léčené původně placebem.
Studie s přípravkem MabThera u pacientů s časnou artritidou (pacienti bez předchozí léčby metotrexátem a pacienti s nedostatečnou odpovědí na metotrexát, ale dosud neléčení inhibitory TNF-alfa) splnily své primární cílové parametry. Přípravek MabThera není u těchto pacientů indikován, protože údaje o bezpečnosti týkající se dlouhodobé léčby přípravkem MabThera nejsou dostatečné, zvláště co se týká rizika rozvoje malignit a PML.
Výsledky z hlediska aktivity onemocnění
Přípravek MabThera v kombinaci s metotrexátem významně zvýšil podíl pacientů vykazujících nejméně 20 % zlepšení ACR skóre ve srovnání s pacienty léčenými samotným metotrexátem (viz Tabulka 10). Ve všech vývojových studiích byl prospěch léčby u pacientů obdobný nezávisle na věku, pohlaví, ploše povrchu těla, rase, počtu předchozích terapií nebo stavu onemocnění.
Klinicky a statisticky významné zlepšení bylo zaznamenáno také ve všech jednotlivých složkách ACR odpovědi (počet oteklých a bolestivých kloubů, celkové hodnocení pacientem a lékařem, skóre indexu HAQ, hodnocení stupně bolesti a C-reagujících proteinů (mg/dl)).
Tabulka 10 Klinické výsledky podle primárního cílového parametru účinnosti ve Studii 1 _ (ITT populace) __
|
Výsledekf |
Placebo+MTX |
MabThera+MTX (2 x 1000 mg) | |
|
Studie 1 |
N= 201 |
N= 298 | |
|
ACR20 ACR50 ACR70 |
36 (18 %) 11 (5 %) 3 (1 %) |
153 (51 %)*** 80 (27 %)*** 37 (12 %)*** | |
|
EULAR odpověď (dobrá/střední) |
44 (22 %) |
193 (65 %)*** | |
|
Průměrná změna DAS |
-0,34 |
-1,83*** |
f Výsledek v 24 týdnech
Významný rozdíl v porovnání s placebem + MTX v době hodnocení primárního cílového parametru účinnosti: ***p < 0,0001
Pacienti léčení přípravkem MabThera v kombinaci s metotrexátem měli významně větší snížení skóre aktivity onemocnění (DAS28) než pacienti dostávající pouze metotrexát (Tabulka 9). Ve všech studiích bylo dosaženo podobně dobré až střední odpovědi dle kritérií Evropské ligy proti revmatismu (EULAR, European League Against Rheumatism) u významně většího počtu pacientů dostávajících přípravek MabThera a metotrexát ve srovnání s pacienty léčenými samotným metotrexátem (viz Tabulka 10).
Radiologická odpověď
Strukturální poškození kloubů bylo hodnoceno radiograficky a bylo vyjádřeno jako změna v modifikovaném celkovém skóre dle Sharpa (mTSS, modified Total Sharp Score) a jeho jednotlivých položkách - ve skóre erozí a skóre zúžení kloubní štěrbiny.
Ve Studii 1 prováděné u pacientů s nedostatečnou odpovědí či s nesnášenlivostí jedné či více léčeb inhibitorem TNF, kteří dostávali přípravek MabThera v kombinaci s metotrexátem, byla prokázána po 56 týdnech významně menší radiologická progrese než u pacientů, kteří byli zpočátku léčeni samotným metotrexátem. Z pacientů léčených původně samotným metotrexátem jich do týdne 56 81 % podstoupilo léčbu přípravkem MabThera buďto jako záchrannou léčbu mezi týdny 16-24 nebo v průběhu prodloužené studie. Větší část pacientů léčená od počátku kombinací přípravku MabThera/MTX také neměla po 56 týdnech progresi erozí (Tabulka 11).
Tabulka 11 Radiografické výsledky ^ v 1. roce (mITT populace)
|
Placebo+MTX |
MabThera +MTX 2 x 1000 mg | |
|
Studie 1 |
(n = 184) |
(n = 273) |
|
Průměrná změna od výchozích hodnot: | ||
|
Modifikované celkové skóre dle Sharpa |
2,30 |
1,01* |
|
Skóre erozí |
1,32 |
0,60* |
|
Skóre zúžení kloubních štěrbin |
0,98 |
0,41** |
|
Podíl pacientů bez radiografických změn |
46 % |
53 %, NS |
|
Podíl pacientů bez erozivních změn |
52 % |
60 %, NS |
150 pacientů původně randomizovaných do skupiny s placebem + MTX ve studii 1 dostalo během jednoho roku alespoň jeden cyklus léčby RTX + MTX * p <0,05, ** p < 0,001. Vysvětlivky: NS: nevýznamný
Inhibice rychlosti progrese kloubního poškození byla rovněž pozorována dlouhodobě. Radiografická analýza ve 2. roce ve studii 1 prokázala významné snížení progrese strukturálního kloubního poškození u pacientů, kteří dostávali přípravek MabThera v kombinaci s metotrexátem v porovnání s metotrexátem samotným, stejně jako významně vyšší podíl pacientů bez progrese kloubního poškození během dvou let.
Fyzické funkce a výsledky z hlediska kvality života
Bylo pozorováno významné snížení indexu HAQ-DI a indexu únavy (FACIT-Fatigue) u pacientů léčených přípravkem MabThera ve srovnání s pacienty léčenými pouze metotrexátem. Podíl pacientů léčených přípravkem MabThera, který vykazoval minimální klinicky významný rozdíl (MCID, minimal clinically important difference) v HAQ-DI (definovaném jako pokles individuálního celkového skóre o > 0,22), byl rovněž vyšší, než mezi pacienty dostávajícími metotrexát samotný (Tabulka 12).
Významné zlepšení kvality života v souvislosti se zdravím bylo rovněž prokázáno významným zlepšením jak ve skóre fyzického zdraví (PHS, physical health score) tak i skóre mentálního zdraví (MHS, mental health score) v dotazníku SF-36. Kromě toho dosáhl MCID v těchto skóre i významně vyšší podíl pacientů (Tabulka 12).
Výsledky fyzických funkcí a kvality života v týdnu 24 ve Studii 1
Tabulka 12
|
Výsledky f |
Placebo+MTX |
MabThera+MTX (2 x 1000 mg) |
|
n=201 |
n=298 | |
|
Průměrná změna v HAQ-DI |
0,1 |
-0,4*** |
|
% HAQ-DI MCID |
20 % |
51 % |
|
Průměrná změna ve FACIT-T |
-0,5 |
-9,1*** |
|
n=197 |
n=294 | |
|
Průměrná změna ve SF-36 |
0,9 |
5,8*** |
|
PHS % SF-36 PHS MCID |
13 % |
48 %*** |
|
Průměrná změna ve SF-36 |
1,3 |
4,7** |
|
MHS % SF-36 MHS MCID |
20 % |
38 %* |
f Výsledky v týdnu 24
Významný rozdíl ve srovnání s placebem v době hodnocení primárního cílového parametru účinnosti: * p < 0,05, **p <
0,001 ***p < 0,0001
MCID HAQ-DI > 0,22, MCID SF-36 PHS > 5,42, MCID SF-36 MHS > 6,33
Účinnost u pacientů séropozitivních na autoprotilátky (RF a/nebo anti-CCP)
Pacienti séropozitivní na revmatoidní faktor (RF) a/nebo anti-CCP (anti-Cyclic Citrullinated Peptide), kteří byli léčeni přípravkem MabThera v kombinaci s metotrexátem, vykazovali lepší odpověď v porovnání s pacienty negativními na obě autoprotilátky.
Parametry účinnosti u pacientů léčených přípravkem MabThera byly analyzovány na základě stavu autoprotilátek před zahájením léčby. V týdnu 24 měli pacienti, kteří byli séropozitivní na RF a/nebo anti-CCP v úvodu léčby, významně větší šanci, že dosáhnou odpovědi ACR20 a ACR50, v porovnání se séronegativními pacienty (p=0,0312 and p=0,0096) (Tabulka 13). Tyto nálezy byly shodné v týdnu 48, kdy séropozitivita autoprotilátek rovněž významně zvyšovala pravděpodobnost dosažení ACR70. V týdnu 48 byla u séropozitivních pacientů 2-3násobně vyšší pravděpodobnost, že dosáhnou ACR odpovědi, ve srovnání s pacienty séronegativními. U séropozitivních pacientů docházelo rovněž k významně většímu poklesu DAS28-ESR v porovnání se séronegativními pacienty (Obrázek 1).
Tabulka 13_Shrnutí účinnosti podle stavu autoprotilátek v úvodu léčby
|
Týde Séropozitivní (n=514) |
;n 24 Séronegativní (n=106) |
Týde Séropozitivní (n=506) |
:n 48 Séronegativní (n=101) | |
|
ACR20 (%) |
62,3* |
50,9 |
71, 1* |
51,5 |
|
ACR50 (%) |
32,7* |
19,8 |
44,9** |
22,8 |
|
ACR70 (%) |
12,1 |
5,7 |
20,9* |
6,9 |
|
EULAR odpověď (%) |
74,8* |
62,9 |
84,3* |
72,3 |
|
Průměrná změna DAS28-ESR |
-1,97** |
-1,50 |
-2 48*** |
-1,72 |
Hladiny významnosti byly definovány jako * p<0,05 **p<0,001, ***p<0,0001.
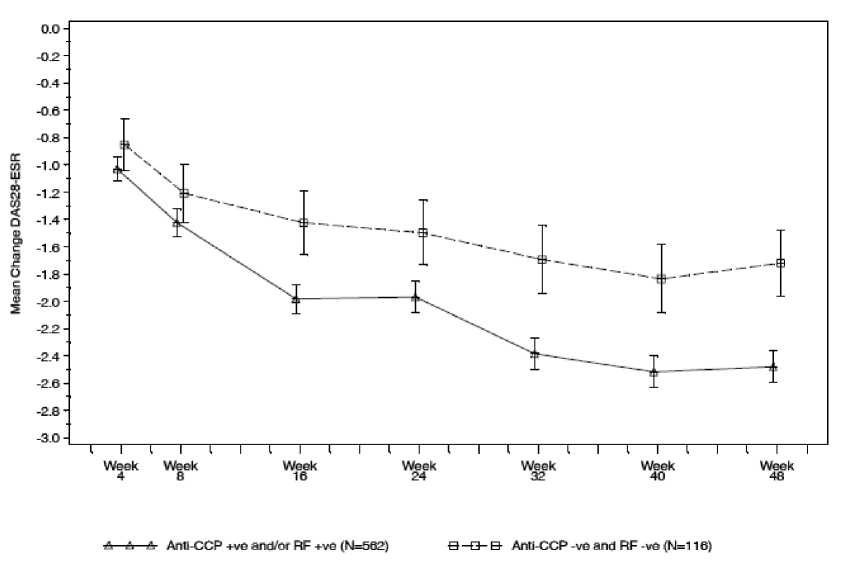
Dlouhodobá účinnost při opakovaných cyklech léčby
Léčba přípravkem MabThera v kombinaci s metotrexátem vedla při opakovaných cyklech léčby k setrvalému zlepšení klinických objektivních i subjektivních příznaků RA, jak vyplývá z ACR, DAS28-ESR a EULAR odpovědí, které jsou průkazné u všech studovaných populací pacientů (Obrázek 2). Bylo pozorováno setrvalé zlepšení fyzických funkcí, což naznačuje HAQ-DI skóre a podíl pacientů, kteří dosáhli MCID pro HAQ-DI.
Obrázek 2: ACR odpovědi ve 4 cyklech léčby (24 týdnů po každém cyklu (na pacienta a návštěvu)) u pacientů s nedostatečnou odpovědí na inhibitory TNF (n=146)
(0
+■»
c
.92
re
o.
4—
O

1st 2nd 3rd 4th Course Course Course Course

■ ACR20
□ ACR50
□ ACR70
Klinické laboratorní nálezy
Celkem 392 z 3095 (12,7 %) pacientů s revmatoidní artritidou v klinických studiích s přípravkem MabThera bylo po terapii pozitivně testováno na přítomnost HACA. Tvorba HACA nebyla u většiny pacientů spojena s klinickým zhoršením ani se zvýšeným rizikem reakce na následné infuze. Tvorba protilátek HACA může být spojena se zhoršením reakcí na infuzi nebo alergických reakcí, které se objevují po druhé infuzi následného cyklu.
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem MabThera u všech podskupin pediatrické populace s autoimunitní artritidou. Informace o použití u dětí viz bod 4.2.
Klinické zkušenosti u granulomatózy s polyangiitidou (Wegenerova granulomatóza) a mikroskopické polvangiitidv
V randomizované, dvojitě zaslepené, placebem kontrolované multicentrické studii s aktivním komparátorem hodnotící non-inferioritu přípravku bylo zařazeno a léčeno celkem 197 pacientů ve věku 15 let nebo starších se závažnou aktivní granulomatózou s polyangiitidou (75 %) a mikroskopickou polyangiitidou (24 %).
Pacienti byli randomizováni v poměru 1:1 k léčbě buď perorálním cyklofosfamidem v dávce 2 mg/kg/den podávané denně po dobu 3-6 měsíců, nebo k léčbě přípravkem MabThera (375 mg/m2) jednou týdně po dobu 4 týdnů. Všichni pacienti v rameni s cyklofosfamidem dostávali udržovací léčbu azathioprinem v průběhu období následného sledování. Pacienti v obou ramenech dostávali pulsní intravenózní (i.v.) léčbu methylprednisolonem v denní dávce 1000 mg (nebo ekvivalentní dávku jiného glukokortikoidu) po dobu 1-3 dnů, po které následovala perorální léčba prednisonem (1 mg/kg/den s maximální dávkou nepřesahující 80 mg/den). Léčba prednisonem musela být ukončena do 6 měsíců od zahájení studijní léčby.
Primárním výsledkem bylo dosažení úplné remise v 6. měsíci definované jako BVAS/WG (Birmingham Vasculitis Activity Score for Wegener’s Granulomatosis) 0 a vysazení léčby glukokortikoidy. Předem určená hranice non-inferiority pro rozdíl v léčbě byla 20 %. Studie prokázala non-inferioritu přípravku MabThera vůči cyklofosfamidu u úplné remise (CR) v 6. měsíci léčby (Tabulka 14).
Účinnost byla pozorována jak u pacientů s nově diagnostikovaným onemocněním, tak i u pacientů s relabujícím onemocněním (Tabulka 15).
Tabulka 14
Procento pacientů, kteří dosáhli úplné remise v 6. měsíci (intent-to-treat populace*)
|
MabThera (n = 99) |
Cyklofosfamid (n = 98) |
Rozdíl v léčbě (MabThera-Cyklofosfamid) | |
|
Výskyt |
63,6 % |
53,1 % |
10,6 % 95,1%b CI (-3,2 %, 24,3 %) a |
|
- CI = interval spolehlivosti - * Nejhorší zaznamenaný případ a Non-inferiorita byla prokázána, protože nižší hranice (-3,2 %) byla vyšší než předem stanované hranice non-inferiority (-20 %). b 95,1% hladina spolehlivosti odpovídá dalšímu 0,001 alfa k výpočtu průběžné analýzy účinnosti. | |||
Tabulka 15 Úplná remise v 6. měsíci podle stavu onemocnění
|
MabThera |
Cyklofosfamid |
Rozdíl (CI 95%) | |
|
Všichni pacienti |
n=99 |
n=98 | |
|
Nově diagnostikovaní |
n=48 |
n=48 | |
|
Relabující |
n=51 |
n=50 | |
|
Úplná remise | |||
|
Všichni pacienti |
63,6 % |
53,1 % |
10,6 % (-3,2, 24,3) |
|
Nově diagnostikovaní |
60,4 % |
64,6 % |
-4,2 % (-23,6, 15,3) |
|
Relabující |
66,7 % |
42,0 % |
24,7 % (5,8, 43,6) |
Nejhorší zaznamenaný případ je použit u pacientů s chybějícími údaji.
Úplná remise ve 12 a 18 měsících
Ve skupině léčené přípravkem MabThera dosáhlo úplné remise 48 % pacientů ve 12 měsících a 39 % pacientů v 18 měsících. U pacientů léčených cyklofosfamidem (následovaným azathioprinem k udržení úplné remise) dosáhlo úplné remise 39 % pacientů ve 12 měsících a 33 % pacientů v 18 měsících. Od 12. do 18. měsíce bylo ve skupině léčené přípravkem MabThera pozorováno 8 relapsů, ve srovnání s 4 relapsy ve skupině léčené cyklofosfamidem.
Opakovaná léčba přípravkem MabThera
Na základě hodnocení zkoušejícím podstoupilo 15 pacientů druhý cyklus léčby přípravkem MabThera k léčbě relapsu aktivity onemocnění, ke kterému došlo mezi 6 a 18 měsíci po prvním cyklu léčby přípravkem MabThera. Omezené údaje ze současné studie znemožňují hodnocení týkající se účinnosti následných cyklů léčby přípravkem MabThera u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou.
Následná imunosupresivní léčba může být obzvláště vhodná u pacientů s rizikem relapsu (např. s dřívějším relapsem v minulosti a granulomatózou s polyangiitidou nebo pacienti s rekonstitucí B lymfocytů kromě sledování PR3-ANCA). Pokud bylo dosaženo remise použitím přípravku MabThera, může se zvážit následná imunosupresivní léčba jako prevence relapsu. Nebyla prokázána účinnost a bezpečnost udržovací terapie přípravkem MabThera.
Laboratorní vyšetření
Celkem 23/99 (23 %) pacientů léčených přípravkem MabThera v této studii bylo HACA pozitivních do 18. měsíce. Žádný z 99 pacientů léčených přípravkem MabThera nebyl HACA pozitivní při screeningu. Klinický význam tvorby HACA u pacientů léčených přípravkem MabThera není zřejmý.
5.2 Farmakokinetické vlastnosti
Nehodgkinské lymfomy
Na základě populační farmakokinetické analýzy u 298 pacientů s NHL, kteří dostali jednu či více infuzí přípravku MabThera samostatně či v kombinaci s chemoterapií CHOP (použité dávky přípravku MabThera se pohybovaly v rozmezí od 100 do 500 mg/m2), byly hodnoty nespecifické clearance
(CLj), specifické clearance (CL2) pravděpodobně ovlivněné B buňkami či nádorovou náloží a centrálním distribučním objemem (Vj) odhadnuty v typické populaci na 0,14 l/den, 0,59 l/den a 2,7 l. Odhadovaná střední hodnota terminálního eliminačního poločasu přípravku MabThera byla 22 dní (rozmezí 6,1 - 52 dní). Vstupní hodnota počtu CD19 pozitivních buněk a velikost měřitelných nádorových ložisek přispěla k jisté variabilitě hodnoty CL2 pro přípravek MabThera u hodnot získaných od 161 pacientů, kteří dostali intravenózní dávku 375 mg/m2 ve 4 týdenních dávkách. Pacienti s vyšším počtem CD19 pozitivních buněk nebo nádorových ložisek měli vyšší hodnotu CL2. Avšak i po korekci hodnot CL2 pro počet CD19 pozitivních buněk a velikost nádorových ložisek byla zřejmá interindividuální variabilita. Hodnota Vi byla ovlivněna hodnotou tělesného povrhu (BSA = body surface area) a terapií CHOP. Tato variabilita hodnoty V1 (27,1 % a 19,0 %) ovlivněná BSA (1,53 do 2,32 m2) a současnou terapií CHOP byla relativně malá. Věk, pohlaví a stavem tělesné aktivity dle WHO nijak neovlivnily farmakokinetiku přípravku MabThera. Tato analýza naznačuje, že úprava dávky přípravku MabThera by u žádné z testovaných proměnných pravděpodobně nevedla k zásadnímu omezení jeho farmakokinetické variability.
Přípravek MabThera podávaný v dávce 375 mg/m2 formou intravenózní infuze ve 4 dávkách s týdenním intervalem 203 pacientům s NHL dosud neléčeným přípravkem MabThera měl za výsledek střední hodnotu Cmax po čtvrté infuzi 486 pg/ml (rozmezí od 77,5 do 996,6 pg/ml). Rituximab byl zjistitelný v séru pacientů 3-6 měsíců po ukončení léčby.
Po podání přípravku MabThera v dávce 375 mg/m2 ve formě intravenózní infuze v 8 infuzích v týdenních odstupech 37 pacientům s NHL se zvyšovala střední hodnota Cmax s každou následnou infuzí, v rozpětí od 243 pg/ml (rozmezí 16 - 582 pg/ml) po první infuzi, až do 550 pg/ml (rozmezí 171 - 1177 pg/ml) po osmé infuzi.
Farmakokinetický profil přípravku MabThera podávaného v 6 infuzích v dávce 375 mg/m2 v kombinaci s 6 cykly chemoterapie CHOP byl podobný profilu přípravku MabThera podávaného samostatně.
Chronická lymfocytární leukemie
Přípravek MabThera byl podáván pomocí intravenózní infuze v prvním cyklu v dávce 375 mg/m2 s následným zvýšením dávky na 500 mg/m2 v každém z 5 dalších cyklů v kombinaci s fludarabinem a cyklofosfamidem. Průměrná Cmax (N=15) byla 408 pg/ml (rozmezí 97 - 764 pg/ml) po páté infuzi 500 mg/m2 a průměrný terminální poločas byl 32 dní (rozmezí 14 - 62 dní).
Revmatoidní artritida
Po podání dvou intravenózních infuzí 1000 mg přípravku MabThera v odstupu dvou týdnů byl průměr terminálního poločasu 20,8 dne (rozmezí 8,58 až 35,9 dne), průměrná systémová clearance 0,23 l/den (rozmezí 0,091 až 0,67 l/den), průměrný distribuční objem v rovnovážném stavu 4,6 l (rozmezí 1,7 až 7,5 l). Populační farmakokinetickou analýzou při použití stejných dat byly získány obdobné průměrné hodnoty systémové clearance (0,26 l) a poločasu (20,4 dne). Z populačních farmakokinetických analýz vyplynulo, že BSA (velikost povrchu těla) a pohlaví byly nejdůležitějšími proměnnými pro vysvětlení variability farmakokinetických parametrů (PK) mezi pacienty. Po úpravě hodnot vzhledem k BSA vykazovali muži větší objem distribuce a rychlejší clearance než ženy. Farmakokinetické rozdíly spojené s pohlavím nebyly považovány za klinicky relevantní a nevyžadovaly úpravu dávky. U pacientů s jaterním poškozením nebo renální nedostatečností nejsou k dispozici žádné farmakokinetické údaje.
Farmakokinetika rituximabu byla hodnocena po podání dvou dávek 500 mg a 1000 mg intravenózně v den 1 a 15 ve čtyřech studiích. Ve všech těchto studiích byla farmakokinetika rituximabu přímo úměrná dávce v celém hodnoceném rozmezí dávek. Průměrná Cmax sérového rituximabu se po podání první infuze pohybovala v rozmezí 157 až 171 pg/ml při dávce 2 x 500 mg a v rozmezí od 298 do 341 pg/ml při dávce 2 x 1000 mg. Po druhé infúzi se průměrná Cmax pohybovala v rozmezí od 183 do 198 pg/ml při dávce 2 x 500 mg a v rozmezí od 355 do 404 pg/ml při dávce 2 x 1000 mg. Průměrný terminální poločas eliminace se pohyboval v rozmezí od 15. do 16. dne při dávce 2 x 500 mg a 17 až 21 dnů při dávce 2 x 1000 mg. Průměrná Cmax byla o 16 až 19 % vyšší po podání druhé infuze v porovnání s první infuzí u obou dávek.
Farmakokinetika rituximabu byla hodnocena po podání dvou dávek 500 mg a 1000 mg i.v. při opakovaném zahájení léčby ve druhém léčebném cyklu. Průměrná Cmax sérového rituximabu po první infuzi byla 170 až 175 pg/ml při dávce 2 x 500 mg a 317 až 370 pg/ml při dávce 2 x 1000 mg. Cmax po podání druhé infuze byla 207 pg/ml při dávce 2 x 500 mg a v rozmezí od 377 do 386 pg/ml při dávce 2 x 1000 mg. Průměrný terminální eliminační poločas po druhé infuzi po druhém cyklu byl 19 dnů při dávce 2 x 500 mg a v rozmezí od 21 do 22 dnů při dávce 2 x 1000 mg. PK parametry rituximabu byly srovnatelné v obou cyklech léčby.
U populace s nedostatečnou odpovědí na anti-TNF terapii byly farmakokinetické (PK) parametry po podání stejných dávek rituximabu (2 x 1000 mg i.v., v odstupu 2 týdnů) podobné, s průměrnou maximální sérovou koncentrací 369 pg/ml a průměrným poločasem 19,2 dne.
Granulomatóza s polyangiitidou a mikroskopická polyangiitida
Na základě populační farmakokinetické analýzy údajů od 97 pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou, kteří byli léčeni přípravkem MabThera v dávce 375 mg/m2 jednou týdně, celkem 4 dávky, byl odhadovaný medián terminálního eliminačního poločasu 23 dnů (rozmezí 9-49 dnů). Průměrná clearance a distribuční objem rituximabu byly 0,313 l/den (rozmezí 0,116-0,726 l/den) resp. 4,50 l (rozmezí 2,25-7,39 l). Farmakokinetické parametry rituximabu u těchto pacientů se zdají podobné parametrům pozorovaným u pacientů s revmatoidní artritidou.
5.3 Předklinické údaje vztahující se k bezpečnosti
Rituximab se ukázal jako látka vysoce specifická k CD20 antigenu na B-lymfocytech. Studie prováděné na opicích cynomolgus neprokázaly jiný druh toxicity než očekávanou farmakologickou depleci B-lymfocytů v periferní krvi a v lymfatických tkáních.
Studie vývojové toxicity byly provedeny u opic rodu cynomolgus při podávání dávek do 100 mg/kg (20.-50. den březosti) a neprokázaly žádnou embryotoxicitu pro plod, která by byla spojena s rituximabem. V závislosti na dávce přípravku však byla pozorována farmakologická deplece B lymfocytů v lymfatických orgánech plodu, která přetrvávala postnatálně a byla doprovázena snížením hladiny IgG u novorozených opic. Počet B lymfocytů se u těchto zvířat vrátil k normální hodnotě během 6 měsíců po narození a nedošlo ke snížené reakci na imunizaci.
Standardní testy pro vyšetření mutagenity nebyly prováděny, neboť tyto testy nejsou pro tento typ molekuly relevantní. Dlouhodobé studie na zvířatech, které by měly určovat karcinogenní potenciál rituximabu, nebyly provedeny. Nebyly provedeny konkrétní studie stanovující účinky rituximabu na fertilitu. V obecných studiích toxicity na opicích cynomolgus nebyly pozorovány žádné škodlivé účinky na reprodukční orgány samců či samic.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Natrium-citrát Polysorbát 80 Chlorid sodný Hydroxid sodný Kyselina chlorovodíková Voda na injekci
6.2 Inkompatibility
Mezi přípravkem MabThera a polyvinylchloridem nebo polyethylenem vaků nebo infuzních setů nebyla pozorována inkompatibilita.
6.3 Doba použitelnosti
Neotevřená injekční lahvička 30 měsíců
Naředěný přípravek
Připravený infuzní roztok přípravku MabThera je fyzikálně a chemicky stabilní po dobu 24 hodin při teplotě 2 °C - 8 °C a následně pak 12 hodin při pokojové teplotě.
Z mikrobiologického hlediska by měl být připravený roztok použit okamžitě. Není-li použit okamžitě, jsou doba a podmínky uchovávání přípravku před použitím v zodpovědnosti uživatele a za normálních okolností by doba neměla překročit 24 hodin při 2 °C - 8 °C, pokud nebyl roztok naředěn za kontrolovaných a validovaných aseptických podmínek.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C). Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Podmínky uchovávání tohoto léčivého přípravku po jeho naředění jsou uvedeny v bodě 6.3.
6.5 Druh obalu a obsah balení
Injekční lahvička z čirého skla typu I, s pryžovou zátkou, obsahující 100 mg rituximabu v 10 ml.
Jedno balení obsahuje 2 injekční lahvičky.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Přípravek MabThera je připravený ve sterilní, nepyrogenní lahvičce pro jedno použití bez přísady konzervačních látek.
Asepticky se natáhne do stříkačky potřebné množství a rozředí se ve sterilním, apyrogenním roztoku chloridu sodného 9 mg/ml (0,9 %) nebo ve vodném roztoku 5 % D-glukózy. Aby se výsledný roztok dobře promíchal, je nutné jemně obrátit vak vzhůru nohama, aby se nevytvořila pěna. Zvláštní péče musí být věnována aseptickým podmínkám při přípravě roztoku, neboť léčebný přípravek neobsahuje žádné antimikrobiální nebo bakteriostatické konzervační látky. Léčebný přípravek k parenterálnímu použití by měl být ještě před aplikací vizuálně zkontrolován z hlediska obsahu pevných částic a změny barvy.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/98/067/001
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 2. června 1998
Datum posledního prodloužení registrace: 2. června 2008
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu/.
NÁZEV PŘÍPRAVKU
1.
MabThera 500 mg koncentrát pro infuzní roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden ml obsahuje 10 mg rituximabum.
Jedna injekční lahvička obsahuje 500 mg rituximabum.
Rituximab je genetickým inženýrstvím získaná chimérická myší/lidská monoklonální protilátka. Jde o glykosylovaný imunoglobulin s lidskou IgG1 konstantní částí, zatímco variabilní části lehkých a těžkých řetězců jsou myšího původu. Protilátka je produkována suspenzí uměle kultivovaných savčích buněk (ovariální buňky čínských křečků) a je purifikována afinitní chromatografií a iontoměničem. Případně přítomné viry jsou v průběhu výroby odstraněny a inaktivovány.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Koncentrát pro infuzní roztok.
Čirý, bezbarvý roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek MabThera se používá k léčbě dospělých pacientů v následujících indikacích:
Nehodgkinské lymfomy (NHL)
Přípravek MabThera je indikován pro léčbu dosud neléčených nemocných s folikulárním lymfomem III. a IV. klinického stádia v kombinaci s chemoterapií.
Udržovací léčba přípravkem MabThera je indikována k léčbě pacientů s folikulárním lymfomem, kteří odpovídají na indukční léčbu.
Přípravek MabThera v monoterapii je indikován k léčbě pacientů s folikulárním lymfomem III.- IV. klinického stádia, kteří se nacházejí ve druhém či dalším relapsu po chemoterapii nebo jejichž nádor je chemorezistentní.
Přípravek MabThera je v kombinaci s chemoterapií CHOP (cyklofosfamid, doxorubicin, vinkristin, prednizolon) indikován k léčbě nemocných s CD20 pozitivním difúzním velkobuněčným nehodgkinským maligním lymfomem z B buněk.
Chronická lymfocytární leukemie (CLL)
Přípravek MabThera je indikován v kombinaci s chemoterapií k léčbě pacientů s dříve neléčenou a relabující/refrakterní CLL. K dispozici jsou pouze omezené údaje týkající se účinnosti a bezpečnosti u pacientů dříve léčených monoklonálními protilátkami včetně přípravku MabThera nebo u pacientů nereagujících na předchozí léčbu přípravkem MabThera a chemoterapií.
Viz bod 5.1 pro další informace.
Přípravek MabThera je v kombinaci s metotrexátem indikován k léčbě dospělých pacientů s těžkou aktivní revmatoidní artritidou, kteří na léčbu dalšími nemoc modifikujícími protirevmatickými léčivými přípravky (DMARD, disease-modifying anti-rheumatic drugs), včetně jedné či více terapií inhibitory tumor nekrotizujícího faktoru (TNF, tumour necrosis factor), odpovídali nedostatečně nebo léčbu netolerovali.
Bylo prokázáno, že přípravek MabThera, pokud se podává v kombinaci s metotrexátem, snižuje rychlost progrese kloubního poškození, měřeného pomocí RTG vyšetření, a zlepšuje fyzické funkce.
Granulomatóza s polyangiitidou a mikroskopická polyangiitida
Přípravek MabThera je v kombinaci s glukokortikoidy indikován k indukci remise u dospělých pacientů se závažnou aktivní granulomatózou s polyangiitidou (Wegenerova granulomatóza) (GPA) a mikroskopickou polyangiitidou (MPA).
4.2 Dávkování a způsob podání
Přípravek MabThera má být podáván pod pečlivým dohledem zkušeného zdravotnického pracovníka a v prostředí, kde je okamžitě dostupné úplné vybavení pro resuscitaci (viz bod 4.4).
Před každým podáním přípravku MabThera je vždy třeba podat premedikaci, kterou tvoří antipyretikum a antihistaminikum, např. paracetamol a difenhydramin.
U pacientů s nehodgkinským lymfomem a chronickou lymfocytární leukemií má být zvážena premedikace glukokortikoidy, pokud není přípravek MabThera podáván v kombinaci s chemoterapeutickým režimem obsahujícím glukokortikoidy.
U pacientů s revmatoidní artritidou je třeba ke snížení incidence a závažnosti reakcí souvisejících s infuzí podat premedikaci 100 mg methylprednisolonu intravenózně 30 minut před podáním infuze přípravku MabThera.
U pacientů s granulomatózou s polyangiitidou (Wegenerova granulomatóza) nebo mikroskopickou polyangiitidou se doporučuje intravenózní podání methylprednisolonu po dobu 1 až 3 dnů v dávce 1000 mg denně před podáním první infuze přípravku MabThera (poslední dávku methylprednisolonu lze podat ve stejný den jako první infuzi přípravku MabThera). Na intravenózní léčbu má navazovat perorální léčba prednisonem v dávce 1 mg/kg/den (celková denní dávka nesmí přesáhnout 80 mg a snižuje se tak rychle, jak je to na základě klinického stavu možné) a to v průběhu léčby přípravkem MabThera i po jejím ukončení.
Dávkování
Je důležité zkontrolovat označení přípravku a ujistit se, že je podáván správný přípravek (pro intravenózní nebo subkutánní podání), který byl pacientovi předepsán.
Nehodskinské lymfomy
Folikulární lymfom
Kombinovaná léčba
Doporučená dávka přípravku MabThera v kombinaci s chemoterapií v rámci indukční léčby pacientů s dosud neléčeným nebo relabujícím/refrakterním folikulárním lymfomem je: 375 mg/m2 tělesného povrchu v každém cyklu, až do celkového počtu 8 cyklů.
Přípravek MabThera má být podáván v den 1 každého cyklu chemoterapie, po nitrožilním podání glukokortikoidu, pokud je součástí chemoterapeutického režimu.
Udržovací léčba
• Dosud neléčený folikulární lymfom
Doporučená dávka přípravku MabThera v udržovací léčbě pacientů s dosud neléčeným folikulárním lymfomem, kteří odpověděli na indukční léčbu, je: 375 mg/m2 tělesného povrchu jednou za 2 měsíce (zahájení udržovací léčby 2 měsíce po poslední dávce indukční léčby) do progrese nemoci či nejdéle po dobu dvou let.
• Relabující/refrakterní folikulární lymfom
Doporučená dávka přípravku MabThera v udržovací léčbě pacientů s relabujícím/refrakterním folikulárním lymfomem, kteří odpověděli na indukční léčbu, je: 375 mg/m2 tělesného povrchu jednou za 3 měsíce (zahájení udržovací léčby 3 měsíce po poslední dávce indukční léčby) do progrese nemoci či nejdéle po dobu dvou let.
Monoterapie
• Relabující/refrakterní folikulární lymfom
Doporučená dávka přípravku MabThera v monoterapii při indukční léčbě dospělých pacientů s folikulárním lymfomem stádia III-IV, jejichž nádor je chemorezistentní, či kteří se nacházejí v druhém či dalším relapsu po předchozí chemoterapii, je: 375 mg/m2 tělesného povrchu, podávaná jako nitrožilní infuze jednou týdně po dobu čtyř týdnů.
Pro opakovanou léčbu přípravkem MabThera v monoterapii u pacientů, kteří odpověděli na předchozí léčbu relabujícího/refrakterního folikulárního lymfomu monoterapií přípravkem MabThera, je doporučená dávka: 375 mg/m2 tělesného povrchu, podávaná jako nitrožilní infuze jednou týdně po dobu čtyř týdnů (viz bod 5.1).
Difúzní velkobuněčný nehodgkinský lymfom z B buněk
Přípravek MabThera by měl být použit v kombinaci s chemoterapií CHOP. Doporučená dávka přípravku, 375 mg/m2 tělesného povrchu, se podává 1. den každého z 8 chemoterapeutických cyklů po intravenózní aplikaci glukokortikoidu, který je součástí režimu CHOP. Bezpečnost a účinnost přípravku MabThera v kombinaci s jinými chemoterapeutickými režimy v léčbě difúzního B-velkobuněčného lymfomu nebyly dosud stanoveny.
Úprava dávkování v průběhu léčby
Redukce dávkování přípravku MabThera není doporučena. Při kombinaci přípravku MabThera s chemoterapií CHOP mohou být chemoterapeutika redukována podle standardních pravidel.
Chronická lvmfocvtární leukemie
K omezení rizika syndromu z rozpadu nádoru je u pacientů s CLL doporučována profylaxe s dostatečnou hydratací a podáním antiuratik zahájená 48 hodin před zahájením léčby. U pacientů s CLL s počtem lymfocytů vyšším než 25 x 109/l je doporučováno podání prednisonu/prednisolonu v dávce 100 mg intravenózně krátce před infuzí přípravku MabThera, aby se snížil výskyt a závažnost akutní reakce na infuzi a/nebo syndromu z uvolnění cytokinů.
Doporučená dávka přípravku MabThera v kombinaci s chemoterapií u dříve neléčených a relabujících/refrakterních pacientů je 375 mg/m2 tělesného povrchu v den 0 prvního cyklu léčby následovaná dávkou 500 mg/m2 tělesného povrchu podávanou v den 1 každého z následujících celkem 6 cyklů léčby. Chemoterapie by měla být podávána po infuzi přípravku MabThera.
Pacientům léčeným přípravkem MabThera musí být při každé infuzi předána Karta pro pacienta.
Cyklus léčby spočívá v podání dvou intravenózních infuzí 1000 mg přípravku MabThera. Doporučená dávka 1000 mg přípravku MabThera podaná intravenózní infuzí je následována druhou intravenózní infuzí 1000 mg o dva týdny později.
Nutnost dalších cyklů léčby je třeba zhodnotit za 24 týdnů po předchozím cyklu. Opakovanou léčbu je třeba zahájit tehdy, pokud reziduální aktivita onemocnění přetrvává, v opačném případě je třeba opakování léčby odložit až do návratu aktivity onemocnění.
Dostupné údaje naznačují, že klinické odpovědi se obvykle dosáhne během 16 - 24 týdnů úvodního léčebného cyklu. U pacientů, kteří v průběhu tohoto období nevykazují žádné známky prospěchu z léčby, je třeba pokračování v léčbě pečlivě zvážit.
Granulomatóza s polyangiitidou a mikroskopická polyangiitida
Pacientům léčeným přípravkem MabThera musí být při každé infuzi předána Karta pro pacienta.
Doporučené dávkování přípravku MabThera při indukci remise v léčbě granulomatózy s polyangiitidou a mikroskopické polyangiitidy je 375 mg/m2 plochy tělesného povrchu podávané ve formě intravenózní infuze jednou týdně po dobu 4 týdnů (celkem 4 infuze).
U pacientů s granulomatózou s polyangiitidou nebo mikroskopickou polyangiitidou se během léčby přípravkem MabThera a po jejím ukončení (podle potřeby) doporučuje profylaxe pneumonie způsobené Pneumocystis jirovecii (PCP).
Zvláštní _ populace
Pediatrická populace
Účinnost a bezpečnost léčby přípravkem MabThera u dětí mladších 18 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
Starší pacienti
U starších pacientů (ve věku > 65 let) není zapotřebí žádná úprava dávkování.
Způsob podání
Připravený roztok MabThera má být podáván ve formě nitrožilní infuze samostatnou infuzní hadičkou. Neaplikujte připravený infuzní roztok jako nitrožilní injekci nebo bolus.
Pacienti by měli být pečlivě monitorováni s ohledem na možnost rozvoje syndromu z uvolnění cytokinů (viz bod 4.4). Pacientům, u nichž dojde k rozvoji těžkých reakcí, především těžké dušnosti, bronchospazmu nebo hypoxie, musí být infuze okamžitě zastavena. U pacientů s nehodgkinským lymfomem by měla být posouzena možnost vzniku syndromu z rozpadu tumoru, měly by být provedeny příslušné laboratorní testy a rentgenové vyšetření plic k průkazu možné plicní infiltrace. Podání infuzní terapie by u žádného pacienta nemělo být obnoveno dříve, než dojde k úplnému vymizení nežádoucích příznaků a k normalizaci laboratorních hodnot a RTG nálezu. Rychlost podání infuze přitom musí být poloviční nebo nižší než původní rychlost infuze. Pokud se znovu objeví stejné těžké nežádoucí účinky, mělo by být individuálně zváženo ukončení léčby.
Mírné až středně závažné nežádoucí účinky vznikající v důsledku podávání infuze (viz bod 4.8) obvykle odpovídají na snížení rychlosti infuze. Rychlost infuze může být po úpravě symptomů opět zvýšena.
První infuze
Doporučená úvodní rychlost infuze je 50 mg/hod; po prvních 30 minutách může být postupně zvyšována o 50 mg/hod, a takto lze postupně pokračovat vždy po 30 minutách až do maximální rychlosti 400 mg/hod.
Následné infuze
Všechny indikace
Následné dávky přípravku MabThera mohou být podávány úvodní rychlostí 100 mg/hod, a v 30minutových intervalech zvyšovány o 100 mg/hod až k nejvyšší rychlosti 400 mg/hod.
Informace týkající se pouze revmatoidní artritidy
Další možnost následného, zrychleného režimu infuze
Pacientům, u kterých se nevyskytly závažné nežádoucí účinky související s infuzí při podání první nebo následné infuze v dávce 1000 mg přípravku MabThera v rámci stanoveného plánu podávání, mohou být druhá a další následné infuze podány ve zrychleném režimu při použití stejné koncentrace jako u předchozích infuzí (4 mg/ml v objemu 250 ml). Počáteční rychlost infuze je 250 mg/hod prvních 30 minut a pak 600 mg/hod následujících 90 minut. Pokud je zrychlený režim infuze dobře snášen, tento režim infuze může být použit při podání následujících infuzí.
Pacientům, kteří mají klinicky významné kardiovaskulární onemocnění, včetně arytmie, nebo kteří prodělali závažné reakce na infuzi jakékoli dřívější biologické léčby nebo na rituximab, nesmí být zrychlený režim infuze podán.
4.3 Kontraindikace
Kontraindikace použití u nehodgkinských lymfomů a chronické lymfocytární leukemie
Hypersenzitivita na léčivou látku nebo na myší bílkoviny nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Aktivní, závažné infekce (viz bod 4.4).
Pacienti se závažným útlumem imunitního systému.
Kontraindikace použití u revmatoidní artritidy, granulomatózy s polyangiitidou a mikroskopické polvangiitidv
Hypersenzitivita na léčivou látku nebo na myší bílkoviny nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Aktivní, závažné infekce (viz bod 4.4).
Pacienti se závažným útlumem imunitního systému.
Těžké selhání srdce (třída IV dle New York Heart Association) nebo těžké, léčbou neupravené onemocnění srdce (další kardiovaskulární onemocnění, viz bod 4.4).
4.4 Zvláštní upozornění a opatření pro použití
Z důvodu snadnější zpětné zjistitelnosti biologických léčivých přípravků má být obchodní název a číslo šarže podávaného přípravku zřetelně zaznamenáno (nebo vyznačeno) v pacientově dokumentaci.
Progresivní multifokální leukoencefalopatie
Všem pacientům léčeným přípravkem MabThera z důvodu revmatoidní artritidy, granulomatózy s polyangiitidou a mikroskopické polyangiitidy musí být při každé infuzi předána Karta pro pacienta. Karta pro pacienta obsahuje důležité bezpečnostní informace pro pacienty týkající se možného zvýšení rizika infekcí, včetně progresivní multifokální leukoencefalopatie (PML).
Ve velmi vzácných případech byla po užití přípravku MabThera hlášena PML končící úmrtím.
Pacienti musí být v pravidelných intervalech sledováni pro jakékoli nové nebo zhoršující se neurologické symptomy nebo příznaky, které by mohly naznačovat PML. V případě podezření na PML musí být další podávání přípravku pozastaveno, dokud není diagnóza PML vyloučena. Lékař by měl vyhodnotit stav pacienta, aby bylo možno určit, zda příznaky ukazují na neurologickou dysfunkci, a v kladném případě, zda příznaky ukazují na PML. Dle klinické indikace by měla být zvážena konzultace s neurologem.
Při jakýchkoli pochybnostech by měla být zvážena další vyšetření včetně magnetické rezonance, přednostně s kontrastem, vyšetření mozkomíšního moku na JC virovou DNA a opakované neurologické vyšetření.
Lékař by měl věnovat zvláštní pozornost symptomům, které naznačují PML, ale kterých si pacient nemusí všimnout (např. kognitivní, neurologické nebo psychiatrické symptomy). Nemocnému by mělo být doporučeno, aby o léčbě informoval svého partnera nebo osobu, která o něho pečuje, protože ti si mohou všimnout příznaků, které sám nemocný nezaznamená.
Pokud dojde ke vniku PML, podávání přípravku MabThera musí být trvale ukončeno.
Po rekonstituci imunitního sytému u imunosuprimovaných nemocných s PML bylo možno pozorovat stabilizaci nebo zlepšení. Nadále není známo, zda časná detekce PML a ukončení léčby přípravkem MabThera může vést k podobné stabilizaci či zlepšení.
Nehodgkinské lymfomy a chronická lymfocytární leukemie
Reakce související s infuzí
Podání přípravku MabThera je spojeno s reakcemi souvisejícími s infuzí, které mohou souviset s uvolněním cytokinů a/nebo dalších chemických mediátorů. Syndrom z uvolnění cytokinů může být klinicky nerozeznatelný od akutních hypersenzitivních reakcí.
Tento soubor reakcí, které zahrnují syndrom z uvolnění cytokinů, syndrom nádorového rozpadu a anafylaktické či hypersenzitivní reakce, je popsán níže. Reakce nejsou specificky spojené s cestou podání přípravku MabThera a lze je pozorovat u obou forem.
Po uvedení přípravku na trh byly hlášeny závažné reakce související s infuzí, které končily úmrtím, při použití přípravku MabThera pro intravenózní podání s nástupem během 30 minut až 2 hodin po zahájení první intravenózní infuze přípravkem MabThera. Ty byly charakterizovány plicními příhodami a v některých případech zahrnovaly rychlý rozpad nádoru s rysy syndromu nádorového rozpadu, navíc horečku, zimnici, třesavku, hypotenzi, kopřivku, angioedém a další symptomy (viz bod 4.8).
Těžký syndrom z uvolnění cytokinů je charakterizován těžkou dušností, často doprovázenou bronchospazmem a hypoxií, dále horečkou, zimnicí, třesavkou, urtikou a angioedémem. Tento syndrom může být spojen s některými příznaky syndromu z rozpadu tumoru, jako jsou hyperurikémie, hyperkalémie, hypokalcémie, hyperfosfatémie, akutní renální selhání, zvýšení laktát dehydrogenázy (LDH), a může být spojen s akutním respiračním selháním a úmrtím pacienta. Akutní respirační selhání může být provázeno plicní intersticiální infiltrací nebo edémem plic, viditelným na rentgenovém vyšetření. Tento syndrom se často objevuje v průběhu jedné až dvou hodin po zahájení první infuze. U pacientů s anamnézou plicní insuficience nebo u pacientů s nádorovou infiltrací plic je větší nebezpečí nepříznivého průběhu, a proto by tito pacienti měli být léčeni se zvýšenou opatrností.
U pacientů, u kterých dojde k rozvoji těžkého syndromu z uvolnění cytokinů, musí být infuze okamžitě zastavena (viz bod 4.2) a musí u nich být zahájena intenzivní symptomatická léčba. Vzhledem k tomu, že počáteční zlepšení klinických příznaků může být následováno opětovným zhoršením celkového stavu, měli by být pacienti pečlivě monitorováni až do doby, kdy projevy syndromu z rozpadu tumoru a plicní infiltrace vymizí nebo tento syndrom je vyloučen. Další pokračování léčby po úplném vymizení příznaků vedlo vzácně k opakování těžkého syndromu z uvolnění cytokinů.
Pacienti s velkou nádorovou zátěží nebo s vysokým počtem (> 25 x 109/l) cirkulujících maligních buněk, jako jsou pacienti s CLL, u kterých může být zvýšené riziko zejména těžkého syndromu z uvolnění cytokinů, mají být léčeni s nejvyšší opatrností. Tito pacienti mají být velmi pečlivě monitorováni v průběhu první infuze. U těchto pacientů je třeba zvážit snížení rychlosti při podávání první infuze nebo rozdělení dávky v prvním a jakémkoli následujícím cyklu léčby do dvou dnů, pokud je počet lymfocytů stále >25 x 109/l.
Nežádoucí reakce všech typů vznikající v souvislosti s podáním infuze byly pozorovány u 77 % pacientů léčených přípravkem MabThera (včetně syndromu z uvolnění cytokinů doprovázeného hypotenzí a bronchospazmem u 10 % pacientů), viz bod 4.8. Tyto symptomy jsou obvykle reverzibilní po přerušení infuze přípravku a po podání antipyretik, antihistaminik, a podle potřeby po podání kyslíku, infuze fyziologického roztoku nebo bronchodilatancií a glukokortikoidů. Těžké reakce při syndromu z uvolnění cytokinů - viz výše.
Po intravenózním podání bílkovin pacientům byly hlášeny anafylaktické nebo jiné hypersenzitivní reakce. Na rozdíl od syndromu z uvolnění cytokinů se skutečná hypersenzitivní reakce objevuje typicky během několika minut po zahájení infuze. Pro případ rozvoje alergické reakce v průběhu podávání přípravku MabThera, musí být léčiva užívaná k léčbě hypersenzitivní reakce, např. epinefrin (adrenalin), antihistaminika a glukokortikoidy, ihned k dispozici. Klinické příznaky anafylaktické reakce mohou být podobné klinickým příznakům syndromu z uvolnění cytokinů (viz výše). Reakce z přecitlivělosti byly hlášeny méně často než reakce vznikající v souvislosti s uvolněním cytokinů.
Dalšími reakcemi hlášenými v některých případech byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie.
Vzhledem k tomu, že se v průběhu podání přípravku MabThera může objevit hypotenze, mělo by být zváženo přechodné vysazení antihypertenziv 12 hodin před infuzí přípravku MabThera.
Srdeční poruchy
U pacientů léčených přípravkem MabThera se objevily angina pectoris, srdeční arytmie typu fibrilace či flutter síní, srdeční selhání a/nebo infarkt myokardu. Pacienti s anamnézou srdečního onemocnění a/nebo kardiotoxickou chemoterapií mají proto být pečlivě monitorováni.
Hematologická toxicita
Přestože MabThera v monoterapii nepůsobí myelosupresivně, je u nemocných s počtem neutrofilů < 1,5 x 109/l a/nebo trombocytů < 75 x 109/l potřeba opatrnosti, vzhledem k tomu, že u této skupiny nemocných jsou jen malé zkušenosti s podáním přípravku MabThera. Přípravek MabThera byl podán 21 nemocným, kteří podstoupili autologní transplantaci kostní dřeně nebo jinak rizikovým nemocným s předpokládanou redukovanou funkcí kostní dřeně, aniž by byla vyvolána myelotoxicita.
Během léčby přípravkem MabThera je třeba pravidelně kontrolovat kompletní krevní obraz, včetně počtu neutrofilů a trombocytů.
Infekce
Během léčby přípravkem MabThera se mohou objevit závažná infekční onemocnění, včetně onemocnění vedoucích k úmrtí (viz bod 4.8) Přípravek MabThera by neměl být podáván pacientům s aktivním závažným infekčním onemocněním (např. tuberkulózou, sepsí a oportunními infekcemi, viz bod 4.3).
Lékaři by měli pečlivě zvážit použití přípravku MabThera u pacientů s anamnézou opakovaných či chronických infekčních onemocnění či u pacientů s průvodními chorobami, které by mohly u pacientů dále přispět k náchylnosti k závažným infekčním chorobám (viz bod 4.8).
U pacientů léčených přípravkem MabThera byly popsány případy reaktivace hepatitidy B, včetně hlášení fulminantní hepatitidy s následným úmrtím. Většina těchto pacientů byla rovněž léčena cytotoxickou chemoterapií. Omezené množství informací z jedné studie s pacienty trpícími relabující/refrakterní CLL naznačuje, že léčba přípravkem MabThera by mohla také zhoršit primární infekci hepatitidou B. U všech pacientů má být před zahájením léčby přípravkem MabThera proveden screening na virus hepatitidy B (HBV). Screening má minimálně zahrnovat vyšetření HBsAg-statusu a HBcAb-statusu. Tato vyšetření mohou být doplněna dalšími vhodnými vyšetřeními v souladu s lokálními postupy. Pacienti s aktivním onemocněním hepatitidy B nemají být léčeni přípravkem MabThera. Pacienti se sérologicky pozitivní hepatitidou B (buď HBsAg nebo HBcAb) mají být před zahájením léčby odesláni na odborné vyšetření ke specialistovi na jaterní onemocnění, v průběhu léčby mají být tito pacienti pečlivě sledováni a léčeni v souladu s lokálními medicínskými postupy k prevenci reaktivace hepatitidy B.
U pacientů s NHL a CLL byly po uvedení přípravku MabThera na trh velmi vzácně hlášeny případy progresivní multifokální leukoencefalopatie (PML) (viz bod 4.8) Většina z pacientů dostávala přípravek MabThera v kombinaci s chemoterapií nebo jako součást transplantace krvetvorných kmenových buněk.
Očkování
Bezpečnost očkování živými virovými vakcínami po léčbě přípravkem MabThera nebyla u pacientů s NHL a CLL studována a očkování živými virovými vakcínami není doporučeno. Pacienti léčení přípravkem MabThera mohou podstoupit očkování neživými vakcínami. Účinnost očkování neživými vakcínami však může být nižší. V nerandomizované studii měli pacienti s relapsem nízce maligního NHL léčení monoterapií přípravkem MabThera ve srovnání se zdravými kontrolami nižší odpověď na přeočkování tetanem (16 % vs. 81 %) a očkování látkou Keyhole Limpet Haemocyanin (KLH) (4 % vs. 76 % při zjišťování dvojnásobného vzestupu titru protilátek). U pacientů s CLL je možné vzhledem k podobnosti obou chorob očekávat podobné výsledky, ale nebylo to dosud ověřeno v klinických studiích.
Průměrné hodnoty titrů protilátek proti panelu antigenů (Streptococcus pneumoniae, chřipka A, příušnice, zarděnky, plané neštovice) byly udrženy nejméně 6 měsíců po léčbě přípravkem MabThera.
Kožní reakce
Byly popsány závažné kožní reakce, jako je například toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím (viz bod 4.8). V případě výskytu takovéto příhody, s podezřením na souvislost s podáním přípravku MabThera, má být léčba trvale přerušena.
Revmatoidní artritida, granulomatóza s polyangiitidou a mikroskopická polyangiitida
Populace pacientů s revmatoidní artritidou, která dosud nebyla léčena metotrexátem (MTX)
Užití přípravku MabThera není doporučeno u pacientů, kteří dosud nebyli léčeni MTX, protože u nich nebylo potvrzeno, zda prospěch z léčby převáží její rizika.
Reakce související s infuzí
Podání přípravku MabThera je spojeno s reakcemi souvisejícími s infuzí (IRR, infusion related reaction), které mohou souviset s uvolněním cytokinů a/nebo dalších chemických mediátorů. Před každou infuzí přípravku MabThera je vždy třeba podat premedikaci, kterou tvoří analgetikum/antipyretikum a antihistaminikum. Ke snížení četnosti a závažnosti reakcí souvisejících s infuzí je třeba u pacientů s revmatoidní artritidou před každou infuzí přípravku MabThera rovněž provést premedikaci glukokortikoidy (viz bod 4.2 a bod 4.8).
U pacientů s revmatoidní artritidou byly po uvedení přípravku na trh hlášeny závažné reakce související s infuzí, které končily úmrtím. Většina příhod souvisejících s infuzí u pacientů s revmatoidní artritidou, které byly hlášeny v klinických studiích, byla mírné až střední závažnosti. Nejčastějšími příznaky byly alergické reakce jako bolest hlavy, svědění, podráždění v krku, návaly horka, vyrážka, kopřivka, hypertenze a pyrexie. Obecně byl podíl pacientů, u kterých se objevila jakákoli infuzní reakce, vyšší po první infuzi než po druhé infuzi jakéhokoli cyklu léčby. Incidence IRR klesala s následujícími cykly léčby (viz bod 4.8). Hlášené reakce byly obvykle reverzibilní po snížení rychlosti infuze nebo po přerušení infuze přípravku MabThera a po podání antipyretik a antihistaminik, podle potřeby po podání kyslíku, infuze fyziologického roztoku nebo bronchodilatancií a glukokortikoidů. Pacienty s preexistujícím kardiálním onemocněním a pacienty s anamnézou kardiopulmonálních nežádoucích účinků je nutné pečlivě sledovat. V závislosti na závažnosti reakce související s infuzí a požadovaném zásahu, je nutné dočasně nebo trvale ukončit léčbu přípravkem MabThera. V mnoha případech mohla být infuze obnovena při 50 % snížení rychlosti (např. ze 100 mg/h na 50 mg/h) po úplném vymizení nežádoucích příznaků.
Pro případ rozvoje alergické reakce v průběhu podávání přípravku MabThera musí být ihned k dispozici léčiva užívaná k léčbě hypersenzitivní reakce, např. epinefrin (adrenalin), antihistaminika a glukokortikoidy.
O bezpečnosti přípravku MabThera u pacientů se středně závažným srdečním selháním (třída III dle NYHA) nebo se závažným nekontrolovaným onemocněním srdce nejsou k dispozici žádné údaje. U pacientů léčených přípravkem MabThera, u nichž se současně vyskytovalo preexistující ischemické onemocnění srdce jako angina pectoris, infarkt myokardu a fibrilace či flutter síní, došlo k symptomatickému výskytu tohoto onemocnění. U pacientů s anamnézou srdečního onemocnění a pacientů s anamnézou kardiopulmonálních nežádoucích účinků má proto být před podáním přípravku MabThera zváženo riziko kardiovaskulárních komplikací způsobených infuzní reakcí a pacienti mají být během podávání infuze pečlivě monitorováni. Vzhledem k tomu, že se v průběhu podání infuze přípravku MabThera může objevit hypotenze, mělo by být zváženo přechodné vysazení antihypertenziv 12 hodin před infuzí přípravku MabThera.
Reakce související s infuzí byly u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou podobné reakcím pozorovaným v klinických studiích u pacientů s revmatoidní artritidou (viz bod 4.8).
Srdeční poruchy
U pacientů léčených přípravkem MabThera se objevily angina pectoris, srdeční arytmie typu fibrilace či flutter síní, srdeční selhání a/nebo infarkt myokardu. Pacienti s anamnézou srdečního onemocnění mají proto být pečlivě monitorováni (viz výše Reakce související s infuzí).
Infekce
Na základě mechanismu účinku přípravku MabThera a znalosti, že B-buňky hrají důležitou roli v udržování normální imunitní odpovědi, může u pacientů po léčbě přípravkem MabThera dojít ke zvýšení rizika infekce (viz bod 5.1). Během terapie přípravkem MabThera se mohou vyskytnout závažné infekce, včetně případů s fatálním průběhem (viz bod 4.8). Přípravek MabThera by neměl být podáván pacientům s akutní, závažnou infekcí (např. tuberkulóza, sepse a oportunní infekce, viz bod 4.3) nebo pacientům se sníženou funkcí imunitního systému (např. při velmi nízkém počtu CD4 a CD8). Lékaři musí pečlivě zvážit použití přípravku MabThera u pacientů s anamnézou chronických infekcí nebo v podmínkách, které mohou zvýšit náchylnost pacientů k vážným infekcím, např. hypogamaglobulinémii (viz bod 4.8). Před zahájením léčby přípravkem MabThera se doporučuje stanovit hladiny imunoglobulinů.
Pacienti vykazující známky a symptomy infekce po léčbě přípravkem MabThera by měli být okamžitě vyšetřeni a vhodně léčeni. Před podáním dalšího cyklu léčby přípravkem MabThera by u pacientů mělo být znovu posouzeno potenciální riziko infekce.
Po podávání přípravku MabThera k léčbě revmatoidní artritidy a autoimunitních onemocnění, včetně systémového lupus erytematodes (SLE) a vaskulitidy, byly velmi vzácně zaznamenány případy fatální progresivní multifokální leukoencefalopatie (PML).
Infekce hepatitidy B
U pacientů s revmatoidní artritidou, granulomatózou s polyangiitidou a mikroskopickou polyangiitidou léčených přípravkem MabThera byly hlášeny případy reaktivace hepatitidy B, včetně těch, které končily úmrtím.
U všech pacientů má být před zahájením léčby přípravkem MabThera proveden screening na virus hepatitidy B (HBV). Screening má minimálně zahrnovat vyšetření HBsAg-statusu a HBcAb-statusu. Tato vyšetření mohou být doplněna dalšími vhodnými vyšetřeními v souladu s lokálními postupy. Pacienti s aktivním onemocněním hepatitidy B nemají být léčeni přípravkem MabThera. Pacienti se sérologicky pozitivní hepatitidou B (buď ABsAg nebo HBcAb) mají být před zahájením léčby odesláni na odborné vyšetření ke specialistovi na jaterní onemocnění, v průběhu léčby mají být tito pacienti pečlivě sledováni a léčeni v souladu s lokálními medicínskými postupy k prevenci reaktivace hepatitidy B.
Pozdní neutropenie
Je třeba měření neutrofilů v krvi před každým cyklem léčby přípravkem MabThera a pravidelně až po dobu 6 měsíců po ukončení léčby a při známkách nebo příznacích infekce (viz bod 4.8).
Kožní reakce
Byly popsány závažné kožní reakce, jako je například toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím (viz bod 4.8). V případě výskytu takovéto příhody, s podezřením na souvislost s podáním přípravku MabThera, má být léčba trvale přerušena.
Očkování
Lékaři by před zahájením léčby přípravkem MabThera měli posoudit stav očkování pacienta a držet se stávajících očkovacích doporučení. Očkování by mělo být dokončeno nejméně 4 týdny před prvním podáním přípravku MabThera.
Bezpečnost očkování živými virovými vakcínami po léčbě přípravkem MabThera nebyla studována. Proto není doporučeno očkování živými virovými vakcínami během léčby přípravkem MabThera a po dobu deplece B-lymfocytů v periferní krvi.
Pacienti léčení přípravkem MabThera mohou podstoupit očkování neživými vakcínami. Účinnost očkování neživými vakcínami však může být nižší. V randomizované studii měli pacienti s revmatoidní artritidou léčení přípravkem MabThera a metotrexátem ve srovnání s pacienty léčenými pouze metotrexátem srovnatelnou odpověď na přeočkování tetanem (39 % vs. 42 %), nižší četnost odpovědí na pneumokokovou polysacharidovou vakcínu (43 % vs. 82 % na alespoň 2 sérotypy pneumokokových protilátek) a očkování antigenem KLH (47 % vs. 93 %) pokud byly podávány 6 měsíců po léčbě přípravkem MabThera. Pokud je potřeba během léčby přípravkem MabThera provést očkování neživou vakcínou, toto očkování by mělo být dokončeno alespoň 4 týdny před dalším cyklem léčby přípravkem MabThera.
Celkově byl u revmatoidní artritidy po opakované léčbě přípravkem MabThera po dobu delší než 1 rok podíl pacientů s pozitivními titry protilátek proti S. pneumoniae, chřipce, spalničkám, zarděnkám, planým neštovicím a tetanovému anatoxinu v zásadě podobný s podíly při zahájení léčby.
Současné/následné užívání jiných DMARD u pacientů s revmatoidní artritidou
Současné užívání přípravku MabThera a protirevmatických terapií jiných, než jsou ty uvedené pod
indikací revmatoidní artritida, se nedoporučuje.
Jsou pouze omezené údaje z klinických studií, které by umožnili plně zhodnotit bezpečnost následného použití DMARDs (včetně inhibitorů TNF a jiných biologických látek) po léčbě přípravkem MabThera (viz bod 4.5). Dostupná data naznačují, že výskyt klinicky významné infekce se při této léčbě u pacientů dříve léčených přípravkem MabThera nemění, pokud jsou však pacienti po léčbě přípravkem MabThera léčeni biologickými léky a/nebo DMARDs, měli by být pečlivě sledováni kvůli příznakům infekce.
Maligní onemocnění
Imunomodulační látky mohou zvyšovat riziko vzniku malignit. Na základě omezených zkušeností s podáváním přípravku MabThera pacientům s revmatoidní artritidou (viz bod 4.8) se nezdá, že by dostupné údaje nasvědčovaly jakémukoli zvýšení rizika vzniku malignit. Možné riziko rozvoje solidních tumorů však nelze v současné době vyloučit.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
V současné době jsou k dispozici pouze omezené údaje o možných lékových interakcích s přípravkem MabThera.
U pacientů s CLL, kterým byl spolu s přípravkem MabThera podáván fludarabin nebo cyklofosfamid, nebyl pozorován žádný účinek na jejich farmakokinetiku. Kromě toho nebyl pozorován žádný zjevný účinek fludarabinu a cyklofosfamidu na farmakokinetiku přípravku MabThera.
U pacientů s revmatoidní artritidou nemělo současné podávání metotrexátu žádný vliv na farmakokinetiku přípravku MabThera.
Nemocní s protilátkami proti myším bílkovinám (HAMA) nebo s protilátkami proti chimérickým protilátkám (HACA) mohou mít hypersenzitivní nebo alergické reakce při podání jiných diagnostických nebo léčebných monoklonálních protilátek.
283 pacientů s revmatoidní artritidou dostávalo po léčbě přípravkem MabThera následnou léčbu DMARD. U těchto pacientů byl výskyt klinicky významných infekcí během léčby přípravkem MabThera 6,01 na 100 paciento-roků ve srovnání s 4,97 na 100 paciento-roků během léčby biologickým DMARD.
4.6 Fertilita, těhotenství a kojení
Antikoncepce u mužů a žen
Vzhledem k tomu, že rituximab zůstává v těle pacientů s deplecí B buněk po delší dobu, musí ženy ve fertilním věku během léčby přípravkem MabThera a 12 měsíců po jejím ukončení používat efektivní antikoncepční metody.
Je známo, že imunoglobuliny IgG přecházejí přes placentární bariéru.
Počet B lymfocytů u lidských novorozenců po podání přípravku MabThera matce nebylo v klinických hodnoceních studováno. Neexistují žádné dostatečné a dobře kontrolované údaje ze studií u těhotných žen, avšak u některých dětí narozených matkám vystaveným v průběhu těhotenství přípravku MabThera byly hlášeny přechodná deplece B buněk a lymfocytopenie. Podobné účinky byly pozorovány ve studiích na zvířatech (viz bod 5.3). Z těchto důvodů by neměla být MabThera podávána těhotným ženám s výjimkou situace, kdy možný prospěch převáží potencionální riziko.
Kojení
Není známo, zda je rituximab vylučován do lidského mléka. Vzhledem k tomu, že mateřské IgG vylučováno je, a u kojících opic byl rituximab v mléku detekován, neměly by ženy léčené přípravkem MabThera kojit během léčby a 12 měsíců po léčbě přípravkem MabThera.
Fertilita
Studie na zvířatech neprokázaly škodlivé účinky rituximabu na reprodukční orgány.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly prováděny žádné studie hodnotící účinky přípravku MabThera na schopnost řídit a obsluhovat stroje, nicméně farmakologická aktivita a dosud hlášené nežádoucí účinky ukazují, že přípravek MabThera nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Zkušenosti u nehodgkinských lymfomů a chronické lymfocytární leukemie
Shrnutí bezpečnostního _profilu
Celkový bezpečností profil přípravku MabThera je u nehodgkinských lymfomů a chronické lymfocytární leukemie založen na údajích pacientů z klinických studií a postmarketingového pozorování. Tito pacienti byli léčeni buď přípravkem MabThera v monoterapii (jako indukční léčbou nebo udržovací léčbou po indukční léčbě) nebo v kombinaci s chemoterapií.
Nej častěji pozorovanými nežádoucími účinky na lék u pacientů, kteří dostávali přípravek MabThera, byly reakce související s podáním infuze, které se u většiny pacientů objevily v průběhu první infuze. Incidence příznaků souvisejících s podáním infuze se významně snižuje u následujících infuzí a po osmi dávkách přípravku MabThera je nižší než 1 %.
K infekčním příhodám (zejména bakteriálním a virovým) došlo u přibližně 30-55 % pacientů v průběhu klinických studií u pacientů s nehodgkinskými lymfomy a u 30-50 % pacientů v klinických studiích u pacientů s CLL.
Nejčastějšími závažnými nežádoucími účinky na lék byly:
• Reakce související s podáním infuze (včetně syndromu z uvolnění cytokinů, syndromu z rozpadu tumoru), viz bod 4.4.
• Infekce, viz bod 4.4.
• Kardiovaskulární události, viz bod 4.4.
Dalšími závažnými hlášenými nežádoucími účinky na lék byly reaktivace hepatitidy B a PML (viz bod 4.4.)
Shrnutí nežádoucích účinků do tabulky
Četnosti nežádoucích účinků léčivého přípravku (NÚ), které byly hlášeny v souvislosti s podáním samotného přípravku MabThera nebo v kombinaci s chemoterapií, jsou shrnuty v Tabulce 1. Ve všech skupinách četností jsou NÚ prezentovány v pořadí podle klesající závažnosti. Četnost je definována jako velmi častá (>1/10), častá (>1/100 až <1/10), méně častá (>1/1000 až <1/100), vzácná (>1/10000 až <1/1000), velmi vzácná (<1/10000) a není známo (z dostupných údajů nelze určit).
Nežádoucí účinky, které byly zjištěny pouze v postmarketingových pozorováních a u nichž nelze určit četnost, jsou uvedeny jako „není známo“.
v postmarketingovém pozorování u pacientů s nehodgkinským lymfomem léčených přípravkem MabThera monoterapií/udržovací léčbou nebo v kombinaci s chemoterapií _____
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Infekce a infestace |
bakteriální infekce, virové infekce, + bronchitida |
sepse, +pneumonie, +febrilní infekce, +herpes zoster, +infekce dechových cest, plísňové infekce, infekce neznámého původu +akutní bronchitida, +sinusitida, hepatitida B1 |
závažné virové infekce2 Pneumocystis jirovecii |
PML | ||
|
Poruchy krve a lymfatického systému |
neutropenie, leukopenie +febrilní neutropenie +trombocytopenie |
+ pancytopenie +granulocytopenie |
poruchy srážlivosti, aplastická anémie, hemolytická anémie, lymfadenopatie |
přechodný vzestup hladin sérových IgM3 |
pozdní neutropenie3 | |
|
Poruchy imunitního systému |
angioedém |
hypersensitivita |
anafylaxe |
syndrom rozpadu nádoru, syndrom z uvolnění cytokinů4, sérová nemoc |
akutní reverzibilní trombocyto- penie související s podáním infuze4 | |
|
Poruchy metabolismu a výživy |
hyperglykémie, pokles hmotnosti, periferní otoky, otok obličeje, vzestup LDH, hypokalcémie | |||||
|
Psychiatrické poruchy | ||||||
|
Poruchy nervového systému |
parestézie, hypestézie, agitovanost, vasodilatace, závratě, úzkost |
porucha vnímání chuti |
periferní neuropatie, paresa lícního nervu5 |
kraniální neuropatie, jiné smyslové poruchy5 | ||
|
Poruchy oka |
poruchy slzení, konjunktivitida |
závažná porucha zraku5 | ||||
|
Poruchy ucha a labyrintu |
tinnitus, bolest uší |
porucha sluchu5 | ||||
|
Srdeční poruchy |
+infarkt myokardu4 a 6, arytmie, +fibrilace síní, tachykardie, +srdeční porucha |
+levostranné srdeční selhání, +supraventrikulární +komorová +angina pectoris, +ischemie myokardu, bradykardie |
závažné kardiální poruchy4 a 6 |
srdeční selhání4 a 6 | ||
|
Cévní poruchy |
hypertenze, ortostatická |
vaskulitida (zejména kožní), leuko-cytoklastická vaskulitida |
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Respirační, hrudní a mediastinální poruchy |
Bronchospasmus4, dechové choroby, bolest na hrudi, dušnost, zhoršení kašle, rýma |
astma, obliterující bronchiolitida, plicní poruchy, hypoxie |
intersticiální plicní 7 onemocněni |
respirační selhání4 |
plicní infiltrace | |
|
Gastrointesti-nální poruchy |
zvracení, průjem, bolesti břicha, dysfagie, stomatitida, zácpa, dyspepsie, nechutenství, podráždění hltanu |
zduření břicha |
gastrointesti- nální perforace7 | |||
|
Poruchy kůže a podkožní tkáně |
kopřivka, pocení, noční poty, +kožní onemocnění |
závažné bulózní kožní reakce, Stevens- Johnsonův syndrom, toxická epidermální nekrolýza (Lyellův syndrom)7 | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
hypertonie, myalgie, bolesti kloubů, bolesti zad, bolesti krku, bolest | |||||
|
Poruchy ledvin a močových cest |
renální selhání4 | |||||
|
Celkové poruchy a reakce v místě aplikace |
bolest nádoru, zrudnutí, únava, příznaky nachlazení, +multiorgánové selhání4 |
bolest v místě infuze | ||||
|
Vyšetření |
pokles hladin IgG | |||||
|
Pro každý příznak byla četnost stanovena na základě výskytu reakcí všech stupňů (lehké až závažné) s výjimkou příznaků označených "+", u kterých byla četnost stanovena na základě závažných reakcí (stupeň > 3 dle obecných kritérií toxicity NCI). Jsou uvedeny pouze nejvyšší četnosti ve studiích. 1 zahrnuje reaktivaci a primární infekce; frekvence je založena na R-FC režimu u relabující/refrakterní CLL 2 viz též níže uvedený bod infekce 3 viz též níže uvedený bod hematologické nežádoucí reakce 4 viz též níže uvedený bod účinky spojené s podáním infuze. Vzácně byly hlášeny fetální případy 5 příznaky kraniální neuropatie. Objevily se v různou dobu nejvýše za několik měsíců po ukončení léčby přípravkem MabThera 6 pozorováno zejména u pacientů s předchozím kardiálním onemocněním a/nebo kardiotoxickou chemoterapií a byly většinou spojeny s účinky spojenými s podáním infuze 7 včetně fatálních případů | ||||||
Následující pojmy byly uváděny jako nežádoucí příhody, jejich četnost však byla ve skupinách pacientů s přípravkem MabThera podobná nebo nižší než v kontrolních skupinách: hematotoxicita, neutropenické infekce, infekce močových cest, poruchy čití, horečka.
U více než 50 % pacientů v klinických studiích byly hlášeny příznaky, které byly suspektní jako účinky spojené s podáním infuze a byly zejména pozorovány v průběhu první infuze, většinou v první nebo v prvých dvou hodinách. Tyto příznaky byly většinou horečka, zimnice a ztuhlost. Mezi další příznaky patří zrudnutí, angioedém, bronchospasmus, zvracení, nevolnost, kopřivka/vyrážka, únava, bolest hlavy, podráždění hltanu, rýma, svědění, bolest, tachykardie, hypertenze, hypotenze, dušnost, dyspepsie, slabost a známky syndrome rozpadu nádoru. Závažné účinky spojené s podáním infuze (například bronchospasmus, hypotense) se vyskytly až u 12 % případů. Další reakce, které byly v několika případech hlášeny, byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie. S nižší nebo neznámou četností byly hlášeny exacerbace již existujících kardiálních
onemocnění, jako jsou angina pectoris nebo městnavé srdeční selhání nebo závažné kardiální poruchy (srdeční selhání, infarkt myokardu, fibrilace síní), edém plic, multiorgánové selhání, příznak rozpadu tumoru, příznak uvolnění cytokinů, renální selhání a respirační selhání. Incidence účinků spojených s podáním infuze se významně snížila u následujících infuzí a je <1 % pacientů při osmém cyklu léčby obsahující přípravek MabThera.
Popis vybraných nežádoucích účinků
Infekce
I když přípravek MabThera způsobuje depleci B-lymfocytů u 70 % až 80 % pacientů, snížení sérových koncentrací imunoglobulinů se vyskytuje jen u malého počtu pacientů.
V randomizovaných studiích byly v ramenech obsahujících přípravek MabThera s vyšší četností hlášeny lokalizované infekce kandidou a herpes zoster. Závažné infekce byly hlášeny u asi 4 % pacientů léčených přípravkem MabThera v monoterapii. V průběhu udržovací léčby přípravkem MabThera až po dobu dvou let byly pozorovány vyšší četnosti infekcí celkové, včetně infekcí stupně 3 a 4 ve srovnání s obdobím observace. Po dobu dvouletého léčebného období nebyla hlášena žádná kumulativní toxicita z hlediska infekce. Dále byly hlášeny při léčbě přípravkem MabThera jiné závažné virové infekce buď nové, reaktivované nebo exacerbované, z nichž některé byly fatální. Většina pacientů dostávala přípravek MabThera v kombinaci s chemoterapií nebo jako součást transplantace hematopoetických kmenových buněk. Příklady těchto závažných virových infekcí jsou infekce způsobené herpetickými viry (cytomegalovirem, virem varicella zoster a herpes simplex virem), JC virem (progresivní multifokální leukoencefalopatie (PML)) a virem hepatitidy C.
V klinických studiích byly rovněž zaznamenány případy fatální PML, které se objevily po progresi onemocnění a jeho opakované léčbě. Byly hlášeny případy reaktivace hepatitidy B, z nichž většina byla u pacientů, kteří dostávali přípravek MabThera v kombinaci s cytotoxickou chemoterapií.
U pacientů s relabující/refrakterní CLL byla incidence infekce 3/4. stupně hepatitidy B (reaktivace a primární infekce) 2 % u R-FC oproti 0 % u FC. Byla pozorována progrese Kaposiho sarkomu u pacientů vystavených přípravku MabThera, kteří již dříve trpěli Kaposiho sarkomem. Tyto případy se vyskytly u neschválených indikací a většina pacientů byla HIV pozitivní.
Hematologické nežádoucí účinky
V klinických studiích s monoterapií přípravkem MabThera podávaným po dobu 4 týdnů se u malého počtu pacientů vyskytly hematologické abnormality a byly většinou mírné a reverzibilní. Závažné (stupně 3/4) neutropenie byly hlášeny u 4,2 %, anémie u 1,1 % a trombocytopenie u 1,7 % pacientů.
V průběhu udržovací léčby přípravkem MabThera po dobu až dvou let byly hlášeny leukopenie (5 % oproti 2 %, stupně 3/4) a neutropenie (10 % oproti.4 %, stupně 3/4) s vyšší incidencí oproti pouhému sledování. Incidence trombocytopenie byla nízká (<1 %, stupně 3/4) a nelišila se mezi jednotlivými léčebnými rameny. V průběhu léčebného cyklu ve studiích s přípravkem MabThera v kombinaci s chemoterapií byly hlášeny leukopenie stupně 3/4 (R-CHOP 88 % oproti CHOP 79 %, R-FC 23 % oproti FC 12 %), neutropenie (R-CVP 24 % oproti CVP 14 %; R-CHOP 97 % oproti CHOP 88 %, R-FC 30 % oproti FC 19 % u doposud neléčené CLL), pancytopenie (R-FC 3 % oproti FC 1 % u doposud neléčené CLL) s obvykle vyšší četností v porovnání se samotnou chemoterapií. Vyšší incidence neutropenie u pacientů léčených přípravkem MabThera a chemoterapií však nebyla spojena s vyšší incidencí infekcí a infestací v porovnání s pacienty léčenými samotnou chemoterapií. Studie u dosud neléčené a relabující/refrakterní CLL ukázaly, že až u 25 % pacientů léčených s R-FC byla neutropenie po léčbě přípravkem MabThera plus FC prolongovaná (definováno jako počet neutrofilů zůstávajících pod hodnotou 1x109/l mezi dnem 24 a 42 po poslední dávce) nebo se projevila opožděně (definováno jako počet neutrofilů pod hodnotou 1x109/l později než 42 dnů po poslední dávce u pacientů, u kterých se dříve prolongovaná neutropenie neprojevila nebo u těch, u kterých došlo ke znovuobjevení před dnem 42). Nebyly hlášeny žádné rozdíly v incidenci anémie. Některé případy pozdní neutropenie se objevily více než 4 týdny po poslední infuzi přípravku MabThera Ve studii u pacientů s CLL ve stádiu C podle Bineta, kterým byl přípravek podáván jako lék první linie léčby, bylo zaznamenáno více nežádoucích účinků ve skupině R-FC v porovnání se skupinou FC (R-FC
83 % vs. FC 71 %). Ve studii s relabující/refrakterní CLL byla trombocytopenie stupně 3/4 zaznamenána u 11 % pacientů v R-FC skupině v porovnání s 9 % pacientů v FC skupině.
Ve studiích s přípravkem MabThera u pacientů s Waldenstromovou makroglobulinemií byly pozorovány přechodné vzestupy hladin sérových IgM po zahájení léčby, které mohou být spojeny s hyperviskozitou a souvisejícími příznaky. Přechodný vzestup IgM se většinou vrátil minimálně k hladině při zahájení v rozmezí 4 měsíců.
Kardiovaskulární nežádoucí účinky
V průběhu klinických studií s monoterapií přípravkem MabThera byly hlášeny kardiovaskulární příhody u 18,8 % pacientů, přičemž nejčastěji hlášenými událostmi byly hypotenze a hypertenze.
V průběhu infuze byly hlášeny případy arytmie stupně 3 nebo 4 (včetně ventrikulární a supraventrikulární tachykardie). V průběhu udržovací léčby byla incidence kardiálních onemocnění stupně 3/4 srovnatelná u pacientů léčených přípravkem MabThera a u pacientů pouze sledovaných. Jako závažné nežádoucí události (včetně fibrilace síní, infarktu myokardu, levostranného komorového selhání a myokardiální ischémie) byly hlášeny kardiální události u 3 % pacientů léčených přípravkem MabThera ve srovnání s <1 % u sledování. Ve studiích hodnotících přípravek MabThera v kombinaci
s chemoterapií byla incidence kardiálních arytmií stupně 3 a 4, především supraventrikulárních arytmií jako je tachykardie a síňový flutter/fibrilace vyšší ve skupině R-CHOP (14 pacientů, 6,9 %) ve srovnání se skupinou CHOP (3 pacienti, 1,5 %). Všechny tyto arytmie se buď vyskytly v souvislosti s infuzí přípravku MabThera nebo souvisely s predisponujícími podmínkami, jako byly horečka, infekce, akutní infarkt myokardu nebo již existujících respiračních a kardiovaskulárních onemocnění. Nebyly pozorovány žádné rozdíly mezi skupinami R-CHOP a CHOP v incidenci jiných kardiálních událostí stupně 3 a 4 včetně srdečního selhání, infarktu myokardu a manifestace onemocnění koronárních tepen. U CLL byl celkový výskyt srdečních chorob stupně 3 nebo 4 nízký jak ve studii s první linií léčby (4 % R-FC, 3 % FC), tak ve studii s relabující/refrakterní CLL (R-FC 4 %, FC 4 %).
Respirační systém:
Byly hlášeny případy intersticiálního plicního onemocnění, některé s fatálním zakončením.
Neurologické poruchy
V průběhu léčebného období (indukční fáze léčby zahrnující R-CHOP pro maximálně 8 cyklů), čtyři pacienti (2 %) léčení ve skupině R-CHOP všichni s kardiovaskulárními rizikovými faktory, prodělali během prvního léčebného cyklu tromboembolickou cerebrovaskulární příhodu v průběhu prvního léčebného cyklu. Ve výskytu dalších tromboembolických příhod nebyl mezi skupinami žádný rozdíl. Naopak, tři pacienti (1,5 %) v rameni CHOP měli cerebrovaskulární příhodu, u všech se objevila v období následného pozorování. U CLL byl celkový výskyt poruch nervového systému stupně 3 nebo 4 nízký jak ve studii s první linií léčby (4 % R-FC, 4 % FC), tak ve studii s relabující/refrakterní CLL (R-FC 3 %, FC 3 %).
Byly hlášeny případy syndromu posteriorní reverzibilní encefalopatie (PRES)/syndromu reverzibilní posteriorní leukoencefalopatie (RPLS). Známky a příznaky zahrnovaly zrakové poruchy, bolest hlavy, křeče a psychické poruchy, s nebo bez průvodní hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovacím vyšetřením mozku. U hlášených případů byly zaznamenány rizikové faktory PRES/RPLS, které zahrnují průvodní onemocnění pacienta, hypertenzi, imunosupresivní léčbu a/nebo chemoterapii.
Gastrointestinální onemocnění
Gastrointestinální perforace v některých případech vedoucí k úmrtí byly pozorovány u pacientů, kteří dostávali přípravek MabThera v léčbě nehodgkinského lymfomu. Ve většině těchto případů byla MabThera podávána s chemoterapií.
Hladiny IgG
V klinických studiích hodnotících udržovací léčbu přípravkem MabThera u relabujícího/refrakterního folikulárního lymfomu byly po indukční léčbě střední hladiny IgG pod dolní hranicí normy (LLN)
(< 7 g/l) v rameni s pouhým sledováním i v rameni s přípravkem MabThera. V rameni se sledováním došlo následně k vzestupu střední hladiny IgG nad LLN, ale v rameni s přípravkem MabThera zůstaly nezměněny. Podíl pacientů se střední hladinou IgG pod LNN byl v rameni s přípravkem MabThera přibližně 60 % po celou dobu 2letého léčebného období, zatímco v rameni se sledováním tento podíl poklesl (36 % po 2 letech).
Nízký počet spontánních a v literatuře popsaných případů hypogamaglobulinemie byl pozorován u pediatrických pacientů léčených přípravkem MabThera, v některých případech závažných a vyžadujících dlouhodobou substituční terapii imunoglobuliny. Následky dlouhodobé deplece B buněk u pediatrických pacientů nejsou známy.
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Vybrané skupiny pacientů - Monoterapie přípravkem MabThera Starší pacienti (> 65 let)
Incidence nežádoucích reakcí na lék všech stupňů a stupně 3/4 byla obdobná ve skupině starších v porovnání s mladšími pacienty (<65 let).
Pacienti s objemným (bulky) onemocněním
U pacientů s objemným onemocněním byla zjištěna vyšší incidence nežádoucích reakcí na lék stupně 3/4 ve srovnání s pacienty bez rozsáhlého nádorového postižení (25,6 % versus 15,4 %). Incidence jakéhokoli stupně nežádoucích reakcí na lék byla mezi oběma skupinami obdobná.
Opakovaná léčba
Procento pacientů hlásících nežádoucí reakci na lék po opětovném zahájení léčby dalšími cykly přípravku MabThera bylo podobné jako procento pacientů uvádějící nežádoucí reakci na lék po prvním podání přípravku (jakýkoliv stupeň a stupeň 3/4 nežádoucích reakcí na lék).
Vybrané skupiny pacientů - kombinovaná terapie přípravkem MabThera Starší pacienti (> 65 let)
Incidence 3/4. stupně nežádoucích účinků týkajících se krve a lymfatického systému byla u starších pacientů vyšší v porovnání s mladšími pacienty (<65 let) s dříve neléčenou nebo relabující/refrakterní CLL.
Zkušenosti u revmatoidní artritidy
Shrnutí bezpečnostního profilu
Celkový bezpečnostní profil přípravku MabThera u revmatoidní artritidy je založen na údajích od pacientů zařazených do klinických studií a na údajích ze sledování přípravku po uvedení na trh.
Bezpečnostní profil přípravku MabThera u pacientů s těžkou revmatoidní artritidou (RA) je shrnutý v bodech níže. V klinických studiích podstoupilo více než 3100 pacientů nejméně jeden léčebný cyklus a bylo sledováno po dobu v rozsahu 6 měsíců až více než 5 let; přibližně 2400 pacientů podstoupilo dva nebo více cyklů léčby, z nichž přes 1000 pacientů podstoupilo více než 5 cyklů léčby. Informace o bezpečnosti shromážděné z údajů po uvedení přípravku na trh odrážejí očekávaný profil nežádoucích účinků, jak byl pozorován v klinických studiích s přípravkem MabThera (viz bod 4.4).
Pacientům bylo podáno 2 x 1000 mg přípravku MabThera v odstupu dvou týdnů a dále metotrexát (10-25 mg/týden). Infuze přípravku MabThera byly podávány po nitrožilní infuzi 100 mg metylprednizolonu; pacientům byl prednizon podáván také perorálně po dobu 15 dní.
Shrnutí nežádoucích účinků do tabulky
Nežádoucí účinky jsou shrnuty v Tabulce 2. Četnost je uvedena jako velmi častá (>1/10), častá (>1/100 až <1/10), méně častá (>1/1000 až <1/100) a velmi vzácná (<1/10000). V každé skupině četností jsou nežádoucí účinky řazeny podle klesající závažnosti.
Nejčastějším nežádoucím účinkem, který byl považován za účinek související s podáním přípravku MabThera, byly reakce související s infuzí. Celková incidence IRR v klinických studiích byla 23 % po
první infuzi a klesala s dalšími infuzemi. Závažné IRR byly méně časté (0,5 % pacientů) a byly pozorovány převážně v průběhu úvodního cyklu léčby. Kromě nežádoucích reakcí zaznamenaných v klinických studiích s přípravkem MabThera při RA, byly v průběhu postmarketingového sledování hlášeny případy progresivní multifokální leukoencefalopatie (PML) (viz bod 4.4) a reakce podobné sérové nemoci.
Tabulka 2 Souhrn NÚ, které se byly hlášeny u pacientů s revmatoidní artritidou léčených _přípravkem MabThera v klinických ^ studií a po uvedení přípravku ^ na trh
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
|
Infekce a infestace |
infekce horních cest dýchacích, močové infekce |
bronchitida, sinusitida, gastroenteritida, tinea pedis |
PML, reaktivace viru hepatitidy B | ||
|
Poruchy krve a lymfatického systému |
neutropenie1 |
pozdní neutropenie2 |
Reakce podobná sérové nemoci | ||
|
Srdeční poruchy |
Angina pectoris, fibrilace síní, srdeční selhání, infarkt myokardu |
Flutter síní | |||
|
Poruchy imunitního systému |
3reakce související s podáním infuze (hypertenze, nauzea, vyrážka, pyrexie, pruritus, kopřivka, podráždění hrdla, návaly horka, hypotenze, rýma, ztuhlost, tachykardie, únava, orofaryngeální bolest, periferní otok, erytém) |
*3reakce související s podáním infuze (generalizovaný otok, bronchospazmus, dušnost, otok laryngu, angioneurotický edém, generalizovaný pruritus, anafylaxe, anafylaktoidní reakce) | |||
|
Celkové poruchy a reakce v místě aplikace | |||||
|
Poruchy metabolismu a výživy |
hypercholesterolémie | ||||
|
Poruchy nervového systému |
parestézie migréna, závrať, ischias | ||||
|
Poruchy kůže a podkožní tkáně |
alopecie |
toxická epidermální nekrolýza (Lyellův syndrom), Stevens-Johnsonův syndrom5 | |||
|
Psychiatrické poruchy | |||||
|
Gastrointestinální poruchy |
dyspepsie, průjem, gastroezofageální reflux, ulcerace v ústech, bolest v horní části břicha | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
bolesti kloubů / muskuloskeletální bolest, artróza, bursitida | ||||
|
Vyšetření |
snížení IgM hladin4 |
snížení IgG hladin4 | |||
|
1 Kategorie četnosti odvozeny z laboratorních hodnot shromážděných z běžných laboratorních měření v klinických studiích. 2 Kategorie četnosti odvozeny z údajů po uvedení přípravku na trh. 3 Reakce, které se objeví do 24 hodin po infuzi. Viz též reakce související s infuzí uvedené níže. Reakce související s infuzí mohou být následkem hypersenzitivity a/nebo mechanismu účinku. 4 Včetně pozorování shromážděných z běžných laboratorních měření. 5 Včetně případů končících úmrtím | |||||
Opakované léčebné cykly
Aplikace opakovaných léčebných cyklů je spojena s podobným profilem NÚ, jaké byly pozorovány po první expozici. Četnost všech NÚ, které následovaly po první expozici přípravku MabThera, byla vyšší v průběhu prvních 6 měsíců a poté klesala. Toto je z větší části přičítáno reakcím souvisejícím s infuzí (které jsou nejčastější v průběhu prvního cyklu léčby), zhoršení RA a infekcím. Všechny tyto reakce byly nej častější právě v průběhu prvních 6 měsíců léčby.
Reakce související s infuzí
Nej častějšími NÚ, které následovaly po podání přípravku MabThera v klinických studiích, byly reakce související s infuzí (IRR) (viz Tabulka 2). Mezi 3189 pacienty léčenými přípravkem MabThera prodělalo 1135 (36 %) pacientů nejméně jednu IRR, přičemž 733/3189 (23 %) pacientů prodělalo IRR po první infuzi při první expozici přípravku MabThera. Incidence IRR klesala u všech následujících infuzí. V klinických studiích prodělalo těžkou IRR méně než 1 % pacientů (174/3189). V souvislosti s IRR nebyly v klinických studiích zaznamenány žádné CTC (obecná kritéria toxicity, common toxicity criteria) stupně 4 ani úmrtí. Procento příhod CTC stupně 3 a procento IRR, které vedlo k ukončení léčby, klesalo v průběhu následujících cyklů a od 3. cyklu byly tyto příhody vzácné. Premedikace intravenózními glukokortikoidy významně snížila incidenci a závažnost IRR (viz body
4.2 a 4.4). Po uvedení přípravku na trh byly hlášeny závažné reakce související s infuzí, které končily úmrtím.
Ve studii zaměřené na vyhodnocení bezpečnosti zrychlené infuze přípravku MabThera u pacientů s revmatoidní artritidou bylo pacientům se středně těžkou až závažnou aktivní RA, u kterých se nevyskytly závažné reakce související s infuzí v průběhu nebo do 24 h od jejich první infuze, umožněno přijímat 2hodinovou infuzi přípravku MabThera intravenózně. Pacienti s anamnézou závažné reakce na infuzi biologickou léčbou RA nesměli být zařazeni. Počet případů, typy a závažnost reakcí souvisejících s infuzí jsou v souladu s dříve pozorovanými údaji. Nebyly pozorovány žádné závažné reakce související s infuzí.
Popis vybraných nežádoucích účinků
Infekce
U pacientů léčených přípravkem MabThera byla celková četnost výskytu infekcí přibližně 94 na 100 paciento-roků. Většinou se jednalo o mírné a středně těžké infekce horních dýchacích cest a infekce močových cest. Incidence těžkých infekcí, nebo infekcí, které vyžadovaly i.v. podání antibiotik, byla přibližně 4 na 100 paciento-roků. Během opakovaných cyklů léčby přípravkem MabThera nedocházelo k žádnému významnému zvýšení četností těžkých infekcí. V průběhu klinických studií byly zaznamenány infekce dolních cest dýchacích (včetně pneumonie), které měly podobnou incidenci v rameni s léčbou přípravkem MabThera ve srovnání s ramenem kontrolním.
Po podávání přípravku MabThera k léčbě autoimunitních onemocnění byly zaznamenány případy progresivní multifokální leukoencefalopatie s fatálním zakončením. Autoimunitní onemocnění zahrnovala revmatoidní artritidu a další nespecifikovaná autoimunitní onemocnění, včetně systémového lupus erytematodes (SLE) a vaskulitidy.
U pacientů s nehodgkinskými lymfomy, kteří jsou léčeni přípravkem MabThera v kombinaci s cytotoxickou chemoterapií, byly hlášeny případy reaktivace viru hepatitidy B (viz Nehodgkinské lymfomy).
Případ reaktivace infekce virem hepatitidy B byl také velmi vzácně hlášen u pacientů s RA léčených přípravkem MabThera (viz bod 4.4).
Kardiovaskulární nežádoucí účinky
U pacientů léčených přípravkem MabThera byly těžké kardiální účinky zaznamenány s četností 1,3 na 100 paciento-roků ve srovnání s 1,3 na 100 paciento-roků ve skupině pacientů dostávajících placebo. Procento pacientů, kteří prodělali srdeční nežádoucí účinky (všechny nebo těžké) se v průběhu opakovaných cyklů léčby nezvyšovalo.
Neurologické příhody
Byly hlášeny případy syndromu posteriomí reverzibilní encefalopatie (PRES - posterior reversible encephalopathy syndrome) / syndromu reverzibilní posteriomí leukoencefalopatie (RPLS - reversible posterior leukoencephalopathy). Známky a příznaky zahrnovaly zrakové poruchy, bolesti hlavy, záchvaty a poruchy vědomí, s přítomností nebo bez přítomnosti hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovací vyšetřovací metodou mozku. U nahlášených případů byly zjištěny rizikové faktory PRES/RPLS, mezi které patří základní onemocnění pacienta, hypertenze, imunosupresivní léčba a/nebo chemoterapie.
Neutropenie
Výskyt příhod neutropenie byl pozorován při léčbě přípravkem MabThera, z nichž většina byla přechodná a mírné nebo střední závažnosti. Neutropenie se může objevit několik měsíců po podání přípravku MabThera (viz bod 4.4).
V placebem kontrolovaných obdobích klinických studií se u 0,94 % (13/1382) pacientů léčených přípravkem MabThera a u 0,27 % (2/731) pacientů s placebem rozvinula závažná neutropenie.
Neutropenické příhody, včetně závažného pozdějšího nástupu a přetrvávající neutropenie, byly vzácně hlášeny po uvedení přípravku na trh, některé z nich byly spojeny s infekcemi končícími úmrtím.
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Laboratorní odchylky
Hypogamaglobulinemie (IgG nebo IgM pod dolní hranicí normy) byla pozorována u pacientů s RA léčených přípravkem MabThera. Po rozvoji nízkých IgG nebo IgM nebyla míra celkových infekcí nebo závažných infekcí zvýšena (viz bod 4.4).
Nízký počet spontánních a v literatuře popsaných případů hypogamaglobulinemie byl pozorován u pediatrických pacientů léčených přípravkem MabThera, v některých případech závažných a vyžadujících dlouhodobou substituční terapii imunoglobuliny. Následky dlouhodobé deplece B buněk u pediatrických pacientů nejsou známy.
Zkušenosti s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou
V klinické studii u granulomatózy s polyangiitidou a mikroskopické polyangiitidy bylo 99 pacientů léčeno přípravkem MabThera (375 mg/m2, jednou týdně po dobu 4 týdnů) a glukokortikoidy (viz bod 5.1).
Shrnutí nežádoucích účinků do tabulky
Nežádoucí účinky uvedené v Tabulce 3 byly všechny nežádoucí účinky, které se objevily s incidencí > 5 % ve skupině léčené přípravkem MabThera.
Tabulka 3 Nežádoucí účinky, které se v klíčové klinické studii v 6 měsících vyskytly u > 5 %
pacientů léčených přípravkem MabThera a s vyšší četností než u druhé srovnávací skupiny
|
Tělesný systém |
Rituximab |
|
Nežádoucí účinek |
(n=99) |
|
Poruchy krve | |
|
a lymfatického systému | |
|
T rombocytopenie |
7 % |
|
Gastrointestinální | |
|
poruchy | |
|
18 % | |
|
6 % | |
|
Zácpa |
5 % |
|
Celkové poruchy | |
|
a reakce v místě aplikace | |
|
Periferní edém |
16 % |
|
Poruchy imunitního systému | |
|
Syndrom uvolňování |
5 % |
|
cytokinů | |
|
Infekce a infestace | |
|
Infekce močových cest |
7 % |
|
Bronchitida |
5 % |
|
5 % | |
|
Nazofaryngitida |
5 % |
|
Vyšetření | |
|
Pokles hemoglobinu |
6 % |
|
Poruchy metabolismu a výživy | |
|
Hyperkalemie |
5 % |
|
Poruchy svalové a kosterní | |
|
soustavy a pojivové tkáně | |
|
Svalové spasmy |
18 % |
|
Artralgie |
15 % |
|
Tělesný systém |
Rituximab |
|
Nežádoucí účinek |
(n=99) |
|
10 % | |
|
Svalová slabost |
5 % |
|
Muskuloskeletální bolest |
5 % |
|
Bolest končetin |
5 % |
|
Poruchy nervového systému | |
|
Závratě |
10 % |
|
Tremor |
10 % |
|
Psychiatrické poruchy | |
|
Insomnie |
14 % |
|
Respirační, hrudní a mediastinální poruchy | |
|
12 % | |
|
11 % | |
|
Epistaxe |
11 % |
|
Nazální překrvení |
6 % |
|
Poruchy kůže a podkožní tkáně | |
|
Akné |
7 % |
|
Cévní poruchy | |
|
Hypertenze |
12 % |
|
5 % | |
Vybrané nežádoucí účinky Reakce související s infuzí
Reakce související s infuzí byly v klinické studii s GPA a MPA definovány jako jakýkoli nežádoucí účinek, který se objevil v průběhu 24 hodin po podání infuze a který byl zkoušejícím považován za nežádoucí účinek související s infuzí u populace hodnocené z důvodu bezpečnosti. Přípravkem MabThera bylo léčeno 99 pacientů a 12 % z nich zaznamenalo alespoň jeden nežádoucí účinek související s infuzí. Všechny nežádoucí účinky související s infuzí byly stupně 1 nebo 2 podle CTC. Nejčastější nežádoucí účinky související s infuzí zahrnovaly syndrom uvolňování cytokinů, návaly horka, podráždění v krku a tremor. Přípravek MabThera byl podáván v kombinaci s intravenózními glukokortikoidy, které mohou incidenci a závažnost těchto nežádoucích účinků snižovat.
Infekce
U 99 pacientů léčených přípravkem MabThera byl celkový výskyt infekce přibližně 237 na 100 pacientoroků (95% interval spolehlivosti 197 - 285) u šestiměsíčního primárního cílového parametru. Infekce byly převážně mírné až středně závažné a byly zastoupeny většinou infekcemi horních cest dýchacích, herpes zoster a infekcemi močových cest. Výskyt závažných infekcí byl přibližně 25 na 100 pacientoroků. Nejčastěji hlášenou závažnou infekcí ve skupině léčené přípravkem MabThera byla pneumonie s četností 4 %.
Malignity
Incidence malignit u pacientů léčených přípravkem MabThera v klinické studii s GPA a MPA byla 2,00 na 100 pacientoroků při běžném uzavření dat ze studie (kdy poslední pacient dokončil období následného sledování). Na základě poměrů standardizované incidence se zdá incidence maligních onemocnění podobná incidenci, která byla dříve zaznamenaná u pacientů s ANCA-asociovanou vaskulitidou.
Kardiovaskulární nežádoucí účinky
Kardiální příhody se vyskytovaly s četností přibližně 273 na 100 pacientoroků (95% interval spolehlivosti 149 - 470) u šestiměsíčního primárního cílového parametru. Výskyt závažných kardiálních příhod byl 2,1 na 100 pacientoroků (95% interval spolehlivosti 3 - 15). Nejčastěji hlášenými příhodami byly tachykardie (4 %) a fibrilace síní (3 %) (viz bod 4.4).
Neurologické příhody
Byly hlášeny případy syndromu posteriorní reverzibilní encefalopatie (PRES - posterior reversible encephalopathy syndrome) / syndromu reverzibilní posteriorní leukoencefalopatie (RPLS - reversible posterior leukoencephalopathy). Známky a příznaky zahrnovaly zrakové poruchy, bolesti hlavy, záchvaty a poruchy vědomí, s přítomností nebo bez přítomnosti hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovací vyšetřovací metodou mozku. U nahlášených případů byly zjištěny rizikové faktory PRES/RPLS, mezi které patří základní onemocnění pacienta, hypertenze, imunosupresivní léčba a/nebo chemoterapie.
Reaktivace hepatitidy B
Po uvedení přípravku na trh byl u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou léčených přípravkem MabThera hlášen malý počet případů reaktivace hepatitidy B, z nichž některé končily úmrtím.
Hypogamaglobulinemie
U pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou, kteří byli léčeni přípravkem MabThera, byla pozorována hypogamaglobulinemie (IgA, IgG nebo IgM pod dolní hranicí normálních hodnot). V randomizované, dvojitě zaslepené, multicentrické studii s aktivním komparátorem hodnotící non-inferioritu přípravku mělo ve skupině léčené přípravkem MabThera v 6. měsíci 27 %, 58 % resp. 51 % pacientů s původně normálními hladinami imunoglobulinů nízké hladiny IgA, IgG resp. IgM ve srovnání s 25 %, 50 % resp. 46 % pacientů ve skupině s cyklofosfamidem. Celkový výskyt infekcí nebo závažných infekcí u pacientů s nízkou hladinou IgA, IgG nebo IgM nebyl zvýšen.
Neutropenie
V randomizované, dvojitě zaslepené, multicentrické studii s aktivním komparátorem hodnotící non-inferioritu přípravku MabThera u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou se u 24 % pacientů ve skupině léčené přípravkem MabThera (jeden cyklus) a 23 % pacientů ve skupině s cyklofosfamidem objevila neutropenie stupně 3 nebo vyšší dle CTC. Neutropenie nebyla spojena s pozorovaným zvýšením závažných infekcí u pacientů léčených přípravkem MabThera. Vliv opakovaných cyklů přípravku MabThera na rozvoj neutropenie u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou nebyl v klinických studiích hodnocen.
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Z klinických studií u lidí jsou dostupné omezené zkušenosti s podáním dávek vyšších než je schválená dávka intravenózního přípravku MabThera. Dosud nejvyšší intravenózní dávka přípravku MabThera testovaná u lidí je 5000 mg (2250 mg/m2), testovaná ve studii se zvyšováním dávek u pacientů s chronickou lymfocytární leukemií. Nebyly zjištěny žádné další bezpečnostní signály.
U pacientů, u kterých se vyskytne předávkování, má být okamžitě přerušena infuze a mají být pečlivě sledováni.
Po uvedení přípravku na trh bylo hlášeno pět případů předávkování přípravkem MabThera. Ve třech případech nebyly hlášeny žádné nežádoucí účinky. Dva nežádoucí účinky, které byly hlášeny, byly chřipkovité (flu-like) příznaky při dávce 1,8 g rituximabu a fatální respirační selhání při dávce 2 g rituximabu.
5. FARMAKOLOGICKÉ VLASTNOSTI 5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: protinádorové látky, monoklonální protilátky, ATC kód: L01XC02
Rituximab se specificky váže na transmembránový antigen CD20, což je neglykosylovaný fosfoprotein vyskytující se na pre-B a zralých B-lymfocytech. Tento antigen je exprimován > 95 % všech nehodgkinských lymfomů původem z B buněk.
CD20 se nachází na normálních i maligních B-lymfocytech, není přítomen na hematopoetických kmenových buňkách, pro-B-buňkách, normálních plazmatických buňkách ani na jiných normálních tkáních. Antigen se po navázání protilátky neinternalizuje a není také uvolňován z povrchu buňky. CD20 necirkuluje v plazmě jako volný antigen a tedy nevzniká kompetice o navázání protilátek.
Rituximab se svým Fab fragmentem naváže na CD20 antigen na povrchu B-lymfocytů a prostřednictvím Fc domény může být zahájena efektorová imunitní reakce, která vede k lýze B-lymfocytů. Možné mechanizmy, kterými je lýza B-lymfocytů zprostředkována, zahrnují jednak cytotoxickou reakci vyvolanou účinkem komplementu (CDC), jejímž prvním krokem je vazba C1q a jednak protilátkami zprostředkovanou buněčnou cytotoxicitu (ADCC), která závisí na aktivaci jednoho či více Fcy receptorů na povrchu granulocytů, makrofágů a NK buněk. Rovněž bylo prokázáno, že vazba rituximabu na antigen CD 20 přítomný na B lymfocytech vyvolává buněčnou smrt navozením apoptózy.
Počet B-lymfocytů v periferní krvi se snižuje pod normu po podání první dávky přípravku MabThera. U pacientů léčených z důvodu hematologických malignit se objevila nová populace B buněk během 6 měsíců po léčbě a obvykle byl jejich normální počet obnoven během 12 měsíců po ukončení terapie, ačkoli u některých pacientů to může trvat déle (se střední dobou do znovuobjevení lymfocytů až 23 měsíců po indukční léčbě). U pacientů s revmatoidní artritidou byla po podání dvou infuzí 1000 mg přípravku MabThera v odstupu 14 dní pozorována bezprostřední deplece B lymfocytů v periferní krvi. Počet B lymfocytů v periferní krvi začal stoupat od 24. týdne a u většiny pacientů bylo pozorováno obnovení populace do 40. týdne, ať byl přípravek MabThera podáván jako monoterapie nebo v kombinaci s metotrexátem. U malého procenta pacientů došlo po poslední dávce přípravku MabThera k prolongované depleci periferních B-buněk trvající 2 roky nebo déle. U pacientů s granulomatózou s polyangiitidou nebo mikroskopickou polyangiitidou se počet periferních B-buněk snížil na <10 buněk/pl po dvoutýdenním podávání infuzí rituximabu 375 mg/m2 a na této úrovni zůstal u většiny pacientů po dobu dalších 6 měsíců. U většiny pacientů (81 %) se po 12 měsících prokázaly známky návratu B-buněk s počtem >10 buněk/pl, po 18 měsících se počet zvýšil u 87 % pacientů.
Klinické zkušenosti v léčbě nehodgkinských lymfomů a chronické lymfocytární leukemie
Folikulární lymfomy
Monoterapie
Úvodní terapie 4 dávky jednou týdně
V klíčové studii bylo léčeno 166 pacientů s relabujícím nebo chemorezistentním nízce maligním nebo folikulárním B nehodgkinským lymfomem. Nemocní dostávali dávku 375 mg/m2 přípravku MabThera podávaného ve formě intravenózní infuze jednou týdně po dobu čtyř po sobě jdoucích týdnů. Celkový výskyt odpovědí na léčbu (ORR) byl v populaci "intent-to-treat" (ITT) zaznamenán ve 48 % (CI95% 41% - 56%) případů, přičemž v 6 % případů se jednalo o odpověď úplnou (CR), v 42 % o odpověď částečnou (PR). Medián doby do progrese onemocnění (TTP) byl u pacientů s léčebnou odpovědí stanoven na 13,0 měsíců. Multivariantní analýza prokázala lepší terapeutickou odpověď u pacientů, jejichž onemocnění bylo řazeno dle IWF (International Working Formulation) do skupiny B, C a D histologických podtypů v porovnání se skupinou A (58 % vs. 12 %), dále u nemocných, jejichž největší zjistitelná nádorová léze ve svém nejdelším rozměru měřila < 5 cm v porovnání s těmi, u kterých byl průměr tumoru > 7 cm (53 % vs. 38 %). Na léčbu lépe odpovídala onemocnění
v chemosenzitivním než v chemorezistentním relapsu (definovaném jako trvání odpovědí < 3 měsíce) (50 % vs. 22 %). Odpověď na léčbu u nemocných, kteří prodělali autologní transplantaci kostní dřeně (ABMT), nastala v 78 % případů oproti 43 % u pacientů bez ABMT. Odpověď na léčbu neovlivňovaly následující faktory: věk, pohlaví, histologický grading, iniciální diagnóza, bulky onemocnění, normální nebo vyšší hodnota LDH či extranodální onemocnění (statisticky hodnoceno Fisherovým exaktním testem). Naopak statisticky signifikantní korelace (p=0,0186) byla zjištěna u nemocných s infiltrací kostní dřeně (KD) - léčebná odpověď u pacientů s postižením KD byla zaznamenána ve 40 %, u nemocných bez infiltrace v 59 %. Tato korelace ale nebyla potvrzena v regresní analýze, ze které jako prognosticky významné vycházejí tyto faktory: histologický typ, bcl-2 pozitivita při zahájení léčby, rezistence na poslední chemoterapii a bulky onemocnění.
Úvodní terapie 8 dávek jednou týdně
V multicentrické jednoramenné studii bylo celkem 37 pacientů s relabujícím nebo resistentním lymfomem nízkého stupně malignity nebo s folikulárním B buněčným NHL léčeno přípravkem MabThera v dávce 375 mg/m2 povrchu těla, podávané v intravenózní infuzi jednou týdně po dobu osmi po sobě jdoucích týdnů. OrR byla 57 % (95% interval spolehlivosti (CI) 41 %-73 %; CR 14 %, PR 43 %), předpokládaná střední doba do progrese u pacientů odpovídajících na léčbu byla 19,4 měsíce (rozmezí 5,3-38,9 měsíce).
Úvodní terapie, bulky onemocnění, 4 dávky jednou týdně
Byla hodnocena souhrnná data ze tří různých studií, kde bylo léčeno 39 pacientů s relabujícím nebo chemorezistentním bulky onemocněním (rozměr jedné léze > 10 cm v průměru), s nízkomaligními lymfomy nebo s folikulárními B-NHL. Pacienti byli léčeni přípravkem MabThera v dávce 375 mg/m2 povrchu těla, podávané v intravenózní infuzi jednou týdně po dobu čtyř po sobě jdoucích týdnů. ORR byla 36 % (CI95% 21 %-51 %; CR 3 %, PR 33 %), předpokládaná střední doba do progrese u pacientů odpovídajících na léčbu byla 9,6 měsíce (rozmezí 4,5-26,8 měsíce).
Opakovaná léčba 4 dávky jednou týdně
V multicentrické jednoramenné studii bylo zařazeno 58 pacientů s relabujícím nebo chemorezistentním nízkomaligním lymfomem nebo folikulárním B-buněčným NHL s prokazatelnou odpovědí na první terapii přípravkem MabThera. Dávkování při léčbě relapsu bylo 375 mg/m2 povrchu těla, podávané v intravenózní infuzi jednou týdně po dobu čtyř po sobě jdoucích týdnů. Tři pacienti byli zařazeni po aplikaci dvou cyklů přípravku MabThera, byli tedy ve třetím cyklu. Dva pacienti byli zařazeni do studie dvakrát. Celkem tedy bylo hodnoceno 60 opakovaných léčebných cyklů, ORR byla 38 % (CI95% 26 %-51 %; 10 % CR, 28 % PR) s předpokládaným mediánem TTP pro pacienty s léčebnou odpovědí 17,8 měsíce (rozmezí 5,4-26,6). Srovnání s TTP pacientů léčených přípravkem MabThera poprvé (TTP 12,4 měsíce) vychází příznivěji pro opakovanou léčbu.
Iniciální léčba v kombinaci s chemoterapií
V otevřené randomizované studii bylo randomizováno celkem 322 nemocných s dříve neléčeným folikulárním lymfomem do skupiny léčené chemoterapií CVP (cyklofosfamid 750 mg/m2, vinkristin 1,4 mg/m2 do celkové dávky maximálně 2 mg v den 1, prednisolon 40 mg/m2/den ve dnech 1-5) opakující se každé 3 týdny do celkového počtu 8 dávek nebo do skupiny léčené přípravkem MabThera (375 mg/m2) v kombinaci s CVP (R-CVP). MabThera byla podávána prvý den každého léčebného cyklu. Celkem bylo léčeno a z pohledu účinnosti analyzováno 321 nemocných (162 R-CVP a 159 CVP). Medián sledování byl 53 měsíce. Léčba R-CVP vedla proti CVP k signifikantnímu zlepšení primárního cíle studie - doby do selhání léčby (27 měsíců proti 6,6 měsícům, p< 0,0001, log-rank test). Ve R-CVP skupině byla zaznamenána signifikantně (p< 0,0001, chí kvadrát test) vyšší odpověď lymfomu na léčbu (CR, Cru, PR) proti skupině CVP (80,9 % proti 57,2 %). Léčba kombinací R-CVP ve srovnání s CVP významně prodloužila dobu do progrese choroby či úmrtí, 33,6 měsíce oproti 14,7 měsíce (p < 0.0001, log-rank test). Medián trvání odpovědi byl ve skupině R-CVP 37,7 měsíce, ve skupině CVP byl 13,5 měsíce (p< 0,0001, log-rank test).
Srovnání celkového přežití mezi léčebnými skupinami ukázalo významný klinický rozdíl: (p=0.029, log-rank test stratifikovaný dle center): četnost přežití po 53 měsících byla u pacientů v rameni R-CVP
80,9 %, zatímco u pacientů v rameni CVP to bylo 71,1 %.
Výsledky tří dalších randomizovaných studií, které použily přípravek MabThera/Rituxan v kombinací s jiným chemoterapeutickým režimem než CVP (CHOP, MCP, CHVP-INF) také prokázaly významné zlepšení četnosti odpovědí, na čase závislých parametrů, včetně celkového přežití. Klíčové výsledky všech 4 studií jsou shrnuty v Tabulce 4.
přípravku MabThera s různými chemoterapeutickými režimy u folikulárního lymfomu. _____
|
Studie |
Léčba Počet pacientů |
Střední doba sledování, měsíce |
ORR % |
CR % |
Střední doba TTF/PFS/ EFS měsíce |
OS % |
|
M39021 |
CVP, 159 R-CVP, 162 |
53 |
57 81 |
10 41 |
Medián TTP: 14,7 33,6 P<0,0001 |
53 měsíce 71,1 80,9 p=0,029 |
|
GLSG’00 |
CHOP, 205 R-CHOP, 223 |
18 |
90 96 |
17 20 |
Medián TTF: 2,6 roků nedosažen p < 0,001 |
18 měsíců 90 95 p = 0,016 |
|
OSHO-39 |
MCP, 96 R-MCP, 105 |
47 |
75 92 |
25 50 |
Medián PFS: 28,8 nedosažen p < 0,0001 |
48 měsíců 74 87 p = 0,0096 |
|
FL2000 |
CHVP-IFN, 183 R-CHVP-IFN, 175 |
42 |
85 94 |
49 76 |
Medián EFS: 36 nedosažen p < 0,0001 |
42 měsíce 84 91 p = 0,029 |
EFS - Přežití bez události TTP - Doba do progrese či úmrtí PFS - Přežití bez progrese TTF - Doba do selhání léčby OS - Přežití v době analýzy
Udržovací terapie
Dosud neléčený folikulární lymfom
V prospektivní, otevřené, mezinárodní, multicentrické studii fáze III 1193 pacientů s dosud neléčeným pokročilým folikulárním lymfomem podstoupilo indukční léčbu R-CHOP (n=881), R-CVP (n=268) nebo R-FCM (n=44) dle volby zkoušejícího. Celkem 1078 pacientů odpovědělo na indukční léčbu, 1018 z nich bylo randomizováno k udržovací léčbě přípravkem MabThera (n=505) nebo ke sledování (n=513). Tyto dvě léčebné skupiny byly dobře vyváženy vzhledem k výchozím charakteristikám a rozsahu onemocnění. Udržovací léčba přípravkem MabThera spočívala v jedné infuzi přípravku MabThera v dávce 375 mg/m2 tělesného povrchu, která byla podávána každé 2 měsíce do progrese onemocnění či nejdéle po dobu 2 let.
Při střední době sledování 25 měsíců od randomizace vedla udržovací léčba přípravkem MabThera ve srovnání se samotným sledováním u dosud neléčených pacientů s folikulárním lymfomem ke klinicky důležitému a statisticky významnému zlepšení v primárním cílovém parametru účinnosti, kterým bylo přežití bez progrese (PFS) hodnocené zkoušejícím (Tabulka 5).
Významný přínos udržovací léčby přípravkem MabThera byl zaznamenán také u sekundárních cílových parametrů studie, kterými byly přežití bez příhody (EFS), doba do další protilymfomové léčby (TNLT), doba do další chemoterapie (TNCT) a celkový výskyt odpovědí (ORR) (tabulka 5). Výsledky primární analýzy byly potvrzeny na základě delší doby sledování (střední doba sledování: 48 měsíců a 73 měsíců), a aktualizované výsledky pak byly vloženy do tabulky 5 pro srovnání 25 a 48 měsíčního období sledování.
střední době sledování 73 měsíců (porovnáno s výsledky primární analýzy založené na střední době sledování 25 měsíců a aktuální analýzy založené na střední době sledování 48 měsíců)____
|
Sledování N=513 |
MabThera N=505 |
Log-rank P hodnota |
Snížení rizika | ||
|
Primární parametr | |||||
|
účinnosti | |||||
|
PFS (medián) |
48,5 měsíce |
NR |
<0,0001 |
42 % | |
|
[48,4 měsíce] |
[NR] |
[<0,0001 ] |
[45 %] | ||
|
(NR) |
(NR) |
(< 0,0001) |
(50 %) | ||
|
Se |
kundární parametry | ||||
|
účinnosti | |||||
|
EFS (medián) |
48,4 měsíce |
NR |
<0,0001 |
39 % | |
|
[47,6 měsíce] |
[NR] |
[<0,0001 ] |
[42 %] | ||
|
(37,8 měsíce) |
(NR) |
(< 0,0001) |
(46 %) | ||
|
OS (medián) |
NR |
NR |
0,8959 |
-2 % | |
|
[NR] |
[NR] |
[0,9298] |
[-2 %] | ||
|
(NR) |
(NR) |
(0,7246) |
(11 %) | ||
|
TNLT (medián) |
71,0 měsíce |
NR |
<0,0001 |
37 % | |
|
[60,2 měsíce] |
[NR] |
[<0,0001 ] |
[39 %] | ||
|
(NR) |
(NR) |
(0,0003) |
(39 %) | ||
|
TNCT (medián) |
85,1 měsíce |
NR |
0,0006 |
30 % | |
|
[NR] |
[NR] |
[0,0006] |
[34 %] | ||
|
(NR) |
(NR) |
(0,0011) |
(40 %) | ||
|
ORR* |
60,7 % |
79,0 % |
<0,0001# |
OR = 2,43 | |
|
[60,7 %] |
[79,0 %] |
[<0,0001#] |
[OR = 2,43] | ||
|
(55,0 %) |
(74,0 %) |
(< 0,0001#) |
(OR = 2,33) | ||
|
Četnost kompletních |
52,7 % |
66,8 % |
<0,0001 |
OR = 2,34 | |
|
remisí (CR/CRu)* |
[52,7 %] |
[72,2 %] |
[<0,0001 ] |
[OR = 2,34] | |
|
(47,7 %) |
(66,8 %) |
(< 0,0001) |
(OR = 2,21) | ||
*Na konci udržovací léčby/sledování; p hodnota chí-kvadrát testu.
Hodnoty na prvních řádcích odpovídají 73 měsícům střední doby sledování, hodnoty v závorkách psané kurzívou odpovídají 48 měsícům střední doby sledování a hodnoty v závorkách odpovídají 25 měsícům střední doby sledování (primární analýza). PFS: přežití bez progrese; EFS: přežití bez příhody; OS: celkové přežití; TNLT: doba do další protilymfomové léčby;
TNCT: doba do další chemoterapie; ORR: celkový výskyt odpovědí; NR: nebylo možno dosáhnout v době klinické uzávěrky; OR: poměr šancí.
Udržovací léčba přípravkem MabThera poskytla konzistentní přínos pro všechny předdefinované hodnocené podskupiny: pohlaví (muži, ženy), věk (do 60 let, nad 60 let včetně), hodnota FLIPI (<=1,
2 nebo >=3), indukční léčba (R-CHOP, R-CVP nebo R-FCM) a bez ohledu na kvalitu léčebné odpovědi na indukční léčbu (CR, CRu nebo PR). Exploratorní analýzy prospěchu udržovací léčby prokázaly méně výrazný účinek u starších pacientů (> 70 let), hodnocený vzorek však byl malý.
Relabující/refrakterní folikulární lymfom
V prospektivní, otevřené, mezinárodní, multicentrické klinické studii fáze III bylo v prvním kroku indukční terapie randomizováno 465 pacientů s relabujícím/refrakterním folikulárním lymfomem do skupiny podstupující CHOP (cyklofosfamid, doxorubicin, vinkristin, prednisolon; n=231) nebo do skupiny léčené přípravkem MabThera plus CHOP (R-CHOP, n=234). Dvě léčebné skupiny byly vyvážené z hlediska vstupních charakteristik a stavu onemocnění. Celkem 334 pacientů, kteří po indukční terapii dosáhli kompletní nebo částečné remise, bylo randomizováno v druhém kroku do skupiny s udržovací terapií přípravkem MabThera (n=167) nebo do skupiny podstupující pouze observaci (n=167). Udržovací léčba přípravkem MabThera spočívala v aplikaci jedné infuze přípravku MabThera v dávce 375 mg/m2 plochy povrchu těla, která byla podávána jedenkrát za 3 měsíce až do doby progrese choroby nebo nejvýše po dobu dvou let.
Závěrečná analýza účinnosti zahrnovala všechny pacienty, kteří byli randomizováni v obou částech studie. Po době observace, která byla u pacientů randomizovaných do indukční fáze průměrně 31
měsíců, se stav pacientů s relabujícím/refraktemím folikulámím lymfomem, kteří podstoupili terapii R-CHOP v porovnání s CHOP, signifikantně zlepšil (viz Tabulka 6).
Tabulka 6 Indukční fáze: přehled výsledků účinnosti CHOP vs. R-CHOP (střední doba
_sledování 31 měsíců)_
|
CHOP |
R-CHOP |
Hodnota p |
Snížení rizika^ | |
|
Primární účinnost orr2) |
74 % |
87 % |
0,0003 |
NA |
|
cr2) |
16 % |
29 % |
0,0005 |
NA |
|
pr2) |
58 % |
58 % |
0,9449 |
NA |
'-1 Odhady vypočítány na základě poměrů rizik
2) Poslední protinádorová odpověď stanovená zkoušejícím. "Primární" statistické testy pro "odpověď" byly vyjádřeny jako trend testu CR versus PR versus nulová odpověď (p < 0,0001)
Vysvětlivky: NA: nedostupná data; ORR: celkový výskyt odpovědí; CR: kompletní odpověď; PR: částečná odpověď
U pacientů randomizovaných do udržovací fáze klinické studie byl medián doby observace 28 měsíců od randomizace. Udržovací léčba přípravkem MabThera vedla ke klinicky relevantnímu a statisticky významnému zlepšení z hlediska primárního cíle, PFS (doba od randomizace do udržovací fáze do relapsu, progrese choroby nebo úmrtí) při srovnání s observační skupinou (bez léčby) (p< 0,0001, log-rank test). Dosažený medián PFS byl 42,2 měsíce ve skupině s udržovací léčbou přípravkem MabThera v porovnání s 14,3 měsíce ve skupině bez léčby. Použití regresní analýzy (Coxův model) ukázalo, že v důsledku udržovací léčby přípravkem MabThera je riziko progrese nebo úmrtí sníženo o 61 % ve srovnání se skupinou bez léčby (95% CI; 45 %-72 %). Odhad počtu odpovědí bez progrese vycházející z Kaplan-Meierových křivek po 12 měsících léčby byl 78 % ve skupině s udržovací léčbou přípravkem MabThera oproti 57 % ve skupině bez léčby. Analýza celkového přežití potvrdila signifikantní výhodnost udržovací léčby přípravkem MabThera oproti observační skupině (p=0,0039 log-rank test). V důsledku udržovací léčby přípravkem MabThera bylo riziko úmrtí sníženo o 56 % (95% CI; 22 %-75 %).
Tabulka 7 Udržovací fáze: přehled výsledků účinnosti ve skupině léčené přípravkem
|
MabThera oproti o |
rservační skupině (střední doba sledování 28 měsíců) | |||
|
Parametr účinnosti |
Určení mediánu doby (měsíce) k dosažení |
Snížení rizika | ||
|
stanoveného parametru metodou | ||||
|
Kaplan-Meier | ||||
|
Observace |
MabThera |
Log-Rank | ||
|
(N = 167) |
(N=167) |
hodnota p | ||
|
Doba přežití bez progrese (PFS) |
14,3 |
42,2 |
<0,0001 |
61 % |
|
Celkové přežití |
NR |
NR |
0,0039 |
56 % |
|
Doba do nové léčby lymfomu |
20,1 |
38,8 |
<0,0001 |
50 % |
|
Doba přežití bez známek onemocnění3 |
16,5 |
53,7 |
0,0003 |
67 % |
|
Analýza podskupin PFS | ||||
|
CHOP |
11,6 |
37,5 |
<0,0001 |
71 % |
|
R-CHOP |
22,1 |
51,9 |
0,0071 |
46 % |
|
CR |
14,3 |
52,8 |
0,0008 |
64 % |
|
PR |
14.3 |
37,8 |
<0,0001 |
54 % |
|
OS | ||||
|
CHOP |
NR |
NR |
0,0348 |
55 % |
|
R-CHOP |
NR |
NR |
0,0482 |
56 % |
NR: nedosaženo; a: relevantní pouze u pacientů, kteří dosáhli kompletní odpovědi
Výhodnost udržovací léčby přípravkem MabThera byla potvrzena ve všech analyzovaných podskupinách bez ohledu na indukční režim (CHOP nebo R-CHOP) nebo kvalitu odpovědi v rámci indukční léčby (CR nebo PR) (viz Tabulka 7). V důsledku udržovací léčby přípravkem MabThera byl významně prodloužen medián PFS u pacientů odpovídajících na indukční terapii CHOP (medián PFS
37,5 měsíce vs. 11,6 měsíce, p< 0,0001), stejně jako u pacientů odpovídajících na indukční léčbu R-CHOP (medián PFS 51,9 měsíce vs. 22,1 měsíce, p=0,0071). Přestože se jednalo o malé podskupiny, ukázala se udržovací léčba přípravkem MabThera signifikantně výhodnou i z hlediska celkového přežití, a to jak u pacientů odpovídajících na CHOP, tak u pacientů odpovídajících na R-CHOP, ačkoli pro potvrzení tohoto zjištění je zapotřebí delší doba sledování po léčbě.
Difúzní velkobuněčný nehodgkinský lymfom z B buněk
399 dosud neléčených starších pacientů (věk 60 až 80 let) s diagnostikovaným difúzním velkobuněčným B-nehodgkinským lymfomem bylo v rámci randomizované, otevřené studie léčeno osmi cykly standardní chemoterapie CHOP (cyklofosfamid 750 mg/m2 den 1, doxorubicin 50 mg/m2 den 1, vinkristin 1,4 mg/m2 den 1 do maximální dávky 2 mg a prednison 40 mg/m2/den podávaný ve dnech 1-5) aplikované v intervalu 3 týdnů po osm cyklů nebo přípravkem MabThera s chemoterapií CHOP (R-CHOP). Přípravek MabThera byl podáván první den každého léčebného cyklu.
Závěrečná analýza účinnosti byla provedena u všech randomizovaných pacientů (197 CHOP, 202 R-CHOP) a střední hodnota trvání následného sledování byla přibližně 31 měsíců. Obě skupiny byly vyrovnané s ohledem na charakteristiku a pokročilost onemocnění na počátku léčby. Závěrečná analýza potvrdila, že léčebný režim R-CHOP byl spojen s klinicky relevantním a statisticky významným prodloužením přežití bez výskytu nežádoucích příhod (což byl hlavní parametr účinnosti, kde příhodou bylo úmrtí, relaps nebo progrese lymfomu, nebo zahájení nové léčby lymfomu) (p=0,0001). Střední hodnota trvání bezpříznakového období stanovená metodou Kaplan-Meier byla 35 měsíců ve skupině léčené režimem R-CHOP, ve srovnání s 13 měsíci ve skupině léčené režimem CHOP, což představuje snížení rizika o 41 %. Celkové přežití ve 24. měsíci bylo 68,2 % ve skupině léčené R-CHOP ve srovnání s 57,4 % ve skupině léčené režimem CHOP. Následná analýza celkového přežití, provedená po 60 měsících následného sledování, potvrdila větší prospěšnost R-CHOP než CHOP (p=0,0071), což představuje snížení rizika o 32 %.
Analýza všech sekundárních parametrů (četnost odezvy na léčbu, přežití bez známek progrese, přežití bez známek nemoci, trvání odpovědi) ověřila léčebný účinek R-CHOP ve srovnání s CHOP. Celková četnost odezvy na léčbu po 8 cyklech byla 76,2 % ve skupině léčené R-CHOP a 62,4 % ve skupině léčené CHOP (p = 0,0028). Riziko progrese nemoci se snížilo o 46 % a riziko relapsu o 51 %. Ve všech podskupinách pacientů (pohlaví, věk, IPI korigovaný na věk, stádium nemoci dle Ann Arbor, ECOG, B2 2 mikroglobulin, LDH, albumin, B-symptomy, bulky disease, mimouzlinová manifestace, postižení kostní dřeně) byly poměry rizik pro asymptomatické přežití a celkové přežití (R-CHOP oproti CHOP) nižší než 0,83 a 0,95. Režim R-CHOP byl spojen se zlepšeným výsledkem léčby u vysoce a nízkorizikových pacientů podle IPI korigovaného na věk.
Klinické laboratorní nálezy
U 67 nemocných vyšetřovaných pro přítomnost HAMA (protilátky proti myším antigenům) nebyla zaznamenána žádná odpověď. Z 356 nemocných vyšetřovaných pro přítomnost HACA (human anti-chimeric antibody) bylo 1,1 % pozitivních (4 pacienti).
Chronická lymfocytární leukemie
Ve dvou otevřených, randomizovaných studiích bylo celkem 817 dosud neléčených pacientů a 552 pacientů s relabující/refrakterní CLL randomizováno k léčbě buď chemoterapií FC (fludarabin 25 mg/m2, cyklofosfamid 250 mg/m2, dny 1-3) podávané každé 4 týdny v 6 cyklech nebo k léčbě přípravkem MabThera v kombinaci s chemoterapií FC (R-FC). Přípravek MabThera byl podáván v dávce 375 mg/m2 během prvního dne prvního cyklu před chemoterapií a v dávce 500 mg/m2 v den 1 následných léčebných cyklů. Ze studie s relabující/refrakterní CLL byli vyloučeni pacienti, kteří byli dříve léčeni monoklonálními protilátkami nebo kteří nereagovali (definováno jako selhání dosažení částečné remise alespoň po dobu 6 měsíců) na léčbu fludarabinem nebo jakýmkoliv nukleosidovým analogem. Analýza účinnosti byla provedena u 810 pacientů (403 R-FC, 407 FC) ze studie s první linií léčby (Tabulka 8a a Tabulka 8b) a u 552 pacientů (276 R-FC, 276 FC) ze studie s relabující/refrakterní CLL (viz Tabulka 9).
Ve studii s první linií léčby při střední době sledování 48,1 měsíce byla střední hodnota přežití bez progrese ve skupině R-FC 55 měsíců a ve skupině FC 33 měsíce (p < 0,0001, log-rank test). Analýza celkového přežití nadále prokazuje významný přínos léčby R-FC oproti samotné chemoterapii FC (p = 0,0319, log-rank test) (Tabulka 8a). Přínos ve smyslu prodloužení PFS byl konzistentně pozorován ve většině podskupin pacientů analyzovaných na základě vstupního rizika choroby (tj. pro stádia choroby dle Bineta A-C) (Tabulka 8b).
Tabulka 8a Léčba chronické lymfocytární leukemie v první linii
Přehled výsledků účinnosti pro kombinaci MabThera plus FC vs. samotné FC -
|
střední doba slet |
ování 48,1 měsíce | |||
|
Parametr účinnosti |
Odhad střední doby do události dle |
Snížení | ||
|
Kaplan-Meiera (měsíce) |
rizika | |||
|
FC |
R-FC |
Log-Rank | ||
|
(N = 409) |
(N=408) |
p hodnota | ||
|
Přežití bez progrese (PFS) |
32,8 |
55,3 |
<0,0001 |
45 % |
|
Celkové přežití |
NR |
NR |
0,0319 |
27 % |
|
Přežití bez události |
31,3 |
51,8 |
<0,0001 |
44 % |
|
Léčebná odpověď (CR, nPR, či |
72,6 % |
85,8 % |
<0,0001 |
n.a. |
|
PR) | ||||
|
Četnost CR |
16,9 % |
36,0 % |
<0,0001 |
n.a. |
|
Trvání odpovědi* |
36,2 |
57,3 |
<0,0001 |
44 % |
|
Přežití bez známek choroby |
48,9 |
60,3 |
0,0520 |
31 % |
|
(DFS)** | ||||
|
Doba do další léčby |
47,2 |
69,7 |
<0,0001 |
42 % |
Analýza léčebné odpovědi a četnosti CR pomocí Chí-kvadrátového testu. NR: nedosaženo; n.a.: není použitelné *: týká se pouze pacientů, kteří dosáhli CR, nPR, PR **: týká se pouze pacientů, kteří dosáhli CR
Tabulka 8b První linie léčby chronické lymfocytární leukemie
Poměry rizik pro přežití bez progrese podle stádia dle Bineta (ITT) - střední doba sledování 48,1 měsíce_
|
Přežití bez progrese (PFS) |
Počet pacientů |
Poměr rizik (95% CI) |
p-hodnota (Wald test, neadjustovaný) | |
|
FC |
R-FC | |||
|
Stádium A dle Bineta |
22 |
18 |
0,39 (0,15; 0,98) |
0,0442 |
|
Stádium B dle Bineta |
259 |
263 |
0,52 (0,41; 0,66) |
<0,0001 |
|
Stádium C dle Bineta |
126 |
126 |
0,68 (0,49; 0,95) |
0,0224 |
CI: Interval spolehlivosti
Ve studii s relabující/refrakterní CLL bylo přežití bez progrese (primární cílový parametr) 30,6 měsíců ve skupině R-FC a 20,6 měsíců ve skupině FC (p=0,0002, log-rank test). Prospěch PFS byl pozorován u téměř všech pacientů analyzovaných subskupin podle rizika onemocnění na začátku studie. Mírné, ale ne významné zlepšení v celkovém přežití bylo zaznamenáno v rameni R-FC v porovnání s FC.
účinnosti přípravku MabThera s FC v porovnání s FC samotným (střední doba sledování 25,3 měsíců)._
|
Parametr účinnosti |
Odhad střední doby do události dle Kaplan-Meiera (měsíce) |
Snížení rizika | ||
|
FC (N = 276) |
R-FC (N=276) |
Log-Rank p hodnota | ||
|
Přežití bez progrese (PFS) |
20,6 |
30,6 |
0,0002 |
35% |
|
Celkové přežití |
51,9 |
NR |
0,2874 |
17% |
|
Přežití bez události |
19,3 |
28,7 |
0,0002 |
36% |
|
Léčebná odpověď (CR, nPR, či PR) |
58,0% |
69,9% |
0,0034 |
n.a. |
|
Četnost CR |
13,0% |
24,3% |
0,0007 |
n.a. |
|
Trvání odpovědi * |
27,6 |
39,6 |
0,0252 |
31% |
|
Přežití bez známek choroby (DFS)** |
42,2 |
39,6 |
0,8842 |
-6% |
|
Doba do další léčby |
34,2 |
NR |
0,0024 |
35% |
Analýza léčebné odpovědi a četnosti CR pomocí Chí-kvadrátového testu.
*: týká se pouze pacientů, kteří dosáhli CR, nPR, PR; NR: nedosaženo n.a.: není použitelné **: týká se pouze pacientů, kteří dosáhli CR;
Výsledky z dalších podpůrných studií, které využívaly v léčbě CLL přípravek MabThera v kombinaci s jinými chemoterapeutickými režimy u dříve neléčených a/nebo relabujících/refrakterních pacientů s CLL (zahrnující CHOP, FCM, PC, PCM, bendamustin a kladribin) také ukázaly vysokou četnost kompletních léčebných odpovědí s prospěchem v PFS, i když s mírně vyšší toxicitou (zvláště myelotoxicitou). Tyto studie podporují užití přípravku MabThera s jakoukoli chemoterapií.
Údaje od přibližně 180 pacientů předléčených přípravkem MabThera prokázaly klinický prospěch (včetně CR) a podporují opakovanou léčbu přípravkem MabThera.
Pediatrická _ populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem MabThera u všech podskupin pediatrické populace s folikulárním lymfomem a chronickou lymfocytární leukemií. Informace o použití u dětí viz bod 4.2.
Klinické zkušenosti v léčbě revmatoidní artritidy
Bezpečnost a účinnost přípravku MabThera z hlediska zmírnění příznaků a známek revmatoidní artritidy u pacientů s nedostatečnou odpovědí na léčbu inhibitory tumor nekrotizujícího faktoru (TNF) byla demonstrována v klíčové randomizované, kontrolované, dvojitě zaslepené, multicentrické studii (Studie 1).
Studie 1 hodnotila 517 pacientů, kteří vykazovali nedostatečné odpovědi nebo nesnášenlivost na jednu či více terapií inhibitory TNF. Pacienti, kteří byli vybráni do studií, měli aktivní revmatoidní artritidu, diagnostikovanou v souladu s kritérii Amerického sdružení pro revmatologii (ACR, American College of Rheumatology). Přípravek MabThera byl podán ve formě dvou i.v. infuzí s odstupem 15 dnů. Pacienti dostávali 2 x 1000 mg přípravku MabThera i.v. infuzí nebo placebo v kombinaci s MTX. Všichni pacienti dostávali souběžnou léčbu 60 mg perorálního prednisonu ve dnech 2 -7 a 30 mg ve dnech 8 - 14 po první infuzi. Primárním cílovým parametrem byl podíl pacientů, kteří dosáhli ve 24. týdnu odpovědi ACR20. Pacienti byli dále sledováni i po týdnu 24 z hlediska dlouhodobých cílů, což zahrnovalo i radiologické vyšetření po 56 týdnech a 104 týdnech. Během této doby dostalo mezi
týdny 24 a 56 přípravek MabThera v rámci prodloužené otevřené klinické studie 81 % pacientů ze skupiny léčené původně placebem.
Studie s přípravkem MabThera u pacientů s časnou artritidou (pacienti bez předchozí léčby metotrexátem a pacienti s nedostatečnou odpovědí na metotrexát, ale dosud neléčení inhibitory TNF-alfa) splnily své primární cílové parametry. Přípravek MabThera není u těchto pacientů indikován, protože údaje o bezpečnosti týkající se dlouhodobé léčby přípravkem MabThera nejsou dostatečné, zvláště co se týká rizika rozvoje malignit a PML.
Výsledky z hlediska aktivity onemocnění
Přípravek MabThera v kombinaci s metotrexátem významně zvýšil podíl pacientů vykazujících nejméně 20 % zlepšení ACR skóre ve srovnání s pacienty léčenými samotným metotrexátem (viz Tabulka 10). Ve všech vývojových studiích byl prospěch léčby u pacientů obdobný nezávisle na věku, pohlaví, ploše povrchu těla, rase, počtu předchozích terapií nebo stavu onemocnění.
Klinicky a statisticky významné zlepšení bylo zaznamenáno také ve všech jednotlivých složkách ACR odpovědi (počet oteklých a bolestivých kloubů, celkové hodnocení pacientem a lékařem, skóre indexu HAQ, hodnocení stupně bolesti a C- reagujících proteinů (mg/dl)).
Tabulka 10 Klinické výsledky podle primárního cílového parametru účinnosti _ ve Studii 1 (ITT populace)__
|
Výsledekf |
Placebo+MTX |
MabThera+MTX (2 x 1000 mg) | |
|
Studie 1 |
N= 201 |
N= 298 | |
|
ACR20 ACR50 ACR70 |
36 (18 %) 11 (5 %) 3 (1 %) |
153 (51 %)*** 80 (27 %)*** 37 (12 %)*** | |
|
EULAR odpověď (dobrá/střední) |
44 (22 %) |
193 (65 %)*** | |
|
Průměrná změna DAS |
-0,34 |
-1,83*** |
f Výsledek v 24 týdnech
Významný rozdíl v porovnání s placebem + MTX v době hodnocení primárního cílového parametru účinnosti: ***p < 0,0001
Pacienti léčení přípravkem MabThera v kombinaci s metotrexátem měli významně větší snížení skóre aktivity onemocnění (DAS28) než pacienti dostávající pouze metotrexát (Tabulka 9). Ve všech studiích bylo dosaženo podobně dobré až střední odpovědi dle kritérií Evropské ligy proti revmatismu (EULAR, European League Against Rheumatism) u významně většího počtu pacientů dostávajících přípravek MabThera a metotrexát ve srovnání s pacienty léčenými samotným metotrexátem (viz Tabulka 10).
Radiologická odpověď
Strukturální poškození kloubů bylo hodnoceno radiograficky a bylo vyjádřeno jako změna v modifikovaném celkovém skóre dle Sharpa (mTSS, modified Total Sharp Score) a jeho jednotlivých položkách - ve skóre erozí a skóre zúžení kloubní štěrbiny.
Ve Studii 1 prováděné u pacientů s nedostatečnou odpovědí či s nesnášenlivostí jedné či více léčeb inhibitorem TNF, kteří dostávali přípravek MabThera v kombinaci s metotrexátem, byla prokázána po 56 týdnech významně menší radiologická progrese než u pacientů, kteří byli zpočátku léčeni samotným metotrexátem. Z pacientů léčených původně samotným metotrexátem jich do týdne 56 81 % podstoupilo léčbu přípravkem MabThera buďto jako záchrannou léčbu mezi týdny 16-24 nebo v průběhu prodloužené studie. Větší část pacientů léčená od počátku kombinací přípravku MabThera/MTX také neměla po 56 týdnech progresi erozí (Tabulka 11).
|
Placebo+MTX |
MabThera +MTX 2 x 1000 mg | |
|
Studie 1 |
(n = 184) |
(n = 273) |
|
Průměrná změna od výchozích hodnot: | ||
|
Modifikované celkové skóre dle Sharpa |
2,30 |
1,01* |
|
Skóre erozí |
1,32 |
0,60* |
|
Skóre zúžení kloubních štěrbin |
0,98 |
0,41** |
|
Podíl pacientů bez radiografických změn |
46 % |
53 %, NS |
|
Podíl pacientů bez erozivních změn |
52 % |
60 %, NS |
150 pacientů původně randomizovaných do skupiny s placebem + MTX ve studii 1 dostalo během jednoho roku alespoň jeden cyklus léčby RTX + MTX * p <0,05, ** p < 0,001. Vysvětlivky: NS: nevýznamný
Inhibice rychlosti progrese kloubního poškození byla rovněž pozorována dlouhodobě. Radiografická analýza ve 2. roce ve studii 1 prokázala významné snížení progrese strukturálního kloubního poškození u pacientů, kteří dostávali přípravek MabThera v kombinaci s metotrexátem v porovnání s metotrexátem samotným, stejně jako významně vyšší podíl pacientů bez progrese kloubního poškození během dvou let.
Fyzické funkce a výsledky z hlediska kvality života
Bylo pozorováno významné snížení indexu HAQ-DI a indexu únavy (FACIT-Fatigue) u pacientů léčených přípravkem MabThera ve srovnání s pacienty léčenými pouze metotrexátem. Podíl pacientů léčených přípravkem MabThera, který vykazoval minimální klinicky významný rozdíl (MCID, minimal clinically important difference) v HAQ-DI (definovaném jako pokles individuálního celkového skóre o > 0,22), byl rovněž vyšší, než mezi pacienty dostávajícími metotrexát samotný (Tabulka 12).
Významné zlepšení kvality života v souvislosti se zdravím bylo rovněž prokázáno významným zlepšením jak ve skóre fyzického zdraví (PHS, physical health score) tak i skóre mentálního zdraví (MHS, mental health score) v dotazníku SF-36. Kromě toho dosáhl MCID v těchto skóre i významně vyšší podíl pacientů (Tabulka 12).
|
Výsledkyf |
Placebo+MTX |
MabThera+MTX (2 x 1000 mg) |
|
n=201 |
n=298 | |
|
Průměrná změna v HAQ-DI |
0,1 |
-0 4*** |
|
% HAQ-DI MCID |
20 % |
51 % |
|
Průměrná změna ve FACIT-T |
-0,5 |
-9 1*** |
|
n=197 |
n=294 | |
|
Průměrná změna ve SF-36 PHS |
0,9 |
5,8*** |
|
% SF-36 PHS MCID |
13 % |
48 %*** |
|
Průměrná změna ve SF-36 MHS |
1,3 |
4 7** |
|
% SF-36 MHS MCID |
20 % |
38 %* |
f Výsledky v týdnu 24
Významný rozdíl ve srovnání s placebem v době hodnocení primárního cílového parametru účinnosti: * p < 0,05, **p <
0,001 ***p < 0,0001
MCID HAQ-DI > 0,22, MCID SF-36 PHS > 5,42, MCID SF-36 MHS > 6,33
Účinnost u pacientů séropozitivních na autoprotilátky (RF a/nebo anti-CCP)
Pacienti séropozitivní na revmatoidní faktor (RF) a/nebo anti-CCP (anti-Cyclic Citrullinated Peptide), kteří byli léčeni přípravkem MabThera v kombinaci s metotrexátem, vykazovali lepší odpověď v porovnání s pacienty negativními na obě autoprotilátky.
Parametry účinnosti u pacientů léčených přípravkem MabThera byly analyzovány na základě stavu autoprotilátek před zahájením léčby. V týdnu 24 měli pacienti, kteří byli séropozitivní na RF a/nebo anti-CCP v úvodu léčby, významně větší šanci, že dosáhnou odpovědi ACR20 a ACR50, v porovnání se séronegativními pacienty (p=0,0312 and p=0,0096) (Tabulka 13). Tyto nálezy byly shodné v týdnu 48, kdy séropozitivita autoprotilátek rovněž významně zvyšovala pravděpodobnost dosažení ACR70. V týdnu 48 byla u séropozitivních pacientů 2-3násobně vyšší pravděpodobnost, že dosáhnou ACR odpovědi, ve srovnání s pacienty séronegativními. U séropozitivních pacientů docházelo rovněž k významně většímu poklesu DAS28-ESR v porovnání se séronegativními pacienty (Obrázek 1).
Tabulka 13 Shrnutí účinnosti podle stavu autoprotilátek v úvodu léčby
|
Týde Séropozitivní (n=514) |
;n 24 Séronegativní (n=106) |
Týde Séropozitivní (n=506) |
:n 48 Séronegativní (n=101) | |
|
ACR20 (%) |
62,3* |
50,9 |
71, 1* |
51,5 |
|
ACR50 (%) |
32,7* |
19,8 |
44,9** |
22,8 |
|
ACR70 (%) |
12,1 |
5,7 |
20,9* |
6,9 |
|
EULAR reakce (%) |
74,8* |
62,9 |
84,3* |
72,3 |
|
Průměrná změna DAS28-ESR |
-1,97** |
-1,50 |
-2 48*** |
-1,72 |
Hladiny významnosti byly definovány jako * p<0,05 **p<0,001, ***p<0,0001.

Dlouhodobá účinnost při opakovaných cyklech léčby
Léčba přípravkem MabThera v kombinaci s metotrexátem vedla při opakovaných cyklech léčby k setrvalému zlepšení klinických objektivních i subjektivních příznaků RA, jak vyplývá z ACR, DAS28-ESR a EULAR odpovědí, které jsou průkazné u všech studovaných populací pacientů (Obrázek 2). Bylo pozorováno setrvalé zlepšení fyzických funkcí, což naznačuje HAQ-DI skóre a podíl pacientů, kteří dosáhli MCID pro HAQ-DI.
Obrázek 2: ACR odpovědi ve 4 cyklech léčby (24 týdnů po každém cyklu (na pacienta a návštěvu)) u pacientů s nedostatečnou odpovědí na inhibitory TNF (n=146)
(0
+■»
c
.92
re
o.
4—
O

1st 2nd 3rd 4th Course Course Course Course

■ ACR20
□ ACR50
□ ACR70
Klinické laboratorní nálezy
Celkem 392 z 3095 (12,7 %) pacientů s revmatoidní artritidou v klinických studiích s přípravkem MabThera bylo po terapii pozitivně testováno na přítomnost HACA. Tvorba HACA nebyla u většiny pacientů spojena s klinickým zhoršením ani se zvýšeným rizikem reakce na následné infuze. Tvorba protilátek HACA může být spojena se zhoršením reakcí na infuzi nebo alergických reakcí, které se objevují po druhé infuzi následného cyklu.
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem MabThera u všech podskupin pediatrické populace s autoimunitní artritidou. Informace o použití u dětí viz bod 4.2.
Klinické zkušenosti u granulomatózy s polyangiitidou (Wegenerova granulomatóza) a mikroskopické polvangiitidv
V randomizované, dvojitě zaslepené, placebem kontrolované multicentrické studii s aktivním komparátorem hodnotící non-inferioritu přípravku bylo zařazeno a léčeno celkem 197 pacientů ve věku 15 let nebo starších se závažnou aktivní granulomatózou s polyangiitidou (75 %) a mikroskopickou polyangiitidou (24 %).
Pacienti byli randomizováni v poměru 1:1 k léčbě buď perorálním cyklofosfamidem v dávce 2 mg/kg/den podávané denně po dobu 3-6 měsíců, nebo k léčbě přípravkem MabThera (375 mg/m2) jednou týdně po dobu 4 týdnů. Všichni pacienti v rameni s cyklofosfamidem dostávali udržovací léčbu azathioprinem v průběhu období následného sledování. Pacienti v obou ramenech dostávali pulsní intravenózní (i.v.) léčbu methylprednisolonem v denní dávce 1000 mg (nebo ekvivalentní dávku jiného glukokortikoidu) po dobu 1-3 dnů, po které následovala perorální léčba prednisonem (1 mg/kg/den s maximální dávkou nepřesahující 80 mg/den). Léčba prednisonem musela být ukončena do 6 měsíců od zahájení studijní léčby.
Primárním výsledkem bylo dosažení úplné remise v 6. měsíci definované jako BVAS/WG (Birmingham Vasculitis Activity Score for Wegener’s Granulomatosis) 0 a vysazení léčby glukokortikoidy. Předem určená hranice non-inferiority pro rozdíl v léčbě byla 20 %. Studie prokázala non-inferioritu přípravku MabThera vůči cyklofosfamidu u úplné remise (CR) v 6. měsíci léčby (Tabulka 14).
Účinnost byla pozorována jak u pacientů s nově diagnostikovaným onemocněním, tak i u pacientů s relabujícím onemocněním (Tabulka 15).
Tabulka 14
Procento pacientů, kteří dosáhli úplné remise v 6. měsíci (intent-to-treat populace*)
|
MabThera (n = 99) |
Cyklofosfamid (n = 98) |
Rozdíl v léčbě (MabThera-Cyklofosfamid) | |
|
Výskyt |
63,6 % |
53,1 % |
10,6 % 95,1%b CI (-3,2 %, 24,3 %) a |
|
- CI = interval spolehlivosti - * Nejhorší zaznamenaný případ a Non-inferiorita byla prokázána, protože nižší hranice (-3,2 %) byla vyšší než předem stanované hranice non-inferiority (-20 %). b 95,1% hladina spolehlivosti odpovídá dalšímu 0,001 alfa k výpočtu průběžné analýzy účinnosti. | |||
Tabulka 15 Úplná remise v 6. měsíci podle stavu onemocnění
|
MabThera |
Cyklofosfamid |
Rozdíl (CI 95%) | |
|
Všichni pacienti |
n=99 |
n=98 | |
|
Nově diagnostikovaní |
n=48 |
n=48 | |
|
Relabující |
n=51 |
n=50 | |
|
Úplná remise | |||
|
Všichni pacienti |
63,6 % |
53,1 % |
10,6 % (-3,2, 24,3) |
|
Nově diagnostikovaní |
60,4 % |
64,6 % |
-4,2 % (-23,6, 15,3) |
|
Relabující |
66,7 % |
42,0 % |
24,7 % (5,8, 43,6) |
Nejhorší zaznamenaný případ je použit u pacientů s chybějícími údaji.
Úplná remise ve 12 a 18 měsících
Ve skupině léčené přípravkem MabThera dosáhlo úplné remise 48 % pacientů ve 12 měsících a 39 % pacientů v 18 měsících. U pacientů léčených cyklofosfamidem (následovaným azathioprinem k udržení úplné remise) dosáhlo úplné remise 39 % pacientů ve 12 měsících a 33 % pacientů v 18 měsících. Od 12. do 18. měsíce bylo ve skupině léčené přípravkem MabThera pozorováno 8 relapsů, ve srovnání s 4 relapsy ve skupině léčené cyklofosfamidem.
Opakovaná léčba přípravkem MabThera
Na základě hodnocení zkoušejícím podstoupilo 15 pacientů druhý cyklus léčby přípravkem MabThera k léčbě relapsu aktivity onemocnění, ke kterému došlo mezi 6 a 18 měsíci po prvním cyklu léčby přípravkem MabThera. Omezené údaje ze současné studie znemožňují hodnocení týkající se účinnosti následných cyklů léčby přípravkem MabThera u pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou.
Následná imunosupresivní léčba může být obzvláště vhodná u pacientů s rizikem relapsu (např. s dřívějším relapsem v minulosti a granulomatózou s polyangiitidou nebo pacienti s rekonstitucí B lymfocytů kromě sledování PR3-ANCA). Pokud bylo dosaženo remise použitím přípravku MabThera, může se zvážit následná imunosupresivní léčba jako prevence relapsu. Nebyla prokázána účinnost a bezpečnost udržovací terapie přípravkem MabThera.
Laboratorní vyšetření
Celkem 23/99 (23 %) pacientů léčených přípravkem MabThera v této studii bylo HACA pozitivních do 18. měsíce. Žádný z 99 pacientů léčených přípravkem MabThera nebyl HACA pozitivní při screeningu. Klinický význam tvorby HACA u pacientů léčených přípravkem MabThera není zřejmý.
5.2 Farmakokinetické vlastnosti
Nehodgkinské lymfomy
Na základě populační farmakokinetické analýzy u 298 pacientů s NHL, kteří dostali jednu či více infuzí přípravku MabThera samostatně či v kombinaci s chemoterapií CHOP (použité dávky přípravku Mabthera se pohybovaly v rozmezí od 100 do 500 mg/m2), byly hodnoty nespecifické clearance (CLj),
specifické clearance (CL2) pravděpodobně ovlivněné B buňkami či nádorovou náloží a centrálním distribučním objemem (V1) odhadnuty v typické populaci na 0,14 l/den, 0,59 l/den a 2,7 l. Odhadovaná střední hodnota terminálního eliminačního poločasu přípravku MabThera byla 22 dní (rozmezí 6,1 - 52 dní). Vstupní hodnota počtu CD19 pozitivních buněk a velikost měřitelných nádorových ložisek přispěla k jisté variabilitě hodnoty CL2 pro přípravek MabThera u hodnot získaných od 161 pacientů, kteří dostali intravenózní dávku 375 mg/m2 ve 4 týdenních dávkách. Pacienti s vyšším počtem CD19 pozitivních buněk nebo nádorových ložisek měli vyšší hodnotu CL2. Avšak i po korekci hodnot CL2 pro počet CD19 pozitivních buněk a velikost nádorových ložisek byla zřejmá interindividuální variabilita. Hodnota Vi byla ovlivněna hodnotou tělesného povrhu (BSA = body surface area) a terapií CHOP. Tato variabilita hodnoty V1 (27,1 % a 19,0 %) ovlivněná BSA (1,53 do 2,32 m2) a současnou terapií CHOP byla relativně malá. Věk, pohlaví a stav tělesné aktivity dle WHO nijak neovlivnily farmakokinetiku přípravku MabThera. Tato analýza naznačuje, že úprava dávky přípravku MabThera by u žádné z testovaných proměnných pravděpodobně nevedla k zásadnímu omezení jeho farmakokinetické variability.
Přípravek MabThera podávaný v dávce 375 mg/m2 formou nitrožilní infuze ve 4 dávkách s týdenním intervalem 203 pacientům s NHL dosud neléčeným přípravkem MabThera měl za výsledek střední hodnotu Cmax po čtvrté infuzi 486 pg/ml (rozmezí od 77,5 do 996,6 pg/ml). Rituximab byl zjistitelný v séru pacientů 3-6 měsíců po ukončení léčby.
Po podání přípravku MabThera v dávce 375 mg/m2 ve formě intravenózní infuze v 8 infuzích v týdenních odstupech 37 pacientům s NHL se zvyšovala střední hodnota Cmax s každou následnou infuzí, v rozpětí od 243 pg/ml (rozmezí 16 - 582 pg/ml) po první infuzi, až do 550 pg/ml (rozmezí 171 - 1177 pg/ml) po osmé infuzi.
Farmakokinetický profil přípravku MabThera podávaného v 6 infuzích v dávce 375 mg/m2 v kombinaci s 6 cykly chemoterapie CHOP byl podobný profilu přípravku MabThera podávaného samostatně.
Chronická lymfocytární leukemie
Přípravek MabThera byl u pacientů s CLL podáván pomocí intravenózní infuze v prvním cyklu v dávce 375 mg/m2 s následným zvýšením dávky na 500 mg/m2 v každém z 5 dalších cyklů v kombinaci s fludarabinem a cyklofosfamidem. Průměrná Cmax (N=15) byla 408 pg/ml (rozmezí 97 -764 pg/ml) po páté infuzi 500 mg/m2 a průměrný terminální poločas byl 32 dní (rozmezí 14 - 62 dní).
Revmatoidní artritida
Po podání dvou intravenózních infuzí 1000 mg přípravku MabThera v odstupu dvou týdnů byl průměr terminálního poločasu 20,8 dne (rozmezí 8,58 až 35,9 dne), průměrná systémová clearance 0,23 l/den (rozmezí 0,091 až 0,67 l/den), průměrný distribuční objem v rovnovážném stavu 4,6 l (rozmezí 1,7 až
7,5 l). Populační farmakokinetickou analýzou při použití stejných dat byly získány obdobné průměrné hodnoty systémové clearance (0,26 l) a poločasu (20,4 dne). Z populačních farmakokinetických analýz vyplynulo, že BSA (velikost povrchu těla) a pohlaví byly nejdůležitějšími proměnnými pro vysvětlení variability farmakokinetických parametrů (PK) mezi pacienty. Po úpravě hodnot vzhledem k BSA vykazovali muži větší objem distribuce a rychlejší clearance než ženy. Farmakokinetické rozdíly spojené s pohlavím nebyly považovány za klinicky relevantní a nevyžadovaly úpravu dávky. U pacientů s jaterním poškozením nebo renální nedostatečností nejsou k dispozici žádné farmakokinetické údaje.
Farmakokinetika rituximabu byla hodnocena po podání dvou dávek 500 mg a 1000 mg intravenózně v den 1 a 15 ve čtyřech studiích. Ve všech těchto studiích byla farmakokinetika rituximabu přímo úměrná dávce v celém hodnoceném rozmezí dávek. Průměrná Cmax sérového rituximabu se po podání první infuze pohybovala v rozmezí 157 až 171 pg/ml při dávce 2 x 500 mg a v rozmezí od 298 do 341 pg/ml při dávce 2 x 1000 mg. Po druhé infuzi se průměrná Cmax pohybovala v rozmezí od 183 do 198 pg/ml při dávce 2 x 500 mg a v rozmezí od 355 do 404 pg/ml při dávce 2 x 1000 mg. Průměrný terminální poločas eliminace se pohyboval v rozmezí od 15. do 16. dne při dávce 2 x 500 mg a 17 až 21 dnů při dávce 2 x 1000 mg. Průměrná Cmax byla o 16 až 19 % vyšší po podání druhé infuze v porovnání s první infuzí u obou dávek.
Farmakokinetika rituximabu byly hodnocena po podání dvou dávek 500 mg a 1000 mg i.v. při opakovaném zahájení léčby ve druhém léčebném cyklu. Průměrná Cmax sérového rituximabu po první infuzi byla 170 až 175 pg/ml při dávce 2 x 500 mg a 317 až 370 pg/ml při dávce 2 x 1000 mg. Cmax po podání druhé infuze byla 207 pg/ml při dávce 2 x 500 mg a v rozmezí od 377 do 386 pg/ml při dávce 2 x 1000 mg. Průměrný terminální eliminační poločas po druhé infuzi po druhém cyklu byl 19 dnů při dávce 2 x 500 mg a v rozmezí od 21 do 22 dnů při dávce 2 x 1000 mg. PK parametry rituximabu byly srovnatelné v obou cyklech léčby.
U populace s nedostatečnou odpovědí na anti-TNF terapii byly farmakokinetické (PK) parametry po podání stejných dávek rituximabu (2 x 1000 mg i.v., v odstupu 2 týdnů) podobné, s průměrnou maximální sérovou koncentrací 369 pg/ml a průměrným poločasem 19,2 dne.
Granulomatóza s polyangiitidou a mikroskopická polyangiitida
Na základě populační farmakokinetické analýzy údajů od 97 pacientů s granulomatózou s polyangiitidou a mikroskopickou polyangiitidou, kteří byli léčeni přípravkem MabThera v dávce 375 mg/m2 jednou týdně, celkem 4 dávky, byl odhadovaný medián terminálního eliminačního poločasu 23 dnů (rozmezí 9-49 dnů). Průměrná clearance a distribuční objem rituximabu byly 0,313 l/den (rozmezí 0,116-0,726 l/den) resp. 4,50 l (rozmezí 2,25-7,39 l). Farmakokinetické parametry rituximabu u těchto pacientů se zdají podobné parametrům pozorovaným u pacientů s revmatoidní artritidou.
5.3 Předklinické údaje vztahující se k bezpečnosti
Rituximab se ukázal jako látka vysoce specifická k CD20 antigenu na B-lymfocytech. Studie prováděné na opicích cynomolgus neprokázaly jiný druh toxicity než očekávanou farmakologickou depleci B-lymfocytů v periferní krvi a v lymfatických tkáních.
Studie vývojové toxicity byly provedeny u opic rodu cynomolgus při podávání dávek do 100 mg/kg (20.-50. den březosti) a neprokázaly žádnou embryotoxicitu pro plod, která by byla spojena s rituximabem. V závislosti na dávce přípravku však byla pozorována farmakologická deplece B lymfocytů v lymfatických orgánech plodu, která přetrvávala postnatálně a byla doprovázena snížením hladiny IgG u novorozených opic. Počet B lymfocytů se u těchto zvířat vrátil k normální hodnotě během 6 měsíců po narození a nedošlo ke snížené reakci na imunizaci.
Standardní testy pro vyšetření mutagenity nebyly prováděny, neboť tyto testy nejsou pro tento typ molekuly relevantní. Dlouhodobé studie na zvířatech, které by měly určovat karcinogenní potenciál rituximabu, nebyly provedeny. Nebyly provedeny konkrétní studie stanovující účinky rituximabu na fertilitu. V obecných studiích toxicity na opicích cynomolgus nebyly pozorovány žádné škodlivé účinky na reprodukční orgány samců či samic.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Natrium-citrát Polysorbát 80 Chlorid sodný Hydroxid sodný Kyselina chlorovodíková Voda na injekci
6.2 Inkompatibility
Mezi přípravkem MabThera a polyvinylchloridem nebo polyethylenem vaků nebo infuzních setů nebyla pozorována inkompatibilita.
6.3 Doba použitelnosti
Neotevřená injekční lahvička 30 měsíců
Naředěný přípravek
Připravený infuzní roztok přípravku MabThera je fyzikálně a chemicky stabilní po dobu 24 hodin při teplotě 2 °C - 8 °C a následně pak 12 hodin při pokojové teplotě.
Z mikrobiologického hlediska by měl být připravený roztok použit okamžitě. Není-li použit okamžitě, jsou doba a podmínky uchovávání přípravku před použitím na zodpovědnosti uživatele a za normálních okolností by doba neměla překročit 24 hodin při 2 °C - 8 °C, pokud nebyl roztok naředěn za kontrolovaných a validovaných aseptických podmínek.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C). Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Podmínky uchovávání tohoto léčivého přípravku po jeho naředění jsou uvedeny v bodě 6.3.
6.5 Druh obalu a obsah balení
Injekční lahvička z čirého skla typu I, s pryžovou zátkou, obsahující 500 mg rituximabu v 50 ml.
Jedno balení obsahuje 1 injekční lahvičku.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Přípravek MabThera je připravený ve sterilní, nepyrogenní lahvičce pro jedno použití bez přísady konzervačních látek.
Asepticky se natáhne do stříkačky potřebné množství a rozředí se ve sterilním, apyrogenním roztoku chloridu sodného 9 mg/ml (0,9 %) nebo ve vodném roztoku 5 % D-glukózy. Aby se výsledný roztok dobře promíchal, je nutné jemně obrátit vak vzhůru nohama, aby se nevytvořila pěna. Zvláštní péče musí být věnována aseptickým podmínkám při přípravě roztoku, neboť léčebný přípravek neobsahuje žádné antimikrobiální nebo bakteriostatické konzervační látky. Léčebný přípravek k parenterálnímu použití by měl být ještě před aplikací vizuálně zkontrolován z hlediska obsahu pevných částic a změny barvy.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/98/067/002
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 2. června 1998
Datum posledního prodloužení registrace: 2. června 2008
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
MabThera 1400 mg subkutánní injekční roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden ml obsahuje 120 mg rituximabum.
Jedna injekční lahvička obsahuje 1400 mg/11,7 ml rituximabum.
Rituximab je genetickým inženýrstvím získaná chimérická myší/lidská monoklonální protilátka. Jde o glykosylovaný imunoglobulin s lidskou IgG1 konstantní částí, zatímco variabilní části lehkých a těžkých řetězců jsou myšího původu. Protilátka je produkována suspenzí uměle kultivovaných savčích buněk (ovariální buňky čínských křečků) a je purifikována afinitní chromatografií a iontoměničem. Případně přítomné viry jsou v průběhu výroby odstraněny a inaktivovány.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční roztok.
Čirý až opalescentní, bezbarvý až nažloutlý roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek MabThera se používá u dospělých pacientů k léčbě nehodgkinských lymfomů (NHL):
Přípravek MabThera je indikován k léčbě dosud neléčených nemocných s folikulárním lymfomem III. a IV. klinického stádia v kombinaci s chemoterapií.
Udržovací léčba přípravkem MabThera je indikována k léčbě pacientů s folikulárním lymfomem, kteří odpovídají na indukční léčbu.
Přípravek MabThera je v kombinaci s chemoterapií CHOP (cyklofosfamid, doxorubicin, vinkristin, prednizolon) indikován k léčbě nemocných s CD20 pozitivním difúzním velkobuněčným nehodgkinským maligním lymfomem z B buněk.
4.2 Dávkování a způsob podání
Přípravek MabThera má být podáván pod pečlivým dohledem zkušeného zdravotnického pracovníka a v prostředí, kde je okamžitě dostupné úplné vybavení pro resuscitaci (viz bod 4.4).
Před každým podáním přípravku MabThera je vždy třeba podat premedikaci, kterou tvoří antipyretikum a antihistaminikum, např. paracetamol a difenhydramin.
Pokud není přípravek MabThera při léčbě nehodgkinských lymfomů podáván v kombinaci s chemoterapeutickým režimem obsahujícím glukokortikoidy, má být zvážena premedikace glukokortikoidy.
Dávkování
Doporučenou dávkou přípravku MabThera pro subkutánní podání používaná u dospělých pacientů je subkutánní injekce v pevně stanovené dávce 1400 mg bez ohledu na velikost tělesného povrchu pacienta.
Před zahájením léčby přípravkem MabThera subkutánní injekce, musí být předem vždy všem pacientům podána plná dávka přípravku MabThera intravenózní infuzí, s použitím přípravku MabThera pro intravenózní podání (viz bod 4.4).
Pokud pacienti nebyli schopni přijmout jednu plnou dávku intravenózní infuze přípravku MabThera před přechodem na jiný typ podání, má se u nich v následných cyklech nadále podávat přípravek MabThera pro intravenózní podání, dokud není plná intravenózní dávka úspěšně podána.
Z tohoto důvodu je přechod na přípravek MabThera pro subkutánní podání možný až v druhém nebo následných cyklech léčby.
Je důležité zkontrolovat označení přípravku a ujistit se, že je podávána správná forma přípravku (pro intravenózní nebo subkutánní podání) a síla, která byla pacientovi předepsána.
Přípravek MabThera pro subkutánní podání není určený k intravenóznímu podání a má být podán pouze subkutánní injekcí. Síla 1400 mg je určena pouze pro subkutánní podání u nehodgkinského lymfomu (NHL).
Folikulární nehodgkinský lymfom
Kombinovaná léčba
Doporučená dávka přípravku MabThera v kombinaci s chemoterapií v rámci indukční léčby pacientů s dosud neléčeným nebo relabujícím/refrakterním folikulárním lymfomem je: první cyklus s přípravkem MabThera pro intravenózní podání 375 mg/m2 tělesného povrchu, dále s následujícími cykly s přípravkem MabThera pro subkutánní podání injektovaný v pevně stanovené dávce 1400 mg, až do celkového počtu 8 cyklů.
Přípravek MabThera má být podáván v den 1 každého cyklu chemoterapie, po podání glukokortikoidu, pokud je součástí chemoterapeutického režimu.
Udržovací léčba
• Dosud neléčený folikulární lymfom
Doporučená dávka přípravku MabThera pro subkutánní podání v udržovací léčbě pacientů s dosud neléčeným folikulárním lymfomem, kteří odpověděli na indukční léčbu, je: 1400 mg jednou za 2 měsíce (zahájení udržovací léčby 2 měsíce po poslední dávce indukční léčby) do progrese nemoci či nejdéle po dobu dvou let.
• Relabující/refrakterní folikulární lymfom
Doporučená dávka přípravku MabThera pro subkutánní podání v udržovací léčbě pacientů s relabujícím/refrakterním folikulárním lymfomem, kteří odpověděli na indukční léčbu, je: 1400 mg jednou za 3 měsíce (zahájení udržovací léčby 3 měsíce po poslední dávce indukční léčby) do progrese nemoci či nejdéle po dobu dvou let.
Difúzní velkobuněčný nehodgkinský lymfom z B buněk
Přípravek MabThera má být použit v kombinaci s chemoterapií CHOP. Doporučená dávka přípravku je: první cyklus, přípravek MabThera pro intravenózní podání: 375 mg/m2 tělesného povrchu, dále následující cykly s přípravkem MabThera pro subkutánní podání injektovaný v pevně stanovené dávce 1400 mg. Celkem: 8 cyklů.
Přípravek MabThera se podává 1. den každého z chemoterapeutických cyklů po intravenózní infuzi glukokortikoidu, který je součástí režimu CHOP.
Bezpečnost a účinnost přípravku MabThera v kombinaci s jinými chemoterapeutickými režimy v léčbě difúzního B-velkobuněčného lymfomu nebyly dosud stanoveny.
Úprava dávky v průběhu léčby
Redukce dávkování přípravku MabThera není doporučena. Při kombinaci přípravku MabThera s chemoterapií mohou být chemoterapeutika redukována podle standardních pravidel (viz bod 4.8).
Zvláštní populace
Pediatrická populace
Bezpečnost a účinnost přípravku MabThera u dětí do 18 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
Starší pacienti
U starších pacientů (ve věku > 65 let) není zapotřebí žádná úprava dávkování.
Způsob podání
Subkutánní injekce:
Přípravek MabThera 1400 mg pro subkutánní podání má být podáván pouze subkutánní injekcí po dobu přibližně 5 minut. Jehla podkožní injekce musí být ihned před podáním pouze připojena k injekční stříkačce, aby se zabránilo případnému ucpání jehly.
Přípravek MabThera pro subkutánní podání má být injektován subkutánně do břišní stěny a nikdy nemá být podán do oblastí, kde je kůže zarudlá, kde je modřina, kde je kůže citlivá, ztvrdlá nebo do jiných částí těla, kde jsou mateřská znaménka nebo jizvy.
Nejsou dostupné žádné údaje o podávání injekce do jiných částí těla, proto injekce mají být výhradně podávány do břišní stěny.
Pokud jsou během léčebné kúry přípravkem MabThera pro subkutánní podání podávány jiné léčivé přípravky pro subkutánní podání, injekce mají být podány pokud možno do jiné oblasti.
Je-li podání injekce přerušeno, může být injekce znovu podána do stejného místa nebo do jiné oblasti, pokud je to vhodné.
Intravenóznípodání infuze:
Informace týkající se dávkování a způsobu podání jsou uvedeny v souhrnu údajů o přípravku (SPC) MabThera 100 mg a 500 mg koncentrátu pro infuzní roztok.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1 nebo na myší bílkoviny či hyaluronidázu.
Aktivní, závažné infekce (viz bod 4.4).
Pacienti se závažným útlumem imunitního systému.
4.4 Zvláštní upozornění a opatření pro použití
Z důvodu snadnější zpětné zjistitelnosti biologických léčivých přípravků má být obchodní název a číslo šarže podávaného přípravku zřetelně zaznamenáno (nebo vyznačeno) v pacientově dokumentaci.
Informace uvedené v bodě 4.4 se vztahují k použití přípravku MabThera pro subkutánní podání ve schválených indikacích Léčba nehodgkinských lymfomů (síla 1400 mg) a Léčba chronické lymfocytární leukemie (síla 1600 mg). Pro informace týkající se dalších indikací, prosím, použijte SPC MabThera pro intravenózní podání.
Užití přípravku MabThera pro subkutánní podání v monoterapii u pacientů s folikulárním lymfomem III. a IV. klinického stádia, kteří jsou chemorezistentní nebo se nacházejí ve druhém či dalším relapsu po chemoterapii, není doporučeno, neboť bezpečnost subkutánního podání jednou týdně nebyla stanovena.
Progresivní multifokální leukoencefalopatie
Použití přípravku MabThera může souviset se zvýšeným rizikem progresivní multifokální leukoencefalopatie (PML). Pacienti musí být v pravidelných intervalech sledováni pro jakékoli nové nebo zhoršující se neurologické symptomy nebo příznaky, které by mohly naznačovat PML. V případě podezření na PML musí být další podávání přípravku pozastaveno, dokud není diagnóza PML vyloučena. Lékař by měl vyhodnotit stav pacienta, aby bylo možno určit, zda příznaky ukazují na neurologickou dysfunkci, a v kladném případě, zda příznaky ukazují na PML. Dle klinické indikace by měla být zvážena konzultace s neurologem.
Při jakýchkoli pochybnostech by měla být zvážena další vyšetření včetně magnetické rezonance, přednostně s kontrastem, vyšetření mozkomíšního moku na JC virovou DNA a opakované neurologické vyšetření.
Lékař by měl věnovat zvláštní pozornost symptomům, které naznačují PML, ale kterých si pacient nemusí všimnout (např. kognitivní, neurologické nebo psychiatrické symptomy). Nemocnému by mělo být doporučeno, aby o léčbě informoval svého partnera nebo osobu, která o něho pečuje, protože ti si mohou všimnout příznaků, které sám nemocný nezaznamená.
Pokud dojde ke vzniku PML, podávání přípravku MabThera musí být trvale ukončeno.
Po rekonstituci imunitního sytému u imunosuprimovaných nemocných s PML bylo možno pozorovat stabilizaci nebo zlepšení. Nadále není známo, zda časná detekce PML a ukončení léčby přípravkem MabThera může vést k podobné stabilizaci či zlepšení.
Infuze/reakce související s infuzí
Podání přípravku MabThera je spojeno s reakcemi souvisejícími s infuzí, které mohou souviset s uvolněním cytokinů a/nebo dalších chemických mediátorů. Syndrom z uvolnění cytokinů může být klinicky nerozeznatelný od akutních hypersenzitivních reakcí.
Tento soubor reakcí, které zahrnují syndrom z uvolnění cytokinů, syndrom nádorového rozpadu a anafylaktické či hypersenzitivní reakce, je popsán níže. Reakce nejsou specificky spojené s cestou podání přípravku MabThera a lze je pozorovat u obou forem.
Po uvedení přípravku na trh byly hlášeny závažné reakce související s infuzí, které končily úmrtím, při použití přípravku MabThera pro intravenózní podání s nástupem během 30 minut až 2 hodin po zahájení první intravenózní infuze přípravkem MabThera. Ty byly charakterizovány plicními příhodami a v některých případech zahrnovaly rychlý rozpad nádoru s rysy syndromu nádorového rozpadu, navíc horečku, zimnici, třesavku, hypotenzi, kopřivku, angioedém a další symptomy (viz bod 4.8).
Těžký syndrom z uvolnění cytokinů je charakterizován těžkou dušností, často doprovázenou bronchospazmem a hypoxií, dále horečkou, zimnicí, třesavkou, urtikou a angioedémem. Tento syndrom může být spojen s některými příznaky syndromu z rozpadu tumoru, jako jsou hyperurikémie, hyperkalémie, hypokalcémie, hyperfosfatémie, akutní renální selhání, zvýšení laktát dehydrogenázy (LDH), a může být spojen s akutním respiračním selháním a úmrtím pacienta. Akutní respirační selhání může být provázeno plicní intersticiální infiltrací nebo edémem plic, viditelným na rentgenovém vyšetření. Tento syndrom se často objevuje v průběhu jedné až dvou hodin po zahájení první infuze. U pacientů s anamnézou plicní insuficience nebo u pacientů s nádorovou infiltrací plic je větší nebezpečí nepříznivého průběhu, a proto by tito pacienti měli být léčeni se zvýšenou opatrností.
U pacientů, u kterých dojde k rozvoji těžkého syndromu z uvolnění cytokinů, musí být infuze okamžitě zastavena (viz bod 4.2) a musí u nich být zahájena intenzivní symptomatická léčba. Vzhledem k tomu, že počáteční zlepšení klinických příznaků může být následováno opětovným zhoršením celkového stavu, měli by být pacienti pečlivě monitorováni až do doby, kdy projevy syndromu z rozpadu tumoru a plicní infiltrace vymizí nebo tento syndrom je vyloučen. Další pokračování léčby po úplném vymizení příznaků vedlo vzácně k opakování těžkého syndromu z uvolnění cytokinů.
Pacienti s velkou nádorovou zátěží nebo s vysokým počtem (> 25 x 109/l) cirkulujících maligních buněk, u kterých může být zvýšené riziko zejména těžkého syndromu z uvolnění cytokinů, mají být léčeni s nejvyšší opatrností. Tito pacienti mají být velmi pečlivě monitorováni v průběhu první infuze. U těchto pacientů je třeba zvážit snížení rychlosti při podávání první infuze nebo rozdělení dávky v prvním a jakémkoli následujícím cyklu léčby do dvou dnů, pokud je počet lymfocytů stále >25 x 109/l.
Po intravenózním podání bílkovin pacientům byly hlášeny anafylaktické nebo jiné hypersenzitivní reakce. Na rozdíl od syndromu z uvolnění cytokinů se skutečná hypersenzitivní reakce objevuje typicky během několika minut po zahájení infuze. Pro případ rozvoje alergické reakce v průběhu podávání přípravku MabThera, musí být léčiva užívaná k léčbě hypersenzitivní reakce, např. epinefrin (adrenalin), antihistaminika a glukokortikoidy, ihned k dispozici. Klinické příznaky anafylaktické reakce mohou být podobné klinickým příznakům syndromu z uvolnění cytokinů (viz výše). Reakce z přecitlivělosti byly hlášeny méně často než reakce vznikající v souvislosti s uvolněním cytokinů.
Dalšími reakcemi hlášenými v některých případech byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie.
Vzhledem k tomu, že se v průběhu podání přípravku MabThera může objevit hypotenze, má být zváženo přechodné vysazení antihypertenziv 12 hodin před podáním přípravku MabThera.
Nežádoucí reakce všech typů vznikající v souvislosti s podáním infuze byly pozorovány u 77 % pacientů léčených přípravkem MabThera pro intravenózní podání (včetně syndromu z uvolnění cytokinů doprovázeného hypotenzí a bronchospazmem u 10 % pacientů), viz bod 4.8. Tyto symptomy jsou obvykle reverzibilní po přerušení infuze přípravku a po podání antipyretik, antihistaminik, a podle potřeby po podání kyslíku, infuze fyziologického roztoku nebo bronchodilatancií a glukokortikoidů. Těžké reakce při syndromu z uvolnění cytokinů - viz výše.
Reakce související s podáním byly v klinických studiích pozorovány až u 50 % pacientů léčených přípravkem MabThera pro subkutánní podání. Reakce, které se objevovaly v průběhu 24 hodin po subkutánní injekci, zahrnovaly především erytém pruritus, vyrážku a reakce v místě vpichu injekce, jako např. bolest, otok a zarudnutí a obecně byly mírné až středně závažné (stupeň 1 nebo 2) a byly přechodného charakteru (viz bod 4.8).
V klinických studiích byly lokální kožní reakce velmi časté u pacientů, kterým byl podáván subkutánní přípravek MabThera. Příznaky zahrnovaly bolest, otok, induraci, krvácení, erytém, pruritus a vyrážku (viz bod 4.8). Některé lokální kožní reakce se objevily po více než 24 hodinách po subkutánním podání přípravku MabThera. Většina lokálních kožních reakcí pozorovaných následně po podání přípravku MabThera pro subkutánní podání byly mírné až středně závažné a vymizely bez jakékoli specifické léčby.
Před zahájením léčby přípravkem MabThera subkutánní injekce, musí být předem vždy všem pacientům podána plná dávka přípravku MabThera intravenózní infuzí, s použitím přípravku MabThera pro intravenózní podání. Nejvyšší riziko výskytu reakcí spojených s podáním bylo obecně pozorováno v cyklu 1. Tím, že léčba je zahájena přípravkem MabThera pro intravenózní podání, lze lépe koordinovat reakce na podání pomalou intravenózní infuzí nebo přerušením intravenózní infuze.
Pokud pacienti nebyli schopni přijmout jednu plnou dávku intravenózní infuze přípravku MabThera před přechodem na jiný typ podání, má se u nich v následných cyklech nadále podávat přípravek MabThera pro intravenózní podání, dokud není plná intravenózní dávka úspěšně podána.
Z tohoto důvodu je přechod na přípravek MabThera pro subkutánní podání možný až v druhém nebo následných cyklech léčby.
Stejně jako u intravenózní lékové formy, přípravek MabThera pro subkutánní podání má být podáván v prostředí, kde je okamžitě dostupné úplné vybavení pro resuscitaci a má být podáván pod pečlivým dohledem zkušeného zdravotnického pracovníka. Před každým podáním přípravku MabThera pro subkutánní podání se má vždy podat premedikace tvořená analgetikem/antipyretikem a antihistaminikem. Současně má být zvážena premedikace glukokortikoidy.
Pacienti mají být pozorování alespoň 15 minut po subkutánním podání přípravku MabThera. Delší interval může být vhodný u pacientů se zvýšeným rizikem hypersenzitivních reakcí.
Pacienti mají být poučeni, aby ihned kontaktovali svého lékaře, pokud se u nich vyskytnou příznaky připomínající závažnou hypersenzitivitu nebo syndrom z uvolnění cytokinů kdykoli po podání léčivého přípravku.
Srdeční poruchy
U pacientů léčených přípravkem MabThera se objevily angina pectoris, srdeční arytmie typu fibrilace či flutter síní, srdeční selhání a/nebo infarkt myokardu. Pacienti s anamnézou srdečního onemocnění a/nebo kardiotoxickou chemoterapií mají proto být pečlivě monitorováni.
Hematologická toxicita
Přestože MabThera v monoterapii nepůsobí myelosupresivně, je u nemocných s počtem neutrofilů < 1,5 x 109/l a/nebo trombocytů < 75 x 109/l potřeba opatrnosti, vzhledem k tomu, že u této skupiny nemocných jsou jen malé zkušenosti s podáním přípravku MabThera. Přípravek MabThera byl podán 21 nemocným, kteří podstoupili autologní transplantaci kostní dřeně nebo jinak rizikovým nemocným s předpokládanou redukovanou funkcí kostní dřeně, aniž by byla vyvolána myelotoxicita.
Během léčby přípravkem MabThera je třeba pravidelně kontrolovat kompletní krevní obraz, včetně počtu neutrofilů a trombocytů.
Infekce
Během léčby přípravkem MabThera se mohou objevit závažná infekční onemocnění, včetně onemocnění vedoucích k úmrtí (viz bod 4.8). Přípravek MabThera nemá být podáván pacientům s aktivním, závažným infekčním onemocněním (např. tuberkulózou, sepsí a oportunními infekcemi, viz bod 4.3).
Lékaři mají pečlivě zvážit použití přípravku MabThera u pacientů s anamnézou opakovaných či chronických infekčních onemocnění či u pacientů s průvodními chorobami, které by mohly u pacientů dále přispět k náchylnosti k závažným infekčním chorobám (viz bod 4.8).
U pacientů léčených přípravkem MabThera pro intravenózní podání byly popsány případy reaktivace hepatitidy B, včetně hlášení fulminantní hepatitidy s následným úmrtím. Většina těchto pacientů byla rovněž léčena cytotoxickou chemoterapií. U všech pacientů má být před zahájením léčby přípravkem MabThera proveden screening na virus hepatitidy B (HBV). Screening má minimálně zahrnovat vyšetření HBsAg-statusu a HBcAb-statusu. Tato vyšetření mohou být doplněna dalšími vhodnými vyšetřeními v souladu s lokálními postupy. Pacienti s aktivním onemocněním hepatitidy B nesmí být léčeni přípravkem MabThera. Pacienti se sérologicky pozitivní hepatitidou B (buď HBsAg nebo HBcAb) mají být před zahájením léčby odesláni na odborné vyšetření ke specialistovi na jaterní onemocnění, v průběhu léčby mají být tito pacienti pečlivě sledováni a léčeni v souladu s lokálními medicínskými postupy k prevenci reaktivace hepatitidy B.
U pacientů s NHL byly po uvedení přípravku MabThera pro intravenózní podání na trh velmi vzácně hlášeny případy progresivní multifokální leukoencefalopatie (PML) (viz bod 4.8). Většina z pacientů dostávala rituximab v kombinaci s chemoterapií nebo jako součást transplantace krvetvorných kmenových buněk.
Očkování
Bezpečnost očkování živými virovými vakcínami po léčbě přípravkem MabThera nebyla u pacientů s NHL studována a očkování živými virovými vakcínami není doporučeno. Pacienti léčení přípravkem MabThera mohou podstoupit očkování neživými vakcínami. Účinnost očkování neživými vakcínami však může být nižší. V nerandomizované studii měli pacienti s relapsem nízce maligního NHL léčení monoterapií přípravkem MabThera pro intravenózní podání ve srovnání se zdravými kontrolami nižší odpověď na přeočkování tetanem (16 % vs. 81 %) a očkování látkou Keyhole Limpet Haemocyanin (KLH) (4 % vs. 69 % při zjišťování dvojnásobného vzestupu titru protilátek).
Průměrné hodnoty titrů protilátek proti panelu antigenů (Streptococcus pneumoniae, chřipka A, příušnice, zarděnky, plané neštovice) byly udrženy nejméně 6 měsíců po léčbě přípravkem MabThera.
Kožní reakce
Byly popsány závažné kožní reakce, jako je například toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím (viz bod 4.8). V případě výskytu takovéto příhody, s podezřením na souvislost s podáním přípravku MabThera, má být léčba trvale ukončena.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
V současné době jsou k dispozici pouze omezené údaje o možných lékových interakcích s přípravkem MabThera.
Při současném podávání přípravku MabThera s fludarabinem nebo cyklofosfamidem, nebyl pozorován žádný účinek na jejich farmakokinetiku. Kromě toho nebyl pozorován žádný zjevný účinek fludarabinu a cyklofosfamidu na farmakokinetiku přípravku MabThera.
Nemocní s protilátkami proti myším bílkovinám (HAMA) nebo s protilátkami proti chimérickým protilátkám (HACA) mohou mít hypersenzitivní nebo alergické reakce při podání jiných diagnostických nebo léčebných monoklonálních protilátek.
4.6 Fertilita, těhotenství a kojení
Antikoncepce u mužů a žen
Vzhledem k tomu, že rituximab zůstává v těle pacientů s deplecí B buněk po delší dobu, musí ženy ve fertilním věku během léčby přípravkem MabThera a 12 měsíců po jejím ukončení používat efektivní antikoncepční metody.
Je známo, že imunoglobuliny IgG přecházejí přes placentární bariéru.
Počet B lymfocytů u lidských novorozenců po podání přípravku MabThera matce nebyl v klinických hodnoceních studován. Neexistují žádné dostatečné a dobře kontrolované údaje ze studií u těhotných žen, avšak u některých dětí narozených matkám vystaveným v průběhu těhotenství přípravku MabThera byla hlášena přechodná deplece B buněk a lymfocytopenie. Podobné účinky byly pozorovány ve studiích na zvířatech (viz bod 5.3). Z těchto důvodů by neměla být MabThera podávána těhotným ženám s výjimkou situace, kdy možný prospěch převáží potencionální riziko.
Kojení
Není známo, zda je rituximab vylučován do lidského mléka. Vzhledem k tomu, že mateřské IgG vylučováno je, a u kojících opic byl rituximab v mléku detekován, neměly by ženy léčené přípravkem MabThera kojit během léčby a 12 měsíců po léčbě přípravkem MabThera.
Fertilita
Studie na zvířatech neprokázaly škodlivé účinky rituximabu nebo rekombinantní lidské hyaluronidázy (rHuPH20) na reprodukční orgány.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly prováděny žádné studie hodnotící účinky přípravku MabThera na schopnost řídit a obsluhovat stroje, nicméně farmakologická aktivita a dosud hlášené nežádoucí účinky naznačují, že přípravek MabThera nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Informace uvedené v tomto bodě se vztahují k použití přípravku MabThera v onkologii.
Pro informace týkající se autoimunitních indikací, prosím, použijte SPC přípravku MabThera pro intravenózní podání.
Shrnutí bezpečnostního profilu
V průběhu klinického programu vývoje byl bezpečnostní profil přípravku MabThera pro subkutánní podání srovnatelný s intravenózní lékovou formou, s výjimkou lokálních kožních reakcí. Lokální kožní reakce, včetně reakcí v místě vpichu injekce, byly u pacientů léčených přípravkem MabThera pro subkutánní podání velmi časté. Ve studii fáze III SABRINA (BO22334) byly lokální kožní reakce hlášeny až u 20 % pacientů, kterým byl podáván přípravek MabThera pro subkutánní podání. Nejčastější lokální kožní reakcí v rameni s přípravkem MabThera pro subkutánní podání byl erytém v místě vpichu injekce (13 %), bolest v místě vpichu injekce (7 %) a edém v místě vpichu injekce (4 %). S výjimkou jednoho pacienta, u kterého se vyskytla lokální kožní reakce stupně 3 (vyrážka v místě vpichu injekce) po prvním podání přípravku MabThera pro subkutánní podání (cyklus 2), byly reakce po subkutánním podání mírné či středně závažné. Lokální kožní reakce jakéhokoli stupně v rameni s přípravkem MabThera pro subkutánní podání byly nejčastější během prvního cyklu subkutánního podání (cyklus 2), následovaném druhým cyklem, a výskyt těchto reakcí se snižoval po podání následujících injekcí.
Nežádoucí účinky hlášené při použití přípravku MabThera pro subkutánní podání
Riziko akutních reakcí souvisejících s podáním subkutánní formy přípravku MabThera bylo hodnoceno ve 2 otevřených studiích, do kterých byli zařazeni pacienti s folikulárním lymfomem léčení indukční i udržovací léčbou (SABRINA/BO22334) a pouze udržovací léčbou (SparkThera/BP22333). Ve studii SABRINA byly závažné reakce (stupně >3) související s podáním subkutánní formy přípravku MabThera hlášeny u 2 pacientů (2 %). Tyto příhody, vyrážka v místě vpichu injekce a sucho v ústech, byly stupně 3.
Ve studii SparkThera nebyly hlášeny žádné závažné reakce související s podáním přípravku.
Nežádoucí účinky hlášené při použití přípravku MabThera pro intravenózní podání
Zkušenosti u nehodgkinských lymfomů a chronické lymfocytární leukemie
Celkový bezpečnostní profil přípravku MabThera je u nehodgkinských lymfomů a chronické lymfocytární leukemie založen na údajích pacientů z klinických studií a postmarketingového pozorování. Tito pacienti byli léčeni buď přípravkem MabThera v monoterapii (jako indukční léčbou nebo udržovací léčbou po indukční léčbě), nebo v kombinaci s chemoterapií.
Nej častěji pozorovanými nežádoucími účinky na lék u pacientů, kteří dostávali přípravek MabThera, byly reakce související s podáním infuze, které se u většiny pacientů objevily v průběhu první infuze. Incidence příznaků souvisejících s podáním infuze se významně snižuje u následujících infuzí a po osmi dávkách přípravku MabThera je nižší než 1 %.
K infekčním příhodám (zejména bakteriálním a virovým) došlo u přibližně 30-55 % pacientů v průběhu klinických studií u pacientů s nehodgkinskými lymfomy a u 30-50 % pacientů v klinických studiích u pacientů s CLL.
Nejčastějšími hlášenými nebo pozorovanými závažnými nežádoucími účinky na lék byly:
• Reakce související s podáním infuze (včetně syndromu z uvolnění cytokinů, syndromu z rozpadu tumoru), viz bod 4.4.
• Infekce, viz bod 4.4.
• Kardiovaskulární poruchy, viz bod 4.4.
Dalšími závažnými hlášenými nežádoucími účinky na lék byly reaktivace hepatitidy B a PML (viz bod 4.4).
Četnosti nežádoucích účinků léčivého přípravku (NÚ), které byly hlášeny v souvislosti s podáním samotného přípravku MabThera nebo v kombinaci s chemoterapií, jsou shrnuty v Tabulce 1. Ve všech skupinách četností jsou NÚ prezentovány v pořadí podle klesající závažnosti. Četnost je definována jako velmi častá (>1/10), častá (>1/100 až <1/10), méně častá (>1/1000 až <1/100), vzácná (>1/10000 až <1/1000), velmi vzácná (<1/10000) a není známo (z dostupných údajů nelze určit).
Nežádoucí účinky na lék, které byly zjištěny pouze v postmarketingových pozorováních a u nichž nelze určit četnost, jsou uvedeny jako „není známo“.
Shrnutí nežádoucích účinků do tabulky
Tabulka 1 Nežádoucí účinky na léky zaznamenané v klinických studiích nebo
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Infekce a infestace |
bakteriální infekce, virové infekce, +bronchitida |
sepse, +pneumonie, +febrilní infekce, +herpes zoster, +infekce dýchacích cest, plísňové infekce, infekce neznámého původu, +akutní bronchitida, +sinusitida, hepatitida B1 |
závažné virové infekce2 | |||
|
Poruchy krve a lymfatického systému |
neutropenie, leukopenie, +febrilní neutropenie, +trombocytopenie |
+pancytopenie, +granulocytopenie |
poruchy srážlivosti, aplastická anémie, hemolytická anémie, lymfadenopatie |
přechodný vzestup hladin sérových IgM3 |
pozdní neutropenie3 | |
|
Poruchy imunitního systému |
reakce spojené s podáním4, angioedém |
hypersensitivita |
anafylaxe |
syndrom rozpadu nádoru, syndrom z uvolnění cytokinů4, sérová nemoc |
akutní reverzibilní trombocyto- penie související s podáním infuze4 | |
|
Poruchy metabolismu a výživy |
hyperglykémie, pokles hmotnosti, periferní edém, otok obličeje, vzestup LDH, hypokalcémie | |||||
|
Psychiatrické poruchy | ||||||
|
Poruchy nervového systému |
parestézie, hypestézie, agitovanost, vasodilatace, závratě, úzkost |
porucha vnímání chuti |
periferní neuropatie, paresa lícního nervu5 |
kraniální neuropatie, jiné smyslové poruchy5 | ||
|
Poruchy oka |
poruchy slzení, konjunktivitida |
závažná porucha zraku5 | ||||
|
Poruchy ucha a labyrintu |
tinnitus, bolest uší |
porucha sluchu5 | ||||
|
Srdeční poruchy |
+infarkt myokardu4 a 6, arytmie, +fibrilace síní, tachykardie, +srdeční porucha |
+levostranné srdeční selhání, +supraventrikulární tachykardie, +komorová tachykardie, +angina pectoris, +ischemie myokardu, bradykardie |
závažné kardiální poruchy4 a 6 |
srdeční selhání4 a 6 | ||
|
Cévní poruchy |
hypertenze, ortostatická |
vaskulitida (zejména kožní), leuko-cytoklastická vaskulitida |
v postmarketingovém pozorování u pacientů s nehodgkinským lymfomem a CLL léčených přípravkem MabThera monoterapií/udržovací léčbou nebo v kombinaci s chemoterapií ___
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Respirační, hrudní a mediastinální poruchy |
Broncho spasmus4, respirační choroby, bolest na hrudi, dušnost, zhoršení kašle, rýma |
astma, obliterující bronchiolitida, plicní poruchy, hypoxie |
intersticiální plicní 7 onemocnění |
respirační selhání4 |
plicní infiltrace | |
|
Gastrointesti-nální poruchy |
zvracení, průjem, bolesti břicha, dysfágie, stomatitida, zácpa, dyspepsie, nechutenství, podráždění hltanu |
zduření břicha |
gastrointesti- nální perforace7 | |||
|
Poruchy kůže a podkožní tkáně |
kopřivka, pocení, noční poty, +kožní onemocnění |
závažné bulózní kožní reakce, Stevens- Johnsonův syndrom, toxická epidermální nekrolýza (Lyellův syndrom)7 | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
hypertonie, myalgie, bolesti kloubů, bolesti zad, bolesti krku, bolest | |||||
|
Poruchy ledvin a močových cest |
renální selhání4 | |||||
|
Celkové poruchy a reakce v místě aplikace |
bolest nádoru, zrudnutí, únava, příznaky nachlazení, +multiorgánové selhání4 |
bolest v místě infuze | ||||
|
Vyšetření |
pokles hladin IgG | |||||
|
Pro každý příznak byla četnost stanovena na základě výskytu reakcí všech stupňů (lehké až závažné) s výjimkou příznaků označených "+", u kterých byla četnost stanovena na základě závažných reakcí (stupeň > 3 dle obecných kritérií toxicity NCI). Jsou uvedeny pouze nejvyšší četnosti ve studiích. 1 zahrnuje reaktivaci a primární infekce; frekvence je založena na R-FC režimu u relabující/refrakterní CLL 2 viz též níže uvedený odstavec infekce 3 viz též níže uvedený odstavec hematologické nežádoucí reakce 4 viz též níže uvedený odstavec účinky spojené s podáním infuze. Vzácně byly hlášeny fatální případy 5 příznaky kraniální neuropatie. Objevily se v různou dobu nejvýše za několik měsíců po ukončení léčby přípravkem MabThera 6 pozorováno zejména u pacientů s předchozím kardiálním onemocněním a/nebo kardiotoxickou chemoterapií a byly většinou spjaty s účinky spojenými s podáním infuze 7 včetně fatálních případů | ||||||
Následující pojmy byly uváděny jako nežádoucí příhody v průběhu klinických studií, jejich četnost však byla ve skupinách pacientů s přípravkem MabThera podobná nebo nižší než v kontrolních skupinách: hematotoxicita, neutropenické infekce, infekce močových cest, poruchy čití, horečka.
U více než 50 % pacientů v klinických studiích týkajících se přípravku MabThera pro intravenózní podání byly hlášeny příznaky, které byly suspektní jako účinky spojené s podáním infuze a byly zejména pozorovány v průběhu první infuze, většinou v první nebo v prvých dvou hodinách. Tyto příznaky byly většinou horečka, zimnice a ztuhlost. Mezi další příznaky patří zrudnutí, angioedém, bronchospasmus, zvracení, nevolnost, kopřivka/vyrážka, únava, bolest hlavy, podráždění hltanu, rýma, svědění, bolest, tachykardie, hypertenze, hypotenze, dušnost, dyspepsie, slabost a známky syndromu rozpadu nádoru. Závažné účinky spojené s podáním infuze (například bronchospasmus, hypotenze) se
vyskytly až u 12 % případů. Další reakce, které byly v několika případech hlášeny, byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie. S nižší nebo neznámou četností byly hlášeny exacerbace již existujících kardiálních onemocnění, jako jsou angina pectoris nebo městnavé srdeční selhání nebo závažné kardiální poruchy (srdeční selhání, infarkt myokardu, fibrilace síní), edém plic, multiorgánové selhání, příznak rozpadu tumoru, příznak uvolnění cytokinů, renální selhání a respirační selhání. Incidence účinků spojených s podáním intravenózní infuze se významně snížila u následujících infuzí a je <1 % pacientů při osmém cyklu léčby obsahující přípravek MabThera.
Popis vybraných nežádoucích účinků
Infekce
I když přípravek MabThera způsobuje depleci B-lymfocytů u 70 % až 80 % pacientů, snížení sérových koncentrací imunoglobulinů se vyskytuje jen u malého počtu pacientů.
V randomizovaných studiích byly v ramenech obsahujících přípravek MabThera s vyšší četností hlášeny lokalizované infekce kandidou a herpes zoster. Závažné infekce byly hlášeny u asi 4 % pacientů léčených přípravkem MabThera v monoterapii. V průběhu udržovací léčby přípravkem MabThera až po dobu dvou let byly pozorovány vyšší četnosti infekcí celkové, včetně infekcí stupně 3 a 4 ve srovnání s obdobím observace. Po dobu dvouletého léčebného období nebyla hlášena žádná kumulativní toxicita z hlediska infekce. Dále byly hlášeny při léčbě přípravkem MabThera jiné závažné virové infekce buď nové, reaktivované nebo exacerbované, z nichž některé byly fatální. Většina pacientů dostávala přípravek MabThera v kombinaci s chemoterapií nebo jako součást transplantace hematopoetických kmenových buněk. Příklady těchto závažných virových infekcí jsou infekce způsobené herpetickými viry (cytomegalovirem, virem varicella zoster a herpes simplex virem), JC virem (PML) a virem hepatitidy C. V klinických studiích byly rovněž zaznamenány případy fatální PML, které se objevily po progresi onemocnění a jeho opakované léčbě. Byly hlášeny případy reaktivace hepatitidy B, z nichž většina byla u pacientů, kteří dostávali přípravek MabThera
v kombinaci s cytotoxickou chemoterapií. Byla pozorována progrese Kaposiho sarkomu u pacientů vystavených přípravku MabThera, kteří již dříve Kaposiho sarkomem trpěli. Tyto případy se vyskytly u neschválených indikací a většina pacientů byla HIV pozitivní.
Hematologické nežádoucí účinky
V klinických studiích s monoterapií přípravkem MabThera podávaným po dobu 4 týdnů se u malého počtu pacientů vyskytly hematologické abnormality a byly většinou mírné a reverzibilní. Závažné (stupně 3/4) neutropenie byly hlášeny u 4,2 %, anémie u 1,1 % a trombocytopenie u 1,7 % pacientů.
V průběhu udržovací léčby přípravkem MabThera po dobu až dvou let byly hlášeny leukopenie (5 % oproti 2 %, stupně 3/4) a neutropenie (10 % oproti.4 %, stupně 3/4) s vyšší incidencí oproti pouhému sledování. Incidence trombocytopenie byla nízká (<1 %, stupně 3/4) a nelišila se mezi jednotlivými léčebnými rameny. V průběhu léčebného cyklu ve studiích s přípravkem MabThera v kombinaci s chemoterapií byly hlášeny leukopenie stupně 3/4 (R-CHOP 88 % oproti CHOP 79 %), neutropenie (R-CVP 24 % oproti CVP 14 %; R-CHOP 97 % oproti CHOP 88 %), s obvykle vyšší četností
v porovnání se samotnou chemoterapií. Vyšší incidence neutropenie u pacientů léčených přípravkem MabThera a chemoterapií však nebyla spojena s vyšší incidencí infekcí a infestací v porovnání s pacienty léčenými samotnou chemoterapií. Nebyly hlášeny žádné rozdíly v incidenci anémie. Některé případy pozdní neutropenie se objevily více než 4 týdny po poslední infuzi přípravku MabThera.
Ve studiích s přípravkem MabThera u pacientů s Waldenstromovou makroglobulinemií byla po zahájení léčby pozorována přechodná zvýšení sérových hladin IgM, což může souviset s hyperviskozitou a souvisejícími příznaky. Přechodný vzestup IgM se obvykle v průběhu 4 měsíců vrátil k alespoň výchozí hodnotě.
Kardiovaskulární nežádoucí účinky
V průběhu klinických studií s monoterapií přípravkem MabThera byly hlášeny kardiovaskulární příhody u 18,8 % pacientů, přičemž nejčastěji hlášenými událostmi byly hypotenze a hypertenze.
V průběhu infuze byly hlášeny případy arytmie stupně 3 nebo 4 (včetně ventrikulární a supraventrikulární tachykardie) a angina pectoris. V průběhu udržovací léčby byla incidence kardiálních onemocnění stupně 3/4 srovnatelná u pacientů léčených přípravkem MabThera a u pacientů pouze sledovaných. Jako závažné nežádoucí události (včetně fibrilace síní, infarktu myokardu, levostranného komorového selhání a myokardiální ischémie) byly hlášeny kardiální události u 3 % pacientů léčených přípravkem MabThera ve srovnání s <1 % u sledování. Ve studiích hodnotících přípravek MabThera v kombinaci s chemoterapií byla incidence kardiálních arytmií stupně 3 a 4, především supraventrikulárních arytmií, jako je tachykardie a síňový flutter/fibrilace vyšší ve skupině R-CHOP (14 pacientů, 6,9 %) ve srovnání se skupinou CHOP (3 pacienti, 1,5 %). Všechny tyto arytmie se buď vyskytly v souvislosti s infuzí přípravku MabThera, nebo souvisely s predisponujícími podmínkami, jako byly horečka, infekce, akutní infarkt myokardu nebo již existujících respiračních a kardiovaskulárních onemocnění. Nebyly pozorovány žádné rozdíly mezi skupinami R-CHOP a CHOP v incidenci jiných kardiálních událostí stupně 3 a 4 včetně srdečního selhání, infarktu myokardu a manifestace onemocnění koronárních tepen.
Respirační systém
Byly hlášeny případy intersticiálního plicního onemocnění, některé končící úmrtím.
Neurologické poruchy
V průběhu léčebného období (indukční fáze léčby zahrnující R-CHOP pro maximálně 8 cyklů), čtyři pacienti (2 %) léčení ve skupině R-CHOP, všichni s kardiovaskulárními rizikovými faktory, prodělali během prvního léčebného cyklu tromboembolickou cerebrovaskulární příhodu. Ve výskytu dalších tromboembolických příhod nebyl mezi skupinami žádný rozdíl. Naopak, tři pacienti (1,5 %) v rameni CHOP měli cerebrovaskulární příhodu, u všech se objevila v období následného pozorování.
Byly hlášeny případy syndromu posteriorní reverzibilní encefalopatie (PRES)/syndromu reverzibilní posteriorní leukoencefalopatie (RPLS). Známky a příznaky zahrnovaly zrakové poruchy, bolest hlavy, křeče a psychické poruchy, s nebo bez průvodní hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovacím vyšetřením mozku. U hlášených případů byly zaznamenány rizikové faktory PRES/RPLS, které zahrnují průvodní onemocnění pacienta, hypertenzi, imunosupresivní léčbu a/nebo chemoterapii.
Gastrointestinální onemocnění
Gastrointestinální perforace, v některých případech vedoucí k úmrtí, byly pozorovány u pacientů, kteří dostávali přípravek MabThera v léčbě nehodgkinského lymfomu (NHL). Ve většině těchto případů byla MabThera podávána s chemoterapií.
Hladiny IgG
V klinických studiích hodnotících udržovací léčbu přípravkem MabThera u relabujícího/refrakterního folikulárního lymfomu byly po indukční léčbě střední hladiny IgG pod dolní hranicí normy (LLN)
(< 7 g/l) v rameni s pouhým sledováním i v rameni s přípravkem MabThera. V rameni se sledováním došlo následně k vzestupu střední hladiny IgG nad LLN, ale v rameni s přípravkem MabThera zůstaly nezměněny. Podíl pacientů se střední hladinou IgG pod LNN byl v rameni s přípravkem MabThera přibližně 60 % po celou dobu 2letého léčebného období, zatímco v rameni se sledováním tento podíl poklesl (36 % po 2 letech).
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Vybrané skupiny pacientů - Monoterapie přípravkem MabThera Starší pacienti (> 65 let):
Incidence nežádoucích účinků na lék všech stupňů a stupně 3/4 byla obdobná u starších pacientů v porovnání s mladšími pacienty (<65 let).
Pacienti s objemným (bulky) onemocněním:
U pacientů s objemným onemocněním byla zjištěna vyšší incidence nežádoucích účinků na lék stupně 3/4 ve srovnání s pacienty bez rozsáhlého nádorového postižení (25,6 % versus 15,4 %). Incidence jakéhokoli stupně nežádoucích účinků na lék byla mezi oběma skupinami obdobná.
Opakovaná léčba:
Procento pacientů hlásících nežádoucí účinek na lék po opětovném zahájení léčby dalšími cykly přípravku MabThera bylo podobné jako procento pacientů uvádějící nežádoucí účinek na lék po prvním podání přípravku (jakýkoliv stupeň a stupeň 3/4 nežádoucích účinků na lék).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Z klinických studií u lidí jsou dostupné omezené zkušenosti s podáním dávek vyšších než je schválená dávka intravenózního přípravku MabThera. Dosud nejvyšší intravenózní dávka přípravku MabThera testovaná u lidí je 5000 mg (2250 mg/m2), testovaná ve studii se zvyšováním dávek u pacientů s chronickou lymfocytární leukemií. Nebyly zjištěny žádné další bezpečnostní signály.
U pacientů, u kterých se vyskytne předávkování, má být okamžitě přerušena infuze a mají být pečlivě sledováni.
V klinické studii SABRINA (BO22334) přípravku MabThera pro subkutánní podání byla třem pacientům nedopatřením podána subkutánní forma intravenózně až do výše maximální dávky rituximabu 2780 mg, a to bez žádných nežádoucích účinků.
Pacienti, u kterých se vyskytne předávkování nebo chybná medikace, mají být pečlivě sledováni.
Po uvedení přípravku na trh bylo hlášeno pět případů předávkování přípravkem MabThera. Ve třech případech nebyly hlášeny žádné nežádoucí účinky. Dva nežádoucí účinky, které byly hlášeny, byly příznaky podobné chřipce (flu-like) při dávce 1,8 g rituximabu a fatální respirační selhání při dávce 2 g rituximabu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: protinádorové látky, monoklonální protilátky, ATC kód: L01XC02
Přípravek MabThera pro subkutánní podání obsahuje rekombinantní lidskou hyaluronidázu (rHuPH20), enzym používaný ke zvýšení disperze a absorpce současně podávaných látek, pokud je podávána subkutánně.
Rituximab se specificky váže na transmembránový antigen CD20, což je neglykosylovaný fosfoprotein vyskytující se na pre-B a zralých B-lymfocytech. Tento antigen je exprimován > 95 % všech nehodgkinských lymfomů původem z B buněk.
CD20 se nachází na normálních i maligních B-lymfocytech, není přítomen na hematopoetických kmenových buňkách, pro-B-buňkách, normálních plazmatických buňkách ani na jiných normálních tkáních. Antigen se po navázání protilátky neinternalizuje a není také uvolňován z povrchu buňky. CD20 necirkuluje v plazmě jako volný antigen a tedy nevzniká kompetice o navázání protilátek.
Rituximab se svým Fab fragmentem naváže na CD20 antigen na povrchu B-lymfocytů a prostřednictvím Fc domény může být zahájena efektorová imunitní reakce, která vede k lýze B-lymfocytů. Možné mechanizmy, kterými je lýza B-lymfocytů zprostředkována, zahrnují jednak cytotoxickou reakci vyvolanou účinkem komplementu (CDC), jejímž prvním krokem je vazba C1q a jednak protilátkami zprostředkovanou buněčnou cytotoxicitu (ADCC), která závisí na aktivaci jednoho či více Fcy receptorů na povrchu granulocytů, makrofágů a NK buněk. Rovněž bylo prokázáno, že vazba rituximabu na antigen CD 20 přítomný na B lymfocytech vyvolává buněčnou smrt navozením apoptózy.
Počet B-lymfocytů v periferní krvi se snižuje pod normu po podání první dávky přípravku MabThera. U pacientů léčených z důvodu hematologických malignit se objevila nová populace B buněk během 6 měsíců po léčbě a obvykle byl jejich normální počet obnoven během 12 měsíců po ukončení terapie, ačkoli u některých pacientů to může trvat déle (se střední dobou do znovuobjevení lymfocytů až 23 měsíců po indukční léčbě). U pacientů s revmatoidní artritidou byla po podání dvou infuzí 1000 mg přípravku MabThera v odstupu 14 dní pozorována bezprostřední deplece B lymfocytů v periferní krvi. Počet B lymfocytů v periferní krvi začal stoupat od 24. týdne a u většiny pacientů bylo pozorováno obnovení populace do 40. týdne, ať byl přípravek MabThera podáván jako monoterapie nebo v kombinaci s metotrexátem.
Klinické zkušenosti v léčbě nehodgkinských lymfomů přípravkem MabThera pro subkutánní podání
Klinické zkušenosti v léčbě nehodgkinských lymfomů přípravkem MabThera pro subkutánní podání jsou založeny na údajích z klinické studie fáze III (SABRINA BO22334) u pacientů s folikulárními lymfomy (FL) a z klinické studie fáze Ib (SparkThera BP22333), ve kterých se stanovovala a potvrzovala dávka u pacientů s folikulárními lymfomy.
Výsledky ze studie BP22333 jsou uvedeny v bodě 5.2.
Klinická studie BO22334 (SABRINA)
Dvoustupňová, mezinárodní, multicentrická, randomizovaná, kontrolovaná, otevřená studie fáze III byla provedena s pacientů s dosud neléčeným folikulárním lymfomem s cílem zhodnotit non-inferioritu farmakokinetického profilu spolu s účinností a bezpečností přípravku MabThera pro subkutánní podání v kombinaci s CHOP nebo CVP ve srovnání s přípravkem MabThera pro intravenózní podání v kombinaci s CHOP nebo CVP.
Cílem prvního stupně studie bylo určit dávku subkutánního rituximabu, která by při podávání v rámci indukční léčby každé 3 týdny dosáhla srovnatelných sérových hladin Ctrough jako intravenózní léková forma přípravku MabThera (viz bod 5.2). Do stupně 1 byly zařazeni dříve neléčení pacienti (n = 127) s CD20 pozitivním folikulárním lymfomem (FL) stupně 1, 2 nebo 3a.
Cílem stupně 2 bylo poskytnout další údaje o účinnosti a bezpečnosti subkutánního podání rituximabu ve srovnání s intravenózním podáním rituximabu, při použití subkutánní dávky 1400 mg stanovené ve stupni 1. Do stupně 2 byly zařazeni dosud neléčení pacienti s CD20 pozitivním folikulárním lymfomem stupně 1, 2 nebo 3a (n = 283).
Plán studie byl totožný u obou stupňů studie a pacienti byli randomizováni do dvou následujících léčebných skupin:
• Přípravek MabThera pro subkutánní podání (n= 205): první cyklus intravenózního podání + 7 cyklů přípravku MabThera pro subkutánní podání v kombinaci s až 8 cykly chemoterapie CHOP nebo CVP podávané každé 3 týdny.
Přípravek MabThera pro intravenózní podání byl podáván ve standardní dávce 375 mg/m2 tělesného povrchu.
Přípravek MabThera pro subkutánní podání byl podáván ve fixní dávce 1400 mg.
Pacienti, kteří dosáhli alespoň částečné léčebné odpovědi (PR), byli zařazeni do udržovací léčby přípravkem MabThera pro subkutánní podání, podávaným každých 8 týdnů po dobu 24 měsíců.
• Přípravek MabThera pro intravenózní podání (n= 205): 8 cyklů přípravku MabThera pro intravenózní podání v kombinaci s až 8 cykly chemoterapie CHOP nebo CVP podávané každé 3 týdny.
Přípravek MabThera pro intravenózní podání byl podáván ve standardní dávce 375 mg/m2 tělesného povrchu.
Pacienti, kteří dosáhli alespoň částečné léčebné odpovědi (PR), byli zařazeni do udržovací léčby přípravkem MabThera pro intravenózní podání, podávaným každých 8 týdnů po dobu 24 měsíců.
Bodové odhady četnosti celkové léčebné odpovědi u 410 pacientů zařazených do souhrnné analýzy stupňů 1 a 2 studie SABRINA jsou uvedeny v tabulce 2.
Tabulka 2 Bodové odhady četnosti léčebné odpovědi studie SABRINA (BO22334) (Intent-to-treat populace)
|
Souhrn stupňů 1 & 2 N = 410 | |||
|
Rituximab intravenózní podání |
Rituximab subkutánní podání | ||
|
ORR |
Bodový odhad |
84,4 % (173/205) |
83,4% (171/205) |
|
95% interval spolehlivosti |
[78,7 %; 89,1 %] |
[77,6 %; 88,2 %] | |
|
CRR |
Bodový odhad |
31,7 % (65/205) |
32,7 % (67/205) |
|
95% interval spolehlivosti |
[25,4 %; 38,6 %] |
[26,3 %; 39,6 %] | |
ORR - četnost celkové odpovědi CRR - četnost kompletních remisí
Průzkumné analýzy ukázaly, že četnosti léčebných odpovědí v podskupinách podle BSA, podané chemoterapie a pohlaví se nijak výrazně nelišily od ITT populace.
Imunogenita
Údaje z programu vývoje přípravku MabThera pro subkutánní podání naznačují, že tvorba protilátek proti rituximabu (HACA) je po subkutánním podání srovnatelná s jejich tvorbou po intravenózním podání. Ve studii SABRINA (BO22334) byl výskyt léčbou indukovaných/zvýšených protilátek proti rituximabu ve skupině se subkutánním podáním (2 %) malý a podobný tomu, který byl pozorován ve skupině s intravenózním podáním (1%). Výskyt léčbou indukovaných/zvýšených protilátek proti rHuPH20 byl 6 % u skupiny s intravenózním podáním ve srovnání s 9 % ve skupině se subkutánním podáním, a žádný z pacientů, kteří byli pozitivně testováni na protilátky proti rHuPH20, nebyl pozitivní při testování na neutralizační protilátky. Není zřejmý žádný zjevný vliv přítomnosti protilátek proti rituximabu nebo proti rHuPH20 na bezpečnost nebo účinnost.
Celkový podíl pacientů, u kterých byly zjištěny protilátky proti rHuPH20, byl v průběhu studie po celou dobu sledování v obou kohortách konstantní. Klinický význam rozvoje HACA či protilátek proti rHuPH20 po léčbě přípravkem MabThera pro subkutánní podání není znám.
Není zřejmý žádný zjevný vliv přítomnosti protilátek proti rituximabu nebo proti rHuPH20 na bezpečnost nebo účinnost (SABRINA).
Klinické zkušenosti v léčbě nehodgkinských lymfomů přípravkem MabThera koncentrát pro infuzní roztok
Folikulární lymfomy
Iniciální léčba v kombinaci s chemoterapií
V otevřené randomizované studii bylo randomizováno celkem 322 nemocných s dříve neléčeným folikulárním lymfomem do skupiny léčené chemoterapií CVP (cyklofosfamid 750 mg/m2, vinkristin
1,4 mg/m2 do celkové dávky maximálně 2 mg v den 1, prednisolon 40 mg/m2/den ve dnech 1-5) opakující se každé 3 týdny do celkového počtu 8 dávek nebo do skupiny léčené přípravkem MabThera (375 mg/m2) v kombinaci s CVP (R-CVP). Přípravek MabThera byl podáván prvý den každého léčebného cyklu. Celkem bylo léčeno a z pohledu účinnosti analyzováno 321 nemocných (162 R-CVP a 159 CVP). Medián sledování byl 53 měsíce. Léčba R-CVP vedla proti CVP k signifikantnímu zlepšení primárního cíle studie - doby do selhání léčby (27 měsíců proti 6,6 měsícům, p< 0,0001, log-rank test). Ve R-CVP skupině byla zaznamenána signifikantně (p< 0,0001, chí kvadrát test) vyšší odpověď lymfomu na léčbu (CR, CRu, PR) proti skupině CVP (80,9 % proti 57,2 %). Léčba kombinací R-CVP ve srovnání s CVP významně prodloužila dobu do progrese choroby či úmrtí,
33,6 měsíce oproti 14,7 měsíce (p < 0.0001, log-rank test). Medián trvání odpovědi byl ve skupině R-CVP 37,7 měsíce, ve skupině CVP byl 13,5 měsíce (p< 0,0001, log rank test).
Srovnání celkového přežití mezi léčebnými skupinami ukázalo významný klinický rozdíl: (p=0,029, log-rank test stratifikovaný dle center): četnost přežití po 53 měsících byla u pacientů v rameni R-CVP
80,9 %, zatímco u pacientů v rameni CVP to bylo 71,1 %.
Výsledky tří dalších randomizovaných studií, které použily přípravek MabThera v kombinaci s jiným chemoterapeutickým režimem než CVP (CHOP, MCP, CHVP/Interferon-a) také prokázaly významné zlepšení četnosti odpovědí, na čase závislých parametrů, včetně celkového přežití. Klíčové výsledky všech 4 studií jsou shrnuty v Tabulce 3.
Tabulka 3 Shrnutí klíčových výsledků 4 randomizovaných studií fáze III hodnotících přínos
přípravku MabThera s různými chemoterapeutickými režimy u folikulárního lymfomu _____
|
Studie |
Léčba, Počet pacientů |
Střední doba sledování, měsíce |
ORR % |
CR % |
Střední doba TTF/PFS/ EFS měsíce |
OS % |
|
M39021 |
CVP, 159 R-CVP, 162 |
53 |
57 81 |
10 41 |
Medián TTP: 14,7 33,6 p<0,0001 |
53 měsíce 71,1 80,9 p=0,029 |
|
GLSG’00 |
CHOP, 205 R-CHOP, 223 |
18 |
90 96 |
17 20 |
Medián TTF: 2,6 roků Nedosažen p < 0,001 |
18 měsíců 90 95 p = 0,016 |
|
OSHO-39 |
MCP, 96 R-MCP, 105 |
47 |
75 92 |
25 50 |
Medián PFS: 28,8 Nedosažen p < 0,0001 |
48 měsíců 74 87 p = 0,0096 |
|
FL2000 |
CHVP-IFN, 183 R-CHVP-IFN, 175 |
42 |
85 94 |
49 76 |
Medián EFS: 36 Nedosažen p < 0,0001 |
42 měsíce 84 91 p = 0,029 |
EFS - Přežití bez události TTP - Doba do progrese či úmrtí PFS - Přežití bez progrese TTF - Doba do selhání léčby OS - Přežití v době analýzy
Udržovací terapie
Dosud neléčený folikulární lymfom
V prospektivní, otevřené, mezinárodní, multicentrické studii fáze III 1193 pacientů s dosud neléčeným pokročilým folikulárním lymfomem podstoupilo indukční léčbu R-CHOP (n=881), R-CVP (n=268) nebo R-FCM (n=44) dle volby zkoušejícího. Celkem 1078 pacientů odpovědělo na indukční léčbu, 1018 z nich bylo randomizováno k udržovací léčbě přípravkem MabThera (n=505) nebo ke sledování (n=513). Tyto dvě léčebné skupiny byly dobře vyváženy vzhledem k výchozím charakteristikám a rozsahu onemocnění. Udržovací léčba přípravkem MabThera spočívala v jedné infuzi přípravku MabThera v dávce 375 mg/m2 tělesného povrchu, která byla podávána každé 2 měsíce do progrese onemocnění či nejdéle po dobu 2 let.
Při střední době sledování 25 měsíců od randomizace vedla udržovací léčba přípravkem MabThera ve srovnání se samotným sledováním u dosud neléčených pacientů s folikulárním lymfomem ke klinicky důležitému a statisticky významnému zlepšení v primárním cílovém parametru účinnosti, kterým bylo přežití bez progrese (PFS) hodnocené zkoušejícím (Tabulka 4).
Významný přínos udržovací léčby přípravkem MabThera byl zaznamenán také u sekundárních cílových parametrů studie, kterými byly přežití bez příhody (EFS), doba do další protilymfomové léčby (TNLT), doba do další chemoterapie (TNCT) a celkový výskyt odpovědí (ORR) (Tabulka 4). Výsledky primární analýzy byly potvrzeny na základě delší doby sledování (střední doba sledování:
48 měsíců), a ty pak byly vloženy do Tabulky 4 pro srovnání 25 a 48 měsíčního období sledování.
Tabulka 4 Udržovací fáze studie: přehled účinnosti přípravku MabThera vs. sledování
po střední době sledování 48 měsíců (porovnáno s výsledky primární analýzy založené na střední době sledování 25 měsíců)_
|
Sledování |
MabThera |
Log-rank P |
Snížení rizika | ||
|
N=513 |
N=505 |
hodnota | |||
|
Primární parametr účinnosti | |||||
|
PFS (medián) |
48,4 měsíce |
NR |
<0,0001 |
45 % | |
|
(NR) |
(NR) |
(<0,0001) |
(50 %) | ||
|
Sekundární parametry účinnosti | |||||
|
EFS (medián) |
47,6 měsíce |
NR |
<0,0001 |
42 % | |
|
(37,8 měsíce) |
(NR) |
(< 0,0001) |
(46 %) | ||
|
OS (medián) |
NR |
NR |
0,9298 |
-2 % | |
|
(NR) |
(NR) |
(0,7246) |
(11 %) | ||
|
TNLT (medián) |
60,2 měsíce |
NR |
< 0,0001 |
39 % | |
|
(NR) |
(NR) |
(0,0003) |
(39 %) | ||
|
TNCT (medián) |
NR |
NR |
0,0006 |
34 % | |
|
(NR) |
(NR) |
(0,0011) |
(40 %) | ||
|
ORR* |
60,7 % |
79,0 % |
<0,0001# |
OR = 2,43 | |
|
(55,0 %) |
(74,0 %) |
(< 0,0001) |
(OR = 2,33) | ||
|
Četnost kompletních remisí (CR/CRu)* |
52,7 % (47,7 %) |
72,2 % (66,8 %) |
<0,0001 (< 0,0001) |
OR = 2,34 (OR = 2,21) | |
*Na konci udržovací léčby/sledování; # p hodnota chí-kvadrát testu.
Hodnoty v závorkách odpovídají 25 měsícům střední doby sledování (primární analýza). Hodnoty před závorkami odpovídají 48 měsícům střední doby sledování (aktuální analýza).
PFS: přežití bez progrese; EFS: přežití bez příhody; OS: celkové přežití; TNLT: doba do další protilymfomové léčby;
TNCT: doba do další chemoterapie; ORR: celkový výskyt odpovědí; NR: nebylo možno dosáhnout v době klinické uzávěrky; OR: poměr šancí.
Udržovací léčba přípravkem MabThera poskytla konzistentní přínos pro všechny předdefinované hodnocené podskupiny: pohlaví (muži, ženy), věk (do 60 let, nad 60 let včetně), hodnota FLIPI (<=1,
2 nebo >=3), indukční léčba (R-CHOP, R-CvP nebo R-FCM) a bez ohledu na kvalitu léčebné
odpovědi na indukční léčbu (CR/CRu nebo PR). Exploratomí analýzy prospěchu udržovací léčby prokázaly méně výrazný účinek u starších pacientů (> 70 let), hodnocený vzorek však byl malý.
Relabující/refrakterní folikulární lymfom
V prospektivní, otevřené, mezinárodní, multicentrické klinické studii fáze III bylo v prvním kroku indukční terapie randomizováno 465 pacientů s relabujícím/refrakterním folikulárním lymfomem do skupiny podstupující CHOP (cyklofosfamid, doxorubicin, vinkristin, prednisolon; n=231) nebo do skupiny léčené přípravkem MabThera plus CHOP (R-CHOP, n=234). Dvě léčebné skupiny byly vyvážené z hlediska vstupních charakteristik a stavu onemocnění. Celkem 334 pacientů, kteří po indukční terapii dosáhli kompletní nebo částečné remise, bylo randomizováno v druhém kroku do skupiny s udržovací terapií přípravkem MabThera (n=167) nebo do skupiny podstupující pouze observaci (n=167). Udržovací léčba přípravkem MabThera spočívala v aplikaci jedné infuze přípravku MabThera v dávce 375 mg/m2 plochy povrchu těla, která byla podávána jedenkrát za 3 měsíce až do doby progrese choroby nebo nejvýše po dobu dvou let.
Závěrečná analýza účinnosti zahrnovala všechny pacienty, kteří byli randomizováni v obou částech studie. Po době observace, která byla u pacientů randomizovaných do indukční fáze průměrně 31 měsíců, se stav pacientů s relabujícím/refrakterním folikulárním lymfomem, kteří podstoupili terapii R-CHOP v porovnání s CHOP, signifikantně zlepšil (viz Tabulka 5).
Tabulka 5 Indukční fáze: přehled výsledků účinnosti CHOP vs. R-CHOP (střední doba
_sledování 31 měsíců)_
|
CHOP |
R-CHOP |
Hodnota p |
Snížení rizika^ | |
|
Primární účinnost ORR2) |
74 % |
87 % |
0,0003 |
NA |
|
CR2) |
16 % |
29 % |
0,0005 |
NA |
|
pr2) |
58 % |
58 % |
0,9449 |
NA |
1J Odhady vypočítány na základě poměrů rizik
2) Poslední protinádorová odpověď stanovená zkoušejícím. "Primární" statistické testy pro "odpověď" byly vyjádřeny jako trend testu CR versus PR versus nulová odpověď (p < 0,0001)
Vysvětlivky: NA: nedostupná data; ORR: celkový výskyt odpovědí; CR: kompletní odpověď; PR: částečná odpověď
U pacientů randomizovaných do udržovací fáze klinické studie byl medián doby observace 28 měsíců od randomizace. Udržovací léčba přípravkem MabThera vedla ke klinicky relevantnímu a statisticky významnému zlepšení z hlediska primárního cíle, PFS (doba od randomizace do udržovací fáze do relapsu, progrese choroby nebo úmrtí) při srovnání s observační skupinou (bez léčby) (p< 0,0001, log-rank test). Dosažený medián PFS byl 42,2 měsíce ve skupině s udržovací léčbou přípravkem MabThera v porovnání s 14,3 měsíce ve skupině bez léčby. Použití regresní analýzy (Coxův model) ukázalo, že v důsledku udržovací léčby přípravkem MabThera je riziko progrese nebo úmrtí sníženo o 61 % ve srovnání se skupinou bez léčby (95 % CI; 45 %-72 %). Odhad počtu odpovědí bez progrese vycházející z Kaplan-Meierových křivek po 12 měsících léčby byl 78 % ve skupině s udržovací léčbou přípravkem MabThera oproti 57 % ve skupině bez léčby. Analýza celkového přežití potvrdila signifikantní výhodnost udržovací léčby přípravkem MabThera oproti observační skupině (p=0,0039 log-rank test). V důsledku udržovací léčby přípravkem MabThera bylo riziko úmrtí sníženo o 56 % (95 % CI; 22 %-75 %).
|
Parametr účinnosti |
Určení mediánu doby (měsíce) |
Snížení | ||
|
k dosažení stanoveného parametru |
rizika | |||
|
metodou Kaplan-Meier | ||||
|
Observace |
MabThera |
Log-Rank | ||
|
(N = 167) |
(N=167) |
hodnota p | ||
|
Doba přežití bez progrese (PFS) |
14,3 |
42,2 |
<0,0001 |
61 % |
|
Celkové přežití |
NR |
NR |
0,0039 |
56 % |
|
Doba do nové léčby lymfomu |
20,1 |
38,8 |
<0,0001 |
50 % |
|
Doba přežití bez známek onemocnění3 |
16,5 |
53,7 |
0,0003 |
67 % |
|
Analýza podskupin PFS | ||||
|
CHOP |
11,6 |
37,5 |
<0,0001 |
71 % |
|
R-CHOP |
22,1 |
51,9 |
0,0071 |
46 % |
|
CR |
14,3 |
52,8 |
0,0008 |
64 % |
|
PR |
14,3 |
37,8 |
<0,0001 |
54 % |
|
OS | ||||
|
CHOP |
NR |
NR |
0,0348 |
55 % |
|
R-CHOP |
NR |
NR |
0,0482 |
56 % |
NR: nedosaženo; a: relevantní pouze u pacientů, kteří dosáhli kompletní odpovědi
Výhodnost udržovací léčby přípravkem MabThera byla potvrzena ve všech analyzovaných podskupinách bez ohledu na indukční režim (CHOP nebo R-CHOP) nebo kvalitu odpovědi v rámci indukční léčby (CR nebo PR) (viz Tabulka 6). V důsledku udržovací léčby přípravkem MabThera byl významně prodloužen medián PFS u pacientů odpovídajících na indukční terapii CHOP (medián PFS
37,5 měsíce vs. 11,6 měsíce, p< 0,0001), stejně jako u pacientů odpovídajících na indukční léčbu R-CHOP (medián PFS 51,9 měsíce vs. 22,1 měsíce, p=0,0071). Přestože se jednalo o malé podskupiny, ukázala se udržovací léčba přípravkem MabThera signifikantně výhodnou i z hlediska celkového přežití, a to jak u pacientů odpovídajících na CHOP, tak u pacientů odpovídajících na R-CHOP, ačkoli pro potvrzení tohoto zjištění je zapotřebí delší doba sledování po léčbě.
Difuzní velkobuněčný nehodgkinský lymfom z B buněk
Celkem 399 dosud neléčených starších pacientů (věk 60 až 80 let) s diagnostikovaným difúzním velkobuněčným B-nehodgkinským lymfomem bylo v rámci randomizované, otevřené studie léčeno osmi cykly standardní chemoterapie CHOP (cyklofosfamid 750 mg/m2 den 1, doxorubicin 50 mg/m2 den 1, vinkristin 1,4 mg/m2 den 1 do maximální dávky 2 mg a prednisolon 40 mg/m2/den podávaný ve dnech 1-5) aplikované v intervalu 3 týdnů po osm cyklů nebo přípravkem MabThera v dávce 375 mg/m2 s chemoterapií CHOP (R-CHOP). Přípravek MabThera byl podáván první den každého léčebného cyklu.
Závěrečná analýza účinnosti byla provedena u všech randomizovaných pacientů (197 CHOP, 202 R-CHOP) a střední hodnota trvání následného sledování byla přibližně 31 měsíců. Obě skupiny byly vyrovnané s ohledem na charakteristiku a pokročilost onemocnění na počátku léčby. Závěrečná analýza potvrdila, že léčebný režim R-CHOP byl spojen s klinicky relevantním a statisticky významným prodloužením přežití bez výskytu nežádoucích příhod (což byl hlavní parametr účinnosti, kde příhodou bylo úmrtí, relaps nebo progrese lymfomu, nebo zahájení nové léčby lymfomu) (p=0,0001). Střední hodnota trvání bezpříznakového období stanovená metodou Kaplan-Meier byla
35 měsíců ve skupině léčené režimem R-CHOP, ve srovnání s 13 měsíci ve skupině léčené režimem CHOP, což představuje snížení rizika o 41 %. Celkové přežití ve 24. měsíci bylo 68,2 % ve skupině léčené R-CHOP ve srovnání s 57,4 % ve skupině léčené režimem CHOP. Následná analýza celkového přežití, provedená po 60 měsících následného sledování, potvrdila větší prospěšnost R-CHOP než CHOP (p=0,0071), což představuje snížení rizika o 32 %.
Analýza všech sekundárních parametrů (četnost odezvy na léčbu, přežití bez známek progrese, přežití bez známek nemoci, trvání odpovědi) ověřila léčebný účinek R-CHOP ve srovnání s CHOP. Celková četnost odezvy na léčbu po 8 cyklech byla 76,2 % ve skupině léčené R-CHOP a 62,4 % ve skupině léčené CHOP (p=0,0028). Riziko progrese nemoci se snížilo o 46 % a riziko relapsu o 51 %. Ve všech podskupinách pacientů (pohlaví, věk, IPI korigovaný na věk, stádium nemoci dle Ann Arbor, ECOG, B2 2 mikroglobulin, LDH, albumin, B-symptomy, bulky disease, mimouzlinová manifestace, postižení kostní dřeně) byly poměry rizik pro asymptomatické přežití a celkové přežití (R-CHOP oproti CHOP) nižší než 0,83 a 0,95. Režim R-CHOP byl spojen se zlepšeným výsledkem léčby u vysoce a nízkorizikových pacientů podle IPI korigovaného na věk.
Klinické laboratorní nálezy
U 67 nemocných vyšetřovaných pro přítomnost HAMA (protilátky proti myším antigenům) nebyla zaznamenána žádná odpověď. Z 356 nemocných vyšetřovaných pro přítomnost HACA (human anti-chimeric antibody) bylo 1,1 % pozitivních (4 pacienti).
Pediatrická populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s rituximabem u všech podskupin pediatrické populace s folikulárním lymfomem. Informace o použití u dětí viz bod 4.2.
5.2 Farmakokinetické vlastnosti
Absorpce
Farmakokinetika rituximabu po jednorázovém podání dávky 375 mg/m2, 625 mg/m2 a 800 mg/m2 přípravku MabThera subkutánní byla porovnána s dávkou 375 mg/m2 přípravku MabThera intravenózní u pacientů s folikulárním lymfomem. Při dalším subkutánním podání je absorpce rituximabu pomalá a asi 3 dny po podání se dosáhne maximální koncentrace. Na základě populační farmakokinetické analýzy byla stanovena 71 % biodostupnost. Expozice rituximabu v závislosti na dávce se úměrně zvyšovala při podání subkutánní dávky v rozsahu od 375 mg/m2 do 800 mg/m2. Farmakokinetické parametry, jako jsou clearance, distribuční objem a eliminační poločas rozpadu, byly srovnatelné u obou forem.
Klinická studie BP22333 (SparkThera)
Dvoustupňová studie fáze Ib zkoumala farmakokinetiku, bezpečnost a snášenlivost přípravku MabThera pro subkutánní podání u pacientů s folikulárním lymfomem v rámci udržovací léčby.
V druhém stupni studie byl pacientům s folikulárním lymfomem, kteří předtím v rámci indukční léčby odpověděli na léčbu přípravkem MabThera pro intravenózní podání, podkožně injekcí podávána během udržovací léčby fixní dávka 1400 mg přípravku MabThera pro subkutánní podání po nejméně jedné dávce přípravku MabThera pro intravenózní podání.
Porovnání odhadované střední hodnoty Cmax u subkutánní a intravenózní formy přípravku MabThera jsou shrnuty v Tabulce 7.
Tabulka 7: Klinická studie BP22333 (SparkThera): Absorpce - Farmakokinetické parametry přípravku MabThera SC v porovnání s přípravkem MabThera IV_
|
MabThera subkutánní |
MabThera intravenózní | |
|
Předpokládaný medián Cmax (q2m) pg/ml |
201 |
209 |
|
Předpokládaný medián Cmax (q3m) pg/ml |
189 |
184 |
Střední hodnota Tmax u přípravku MabThera pro subkutánní podání byla přibližně 3 dny v porovnání s Tmax vyskytující se nebo blížící se konci infuze u intravenózního podání.
Klinická studie BO22334 (SABRINA)
Přípravek MabThera pro subkutánní podání ve fixní dávce 1400 mg byl po úvodním cyklu s intravenózní formou přípravku MabThera podáván podkožně v 6 cyklech během indukční léčby v 3týdenních intervalech u dosud neléčeným pacientů s folikulárním lymfomem v kombinaci s chemoterapií. Sérové hladiny rituximabu Cmax v 7. cyklu byly v obou ramenech podobné, přitom geometrická střední hodnota byla pro intravenózní lékovou formu 250,63 (19,01) pg/ml a pro subkutánní formu 236,82 (29,41) pg/ml, což vedlo k poměru geometrických středních hodnot (Cmax, SC/Cmax, iv) 0,941 (90% CI: 0,872, 1,015).
Distribuce/eliminace
Geometrický průměr Ctrough a geometrický průměr AUCt v klinických studiích BP22333 a BO22334 jsou shrnuty v Tabulce 8.
Tabulka 8: Distribuce/eliminace - Farmakokinetické parametry přípravku MabThera subkutánní v porovnání s přípravkem MabThera intravenózní_
|
Klinická studie BP22333 (SparkThera) | ||||
|
Geometrický průměr Ctrough (q2m) pg/ml |
Geometrický průměr Ctrough (q3m) pg/ml |
Geometrický průměr AUCt cyklu 2 (q2m) pg.den/ml |
Geometrický průměr AUCt cyklu 2 (q3m) pg.den/ml | |
|
MabThera subkutánní podání |
32,2 |
12,1 |
5430 |
5320 |
|
MabThera intravenózní podání |
25,9 |
10,9 |
4012 |
3947 |
|
Klinická studie BO22334 (SABRINA) | ||||
|
Geometrický průměr Ctrough hodnot před podáním další dávky cyklu 8 pg/ml |
Geometrický průměr AUC hodnot cyklu 7 pg.den/ml | |||
|
MabThera subkutánní podání |
134,6 |
3778 | ||
|
MabThera intravenózní podání |
83,1 |
2734 | ||
V populační farmakokinetické analýze u 403 pacientů s folikulárními lymfomy, kteří dostali subkutánně a/nebo intravenózně přípravek MabThera, jednu či více infuzí přípravku MabThera samostatně či v kombinaci s chemoterapií, byly hodnoty nespecifické clearance (CL1), úvodní specifické clearance (CL2) pravděpodobně ovlivněné B buňkami či nádorovou náloží a centrálním distribučním objemem (Vj) odhadnuty v typické populaci na 0,194 l/den, 0,535 l/den a 4,37 l/den.
Odhadovaná střední hodnota terminálního eliminačního poločasu přípravku MabThera pro subkutánní podání byla 29,7 dní (rozmezí 9,9 - 91,2 dní). Analytický soubor dat obsahoval 6003 kvantifikovatelných vzorků od 403 pacientů, kterým byl podáván subkutánně a/nebo intravenózně rituximab v klinických studiích BP22333 (3736 vzorků od 277 pacientů) a BO22334 (2267 vzorků od 126 pacientů). 29 (0,48 %) vzorků po podání dávky (všechny ze studie BP22333) bylo pod úrovní kvantifikačního limitu. Nechyběly žádné hodnoty závislých proměnných s výjimkou vstupní hodnoty počtu B buněk. Nádorová nálož při vstupu do studie byla dostupná pouze ve studii BO22334.
Zvláštní populace
V klinické studii BO22334 byl pozorován vliv objemu těla na poměry expozic hlášené v 7. cyklu, mezi subkutánním rituximabem podávaným v dávce 1400 mg každé 3 týdny a intravenózním rituximabem podávaným v dávce 375 mg/m2 každé 3 týdny, přičemž u pacientů s nízkým, středním a vysokým BSA byly hodnoty poměru Ctrough 2,29, 1,31 a 1,41 (nízké BSA < 1,70 m2; střední BSA 1,70 - 1,90 m2; vysoké BSA > 1,90 m2). Odpovídající hodnoty poměrů AUCt byly 1,66, 1,17 a 1,32.
Nebyl zjištěn žádný důkaz klinicky významné závislosti farmakokinetiky rituximabu na věku a pohlaví.
Protilátky proti rituximabu byly zjištěny pouze u 13 pacientů a nevedly k žádnému klinicky významnému vzestupu clearance během stavu “steady- state”.
5.3 Předklinické údaje vztahující se k bezpečnosti
Rituximab se ukázal jako látka vysoce specifická k CD20 antigenu na B-lymfocytech. Studie prováděné na opicích cynomolgus neprokázaly jiný druh toxicity než očekávanou farmakologickou depleci B-lymfocytů v periferní krvi a v lymfatických tkáních.
Studie vývojové toxicity byly provedeny u opic rodu cynomolgus při podávání dávek do 100 mg/kg (20.-50. den březosti) a neprokázaly žádnou embryotoxicitu pro plod, která by byla spojena s rituximabem. V závislosti na dávce přípravku však byla pozorována farmakologická deplece B lymfocytů v lymfatických orgánech plodu, která přetrvávala postnatálně a byla doprovázena snížením hladiny IgG u novorozených opic. Počet B lymfocytů se u těchto zvířat vrátil k normální hodnotě během 6 měsíců po narození a nedošlo ke snížené reakci na imunizaci.
Standardní testy pro vyšetření mutagenity nebyly prováděny, neboť tyto testy nejsou pro tento typ molekuly relevantní. Dlouhodobé studie na zvířatech, které by měly určovat karcinogenní potenciál rituximabu, nebyly provedeny.
Nebyly provedeny konkrétní studie stanovující účinky rituximabu nebo rHuPH20 na fertilitu.
V obecných studiích toxicity na opicích cynomolgus nebyly pozorovány žádné škodlivé účinky na reprodukční orgány samců či samic. Navíc nebyly prokázány žádné účinky rHuPH20 na kvalitu spermatu.
V embryofetálních vývojových studiích u myší, rHuPH20 způsobil snížení hmotnosti plodu a ztrátu implantací vajíčka při systémových expozicích dostatečně převyšujících terapeutické expozice u lidí. Neexistují žádné důkazy o dysmorfogenezi (tj. teratogenitě) v důsledku systémové expozice rHuPH20.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Biosyntetická lidská hyaluronidáza Histidin
Monohydrát histidin-hydrochloridu
Dihydrát trehalózy
Methionin
Polysorbát 80
Voda na injekci
6.2 Inkompatibility
Mezi přípravkem MabThera pro subkutánní podání a polypropylenovým nebo polykarbonátovým materiálem injekční stříkačky nebo transferem z nerezové oceli a injekčními jehlami a polyetylenovou Luer kuželovitou zátkou nebyla pozorována inkompatibilita.
6.3 Doba použitelnosti
Neotevřená injekční lahvička 30 měsíců
Po prvním otevření
Po přenosu roztoku přípravku MabThera pro subkutánní podání z injekční lahvičky do injekční stříkačky je roztok fyzikálně a chemicky stabilní po dobu 48 hodin při teplotě 2 °C - 8 °C a následně pak 8 hodin při 30 °C při difúzním denním světle.
Z mikrobiologického hlediska má být přípravek použit okamžitě. Není-li použit okamžitě, příprava má být provedena za kontrolovaných a validovaných aseptických podmínek. Doba a podmínky uchovávání přípravku před použitím jsou v zodpovědnosti uživatele.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C). Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Podmínky uchovávání tohoto léčivého přípravku po jeho prvním otevření jsou uvedeny v bodě 6.3.
6.5 Druh obalu a obsah balení
Injekční lahvička z bezbarvého skla typu I, s pryžovou zátkou s hliníkovým uzávěrem a růžovým plastovým „flip-off" diskem, obsahující 1400 mg/11,7 ml rituximabu.
Jedno balení obsahuje 1 injekční lahvičku.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Přípravek MabThera je dodáván ve sterilních, nepyrogenních lahvičkách na jedno použití bez konzervačních látek. Injekční lahvička obsahuje odlepovací nálepku, na které je uvedena síla, cesta podání a indikace. Tato nálepka má být z injekční lahvičky před použitím odstraněna a přilepena na injekční stříkačku. Následující body musí být přesně dodržovány, pokud jde o používání a likvidaci injekčních stříkaček a jiných ostrých předmětů:
• Jehly a injekční stříkačky nesmí být nikdy znovu použity
• Všechny použité jehly a injekční stříkačky vložte do kontejneru na ostré předměty (kontejner odolný proti propíchnutí).
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/98/067/003
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 2. června 1998
Datum posledního prodloužení registrace: 2. června 2008
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu/
NÁZEV PŘÍPRAVKU
1.
MabThera 1600 mg subkutánní injekční roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden ml obsahuje 120 mg rituximabum.
Jedna injekční lahvička obsahuje 1600 mg/13,4 ml rituximabum.
Rituximab je genetickým inženýrstvím získaná chimérická myší/lidská monoklonální protilátka. Jde o glykosylovaný imunoglobulin s lidskou IgG1 konstantní částí, zatímco variabilní části lehkých a těžkých řetězců jsou myšího původu. Protilátka je produkována suspenzí uměle kultivovaných savčích buněk (ovariální buňky čínských křečků) a je purifikována afinitní chromatografií a iontoměničem. Případně přítomné viry jsou v průběhu výroby odstraněny a inaktivovány.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční roztok.
Čirý až opalescentní, bezbarvý až nažloutlý roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek MabThera je indikován v kombinaci s chemoterapií k léčbě dospělých pacientů s dříve neléčenou a relabující/refrakterní chronickou lymfocytární leukemií (CLL). Jsou k dispozici pouze omezené údaje o účinnosti a bezpečnosti u pacientů dříve léčených monoklonálními protilátkami včetně přípravku MabThera nebo u pacientů refrakterních k předchozí léčbě přípravkem MabThera společně s chemoterapií.
Další informace viz bod 5.1.
4.2 Dávkování a způsob podání
Přípravek MabThera má být podáván pod pečlivým dohledem zkušeného zdravotnického pracovníka a v prostředí, kde je okamžitě dostupné úplné vybavení pro resuscitaci (viz bod 4.4).
Před každým podáním přípravku MabThera je vždy třeba podat premedikaci, kterou tvoří antipyretikum a antihistaminikum, např. paracetamol a difenhydramin.
Pokud není přípravek MabThera podáván v kombinaci s chemoterapeutickým režimem obsahujícím glukokortikoidy, má být zvážena premedikace glukokortikoidy.
Dávkování
Doporučenou dávkou přípravku MabThera pro subkutánní podání používaná u dospělých pacientů je subkutánní injekce v pevně stanovené dávce 1600 mg bez ohledu na velikost tělesného povrchu pacienta.
Před zahájením léčby přípravkem MabThera subkutánní injekce, musí být předem vždy všem pacientům podána plná dávka přípravku MabThera intravenózní infuzí, s použitím přípravku MabThera pro intravenózní podání (viz bod 4.4).
Pokud pacienti nebyli schopni přijmout jednu plnou dávku intravenózní infuze přípravku MabThera před přechodem na jiný typ podání, má se u nich v následných cyklech nadále podávat přípravek MabThera pro intravenózní podání, dokud není plná intravenózní dávka úspěšně podána.
Z tohoto důvodu je přechod na přípravek MabThera pro subkutánní podání možný až v druhém nebo následných cyklech léčby.
Je důležité zkontrolovat označení přípravku a ujistit se, že je podávána správná forma přípravku (pro intravenózní nebo subkutánní podání) a síla, která byla pacientovi předepsána.
Přípravek MabThera pro subkutánní podání není určený k intravenóznímu podání a má být podán pouze subkutánní injekcí. Síla 1600 mg je určena pouze pro subkutánní podání u CLL.
U pacientů s CLL se jako profylaxe ke snížení rizika syndromu z rozpadu nádoru doporučuje dostatečná hydratace a podání antiuratik počínaje 48 hodinami před zahájením léčby. U pacientů s CLL, kteří mají počet lymfocytů > 25 x 109/l, se doporučuje podat krátce před podáním přípravku MabThera 100 mg prednisonu/prednisolonu intravenózně, aby se snížila četnost a závažnost akutních reakcí na infuzi a/nebo syndromu z uvolnění cytokinů.
Doporučené dávkování přípravku MabThera v kombinaci s chemoterapií u dosud neléčených a relabujících/refrakterních pacientů je: intravenózní forma přípravku MabThera 375 mg/m2 plochy tělesného povrchu podaná 0. den prvního cyklu léčby, následovaná subkutánní formou přípravku MabThera podávanou injekčně ve fixní dávce 1600 mg na cyklus, 1. den každého následujícího cyklu (celkově: 6 cyklů).
Chemoterapie má být podávána po podání přípravku MabThera.
Úprava dávky v průběhu léčby
Redukce dávkování přípravku MabThera není doporučena. Při kombinaci přípravku MabThera s chemoterapií mohou být chemoterapeutika redukována podle standardních pravidel (viz bod 4.8).
Zvláštní populace
Pediatrická populace
Bezpečnost a účinnost přípravku MabThera u dětí do 18 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
Starší pacienti
U starších pacientů (ve věku > 65 let) není zapotřebí žádná úprava dávkování.
Způsob podání
Subkutánní injekce
Přípravek MabThera 1600 mg pro subkutánní podání má být podáván pouze subkutánní injekcí po dobu přibližně 7 minut. Jehla podkožní injekce musí být ihned před podáním pouze připojena k injekční stříkačce, aby se zabránilo případnému ucpání jehly.
Přípravek MabThera pro subkutánní podání má být injektován subkutánně do břišní stěny a nikdy nemá být podán do oblastí, kde je kůže zarudlá, kde je modřina, kde je kůže citlivá, ztvrdlá nebo do jiných částí těla, kde jsou mateřská znaménka nebo jizvy.
Nejsou dostupné žádné údaje o podávání injekce do jiných částí těla, proto injekce mají být výhradně podávány do břišní stěny.
Pokud jsou během léčebné kúry přípravkem MabThera pro subkutánní podání podávány jiné léčivé přípravky pro subkutánní podání, injekce mají být podány pokud možno do jiné oblasti.
Je-li podání injekce přerušeno, může být injekce znovu podána do stejného místa nebo do jiné oblasti, pokud je to vhodné.
Intravenózní podání infuze
Informace týkající se dávkování a způsobu podání jsou uvedeny v souhrnu údajů o přípravku (SPC) MabThera 100 mg a 500 mg koncentrátu pro infuzní roztok.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1 nebo na myší bílkoviny či hyaluronidázu.
Aktivní, závažné infekce (viz bod 4.4).
Pacienti se závažným útlumem imunitního systému.
4.4 Zvláštní upozornění a opatření pro použití
Z důvodu snadnější zpětné zjistitelnosti biologických léčivých přípravků má být obchodní název a číslo šarže podávaného přípravku zřetelně zaznamenáno (nebo vyznačeno) v pacientově dokumentaci.
Informace uvedené v bodě 4.4 se vztahují k použití přípravku MabThera pro subkutánní podání ve schválených indikacích Léčba nehodgkinských lymfomů (síla 1400 mg) a Léčba chronické lymfocytární leukemie (síla 1600 mg). Pro informace týkající se dalších indikací, prosím, použijte SPC MabThera pro intravenózní podání.
Progresivní multifokální leukoencefalopatie
Použití přípravku MabThera může souviset se zvýšeným rizikem progresivní multifokální leukoencefalopatie (PML). Pacienti musí být v pravidelných intervalech sledováni pro jakékoli nové nebo zhoršující se neurologické symptomy nebo příznaky, které by mohly naznačovat PML. V případě podezření na PML musí být další podávání přípravku pozastaveno, dokud není diagnóza PML vyloučena. Lékař by měl vyhodnotit stav pacienta, aby bylo možno určit, zda příznaky ukazují na neurologickou dysfunkci, a v kladném případě, zda příznaky ukazují na PML. Dle klinické indikace by měla být zvážena konzultace s neurologem.
Při jakýchkoli pochybnostech by měla být zvážena další vyšetření včetně magnetické rezonance, přednostně s kontrastem, vyšetření mozkomíšního moku na JC virovou DNA a opakované neurologické vyšetření.
Lékař by měl věnovat zvláštní pozornost symptomům, které naznačují PML, ale kterých si pacient nemusí všimnout (např. kognitivní, neurologické nebo psychiatrické symptomy). Nemocnému by mělo být doporučeno, aby o léčbě informoval svého partnera nebo osobu, která o něho pečuje, protože ti si mohou všimnout příznaků, které sám nemocný nezaznamená.
Pokud dojde ke vzniku PML, podávání přípravku MabThera musí být trvale ukončeno.
Po rekonstituci imunitního sytému u imunosuprimovaných nemocných s PML bylo možno pozorovat stabilizaci nebo zlepšení. Nadále není známo, zda časná detekce PML a ukončení léčby přípravkem MabThera může vést k podobné stabilizaci či zlepšení.
Infuze/reakce související s infuzí
Podání přípravku MabThera je spojeno s reakcemi souvisejícími s infuzí, které mohou souviset s uvolněním cytokinů a/nebo dalších chemických mediátorů. Syndrom z uvolnění cytokinů může být klinicky nerozeznatelný od akutních hypersenzitivních reakcí.
Tento soubor reakcí, které zahrnují syndrom z uvolnění cytokinů, syndrom nádorového rozpadu a anafylaktické či hypersenzitivní reakce, je popsán níže. Reakce nejsou specificky spojené s cestou podání přípravku MabThera a lze je pozorovat u obou forem.
Po uvedení přípravku na trh byly hlášeny závažné reakce související s infuzí, které končily úmrtím, při použití přípravku MabThera pro intravenózní podání s nástupem během 30 minut až 2 hodin po zahájení první intravenózní infuze přípravkem MabThera. Ty byly charakterizovány plicními příhodami a v některých případech zahrnovaly rychlý rozpad nádoru s rysy syndromu nádorového rozpadu, navíc horečku, zimnici, třesavku, hypotenzi, kopřivku, angioedém a další symptomy (viz bod 4.8).
Těžký syndrom z uvolnění cytokinů je charakterizován těžkou dušností, často doprovázenou bronchospazmem a hypoxií, dále horečkou, zimnicí, třesavkou, urtikou a angioedémem. Tento syndrom může být spojen s některými příznaky syndromu z rozpadu tumoru, jako jsou hyperurikémie, hyperkalémie, hypokalcémie, hyperfosfatémie, akutní renální selhání, zvýšení laktát dehydrogenázy (LDH), a může být spojen s akutním respiračním selháním a úmrtím pacienta. Akutní respirační selhání může být provázeno plicní intersticiální infiltrací nebo edémem plic, viditelným na rentgenovém vyšetření. Tento syndrom se často objevuje v průběhu jedné až dvou hodin po zahájení první infuze. U pacientů s anamnézou plicní insuficience nebo u pacientů s nádorovou infiltrací plic je větší nebezpečí nepříznivého průběhu, a proto by tito pacienti měli být léčeni se zvýšenou opatrností. U pacientů, u kterých dojde k rozvoji těžkého syndromu z uvolnění cytokinů, musí být infuze okamžitě zastavena (viz bod 4.2) a musí u nich být zahájena intenzivní symptomatická léčba. Vzhledem k tomu, že počáteční zlepšení klinických příznaků může být následováno opětovným zhoršením celkového stavu, měli by být pacienti pečlivě monitorováni až do doby, kdy projevy syndromu z rozpadu tumoru a plicní infiltrace vymizí nebo tento syndrom je vyloučen. Další pokračování léčby po úplném vymizení příznaků vedlo vzácně k opakování těžkého syndromu z uvolnění cytokinů.
Pacienti s velkou nádorovou zátěží nebo s vysokým počtem (> 25 x 109/l) cirkulujících maligních buněk, jako například pacienti s CLL, u kterých může být zvýšené riziko zejména těžkého syndromu z uvolnění cytokinů, mají být léčeni s nejvyšší opatrností. Tito pacienti mají být velmi pečlivě monitorováni v průběhu první infuze. U těchto pacientů je třeba zvážit snížení rychlosti při podávání první infuze nebo rozdělení dávky v prvním a jakémkoli následujícím cyklu léčby do dvou dnů, pokud je počet lymfocytů stále >25 x 109/l.
Po intravenózním podání bílkovin pacientům byly hlášeny anafylaktické nebo jiné hypersenzitivní reakce. Na rozdíl od syndromu z uvolnění cytokinů se skutečná hypersenzitivní reakce objevuje typicky během několika minut po zahájení infuze. Pro případ rozvoje alergické reakce v průběhu podávání přípravku MabThera, musí být léčiva užívaná k léčbě hypersenzitivní reakce, např. epinefrin (adrenalin), antihistaminika a glukokortikoidy, ihned k dispozici. Klinické příznaky anafylaktické reakce mohou být podobné klinickým příznakům syndromu z uvolnění cytokinů (viz výše). Reakce z přecitlivělosti byly hlášeny méně často než reakce vznikající v souvislosti s uvolněním cytokinů.
Dalšími reakcemi hlášenými v některých případech byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie.
Vzhledem k tomu, že se v průběhu podání přípravku MabThera může objevit hypotenze, má být zváženo přechodné vysazení antihypertenziv 12 hodin před podáním přípravku MabThera.
Nežádoucí reakce všech typů vznikající v souvislosti s podáním infuze byly pozorovány u 77 % pacientů léčených přípravkem MabThera pro intravenózní podání (včetně syndromu z uvolnění cytokinů doprovázeného hypotenzí a bronchospazmem u 10 % pacientů), viz bod 4.8. Tyto symptomy jsou obvykle reverzibilní po přerušení infuze přípravku a po podání antipyretik, antihistaminik, a podle potřeby po podání kyslíku, infuze fyziologického roztoku nebo bronchodilatancií a glukokortikoidů. Těžké reakce při syndromu z uvolnění cytokinů - viz výše.
Reakce související s podáním byly v klinických studiích pozorovány až u 50 % pacientů léčených přípravkem MabThera pro subkutánní podání. Reakce, které se objevovaly v průběhu 24 hodin po subkutánní injekci, zahrnovaly především erytém pruritus, vyrážku a reakce v místě vpichu injekce, jako např. bolest, otok a zarudnutí a obecně byly mírné až středně závažné (stupeň 1 nebo 2) a byly přechodného charakteru (viz bod 4.8).
V klinických studiích byly lokální kožní reakce velmi časté u pacientů, kterým byl podáván subkutánní přípravek MabThera. Příznaky zahrnovaly bolest, otok, induraci, krvácení, erytém, pruritus a vyrážku (viz bod 4.8). Některé lokální kožní reakce se objevily po více než 24 hodinách po subkutánním podání přípravku MabThera. Většina lokálních kožních reakcí pozorovaných následně po podání přípravku MabThera pro subkutánní podání byly mírné až středně závažné a vymizely bez jakékoli specifické léčby.
Před zahájením léčby přípravkem MabThera subkutánní injekce, musí být předem vždy všem pacientům podána plná dávka přípravku MabThera intravenózní infuzí, s použitím přípravku MabThera pro intravenózní podání. Nejvyšší riziko výskytu reakcí spojených s podáním bylo obecně pozorováno v cyklu 1. Tím, že léčba je zahájena přípravkem MabThera pro intravenózní podání, lze lépe koordinovat reakce na podání pomalou intravenózní infuzí nebo přerušením intravenózní infuze.
Pokud pacienti nebyli schopni přijmout jednu plnou dávku intravenózní infuze přípravku MabThera před přechodem na jiný typ podání, má se u nich v následných cyklech nadále podávat přípravek MabThera pro intravenózní podání, dokud není plná intravenózní dávka úspěšně podána.
Z tohoto důvodu je přechod na přípravek MabThera pro subkutánní podání možný až v druhém nebo následných cyklech léčby.
Stejně jako u intravenózní lékové formy, přípravek MabThera pro subkutánní podání má být podáván v prostředí, kde je okamžitě dostupné úplné vybavení pro resuscitaci a má být podáván pod pečlivým dohledem zkušeného zdravotnického pracovníka. Před každým podáním přípravku MabThera pro subkutánní podání se má vždy podat premedikace tvořená analgetikem/antipyretikem a antihistaminikem. Současně má být zvážena premedikace glukokortikoidy.
Pacienti mají být pozorování alespoň 15 minut po subkutánním podání přípravku MabThera. Delší interval může být vhodný u pacientů se zvýšeným rizikem hypersenzitivních reakcí.
Pacienti mají být poučeni, aby ihned kontaktovali svého lékaře, pokud se u nich vyskytnou příznaky připomínající závažnou hypersenzitivitu nebo syndrom z uvolnění cytokinů kdykoli po podání léčivého přípravku.
Srdeční poruchy
U pacientů léčených přípravkem MabThera se objevily angina pectoris, srdeční arytmie typu fibrilace či flutter síní, srdeční selhání a/nebo infarkt myokardu. Pacienti s anamnézou srdečního onemocnění a/nebo kardiotoxickou chemoterapií mají proto být pečlivě monitorováni.
Hematologická toxicita
Přestože MabThera v monoterapii nepůsobí myelosupresivně, je u nemocných s počtem neutrofilů < 1,5 x 109/l a/nebo trombocytů < 75 x 109/l potřeba opatrnosti, vzhledem k tomu, že u této skupiny nemocných jsou jen malé zkušenosti s podáním přípravku MabThera. Přípravek MabThera byl podán 21 nemocným, kteří podstoupili autologní transplantaci kostní dřeně nebo jinak rizikovým nemocným s předpokládanou redukovanou funkcí kostní dřeně, aniž by byla vyvolána myelotoxicita.
Během léčby přípravkem MabThera je třeba pravidelně kontrolovat kompletní krevní obraz, včetně počtu neutrofilů a trombocytů.
Infekce
Během léčby přípravkem MabThera se mohou objevit závažná infekční onemocnění, včetně onemocnění vedoucích k úmrtí (viz bod 4.8). Přípravek MabThera nemá být podáván pacientům s aktivním, závažným infekčním onemocněním (např. tuberkulózou, sepsí a oportunními infekcemi, viz bod 4.3).
Lékaři mají pečlivě zvážit použití přípravku MabThera u pacientů s anamnézou opakovaných či chronických infekčních onemocnění či u pacientů s průvodními chorobami, které by mohly u pacientů dále přispět k náchylnosti k závažným infekčním chorobám (viz bod 4.8).
U pacientů léčených přípravkem MabThera pro intravenózní podání byly popsány případy reaktivace hepatitidy B, včetně hlášení fulminantní hepatitidy s následným úmrtím. Většina těchto pacientů byla rovněž léčena cytotoxickou chemoterapií. Omezené údaje z jedné studie u pacientů s relabující/refrakterní CLL ukazují, že léčba přípravkem MabThera může také zhoršit následky primárních infekcí hepatitidy B. U všech pacientů má být před zahájením léčby přípravkem MabThera proveden screening na virus hepatitidy B (HBV). Screening má minimálně zahrnovat vyšetření HBsAg-statusu a HBcAb-statusu. Tato vyšetření mohou být doplněna dalšími vhodnými vyšetřeními v souladu s lokálními postupy. Pacienti s aktivním onemocněním hepatitidy B nesmí být léčeni přípravkem MabThera. Pacienti se sérologicky pozitivní hepatitidou B (buď HBsAg nebo HBcAb) mají být před zahájením léčby odesláni na odborné vyšetření ke specialistovi na jaterní onemocnění, v průběhu léčby mají být tito pacienti pečlivě sledováni a léčeni v souladu s lokálními medicínskými postupy k prevenci reaktivace hepatitidy B.
U pacientů s CLL byly po uvedení přípravku MabThera pro intravenózní podání na trh velmi vzácně hlášeny případy progresivní multifokální leukoencefalopatie (PML) (viz bod 4.8). Většina z pacientů dostávala rituximab v kombinaci s chemoterapií nebo jako součást transplantace krvetvorných kmenových buněk.
Očkování
Bezpečnost očkování živými virovými vakcínami po léčbě přípravkem MabThera nebyla u pacientů s NHL a CLL studována a očkování živými virovými vakcínami není doporučeno. Pacienti léčení přípravkem MabThera mohou podstoupit očkování neživými vakcínami. Účinnost očkování neživými vakcínami však může být nižší. V nerandomizované studii měli pacienti s relapsem nízce maligního NHL léčení monoterapií přípravkem MabThera pro intravenózní podání ve srovnání se zdravými kontrolami nižší odpověď na přeočkování tetanem (16 % vs. 81 %) a očkování látkou Keyhole Limpet Haemocyanin (KLH) (4 % vs. 69 % při zjišťování dvojnásobného vzestupu titru protilátek).
U pacientů s CLL lze vzhledem k podobnostem mezi oběma nemocemi předpokládat obdobné výsledky, avšak v klinických hodnoceních toto nebylo zkoumáno.
Průměrné hodnoty titrů protilátek proti panelu antigenů (Streptococcus pneumoniae, chřipka A, příušnice, zarděnky, plané neštovice) byly udrženy nejméně 6 měsíců po léčbě přípravkem MabThera.
Kožní reakce
Byly popsány závažné kožní reakce, jako je například toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím (viz bod 4.8). V případě výskytu takovéto příhody, s podezřením na souvislost s podáním přípravku MabThera, má být léčba trvale ukončena.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
V současné době jsou k dispozici pouze omezené údaje o možných lékových interakcích s přípravkem MabThera.
Při současném podávání přípravku MabThera s fludarabinem nebo cyklofosfamidem pacientům s CLL nebyl pozorován žádný účinek na jejich farmakokinetiku. Kromě toho nebyl pozorován žádný zjevný účinek fludarabinu a cyklofosfamidu na farmakokinetiku přípravku MabThera.
Nemocní s protilátkami proti myším bílkovinám (HAMA) nebo s protilátkami proti chimérickým protilátkám (HACA) mohou mít hypersenzitivní nebo alergické reakce při podání jiných diagnostických nebo léčebných monoklonálních protilátek.
4.6 Fertilita, těhotenství a kojení
Antikoncepce u mužů a žen
Vzhledem k tomu, že rituximab zůstává v těle pacientů s deplecí B buněk po delší dobu, musí ženy ve fertilním věku během léčby přípravkem MabThera a 12 měsíců po jejím ukončení používat efektivní antikoncepční metody.
Je známo, že imunoglobuliny IgG přecházejí přes placentární bariéru.
Počet B lymfocytů u lidských novorozenců po podání přípravku MabThera matce nebyl v klinických hodnoceních studován. Neexistují žádné dostatečné a dobře kontrolované údaje ze studií u těhotných žen, avšak u některých dětí narozených matkám vystaveným v průběhu těhotenství přípravku MabThera byla hlášena přechodná deplece B buněk a lymfocytopenie. Podobné účinky byly pozorovány ve studiích na zvířatech (viz bod 5.3). Z těchto důvodů by neměla být MabThera podávána těhotným ženám s výjimkou situace, kdy možný prospěch převáží potencionální riziko.
Kojení
Není známo, zda je rituximab vylučován do lidského mléka. Vzhledem k tomu, že mateřské IgG vylučováno je, a u kojících opic byl rituximab v mléku detekován, neměly by ženy léčené přípravkem MabThera kojit během léčby a 12 měsíců po léčbě přípravkem MabThera.
Fertilita
Studie na zvířatech neprokázaly škodlivé účinky rituximabu nebo rekombinantní lidské hyaluronidázy (rHuPH20) na reprodukční orgány.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly prováděny žádné studie hodnotící účinky přípravku MabThera na schopnost řídit a obsluhovat stroje, nicméně farmakologická aktivita a dosud hlášené nežádoucí účinky naznačují, že přípravek MabThera nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Informace uvedené v tomto bodě se vztahují k použití přípravku MabThera v onkologii.
Pro informace týkající se autoimunitních indikací, prosím, použijte SPC přípravku MabThera pro intravenózní podání.
Shrnutí bezpečnostního profilu
V průběhu klinického programu vývoje byl bezpečnostní profil přípravku MabThera pro subkutánní podání srovnatelný s intravenózní lékovou formou, s výjimkou lokálních kožních reakcí. Lokální kožní reakce, včetně reakcí v místě vpichu injekce, byly u pacientů léčených přípravkem MabThera pro subkutánní podání velmi časté. Ve studii NHL fáze III SABRINA (BO22334) byly lokální kožní reakce hlášeny až u 20 % pacientů, kterým byl podáván přípravek MabThera pro subkutánní podání. Nejčastější lokální kožní reakcí v rameni s přípravkem MabThera pro subkutánní podání byl erytém v místě vpichu injekce (13 %), bolest v místě vpichu injekce (7 %) a edém v místě vpichu injekce (4 %). S výjimkou jednoho pacienta, u kterého se vyskytla lokální kožní reakce stupně 3 (vyrážka v místě vpichu injekce) po prvním podání přípravku MabThera pro subkutánní podání (cyklus 2), byly reakce po subkutánním podání mírné či středně závažné. Lokální kožní reakce jakéhokoli stupně v rameni s přípravkem MabThera pro subkutánní podání byly nejčastější během prvního cyklu subkutánního podání (cyklus 2), následovaném druhým cyklem, a výskyt těchto reakcí se snižoval po podání následujících injekcí. Podobné příhody byly pozorovány ve studii SAWYER u CLL (BO25341) a byly hlášeny až u 42 % pacientů v rameni s přípravkem MabThera pro subkutánní podání. Nejčastějšími lokálními kožními reakcemi byl erytém v místě vpichu injekce (26 %), bolest v místě vpichu injekce (16 %) a otok v místě vpichu injekce (5 %). U dvou pacientů ve studii SAWYER došlo k lokálním kožním reakcím stupně 3 (erytém v místě vpichu injekce, bolest v místě vpichu injekce a otok v místě vpichu injekce).
Nežádoucí účinky hlášené při použití přípravku MabThera pro subkutánní podání
Riziko akutních reakcí souvisejících s podáním subkutánní formy přípravku MabThera bylo hodnoceno ve třech klinických studiích: SparkThera a SABRINA (dvě klinické studie NHL) a SAWYER, klinická studie u CLL.
Ve studii SABRINA byly závažné reakce (stupně >3) související s podáním subkutánní formy přípravku MabThera hlášeny u 2 pacientů (2 %). Tyto příhody, vyrážka v místě vpichu injekce a sucho v ústech, byly stupně 3.
Ve studii SparkThera nebyly hlášeny žádné závažné reakce související s podáním přípravku.
Ve studii SAWYER (BO25341) byly po podání subkutánní formy přípravku MabThera hlášeny závažné reakce související s podáním (stupeň >3) u čtyř pacientů (5 %). Tyto příhody byly trombocytopenie stupně 4 a úzkost, erytém v místě vpichu injekce a kopřivka stupně 3.
Nežádoucí účinky hlášené _při _použití_přípravku MabThera _pro intravenózní_podání
Zkušenosti u nehodgkinských lymfomů a chronické lymfocytární leukemie
Celkový bezpečnostní profil přípravku MabThera je u nehodgkinských lymfomů a chronické lymfocytární leukemie založen na údajích pacientů z klinických studií a postmarketingového pozorování. Tito pacienti byli léčeni buď přípravkem MabThera v monoterapii (jako indukční léčbou nebo udržovací léčbou po indukční léčbě), nebo v kombinaci s chemoterapií.
Nej častěji pozorovanými nežádoucími účinky na lék u pacientů, kteří dostávali přípravek MabThera, byly reakce související s podáním infuze, které se u většiny pacientů objevily v průběhu první infuze. Incidence příznaků souvisejících s podáním infuze se významně snižuje u následujících infuzí a po osmi dávkách přípravku MabThera je nižší než 1 %.
K infekčním příhodám (zejména bakteriálním a virovým) došlo u přibližně 30-55 % pacientů v průběhu klinických studií u pacientů s nehodgkinskými lymfomy a u 30-50 % pacientů v klinických studiích u pacientů s CLL.
Nejčastějšími hlášenými nebo pozorovanými závažnými nežádoucími účinky na lék byly:
• Reakce související s podáním infuze (včetně syndromu z uvolnění cytokinů, syndromu z rozpadu tumoru), viz bod 4.4.
• Infekce, viz bod 4.4.
• Kardiovaskulární poruchy, viz bod 4.4.
Dalšími závažnými hlášenými nežádoucími účinky na lék byly reaktivace hepatitidy B a PML (viz bod 4.4).
Četnosti nežádoucích účinků léčivého přípravku (NÚ), které byly hlášeny v souvislosti s podáním samotného přípravku MabThera nebo v kombinaci s chemoterapií, jsou shrnuty v Tabulce 1. Ve všech skupinách četností jsou NÚ prezentovány v pořadí podle klesající závažnosti. Četnost je definována jako velmi častá (>1/10), častá (>1/100 až <1/10), méně častá (>1/1000 až <1/100), vzácná (>1/10000 až <1/1000), velmi vzácná (<1/10000) a není známo (z dostupných údajů nelze určit).
Nežádoucí účinky na lék, které byly zjištěny pouze v postmarketingových pozorováních a u nichž nelze určit četnost, jsou uvedeny jako „není známo“.
Shrnutí nežádoucích účinků do tabulky
Tabulka 1 Nežádoucí účinky na léky zaznamenané v klinických studiích nebo
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Infekce a infestace |
bakteriální infekce, virové infekce, +bronchitida |
sepse, +pneumonie, +febrilní infekce, +herpes zoster, +infekce dýchacích cest, plísňové infekce, infekce neznámého původu, +akutní bronchitida, +sinusitida, hepatitida B1 |
závažné virové infekce2 | |||
|
Poruchy krve a lymfatického systému |
neutropenie, leukopenie, +febrilní neutropenie, +trombocytopenie |
+pancytopenie, +granulocytopenie |
poruchy srážlivosti, aplastická anémie, hemolytická anémie, lymfadenopatie |
přechodný vzestup hladin sérových IgM3 |
pozdní neutropenie3 | |
|
Poruchy imunitního systému |
reakce spojené s podáním4, angioedém |
hypersensitivita |
anafylaxe |
syndrom rozpadu nádoru, syndrom z uvolnění cytokinů4, sérová nemoc |
akutní reverzibilní trombocyto- penie související s podáním infuze4 | |
|
Poruchy metabolismu a výživy |
hyperglykémie, pokles hmotnosti, periferní edém, otok obličeje, vzestup LDH, hypokalcémie | |||||
|
Psychiatrické poruchy | ||||||
|
Poruchy nervového systému |
parestézie, hypestézie, agitovanost, vasodilatace, závratě, úzkost |
porucha vnímání chuti |
periferní neuropatie, paresa lícního nervu5 |
kraniální neuropatie, jiné smyslové poruchy5 | ||
|
Poruchy oka |
poruchy slzení, konjunktivitida |
závažná porucha zraku5 |
v postmarketingovém pozorování u pacientů s nehodgkinským lymfomem a CLL léčených přípravkem MabThera monoterapií/udržovací léčbou nebo v kombinaci s chemoterapií ___
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
Poruchy ucha a labyrintu |
tinnitus, bolest uší |
porucha sluchu5 | ||||
|
Srdeční poruchy |
+infarkt myokardu4 a 6, arytmie, +fibrilace síní, tachykardie, +srdeční porucha |
+levostranné srdeční selhání, +supraventrikulární tachykardie, +komorová tachykardie, +angina pectoris, +ischemie myokardu, bradykardie |
závažné kardiální poruchy4 a 6 |
srdeční selhání4 a 6 | ||
|
Cévní poruchy |
hypertenze, ortostatická |
vaskulitida (zejména kožní), leuko-cytoklastická vaskulitida | ||||
|
Respirační, hrudní a mediastinální poruchy |
Broncho spasmus4, respirační choroby, bolest na hrudi, dušnost, zhoršení kašle, rýma |
astma, obliterující bronchiolitida, plicní poruchy, hypoxie |
intersticiální plicní - '! onemocnění |
respirační selhání4 |
plicní infiltrace | |
|
Gastrointesti-nální poruchy |
zvracení, průjem, bolesti břicha, dysfágie, stomatitida, zácpa, dyspepsie, nechutenství, podráždění hltanu |
zduření břicha |
gastrointesti- nální perforace7 | |||
|
Poruchy kůže a podkožní tkáně |
kopřivka, pocení, noční poty, +kožní onemocnění |
závažné bulózní kožní reakce, Stevens- Johnsonův syndrom, toxická epidermální nekrolýza (Lyellův syndrom)7 | ||||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
hypertonie, myalgie, bolesti kloubů, bolesti zad, bolesti krku, bolest | |||||
|
Poruchy ledvin a močových cest |
renální selhání4 | |||||
|
Celkové poruchy a reakce v místě aplikace |
bolest nádoru, zrudnutí, únava, příznaky nachlazení, +multiorgánové selhání4 |
bolest v místě infuze | ||||
|
Vyšetření |
pokles hladin IgG | |||||
|
Pro každý příznak byla četnost stanovena na základě výskytu reakcí všech stupňů (lehké až závažné) s výjimkou příznaků označených "+", u kterých byla četnost stanovena na základě závažných reakcí (stupeň > 3 dle obecných kritérií toxicity NCI). Jsou uvedeny pouze nejvyšší četnosti ve studiích. 1 zahrnuje reaktivaci a primární infekce; frekvence je založena na R-FC režimu u relabující/refrakterní CLL 2 viz též níže uvedený odstavec infekce 3 viz též níže uvedený odstavec hematologické nežádoucí reakce 4 viz též níže uvedený odstavec účinky spojené s podáním infuze. Vzácně byly hlášeny fatální případy 5 příznaky kraniální neuropatie. Objevily se v různou dobu nejvýše za několik měsíců po ukončení léčby přípravkem MabThera 6 pozorováno zejména u pacientů s předchozím kardiálním onemocněním a/nebo kardiotoxickou chemoterapií a byly většinou spjaty s | ||||||
|
Třída |
Velmi časté |
Časté |
Méně časté |
Vzácné |
Velmi vzácné |
Není známo |
|
orgánových systémů |
účinky spojenými s podáním infuze 7 včetně fatálních případů_
Následující pojmy byly uváděny jako nežádoucí příhody v průběhu klinických studií, jejich četnost však byla ve skupinách pacientů s přípravkem MabThera podobná nebo nižší než v kontrolních skupinách: hematotoxicita, neutropenické infekce, infekce močových cest, poruchy čití, horečka.
U více než 50 % pacientů v klinických studiích týkajících se přípravku MabThera pro intravenózní podání byly hlášeny příznaky, které byly suspektní jako účinky spojené s podáním infuze a byly zejména pozorovány v průběhu první infuze, většinou v první nebo v prvých dvou hodinách. Tyto příznaky byly většinou horečka, zimnice a ztuhlost. Mezi další příznaky patří zrudnutí, angioedém, bronchospasmus, zvracení, nevolnost, kopřivka/vyrážka, únava, bolest hlavy, podráždění hltanu, rýma, svědění, bolest, tachykardie, hypertenze, hypotenze, dušnost, dyspepsie, slabost a známky syndromu rozpadu nádoru. Závažné účinky spojené s podáním infuze (například bronchospasmus, hypotenze) se vyskytly až u 12 % případů. Další reakce, které byly v několika případech hlášeny, byly infarkt myokardu, fibrilace síní, plicní edém a akutní reverzibilní trombocytopenie. S nižší nebo neznámou četností byly hlášeny exacerbace již existujících kardiálních onemocnění, jako jsou angina pectoris nebo městnavé srdeční selhání nebo závažné kardiální poruchy (srdeční selhání, infarkt myokardu, fibrilace síní), edém plic, multiorgánové selhání, příznak rozpadu tumoru, příznak uvolnění cytokinů, renální selhání a respirační selhání. Incidence účinků spojených s podáním intravenózní infuze se významně snížila u následujících infuzí a je <1 % pacientů při osmém cyklu léčby obsahující přípravek MabThera.
Popis vybraných nežádoucích účinků
Infekce
I když přípravek MabThera způsobuje depleci B-lymfocytů u 70 % až 80 % pacientů, snížení sérových koncentrací imunoglobulinů se vyskytuje jen u malého počtu pacientů.
V randomizovaných studiích byly v ramenech obsahujících přípravek MabThera s vyšší četností hlášeny lokalizované infekce kandidou a herpes zoster. Závažné infekce byly hlášeny u asi 4 % pacientů léčených přípravkem MabThera v monoterapii. V průběhu udržovací léčby přípravkem MabThera až po dobu dvou let byly pozorovány vyšší četnosti infekcí celkové, včetně infekcí stupně 3 a 4 ve srovnání s obdobím observace. Po dobu dvouletého léčebného období nebyla hlášena žádná kumulativní toxicita z hlediska infekce. Dále byly hlášeny při léčbě přípravkem MabThera jiné závažné virové infekce buď nové, reaktivované nebo exacerbované, z nichž některé byly fatální. Většina pacientů dostávala přípravek MabThera v kombinaci s chemoterapií nebo jako součást transplantace hematopoetických kmenových buněk. Příklady těchto závažných virových infekcí jsou infekce způsobené herpetickými viry (cytomegalovirem, virem varicella zoster a herpes simplex virem), JC virem (PML) a virem hepatitidy C. V klinických studiích byly rovněž zaznamenány případy fatální PML, které se objevily po progresi onemocnění a jeho opakované léčbě. Byly hlášeny případy reaktivace hepatitidy B, z nichž většina byla u pacientů, kteří dostávali přípravek MabThera
v kombinaci s cytotoxickou chemoterapií. U pacientů s relabující/refrakterní CLL byla incidence infekce hepatitidou B stupně 3/4 (reaktivace a primární infekce) 2 % v rameni R-FC oproti 0 % v rameni FC. Byla pozorována progrese Kaposiho sarkomu u pacientů vystavených přípravku MabThera, kteří již dříve Kaposiho sarkomem trpěli. Tyto případy se vyskytly u neschválených indikací a většina pacientů byla HIV pozitivní.
Hematologické nežádoucí účinky
V klinických studiích s monoterapií přípravkem MabThera podávaným po dobu 4 týdnů se u malého počtu pacientů vyskytly hematologické abnormality a byly většinou mírné a reverzibilní. Závažné (stupně 3/4) neutropenie byly hlášeny u 4,2 %, anémie u 1,1 % a trombocytopenie u 1,7 % pacientů.
V průběhu udržovací léčby přípravkem MabThera po dobu až dvou let byly hlášeny leukopenie (5 % oproti 2 %, stupně 3/4) a neutropenie (10 % oproti.4 %, stupně 3/4) s vyšší incidencí oproti pouhému sledování. Incidence trombocytopenie byla nízká (<1 %, stupně 3/4) a nelišila se mezi jednotlivými léčebnými rameny. V průběhu léčebného cyklu ve studiích s přípravkem MabThera v kombinaci s chemoterapií byly hlášeny leukopenie stupně 3/4 (R-CHOP 88 % oproti CHOP 79 %, R-FC 23 % oproti FC 12 %), neutropenie stupně 3/4 (R-CVP 24 % oproti CVP 14 %; R-CHOP 97 % oproti CHOP 88 %, R-FC 30 % oproti FC 19 % u dříve neléčených pacientů s CLL), pancytopenie stupně 3/4 (R-FC 3 % oproti FC 1 % u dříve neléčených pacientů s CLL) s obvykle vyšší četností v porovnání se samotnou chemoterapií. Vyšší incidence neutropenie u pacientů léčených přípravkem MabThera a chemoterapií však nebyla spojena s vyšší incidencí infekcí a infestací v porovnání s pacienty léčenými samotnou chemoterapií. Studie s intravenózní formou přípravku MabThera u dosud neléčené a relabující/refrakterní CLL prokázaly, že až u 25 % pacientů léčených R-FC byla neutropenie po léčbě přípravkem MabThera společně s FC prolongovaná (definováno jako počet neutrofilů, který zůstává nižší než 1x109/l mezi 24. dnem a 42. dnem po poslední dávce) nebo se vyskytla s opožděným nástupem (definováno jako počet neutrofilů nižších než 1x109/l později než 42 dnů po poslední dávce u pacientů bez předchozí prolongované neutropenie nebo u těch, u nichž před 42. dnem došlo k úpravě). Nebyly hlášeny žádné rozdíly v incidenci anémie. Některé případy pozdní neutropenie se objevily více než 4 týdny po poslední infuzi přípravku MabThera. Ve studii první linie u CLL došlo u pacientů ve stádiu C dle Bineta v rameni R-FC k více nežádoucím příhodám ve srovnání s ramenem FC (R-FC 83 % oproti FC 71 %). Ve studii s relabující/refrakterní CLL byla hlášena trombocytopenie stupně 3/4 u 11 % pacientů ve skupině R-FC ve srovnání s 9 % pacientů ve skupině FC.
Ve studiích s přípravkem MabThera u pacientů s Waldenstromovou makroglobulinemií byla po zahájení léčby pozorována přechodná zvýšení sérových hladin IgM, což může souviset s hyperviskozitou a souvisejícími příznaky. Přechodný vzestup IgM se obvykle v průběhu 4 měsíců vrátil k alespoň výchozí hodnotě.
Kardiovaskulární nežádoucí účinky
V průběhu klinických studií s monoterapií přípravkem MabThera byly hlášeny kardiovaskulární příhody u 18,8 % pacientů, přičemž nejčastěji hlášenými událostmi byly hypotenze a hypertenze.
V průběhu infuze byly hlášeny případy arytmie stupně 3 nebo 4 (včetně ventrikulární a supraventrikulární tachykardie) a angina pectoris. V průběhu udržovací léčby byla incidence kardiálních onemocnění stupně 3/4 srovnatelná u pacientů léčených přípravkem MabThera a u pacientů pouze sledovaných. Jako závažné nežádoucí události (včetně fibrilace síní, infarktu myokardu, levostranného komorového selhání a myokardiální ischémie) byly hlášeny kardiální události u 3 % pacientů léčených přípravkem MabThera ve srovnání s <1 % u sledování. Ve studiích hodnotících přípravek MabThera v kombinaci s chemoterapií byla incidence kardiálních arytmií stupně 3 a 4, především supraventrikulárních arytmií, jako je tachykardie a síňový flutter/fibrilace vyšší ve skupině R-CHOP (14 pacientů, 6,9 %) ve srovnání se skupinou CHOP (3 pacienti, 1,5 %). Všechny tyto arytmie se buď vyskytly v souvislosti s infuzí přípravku MabThera, nebo souvisely
s predisponujícími podmínkami, jako byly horečka, infekce, akutní infarkt myokardu nebo již existujících respiračních a kardiovaskulárních onemocnění. Nebyly pozorovány žádné rozdíly mezi skupinami R-CHOP a CHOP v incidenci jiných kardiálních událostí stupně 3 a 4 včetně srdečního selhání, infarktu myokardu a manifestace onemocnění koronárních tepen. U CLL byla celková incidence kardiálních onemocnění stupně 3 nebo 4 nízká jak ve studii první linie (4 % R-FC, 3 % FC), tak i ve studii u relabující/refrakterní CLL (4 % R-FC, 4 % FC).
Respirační systém
Byly hlášeny případy intersticiálního plicního onemocnění, některé končící úmrtím.
Neurologické poruchy
V průběhu léčebného období (indukční fáze léčby zahrnující R-CHOP pro maximálně 8 cyklů), čtyři pacienti (2 %) léčení ve skupině R-CHOP, všichni s kardiovaskulárními rizikovými faktory, prodělali během prvního léčebného cyklu tromboembolickou cerebrovaskulární příhodu. Ve výskytu dalších tromboembolických příhod nebyl mezi skupinami žádný rozdíl. Naopak, tři pacienti (1,5 %) v rameni CHOP měli cerebrovaskulární příhodu, u všech se objevila v období následného pozorování. U CLL byla celková incidence onemocnění nervového systému stupně 3 nebo 4 nízká jak ve studii první linie (4 % R-FC, 4 % FC), tak i ve studii u relabující/refrakterní CLL (3 % R-FC, 3 % FC).
Byly hlášeny případy syndromu posteriomí reverzibilní encefalopatie (PRES)/syndromu reverzibilní posteriomí leukoencefalopatie (RPLS). Známky a příznaky zahrnovaly zrakové poruchy, bolest hlavy, křeče a psychické poruchy, s nebo bez průvodní hypertenze. Diagnóza PRES/RPLS vyžaduje potvrzení zobrazovacím vyšetřením mozku. U hlášených případů byly zaznamenány rizikové faktory PRES/RPLS, které zahrnují průvodní onemocnění pacienta, hypertenzi, imunosupresivní léčbu a/nebo chemoterapii.
Gastrointestinální onemocnění
Gastrointestinální perforace, v některých případech vedoucí k úmrtí, byly pozorovány u pacientů, kteří dostávali přípravek MabThera v léčbě nehodgkinského lymfomu (NHL). Ve většině těchto případů byla MabThera podávána s chemoterapií.
Hladiny IgG
V klinických studiích hodnotících udržovací léčbu přípravkem MabThera u relabujícího/refrakterního folikulárního lymfomu byly po indukční léčbě střední hladiny IgG pod dolní hranicí normy (LLN)
(< 7 g/l) v rameni s pouhým sledováním i v rameni s přípravkem MabThera. V rameni se sledováním došlo následně k vzestupu střední hladiny IgG nad LLN, ale v rameni s přípravkem MabThera zůstaly nezměněny. Podíl pacientů se střední hladinou IgG pod LNN byl v rameni s přípravkem MabThera přibližně 60 % po celou dobu 2letého léčebného období, zatímco v rameni se sledováním tento podíl poklesl (36 % po 2 letech).
Poruchy kůže a podkožní tkáně
Velmi vzácně byly hlášeny toxická epidermální nekrolýza (Lyellův syndrom) a Stevens-Johnsonův syndrom, některé končící úmrtím.
Vybrané skupiny pacientů - Monoterapie přípravkem MabThera Starší pacienti (> 65 let):
Incidence nežádoucích účinků na lék všech stupňů a stupně 3/ 4 byla obdobná u starších pacientů v porovnání s mladšími pacienty (<65 let).
Pacienti s objemným (bulky) onemocněním:
U pacientů s objemným onemocněním byla zjištěna vyšší incidence nežádoucích účinků na lék stupně 3/ 4 ve srovnání s pacienty bez rozsáhlého nádorového postižení (25,6 % versus 15,4 %). Incidence jakéhokoli stupně nežádoucích účinků na lék byla mezi oběma skupinami obdobná.
Opakovaná léčba:
Procento pacientů hlásících nežádoucí účinek na lék po opětovném zahájení léčby dalšími cykly přípravku MabThera bylo podobné jako procento pacientů uvádějící nežádoucí účinek na lék po prvním podání přípravku (jakýkoliv stupeň a stupeň 3/4 nežádoucích účinků na lék).
Dílčí populace pacientů - kombinovaná léčba s přípravkem MabThera Starší pacienti (>65 let)
Incidence nežádoucích příhod týkajících se krve a lymfatického systému stupně 3/4 byla u starších pacientů s dosud neléčenou nebo relabující/refrakterní CLL vyšší ve srovnání s mladšími pacienty (<65 let).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Z klinických studií u lidí jsou dostupné omezené zkušenosti s podáním dávek vyšších než je schválená dávka intravenózního přípravku MabThera. Dosud nejvyšší intravenózní dávka přípravku MabThera testovaná u lidí je 5000 mg (2250 mg/m2), testovaná ve studii se zvyšováním dávek u pacientů s chronickou lymfocytámí leukemií. Nebyly zjištěny žádné další bezpečnostní signály.
U pacientů, u kterých se vyskytne předávkování, má být okamžitě přerušena infuze a mají být pečlivě sledováni.
V klinické studii SABRINA(BO22334) přípravku MabThera pro subkutánní podání byla třem pacientům s NHL nedopatřením podána subkutánní forma intravenózně až do výše maximální dávky rituximabu 2780 mg, a to bez žádných nežádoucích účinků.
Pacienti, u kterých se vyskytne předávkování nebo chybná medikace přípravkem MabThera, mají být pečlivě sledováni.
Po uvedení přípravku na trh bylo hlášeno pět případů předávkování přípravkem MabThera. Ve třech případech nebyly hlášeny žádné nežádoucí účinky. Dva nežádoucí účinky, které byly hlášeny, byly příznaky podobné chřipce (flu-like) při dávce 1,8 g rituximabu a fatální respirační selhání při dávce 2 g rituximabu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: protinádorové látky, monoklonální protilátky, ATC kód: L01XC02
Přípravek MabThera pro subkutánní podání obsahuje rekombinantní lidskou hyaluronidázu (rHuPH20), enzym používaný ke zvýšení disperze a absorpce současně podávaných látek, pokud je podávána subkutánně.
Rituximab se specificky váže na transmembránový antigen CD20, což je neglykosylovaný fosfoprotein vyskytující se na pre-B a zralých B-lymfocytech. Tento antigen je exprimován > 95 % všech nehodgkinských lymfomů původem z B buněk.
CD20 se nachází na normálních i maligních B-lymfocytech, není přítomen na hematopoetických kmenových buňkách, pro-B-buňkách, normálních plazmatických buňkách ani na jiných normálních tkáních. Antigen se po navázání protilátky neinternalizuje a není také uvolňován z povrchu buňky. CD20 necirkuluje v plazmě jako volný antigen a tedy nevzniká kompetice o navázání protilátek.
Rituximab se svým Fab fragmentem naváže na CD20 antigen na povrchu B-lymfocytů a prostřednictvím Fc domény může být zahájena efektorová imunitní reakce, která vede k lýze B-lymfocytů. Možné mechanizmy, kterými je lýza B-lymfocytů zprostředkována, zahrnují jednak cytotoxickou reakci vyvolanou účinkem komplementu (CDC), jejímž prvním krokem je vazba C1q a jednak protilátkami zprostředkovanou buněčnou cytotoxicitu (ADCC), která závisí na aktivaci jednoho či více Fcy receptorů na povrchu granulocytů, makrofágů a NK buněk. Rovněž bylo prokázáno, že vazba rituximabu na antigen CD 20 přítomný na B lymfocytech vyvolává buněčnou smrt navozením apoptózy.
Počet B-lymfocytů v periferní krvi se snižuje pod normu po podání první dávky přípravku MabThera. U pacientů léčených z důvodu hematologických malignit se objevila nová populace B buněk během 6 měsíců po léčbě a obvykle byl jejich normální počet obnoven během 12 měsíců po ukončení terapie, ačkoli u některých pacientů to může trvat déle (se střední dobou do znovuobjevení lymfocytů až 23 měsíců po indukční léčbě). U pacientů s revmatoidní artritidou byla po podání dvou infuzí 1000 mg přípravku MabThera v odstupu 14 dní pozorována bezprostřední deplece B lymfocytů v periferní krvi. Počet B lymfocytů v periferní krvi začal stoupat od 24. týdne a u většiny pacientů bylo pozorováno obnovení populace do 40. týdne, ať byl přípravek MabThera podáván jako monoterapie nebo v kombinaci s metotrexátem.
Klinické zkušenosti se subkutánní formou přípravku MabThera u chronické lvmfocvtámí leukemie
U pacientů s dosud neléčenou CLL byla provedena multicentrická, randomizovaná, otevřená studie s paralelními skupinami, fáze Ib, složená ze dvou částí, která zkoumala non-inferioritu farmakokinetického profilu společně s účinností a bezpečností subkutánní formy přípravku MabThera v kombinaci s chemoterapií.
Cílem 1. části bylo vybrat dávku subkutánní formy přípravku MabThera, u níž byly dosaženy srovnatelné nejnižší sérové (Ctrough) hladiny přípravku MabThera jako u intravenózní formy přípravku MabThera. Bylo zařazeno 64 pacientů s CLL v kterémkoli okamžiku jejich léčby intravenózní formou přípravku MabThera v kombinaci s chemoterapií. Pro 2. část studie byla vybrána dávka 1600 mg subkutánní formy přípravku MabThera.
Cílem 2. části bylo stanovit non-inferioritu u pozorovaných nejnižších Ctm..gh hladin mezi potvrzenou subkutánní dávkou přípravku MabThera a referenční intravenózní dávkou přípravku MabThera.
Do následujících dvou léčebných skupin bylo randomizováno celkem 176 pacientů s CLL:
• MabThera subkutánní (n= 88); 1. cyklus podání přípravku MabThera intravenózně 375 mg/m2 v kombinaci s chemoterapií a následující cykly (2-6) podávání přípravku MabThera subkutánně 1600 mg v kombinaci s chemoterapií.
• MabThera intravenózní (n= 88): 1. cyklus podání přípravku MabThera intravenózně
375 mg/m2 v kombinaci s chemoterapií následovaný až 5 cykly podávání přípravku MabThera intravenózně 500 mg/m2 v kombinaci s chemoterapií.
Četnosti odpovědí byly v obou ramenech podobné, přičemž četnost celkových odpovědí byla 80,7 % (95% interval spolehlivosti: 70,9; 88,3) u přípravku MabThera intravenózně a 85,2 % (95% interval spolehlivosti: 76,1; 91,9) u přípravku MabThera subkutánně. Bodové odhady četnosti úplné odpovědi byly 33,0 % (95% interval spolehlivosti: 23,3; 43,8) v rameni s intravenózním přípravkem MabThera a 26,1 % (95% interval spolehlivosti: 17,3; 36,6) v rameni se subkutánní formou. Celkově výsledky potvrzují, že subkutánní forma přípravku MabThera 1600 mg má srovnatelný profil přínosu/rizika jako intravenózní forma přípravku MabThera 500 mg/m2.
Imunogenita
Údaje z programu vývoje přípravku MabThera pro subkutánní podání naznačují, že tvorba protilátek proti rituximabu (HACA) je po subkutánním podání srovnatelná s jejich tvorbou po intravenózním podání. Ve studii SAWYER (BO25341) byla incidence léčbou indukovaných/zvýšených protilátek proti rituximabu podobná v obou léčebných ramenech; 6,7 % u intravenózního podání oproti 2,4 % u subkutánního podání. Incidence léčbou indukovaných/zvýšených protilátek proti rHuPH20, měřená pouze u pacientů v rameni se subkutánní léčbou, byla 10,6 %. Žádný z pacientů, kteří byli pozitivně testováni na přítomnost protilátek anti-rHuPH20, nebyl pozitivně testován na přítomnost neutralizujících protilátek.
Klinický význam rozvoje protilátek proti rituximabu či proti rHuPH20 po léčbě přípravkem MabThera pro subkutánní podání není znám.
Není zřejmý žádný zjevný vliv přítomnosti protilátek proti rituximabu nebo proti rHuPH20 na bezpečnost, účinnost nebo farmakokinetiku přípravku MabThera.
Klinické zkušenosti s přípravkem MabThera koncentrát pro infíizní roztok u chronické lymfocytární leukemie
Ve dvou otevřených, randomizovaných studiích bylo randomizováno celkem 817 dosud neléčených pacientů a 552 pacientů s relabující/refrakterní CLL k léčbě buď chemoterapií FC (fludarabin 25 mg/m2, cyklofosfamid 250 mg/m2, 1.-3. den) každé 4 týdny po dobu 6 cyklů nebo přípravkem MabThera v kombinaci s FC (R-FC). Přípravek MabThera byl v průběhu 1. cyklu podáván v dávce 375 mg/m2 den před chemoterapií a v dávce 500 mg/m2 1. den každého následujícího léčebného cyklu.
Pacienti byli ze studie u relabující/refraktemí CLL vyloučeni, pokud byli v minulosti léčeni monoklonálními protilátkami nebo pokud byli refrakterní (definováno jako neschopnost dosáhnout parciální remise po dobu alespoň 6 měsíců) vůči fludarabinu nebo jakémukoli nukleosidovému analogu. Analýza účinnosti byla provedena u celkem 810 pacientů (403 R-FC, 407 FC) ve studii léčby první linie (tabulka 2a a tabulka 2b) a u 552 pacientů (276 R-FC, 276 FC) ve studii s relabující/refraktemí CLL (tabulka 3).
Ve studii první linie léčby byl po střední době pozorování 48,1 měsíce medián PFS ve skupině R-FC 55 měsíců a ve skupině FC 33 měsíců (p < 0,0001, log-rank test). Analýza celkového přežití ukázala významnou prospěšnost léčby R-FC oproti samotné chemoterapii FC (p = 0,0319, log-rank test) (tabulka 2a). Prospěšnost z hlediska PFS byla konzistentně pozorovaná ve většině pacientských podskupin analyzovaných podle rizika onemocnění při zahájení (tj. stádia dle Bineta A-C) (tabulka 2b).
Tabulka 2a První linie léčby chronické lymfocytární leukemie
|
Parametr účinnosti |
Kaplan-Meierův odhad střední doby do události (měsíce) |
Redukce rizika | ||
|
FC (N = 409) |
R-FC (N=408) |
Log-Rank p hodnota | ||
|
Přežití bez progrese (PFS) |
32,8 |
55,3 |
<0,0001 |
45 % |
|
Celkové přežití |
NR |
NR |
0,0319 |
27 % |
|
Přežití bez události |
31,3 |
51,8 |
<0,0001 |
44 % |
|
Četnost odpovědi (CR, nPR, |
72,6 % |
85,8 % |
<0,0001 |
n.a. |
|
nebo PR) Četnosti CR |
16,9 % |
36,0 % |
<0,0001 |
n.a. |
|
Trvání odpovědi* |
36,2 |
57,3 |
<0,0001 |
44 % |
|
Přežití bez onemocnění (DFS)** |
48,9 |
60,3 |
0,0520 |
31 % |
|
Doba do nové léčby |
47,2 |
69,7 |
<0,0001 |
42 % |
Četnosti odpovědi a četnosti CR analyzované pomocí Chí-kvadrát testu. NR: nedosaženo; n.a.: nepoužitelné *: použitelné pouze u pacientů, kteří dosáhli CR, nPR, PR **: použitelné pouze u pacientů, kteří dosáhli CR
Přehled výsledků účinnosti pro přípravek MabThera společně s FC oproti samotné _FC - průměrná doba pozorování 48,1 měsíce__
Tabulka 2b Léčba první linie chronické lymfocytární leukemie
Poměry rizika přežití bez progrese podle stádia dle Bineta (ITT) - střední doba pozorování 48,1 měsíce ___
|
Přežití bez progrese (PFS) |
Počet pacientů |
Poměr rizik (95% CI) |
p-hodnota (Waldův test, neupraveno) | |
|
FC |
R-FC | |||
|
Stádium dle Bineta A |
22 |
18 |
0,39 (0,15; 0,98) |
0,0442 |
|
Stádium dle Bineta B |
259 |
263 |
0.52 (0.41: 0.66) |
<0,0001 |
|
Stádium dle Bineta C |
126 |
126 |
0,68 (0,49; 0,95) |
0,0224 |
CI: Interval spolehlivosti
Ve studii s relabující/refrakterní CLL bylo střední přežití bez progrese (primární cílový parametr)
30,6 měsíce ve skupině R-FC a 20,6 měsíce ve skupině FC (p=0,0002, log-rank test). Prospěšnost z hlediska PFS byla konzistentně pozorovaná v téměř všech pacientských podskupinách analyzovaných podle rizika onemocnění při zahájení. Ve skupině R-FC bylo hlášeno mírné, ale nevýznamné zlepšení celkového přežití oproti rameni FC.
U pacientů s relabujícím nebo refrakterním onemocněním nejsou dostupná žádná PK/klinická data.
Tabulka 3 Léčba relabující/refrakterní chronické lymfocytární leukemie - přehled výsledků účinnosti pro přípravek MabThera společně s FC oproti samotné FC (střední doba _pozorování 25,3 měsíce)__
|
Parametr účinnosti |
Kaplan-Meierův odhad střední doby do |
Redukce | ||
|
události (měsíce) |
rizika | |||
|
FC |
R-FC |
Log-Rank | ||
|
(N = 276) |
(N=276) |
p hodnota | ||
|
Přežití bez progrese (PFS) |
20,6 |
30,6 |
0,0002 |
35 % |
|
Celkové přežití |
51,9 |
NR |
0,2874 |
17 % |
|
Přežití bez události |
19,3 |
28,7 |
0,0002 |
36 % |
|
Četnost odpovědi (CR, nPR, nebo PR) |
58,0 % |
69,9 % |
0,0034 |
n.a. |
|
Četnosti CR |
13,0 % |
24,3 % |
0,0007 |
n.a. |
|
Trvání odpovědi * |
27,6 |
39,6 |
0,0252 |
31 % |
|
Přežití bez onemocnění (DFS)** |
42,2 |
39,6 |
0,8842 |
-6 % |
|
Doba do nové léčby CLL |
34,2 |
NR |
0,0024 |
35 % |
Četnosti odpovědi a četnosti CR analyzované pomocí Chí-kvadrát testu.
*: použitelné pouze u pacientů, kteří dosáhli CR, nPR, PR NR: nedosaženo; n.a.: nepoužitelné
**: použitelné pouze u pacientů, kteří dosáhli CR
Výsledky dalších podpůrných studií používajících přípravek MabThera v kombinaci s dalšími chemoterapeutickými režimy (včetně CHOP, FCM, PC, PCM, bendamustinu a kladribinu) v léčbě pacientů s dosud neléčenou a/nebo relabující/refrakterní CLL také prokázaly vysoké četnosti celkových odpovědí s prospěšností z hlediska četností PFS, i když s mírně vyšší toxicitou (zvláště myelotoxicitou). Tyto studie podporují použití přípravku MabThera s jakoukoli chemoterapií.
Údaje u přibližně 180 pacientů předléčených přípravkem MabThera prokázaly klinickou prospěšnost (včetně CR) a odůvodňují opakování léčby přípravkem MabThera.
Pediatrická populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s rituximabem u všech podskupin pediatrické populace s chronickou lymfocytární leukemií. Informace o použití u dětí viz bod 4.2.
5.2 Farmakokinetické vlastnosti
Absorpce
Přípravek MabThera byl ve fixní dávce 1600 mg podáván subkutánně po dobu 5 cyklů ve 4týdenních intervalech následujících po prvním cyklu intravenózní formy přípravku MabThera u dosud neléčených pacientů s CLL v kombinaci s chemoterapií (fludarabin a cyklofosfamid (FC)). Sérová hladina přípravku MabThera Cmax byla v rameni se subkutánní léčbou v 6. cyklu nižší než v rameni s intravenózní léčbou, s hodnotami geometrického průměru (CV %) 202 (36,1) pg/ml a 280 (24,6) pg/ml s výsledným poměrem geometrických průměrů (Cmax, SC/Cmax, iV) 0,719 (90% interval spolehlivosti: 0,653; 0,792). Geometricky průměrný tmax byl ve skupině se subkutánním přípravkem MabThera přibližně 3 dny ve srovnání s tmax, který se ve skupině s intravenózním přípravkem MabThera vyskytuje při nebo těsně na konci infuze. Geometricky průměrné nejnižší hodnoty Ctrough (CV%) v 5. cyklu (před podáním dávky v 6. cyklu) byly ve skupině se subkutánním přípravkem MabThera vyšší než ve skupině s intravenózním přípravkem MabThera; 97,5 pg/ml (42,6) oproti
61,5 pg/ml (63,9) v tomto pořadí s výsledným poměrem upravených geometrických průměrů [90% interval spolehlivosti] 1,53 [1,27-1,85]. Obdobně byly hodnoty geometricky průměrné AUC (CV %) v 6. cyklu vyšší ve skupině se subkutánním přípravkem MabThera než ve skupině s intravenózním přípravkem MabThera; 4088 pg^den/ml (34,2) oproti 3630 pg^den/ml (32,8) v tomto pořadí s výsledným poměrem upravených geometrických průměrů [90% interval spolehlivosti] 1,10 [0,98-1,24].
Podle populační farmakokinetické analýzy studie BO25341 (SAWYER) byla odhadnutá absolutní biologická dostupnost 68,4%.
Distribuce/Eliminace
Odhadovaný poločas subkutánní formy přípravku MabThera 1600 mg je 30 dnů, odhadovaná clearance je 0,22 l/den a distribuční objem v centrálním kompartmentu je 4,65 l.
Zvláštní populace
Jak je u monoklonálních protilátek typické, záležely farmakokinetické parametry rituximabu na velikosti tělesných rozměrů. Všechny parametry clearance a objemu se zvyšovaly s BSA. Centrální objem byl navíc mírně (9 %) nižší u žen ve srovnání s muži. Absorpční parametry subkutánní formy se snižovaly se stoupajícím BMI. Podmíněné simulace, které shrnovaly dopad závislostí všech tělesných rozměrů na expozici rituximabu prokázaly, že přestože fixní dávkování subkutánně vede k vyšším rozdílům v expozici (Ctrough a AUCT) mezi pacienty s malými a velkými tělesnými rozměry ve srovnání s intravenózním dávkováním upraveným podle hmotnosti, umožňuje zachovat hodnoty Ctrough a AUCT ve skupinách všech tělesných rozměrů na hladinách, které nejsou nižší než hladiny dosažené při intravenózním podávání, a tedy dosahují přinejmenším stejné cílové saturace jako při intravenózním podání. U pacientů vážících > 90 kg byly hodnoty Ctrough stejné u intravenózních i subkutánních režimů. U pacientů vážících mezi 60-90 kg a < 60 kg, byly průměrné hodnoty Ctrough po intravenózním podání přibližně o 16 % a 34 % nižší ve srovnání se subkutánním režimem. Obdobně byly u pacientů ve vysokém tercilu BSA hodnoty Ctrough stejné u intravenózních i subkutánních režimů. U pacientů ve středních a dolních tercilech BSA byly průměrné hodnoty Ctrough po intravenózním podání přibližně o 12 % a 26 % nižší ve srovnání se subkutánním režimem.
Kromě závislosti na tělesných rozměrech byla u pacientů s větší výchozí velikostí nádoru vyšší na čase závislá clearance, což odpovídá eliminaci zprostředkované cílovým místem („target-mediated“). Vyšší na čase závislá clearance u pacientů s větší náloží onemocnění by vedla k nižší úvodní expozici a delšímu času potřebnému pro dosažení stejné expozice jako u pacientů s nízkou náloží onemocnění.
5.3 Předklinické údaje vztahující se k bezpečnosti
Rituximab se ukázal jako látka vysoce specifická k CD20 antigenu na B-lymfocytech. Studie prováděné na opicích cynomolgus neprokázaly jiný druh toxicity než očekávanou farmakologickou depleci B-lymfocytů v periferní krvi a v lymfatických tkáních.
Studie vývojové toxicity byly provedeny u opic rodu cynomolgus při podávání dávek do 100 mg/kg (20.-50. den březosti) a neprokázaly žádnou embryotoxicitu pro plod, která by byla spojena s rituximabem. V závislosti na dávce přípravku však byla pozorována farmakologická deplece B lymfocytů v lymfatických orgánech plodu, která přetrvávala postnatálně a byla doprovázena snížením hladiny IgG u novorozených opic. Počet B lymfocytů se u těchto zvířat vrátil k normální hodnotě během 6 měsíců po narození a nedošlo ke snížené reakci na imunizaci.
Standardní testy pro vyšetření mutagenity nebyly prováděny, neboť tyto testy nejsou pro tento typ molekuly relevantní. Dlouhodobé studie na zvířatech, které by měly určovat karcinogenní potenciál rituximabu, nebyly provedeny.
Nebyly provedeny konkrétní studie stanovující účinky rituximabu nebo rHuPH20 na fertilitu.
V obecných studiích toxicity na opicích cynomolgus nebyly pozorovány žádné škodlivé účinky na reprodukční orgány samců či samic. Navíc nebyly prokázány žádné účinky rHuPH20 na kvalitu spermatu.
V embryofetálních vývojových studiích u myší, rHuPH20 způsobil snížení hmotnosti plodu a ztrátu implantací vajíčka při systémových expozicích dostatečně převyšujících terapeutické expozice u lidí. Neexistují žádné důkazy o dysmorfogenezi (tj. teratogenitě) v důsledku systémové expozice rHuPH20.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Biosyntetická lidská hyaluronidáza Histidin
Monohydrát histidin-hydrochloridu
Dihydrát trehalózy
Methionin
Polysorbát 80
Voda na injekci
6.2 Inkompatibility
Mezi přípravkem MabThera pro subkutánní podání a polypropylenovým nebo polykarbonátovým materiálem injekční stříkačky nebo transferem z nerezové oceli a injekčními jehlami a polyetylenovou Luer kuželovitou zátkou nebyla pozorována inkompatibilita.
6.3 Doba použitelnosti
Neotevřená injekční lahvička 30 měsíců
Po prvním otevření
Po přenosu roztoku přípravku MabThera pro subkutánní podání z injekční lahvičky do injekční stříkačky je roztok fyzikálně a chemicky stabilní po dobu 48 hodin při teplotě 2 °C - 8 °C a následně pak 8 hodin při 30 °C při difúzním denním světle.
Z mikrobiologického hlediska má být přípravek použit okamžitě. Není-li použit okamžitě, příprava má být provedena za kontrolovaných a validovaných aseptických podmínek. Doba a podmínky uchovávání přípravku před použitím jsou v zodpovědnosti uživatele.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C). Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Podmínky uchovávání tohoto léčivého přípravku po jeho prvním otevření jsou uvedeny v bodě 6.3.
6.5 Druh obalu a obsah balení
Injekční lahvička z bezbarvého skla typu I, s pryžovou zátkou s hliníkovým uzávěrem a modrým plastovým „flip-off“ diskem, obsahující 1600 mg/13,4 ml rituximabu.
Jedno balení obsahuje 1 injekční lahvičku.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Přípravek MabThera je dodáván ve sterilních, nepyrogenních lahvičkách na jedno použití bez konzervačních látek. Injekční lahvička obsahuje odlepovací nálepku, na které je uvedena síla, cesta podání a indikace. Tato nálepka má být z injekční lahvičky před použitím odstraněna a přilepena na
injekční stříkačku. Následující body musí být přesně dodržovány, pokud jde o používání a likvidaci injekčních stříkaček a jiných ostrých předmětů:
• Jehly a injekční stříkačky nesmí být nikdy znovu použity
• Všechny použité jehly a injekční stříkačky vložte do kontejneru na ostré předměty (kontejner odolný proti propíchnutí).
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/98/067/004
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 2. června 1998
Datum posledního prodloužení registrace: 2. června 2008
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu/
A. VÝROBCI BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCI BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCI ODPOVĚDNÍ ZA
PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce biologické léčivé látky
Genentech, Inc.
1000 New Horizons Way Vacaville, CA 95688 USA
Genentech, Inc.
1 Antibody Way Oceanside, CA 92056 5802 USA
Samsung BioLogics 125, Cheomdan-daero Yeonsu-gu, Incheon,
Korea 21987
Název a adresa výrobce odpovědného za propouštění šarží
Roche Pharma AG Emil-Barell-Str. 1 D-79639, Grenzach-Wyhlen Německo
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis s omezením (viz příloha I: Souhrn údajů o přípravku, bod 4.2).
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
• Pravidelně aktualizované zprávy o bezpečnosti
Držitel rozhodnutí o registraci předkládá pravidelně aktualizované zprávy o bezpečnosti pro tento léčivý přípravek v souladu s požadavky uvedenými v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a zveřejněném na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ
LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
Pokud se shodují data předložení aktualizované zprávy o bezpečnosti (PSUR) a aktualizovaného RMP, je možné je předložit současně.
• Další opatření k minimalizaci rizik
Revmatoidní artritida:
Držitel rozhodnutí o registraci musí zajistit, že všem lékařům, kteří budou předepisovat přípravek MabThera, jsou poskytnuty následující materiály:
Informace o přípravku Informace pro lékaře Informace pro pacienta Karta pro pacienta
Informace o přípravku MabThera určená pro lékaře má obsahovat následující základní údaje:
• Nutnost pečlivého sledování v průběhu podání v prostředí, kde jsou prostředky k resuscitaci ihned dostupné
• Před zahájením léčby přípravkem MabThera je nutnost kontroly z důvodu infekce, imunosuprese, předchozí/současné medikace i nedávno užívané, která by mohla ovlivnit imunitní systém, nebo plánované očkování
• Nutnost pečlivého monitorování pacienta z důvodu infekce, zvláště pak PML v průběhu a po léčbě přípravkem MabThera
• Podrobné informace o riziku PML, potřebu včasné diagnózy PML a odpovídající opatření u diagnózy PML
• Nutnost informovat pacienty o riziku infekcí a PML včetně upozornění na příznaky a nutnost ihned kontaktovat lékaře, jakmile se kterýkoliv z těchto příznaků objeví
• Nutnost poskytnout pacientům při každé infuzi Kartu pro pacienta
Informace pro pacienta léčeného přípravkem MabThera má obsahovat následující základní údaje:
• Podrobné informace o riziku infekcí a PML
• Informace o známkách a příznacích infekcí, obzvláště PML a nutnost ihned kontaktovat lékaře, jakmile se kterékoliv příznaky objeví
• Důležitost poskytnutí těchto informací partnerovi nebo poskytovateli péče
• Informace o Kartě pro pacienta
Karta pro pacienta s jiným než onkologickým onemocněním léčeného přípravkem MabThera má obsahovat následující základní údaje:
• Nezbytnost mít kartu stále u sebe a ukázat ji každému ošetřujícímu lékaři nebo zdravotnickému personálu
• Upozornění na riziko infekcí a PML, včetně příznaků
• Nezbytnost kontaktovat ošetřujícího lékaře, jakmile se příznaky objeví
Informace pro lékaře, informace pro pacienta a Karta pro pacienta musí být před distribucí odsouhlaseny národní autoritou.
Subkutánní podání:
Všichni zdravotničtí pracovníci podávající přípravek MabThera pro subkutánní podání obdrží edukační materiály (« návod krok za krokem » a « srovnávací karta »), aby se snížilo riziko používání mimo předepsanou indikaci a chyby v podání.
• Povinnost uskutečnit poregistrační opatření
Držitel rozhodnutí o registraci uskuteční v daném termínu níže uvedená opatření:
|
Popis |
Termín splnění |
|
Podání hlášení z klinických studií BO22334 a BO25341 včetně hlášení o dlouhodobé bezpečnosti ve vztahu k BSA (jako opatření při změně expozice) a k pohlaví následovně: | |
|
Závěrečné hlášení klinické studie BO22334a (obě fáze) |
Q3/2018 |
|
Závěrečné hlášení klinické studie BO25341a (obě části) |
Q4/2018 |
|
a Hlášení primárního cílového parametru analýzy (Ctrough non-inferiority) ve 2. části a dostupných údajů o bezpečnosti a imunogenitě z obou částí probíhající studie. | |
|
Údaje o imunogenitě ze studií BO22334/SABRINA a BO25341/SAWYER budou vyhodnocovány průběžně. Hlášení o imunogenitě z obou fází studií BO22334/SABRINA a BO25341/SAWYER mají být předložena ve Q4/2016 a dle plánu ve Q3/2018 a Q4/2018. |
do konce Q4/2016 (hlášení o imunogenitě) ve Q3 a Q4/2018 (viz výše) |
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
MabThera 100 mg koncentrát pro infuzní roztok Rituximabum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
1 injekční lahvička obsahuje 10 mg/ml rituximabum.
3. SEZNAM POMOCNÝCH LÁTEK
Natrium-citrát, polysorbát 80, chlorid sodný, hydroxid sodný, kyselina chlorovodíková, voda na injekce.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Koncentrát pro infuzní roztok 100 mg / 10 ml
2 injekční lahvičky o objemu 10 ml
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pro intravenózní podání po naředění
Před použitím si přečtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem
11 NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/98/067/001
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
<Nevyžaduje se - odůvodnění přijato>
17. JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD
2D čárový kód s jedinečným identifikátorem.
18. JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM
PC:
SN:
NN:
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU NÁLEPKA NA INJEKČNÍ LAHVIČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
MabThera 100 mg koncentrát pro infuzní roztok
Rituximabum
i.v.
2. ZPŮSOB PODÁNÍ
Pro intravenózní podání po naředění
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
Injekční lahvička 10 ml (10 mg/ml) 100 mg / 10 ml
6. JINÉ
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
MabThera 500 mg koncentrát pro infuzní roztok Rituximabum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
1 injekční lahvička obsahuje 10 mg/ml rituximabum.
3. SEZNAM POMOCNÝCH LÁTEK
Natrium-citrát, polysorbát 80, chlorid sodný, hydroxid sodný, kyselina chlorovodíková, voda na injekce.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Koncentrát pro infuzní roztok 1 injekční lahvička o objemu 50 ml 500 mg / 50 ml
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pro intravenózní podání po naředění
Před použitím si přečtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/98/067/002
13. ČÍSLO ŠARŽE
c.s.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
<Nevyžaduje se - odůvodnění přijato>
17. JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD
2D čárový kód s jedinečným identifikátorem.
18. JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM
PC:
SN:
NN:
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU NÁLEPKA NA INJEKČNÍ LAHVIČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
MabThera 500 mg koncentrát pro infuzní roztok
Rituximabum
i.v.
2. ZPŮSOB PODÁNÍ
Pro intravenózní podání po naředění
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
Injekční lahvička 50 ml (10 mg/ml) 500 mg / 50 ml
6. JINÉ
TEXT KARTY PRO PACIENTA S JINÝM NEŽ ONKOLOGICKÝM ONEMOCNĚNÍM
Karta pacienta s neonkologickým onemocněním léčeného přípravkem MABTHERA (rituximab)
Proč jsem dostal(a) tuto kartu?
U tohoto léčivého přípravku se může projevit vyšší náchylnost k infekcím. Tato karta Vám říká:
• Čemu musíte věnovat pozornost, než začnete přípravek MabThera užívat
• Jaké jsou příznaky infekce
• Co máte dělat, jestliže se u Vás infekce projeví.
Na zadní straně této karty je také uvedeno Vaše jméno, jméno lékaře a jeho telefonní číslo.
Co mám dělat s touto kartou?
• Tuto kartu mějte vždy u sebe -např.v peněžence.
• Ukažte tuto kartu každému lékaři, zdravotní sestře nebo zubaři, které navštívíte - nejen svému ošetřujícímu specialistovi, který Vám předepisuje přípravek MabThera.
Noste tuto kartu u sebe po dobu 2 let po poslední dávce přípravku MabThera. To je z důvodu, že může dojít k projevům nežádoucích účinků i několik měsíců po ukončení léčby.
Kdy nemám užívat přípravek MabThera?
Neužívejte přípravek MabThera, pokud trpíte závažnou infekcí nebo máte závažné problémy s imunitním systémem.
Upozorněte svého lékaře nebo zdravotní sestru, pokud užíváte nebo jste v minulosti užíval(a) léky, které by mohly ovlivnit Váš imunitní systém, včetně chemoterapie.
Jaké jsou příznaky infekce?
Dávejte si pozor na následující možné příznaky infekce:
• Horečka nebo přetrvávající kašel
• Úbytek hmotnosti_
Co dalšího musím vědět?
Vzácně může přípravek MabThera způsobit závažnou mozkovou infekci, která se nazývá „progresivní multifokální leukoencefalopatie (PML)“. Ta může vést k úmrtí.
• Příznaky PML zahrnují:
-Zmatenost, ztrátu paměti nebo poruchy myšlení
-Ztrátu rovnováhy nebo změna ve způsobu, jak budete chodit nebo mluvit
-Menší síla nebo slabost na jedné straně Vašeho těla
-Rozmazané vidění nebo ztráta zraku.
V případě, že se u Vás projeví kterýkoli z těchto příznaků, informujte okamžitě lékaře či zdravotní sestru. Také je informujte o Vaší léčbě přípravkem MabThera.
Kde mohu získat více informací?
Více údajů naleznete v příbalové informaci přípravku MabThera.
Datum zahájení léčby a kontaktní údaje
Datum poslední infuze:_
Datum první infuze:_
Jméno pacienta:_
Jméno lékaře:_
Kontakt na lékaře:_
Ujistěte se, že máte s sebou při každé návštěvě lékaře seznam všech ostatních léků, které užíváte.
Pokud máte jakékoli otázky týkající se této karty, zeptejte se, prosím, svého lékaře nebo zdravotní sestry.
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků Podrobnosti o hlášení najdete na: http://www.olecich.cz/hlaseni-pro-sukl/nahlasit-nezadouci-ucinek Adresa pro zasílání je: Státní ústav pro kontrolu léčiv, oddělení farmakovigilance, Šrobárova 48, Praha 10, 100 41, email:
|
• Bolest bez poranění | |
|
• Celkově se nebudete cítit dobře, apatie. | |
|
V případě, že se u Vás projeví kterýkoli | |
|
z těchto příznaků, informujte okamžitě | |
|
lékaře či zdravotní sestru. | |
|
Také je informujte o Vaší léčbě | |
|
přípravkem MabThera. |
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
MabThera 1400 mg subkutánní injekční roztok Rituximabum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
1 injekční lahvička obsahuje rituximabum 1400 mg/11,7 ml.
3. SEZNAM POMOCNÝCH LÁTEK
Biosyntetická lidská hyaluronidáza Histidin
Monohydrát histidin-hydrochloridu
Dihydrát trehalózy
Methionin
Polysorbát 80
Voda na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční roztok 1400 mg / 11,7 ml 1 injekční lahvička
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pouze pro subkutánní podání
Před použitím si přečtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
Uchovávejte v chladničce (2 °C - 8 °C). Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem
10 ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11 NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/98/067/003 13 ČÍSLO ŠARŽE
č.š.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
<Nevyžaduje se - odůvodnění přijato>
17. JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD
2D čárový kód s jedinečným identifikátorem.
18. JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM
PC:
SN:
NN:
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU NÁLEPKA NA INJEKČNÍ LAHVIČKU
1 NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
MabThera 1400 mg subkutánní injekční roztok Rituximabum
subkutánní
2. ZPŮSOB PODÁNÍ
Pouze pro subkutánní podání
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1400 mg / 11,7 ml
6. JINÉ
Informace uvedené na odlepovací nálepce
MabThera 1400 mg Rituximabum
1400 mg/11,7 ml
s.c. u Nehodgkinského lymfomu
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU KRABIČKA
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
MabThera 1600 mg subkutánní injekční roztok Rituximabum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
1 injekční lahvička obsahuje rituximabum 1600 mg/13,4 ml.
3. SEZNAM POMOCNÝCH LÁTEK
Biosyntetická lidská hyaluronidáza Histidin
Monohydrát histidin-hydrochloridu
Dihydrát trehalózy
Methionin
Polysorbát 80
Voda na injekci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Injekční roztok 1600 mg / 13,4 ml 1 injekční lahvička
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pouze pro subkutánní podání
Před použitím si přečtěte příbalovou informaci
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do:
Uchovávejte v chladničce (2 °C - 8 °C). Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem
10 ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11 NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/98/067/004 13 ČÍSLO ŠARŽE
č.š.:
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
<Nevyžaduje se - odůvodnění přijato>
17. JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD
2D čárový kód s jedinečným identifikátorem.
18. JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM
PC:
SN:
NN:
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU NÁLEPKA NA INJEKČNÍ LAHVIČKU
1 NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
MabThera 1600 mg subkutánní injekční roztok Rituximabum
subkutánní
2. ZPŮSOB PODÁNÍ
Pouze pro subkutánní podání
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1600 mg / 13,4 ml
6. JINÉ
Informace uvedené na odlepovací nálepce
MabThera 1600 mg Rituximabum
1600 mg/13,4 ml
s.c. u chronické lymfocytární leukemie
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro pacienta
MabThera 100 mg koncentrát pro infuzní roztok
rituximabum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek MabThera a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek MabThera používat
3. Jak se přípravek MabThera podává
4. Možné nežádoucí účinky
5. Jak přípravek MabThera uchovávat
6. Obsah balení a další informace
1. Co je přípravek MabThera a k čemu se používá
Co je přípravek MabThera
Přípravek MabThera obsahuje léčivou látku „rituximab“. To je zvláštní druh bílkoviny nazývaný „monoklonální protilátka“. Váže se na povrch jednoho typu bílých krvinek nazývaných „B lymfocyty“. Po vazbě na povrch této buňky, rituximab navodí její zánik.
K čemu se přípravek MabThera používá
Přípravek MabThera se používá k léčbě několika různých onemocnění u dospělých. Lékař Vám může přípravek MabThera předepsat k léčbě:
a) nehodgkinského lymfomu
To je onemocnění lymfatické tkáně (část imunitního systému), která ovlivňuje jeden typ bílých krvinek nazývaných B lymfocyty.
Přípravek MabThera může být podán samostatně nebo s jinými dalšími léky nazývanými „chemoterapeutika“.
U pacientů, u kterých je léčba účinná, může být přípravek MabThera používán v udržovací léčbě po dobu 2 let po dokončení úvodní léčby.
b) chronické lymfocytární leukemie
Chronická lymfocytární leukemie (CLL) je nejčastější formou leukemie u dospělých. CLL postihuje zejména lymfocyty, B-buňky, které pocházejí z kostní dřeně a vyvíjejí se v lymfatických uzlinách. Pacienti s CLL mají příliš mnoho abnormálních lymfocytů, které se hromadí zejména v kostní dřeni a krvi. Růst těchto abnormálních B-lymfocytů je příčinou příznaků, které můžete pociťovat. Přípravek MabThera v kombinaci s chemoterapií ničí tyto buňky, které jsou postupně odstraňovány z organismu pomocí biologických mechanismů.
c) revmatoidní artritidy
Přípravek MabThera se používá k léčbě revmatoidní artritidy. Revmatoidní artritida je onemocnění kloubů. B lymfocyty se podílí na vzniku některých příznaků, které se u Vás projevují. Přípravek MabThera se používá k léčbě revmatoidní artritidy u pacientů, kteří již podstoupili jinou léčbu, která však přestala být účinná, neúčinkovala dostatečně nebo způsobovala nežádoucí účinky. Přípravek MabThera se obvykle používá v kombinaci s dalším lékem zvaným metotrexát.
Přípravek MabThera zpomaluje poškození kloubů, které způsobuje revmatoidní artritida, a zlepšuje schopnost provádět obvyklé denní aktivity.
Nejlepší odpověď na léčbu přípravkem MabThera byla pozorována u pacientů, kteří měli pozitivní krevní testy na revmatoidní faktor (RF) a/nebo protilátky proti bílkovině citrulinu (anti-CCP). Oba testy jsou u pacientů s revmatoidní artritidou běžně pozitivní a pomáhají k potvrzení diagnózy.
d) granulomatózy s polyangiitidou nebo mikroskopické polyangiitidy
Přípravek MabThera se používá k navození remise u granulomatózy s polyangiitidou (dříve nazývané Wegenerova granulomatóza) nebo mikroskopické polyangiitidy; podává se v kombinaci s kortikosteroidy. Granulomatóza s polyangiitidou a mikroskopická polyangiitida jsou dvě formy zánětlivého onemocnění krevních cév, které postihuje převážně cévy plic a ledvin, ale může postihnout i cévy jiných orgánů. U těchto onemocnění hrají roli i B lymfocyty.
2. Čemu musíte věnovat pozornost, než začnete přípravek MabThera používat
Nepoužívejte přípravek MabThera pokud:
• jste alergický(á) na rituximab, na jiné proteiny podobného typu nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6)
• máte v současnosti závažnou aktivní infekci
• máte oslabenou funkci imunitního systému
• máte závažné srdeční selhání nebo závažné nekontrolované srdeční onemocnění a máte revmatoidní artritidu, granulomatózu s polyangiitidou nebo mikroskopickou polyangiitidu.
Nepoužívejte přípravek MabThera, pokud se Vás cokoliv z výše uvedeného týká. Pokud si nejste jistý(á), zeptejte se svého lékaře, lékárníka nebo zdravotní sestry dříve, než Vám bude přípravek MabThera podán.
Upozornění a opatření
Předtím, než Vám bude podán přípravek MabThera, poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou, pokud:
• jste někdy měl(a) nebo možná právě máte žloutenku. To je proto, že v některých případech by přípravek MabThera mohl znovu vyvolat žloutenku typu B (hepatitidu B), která může velmi vzácně vést k úmrtí. U pacientů s anamnézou hepatitidy B musí lékař pečlivě sledovat příznaky aktivní hepatitidy B.
• jste někdy trpěl(a) onemocněním srdce (jako je angina, palpitace nebo selhání srdce) nebo pokud jste někdy měl(a) obtíže s dýcháním.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán. Lékař Vám bude muset během léčby přípravkem MabThera věnovat zvláštní péči.
Máte-li revmatoidní artritidu, granulomatózu s polyangiitidou nebo mikroskopickou polyangiitidu, informujte lékaře
• jestliže si myslíte, že máte infekční onemocnění, dokonce i v případě lehkého nachlazení. Buňky, které jsou likvidovány přípravkem MabThera, pomáhají organismu bojovat s infekcemi, a proto byste během léčby přípravkem MabThera mohl(a) dostat infekci. Pokud infekcemi trpíte často anebo mají těžký průběh, řekněte to, prosím, rovněž svému lékaři.
• jestliže je pravděpodobné, že budete v blízké budoucnosti potřebovat nějaké očkování, včetně očkování před odjezdem do ciziny. Některé očkovací látky by neměly být aplikovány současně s přípravkem MabThera nebo v měsících, kdy se přípravkem MabThera léčíte. Před léčbou přípravkem MabThera lékař zkontroluje, zda byste neměl(a) nějaké očkování dostat.
Děti a dospívající
Poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán, pokud jste Vy nebo Vaše dítě mladší 18 let. To je z důvodu, že není k dispozici mnoho informací o používání přípravku MabThera u dětí a dospívajících.
Další léčivé přípravky a přípravek MabThera
Informujte svého lékaře, lékárníka nebo zdravotní sestru o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. To se týká i léků, které jsou dostupné bez lékařského předpisu a rostlinných přípravků. Důvodem je, že přípravek MabThera může ovlivňovat způsob účinku některých dalších léků. Stejně tak ostatní léky mohou ovlivňovat účinek přípravku MabThera.
Konkrétně, informujte svého lékaře:
• jestliže užíváte léky na vysoký krevní tlak. Můžete být požádán(a), abyste tyto léky neužíval(a) 12 hodin předtím, než Vám bude podán přípravek MabThera. To je proto, že u některých osob dochází během podání přípravku MabThera k poklesu krevního tlaku.
• jestliže jste v minulosti užíval(a) léky, které mohou ovlivnit Váš imunitní systém - jako jsou chemoterapeutika nebo imunosupresiva.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán.
Těhotenství a kojení
Musíte sdělit svému lékaři nebo zdravotní sestře, že jste těhotná, nebo že si nejste jistá, zda nejste těhotná, nebo že zamýšlíte otěhotnět. Přípravek MabThera je totiž protilátka, která může procházet placentou a ovlivnit dítě.
Pokud byste mohla otěhotnět, musíte Vy i Váš partner během léčby přípravkem MabThera a ještě 12 měsíců po jejím ukončení používat účinné antikoncepční prostředky.
Nekojte během Vaší léčby přípravkem MabThera. Nekojte také 12 měsíců po ukončení Vaší poslední léčby přípravkem MabThera. Přípravek MabThera může procházet do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Není známo, zda přípravek MabThera ovlivňuje schopnost řídit, používat jakékoli přístroje nebo obsluhovat stroje.
3. Jak se přípravek MabThera podává Jak se přípravek podává
Přípravek MabThera Vám bude podávat Váš lékař nebo zdravotní sestra, kteří mají zkušenosti s užíváním této léčby. Budou Vás pečlivě sledovat během podání tohoto léčivého přípravku. Je to pro případ, že by se u Vás projevily nežádoucí účinky.
Vždy na začátku léčby Vám přípravek MabThera bude podán“ kapačkou“ (intravenózní infuze).
Léčivé přípravky podávané před každým podáním přípravku MabThera
Před podáním přípravku MabThera Vám budou podány další léky (premedikace) k zabránění nebo ke snížení možného rizika nežádoucích účinků.
Kolik a jak často budete dostávat Vaši léčbu
a) Pokud jste léčen(a) z důvodu nehodgkinského lymfomu
• Dostáváte-li pouze přípravek MabThera samotný
Přípravek MabThera Vám bude podáván jedenkrát týdně po dobu 4 týdnů. Léčbu přípravkem MabThera lze opakovat.
• Dostáváte-li přípravek MabThera v kombinaci s chemoterapií
Přípravek MabThera Vám bude podáván ve stejný den jako chemoterapie. Většinou je podáván každé 3 týdny, celkem 8krát.
• Pokud budete dobře reagovat na léčbu, může Vám být přípravek MabThera podáván v rámci udržovací léčby každé 2 nebo 3 měsíce po dobu 2 let.
V závislosti na tom, jak budete reagovat na tento léčivý přípravek, Váš lékař může toto dávkování změnit.
b) Pokud jste léčen(a) z důvodu chronické lymfocytární leukemie
Jste-li léčen(a) přípravkem MabThera v kombinaci s chemoterapií, budete dostávat infuzi s přípravkem MabThera v den 0 1. cyklu léčby a potom v den 1 každého z celkem 6 cyklů léčby. Jeden cyklus léčby má 28 dní. Chemoterapie má být podávána po infuzi přípravku MabThera. Lékař rozhodne, zda budete dostávat průvodní podpůrnou léčbu.
c) Pokud jste léčen(a) z důvodu revmatoidní artritidy
Jeden cyklus léčby sestává ze dvou infuzí, které jsou podávány v odstupu alespoň 2 týdnů. Opakování cyklů léčby přípravkem MabThera je možné. Na základě příznaků a projevů Vaší nemoci lékař rozhodne, zda byste měl(a) dostat více přípravku MabThera. K tomu může dojít i za několik měsíců.
d) Pokud jste léčen(a) z důvodu granulomatózy s polyangiitidou nebo mikroskopické polyangiitidy
Léčba přípravkem MabThera je tvořena čtyřmi oddělenými infuzemi, které se podávají v týdenních intervalech. Kortikosteroidy se obvykle podávají v injekcích před začátkem léčby přípravkem MabThera. Perorální (ústy podávanou) léčbu kortikosteroidy může lékař zahájit kdykoli.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Většina nežádoucích účinků je mírného až středně závažného stupně, některé však mohou být vážné a mohou vyžadovat léčbu. Vzácně mohou mít některé z těchto účinků fatální průběh.
Reakce na infuzi
Během infuze nebo v prvních 2 hodinách první infuze se může objevit horečka, zimnice a třesavka. Méně často se u některých pacientů mohou objevit bolest v místě vpichu infuze, puchýřky, svědění, nevolnost, únava, bolest hlavy, dechové obtíže, otok jazyka nebo hrdla, svědění v nose nebo příznaky rýmy, zvracení, návaly horka nebo nepravidelnosti srdečního rytmu, srdeční infarkt nebo snížení počtu krevních destiček. Jestliže máte srdeční onemocnění, jako je např. angina pectoris, mohou se tyto reakce zhoršit. Pokud se u Vás objeví některý z těchto příznaků, řekněte to okamžitě zdravotníkovi, který Vám podává infuzi a který může průběh infuze zpomalit nebo zastavit. Může být zapotřebí další léčba, např. podání antihistaminik nebo paracetamolu. Poté, co příznaky odezní nebo se zmírní, může infuze pokračovat. Po druhé infuzi je již výskyt reakcí méně pravděpodobný. Pokud jsou tyto reakce závažné, Váš lékař může rozhodnout ukončit Vaši léčbu přípravkem MabThera.
Infekce
Informujte ihned svého lékaře, pokud se u Vás objeví příznaky infekčního onemocnění, které zahrnují:
• horečku, kašel, bolest v krku, pocit pálení při močení nebo pokud budete pociťovat slabost nebo se celkově nebudete cítit dobře
• ztrátu paměti, poruchy myšlení, problémy s chůzí nebo ztráta vidění - to může být z důvodu velmi vzácné, závažné mozkové infekce, která může vést k úmrtí (Progresivní multifokální leukoencefalopatie nebo PML).
V průběhu léčby přípravkem MabThera se může projevit vyšší náchylnost k infekcím. Často jde o nachlazení, mohou se však vyskytnout případy zápalu plic nebo infekce močových cest.
Tyto nežádoucí účinky jsou uvedeny níže v odstavci „Další nežádoucí účinky“.
Jste-li léčen(a) na revmatoidní artritidu, najdete tyto informace také v Kartě pro pacienta, kterou jste obdržel(a) od svého lékaře. Je důležité, abyste si ponechal(a) tuto kartu a ukázal(a) ji svému partnerovi nebo poskytovateli péče.
Kožní reakce
Velmi vzácně se vyskytují závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst, v oblasti genitálu či na očních víčkách. V případě, že zaznamenáte kterýkoliv z těchto příznaků, informujte okamžitě svého lékaře.
Další nežádoucí účinky zahrnují:
a) Pokud jste léčen(a) z důvodu nehodgkinského lymfomu či chronické lymfocytární
leukemie
Velmi časté nežádoucí účinky (mohou postihnout více než 1 pacienta z 10):
• bakteriální nebo virová infekce, zánět průdušek (bronchitida)
• pokles počtu bílých krvinek provázený horečkou nebo bez horečky nebo snížení počtu krevních buněk nazývaných „krevní destičky“
• nevolnost (nauzea)
• vypadávání vlasů na temeni hlavy, zimnice, bolesti hlavy
• snížená imunita - z důvodu poklesu hladiny protilátek nazývaných „imunoglobuliny“ (IgG) v krvi, které se podílejí na ochraně proti infekci.
Časté nežádoucí účinky (mohou postihnout až 1 pacienta z 10):
• infekce krve (sepse), zápal plic, pásový opar, nachlazení, infekce dýchacích cest, plísňová infekce, infekce neznámého původu, infekce dutin, žloutenka typu B
• pokles počtu červených krvinek (anémie), pokles počtu všech krevních buněk
• alergické reakce (přecitlivělost)
• zvýšená hladina cukru, pokles hmotnosti, otoky v obličeji či v celém těle, vzestup hladiny enzymu „LDH“ v krvi, pokles hladiny vápníku v krvi
• poruchy kožního čití jako například snížená citlivost, brnění, bodání, pálení, nepříjemné pocity, zhoršení hmatu
• pocity podrážděnosti, potíže s usínáním
• zrudnutí v obličeji a dalších místech kůže jako důsledek rozšíření krevních cév
• závratě nebo úzkost
• zvýšená tvorba slz, poruchy slzného kanálku, záněty očí (zánět spojivek)
• hučení v uších, bolest uší
• srdeční obtíže - jako jsou infarkt myokardu, nepravidelná nebo zrychlená srdeční činnost
• vzestup či pokles krevního tlaku (snížení krevního tlaku po postavení)
• stažení svalů dýchacích cest způsobující sípání (bronchospazmus), zánět, podráždění na hrudi, v hrdle nebo dutinách, dušnost, rýma
• nevolnost (zvracení), průjem, bolest žaludku, podráždění nebo vřídky v hrdle a ústech, poruchy polykání, zácpa, trávicí obtíže
• poruchy příjmu potravy, snížení množství přijímané potravy s následným poklesem hmotnosti
• kopřivka, zvýšené pocení, noční poty
• svalové poruchy - jako jsou napětí svalů, bolesti kloubů nebo svalů, bolesti zad a krku
• celkové nepohodlí nebo pocit stísněnosti nebo únavy, třes, příznaky podobné chřipce
• poruchy více tělních orgánů.
Méně časté nežádoucí účinky (mohou postihnout až 1 pacienta ze 100):
• poruchy krevní srážlivosti, pokles tvorby červených krvinek, zvýšená destrukce červených krvinek (aplastická hemolytická anémie), otok nebo zvětšení lymfatických uzlin
• pokles nálady a ztráta zájmu a potěšení z obvyklých činností, nervozita
• poruchy vnímání chuti - jako například změna vnímání, jak věci chutnají
• srdeční obtíže - jako například zpomalení srdečního rytmu nebo bolest na hrudi (angina)
• astma, nedostatečné okysličení tělesných orgánů
• zvětšení břicha.
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 pacienta z 10 000):
• krátkodobé zvýšení množství některých typů protilátek v krvi (zvané imunoglobuliny IgM), chemické poruchy krve způsobené rozpadem umírajících rakovinových buněk
• poškození nervů v rukách a nohách, ochrnutí obličeje
• srdeční selhání
• záněty krevních cév včetně těch, které vedou ke kožním příznakům
• respirační (plicní) selhání
• perforace (proděravění) střevní stěny
• závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst,
v oblasti genitálu či na očních víčkách.
• selhání ledvin
• závažná ztráta zraku.
Není známo (nežádoucí účinky vyskytující se s neznámou četností):
• snížení bílých krvinek, ke kterému dochází se zpožděním
• okamžité snížení počtu krevních destiček související s infuzí - to může být vratné, ale ve vzácných případech může končit úmrtím
• ztráta sluchu, ztráta jiných smyslů.
b) Pokud jste léčen(a) z důvodu revmatoidní artritidy
Velmi časté nežádoucí účinky (mohou postihnout více než 1 pacienta z 10):
• infekce, jako je zápal plic (bakteriální pneumonie)
• bolest při močení (infekce močových cest)
• alergické reakce, které se nejpravděpodobněji vyskytnou v průběhu infuze, ale mohou se vyskytnout až do 24 hodin po podání infuze
• změny krevního tlaku, nevolnost, vyrážka, horečka, pocit svědění, příznaky rýmy nebo ucpaný nos a kýchání, třes, zrychlená srdeční frekvence a únava
• bolest hlavy
• změny v laboratorních testech provedených Vaším lékařem. Ty zahrnují snížení množství některých specifických bílkovin v krvi (imunoglobulinů), které se podílejí na ochraně proti infekci.
Časté nežádoucí účinky (mohou postihnout až 1 pacienta z 10):
• infekce, jako je zánět průdušek (bronchitida)
• pocit plnosti nebo pulzující bolest za nosem, čelem a očima (zánět vedlejších nosních dutin, sinusitida), bolest břicha, zvracení a průjem, potíže s dýcháním
• plísňové infekce nohou (atletická noha)
• vysoké hladiny cholesterolu v krvi
• nenormální pocity na kůži, jako je necitlivost, brnění, píchání nebo pálení, bederní ústřel (ischias), migréna, závrať
• ztráta vlasů
• úzkost, deprese
• poruchy trávení, průjem, kyselý reflux, podráždění a/nebo vředy v krku a ústech
• bolest břicha, zad, svalů a/nebo kloubů.
Méně časté nežádoucí účinky (mohou postihnout až 1 pacienta ze 100):
• přílišné zadržování tekutin v obličeji i těle
• zánět, podráždění a/nebo pocit sevření na plicích a v krku, kašel
• kožní reakce, které zahrnují kopřivku, svědění a vyrážku
• alergické reakce včetně chrapotu a dušnosti, otoků obličeje a jazyka, kolaps.
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 pacienta z 10 000):
• soubor příznaků, které se objevují během několika týdnů po infuzi přípravku MabThera a které zahrnují reakce podobné alergické reakci, jako je vyrážka, svědění, bolest kloubů, otoky lymfatických uzlin a horečka
• závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst,
v oblasti genitálu či na očních víčkách.
Další vzácně hlášené nežádoucí účinky přípravku MabThera zahrnují snížený počet bílých krvinek (neutrofilů) v krvi, které napomáhají bojovat proti infekci. Některé infekce mohou být závažné (prosím přečtěte si informace v odstavci Infekce uvedeném v tomto bodě).
c) Pokud jste léčen(a) z důvodu granulomatózy s polyangiitidou nebo mikroskopické
polyangiitidy
Velmi časté nežádoucí účinky (mohou postihnout více než 1 pacienta z 10):
• infekce, jako jsou hrudní infekce, infekce močových cest (bolest při močení), nachlazení a herpetické infekce
• alergické reakce, které se s větší pravděpodobností objeví v průběhu infuze, ale mohou se objevit během až 24 hodin po podání infuze
• průjem
• kašel nebo dušnost
• krvácení z nosu
• zvýšení krevního tlaku
• bolest kloubů nebo zad
• svalové záškuby nebo chvění
• pocit závrati
• třes (chvění, nej častěji rukou)
• obtíže se spánkem (nespavost)
• otoky rukou nebo kotníků.
Časté nežádoucí účinky (mohou postihnout až 1 pacienta z 10):
• porucha trávení
• zácpa
• kožní vyrážky, včetně akné nebo pupínků
• návaly horka nebo zarudnutí kůže
• ucpaný nos
• ztuhlost nebo bolest svalů
• bolest ve svalech nebo v rukou nebo nohou
• nízký počet červených krvinek (anémie)
• nízký počet krevních destiček v krvi
• zvýšení množství draslíku v krvi
• změny srdečního rytmu nebo zrychlení srdečního rytmu.
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 pacienta z 10 000):
• závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst, v oblasti genitálu či na očních víčkách.
• opětovný výskyt žloutenky (hepatitida B), na kterou jste předtím byl(a) léčen(a).
Přípravek MabThera může rovněž způsobit změny v laboratorních testech, které Vám provádí Váš lékař.
Pokud je Vám podáván přípravek MabThera v kombinaci s jinými přípravky, mohou se u Vás objevit nežádoucí účinky spojené s užíváním jiných přípravků.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek MabThera uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce za „Použitelné do:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2 °C - 8 °C). Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek MabThera obsahuje
• Léčivou látkou přípravku MabThera je rituximab. Injekční lahvička obsahuje 100 mg rituximabu (10 mg/ml).
• Dalšími složkami jsou natrium-citrát, polysorbát 80, chlorid sodný, hydroxid sodný, kyselina chlorovodíková a voda na injekci.
Jak přípravek MabThera vypadá a co obsahuje toto balení
Přípravek MabThera je čirý, bezbarvý roztok ve formě koncentrátu pro infuzní roztok. Balení obsahuje 2 injekční lahvičky o objemu 10 ml.
Držitel rozhodnutí o registraci
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
Výrobce
Roche Pharma AG Emil-Barell-Str. 1 D-79639 Grenzach-Wyhlen Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci
|
Belgie/Belgique/Belgien N.V. Roche S.A. Tél/Tel: +32 (0) 2 525 82 11 |
Lietuva UAB “Roche Lietuva” Tel: +370 5 2546799 |
|
BtarapHH Pom Etnrapua EOOfl Tea: +359 2 818 44 44 |
Luxembourg/Luxemburg (Voir/siehe Belgique/Belgien) |
|
Česká republika Roche s. r. o. Tel: +420 - 2 20382111 |
Magyarország Roche (Magyarország) Kft. Tel: +36 - 23 446 800 |
|
Danmark Roche a/s Tlf: +45 - 36 39 99 99 |
Malta (See United Kingdom) |
|
Deutschland Roche Pharma AG Tel: +49 (0) 7624 140 |
Nederland Roche Nederland B.V. Tel: +31 (0) 348 438050 |
|
Eesti Roche Eesti OU Tel: + 372 - 6 177 380 |
Norge Roche Norge AS Tlf: +47 - 22 78 90 00 |
|
EXlába Roche (Hellas) A.E. Ttfk: +30 210 61 66 100 |
Osterreich Roche Austria GmbH Tel: +43 (0) 1 27739 |
|
Espaňa Roche Farma S.A. Tel: +34 - 91 324 81 00 |
Polska Roche Polska Sp.z o.o. Tel: +48 - 22 345 18 88 |
|
France Roche Tél: +33 (0) 1 47 61 40 00 |
Portugal Roche Farmaceutica Química, Lda Tel: +351 - 21 425 70 00 |
|
Hrvatska Roche d.o.o. Tel: + 385 1 47 22 333 |
Románia Roche Románia S.R.L. Tel: +40 21 206 47 01 |
|
Ireland Roche Products (Ireland) Ltd. Tel: +353 (0) 1 469 0700 |
Slovenija Roche farmacevtska družba d.o.o. Tel: +386 - 1 360 26 00 |
Latvija
Roche Latvija SIA
Tel: +371 - 6 7039831
Sími: +354 540 8000
Sverige Roche AB
Tel: +46 (0) 8 726 1200
United Kingdom Roche Products Ltd.
Tel: +44 (0) 1707 366000
Tato příbalová informace byla naposledy revidována {měsíc RRRR}.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
Příbalová informace: informace pro pacienta
MabThera 500 mg koncentrát pro infuzní roztok
rituximabum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek MabThera a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek MabThera používat
3. Jak se přípravek MabThera podává
4. Možné nežádoucí účinky
5. Jak přípravek MabThera uchovávat
6. Obsah balení a další informace
1. Co je přípravek MabThera a k čemu se používá
Co je přípravek MabThera
Přípravek MabThera obsahuje léčivou látku „rituximab“. To je zvláštní druh bílkoviny nazývaný „monoklonální protilátka“. Váže se na povrch jednoho typu bílých krvinek nazývaných „B lymfocyty“. Po vazbě na povrch této buňky, rituximab navodí její zánik.
K čemu se přípravek MabThera používá
Přípravek MabThera se používá k léčbě několika různých onemocnění u dospělých. Lékař Vám může přípravek MabThera předepsat k léčbě:
a) nehodgkinského lymfomu
To je onemocnění lymfatické tkáně (část imunitního systému), která ovlivňuje jeden typ bílých krvinek nazývaných B lymfocyty.
Přípravek MabThera může být podán samostatně nebo s jinými dalšími léky nazývanými „chemoterapeutika“.
U pacientů, u kterých je léčba účinná, může být přípravek MabThera používán v udržovací léčbě po dobu 2 let po dokončení úvodní léčby.
b) chronické lymfocytární leukemie
Chronická lymfocytární leukemie (CLL) je nejčastější formou leukemie u dospělých. CLL postihuje zejména lymfocyty, B-buňky, které pocházejí z kostní dřeně a vyvíjejí se v lymfatických uzlinách. Pacienti s CLL mají příliš mnoho abnormálních lymfocytů, které se hromadí zejména v kostní dřeni a krvi. Růst těchto abnormálních B-lymfocytů je příčinou příznaků, které můžete pociťovat. Přípravek MabThera v kombinaci s chemoterapií ničí tyto buňky, které jsou postupně odstraňovány z organismu pomocí biologických mechanismů.
c) revmatoidní artritidy
Přípravek MabThera se používá k léčbě revmatoidní artritidy. Revmatoidní artritida je onemocnění kloubů. B lymfocyty se podílí na vzniku některých příznaků, které se u Vás projevují. Přípravek MabThera se používá k léčbě revmatoidní artritidy u pacientů, kteří již podstoupili jinou léčbu, která však přestala být účinná, neúčinkovala dostatečně nebo způsobovala nežádoucí účinky. Přípravek MabThera se obvykle používá v kombinaci s dalším lékem zvaným metotrexát.
Přípravek MabThera zpomaluje poškození kloubů, které způsobuje revmatoidní artritida, a zlepšuje schopnost provádět obvyklé denní aktivity.
Nejlepší odpověď na léčbu přípravkem MabThera byla pozorována u pacientů, kteří měli pozitivní krevní testy na revmatoidní faktor (RF) a/nebo protilátky proti bílkovině citrulinu (anti-CCP). Oba testy jsou u pacientů s revmatoidní artritidou běžně pozitivní a pomáhají k potvrzení diagnózy.
d) granulomatózy s polyangiitidou nebo mikroskopické polyangiitidy
Přípravek MabThera se používá k navození remise u granulomatózy s polyangiitidou (dříve nazývané Wegenerova granulomatóza) nebo mikroskopické polyangiitidy; podává se v kombinaci s kortikosteroidy. Granulomatóza s polyangiitidou a mikroskopická polyangiitida jsou dvě formy zánětlivého onemocnění krevních cév, které postihuje převážně cévy plic a ledvin, ale může postihnout i cévy jiných orgánů. U těchto onemocnění hrají roli i B lymfocyty.
2. Čemu musíte věnovat pozornost, než začnete přípravek MabThera používat
Nepoužívejte přípravek MabThera pokud:
• jste alergický(á) na rituximab, na jiné proteiny podobného typu nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6)
• máte v současnosti závažnou aktivní infekci
• máte oslabenou funkci imunitního systému
• máte závažné srdeční selhání nebo závažné nekontrolované srdeční onemocnění a máte revmatoidní artritidu, granulomatózu s polyangiitidou nebo mikroskopickou polyangiitidu.
Nepoužívejte přípravek MabThera, pokud se Vás cokoliv z výše uvedeného týká. Pokud si nejste jistý(á), zeptejte se svého lékaře, lékárníka nebo zdravotní sestry dříve, než Vám bude přípravek MabThera podán.
Upozornění a opatření
Předtím, než Vám bude podán přípravek MabThera, poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou, pokud:
• jste někdy měl(a) nebo možná právě máte žloutenku. To je proto, že v některých případech by přípravek MabThera mohl znovu vyvolat žloutenku typu B (hepatitidu B), která může velmi vzácně vést k úmrtí. U pacientů s anamnézou hepatitidy B musí lékař pečlivě sledovat příznaky aktivní hepatitidy B.
• jste někdy trpěl(a) onemocněním srdce (jako je angina, palpitace nebo selhání srdce) nebo pokud jste někdy měl(a) obtíže s dýcháním.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán. Lékař Vám bude muset během léčby přípravkem MabThera věnovat zvláštní péči.
Máte-li revmatoidní artritidu, granulomatózu s polyangiitidou nebo mikroskopickou polyangiitidu, informujte lékaře
• jestliže si myslíte, že máte infekční onemocnění, dokonce i v případě lehkého nachlazení. Buňky, které jsou likvidovány přípravkem MabThera, pomáhají organismu bojovat s infekcemi, a proto byste během léčby přípravkem MabThera mohl(a) dostat infekci. Pokud infekcemi trpíte často anebo mají těžký průběh, řekněte to, prosím, rovněž svému lékaři.
• jestliže je pravděpodobné, že budete v blízké budoucnosti potřebovat nějaké očkování, včetně očkování před odjezdem do ciziny. Některé očkovací látky by neměly být aplikovány současně s přípravkem MabThera nebo v měsících, kdy se přípravkem MabThera léčíte. Před léčbou přípravkem MabThera lékař zkontroluje, zda byste neměl(a) nějaké očkování dostat.
Děti a dospívající
Poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán, pokud jste Vy nebo Vaše dítě mladší 18 let. To je z důvodu, že není k dispozici mnoho informací o používání přípravku MabThera u dětí a dospívajících.
Další léčivé přípravky a přípravek MabThera
Informujte svého lékaře, lékárníka nebo zdravotní sestru o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. To se týká i léků, které jsou dostupné bez lékařského předpisu a rostlinných přípravků. Důvodem je, že přípravek MabThera může ovlivňovat způsob účinku některých dalších léků. Stejně tak ostatní léky mohou ovlivňovat účinek přípravku MabThera.
Konkrétně, informujte svého lékaře:
• jestliže užíváte léky na vysoký krevní tlak. Můžete být požádán(a), abyste tyto léky neužíval(a) 12 hodin předtím, než Vám bude podán přípravek MabThera. To je proto, že u některých osob dochází během podání přípravku MabThera k poklesu krevního tlaku.
• jestliže jste v minulosti užíval(a) léky, které mohou ovlivnit Váš imunitní systém - jako jsou chemoterapeutika nebo imunosupresiva.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán.
Těhotenství a kojení
Musíte sdělit svému lékaři nebo zdravotní sestře, že jste těhotná, nebo že si nejste jistá, zda nejste těhotná, nebo že zamýšlíte otěhotnět. Přípravek MabThera je totiž protilátka, která může procházet placentou a ovlivnit dítě.
Pokud byste mohla otěhotnět, musíte Vy i Váš partner během léčby přípravkem MabThera a ještě 12 měsíců po jejím ukončení používat účinné antikoncepční prostředky.
Nekojte během Vaší léčby přípravkem MabThera. Nekojte také 12 měsíců po ukončení Vaší poslední léčby přípravkem MabThera. Přípravek MabThera může procházet do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Není známo, zda přípravek MabThera ovlivňuje schopnost řídit, používat jakékoli přístroje nebo obsluhovat stroje.
3. Jak se přípravek MabThera podává Jak se přípravek podává
Přípravek MabThera Vám bude podávat Váš lékař nebo zdravotní sestra, kteří mají zkušenosti s užíváním této léčby. Budou Vás pečlivě sledovat během podání tohoto léčivého přípravku. Je to pro případ, že by se u Vás projevily nežádoucí účinky.
Vždy na začátku léčby Vám přípravek MabThera bude podán „kapačkou“ (intravenózní infuze).
Léčivé přípravky podávané před každým podáním přípravku MabThera
Před podáním přípravku MabThera Vám budou podány další léky (premedikace) k zabránění nebo ke snížení možného rizika nežádoucích účinků.
Kolik a jak často budete dostávat Vaši léčbu
a) Pokud jste léčen(a) z důvodu nehodgkinského lymfomu
• Dostáváte-li pouze přípravek MabThera samotný
Přípravek MabThera Vám bude podáván jedenkrát týdně po dobu 4 týdnů. Léčbu přípravkem MabThera lze opakovat.
• Dostáváte-li přípravek MabThera v kombinaci s chemoterapií
Přípravek MabThera Vám bude podáván ve stejný den jako chemoterapie. Většinou je podáván každé 3 týdny, celkem 8krát.
• Pokud budete dobře reagovat na léčbu, může Vám být přípravek MabThera podáván v rámci udržovací léčby každé 2 nebo 3 měsíce po dobu 2 let.
V závislosti na tom, jak budete reagovat na tento léčivý přípravek, Váš lékař může toto dávkování změnit.
b) Pokud jste léčen(a) z důvodu chronické lymfocytární leukemie
Jste-li léčen(a) přípravkem MabThera v kombinaci s chemoterapií, budete dostávat infuzi s přípravkem MabThera v den 0 1. cyklu léčby a potom v den 1 každého z celkem 6 cyklů léčby. Jeden cyklus léčby má 28 dní. Chemoterapie má být podávána po infuzi přípravku MabThera. Lékař rozhodne, zda budete dostávat průvodní podpůrnou léčbu.
c) Pokud jste léčen(a) z důvodu revmatoidní artritidy
Jeden cyklus léčby sestává ze dvou infuzí, které jsou podávány v odstupu alespoň 2 týdnů. Opakování cyklů léčby přípravkem MabThera je možné. Na základě příznaků a projevů Vaší nemoci lékař rozhodne, zda byste měl(a) dostat více přípravku MabThera. K tomu může dojít i za několik měsíců.
d) Pokud jste léčen(a) z důvodu granulomatózy s polyangiitidou nebo mikroskopické polyangiitidy
Léčba přípravkem MabThera je tvořena čtyřmi oddělenými infuzemi, které se podávají v týdenních intervalech. Kortikosteroidy se obvykle podávají v injekcích před začátkem léčby přípravkem MabThera. Perorální (ústy podávanou) léčbu kortikosteroidy může lékař zahájit kdykoli.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Většina nežádoucích účinků je mírného až středně závažného stupně, některé však mohou být vážné a mohou vyžadovat léčbu. Vzácně mohou mít některé z těchto účinků fatální průběh.
Reakce na infuzi
Během infuze nebo v prvních 2 hodinách první infuze se může objevit horečka, zimnice a třesavka. Méně často se u některých pacientů mohou objevit bolest v místě vpichu infuze, puchýřky, svědění, nevolnost, únava, bolest hlavy, dechové obtíže, otok jazyka nebo hrdla, svědění v nose nebo příznaky rýmy, zvracení, návaly horka nebo nepravidelnosti srdečního rytmu, srdeční infarkt nebo snížení počtu krevních destiček. Jestliže máte srdeční onemocnění, jako je např. angina pectoris, mohou se tyto reakce zhoršit. Pokud se u Vás objeví některý z těchto příznaků, řekněte to okamžitě zdravotníkovi, který Vám podává infuzi a který může průběh infuze zpomalit nebo zastavit. Může být zapotřebí další léčba, např. podání antihistaminik nebo paracetamolu. Poté, co příznaky odezní nebo se zmírní, může infuze pokračovat. Po druhé infuzi je již výskyt reakcí méně pravděpodobný. Pokud jsou tyto reakce závažné, Váš lékař může rozhodnout ukončit Vaši léčbu přípravkem MabThera.
Infekce
Informujte ihned svého lékaře, pokud se u Vás objeví příznaky infekčního onemocnění, které
zahrnují:
• horečku, kašel, bolest v krku, pocit pálení při močení nebo pokud budete pociťovat slabost nebo se celkově nebudete cítit dobře.
• ztrátu paměti, poruchy myšlení, problémy s chůzí nebo ztráta vidění - to může být z důvodu velmi vzácné, závažné mozkové infekce, která může vést k úmrtí (Progresivní multifokální leukoencefalopatie nebo PML).
V průběhu léčby přípravkem MabThera se může projevit vyšší náchylnost k infekcím. Často jde o nachlazení, mohou se však vyskytnout případy zápalu plic nebo infekce močových cest.
Tyto nežádoucí účinky jsou uvedeny níže v odstavci „Další nežádoucí účinky“.
Jste-li léčen(a) na revmatoidní artritidu, najdete tyto informace také v Kartě pro pacienta, kterou jste obdržel(a) od svého lékaře. Je důležité, abyste si ponechal(a) tuto kartu a ukázal(a) ji svému partnerovi nebo poskytovateli péče.
Kožní reakce
Velmi vzácně se vyskytují závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst, v oblasti genitálu či na očních víčkách. V případě, že zaznamenáte kterýkoliv z těchto příznaků, informujte okamžitě svého lékaře.
Další nežádoucí účinky zahrnují:
a) Pokud jste léčen(a) z důvodu nehodgkinského lymfomu či chronické lymfocytární
leukemie
Velmi časté nežádoucí účinky (mohou postihnout více než 1 pacienta z 10):
• bakteriální nebo virová infekce, zánět průdušek (bronchitida)
• pokles počtu bílých krvinek provázený horečkou nebo bez horečky nebo snížení počtu krevních buněk nazývaných „krevní destičky“
• nevolnost (nauzea)
• vypadávání vlasů na temeni hlavy, zimnice, bolesti hlavy
• snížená imunita - z důvodu poklesu hladiny protilátek nazývaných „imunoglobuliny“ (IgG) v krvi, které se podílejí na ochraně proti infekci.
Časté nežádoucí účinky (mohou postihnout až 1 pacienta z 10):
• infekce krve (sepse), zápal plic, pásový opar, nachlazení, infekce dýchacích cest, plísňová infekce, infekce neznámého původu, infekce dutin, žloutenka typu B
• pokles počtu červených krvinek (anémie), pokles počtu všech krevních buněk
• alergické reakce (přecitlivělost)
• zvýšená hladina cukru, pokles hmotnosti, otoky v obličeji či v celém těle, vzestup hladiny enzymu „LDH“ v krvi, pokles hladiny vápníku v krvi
• poruchy kožního čití jako například snížená citlivost, brnění, bodání, pálení, nepříjemné pocity, zhoršení hmatu
• pocity podrážděnosti, potíže s usínáním
• zrudnutí v obličeji a dalších místech kůže jako důsledek rozšíření krevních cév
• závratě nebo úzkost
• zvýšená tvorba slz, poruchy slzného kanálku, záněty očí (zánět spojivek)
• hučení v uších, bolest uší
• srdeční obtíže - jako jsou infarkt myokardu, nepravidelná nebo zrychlená srdeční činnost
• vzestup či pokles krevního tlaku (snížení krevního tlaku po postavení)
• stažení svalů dýchacích cest způsobující sípání (bronchospazmus), zánět, podráždění na hrudi, v hrdle nebo dutinách, dušnost, rýma
• nevolnost (zvracení), průjem, bolest žaludku, podráždění nebo vřídky v hrdle a ústech, poruchy polykání, zácpa, trávicí obtíže
• poruchy příjmu potravy, snížení množství přijímané potravy s následným poklesem hmotnosti
• kopřivka, zvýšené pocení, noční poty
• svalové poruchy - jako jsou napětí svalů, bolesti kloubů nebo svalů, bolesti zad a krku
• celkové nepohodlí nebo pocit stísněnosti nebo únavy, třes, příznaky podobné chřipce
• poruchy více tělních orgánů.
Méně časté nežádoucí účinky (mohou postihnout až 1 pacienta ze 100):
• poruchy krevní srážlivosti, pokles tvorby červených krvinek, zvýšená destrukce červených krvinek (aplastická hemolytická anémie), otok nebo zvětšení lymfatických uzlin
• pokles nálady a ztráta zájmu a potěšení z obvyklých činností, nervozita
• poruchy vnímání chuti - jako například změna vnímání, jak věci chutnají
• srdeční obtíže - jako například zpomalení srdečního rytmu nebo bolest na hrudi (angina)
• astma, nedostatečné okysličení tělesných orgánů
• zvětšení břicha.
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 pacienta z 10 000):
• krátkodobé zvýšení množství některých typů protilátek v krvi (zvané imunoglobuliny IgM), chemické poruchy krve způsobené rozpadem umírajících rakovinových buněk
• poškození nervů v rukách a nohách, ochrnutí obličeje
• srdeční selhání
• záněty krevních cév včetně těch, které vedou ke kožním příznakům
• respirační (plicní) selhání
• perforace (proděravění) střevní stěny
• závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst,
v oblasti genitálu či na očních víčkách.
• selhání ledvin
• závažná ztráta zraku.
Není známo (nežádoucí účinky vyskytující se s neznámou četností):
• snížení bílých krvinek, ke kterému dochází se zpožděním
• okamžité snížení počtu krevních destiček související s infuzí - to může být vratné, ale ve vzácných případech může končit úmrtím
• ztráta sluchu, ztráta jiných smyslů.
b) Pokud jste léčen(a) z důvodu revmatoidní artritidy
Velmi časté nežádoucí účinky (mohou postihnout více než 1 pacienta z 10):
• infekce, jako je zápal plic (bakteriální pneumonie)
• bolest při močení (infekce močových cest)
• alergické reakce, které se nejpravděpodobněji vyskytnou v průběhu infuze, ale mohou se vyskytnout až do 24 hodin po podání infuze
• změny krevního tlaku, nevolnost, vyrážka, horečka, pocit svědění, příznaky rýmy nebo ucpaný nos a kýchání, třes, zrychlená srdeční frekvence a únava
• bolest hlavy
• změny v laboratorních testech provedených Vaším lékařem. Ty zahrnují snížení množství některých specifických bílkovin v krvi (imunoglobulinů), které se podílejí na ochraně proti infekci.
Časté nežádoucí účinky (mohou postihnout až 1 pacienta z 10):
• infekce, jako je zánět průdušek (bronchitida)
• pocit plnosti nebo pulzující bolest za nosem, čelem a očima (zánět vedlejších nosních dutin, sinusitida), bolest břicha, zvracení a průjem, potíže s dýcháním
• plísňové infekce nohou (atletická noha)
• vysoké hladiny cholesterolu v krvi
• nenormální pocity na kůži, jako je necitlivost, brnění, píchání nebo pálení, bederní ústřel (ischias), migréna, závrať
• ztráta vlasů
• úzkost, deprese
• poruchy trávení, průjem, kyselý reflux, podráždění a/nebo vředy v krku a ústech
• bolest břicha, zad, svalů a/nebo kloubů.
Méně časté nežádoucí účinky (mohou postihnout až 1 pacienta ze 100):
• přílišné zadržování tekutin v obličeji i těle
• zánět, podráždění a/nebo pocit sevření na plicích a v krku, kašel
• kožní reakce, které zahrnují kopřivku, svědění a vyrážku
• alergické reakce včetně chrapotu a dušnosti, otoků obličeje a jazyka, kolaps.
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 pacienta z 10 000):
• soubor příznaků, které se objevují během několika týdnů po infuzi přípravku MabThera a které zahrnují reakce podobné alergické reakci, jako je vyrážka, svědění, bolest kloubů, otoky lymfatických uzlin a horečka
• závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst,
v oblasti genitálu či na očních víčkách.
Další vzácně hlášené nežádoucí účinky přípravku MabThera zahrnují snížený počet bílých krvinek (neutrofilů) v krvi, které napomáhají bojovat proti infekci. Některé infekce mohou být závažné (prosím přečtěte si informace v odstavci Infekce uvedeném v tomto bodě).
c) Pokud jste léčen(a) z důvodu granulomatózy s polyangiitidou nebo mikroskopické
polyangiitidy
Velmi časté nežádoucí účinky (mohou postihnout více než 1 pacienta z 10):
• infekce, jako jsou hrudní infekce, infekce močových cest (bolest při močení), nachlazení a herpetické infekce
• alergické reakce, které se s větší pravděpodobností objeví v průběhu infuze, ale mohou se objevit během až 24 hodin po podání infuze
• průjem
• kašel nebo dušnost
• krvácení z nosu
• zvýšení krevního tlaku
• bolest kloubů nebo zad
• svalové záškuby nebo chvění
• pocit závrati
• třes (chvění, nej častěji rukou)
• obtíže se spánkem (nespavost)
• otoky rukou nebo kotníků.
Časté nežádoucí účinky (mohou postihnout až 1 pacienta z 10):
• porucha trávení
• zácpa
• kožní vyrážky, včetně akné nebo pupínků
• návaly horka nebo zarudnutí kůže
• ucpaný nos
• ztuhlost nebo bolest svalů
• bolest ve svalech nebo v rukou nebo nohou
• nízký počet červených krvinek (anémie)
• nízký počet krevních destiček v krvi
• zvýšení množství draslíku v krvi
• změny srdečního rytmu nebo zrychlení srdečního rytmu.
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 pacienta z 10 000):
• závažné puchýřky na kůži, které mohou být život ohrožující. Zarudnutí, často spojené s puchýři a někdy doprovázené horečkou, se může objevit na kůži nebo na sliznici úst, v oblasti genitálu či na očních víčkách.
• opětovný výskyt žloutenky (hepatitida B), na kterou jste předtím byl(a) léčen(a).
Přípravek MabThera může rovněž způsobit změny v laboratorních testech, které Vám provádí Váš lékař.
Pokud je Vám podáván přípravek MabThera v kombinaci s jinými přípravky, mohou se u Vás objevit nežádoucí účinky spojené s užíváním jiných přípravků.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek MabThera uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce za „Použitelné do:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2 °C - 8 °C). Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek MabThera obsahuje
• Léčivou látkou přípravku MabThera je rituximab. Injekční lahvička obsahuje 500 mg rituximabu (10 mg/ml).
• Dalšími složkami jsou natrium-citrát, polysorbát 80, chlorid sodný, hydroxid sodný, kyselina chlorovodíková a voda na injekci.
Jak přípravek MabThera vypadá a co obsahuje toto balení
Přípravek MabThera je čirý, bezbarvý roztok ve formě koncentrátu pro infuzní roztok. Balení po 1 injekční lahvičce.
Držitel rozhodnutí o registraci
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
Výrobce
Roche Pharma AG Emil-Barell-Str. 1 D-79639 Grenzach-Wyhlen Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci
|
Belgie/Belgique/Belgien N.V. Roche S.A. Tél/Tel: +32 (0) 2 525 82 11 |
Lietuva UAB “Roche Lietuva” Tel: +370 5 2546799 |
|
BtarapHH Pom Etnrapua EOOfl Tea: +359 2 818 44 44 |
Luxembourg/Luxemburg (Voir/siehe Belgique/Belgien) |
|
Česká republika Roche s. r. o. Tel: +420 - 2 20382111 |
Magyarország Roche (Magyarország) Kft. Tel: +36 - 23 446 800 |
|
Danmark Roche a/s Tlf: +45 - 36 39 99 99 |
Malta (See United Kingdom) |
|
Deutschland Roche Pharma AG Tel: +49 (0) 7624 140 |
Nederland Roche Nederland B.V. Tel: +31 (0) 348 438050 |
|
Eesti Roche Eesti OU Tel: + 372 - 6 177 380 |
Norge Roche Norge AS Tlf: +47 - 22 78 90 00 |
|
EXlába Roche (Hellas) A.E. Ttfk: +30 210 61 66 100 |
Osterreich Roche Austria GmbH Tel: +43 (0) 1 27739 |
|
Espaňa Roche Farma S.A. Tel: +34 - 91 324 81 00 |
Polska Roche Polska Sp.z o.o. Tel: +48 - 22 345 18 88 |
|
France Roche Tél: +33 (0) 1 47 61 40 00 |
Portugal Roche Farmaceutica Química, Lda Tel: +351 - 21 425 70 00 |
|
Hrvatska Roche d.o.o. Tel: + 385 1 47 22 333 |
Románia Roche Románia S.R.L. Tel: +40 21 206 47 01 |
|
Ireland Roche Products (Ireland) Ltd. Tel: +353 (0) 1 469 0700 |
Slovenija Roche farmacevtska družba d.o.o. Tel: +386 - 1 360 26 00 |
Latvija
Roche Latvija SIA
Tel: +371 - 6 7039831
Sími: +354 540 8000
Sverige Roche AB
Tel: +46 (0) 8 726 1200
United Kingdom Roche Products Ltd.
Tel: +44 (0) 1707 366000
Tato příbalová informace byla naposledy revidována {měsíc RRRR}.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
Příbalová informace: informace pro pacienta
MabThera 1400 mg subkutánní injekční roztok
rituximabum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek MabThera a k čemu se používá
2. Čemu musíte věnovat pozornost, než Vám bude přípravek MabThera podán
3. Jak se přípravek MabThera podává
4. Možné nežádoucí účinky
5. Jak přípravek MabThera uchovávat
6. Obsah balení a další informace
1. Co je přípravek MabThera a k čemu se používá Co je přípravek MabThera
Přípravek MabThera obsahuje léčivou látku „rituximab“. To je zvláštní druh bílkoviny nazývaný „monoklonální protilátka“. Váže se na povrch jednoho typu bílých krvinek nazývaných „B lymfocyty“. Po vazbě na povrch této buňky rituximab navodí její zánik.
Přípravek MabThera je dostupný jako léčivý přípravek podávaný kapačkou (MabThera 100 mg nebo MabThera 500 mg, koncentrát pro infuzní roztok) a nebo jako léčivý přípravek podávaný injekčně pod kůži (MabThera 1400 mg nebo MabThera 1600 mg, subkutánní injekční roztok).
K čemu se přípravek MabThera používá
Přípravek MabThera 1400 mg se používá k léčbě nehodgkinského lymfomu u dospělých.
• To je onemocnění lymfatické tkáně (část imunitního systému), která ovlivňuje jeden typ bílých krvinek nazývaných B lymfocyty.
Přípravek MabThera 1400 mg může být podán samostatně nebo s jinými dalšími léky nazývanými „chemoterapeutika“.
Vždy na začátku léčby Vám přípravek MabThera bude podán kapačkou (intravenózní infuze).
Potom Vám bude přípravek MabThera podán injekčně pod kůži. Váš lékař rozhodne, kdy začít s injekčním podáním přípravku MabThera.
U pacientů, u kterých je léčba účinná, může být přípravek MabThera používán v udržovací léčbě po dobu 2 let po dokončení úvodní léčby.
2. Čemu musíte věnovat pozornost, než Vám bude přípravek MabThera podán
Nepoužívejte přípravek MabThera pokud:
• jste alergický(á) na rituximab, na jiné proteiny podobného typu nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6)
• jste alergický(á) na hyaluronidázu (enzym, který napomáhá ke zvýšení absorpce injektované léčivé látky)
máte aktivní, závažné infekční onemocnění máte výrazně sníženou funkci imunitního systému.
Nepoužívejte přípravek MabThera, pokud se Vás cokoliv z výše uvedeného týká. Pokud si nejste jistý(á), zeptejte se svého lékaře, lékárníka nebo zdravotní sestry dříve, než Vám bude přípravek MabThera podán.
Upozornění a opatření
Předtím, než Vám bude podán přípravek MabThera, poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou, pokud:
• jste někdy měl(a) nebo možná právě máte žloutenku. To je proto, že v některých případech by přípravek MabThera mohl znovu vyvolat žloutenku typu B (hepatitidu B), která může velmi vzácně vést k úmrtí. U pacientů s anamnézou hepatitidy B musí lékař pečlivě sledovat příznaky aktivní hepatitidy B.
• jste někdy trpěl(a) onemocněním srdce (jako je angina, palpitace nebo selhání srdce) nebo pokud jste někdy měl(a) obtíže s dýcháním.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán. Lékař Vám bude muset během léčby přípravkem MabThera věnovat zvláštní péči.
Děti a dospívající
Poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve než Vám bude přípravek MabThera podán, pokud jste Vy nebo Vaše dítě mladší 18 let. To je z důvodu, že není k dispozici mnoho informací o používání přípravku MabThera u dětí a dospívajících.
Další léčivé přípravky a přípravek MabThera
Informujte svého lékaře, lékárníka nebo zdravotní sestru o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. To se týká i léků, které jsou dostupné bez lékařského předpisu a rostlinných přípravků. Důvodem je, že přípravek MabThera může ovlivňovat způsob účinku některých dalších léků. Stejně tak ostatní léky mohou ovlivňovat účinek přípravku MabThera.
Konkrétně, informujte svého lékaře:
• jestliže užíváte léky na vysoký krevní tlak. Můžete být požádán(a), abyste tyto léky neužíval(a) 12 hodin předtím, než Vám bude podán přípravek MabThera. To je proto, že u některých osob dochází během podání přípravku MabThera k poklesu krevního tlaku.
• jestliže jste v minulosti užíval(a) léky, které mohou ovlivnit Váš imunitní systém, jako jsou chemoterapeutika nebo imunosupresiva.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán.
Těhotenství a kojení
Musíte sdělit svému lékaři nebo zdravotní sestře, že jste těhotná, nebo že si nejste jistá, zda nejste těhotná, nebo že zamýšlíte otěhotnět. Přípravek MabThera je totiž protilátka, která může procházet placentou a ovlivnit dítě.
Pokud byste mohla otěhotnět, musíte Vy i Váš partner během léčby přípravkem MabThera a ještě 12 měsíců po jejím ukončení používat účinné antikoncepční prostředky.
Nekojte během Vaší léčby přípravkem MabThera. Nekojte také 12 měsíců po ukončení Vaší poslední léčby přípravkem MabThera. Přípravek MabThera může procházet do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Není známo, zda přípravek MabThera ovlivňuje schopnost řídit, používat některé přístroje nebo obsluhovat stroje.
Jak se přípravek MabThera podává
3.
Jak se přípravek podává
Přípravek MabThera Vám bude podávat Váš lékař nebo zdravotní sestra, kteří mají zkušenosti s užíváním této léčby. Budou Vás pečlivě sledovat během podání tohoto léčivého přípravku. Je to pro případ, že by se u Vás projevila nežádoucí reakce.
Vždy na začátku léčby Vám přípravek MabThera bude podán kapačkou (intravenózní infuze).
Potom Vám bude přípravek MabThera podán injekčně pod kůži (podkožní injekce) po dobu přibližně 5 minut. Na skleněné injekční lahvičce je odlepovací nálepka s informacemi o přípravku. Před podáním injekce Váš lékař nebo sestra přelepí nálepku na injekční stříkačku.
Váš lékař rozhodne, kdy začít s injekčním podáním přípravku MabThera.
Při injekci pod kůži se přípravek podává v oblasti břicha, nepodává se do jiných částí těla ani do oblastí břicha, kde je kůže zarudlá, kde je modřina, kde je kůže citlivá, ztvrdlá nebo tam, kde jsou mateřská znaménka nebo jizvy.
Léčivé přípravky podávané před každým podáním přípravku MabThera
Před podáním přípravku MabThera Vám budou podány další léky (premedikace) k zabránění nebo ke snížení možného rizika nežádoucích účinků.
Kolik a jak často budete dostávat Vaší léčbu
• Přípravek MabThera Vám bude podáván ve stejný den jako chemoterapie. Většinou je podáván každé 3 týdny, celkem 8krát.
• Pokud budete dobře reagovat na léčbu, může Vám být přípravek MabThera podáván v rámci udržovací léčby každé 2 nebo 3 měsíce po dobu 2 let.
V závislosti na tom, jak budete reagovat na tento léčivý přípravek, Váš lékař může toto dávkování změnit.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Většina nežádoucích účinků je mírného až středně závažného stupně, některé však mohou být závažné a mohou vyžadovat léčbu. Vzácně mohou některé z těchto účinků vést k úmrtí.
Reakce v místě injekce
U mnoha pacientů se v místě, kde byl přípravek MabThera injekčně podán, vyskytly lokálně nežádoucí účinky. Tyto zahrnovaly: bolesti, otok, modřinu, krvácení, zarudnutí kůže, svědění a vyrážku.
Pokud jsou tyto reakce závažné, Váš lékař se může rozhodnout ukončit Vaši léčbu přípravkem MabThera.
Infekce
Informujte ihned svého lékaře, pokud se u Vás objeví jakékoli příznaky infekčního onemocnění:
• horečka, kašel, bolest v krku, pocit pálení při močení nebo pocit slabosti nebo se celkově nebudete cítit dobře
• ztráta paměti, poruchy myšlení, problémy s chůzí či ztráta zraku - to může být způsobeno
z důvodu velmi vzácné závažné mozkové infekce, která vede k úmrtí (progresivní multifokální leukoencefalopatie nebo zkráceně PML).
V důsledku léčby přípravkem MabThera se může projevit vyšší náchylnost k infekcím. Často jde
pouze o nachlazení, mohou se však vyskytnout případy zápalu plic nebo infekce močových cest. Tyto
jsou uvedeny níže v odstavci „Další nežádoucí účinky“.
Další nežádoucí účinky zahrnují:
Velmi časté nežádoucí účinky (mohou se vyskytnout u více než 1 pacienta z 10):
• bakteriální nebo virová infekce, zánět průdušek (bronchitida)
• pokles počtu bílých krvinek provázený horečkou nebo bez horečky nebo snížení počtu krevních destiček
• nevolnost (nausea)
• vypadávání vlasů na temeni hlavy, zimnice, bolesti hlavy
• snížená imunita - z důvodu poklesu hladiny protilátek nazývaných “imunoglobuliny” (IgG) v krvi, které se podílejí na ochraně proti infekci.
Časté nežádoucí účinky (mohou se vyskytnout až u 1 pacienta z 10):
• infekce krve (sepse) a zápal plic, pásový opar, nachlazení, infekce dýchacích cest, plísňová infekce, infekce neznámého původu, infekce dutin, žloutenka typu B
• pokles počtu červených krvinek (anémie), pokles počtu všech krevních buněk
• alergické reakce (přecitlivělost)
• zvýšená hladina cukru, pokles hmotnosti, otoky v obličeji či v celém těle, vzestup hladiny enzymu LDH v krvi, pokles hladiny vápníku v krvi
• poruchy kožního čití jako například snížená citlivost, brnění, bodání, pálení, nepříjemné pocity, zhoršení hmatu
• pocity podrážděnosti, potíže s usínáním
• zrudnutí v obličeji a tvorba kožních podlitin jako důsledek rozšíření krevních cév
• závratě nebo úzkost
• zvýšená tvorba slz, poruchy slzného kanálku, záněty očí (zánět spojivek)
• hučení v uších, bolest uší
• srdeční obtíže - jako jsou infarkt myokardu, nepravidelná nebo zrychlená srdeční činnost
• vzestup či pokles krevního tlaku (snížení krevního tlaku po postavení)
• stažení svalů dýchacích cest způsobující sípání (bronchospasmus), zánět, podráždění na hrudi, v hrdle nebo dutinách, dušnost, rýma
• nevolnost (zvracení), průjem, bolest břicha, podráždění nebo vřídky v hrdle a ústech, poruchy polykání, zácpa, trávicí obtíže
• poruchy příjmu potravy, snížení množství přijímané potravy s následným nebezpečím poklesu hmotnosti
• kopřivka, zvýšené pocení, noční poty
• svalové poruchy - jako jsou napětí svalů, bolesti kloubů nebo svalů, bolesti zad a krku
• bolest vyvolaná nádorem
• celkové nepohodlí nebo pocit stísněnosti nebo únava, třes, příznaky podobné chřipce
• poruchy více tělních orgánů.
Méně časté nežádoucí účinky (mohou se vyskytnout až u 1 pacienta ze 100):
• poruchy krevní srážlivosti, pokles tvorby červených krvinek, zvýšená destrukce červených krvinek (aplastická hemolytická anémie), otok nebo zvětšení lymfatických uzlin
• pokles nálady a ztráta zájmu a potěšení z obvyklých činností, nervozita
• poruchy vnímání chuti - jako například změna vnímání, jak věci chutnají
srdeční obtíže - jako například zpomalení srdečního rytmu nebo bolest na hrudi (angina) astma, nedostatečné okysličení tělesných orgánů zvětšení břicha.
Velmi vzácné nežádoucí účinky (mohou se vyskytnout až u 1 pacienta z 10 000):
• krátkodobé zvýšení množství některých typů protilátek v krvi (zvané imunoglobuliny - IgM), chemické poruchy krve způsobené rozpadem zničených rakovinových buněk
• poškození nervů v rukách a nohách, ochrnutí obličeje
• srdeční selhání
• záněty krevních cév včetně těch, které vedou ke kožním příznakům
• respirační (plicní) selhání
• perforace (proděravění) střevní stěny
• závažné puchýřky na kůži, které mohou být život ohrožující
• selhání ledvin
• závažná ztráta zraku (známka poškození nervů v mozku).
Není známo (nežádoucí účinky vyskytující se s neznámou četností):
• snížení bílých krvinek, ke kterému dochází se zpožděním
• okamžité snížení počtu krevních destiček související s infuzí - to může být vratné, ale ve vzácných případech to může končit úmrtím
• ztráta sluchu, ztráta jiných smyslů.
Přípravek MabThera může rovněž způsobit změny laboratorních testů, které Vám provádí Váš lékař.
Používáte-li přípravek MabThera v kombinaci s jinými přípravky, mohou se u Vás objevit nežádoucí účinky spojené s užíváním jiného přípravku.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek MabThera uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce za „Použitelné do:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2 °C - 8 °C). Chraňte před mrazem. Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
Obsah balení a další informace
6.
Co přípravek MabThera 1400 mg subkutánní injekční roztok obsahuje
• Léčivou látkou je rituximab. Jedna injekční lahvička obsahuje 1400 mg/11,7 ml rituximabu.
V jednom ml je obsaženo 120 mg rituximabu.
• Dalšími složkami jsou biosyntetická lidská hyaluronidáza, histidin, monohydrát histidin-hydrochloridu, dihydrát trehalózy, methionin, polysorbát 80 a voda na injekci.
Jak přípravek MabThera 1400 mg subkutánní injekční roztok vypadá a co obsahuje toto balení
Přípravek MabThera je přípraven k použití, je to čirá až opalescentní, bezbarvá až nažloutlá tekutina, dodávaná ve formě subkutánního injekčního roztoku v bezbarvé skleněné injekční lahvičce s butylovou gumovou zátkou, hliníkovým těsněním a růžovým strhávacím plastovým víčkem.
Jedna injekční lahvička obsahuje 1400 mg/11,7 ml rituximabu. Balení obsahuje 1 injekční lahvičku.
Držitel rozhodnutí o registraci
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
Výrobce
Roche Pharma AG Emil-Barell-Str. 1 D-79639 Grenzach-Wyhlen Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Belgie/Belgique/Belgien
N.V. Roche S.A.
Tél/Tel: +32 (0) 2 525 82 11
Btnrapnn
Pom Enarapna EOOfl Ten +359 2 818 44 44
Česká republika
Roche s. r. o.
Tel: +420 - 2 20382111
Danmark
Roche a/s
Tlf: +45 - 36 39 99 99
Deutschland
Roche Pharma AG Tel: +49 (0) 7624 140
|
Eesti Roche Eesti OU Tel: + 372 - 6 177 380 |
Norge Roche Norge AS Tlf: +47 - 22 78 90 00 |
|
EXlába Roche (Hellas) A.E. Tnk: +30 210 61 66 100 |
Osterreich Roche Austria GmbH Tel: +43 (0) 1 27739 |
|
Espaňa Roche Farma S.A. Tel: +34 - 91 324 81 00 |
Polska Roche Polska Sp.z o.o. Tel: +48 - 22 345 18 88 |
|
France Roche Tél: +33 (0) 1 47 61 40 00 |
Portugal Roche Farmaceutica Química, Lda Tel: +351 - 21 425 70 00 |
|
Hrvatska Roche d.o.o. Tel: + 385 1 47 22 333 |
Románia Roche Románia S.R.L. Tel: +40 21 206 47 01 |
|
Ireland Roche Products (Ireland) Ltd. Tel: +353 (0) 1 469 0700 |
Slovenija Roche farmacevtska družba d.o.o. Tel: +386 - 1 360 26 00 |
|
Island Roche a/s c/o Icepharma hf Sími: +354 540 8000 |
Slovenská republika Roche Slovensko, s.r.o. Tel: +421 - 2 52638201 |
|
Italia Roche S.p.A. Tel: +39 - 039 2471 |
Suomi/Finland Roche Oy Puh/Tel: +358 (0) 10 554 500 |
|
Kónpoq r.A.Exapáxn? & Eia AxS. Tnk: +357 - 22 76 62 76 |
Sverige Roche AB Tel: +46 (0) 8 726 1200 |
|
Latvija Roche Latvija SIA Tel: +371 - 6 7039831 |
United Kingdom Roche Products Ltd. Tel: +44 (0) 1707 366000 |
Tato příbalová informace byla naposledy revidována {měsíc RRRR}.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
Příbalová informace: informace pro pacienta
MabThera 1600 mg subkutánní injekční roztok
rituximabum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
• Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
• Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
• Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je přípravek MabThera a k čemu se používá
2. Čemu musíte věnovat pozornost, než Vám bude přípravek MabThera podán
3. Jak se přípravek MabThera podává
4. Možné nežádoucí účinky
5. Jak přípravek MabThera uchovávat
6. Obsah balení a další informace
1. Co je přípravek MabThera a k čemu se používá
Co je přípravek MabThera
Přípravek MabThera obsahuje léčivou látku „rituximab“. To je zvláštní druh bílkoviny nazývaný „monoklonální protilátka“. Váže se na povrch jednoho typu bílých krvinek nazývaných „B lymfocyty“. Po vazbě na povrch této buňky rituximab navodí její zánik.
Přípravek MabThera je dostupný jako léčivý přípravek podávaný kapačkou (MabThera 100 mg nebo MabThera 500 mg, koncentrát pro infuzní roztok) a nebo jako léčivý přípravek podávaný injekčně pod kůži (MabThera 1400 mg nebo MabThera 1600 mg, subkutánní injekční roztok).
K čemu se přípravek MabThera používá
Přípravek MabThera 1600 mg se používá k léčbě chronické lymfocytární leukemie u dospělých.
• Chronická lymfocytární leukemie (CLL) je nejčastější formou leukemie u dospělých. CLL
postihuje typ bílých krvinek nazývaných B lymfocyty, které pocházejí z kostní dřeně a vyvíjejí se v lymfatických uzlinách. Pacienti s CLL mají příliš mnoho odchylných lymfocytů, které se hromadí především v kostní dřeni a krvi. Množení těchto odchylných B lymfocytů je příčinou příznaků, kterými pravděpodobně trpíte.
Přípravek MabThera v kombinaci s chemoterapií tyto buňky ničí a ty jsou pak postupně z těla odstraňovány biologickými procesy.
Přípravek MabThera 1600 mg Vám bude podán s dalšími léky nazývanými „chemoterapeutika“.
Vždy na začátku léčby Vám přípravek MabThera bude podán kapačkou (intravenózní infuze).
Potom Vám bude přípravek MabThera podán injekčně pod kůži. Váš lékař rozhodne, kdy začít s injekčním podáním přípravku MabThera.
2. Čemu musíte věnovat pozornost, než Vám bude přípravek MabThera podán
Nepoužívejte přípravek MabThera pokud:
• jste alergický(á) na rituximab, na jiné proteiny podobného typu nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6)
• jste alergický(á) na hyaluronidázu (enzym, který napomáhá ke zvýšení absorpce injektované léčivé látky)
máte aktivní, závažné infekční onemocnění máte výrazně sníženou funkci imunitního systému.
Nepoužívejte přípravek MabThera, pokud se Vás cokoliv z výše uvedeného týká. Pokud si nejste jistý(á), zeptejte se svého lékaře, lékárníka nebo zdravotní sestry dříve, než Vám bude přípravek MabThera podán.
Upozornění a opatření
Předtím, než Vám bude podán přípravek MabThera, poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou, pokud:
• jste někdy měl(a) nebo možná právě máte žloutenku. To je proto, že v některých případech by přípravek MabThera mohl znovu vyvolat žloutenku typu B (hepatitidu B), která může velmi vzácně vést k úmrtí. U pacientů s anamnézou hepatitidy B musí lékař pečlivě sledovat příznaky aktivní hepatitidy B.
• jste někdy trpěl(a) onemocněním srdce (jako je angina, palpitace nebo selhání srdce) nebo pokud jste někdy měl(a) obtíže s dýcháním.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán. Lékař Vám bude muset během léčby přípravkem MabThera věnovat zvláštní péči.
Děti a dospívající
Poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve než Vám bude přípravek MabThera podán, pokud jste Vy nebo Vaše dítě mladší 18 let. To je z důvodu, že není k dispozici mnoho informací o používání přípravku MabThera u dětí a dospívajících.
Další léčivé přípravky a přípravek MabThera
Informujte svého lékaře, lékárníka nebo zdravotní sestru o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. To se týká i léků, které jsou dostupné bez lékařského předpisu a rostlinných přípravků. Důvodem je, že přípravek MabThera může ovlivňovat způsob účinku některých dalších léků. Stejně tak ostatní léky mohou ovlivňovat účinek přípravku MabThera.
Konkrétně, informujte svého lékaře:
• jestliže užíváte léky na vysoký krevní tlak. Můžete být požádán(a), abyste tyto léky neužíval(a) 12 hodin předtím, než Vám bude podán přípravek MabThera. To je proto, že u některých osob dochází během podání přípravku MabThera k poklesu krevního tlaku.
• jestliže jste v minulosti užíval(a) léky, které mohou ovlivnit Váš imunitní systém, jako jsou chemoterapeutika nebo imunosupresiva.
Pokud se Vás cokoliv z výše uvedeného týká (nebo si nejste jistý(á)), poraďte se se svým lékařem, lékárníkem nebo zdravotní sestrou dříve, než Vám bude přípravek MabThera podán.
Těhotenství a kojení
Musíte sdělit svému lékaři nebo zdravotní sestře, že jste těhotná, nebo že si nejste jistá, zda nejste těhotná, nebo že zamýšlíte otěhotnět. Přípravek MabThera je totiž protilátka, která může procházet placentou a ovlivnit dítě.
Pokud byste mohla otěhotnět, musíte Vy i Váš partner během léčby přípravkem MabThera a ještě 12 měsíců po jejím ukončení používat účinné antikoncepční prostředky.
Nekojte během Vaší léčby přípravkem MabThera. Nekojte také 12 měsíců po ukončení Vaší poslední léčby přípravkem MabThera. Přípravek MabThera může procházet do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Není známo, zda přípravek MabThera ovlivňuje schopnost řídit, používat některé přístroje nebo obsluhovat stroje.
Jak se přípravek MabThera podává
3.
Jak se přípravek podává
Přípravek MabThera Vám bude podávat Váš lékař nebo zdravotní sestra, kteří mají zkušenosti s užíváním této léčby. Budou Vás pečlivě sledovat během podání tohoto léčivého přípravku. Je to pro případ, že by se u Vás projevila nežádoucí reakce.
Vždy na začátku léčby Vám přípravek MabThera bude podán kapačkou (intravenózní infuze).
Potom Vám bude přípravek MabThera podán injekčně pod kůži (podkožní injekce) po dobu přibližně 7 minut. Na skleněné injekční lahvičce je odlepovací nálepka s informacemi o přípravku. Před podáním injekce Váš lékař nebo sestra přelepí nálepku na injekční stříkačku.
Váš lékař rozhodne, kdy začít s injekčním podáním přípravku MabThera.
Při injekci pod kůži se přípravek podává v oblasti břicha, nepodává se do jiných částí těla ani do oblastí břicha, kde je kůže zarudlá, kde je modřina, kde je kůže citlivá, ztvrdlá nebo tam, kde jsou mateřská znaménka nebo jizvy.
Léčivé přípravky podávané před každým podáním přípravku MabThera
Před podáním přípravku MabThera Vám budou podány další léky (premedikace) k zabránění nebo ke snížení možného rizika nežádoucích účinků.
Kolik a jak často budete dostávat Vaší léčbu
Jestliže budete léčen(a) přípravkem MabThera v kombinaci s chemoterapií, dostanete infuzi přípravku MabThera nultý den 1. cyklu a poté budete dostávat podkožní injekce 1. den každého následujícího cyklu. Celkový počet cyklů je 6. Každý cyklus trvá 28 dnů. Chemoterapii je třeba podávat po podání přípravku MabThera.
Váš lékař rozhodne, jestli budete dostávat souběžně podávanou podpůrnou léčbu.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Většina nežádoucích účinků je mírného až středně závažného stupně, některé však mohou být závažné a mohou vyžadovat léčbu. Vzácně mohou některé z těchto účinků vést k úmrtí.
Reakce v místě injekce
U mnoha pacientů se v místě, kde byl přípravek MabThera injekčně podán, vyskytly lokálně nežádoucí účinky. Tyto zahrnovaly: bolesti, otok, modřinu, krvácení, zarudnutí kůže, svědění a vyrážku.
Pokud jsou tyto reakce závažné, Váš lékař se může rozhodnout ukončit Vaši léčbu přípravkem MabThera.
Infekce
Informujte ihned svého lékaře, pokud se u Vás objeví jakékoli příznaky infekčního onemocnění:
• horečka, kašel, bolest v krku, pocit pálení při močení nebo pocit slabosti nebo se celkově nebudete cítit dobře
• ztráta paměti, poruchy myšlení, problémy s chůzí či ztráta zraku - to může být způsobeno
z důvodu velmi vzácné závažné mozkové infekce, která vede k úmrtí (progresivní multifokální leukoencefalopatie nebo zkráceně PML).
V důsledku léčby přípravkem MabThera se může projevit vyšší náchylnost k infekcím. Často jde
pouze o nachlazení, mohou se však vyskytnout případy zápalu plic nebo infekce močových cest. Tyto
jsou uvedeny níže v odstavci „Další nežádoucí účinky“.
Další nežádoucí účinky zahrnují:
Velmi časté nežádoucí účinky (mohou se vyskytnout u více než 1 pacienta z 10):
• bakteriální nebo virová infekce, zánět průdušek (bronchitida)
• pokles počtu bílých krvinek provázený horečkou nebo bez horečky nebo snížení počtu krevních destiček
• nevolnost (nausea)
• vypadávání vlasů na temeni hlavy, zimnice, bolesti hlavy
• snížená imunita - z důvodu poklesu hladiny protilátek nazývaných “imunoglobuliny” (IgG) v krvi, které se podílejí na ochraně proti infekci.
Časté nežádoucí účinky (mohou se vyskytnout až u 1 pacienta z 10):
• infekce krve (sepse) a zápal plic, pásový opar, nachlazení, infekce dýchacích cest, plísňová infekce, infekce neznámého původu, infekce dutin, žloutenka typu B
• pokles počtu červených krvinek (anémie), pokles počtu všech krevních buněk
• alergické reakce (přecitlivělost)
• zvýšená hladina cukru, pokles hmotnosti, otoky v obličeji či v celém těle, vzestup hladiny enzymu LDH v krvi, pokles hladiny vápníku v krvi
• poruchy kožního čití jako například snížená citlivost, brnění, bodání, pálení, nepříjemné pocity, zhoršení hmatu
• pocity podrážděnosti, potíže s usínáním
• zrudnutí v obličeji a tvorba kožních podlitin jako důsledek rozšíření krevních cév
• závratě nebo úzkost
• zvýšená tvorba slz, poruchy slzného kanálku, záněty očí (zánět spojivek)
• hučení v uších, bolest uší
• srdeční obtíže - jako jsou infarkt myokardu, nepravidelná nebo zrychlená srdeční činnost
• vzestup či pokles krevního tlaku (snížení krevního tlaku po postavení)
• stažení svalů dýchacích cest způsobující sípání (bronchospasmus), zánět, podráždění na hrudi, v hrdle nebo dutinách, dušnost, rýma
• nevolnost (zvracení), průjem, bolest břicha, podráždění nebo vřídky v hrdle a ústech, poruchy polykání, zácpa, trávicí obtíže
• poruchy příjmu potravy, snížení množství přijímané potravy s následným nebezpečím poklesu hmotnosti
• kopřivka, zvýšené pocení, noční poty
• svalové poruchy - jako jsou napětí svalů, bolesti kloubů nebo svalů, bolesti zad a krku
• bolest vyvolaná nádorem
• celkové nepohodlí nebo pocit stísněnosti nebo únava, třes, příznaky podobné chřipce
• poruchy více tělních orgánů.
Méně časté nežádoucí účinky (mohou se vyskytnout až u 1 pacienta ze 100):
• poruchy krevní srážlivosti, pokles tvorby červených krvinek, zvýšená destrukce červených krvinek (aplastická hemolytická anémie), otok nebo zvětšení lymfatických uzlin
• pokles nálady a ztráta zájmu a potěšení z obvyklých činností, nervozita
• poruchy vnímání chuti - jako například změna vnímání, jak věci chutnají
srdeční obtíže - jako například zpomalení srdečního rytmu nebo bolest na hrudi (angina) astma, nedostatečné okysličení tělesných orgánů zvětšení břicha.
Velmi vzácné nežádoucí účinky (mohou se vyskytnout až u 1 pacienta z 10 000):
• krátkodobé zvýšení množství některých typů protilátek v krvi (zvané imunoglobuliny - IgM), chemické poruchy krve způsobené rozpadem zničených rakovinových buněk
• poškození nervů v rukách a nohách, ochrnutí obličeje
• srdeční selhání
• záněty krevních cév včetně těch, které vedou ke kožním příznakům
• respirační (plicní) selhání
• perforace (proděravění) střevní stěny
• závažné puchýřky na kůži, které mohou být život ohrožující
• selhání ledvin
• závažná ztráta zraku (známka poškození nervů v mozku).
Není známo (nežádoucí účinky vyskytující se s neznámou četností):
• snížení bílých krvinek, ke kterému dochází se zpožděním
• okamžité snížení počtu krevních destiček související s infuzí - to může být vratné, ale ve vzácných případech to může končit úmrtím
• ztráta sluchu, ztráta jiných smyslů.
Přípravek MabThera může rovněž způsobit změny laboratorních testů, které Vám provádí Váš lékař.
Používáte-li přípravek MabThera v kombinaci s jinými přípravky, mohou se u Vás objevit nežádoucí účinky spojené s užíváním jiného přípravku.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek MabThera uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce za „Použitelné do:“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2 °C - 8 °C). Chraňte před mrazem. Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
Obsah balení a další informace
6.
Co přípravek MabThera 1600 mg subkutánní injekční roztok obsahuje
• Léčivou látkou je rituximab. Jedna injekční lahvička obsahuje 1600 mg/13,4 ml rituximabu.
V jednom ml je obsaženo 120 mg rituximabu.
• Dalšími složkami jsou biosyntetická lidská hyaluronidáza, histidin, monohydrát histidin-hydrochloridu, dihydrát trehalózy, methionin, polysorbát 80 a voda na injekci.
Jak přípravek MabThera 1600 mg subkutánní injekční roztok vypadá a co obsahuje toto balení
Přípravek MabThera je přípraven k použití, je to čirá až opalescentní, bezbarvá až nažloutlá tekutina, dodávaná ve formě subkutánního injekčního roztoku v bezbarvé skleněné injekční lahvičce s butylovou gumovou zátkou, hliníkovým těsněním a modrým strhávacím plastovým víčkem.
Jedna injekční lahvička obsahuje 1600 mg/13,4 ml rituximabu. Balení obsahuje 1 injekční lahvičku.
Držitel rozhodnutí o registraci
Roche Registration Limited 6 Falcon Way Shire Park
Welwyn Garden City AL7 1TW Velká Británie
Výrobce
Roche Pharma AG Emil-Barell-Str. 1 D-79639 Grenzach-Wyhlen Německo
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Belgie/Belgique/Belgien
N.V. Roche S.A.
Tél/Tel: +32 (0) 2 525 82 11
Btnrapnn
Pom Enarapna EOOfl Ten +359 2 818 44 44
Česká republika
Roche s. r. o.
Tel: +420 - 2 20382111
Danmark
Roche a/s
Tlf: +45 - 36 39 99 99
Deutschland
Roche Pharma AG Tel: +49 (0) 7624 140
|
Eesti Roche Eesti OU Tel: + 372 - 6 177 380 |
Norge Roche Norge AS Tlf: +47 - 22 78 90 00 |
|
EXlába Roche (Hellas) A.E. Tnk: +30 210 61 66 100 |
Osterreich Roche Austria GmbH Tel: +43 (0) 1 27739 |
|
Espaňa Roche Farma S.A. Tel: +34 - 91 324 81 00 |
Polska Roche Polska Sp.z o.o. Tel: +48 - 22 345 18 88 |
|
France Roche Tél: +33 (0) 1 47 61 40 00 |
Portugal Roche Farmaceutica Química, Lda Tel: +351 - 21 425 70 00 |
|
Hrvatska Roche d.o.o. Tel: + 385 1 47 22 333 |
Románia Roche Románia S.R.L. Tel: +40 21 206 47 01 |
|
Ireland Roche Products (Ireland) Ltd. Tel: +353 (0) 1 469 0700 |
Slovenija Roche farmacevtska družba d.o.o. Tel: +386 - 1 360 26 00 |
|
Island Roche a/s c/o Icepharma hf Sími: +354 540 8000 |
Slovenská republika Roche Slovensko, s.r.o. Tel: +421 - 2 52638201 |
|
Italia Roche S.p.A. Tel: +39 - 039 2471 |
Suomi/Finland Roche Oy Puh/Tel: +358 (0) 10 554 500 |
|
Kónpoq r.A.Exapáxn? & Eia AxS. Tnk: +357 - 22 76 62 76 |
Sverige Roche AB Tel: +46 (0) 8 726 1200 |
|
Latvija Roche Latvija SIA Tel: +371 - 6 7039831 |
United Kingdom Roche Products Ltd. Tel: +44 (0) 1707 366000 |
Tato příbalová informace byla naposledy revidována {měsíc RRRR}.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
185