Incruse 55 Mikrogramů
PŘÍLOHA I
SOUHRN ÚDAJŮ O PŘÍPRAVKU
Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Podrobnosti o hlášení nežádoucích účinků viz bod 4.8.
1. NÁZEV PŘÍPRAVKU
Incruse 55 mikrogramů dávkovaný prášek k inhalaci
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna inhalace poskytuje dávku (podaná dávka, která vychází z náustku) umeclidinium 55 mikrogramů (ve formě umeclidinii bromidum 65 mikrogramů). To odpovídá odměřené dávce umeclidinium 62,5 mikrogramů (ve formě umeclidinii bromidum 74,2 mikrogramů).
Pomocná látka se známým účinkem:
Jedna podaná dávka obsahuje přibližně 12,5 mg laktosy (ve formě monohydrátu).
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Dávkovaný prášek k inhalaci (prášek k inhalaci).
Bílý prášek v šedém inhalátoru (Ellipta) se světle zeleným krytem náustku a počítadlem dávek.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek Incruse je indikován jako udržovací bronchodilatační léčba ke zmírnění příznaků chronické obstrukční plicní nemoci (CHOPN) u dospělých pacientů.
4.2 Dávkování a způsob podání
Dávkování
Dospělí
Doporučená dávka je jedna inhalace umeklidinium-bromidu jednou denně.
K zachování bronchodilatačního účinku je nutné přípravek Incruse podávat jednou denně, každý den ve stejnou dobu.
Maximální dávka je jedna inhalace umeklidinium-bromidu jednou denně.
Zvláštní populace Starší pacienti
U pacientů starších 65 let není úprava dávkování nutná (viz bod 5.2).
Porucha funkce ledvin
U pacientů s poruchou funkce ledvin není úprava dávkování nutná (viz bod 5.2).
Porucha funkce jater
U pacientů s lehkou nebo středně závažnou poruchou funkce jater není úprava dávkování nutná. Přípravek Incruse nebyl hodnocen u pacientů se závažnou poruchou funkce jater, a je třeba ho u takových pacientů používat s opatrností (viz bod 5.2).
Pediatrická populace
U pediatrické populace (do 18 let) neexistují žádné relevantní důvody pro použití přípravku Incruse v indikaci CHOPN.
Způsob podání
Přípravek Incruse je určen pouze k inhalačnímu podání.
Návod k použití
Následující návod k použití pro 30dávkový inhalátor lze rovněž použít pro 7dávkový inhalátor.
Inhalátor ELLIPTA obsahuje odměřené dávky a je připravený přímo k použití.
Inhalátor je uložený v ochranné vaničce obsahující sáček s vysoušedlem, které snižuje vlhkost. Po otevření je nutné sáček s vysoušedlem vyhodit; sáček se neinhaluje ani nejí.
Pacient má být poučen, aby vaničku neotevíral dříve, než bude připraven k inhalaci dávky.
Inhalátor je po prvním vyjmutí ze zatavené vaničky v „uzavřené“ pozici. Označení “Spotřebujte do“ vyjadřuje datum, které by mělo být zapsáno na štítek inhalátoru. Datum „Spotřebujte do“ je 6 týdnů od data otevření vaničky. Po tomto datu se již nemá inhalátor dále používat. Vanička může být znehodnocena po prvním otevření.
Pokud se kryt inhalátoru otevře a zavře bez toho, že by došlo k inhalaci léku, dojde ke ztrátě dávky. Ztracená dávka zůstane bezpečně uzavřená v inhalátoru, ale nebude již dostupná k inhalaci.
Při jedné inhalaci není možné náhodně použít dávku navíc ani dvojnásobnou dávku.
a) Příprava dávky
Pokud jste připraven(a) k použití dávky, otevřete kryt inhalátoru. Inhalátorem netřeste.
Stahujte víčko dolů, dokud neuslyšíte „cvaknutí“. Přípravek je připraven k inhalaci.
Počítadlo dávek pro potvrzení odečetlo 1 dávku. Pokud počítadlo neodečte dávku v okamžiku, kdy uslyšíte „cvaknutí“, inhalátor neumožní inhalaci léku. Vezměte jej zpět k lékárníkovi, aby Vám poradil.
b) Jak se léčivý přípravek inhaluje
Držte inhalátor dále od úst a co nejvíce vydechněte, jak je Vám pohodlné. Nevydechujte do inhalátoru. Vložte náustek mezi rty a pevně jej svými rty stiskněte. Neblokujte vzduchové otvory prsty.
• Jednou se dlouze, rovnoměrně a zhluboka nadechněte. Zadržte dech po co nejdelší dobu (alespoň 3 -4 sekundy).
• Vyjměte inhalátor z úst.
• Pomalu a lehce vydechněte.
Lék by neměl mít žádnou chuť ani by neměl být cítit, a to ani v případě, že se inhalátor použije správně.
c) Uzavření inhalátoru
Pokud chcete náustek očistit, otřete jej před uzavřením suchou tkaninou.
Vysuňte kryt zpět nahoru co nejvíce, až je náustek zakrytý.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Umeklidinium-bromid se nemá používat u pacientů s astmatem, protože u této populace pacientů nebyl přípravek hodnocen.
Paradoxní bronchospasmus
Stejně jako u jiné inhalační léčby, může i podání umeklidinium-bromidu vést k paradoxnímu bronchospasmu, který může být život ohrožující. Pokud dojde k paradoxnímu bronchospasmu, je nutné léčbu okamžitě přerušit a dle potřeby zahájit alternativní léčbu.
Zhoršení základního onemocnění
Umeklidinium-bromid je určen k udržovací léčbě CHOPN. Nesmí se používat ke zmírnění akutních příznaků, tj. jako záchranná léčba k léčbě akutních záchvatů bronchospasmu. Akutní příznaky je nutné léčit podáním inhalačního bronchodilatancia s krátkodobým účinkem. Častější používání krátkodobě působících bronchodilatancií ke zmírnění příznaků ukazuje na zhoršení kontroly onemocnění. V případě zhoršení CHOPN v průběhu léčby umeklidinium-bromidem je třeba přehodnotit zdravotní stav pacienta i režim léčby CHOPN.
Kardiovaskulární účinky
Při podávání antagonistů muskarinových receptorů, včetně umeklidinium-bromidu, se mohou objevit kardiovaskulární účinky jako srdeční arytmie, např. fibrilace síní nebo síňová tachykardie. Pacienti s klinicky významným, léčbou neupraveným, kardiovaskulárním onemocněním byli navíc z klinických studií vyloučeni. Proto je nutné umeklidinium-bromid podávat pacientům se závažným srdečním onemocněním, zejména se srdeční arytmií, s opatrností.
Antimuskarinové účinky
V souladu s antimuskarinovou aktivitou je třeba umeklidinium-bromid podávat pacientům s retencí moči nebo s glaukomem s úzkým úhlem s opatrností.
Pomocné látky
Tento léčivý přípravek obsahuje laktózu. Pacienti se vzácnými dědičnými poruchami s galaktózovou intolerancí, vrozenou deficiencí laktázy nebo malabsorpcí glukózy a galaktózy by tento léčivý přípravek neměli používat.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Klinicky významné lékové interakce zprostředkované umeklidinium-bromidem v klinických dávkách jsou považovány za nepravděpodobné z důvodu nízkých plazmatických koncentrací, kterých je dosaženo po inhalačním podání.
Další antagonisté muskarinových receptorů
Společné podávání umeklidinium-bromidu s jinými dlouhodobě účinkujícími antagonisty muskarinových receptorů nebo s léčivými přípravky obsahujícími tuto látku nebylo hodnoceno a nedoporučuje se, protože může zvýrazňovat známé nežádoucí účinky inhalačně podávaných antagonistů muskarinových receptorů.
Interakce na úrovni metabolismu a transportních systémů
Umeklidinium-bromid je substrátem cytochromu P450 2D6 (CYP2D6). Farmakokinetika umeklidinium-bromidu v rovnovážném stavu byla hodnocena u zdravých dobrovolníků s nedostatkem
CYP2D6 (pomalí metabolizáton). Při podání 4násobně vyšší dávky, než je dávka terapeutická, nebyly pozorovány žádné účinky na AUC ani Cmax umeklidinia. Při podání 8násobně vyšší dávky bylo pozorováno 1,3násobné zvýšení AUC umeklidinium-bromidu bez účinku na Cmax umeklidinium-bromidu. Na základě rozsahu těchto změn se při společném podávání umeklidinia s inhibitory CYP2D6 ani při podávání subjektům s genetickým deficitem aktivity CYP2D6 (pomalí metabolizáton) neočekávají žádné klinicky relevantní lékové interakce.
Umeklidinium-bromid je substrátem transportéru pro glykoprotein P (P-gp). U zdravých dobrovolníků byl hodnocen účinek středně silného inhibitoru P-gp verapamilu (240 mg jednou denně) na farmakokinetiku umeklidinium-bromidu v rovnovážném stavu. Nebyly pozorovány žádné účinky verapamilu na Cmax umeklidinium-bromidu. Bylo pozorováno přibližně 1,4násobné zvýšení AUC umeklidinium-bromidu. Na základě rozsahu těchto změn se při společném podávání umeklidinium-bromidu s inhibitory P-gp neočekávají žádné klinicky relevantní lékové interakce.
Další léčivé přípravky k léčbě CHOPN
Ačkoli nebyly provedeny formální studie lékových interakcí in vivo, byla inhalace umeklidinium-bromidu podávána společně s jinými léčivými přípravky k léčbě CHOPN, včetně krátkodobě i dlouhodobě působících bronchodilatancií se sympatomimetickým účinkem a inhalačních kortikoidů, bez prokázání klinicky významných lékových interakcí.
4.6 Fertilita, těhotenství a kojení
K dispozici nejsou žádné údaje týkající se používání umeklidinium-bromidu u těhotných žen. Studie u zvířat neprokázaly přímé ani nepřímé škodlivé účinky s ohledem na reprodukční toxicitu (viz bod 5.3).
Umeklidinium-bromid se má v průběhu těhotenství používat pouze tehdy, pokud očekávaný prospěch pro matku převáží možná rizika pro plod.
Kojení
Není známo, zda se umeklidinium-bromid vylučuje do mateřského mléka. Riziko pro novorozence/kojence nelze vyloučit.
Při rozhodování, zda přerušit kojení nebo přerušit léčbu přípravkem Incruse, je třeba vzít v úvahu prospěch z kojení pro dítě a prospěch z léčby pro ženu.
Fertilita
K dispozici nejsou žádné údaje týkající se účinků umeklidinium-bromidu na fertilitu u člověka. Studie u zvířat neprokázaly žádné účinky umeklidinium-bromidu na fertilitu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Umeklidinium-bromid nemá žádný nebo má pouze zanedbatelný vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky Souhrn bezpečnostního profilu
Nejčastěji hlášenými nežádoucími účinky přípravku Incruse byly nazofaryngitida a infekce horních cest dýchacích.
Seznam nežádoucích účinků v tabulce
Bezpečnostní profil umeklidinium-bromidu byl hodnocen u 1 663 pacientů s CHOPN, kteří dostávali po dobu jednoho roku dávky 55 mikrogramů nebo vyšší. To zahrnovalo i 576 pacientů, kteří dostávali doporučenou dávku 55 mikrogramů jednou denně.
Četnosti přiřazené jednotlivým nežádoucím účinkům uvedeným v tabulce níže zahrnují přibližný výskyt incidence zaznamenaný ve čtyřech studiích účinnosti a v jedné dlouhodobé studii bezpečnosti (která zahrnovala 1 412 pacientů léčených umeklidinium-bromidem).
Četnosti nežádoucích účinků jsou definovány s použitím následující konvence: velmi časté (> 1/10), časté (> 1/100 až < 1/10), méně časté (> 1/1 000 až < 1/100), vzácné (> 1/10 000 až < 1/1 000), velmi vzácné (< 1/10 000) a není známo (z dostupných údajů nelze určit).
|
Třídy orgánových systémů |
Nežádoucí účinek |
Četnost |
|
Infekce a infestace |
Nazofaryngitida Infekce horních cest dýchacích Infekce močových cest Sinusitida Faryngitida |
Časté Časté Časté Časté Méně časté |
|
Poruchy nervového systému |
Bolest hlavy Dysgeuzie |
Časté Méně časté |
|
Srdeční poruchy |
Fibrilace síní Idioventrikulární rytmus Supraventrikulární tachykardie Supraventrikulární extrasystoly Tachykardie |
Méně časté Méně časté Méně časté Méně časté Časté |
|
Respirační, hrudní a mediastinální poruchy |
Časté | |
|
Gastrointestinální poruchy |
Zácpa Sucho v ústech |
Méně časté Méně časté |
|
Poruchy kůže a podkožní tkáně |
Méně časté |
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Předávkování umeklidinium-bromidem pravděpodobně povede k subjektivním a objektivním příznakům odpovídajícím známým nežádoucím účinkům inhalačních antagonistů muskarinových receptorů (např. sucho v ústech, poruchy akomodace a tachykardie).
Pokud dojde k předávkování, je třeba zavést podpůrná opatření s odpovídající monitorací v případě potřeby.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Léčiva k terapii onemocnění spojených s obstrukcí dýchacích cest, anticholinergika, ATC kód: R03BB07.
Mechanismus účinku
Umeklidinium-bromid je dlouhodobě působící antagonista muskarinových receptorů (rovněž nazývaný anticholinergikum). Je to derivát chinuklidinu, který je antagonistou muskarinových receptorů s aktivitou napříč mnoha podtypy muskarinových cholinergních receptorů. Umeklidinium-bromid vykazuje svoji bronchodilatační aktivitu kompetitivní inhibicí vazby acetylcholinu s muskarinovými cholinergními
receptory v hladké svalovině dýchacích cest. Vykazuje pomalou reverzibilitu na M3 podtypu muskarinových receptorů u člověka in vitro a dlouhodobý účinek in vivo, pokud se v preklinických modelech podával přímo do plic.
Farmakodynamické účinky
V šestiměsíční studii fáze III (DB2113373) vykazoval přípravek Incruse klinicky významné zlepšení oproti placebu při hodnocení plicních funkcí (měřeno pomocí forsírovaného expiračního objemu za první sekundu [FEVi]) v průběhu 24 hodin při podávání jednou denně, které bylo zřejmé po 30 minutách po podání první dávky (zlepšení ve srovnání s placebem o 102 ml, p < 0,0011). Průměrné maximální zlepšení FEVi v průběhu prvních 6 hodin po podání dávky oproti placebu ve 24. týdnu bylo 130 ml (p < 0,0011). V průběhu léčby nebyla v účinku přípravku Incruse zaznamenána tachyfylaxe.
Srdeční elektrofyziologie
Účinky umeklidinia v dávce 500 mikrogramů (nominální dávka) na QT interval byly hodnoceny v placebem a aktivním komparátorem (moxifloxacin) kontrolované klinické studii hodnotící QT interval u 103 zdravých dobrovolníků. Při podávání opakovaných dávek umeklidinia (500 mikrogramů) jednou denně po dobu 10 dnů nebyly pozorovány žádné účinky na prodloužení QT intervalu (korekce s použitím metody dle Fridericia) ani na srdeční frekvenci.
Klinická účinnost
Klinická účinnost přípravku Incruse podávaného jednou denně byla hodnocena u 904 dospělých pacientů s klinickou diagnózou CHOPN léčených umeklidinium-bromidem nebo placebem v průběhu dvou pivotních klinických studií fáze III: 12týdenní studii (AC4115408) a 24týdenní studii (DB2113373).
Pivotní studie účinnosti
Účinky na plicní funkce
Přípravek Incruse vykazoval ve 12týdenní a 24týdenní pivotní studii statisticky i klinicky významné zlepšení plicních funkcí [definované jako změna výchozích hodnot minimálního FEV1 (prebronchodilatační hodnoty FEV1) ve 12. a 24. týdnu, což byl primární cílový parametr účinnosti v obou studiích] oproti placebu (viz tabulka 1). Bronchodilatační účinky přípravku Incruse oproti placebu byly zřejmé po prvním dni léčby v obou studiích a zůstávaly zachovány v průběhu 12týdenního i 24týdenních období léčby.
V průběhu léčby nedocházelo k oslabení bronchodilatačního účinku.
Tabulka 1: Minimální FEV1 (ml) ve 12. a 24. týdnu (primární cílový parametr)
|
Léčba přípravkem Incruse 55 mcg |
12týdenní studie rozdíl v léčbě1 95% intervaly spolehlivosti Hodnota - p |
24týdenní studie rozdíl v léčbě1 95% intervaly spolehlivosti Hodnota - p |
|
Versus |
127 |
115 |
|
placebo |
(52, 202) |
(76, 155) |
|
< 0,001 |
< 0,001 |
mcg = mikrogramy
1S použitím metody nejmenších čtverců (95% interval spolehlivosti)
Přípravek Incruse vykazoval ve 12týdenní pivotní studii statisticky významně větší zlepšení od výchozích hodnot ve 12. týdnu u vážených průměrů FEV1 v průběhu 0 - 6 hodin po podání dávky oproti placebu (166 ml, p < 0,001). Přípravek Incruse vykazoval ve 24týdenní pivotní studii větší zlepšení od výchozích hodnot ve 24. týdnu u vážených průměrů FEVi v průběhu 0 - 6 hodin po podání dávky oproti placebu (150 ml, p < 0,0012).
Symptomatické výsledky Dusnost:
Přípravek Incruse nevykazoval ve 12týdenní studii statisticky významné zlepšení v indexu přechodné dušnosti TDI ve 12. týdnu ve srovnání s placebem (1,0 jednotky; p = 0,05). U přípravku Incruse bylo ve 24týdenní studii prokázáno statisticky významné zlepšení indexu TDI ve srovnání s placebem ve 24. týdnu (1,0 jednotky; p < 0,001).
Poměr pacientů, kteří reagovali alespoň minimálním klinicky významným rozdílem (MCID, minimum clinically important difference) 1 jednotky indexu TDI ve 12. týdnu, byl ve 12týdenní studii vyšší u přípravku Incruse (38 %) ve srovnání s placebem (15 %). Podobně vyšší poměr pacientů dosáhl ve 24. týdnu > 1 jednotku indexu TDI u přípravku Incruse (53 %) ve srovnání s placebem (41 %) ve 24týdenní studii.
Kvalita života v souvislosti se zdravím:
Přípravek Incruse rovněž vykázal statisticky významné zlepšení kvality života v souvislosti se zdravím hodnoceným s použitím dotazníku SGRQ (St. George’s Respiratory Questionnaire), což bylo prokázáno snížením celkového skóre SGRQ ve 12. týdnu ve srovnání s placebem (-7,90 jednotky, p < 0,001) ve 12týdenní studii. Větší zlepšení ve srovnání s placebem ve změně od výchozích hodnot při použití dotazníku SGRQ vykázal přípravek Incruse ve 24. týdnu (-4,69 jednotky, p < 0,0012) ve 24týdenní studii.
Poměr pacientů, kteří reagovali alespoň MCID ve skóre SGRQ (definovaném jako snížení o 4 jednotky od výchozích hodnot) ve 12. týdnu, byl vyšší u přípravku Incruse 55 mikrogramů (44 %) ve srovnání s placebem (26 %) ve 12týdenní studii. Podobně větší poměr pacientů dosáhl alespoň MCID u přípravku Incruse (44 %) ve srovnání s placebem (34 %) ve 24. týdnu ve 24týdenní studii.
Exacerbace CHOPN
Přípravek Incruse snižoval ve 24. týdnu riziko exacerbace CHOPN ve srovnání s placebem (analýza doby do první exacerbace, poměr rizik 0,6; p < 0,0352). Pravděpodobnost výskytu exacerbace u pacientů léčených přípravkem Incruse ve 24. týdnu byla 8,9 % ve srovnání s 13,7 % u placeba. Tyto studie nebyly speciálně vytvořeny, aby zhodnotily účinek léčby na exacerbaci CHOPN, a pokud došlo k exacerbaci, pacienti byli ze studie vyloučeni.
Použití záchranné medikace
Ve 12týdenní studii přípravek Incruse statisticky významně snižoval nutnost použití záchranné medikace se salbutamolem ve srovnání s placebem (průměrné snížení o 0,7 vstřiků za den v průběhu 12 týdnů, p = 0,025) a vykazoval vyšší procento výskytu dnů bez nutnosti použití záchranné medikace (průměrně 46,3 %) ve srovnání s placebem (průměrně 35,2 %, u tohoto cílového parametru nebyla provedena formální statistická analýza). Ve 24týdenní studii léčby přípravkem Incruse byla průměrná (SD) změna od výchozích hodnot, pokud jde o počet vstřiků záchranné medikace salbutamolem, v průběhu 24 týdnů léčby -1,4 (0,20) u placeba a -1,7 (0,16) u přípravku Incruse (rozdíl = -0,03; 95% CI: -0,8; 0,2; p = 0,276). Pacienti léčení přípravkem Incruse vykazovali vyšší procento dnů bez nutnosti použití záchranné medikace (v průměru 31,1 %) ve srovnání s placebem (průměrně 21,7 %). U tohoto cílového parametru nebyly provedeny formální statistické analýzy.
Podpůrné studie účinnosti
Ve dvou 12týdenních placebem kontrolovaných studiích (200109 a 200110) vedlo, přidání přípravku Incruse k flutikason-furoátu/vilanterolu (FF/VI) (92/22 mikrogramů) jednou denně u dospělých pacientů s klinickou diagnózou CHOPN ke statisticky významnému a klinicky důležitému zlepšení v primárním parametru účinnosti FEVj v den 85 ve srovnání s placebem plus FF/VI (124 ml (95% CI 93, 154, p < 0,001) a 122 ml (95% CI 91, 152, p < 0,001)).
Zlepšení funkce plic bylo podpořeno snížením použití salbutamolu v týdnech 1-12 (-0,4 vstřiků za den (95% CI -0,7; -0,2; p < 0,001) a -0,3 vstřiků za den (95% CI -0,5; -0,1; p = 0,003)) ve srovnání s placebem plus FF/VI, ale zlepšení SGRQ ve 12. týdnu nebylo statisticky signifikantní (200109), nebo klinicky významné (200109 a 200110). Krátké trvání studií a omezený počet exacerbačních příhod brání jakýmkoliv závěrům ohledně dodatečného účinku přípravku Incruse na míru exacerbací CHOPN.
V těchto studiích nebyly identifikovány žádné nové nežádoucí účinky související s přidáním přípravku Incruse k FF/VI.
Pediatrická populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem Incruse u všech podskupin pediatrické populace s CHOPN (informace o použití u dětí viz bod 4.2).
5.2 Farmakokinetické vlastnosti
Absorpce
Po inhalačním podání umeklidinium-bromidu zdravým dobrovolníkům bylo Cmax dosaženo za 5 až 15 minut. Absolutní biologická dostupnost po inhalačním podání umeklidinium-bromidu byla průměrně 13 % dávky, se zanedbatelným podílem z perorální absorpce. Po opakovaných inhalacích umeklidinium-bromidu bylo rovnovážného stavu dosaženo během 7 až 10 dnů, s 1,5 až 1,8násobnou kumulací.
Distribuce
Po intravenózním podání zdravým subjektům byl průměrný distribuční objem 86 litrů. Vazba na plazmatické bílkoviny v lidské plazmě in vitro byla průměrně 89 %.
Biotransformace
Studie in vitro prokázaly, že umeklidinium-bromid je metabolizován převážně cytochromem P450 2D6 (CYP2D6) a je substrátem transportéru pro glykoprotein P (P-gp). Primární metabolické cesty umeklidinium-bromidu jsou oxidativní (hydroxylace, O-dealkylace), následované konjugací (glukuronidace, atd.) a vedou k množství metabolitů se sníženou farmakologickou aktivitou, nebo metabolitů, u kterých nebyla farmakologická aktivita stanovena. Systémová expozice těmto metabolitům je nízká.
Eliminace
Plasmatická clearance po intravenózním podání byla 151 litrů/hodinu. Po intravenózním podání je přibližně 58 % podané radioaktivně značené dávky (nebo 73 % zachycené radioaktivity) vyloučeno stolicí do 192 hodin po podání dávky. Vylučování močí se na vylučování radioaktivně značené dávky do 168 hodin podílí 22 % (27 % zachycené radioaktivity). Vylučování materiálu souvisejícího s podaným lékem stolicí po intravenózním podání dávky ukazuje na aktivní vylučování do žluče. Po perorálním podání zdravým mužům byla celková radioaktivita vyloučena primárně stolicí (92 % podané radioaktivně značené dávky nebo 99 % zachycené radioaktivity) do 168 hodin po podání dávky. Méně než 1 % perorálně podané dávky (1 % zachycené radioaktivity) bylo vyloučeno močí, což naznačuje zanedbatelnou absorpci po perorálním podání. Plasmatický eliminační poločas umeklidinium-bromidu v rovnovážném stavu po inhalačním podávání po dobu 10 dnů byl průměrně 19 hodin, se 3 % až 4 % léčivé látky vyloučenými v nezměněné formě močí.
Charakteristiky u zvláštních skupin subjektů nebo pacientů
Starší pacienti
Populační farmakokinetická analýza prokázala, že farmakokinetika umeklidinium-bromidu byla mezi pacienty s CHOPN ve věku 65 let a staršími a pacienty s CHOPN mladšími 65 let podobná.
Porucha funkce ledvin
Subjekty se závažnou poruchou funkce ledvin (clearance kreatininu < 30 ml/min) nevykazovaly žádné známky zvýšení systémové expozice umeklidinium-bromidu (Cmax a AUC) a mezi subjekty se závažnou poruchou funkce ledvin a zdravými dobrovolníky nebyla zaznamenána změna vazby na bílkoviny.
Porucha funkce jater
Subjekty se středně závažnou poruchou funkce jater nevykazovaly žádné známky zvýšení systémové expozice umeklidinium-bromidu (Cmax a AUC) a mezi subjekty se středně závažnou poruchou funkce jater a zdravými dobrovolníky nebyla zaznamenána změna vazby na bílkoviny. Umeklidinium-bromid nebyl hodnocen u subjektů se závažnou poruchou funkce jater.
Další zvláštní populace
Analýza populační farmakokinetiky prokázala, že na základě věku, rasy, pohlaví, používání inhalačních kortikosteroidů ani tělesné hmotnosti není u umeklidinium-bromidu nutná úprava dávkování. Studie u pomalých metabolizátorů CYP2D6 neprokázala klinicky významný vliv genetického polymorfismu CYP2D6 na systémovou expozici umeklidinium-bromidu.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po opakovaném podávání, genotoxicity a hodnocení kancerogenního potenciálu neodhalily žádné zvláštní riziko pro člověka. V neklinických studiích s umeklidinium-bromidem byly nálezy typicky spojené s primárními farmakologickými účinky antagonistů muskarinových receptorů a/nebo lokální dráždi vostí.
Reprodukční toxicita
Umeklidinium-bromid nebyl u potkanů ani králíků teratogenní. V pre- a postnatální studii vedlo subkutánní podávání umeklidinium-bromidu potkanům k nižšímu přírůstku tělesné hmotnosti u březích samic, nižšímu příjmu potravy a mírnému snížení předporodní tělesné hmotnosti mláďat při dávkách 180 mikrogramů/kg/den (přibližně 80násobek klinické expozice umeklidiniu při dávce 55 mikrogramů u člověka, na základě AUC).
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Monohydrát laktosy Magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
2 roky
Doba použitelnosti po prvním otevření vaničky: 6 týdnů.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 30 °C. Pokud je přípravek uchováván v chladničce, nechte inhalátor alespoň jednu hodinu před použitím ohřát na pokojovou teplotu.
Uchovávejte inhalátor v zatavené ochranné vaničce, aby byl chráněn před vlhkostí, vyjměte ho až těsně před prvním použitím.
Po prvním otevření vaničky využijte v průběhu 6 týdnů.
Na štítek inhalátoru napište datum, do kdy má být inhalátor spotřebován. Datum má být zapsáno ihned, jakmile byl inhalátor vyndán z vaničky.
6.5 Druh obalu a obsah balení
Inhalátor Ellipta se skládá z šedého těla, světle zeleného krytu náustku a počítadla dávek a je uložen v ochranné vaničce z laminované fólie, která obsahuje vysoušedlo. Tato vanička je zatavena odlupovacím fóliovým víčkem.
Inhalátor obsahuje jeden hliníkový strip z laminované folie po 7 nebo 30 dávkách.
Inhalátor je zařízení složené z několika komponent, které jsou vyrobeny z polypropylenu, polyethylenu s vysokou hustotou, polyoxymethylenu, polybutylen-tereftalátu, akrylonitril-butadien-styrenu, polykarbonátu a nerezové oceli.
Balení obsahuje inhalátor se 7 nebo 30 dávkami.
Vícečetné balení obsahuje 3 inhalátory po 30 dávkách.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky. Návod k použití viz bod 4.2.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Glaxo Group Limited
980 Great West Road
Brentford
Middlesex
TW8 9GS
Velká Británie
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/14/922/001
EU/1/14/922/002
EU/1/14/922/003
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 28. dubna 2014.
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
12
A. VÝROBCE ODPOVĚDNÝ /VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE ODPOVĚDNÝ/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce odpovědného/výrobců odpovědných za propouštění šarží
Glaxo Operations UK Ltd. (trading as Glaxo Wellcome Operations)
Priory Street
Ware, Hertfordshire SG12 0DJ Velká Biránie
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst.
7 směrnice 2001/83/ES a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku
(v rámci farmakovigilance nebo minimalizace rizik).
• Povinnost uskutečnit poregistrační opatření
Držitel rozhodnutí o registraci uskuteční v daném termínu níže uvedená opatření:
|
Popis |
Termín splnění |
|
Předložení závěrečné zprávy klinické studie z poregistrační bezpečnostní studie (kohorty), která dále sleduje riziko vybraných kardiovaskulárních a cerebrovaskulárních nežádoucích účinků při léčbě léčivým přípravkem Incruse v provnání s tiotropiem v léčbě CHOPN (studie 201038) podle protokolu schváleného PRAC. |
do 3Q 2024 |
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU
KRABIČKA (POUZE JEDNOTLIVÁ BALENÍ A MULTIPACK)
55 mikrogramů_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Incruse 55 mikrogramů dávkovaný prášek k inhalaci Umeclidinium (umeclidinii bromidům)
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna podaná dávka obsahuje umeclidinium 55 mikrogramů (což odpovídá umeclidinii bromidům 65 mikrogramů).
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje rovněž laktosu a magnesium-stearát.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Dávkovaný prášek k inhalaci.
7 dávek 30 dávek 3x 30 dávek
1 inhalátor (Ellipta) po 7 dávkách.
1 inhalátor (Ellipta) po 30 dávkách.
Vícečetné balení: 90 dávek (3 inhalátory Ellipta po 30 dávkách) - 3x 30 dávek.
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Inhalační podání, JEDNOU DENNĚ
Před použitím si přečtěte příbalovou informaci.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
Doba použitelnosti po prvním otevření: 6 týdnů.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11 NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Glaxo Group Limited, 980 Great West Road, Brentford, Middlesex, TW8 9GS Velká Británie Logo Glaxo Group Ltd
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/14/922/001 1 inhalátor (Ellipta) po 7 dávkách EU/1/14/922/002 1 inhalátor (Ellipta) po 30 dávkách
EU/1/14/922/003 Vícečetné balení: 90 dávek (3 inhalátory Ellipta po 30 dávkách) - 3x 30 dávek
13. ČÍSLO ŠARŽE
Lot
|
14. |
KLASIFIKACE PRO VÝDEJ |
|
15. |
NÁVOD K POUŽITÍ |
|
16. |
INFORMACE V BRAILLOVĚ PÍSMU |
|
incruse ellipta | |
|
17. |
JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD |
|
2D |
čárový kód s jedinečným identifikátorem. |
|
18. |
JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM |
PC:
SN:
NN:
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU
VNITŘNÍ KRABIČKA (POUZE MULTIPACK BEZ BLUE-BOXU) 55 mikrogramů_
1 NÁZEV LÉČIVÉHO PŘÍPRAVKU
Incruse 55 mikrogramů dávkovaný prášek k inhalaci Umeclidinium (umeclidinii bromidům)
2 OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna podaná dávka obsahuje umeclidinium 55 mikrogramů (což odpovídá umeclidinii bromidům 65 mikrogramů).
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje rovněž laktosu a magnesium stearát.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 inhalátor po 30 dávkách.
Ellipta
Součást vícečetného balení, samostatně neprodejné.
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Inhalační podání, JEDNOU DENNĚ.
Před použitím si přečtěte příbalovou informaci.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ZE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
Doba použitelnosti po prvním otevření: 6 týdnů.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte při teplotě do 30 °C.
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH
PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11 NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Glaxo Group Limited, 980 Great West Road, Brentford, Middlesex, TW8 9GS Velká Británie Logo Glaxo Group Ltd
12 REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/14/922/003
|
13. |
ČÍSLO ŠARŽE |
|
Lot | |
|
14. |
KLASIFIKACE PRO VÝDEJ |
|
Výdej léčivého přípravku vázán na lékařský předpis. | |
|
15. |
NÁVOD K POUŽITÍ |
|
16. |
INFORMACE V BRAILLOVĚ PÍSMU |
|
incruse |
ellipta |
|
17. |
JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD |
|
18. |
JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM |
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA BLISTRECH NEBO STRIPECH VÍČKO VANIČKY Z LAMINOVANÉ FOLIE
55 mikrogramů_
1 NÁZEV LÉČIVÉHO PŘÍPRAVKU
Incruse 55 mcg prášek k inhalaci Umeclidinium (umeclidinii bromidům)
2 NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Glaxo Group Ltd logo
3 POUŽITELNOST
EXP
4. ČÍSLO SARZE
Lot
5. JINÉ
Neotevírejte, dokud nejste připraven(a) k inhalaci. Doba použitelnosti po prvním otevření: 6 týdnů.
7 dávek 30 dávek Ellipta
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU ŠTÍTEK INHALÁTORU
55 mikrogramů_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Incruse 55 mcg prášek k inhalaci Umeclidinium (umeclidinii bromidům)
Inhalační podání
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
Doba použitelnosti po prvním otevření: 6 týdnů. Spotřebujte do:
4. ČÍSLO SARZE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
7 dávek 30 dávek
6. JINÉ
Ellipta
B. PŘÍBALOVÁ INFORMACE
Incruse 55 mikrogramů dávkovaný prášek k inhalaci
Umeclidinium (umeclidinii bromidům)
Tento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4.
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Incruse a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Incruse používat
3. Jak se přípravek Incruse používá
4. Možné nežádoucí účinky
5. Jak přípravek Incruse uchovávat
6. Obsah balení a další informace Podrobný návod k použití
1. Co je přípravek Incruse a k čemu se používá Co je přípravek Incruse
Přípravek Incruse obsahuje léčivou látku nazývanou umeklidinium-bromid, která patří do skupiny léků zvaných bronchodilatancia.
K čemu se přípravek Incruse používá
Tento přípravek se používá k léčbě chronické obstrukčníplicní nemoci (CHOPN) u dospělých. CHOPN je dlouhodobé onemocnění, při kterém dochází k uzavírání nebo poškození dýchacích cest a plicních sklípků vedoucímu k postupnému zhoršení dýchání. Potíže s dýcháním jsou způsobeny tím, že se svalovina okolo dýchacích cest stahuje a způsobuje zužování dýchacích cest a omezení průtoku vzduchu.
Tento lék brání stahování této svaloviny v plicích a tím pomáhá udržet otevřené dýchací cesty, což usnadňuje proudění vzduchu do plic i z plic. Pokud se používá pravidelně, pomáhá ke kontrole dechových obtíží a snižuje vliv CHOPN na Váš každodenní život.
Přípravek Incruse se nesmí používat k úlevě při náhlém záchvatu dušnosti nebo sípotu. Pokud se u Vás objeví takový druh záchvatu, musíte použít inhalátor s rychle účinkujícím přípravkem (jako např. salbutamol).
2. Čemu musíte věnovat pozornost, než začnete přípravek Incruse používat Nepoužívejte přípravek Incruse:
- jestliže j ste alergický(á) na umeklidinium nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
Pokud si myslíte, že se Vás to týká, nepoužívejte tento léčivý přípravek, dokud se neporadíte se svým lékařem.
Upozornění a opatření
Před použitím tohoto přípravku se poraďte se svým lékařem:
- jestliže máte astma (nepoužívejte přípravek Incruse k léčbě astmatu);
- jestliže máte problémy se srdcem;
- jestliže máte problém s očima nazývaný glaukom (zelený zákal) s úzkým úhlem;
- jestliže máte zbytnělou prostatu, obtíže s močením nebo překážku v močovém měchýři;
- jestliže máte závažné problémy s játry.
Pokud si myslíte, že se Vás něco z tohoto může týkat, poraďte se se svým lékařem.
Okamžité dýchací potíže
Pokud se bezprostředně po použití přípravku Incruse objeví pocit tíhy na hrudi, kašel, sípání nebo dušnost: Přestaňte tento přípravek používat a neprodleně vyhledejte lékařskou pomoc, protože můžete mít závažnou zdravotní komplikaci, která se nazývá paradoxní bronchospasmus.
Oční problémy v průběhu léčby přípravkem Incruse
Pokud se u Vás v průběhu léčby přípravkem Incruse objeví bolest oka nebo nepříjemný pocit v oku, dočasně rozmazané vidění, zrakové haló nebo barevné obrazy v souvislosti se zarudnutím očí:
Přestaňte tento lék používat a okamžitě vyhledejte lékařskou pomoc, protože to mohou být příznaky akutního záchvatu glaukomu (zeleného zákalu) s úzkým úhlem.
Děti a dospívající
Tento přípravek se nemá podávat dětem a dospívajícím mladším 18 let.
Další léčivé přípravky a přípravek Incruse
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Zvláště informujte svého lékaře nebo lékárníka, pokud užíváte jiné přípravky s dlouhodobým účinkem podobné tomuto přípravku a užívané k léčbě problémů s dýcháním, např. tiotropium. Přípravek Incruse nesmíte používat současně s těmito dalšími přípravky.
Těhotenství, kojení a plodnost
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek používat. Lékař zváží prospěch z léčby tímto přípravkem v průběhu těhotenství pro Vás a rizika pro Vaše dítě.
Není známo, zda složky přípravku Incruse mohou procházet do mateřského mléka. Pokud kojíte, musíte se před použitím přípravku Incruse poradit se svým lékařem.
Řízení dopravních prostředků a obsluha strojů
Není pravděpodobné, že by přípravek Incruse ovlivnil schopnost řídit nebo obsluhovat stroje.
Přípravek Incruse obsahuje laktózu
Pokud Vám někdy lékař řekl, že trpíte nesnášenlivostí některých cukrů, sdělte to svému lékaři dříve, než začnete používat tento lék.
3. Jak se přípravek Incruse používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka přípravku je jedna inhalace každý den ve stejnou dobu tak, jak Vám doporučil Váš lékař. Potřebujete pouze jednu inhalaci denně, jelikož účinek tohoto léčiva trvá 24 hodin.
Nepoužívejte více přípravku, než Vám řekl Váš lékař.
Používejte přípravek Incruse pravidelně
Je velmi důležité, abyste přípravek Incruse používal(a) každý den tak, jak Vám doporučil Váš lékař. To pomáhá zajistit odstranění příznaků onemocnění v průběhu dne i noci.
Přípravek Incruse se nesmí používat k úlevě od náhlého záchvatu dusnosti nebo sípotu. Pokud se u Vás objeví tento druh záchvatu, musíte použít inhalátor s rychle účinkujícím přípravkem (jako je např. salbutamol).
Jak se inhalátor používá
Úplné informace naleznete v části „Podrobný návodkpoužití“ této příbalové informace.
Přípravek Incruse se vdechuje ústy do plic pomocí inhalátoru Ellipta.
Pokud se příznaky nezlepšují
Pokud se příznaky CHOPN (dušnost, sípot, kašel) nezlepšují, nebo pokud se zhoršují, nebo pokud musíte používat inhalátor s rychle účinkujícím přípravkem častěji: vyhledejte co nejdříve svého lékaře.
Jestliže jste použil(a) více přípravku Incruse, než jste měl(a)
Pokud omylem použijete příliš mnoho tohoto přípravku, poraďte se ihned se svým lékařem nebo lékárníkem, protože je možné, že budete potřebovat lékařskou pomoc. Je-li to možné, ukažte mu inhalátor, balení přípravku a tuto příbalovou informaci. Můžete zaznamenat rychlejší tlukot srdce než obvykle, poruchy zraku nebo sucho v ústech.
Jestliže jste zapomněl(a) použít přípravek Incruse
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku. Vezměte si pouze následující dávku v obvyklý čas.
Pokud se objeví dušnost nebo sípot, použijte inhalátor s rychle účinkujícím přípravkem (např. salbutamol) a poté se poraďte s lékařem.
Jestliže jste přestal(a) používat přípravek Incruse
Používejte tento přípravek tak dlouho, jak Vám doporučil Váš lékař. Tento přípravek bude účinný pouze tak dlouho, jak dlouho jej budete používat. Nepřestávejte používat tento přípravek dříve, než Vám to doporučí lékař, a to ani v případě, že se budete cítit lépe.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Časté nežádoucí účinky
Mohou postihnout až 1 osobu z 10
• zrychlení tlukotu srdce;
• bolestivé a časté močení (může být známkou infekce močových cest);
• častá nachlazení;
• infekce nosu a hrdla;
• kašel;
• pocit tlaku nebo bolesti na tvářích a čelu (mohou být známkami zánětu vedlejších dutin, kterému se říká sinusitida);
• bolest hlavy.
Méně časté nežádoucí účinky
Mohou postihnout až 1 osobu ze 100
• nepravidelná srdeční akce;
• zácpa;
• sucho v ústech;
• vyrážka;
• poruchy vnímání chuti.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Incruse uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na obalu za „EXP“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte inhalátor v zatavené ochranné vaničce, aby byl chráněn před vlhkostí. Neotevírejte foliové víčko ochranné vaničky, dokud nejste připraven(a) k prvnímu použití. Jakmile je vanička otevřena, inhalátor může být používán po dobu 6 týdnů od data otevření. Napište na štítek inhalátoru datum, do kdy má být inhalátor spotřebován. Datum zapište ihned, jakmile vyjmete inhalátor z vaničky.
Uchovávejte při teplotě do 30 °C.
Pokud inhalátor uchováváte v chladničce, nechte jej alespoň hodinu před použitím ohřát na pokojovou teplotu.
Nevyhazujte žádné léčivé přípravky do odpadních vod ani domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek Incruse obsahuje
Léčivou látkou je umeclidinii bromidum.
Jedna inhalace poskytne dávku (podaná dávka, která vyjde z náustku) umeclidinium 55 mikrogramů (což odpovídá umeclidinii bromidum 65 mikrogramů).
Dalšími složkami jsou monohydrát laktózy (viz bod 2 „Přípravek Incruse obsahuje laktózu“) a magnesium-stearát.
Jak přípravek Incruse vypadá a co obsahuje toto balení
Samotný přístroj je šedý inhalátor se světle zeleným krytem náustku a počítadlem dávek. Je zabalený ve vaničce z laminované fólie s odlupovacím fóliovým víčkem. Vanička obsahuje vysoušedlo, které snižuje vlhkost uvnitř balení.
Léčivá látka je přítomna ve formě bílého prášku v oddělených stripech z laminované fólie uvnitř inhalátoru. Inhalátor obsahuje 7 nebo 30 dávek. K dispozici je rovněž vícečetné balení, obsahující 90 dávek (3 inhalátory po 30 dávkách).
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci:
Glaxo Group Limited
980 Great West Road
Brentford
Middlesex
TW8 9GS
Velká Británie
Výrobce:
Glaxo Operations UK Limited (obchodující pod značkou Glaxo Wellcome Operations)
Priory Street Ware
Hertfordshire SG12 0DJ Velká Británie
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Česká republika
GlaxoSmithKline s.r.o. Tel: + 420 222 001 111 cz.info@gsk.com
Lietuva
GlaxoSmithKline Lietuva UAB Tel: + 370 5 264 90 00 info.lt@gsk.com
Luxembourg/Luxemburg
GlaxoSmithKline Pharmaceuticals s.a./n.v.
Belgique/Belgien
Tél/Tel: + 32 (0) 10 85 52 00
Magyarország
GlaxoSmithKline Kft.
Tel.: + 36 1 225 5300
Danmark
GlaxoSmithKline Pharma A/S Tlf: + 45 36 35 91 00 dk-info@gsk.com
Deutschland
GlaxoSmithKline GmbH & Co. KG Tel.: + 49 (0)89 36044 8701 produkt.info@gsk.com
Nederland
GlaxoSmithKline BV Tel: + 31 (0)30 6938100 nlinfo@gsk.com
Eesti
GlaxoSmithKline Eesti OU Tel: + 372 6676 900 estonia@gsk.com
Norge
GlaxoSmithKline AS Tlf: + 47 22 70 20 00 firmapost@gsk.no
EkXáda
|
GlaxoSmithKline A.E.B.E. Tr|^: + 30 210 68 82 100 |
GlaxoSmithKline Pharma GmbH Tel: + 43 (0)1 97075 0 at.info@gsk.com |
|
Espaňa GlaxoSmithKline, S.A. Tel: + 34 902 202 700 es-ci@gsk.com |
Polska GSK Services Sp. z o.o. Tel.: + 48 (0)22 576 9000 |
|
France Laboratoire GlaxoSmithKline Tél.: + 33 (0)1 39 17 84 44 diam@gsk.com |
Portugal GlaxoSmithKline - Produtos Farmaceuticos, Lda. Tel: + 351 21 412 95 00 |
|
Hrvatska GlaxoSmithKline d.o.o. Tel: + 385 1 6051 999 |
Románia GlaxoSmithKline (GSK) S.R.L. Tel: + 4021 3028 208 |
|
Ireland GlaxoSmithKline (Ireland) Limited Tel: + 353 (0)1 4955000 |
Slovenija GlaxoSmithKline d.o.o. Tel: + 386 (0)1 280 25 00 medical.x.si@gsk.com |
|
Ísland Vistor hf. Sími: + 354 535 7000 |
Slovenská republika GlaxoSmithKline Slovakia s. r. o. Tel: + 421 (0)2 48 26 11 11 recepcia.sk@gsk.com |
|
Italia GlaxoSmithKline S.p.A. Tel: + 39 (0)45 9218 111 |
Suomi/Finland GlaxoSmithKline Oy Puh/Tel: + 358 (0)10 30 30 30 F inland.tuoteinfo@gsk .com |
|
Kónpoq GlaxoSmithKline (Cyprus) Ltd Tp^: + 357 22 39 70 00 gskcyprus@gsk.com |
Sverige GlaxoSmithKline AB Tel: + 46 (0)8 638 93 00 info.produkt@gsk.com |
|
Latvija GlaxoSmithKline Latvia SIA Tel: + 371 67312687 lv-epasts@gsk.com |
United Kingdom GlaxoSmithKline UK Ltd. Tel: + 44 (0)800 221441 customercontactuk@gsk.com |
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
Podrobný návod k použití Co je inhalátor?
Před prvním použitím přípravku Incruse nemusíte inhalátor kontrolovat, zda funguje správně, obsahuje odměřené dávky a je připravený přímo k použití.
Inhalátor je zabalen v ochranné vaničce obsahující sáček s vysoušedlem, které snižuje vlhkost. Tento sáček vyhoďte - nejezte ho ani neinhalujte.
Když vyjmete inhalátor ze zatavené vaničky, je v „uzavřené“ pozici. Neotevírejte jej, dokud nejste připraven(a) k inhalaci léku. Jakmile je vanička otevřena, dopište na určené místo na štítku inhalátoru datum „Spotřebujte do“. Datum „Spotřebujte do“ je 6 týdnů od data otevření vaničky. Po tomto datu se již nemá inhalátor dále používat. Vaničku je možné po prvním otevření vyhodit.
Návod k použití inhalátoru uvedený níže lze použít pro inhalátor s 30 dávkami i se 7 dávkami.
Před použitím si přečtěte následující informace
Pokud kryt inhalátoru otevřete a zavřete bez toho, že byste inhaloval(a) lék, dojde ke ztrátě dávky.
Ztracená dávka zůstane bezpečně uzavřená v inhalátoru, ale nebude již dostupná k inhalaci.
Při jedné inhalaci není možné náhodně použít dávku navíc ani dvojnásobnou dávku.
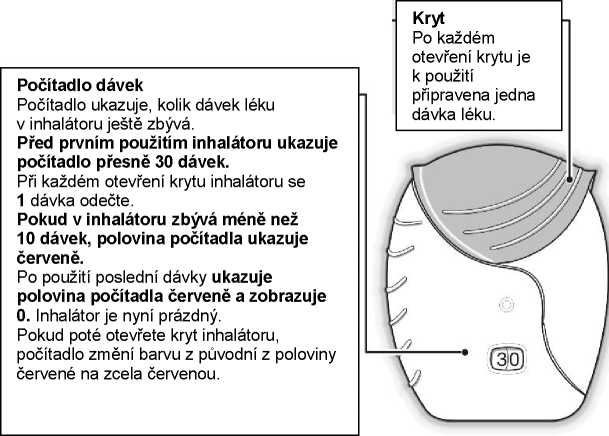
1) Příprava dávky
Počkejte s otevřením krytu, dokud nejste připraven(a) k použití své dávky. Inhalátorem netřeste.
• Stahujte víčko dolů, dokud není slyšet „cvaknutí“.
Lék je nyní připraven k inhalaci.
Počítadlo dávky pro potvrzení odečetlo 1 dávku.
• Pokud počítadlo neodečte dávku v okamžiku, kdy je slyšet „cvaknutí,“ inhalátor neumožní inhalaci léku.
Vezměte jej zpět k lékárníkovi, aby Vám poradil.
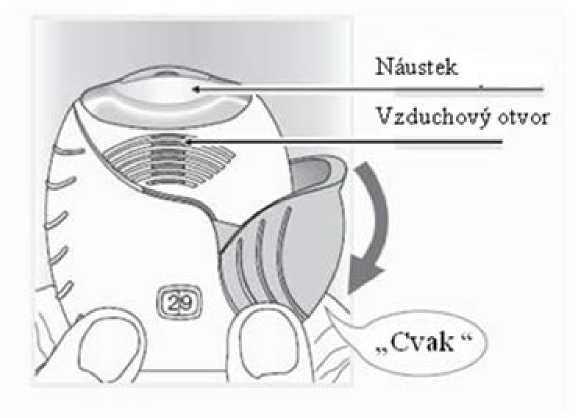
2) Inhalace léku
• Držte inhalátor dále od úst a co nejvíce vydechněte jak je Vám pohodlné.
Nevydechujte do inhalátoru.
• Vložte náustek mezi rty a pevně jej svými rty stiskněte.
Neblokujte vzduchový otvor prsty.
Při inhalaci dávkv držte své rtv přitisknuté na tvarovaném okraji oáustku. ^ezakrÝvejte prstv vzduchově otvor.
• Jednou se dlouze, rovnoměrně a zhluboka nadechněte. Zadržte dech po co nejdelší dobu (alespoň 3 -4 sekundy).
• Vyjměte inhalátor z úst.
• Pomalu a lehce vydechněte.
Lék by neměl mít žádnou chuť, ani byste jej neměl(a) cítit, a to ani v případě, že jste inhalátor použil(a) správně.
3) Uzavření inhalátoru
Pokud chcete náustek očistit, otřete jej před uzavřením suchou tkaninou.
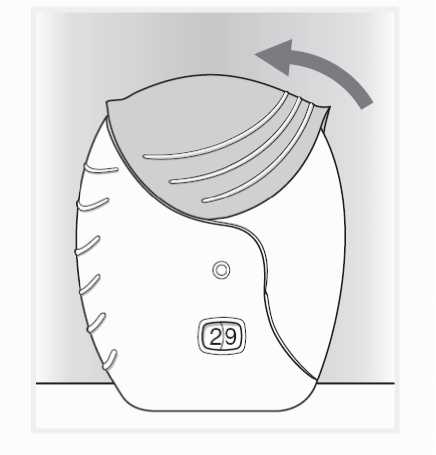
Vysuňte kryt zpět nahoru co nejdále, až je náustek zakrytý.
32
V této studii byla použita step-down statistická procedura a toto srovnání bylo pod srovnáním, které nedosáhlo statistické významnosti. Proto statistický význam tohoto porovnání nelze vyvodit
V této studii byla použita step-down statistická procedura a toto srovnání bylo pod srovnáním, které nedosáhlo statistické významnosti. Proto statistický význam tohoto porovnání nelze vyvodit