Fanhdi 25 I.u./Ml
sp.zn.: sukls37818/2011, sukls37843/2011, sukls37850/2011
PŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE
Fanhdi 25 IU/ml, 50 IU/ml a 100 IU/ml Prášek a rozpouštědlo pro injekční roztok
Factor VIII coagulationis humanus, factor von Willebrand humanus.
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se Vám vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Fanhdi a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Fanhdi používat
3. Jak se přípravek Fanhdi používá
4. Možné nežádoucí účinky
5 Jak přípravek Fanhdi uchovávat
6. Obsah balení a další informace
1. CO JE PŘÍPRAVEK FANHDI A K ČEMU SE POUŽÍVÁ
Fanhdi je dodáván ve formě prášku , určeného k přípravě injekčního roztoku obsahujícího 250, 500, 1000 nebo 1500 IU koagulačního faktoru VIII a 300, 600, 1200 nebo 1800 IU lidského von Willebrandova faktoru v jedné lahvičce.
Po naředění s odpovídajícím množství rozpouštědla (voda na injekci) obsahuje každá lahvička 25, 50 nebo 100 IU FVIII/ml a 30, 60 nebo 120 IU vWF/ml.
Farmakoterapeutická skupina: Antihemoragika; krevní koagulační faktory VIII: von Willebrandův faktor a krevní koagulační faktor VIII v kombinaci.
Fanhdi je indikován k profylaxi a léčbě krvácení u pacientů s hemofilií A (vrozený deficit faktoru VIII).
Fanhdi je indikován k profylaxi a léčbě krvácení u osob s von Willebrandovou chorobou (vWD), když je léčba samotným desmopresinem (DDAVP) neúčinná nebo kontraindikována.
Tento produkt lze použít při léčbě získaného deficitu faktoru VIII.
2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE PŘÍPRAVEK FANHDI
UŽÍVAT
Neužívejte Fanhdi
- jestliže jste alergický(á) na léčivé látky nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
Chcete-li podrobnější informace, zeptejte se svého lékaře.
Upozornění a opatření
• ve vzácných případech může dojít k anafylaktické reakci (náhlá těžká alergická reakce). Pozorujete-li na sobě vyrážku nebo generalizovanou kopřivku, tlak na prsou, točení hlavy, závrať nebo nevolnost, nebo pociťujete-li točení hlavy, když stojíte, je možné, že trpíte anafylaktickou reakcí na přípravek Fanhdi. V případě, že se vyskytnou tyto příznaky, musíte okamžitě přerušit užívání přípravku a kontaktovat svého lékaře.
• Váš lékař pravděpodobně provede některé testy, aby se ujistil, že dávka přípravku Fanhdi, kterou dostáváte, je dostatečná k dosažení a udržení odpovídající hladiny faktoru VIII.
• jestliže nelze vaše krvácení zvládnout pomocí přípravku Fanhdi, ihned to konzultujte se svým lékařem. Pravděpodobně se u vás vyvinuly inhibitory faktoru VIII, a proto Váš lékař provede některé testy, které to potvrdí. Inhibitory faktoru VIII jsou protilátky přítomné v krvi, které blokují faktor VIII, jenž užíváte. Výsledkem je menší účinnost faktoru VIII při zvládání krvácení.
• když při léčbě von Willebrandovy choroby existuje riziko výskytu trombóz, zejména u pacientů se známými faktory klinického rizika. Proto by měl váš lékař provést některé testy ke zjištění časných příznaků trombózy a zahájit léčbu žilní tromboembolie podle aktuálních doporučení.
• u pacientů s von Willebrandovou chorobou, zejména u pacientů s typem 3, se mohou vyvinout neutralizující protilátky (inhibitory) proti von Willebrandovu faktoru. Inhibitory von Willebrandova faktoru jsou protilátky přítomné v krvi, které mohou blokovat von Willebrandův faktor, jenž užíváte. Není-li dosaženo očekávané úrovně aktivity von Willebrandova faktoru v plazmě nebo nelze-li krvácení příslušnou dávkou zvládnout, měla by být provedena zkouška na stanovení toho, zda je inhibitor von Willebrandova faktoru přítomen. U pacientů s vysokou hladinou inhibitoru je terapie von Willebrandovým faktorem méně účinná.
Při výrobě léčivých přípravků z lidské krve nebo plazmy jsou zavedena standardní opatření k prevenci přenosu infekce na pacienty. Tato opatření zahrnují:
- pečlivý výběr dárců krve a plazmy k vyloučení těch dárců krve, u kterých je shledáno možné riziko přenosu infekce
- testování každého odběru a směsné plazmy na ukazatele virů/infekce
- zařazení výrobních kroků do zpracování krve a plazmy, které jsou schopny viry inaktivovat nebo odstanit.
Přes tato opatření nelze možnost přenosu infekce zcela vyloučit. To rovněž platí pro jakékoli neznámé nebo nově vznikající viry či jiné patogeny.
Přijatá opatření se pokládají za účinná u obalených virů, jako je virus lidské imunitní nedostatečnosti HIV, virus hepatitidy B a virus hepatitidy C, a u neobaleného viru hepatitidy A. Přijatá opatření mohou mít omezenou účinnost u neobalených virů, jako je parvovirus B19. Infekce parvovirem B19 může být závážná u těhotných žen (infekce plodu) a u jedinců, jejichž imunitní systém je oslaben nebo kteří mají některé typy anémie (např. srpkovitá nebo hemolytická anémie).
Váš lékař vám možná doporučí, abyste uvažovali o očkování proti hepatitidě A a B, pokud přípravky s faktorem VIII na bázi lidské plazmy dostáváte pravidelně.
Důrazně se doporučuje poznamenat si název a číslo šarže přípravku pokaždé, když dostanete dávku přípravku Fanhdi, aby se zachoval záznam o použitých šaržích.
Viz rovněž bod 4. Možné nežádoucí účinky Další léčivé přípravky a Fanhdi
Informujte svého lékaře o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat.
Nejsou známy žádné interakce komplexu koagulačního faktoru VIII a von Willebrandova faktoru s jinými léky.
Těhotenství a kojení
Vzhledem ke vzácnému výskytu hemofilie A u žen nejsou zkušenosti s použitím komplexu FVIII/vWF v těhotenství a při kojení k dispozici. Proto se doporučuje používat přípravek v těhotenství jen v nutném případě.
Než začnete brát jakýkoli lék, požádejte o radu svého lékaře nebo lékárníka.
Řízení dopravních prostředků a obsluha strojů
Přípravek Fanhdi nemá žádný nebo má zanedbatelný vliv na schopnost řídit motorová vozidla nebo obsluhovat stroje.
3. JAK SE PŘÍPRAVEK FANHDI UŽÍVÁ
Nařeďte přípravek, jak je popsáno v bodě „Návod k použití přípravku“ (na konci tohoto letáku). Přípravek musí být podán intravenózně. Rychlost podání nesmí být větší než 10 ml/min.
Množství přípravku Fanhdi, které je třeba použít, závisí na mnoha faktorech, například na vaší hmotnosti, klinickém stavu a druhu a závažnosti krvácení. Váš lékař vypočítá dávku, frekvenci a intervaly podávání přípravku Fanhdi tak, aby bylo dosaženo potřebné hladiny faktoru VIII nebo von Willebrandova faktoru ve vaší krvi.
Váš lékař vás informuje o době trvání vaší léčby přípravkem Fanhdi.
Jestliže jste použil(a) více přípravku Fanhdi, než jste měl(a)
Nebyly hlášeny žádné případy předávkování komplexem koagulačního faktoru VIII a von Willebrandova faktoru. Jestliže jste si však vzali větší množství přípravku Fanhdi, než jste měli, obraťte se ihned na svého lékaře.
Jestliže jste zapomněl(a) užít přípravek Fanhdi
• Okamžitě si vezměte další dávku a pokračujte v pravidelných intervalech podle pokynů lékaře.
• Namísto zapomenuté dávky si neberte dvojitou dávku.
4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Ve vzácných případech se u Vás po podání přípravku Fanhdi mohou projevit některé z těchto nežádoucích účinků:
• Svědění, reakce v místě vpichu (např. pálení a přechodné zrudnutí)
• Alergické reakce (např. tlak na prsou/pocit nevolnosti, točení hlavy, nevolnost a lehký pokles krevního tlaku, který může způsobit pocit točení hlavy, když stojíte)
• Podivná chuť v ústech
• Horečka
• Tachykardie
Někdy může dojít k anafylaktickému šoku. Pozorujete-li během injekce/infúze některý z těchto příznaků:
• Tlak na prsou/pocit nevolnosti
• Točení hlavy
• Lehká hypotenze (mírný pokles krevního tlaku s točením hlavy, když stojíte)
• Nevolnost
může to být příznak přecitlivělosti a anafylaktické reakce. V případě anafylaktické nebo alergické reakce přerušte injekci/infúzi a okamžitě se obraťte na lékaře.
Reakce přecitlivělosti na složky přípravku nelze zcela vyloučit. Známou komplikací při léčbě pacientů s hemofilií A je vznik protilátek neutralizujících faktor VIII (inhibitorů). Podle studií provedených u přípravků s faktorem VIII lidského původu je rozvoj inhibitorů zejména pozorován u hemofilických pacientů, kteří nebyli dříve léčeni. Pro zjištění vzniku těchto inhibitorů musíte být pečlivě sledován pomocí příslušných klinických pozorování a laboratorních testů.
Zejména jste-li pacientem s von Willebrandovou chorobou 3. typu, mohou u vás ve vzácných případech vzniknout neutralizující protilátky (inhibitory) na von Willebrandův faktor. Pokud se tyto inhibitory objeví, je von Willebrandův faktor při zvládání krvácení méně účinný. Tyto protilátky se mohou objevit v souvislosti s anafylaktickými reakcemi. Proto by se u těchto pacientů prodělávajících anafylaktické reakce měla vyhodnocovat přítomnost inhibitorů. V těchto případech se okamžitě poraďte se svým lékařem.
Existuje riziko výskytu trombóz, zejména u pacientů se známými klinickými rizikovými faktory.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
webové stránky: www.sukl. cz/nahlasit-nezadouci-ucinek.
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. JAK PŘÍPRAVEK FANHDI UCHOVÁVAT
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte při teplotě do 30°C. Chraňte před mrazem.
Nepoužívejte tento přípravek po datu použitelnosti uvedeném na štítku a na krabici za písmeny EXP.
Nepoužívejte tento přípravek, jestliže jste si všimli, že je roztok zakalený nebo jsou v něm usazeniny. Roztok má být čirý nebo lehce opalescentní.
Roztok musí být zlikvidován, pokud jsou v něm patrné viditelné částice nebo změna barvy.
Chemická a fyzikální stabilita po naředění byla prokázána na dobu 12 hodin při teplotě 25°C. Z mikrobiologického hlediska má být přípravek použit okamžitě. Není-li použit okamžitě, doba a podmínky uchovávání po naředění před použitím jsou v odpovědnosti uživatele a normálně by doba neměla být delší než 24 hodin při teplotě 2 až 8 °C, pokud k rekonstituci nedošlo za kontrolovaných a validovaných aseptických podmínek
Veškerý nevyužitý přípravek či odpadní materiál je třeba zlikvidovat v souladu s místními předpisy.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. OBSAH BALENÍ A DALŠÍ INFORMACE
Co přípravek Fanhdi obsahuje
Léčivou látkou je Factor VIII coagulationis a Factor von Willebrand humanus.
Fanhdi je dodáván jako prášek a rozpouštědlo k přípravě injekčního roztoku obsahující v 1 lahvičce 250, 500, 1000 nebo 1500 IU koagulačního faktoru VIII a 300, 600, 1200 nebo 1800 IU von Willebrandova faktoru. Přípravek se ředí 10 ml vody na injekcí (250, 500 a 1000 IU) nebo 15 ml vody na injekcí (1500 IU)
Pomocnými latkami jsou lidský albumin, histidin a arginin.
Rozpouštědlo je voda na injekci.
Jak přípravek Fanhdi vypadá a co obsahuje toto balení
Injekční lahvička obsahuje bílý nebo světle žlutý hygroskopický prášek nebo křehkou (drobivou) pevnou látku a injekční stříkačka obsahuje čirou bezbarvou tekutinu (rozpouštědlo).
Velikost balení
Fanhdi 25 IU/ml Fanhdi 50 IU/ml Fanhdi 100 IU/ml Fanhdi 100IU/ml
1 x 250 IU + 10 ml rozpouštědla 1 x 500 IU + 10 ml rozpouštědla 1 x 1000 IU +10 ml rozpouštědla 1 x 1500 IU + 15 ml rozpouštědla
Balení obsahuje: 1 injekční lahvičku s práškem, 1 předplněnou injekční stříkačku s rozpouštědlem a příslušenství (adaptér lahvičky, filtr, 2 tampóny s alkoholem a aplikační set).
Držitel rozhodnutí o registraci a výrobce
Instituto Grifols, S.A.
Can Guasc, 2 - Parets del Valles 08150 Barcelona - ŠPANĚLSKO
Tato příbalová informace byla naposledy revidována
25.6.2014
Podrobné informace o tomto léku j sou dostupné na internetové stránce Státního ústavu pro kontrolu léčiv (SÚKL) http://www.sukl.cz/
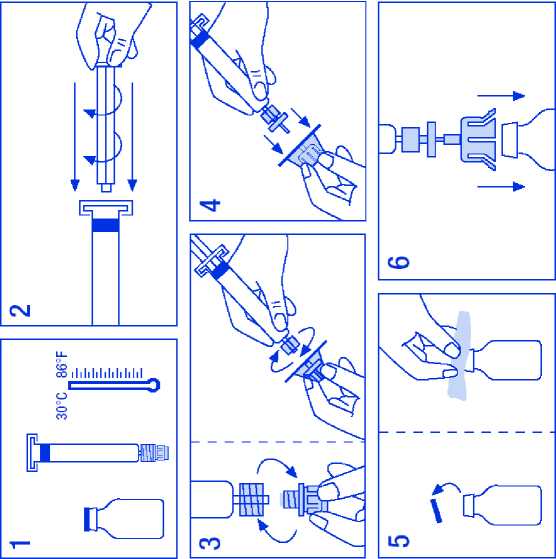
Návod k použití přípravku, zacházení s ním
Dodržujte tyto pokyny, pokud váš lékař neuvedl jinak.
Nepoužitý přípravek nesmí být nikdy ukládán k pozdějšímu použití ani uchováván v ledničce.
Příprava roztoku
1. Injekční lahvičku s práškem a injekční stříkačku zahřejte maximálně na 30 °C.
2. Na injekční stříkačku s rozpouštědlem nasaďte píst.
3. Z krabičky vyjměte filtr. Z injekční stříkačky sejměte kryt a nasaďte na něj filtr.
4. Z krabičky vyjměte adaptér lahvičky a nasaďte ho na filtr se stříkačkou.
5. Z injekční lahvičky s práškem sejměte víčko a zátku injekční lahvičky otřete přiloženým
antiseptickým tampónem.
6. Zátku injekční lahvičky propíchněte jehlou adaptéru.
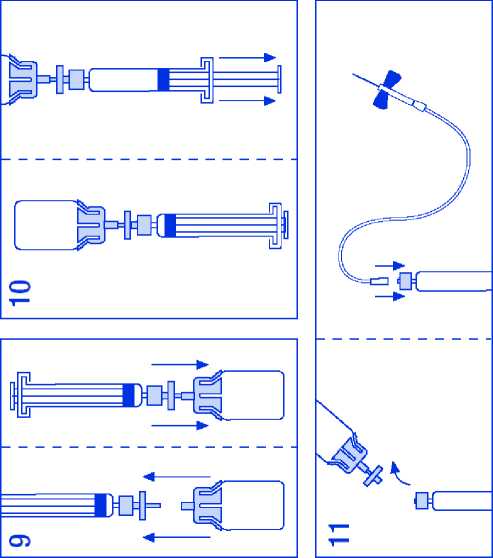
7. Roztok z injekční stříkačky přeneste kompletně do injekční lahvičky s práškem.
8. Injekční lahvičkou jemně míchejte, až se prášek dokonale rozpustí. Stejně jako u ostatních
parenterálně aplikovaných roztoků nepoužijte přípravek, který není dokonale rozpuštěný, nebo jsou v něm patrné částice.
9. Pro odstranění vakua na okamžik oddělte stříkačku/filtr od nádobky/adaptéru.
10. Obraťte injekční lahvičku a roztok natáhněte do injekční stříkačky.
11. Připravte místo vpichu. Injekční stříkačku oddělte, aplikujte přípravek za použití dodané jehly s křidélky. Rychlost intravenózní aplikace musí být okolo 3 ml/min. a nesmí překročit
10 ml/min., aby nedošlo k nežádoucím vasomotorickým reakcím.
Aplikační set je určen výhradně na jedno použití.