Coagadex 250 Iu
PŘÍLOHA I
SOUHRN ÚDAJŮ O PŘÍPRAVKU
^ Tento léčivý přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Žádáme zdravotnické pracovníky, aby hlásili jakákoli podezření na nežádoucí účinky. Podrobnosti o hlášení nežádoucích účinků viz bod 4.8.
1. NÁZEV PŘÍPRAVKU
Coagadex 250 IU, prášek a rozpouštědlo pro injekční roztok.
Coagadex 500 IU, prášek a rozpouštědlo pro injekční roztok.
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna injekční lahvička obsahuje nominálně 250 IU nebo 500 IU lidského koagulačního faktoru X (Factor X coagulations humanus).
Coagadex obsahuje přibližně 100 IU/ml lidského koagulačního faktoru X po rekonstituci s 2,5 ml (250 IU) nebo 5 ml (500 IU) sterilní vody na injekci
Vyrobeno z plazmy lidských dárců.
Pomocné látky se známým účinkem:
Coagadex obsahuje až 0,4 mmol/ml (9,2 mg/ml) sodíku.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Prášek a rozpouštědlo pro injekční roztok.
Injekční lahvička s práškem obsahuje bílý až téměř bílý prášek. Injekční lahvička s rozpouštědlem obsahuje čirou, bezbarvou tekutinu.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Coagadex je indikován k léčbě a profylaxi krvácivých příhod a k perioperační péči u pacientů s dědičnou deficiencí faktoru X.
4.2 Dávkování a způsob podání
Léčbu je nutné zahájit pod dohledem lékaře, který má zkušenosti s léčbou vzácných krvácivých poruch.
Dávkování
Dávka a délka trvání léčby u dospělých a dětí j sou stejné.
Dávka a délka trvání léčby závisí na závažnosti deficience faktoru X (tj. pacientova výchozí hladina faktoru X), na místě a rozsahu krvácení a na klinickém stavu pacienta. V případě velkých chirurgických zákroků či životu nebezpečných krvácivých příhod je pečlivé monitorování substituční terapie obzvláště důležité.
Nemá být aplikováno více než 60 IU/kg denně.
Očekávané nejvyšší zvýšení hladiny faktoru X in vivo vyjádřené v IU/dl (nebo % normálních hodnot) lze stanovit pomocí následujícího vzorce:
Dávka (IU) = tělesná hmotnost (kg) x požadovaný vzestup hladiny faktoru X (IU/dl nebo %
normálních hodnot) x 0,5
NEBO
Zvýšení hladiny faktoru X
(IU/dl nebo % normálních hodnot) = [celková dávka (IU) / tělesná hmotnost (kg)] x 2
Následující příklady jsou založeny na předpokladu, že pacientova výchozí hladina faktoru X je <
1 IU/dl:
1. Lze očekávat, že dávka 2000 U přípravku Coagadex podaná pacientovi s hmotností 70 kg bude mít za následek nejvyšší zvýšení hladiny faktoru X po podání infuze na 2000násobek {[2 IU/dl]/[IU/kg]}/[70 kg] = 57 IU/dl (tj. 57 % normálních hodnot).
2. U dětí s hmotností 40 kg je požadovaná nejvyšší hladina faktoru X 90 % normálních hodnot. V tomto případě bude vhodná dávka činit:
40 kg x 90 IU/dl/{[2 IU/dl]/[IU/kg]} = 1800 IU.
Dávka a frekvence podávání mají být přizpůsobeny individuální klinické odpovědi. Pacienti mohou vykazovat různou farmakokinetickou (např. dosažení různého poločasu rozpadu nebo hodnot obnovy faktoru in vivo) a klinickou odpověď na Coagadex. Přestože dávky lze předem stanovit pomocí výše uvedených výpočtů, doporučuje se pokud možno provádět vhodné testy ke stanovení hladiny faktoru X v plazmě a podle výsledků upravovat dávkování.
Zástava a prevence krvácivých příhod
Léčba krvácivých příhod: má být aplikováno 25 IU/kg přípravku Coagadex při výskytu prvních známek krvácení nebo hned před očekávaným nástupem menstruačního krvácení. Opakujte v intervalech 24 hodin, dokud se krvácení nezastaví. Posuzujte každé jednotlivé krvácení z hlediska závažnosti.
Sekundární profylaxe zaměřená proti opětovnému krvácení nebo krátkodobá profylaxe před plánovanou fyzickou aktivitou nebo stomatologickými výkony: má být aplikováno 25 IU/kg přípravku Coagadex a opakováno dle potřeby.
Údaje týkající se použití přípravku Coagadex k dlouhodobé profylaxi jsou omezené, ale bylo zaznamenáno použití 24,6 až 28 IU/kg jednou týdně nebo 25 IU/kg každé dva týdny po dobu několika týdnů či měsíců (viz bod 5.1).
Perioperační péče
Před operací: vypočtěte dávku přípravku Coagadex tak, aby došlo k vzestupu hladiny faktoru X na 70-90 IU/dl. V případě velkých chirurgických zákroků je pečlivé monitorování dávky a délky trvání léčby obzvláště důležité.
Požadovaná dávka (IU) = tělesná hmotnost (kg) x požadovaný vzestup hladiny faktoru X (IU/dl)
x 0,5
Požadovaný vzestup hladiny faktoru X spočívá v rozdílu mezi hladinou faktoru X v plazmě pacienta a požadovanou hladinou a je založen na pozorovaných hodnotách obnovy o 2 IU/dl na IU/kg.
Příklad: vhodná dávka ke zvýšení hladiny faktoru X v plazmě z 15 IU/dl na 90 IU/dl u pacienta s hmotností 70 kg je:
70 x (90-15) x 0,5 = 2 625 IU.
Po operaci: aplikujte dávku dle potřeby k udržení hladiny faktoru X v plazmě minimálně na 50 IU/dl, dokud pacientovi bude hrozit riziko krvácení v důsledku operace.
Doporučuje se měřit hladinu faktoru X v plazmě po podání infuze u každého pacienta před operací a po ní k dosažení a udržení hemostatické hladiny.
Starší osoby
Není nutná žádná úprava dávky.
Porucha funkce ledvin
Není nutná žádná úprava dávky.
Porucha funkce jater
Není nutná žádná úprava dávky.
Pediatrická populace
Bezpečnost a účinnost přípravku Coagadex u dětí mladších 12 let nebyla dosud stanovena.
Způsob podání Intravenózní podání.
Po rekonstituci má být přípravek podán intravenózně do jedné hodiny při doporučené rychlosti 10 ml/min, která nesmí překročit 20 ml/min.
V případě domácí léčby musí být pacient řádně vyškolen a pravidelně sledován.
Návod k rekonstituci tohoto léčivého přípravku před jeho podáním je uveden v bodě 6.6.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Hypersenzitivita
Mohou nastat hypersenzitivní reakce alergického typu, včetně anafylaxe. Coagadex obsahuje stopy lidských proteinů jiných než faktor X. Pacienty je proto nutné informovat o prvních známkách hypersenzitivních reakcí, které zahrnují angioedém, zánět v místě podání infuze (např. pálení, štípání, erytém), zimnici, kašel, závrať, horečku, návaly horka, generalizovanou urtikarii, bolest hlavy, kopřivku, hypotenzi, letargii, muskuloskeletální bolest, nauzeu, pruritus, vyrážku, neklid, tachykardii, tlak na hrudi, mravenčení, zvracení, sípot. Pokud se u pacienta vyskytne kterýkoli z těchto příznaků, má léčbu přípravkem ihned ukončit a obrátit se na svého lékaře. V případě šoku je nutno dodržovat aktuální standardní lékařské postupy pro léčbu šoku.
Inhibitory
Tvorba neutralizujících protilátek (inhibitorů) proti faktoru X je možnou komplikací léčby osob s deficiencí faktoru X.
Obecně platí, že všichni pacienti léčení přípravkem Coagadex musí být pečlivě sledováni pro případ tvorby inhibitorů prostřednictvím příslušných klinických pozorování a laboratorních testů. Pokud není dosaženo očekávané hladiny aktivity faktoru X v plazmě, nebo pokud není krvácení patřičnou dávkou zastaveno, je třeba provést test měřící koncentrace inhibitoru faktoru X.
Přenos původců infekcí
Standardní opatření zabraňující přenosu infekce v souvislosti s používáním léčivých přípravků vyrobených z lidské krve nebo plazmy zahrnují pečlivý výběr dárců, testování jednotlivých odběrů krve a plazmatických poolů na specifické ukazatele infekce a určité výrobní kroky odstraňující nebo deaktivující viry. Přesto nemůže být při podávání léčiv vyráběných z lidské krve nebo plazmy zcela vyloučena možnost přenosu infekce. To se vztahuje též na jakékoli neznámé nebo vznikající viry či jiné patogeny.
Přijatá opatření jsou považována za účinná u obalených virů, jako HIV, HBV a HCV, a u neobaleného viru HAV a parvoviru B19.
U pacientů, kterým j sou pravidelně nebo opakovaně podávány přípravky s lidským faktorem X získaným z plazmy, může být nutná vakcinace proti hepatitidě A a B.
Při každém podání přípravku Coagadex pacientovi důrazně doporučujeme zaznamenat název a číslo šarže přípravku, aby bylo možné zpětně zjistit údaje o použité šarži.
Obsah sodíku
Coagadex obsahuje až 0,4 mmol/ml (9,2 mg/ml) sodíku. Nutno vzít v úvahu u pacientů na dietě s nízkým obsahem sodíku.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Působení přípravku Coagadex mohou ovlivnit inhibitory faktoru Xa, přímé či nepřímé. Tato antitrombotika nemají být používána u pacientů s deficiencí faktoru X. Coagadex by neměl být použit jako antidotum proti účinkům přímých perorálních antikoagulancií (DOAC) u pacientů, kteří nemají deficienci faktoru X.
4.6 Fertilita, těhotenství a kojení
Vzhledem k vzácnému výskytu dědičné deficience faktoru X nejsou údaje o podávání přípravku Coagadex těhotným a kojícím ženám k dispozici. Přípravek Coagadex lze proto v těhotenství podávat, pouze pokud je léčba jasně indikována.
Kojení
Vzhledem k vzácnému výskytu dědičné deficience faktoru X nejsou údaje o podávání přípravku Coagadex těhotným a kojícím ženám k dispozici. Přípravek Coagadex lze proto během kojení podávat, pouze pokud je léčba jasně indikována.
Fertilita
Studie reprodukční toxicity na zvířatech s přípravkem Coagadex nebyly provedeny.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Coagadex nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Nežádoucí účinky, které se vyskytly s nejvyšší četností zahrnovaly erytém v místě podání infuze, bolest v místě podání infuze, únavu a bolest zad.
Hypersenzitivní nebo alergické reakce (které mohou zahrnovat angioedém, pálení a štípání v místě podání infuze, zimnici, návaly horka, generalizovanou urtikarii, bolest hlavy, kopřivku, hypotenzi, letargii, nauzeu, neklid, tachykardii, tlak na hrudi, mravenčení, zvracení, sípot) byly pozorovány vzácně v souvislosti s léčbou jiných hemofilií a v některých případech mohou progredovat do těžké anafylaxe (včetně šoku). Hypersenzitivní reakce, alergické reakce a anafylaxe nebyly hlášeny v klinických hodnoceních s přípravkem Coagadex.
Tabulkový seznam nežádoucích účinků
V klinických studiích, které zahrnovaly 18 pacientů léčených přípravkem Coagadex, byly hlášeny níže uvedené nežádoucí účinky.
Kategorie četností jsou vyjádřeny jako: velmi časté: (>1/10); časté: (>1/100 až <1/10); méně časté: (>1/1000 až <1/100); vzácné: (>1/10000 až <1/1000); velmi vzácné: (<1/10000); z dostupných údajů nelze určit.
Seznam nežádoucích účinků (ADR) u 18 léčených pacientů
|
Třídy orgánových systémů podle databáze MedDRA |
Nežádoucí účinek |
Četnost |
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Časté | |
|
Celkové poruchy a reakce v místě aplikace |
Erytém v místě podání infuze Únava Bolest v místě podání infuze |
Časté |
Pediatrická populace
Očekává se, že četnost, typ a závažnost nežádoucích účinků u dětí budou stejné jako u dospělých. Údaje o bezpečnosti týkající se přenosu původců infekcí viz bod 4.4.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
V klinických hodnoceních, během kterých bylo pacientovi podáno přibližně 80 IU/kg přípravku Coagadex k léčbě krvácení, byl hlášen jeden případ neúmyslného předávkování. V souvislosti s tímto předávkováním nebyly hlášeny žádné nežádoucí účinky. V případě předávkování existuje riziko rozvoje tromboembolie.
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antihemoragika, vitamín K a jiná hemostatika, koagulační faktor X, ATC kód: B02BD13.
Mechanismus účinku
Faktor X je inaktivní zymogen, k jehož aktivaci dochází prostřednictvím faktoru IXa (vnitřní cestou) nebo faktoru VIIa (vnější cestou). K přeměně faktoru X z inaktivního na aktivní (faktor Xa) dochází odštěpením peptidu tvořeného 52 aminokyselinami od těžkého řetězce. Faktor Xa za spoluúčasti faktoru Va na fosfolipidovém povrchu tvoří protrombinázový komplex, který aktivuje protrombin na trombin v přítomnosti vápníkových iontů. Trombin poté působí na rozpustný fibrinogen a faktor XIII, čímž dochází k tvorbě fibrinové sraženiny (fibrinové síťky).
Farmakodynamické účinky
Coagadex se získává z lidské plazmy a používá se jako náhrada přirozeně se vyskytujícího koagulačního faktoru X u pacientů s dědičnou deficiencí faktoru X.
Klinická účinnost
V multicentrickém, otevřeném, nerandomizovaném klinickém hodnocení k posouzení farmakokinetiky, bezpečnosti a účinnosti přípravku Coagadex obdrželo dávku 25 IU/kg přípravku Coagadex k léčbě spontánních, traumatických a menstruačních krvácivých příhod 16 pacientů (ve věku 12 let a starších) se středně těžkou až těžkou dědičnou deficiencí faktoru X (FX:C < 5 IU/dl).
Účinnost přípravku Coagadex v léčbě krvácivých příhod byla hodnocena pacientem a/nebo zkoušejícím z hlediska každé nové krvácivé příhody pomocí predeterminované ordinální hodnotící škály pro posuzování účinnosti léčby konkrétního typu krvácení s hodnocením účinnosti jako velmi dobrá, dobrá, špatná a nehodnotitelná. Z 208 krvácivých příhod léčených přípravkem Coagadex bylo 187 krvácivých příhod u 15 pacientů hodnoceno z hlediska účinnosti. Devadesát osm (53 %) z nich byly významné krvácivé příhody a 88 (47 %) zahrnovalo mírné krvácení (jedno krvácení nebylo hodnoceno). Účinnost přípravku Coagadex byla hodnocena jako dobrá (7 %) nebo velmi dobrá (91 %) v léčbě 98 % krvácivých příhod. Ze 187 krvácivých příhod v analýze účinnosti bylo 155 krvácení (83 %) léčeno jednou infuzí, 28 krvácení (15 %) dvěma infuzemi, 3 krvácení (2 %) třemi infuzemi a 1 krvácení (0,5 %) čtyřmi infuzemi. Průměrná dávka na infuzi a celková dávka přípravku Coagadex byly 25,4 IU/kg a 30,4 IU/kg. Čtyři krvácivé příhody u dvou pacientů byly hodnoceny jako nereagující na léčbu. Doporučená dávka 25 IU/kg přípravku Coagadex k léčbě krvácení byla během studie dodržena u 14 z 16 pacientů. Zbývající dva pacienti byli léčeni dávkou až 30 IU/kg a 33 IU/kg.
Jako preventivní opatření bylo podáno celkem 184 infuzí přípravku Coagadex. Pravidelná profylaxe byla použita u dvou pacientů. Jeden pacient dostával 28 IU/kg jednou týdně po dobu 8 týdnů a poté 25 IU/kg každé 2 týdny po dobu více než 5 měsíců. Druhý pacient dostával 24,6 IU/kg jednou týdně po dobu 8,5 měsíců. U žádného z nich nedošlo během této doby k žádnému krvácení.
Bezpečnost a účinnost přípravku Coagadex z hlediska perioperační péče byla hodnocena u pěti pacientů ve věku od 14 až 59 let s mírným (n = 2), středně těžkým (n = 1) a těžkým (n = 2) onemocněním, kteří podstoupili celkem sedm chirurgických zákroků.
Z hlediska všech chirurgických zákroků byl Coagadex hodnocen jako velmi dobrý (nedošlo k žádnému pooperačnímu krvácení, nebyla nutná žádná transfuze krve a nedošlo k žádné neočekávaně vyšší ztrátě krve), co se týče zástavy ztráty krve během chirurgického zákroku a po něm.
V případě velkého chirurgického zákroku bylo k zachování hemostázy zapotřebí v průměru 13 infuzí (2 až 15 infuzí) a průměrná kumulativní dávka 181 IU/kg (45 až 210 IU/kg). U menších chirurgických zákroků bylo k zachování hemostázy zapotřebí v průměru 2,5 infuzí (1 až 4 infuze) a průměrná kumulativní dávka 89 IU/kg (51 až 127 IU/kg).
5.2 Farmakokinetické vlastnosti
V klinické studii přípravku Coagadex u pacientů s těžkou až středně těžkou deficiencí faktoru X (bazální FX:C < 5 IU/dl) bylo vyhodnocení farmakokinetických parametrů provedeno u 16 pacientů po podání nominální dávky 25 IU/kg. Farmakokinetické (FK) parametry byly vypočteny z naměřených hodnot aktivity plazmatického faktoru X:C (jednostupňový test srážení krve) po odečtení hodnoty před podáním dávky. Sloučení hodnot IR z hlediska FX:C při výchozí návštěvě (n = 16) a opakovaném vyhodnocení FK (n = 15) poskytlo celkovou geometrickou střední hodnotu IR 2,07 IU/dl na podanou dávku IU/kg (n = 31). Stejně tak sloučení hodnot t/ při výchozí návštěvě a opakovaném vyhodnocení FK poskytlo celkovou geometrickou střední hodnotu t/ 29,36 hodin. Systémová expozice FX:C při návštěvě s opakovaným vyhodnocením FK (nejméně za 6 měsíců) byla stejná jako při výchozí návštěvě, neboť poměr mezi opakovanými a výchozími hodnotami z hlediska všech FK parametrů byl v rozmezí 90 % až 110 %.
Střední hodnota (CV %) z hlediska postupné obnovy byla 2,08 (18,1). Střední hodnota (CV %) nejvyšší plazmatické koncentrace (Cmax) byla 0,504 (17,2) IU/ml.
Střední hodnota (CV %) z hlediska plochy pod křivkou (AUC 0_i44h) byla 17,1 (21,0) IU.hod/ml.
Lidský koagulační faktor X zůstává z velké části ve vaskulárním kompartmentu: průměrný zdánlivý distribuční objem (Vss) byl 56,3 (24,0) ml/kg.
Průměrný (CV %) poločas lidského koagulačního faktoru X byl 30,3 (22,8) hodin a clearance byla 1,35 (21,7) ml/kg/hod.
Porucha funkce ledvin
Nebyly provedeny žádné farmakokinetické studie, ale neočekává se, že pohlaví nebo funkce ledvin ovlivní farmakokinetický profil přípravku Coagadex.
Porucha funkce jater
Nebyly provedeny žádné farmakokinetické studie, ale neočekává se, že pohlaví nebo funkce jater ovlivní farmakokinetický profil přípravku Coagadex.
Starší osoby
Nebyly provedeny žádné farmakokinetické studie, ale neočekává se, že věk ovlivní farmakokinetický profil přípravku Coagadex.
Dlouhodobé používání
Existují omezené údaje týkající se dlouhodobého používání.
Pediatrická populace
Farmakokinetické studie nebyly provedeny u dětí mladších 12 let. Údaje týkající se postupné obnovy jsou omezené, ale jsou srovnatelné s údaji hlášenými u populace pacientů ve věku 12 let a starších.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje získané na základě konvenčních farmakologických studií bezpečnosti, toxicity po jednorázovém a opakovaném podávání, trombogenicity a lokální snášenlivosti neodhalily žádné zvláštní riziko pro člověka.
Genotoxicita, karcinogenicita a reprodukční a vývojová toxicita nebyly zkoumány, neboť lidský plazmatický koagulační faktor X (obsažený v přípravku Coagadex) je endogenní protein.
6.1 Seznam pomocných látek
Prášek
Kyselina citrónová Hydroxid sodný (pro úpravu pH)
Dihydrogenfosforečnan sodný
Chlorid sodný
Sacharóza
Rozpouštědlo Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto nesmí být tento léčivý přípravek mísen s jinými léčivými přípravky.
Přípravek může být rekonstituován pouze za použití filtračního přepouštěcího adaptéru Mix2Vial, který je součástí balení.
6.3 Doba použitelnosti
3 roky.
Z mikrobiologického hlediska má být přípravek po rekonstituci použit okamžitě. Chemická a fyzikální stabilita přípravku připraveného k použití byla prokázána na dobu 1 hodiny při pokojové teplotě (až 25 °C +/-2 °C).
6.4 Zvláštní opatření pro uchovávání
Neuchovávejte při teplotě nad 30 °C.
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
Podmínky uchovávání tohoto léčivého přípravku po jeho rekonstituci jsou uvedeny v bodě 6.3.
6.5 Druh obalu a obsah balení Vnitřní obal
Injekční lahvička s práškem: 250 IU nebo 500 IU lidského koagulačního faktoru X v injekční lahvičce ze skla třídy I opatřenou halobutylovou pryžovou zátkou s odtrhávacím polypropylenovým uzávěrem a lakovaným hliníkovým okrajem.
Injekční lahvička s rozpouštědlem: 2,5 ml nebo 5 ml roztoku v injekční lahvičce ze skla třídy I uzavřené halobutylovou pryžovou zátkou a uzávěrem.
Filtrační přepouštěcí adaptér (Mix2Vial).
Velikost balení Coagadex 250 IU
1 injekční lahvička obsahující 250 IU lidského koagulačního faktoru X ve formě prášku pro injekční roztok
1 injekční lahvička obsahující 2,5 ml vody na injekci 1 adaptér (Mix2Vial)
Coagadex 500 IU
1 injekční lahvička obsahující 500 IU lidského koagulačního faktoru X ve formě prášku pro injekční roztok
1 injekční lahvička obsahující 5 ml vody na injekci 1 adaptér (Mix2Vial)
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Prášek musí být rekonstituován pouze ve vodě na injekce, která je součástí balení. 250 IU přípravku rekonstituujte v 2,5 ml vody na injekci a 500 IU přípravku v 5 ml vody na injekci.
Nepoužívejte vodu na injekci, pokud jsou patrné známky částic.
Injekční lahvičky před odstraněním odtrhávacího uzávěru z lahvičky s práškem nejdříve zahřejte na pokojovou teplotu (maximálně 30 °C).

1. krok: Odstraňte uzávěr z injekční lahvičky s práškem a očistěte horní část zátky alkoholovým tamponem.
Stejně postupujte i s injekční lahvičkou s rozpouštědlem.
Odtrhněte horní část obalu filtračního přepouštěcího adaptéru, ale adaptér ponechte v
2. krok: Umístěte modrou část adaptéru na injekční lahvičku s rozpouštědlem a stlačujte, dokud hrot nepropíchne pryžovou zátku a nezacvakne na místo.
Odstraňte vnější plastový obal z adaptéru a zlikvidujte jej. Dbejte na to, abyste se nedotkli odkrytého konce adaptéru.
3. krok: Otočte injekční lahvičku s rozpouštědlem s nasazeným adaptérem dnem nahoru.Umístěte průhlednou část adaptéru na injekční lahvičku s práškem a stlačujte, dokud hrot nepropíchne pryžovou zátku a nezacvakne na místo.


4. krok: Rozpouštědlo začne pomocí vakua vtékat do injekční lahvičky s práškem. Injekční lahvičkou jemně otáčejte, aby se prášek řádně promíchal. Injekční lahvičkou netřepejte. Měli byste získat čirý až jemně perleťový roztok, obvykle během 1 minuty (nebo nanejvýš do 5 minut).

5. krok: Odšroubujte prázdnou injekční lahvičku, ve které bylo rozpouštědlo, a modrou část adaptéru od průhledné části adaptéru proti směru hodinových ručiček.

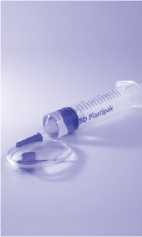
Nasajte vzduch do injekční stříkačky vytažením pístu do požadovaného množství přidané vody. Injekční stříkačku nasaďte na průhlednou část adaptéru a vtlačte vzduch do injekční lahvičky.
6. krok: Injekční lahvičku s roztokem ihned převraťte, aby roztok natekl do injekční stříkačky. Vyjměte naplněnou stříkačku z adaptéru.
Dodržujte běžné bezpečnostní postupy k podání přípravku.
Poznámka: Pokud je k podání dávky nutné použít více injekčních lahviček, opakujte 1. až 6. krok a natáhněte roztok z injekční lahvičky do stejné injekční stříkačky.
Přepouštěcí adaptér, který je součástí balení, je sterilní a nelze jej použít opakovaně. Po rekonstituci má být použitý adaptér zlikvidován do nádoby na ostré předměty.
Při podání musí být roztok bezbarvý, čirý nebo jemně opalescenční. Nepoužívejte roztoky, které jsou zkalené nebo obsahují usazeniny. Rekonstituovaný roztok je nutno před podáním prohlédnout, zda neobsahuje částice či nezměnil barvu.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Bio Products Laboratory Limited,
Dagger Lane,
Elstree,
Hertfordshire,
WD6 3BX,
Velká Británie
8. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/16/1087/001
EU/1/16/1087/002
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace:
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
A. VÝROBCE BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce biologické léčivé látky
Bio Products Laboratory Limited Dagger Lane,
Elstree,
Hertfordshire,
WD6 3BX,
Velká Británie
Název a adresa výrobce odpovědného za propouštění šarží
Bio Products Laboratory Limited Dagger Lane,
Elstree,
Hertfordshire,
WD6 3BX,
Velká Británie
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis s omezením (viz příloha I: Souhrn údajů o přípravku, bod 4.2).
TTV I r V, V f V V r
• Úřední propouštění sarzí
Podle článku 114 směrnice 2001/83/ES bude úřední propouštění šarží provádět některá státní laboratoř nebo laboratoř k tomuto účelu určená.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
• Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
Držitel rozhodnutí o registraci předloží první pravidelně aktualizovanou zprávu o bezpečnosti pro tento léčivý přípravek do 6 měsíců od jeho registrace.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
• Další opatření k minimalizaci rizik
Neuplatňuje se.
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU
KRABIČKA 250 IU_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Coagadex 250 IU
prášek a rozpouštědlo pro injekční roztok factor X coagulationis humanus
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
250 IU lidského koagulačního faktoru X, přibližně 100 IU/ml
3. SEZNAM POMOCNÝCH LÁTEK
Dále obsahuje:
Injekční lahvička s práškem: Kyselina citronová, hydroxid sodný, hydrogenfosforečnan sodný, chlorid sodný, sacharóza.
Injekční lahvička s rozpouštědlem: voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Prášek a rozpouštědlo pro injekční roztok.
Jedno balení obsahuje:
1 injekční lahvička s práškem 1 filtrační přepouštěcí adaptér
1 injekční lahvička s rozpouštědlem, které obsahuje 2,5 ml vody na injekci
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pro intravenózní podání po rekonstituci Před použitím si přečtěte příbalovou informaci.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do (EXP):
Použijte do 1 hodiny po rekonstituci.
Neuchovávejte při teplotě nad 30 °C.
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Bio Products Laboratory Limited, Dagger Lane,
Elstree,
Hertfordshire,
WD6 3BX,
Velká Británie
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/16/1087/001
13. ČÍSLO ŠARŽE
Č. š.:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
coagadex 250 iu
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Coagadex 500 IU
prášek a rozpouštědlo pro injekční roztok factor X coagulationis humanus
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
500 IU lidského koagulačního faktoru X, přibližně 100 IU/ml
3. SEZNAM POMOCNÝCH LÁTEK
Dále obsahuje:
Injekční lahvička s práškem: kyselina citronová, hydroxid sodný, dihydrogenfosforečnan sodný, chlorid sodný, sacharóza.
Injekční lahvička s rozpouštědlem: voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Prášek a rozpouštědlo pro injekční roztok.
Jedno balení obsahuje:
1 injekční lahvička s práškem 1 filtrační přepouštěcí adaptér
1 injekční lahvička s rozpouštědlem, které obsahuje 5 ml vody na injekci
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Pro intravenózní podání po rekonstituci Před použitím si přečtěte příbalovou informaci.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
Použitelné do (EXP):
Použijte do 1 hodiny po rekonstituci.
Neuchovávejte při teplotě nad 30 °C.
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Bio Products Laboratory Limited, Dagger Lane,
Elstree,
Hertfordshire,
WD6 3BX,
Velká Británie.
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/16/1087/002
13. ČÍSLO ŠARŽE
Č. š.:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
coagadex 500 iu
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Coagadex 250 IU
prášek pro injekční roztok
factor X coagulationis humanus
2. ZPŮSOB PODÁNÍ_
Pro i.v. podání po rekonstituci.
Před použitím si přečtěte příbalovou informaci.
3. POUŽITELNOST_
EXP:
4. ČÍSLO ŠARŽE_
Č. š.:
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
250 IU
6. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Coagadex 500 IU
prášek pro injekční roztok
factor X coagulationis humanus
2. ZPŮSOB PODÁNÍ
Pro i.v. po rekonstituci
Před použitím si přečtěte příbalovou informaci.
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Č. š.:
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
500 IU
6. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Voda na injekci 2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Č. š.:
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
2,5 ml
6. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Voda na injekci 2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP:
4. ČÍSLO ŠARŽE
Č. š.:
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
5 ml
6. JINÉ
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro pacienta
Coagadex 250 IU Coagadex 500 IU
prášek a rozpouštědlo pro injekční roztok
Factor X coagulationis humanus
'VTento přípravek podléhá dalšímu sledování. To umožní rychlé získání nových informací o bezpečnosti. Můžete přispět tím, že nahlásíte jakékoli nežádoucí účinky, které se u Vás vyskytnou. Jak hlásit nežádoucí účinky je popsáno v závěru bodu 4.
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Coagadex a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Coagadex používat
3. Jak se Coagadex používá
4. Možné nežádoucí účinky
5. Jak Coagadex uchovávat
6. Obsah balení a další informace
1. Co je Coagadex a k čemu se používá
Coagadex je koncentrát lidského koagulačního faktoru X, proteinu, který je nutný pro srážení krve. Faktor X obsažený v přípravku Coagadex je získán z lidské plazmy (tekutá část krve). Používá se k léčbě a prevenci krvácení u pacientů s dědičnou deficiencí (nedostatkem) faktoru X, včetně během chirurgického zákroku.
Pacienti s deficiencí faktoru X nemají dostatečné množství faktoru X potřebné ke správnému srážení krve, což vede k nadměrnému krvácení. Coagadex nahrazuje chybějící faktor X a umožňuje normální srážení krve.
2. Čemu musíte věnovat pozornost, než začnete Coagadex používat.
Nepoužívejte Coagadex:
- jestliže jste alergický(á) na lidský koagulační faktor X nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
Promluvte si se svým lékařem, jestliže se domníváte, že se Vás týká cokoli z výše uvedeného.
Upozornění a opatření
Před použitím přípravku Coagadex se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou:
-jestliže u Vás došlo k rozsáhlému nebo delšímu krvácení než obvykle a k zastavení krvácení nedojde po podání injekce přípravku Coagadex.
U některých pacientů s nedostatkem faktoru X může dojít k rozvoji inhibitorů (protilátek) faktoru X během léčby. V takovém případě by to mohlo znamenat, že léčba nebude účinná. Lékař Vás bude pravidelně kontrolovat pro případ tvorby těchto protilátek, a zvláště pak před chirurgickým zákrokem. Před léčbou tímto lékem a po jejím skončení, zejména během prvního léčebného cyklu, provede lékař několik testů ke kontrole hladiny faktoru X v krvi.
Virová bezpečnost
V případě léků vyráběných z lidské krve nebo plazmy jsou přijata určitá opatření zabraňující přenos infekcí na příjemce. Tato opatření zahrnují:
- pečlivý výběr dárců krve a plazmy za účelem vyloučení osob, u nichž hrozí riziko přenosu infekce,
- testování všech jednotlivých odběrů a plazmatických poolů pro případ výskytu známek přítomnosti virů/infekcí,
- přijetí kroků pro inaktivaci nebo odstranění virů při zpracovávání krve nebo plazmy.
Přijatá opatření jsou považována za účinná u těchto virů: lidský virus imunodeficience (HIV), virus hepatitidy B, virus hepatitidy C, virus hepatitidy A a parvovirus B19. Přes tato opatření při podávání léků vyráběných z lidské krve nebo plazmy nelze možnost přenosu infekce zcela vyloučit. To platí i pro jakékoli neznámé nebo vznikající viry či jiné druhy infekcí.
Při každém podání dávky přípravku Coagadex důrazně doporučujeme zaznamenat název a číslo šarže přípravku, aby se uchoval záznam o použitých šaržích.
Pokud jsou Vám přípravky s lidským faktorem X získaným z plazmy podávány pravidelně nebo opakovaně, může Vám lékař doporučit očkování proti hepatitidě A a B.
Děti a dospívající
Uvedená upozornění a opatření pro dospělé se týkají také dětí (ve věku od 2 do 11 let) a dospívajících (ve věku od 12 do 18 let).
Další léčivé přípravky a Coagadex
Informujte svého lékaře o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. Určitá antikoagulancia (léky snižující srážlivost krve), včetně léků blokujících faktor srážení krve (faktor Xa), nemá být používána u pacientů s deficiencí faktoru X, kteří jsou léčeni přípravkem Coagadex, z důvodu rizika vzniku krevních sraženin.
Těhotenství, kojení a plodnost
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek používat.
Řízení dopravních prostředků a obsluha strojů
Nebyly pozorovány žádné účinky tohoto přípravku na schopnost řídit nebo obsluhovat stroje. Coagadex obsahuje sodík
Tento léčivý přípravek obsahuje až 0,4 mmol/ml (9,2 mg/ml) sodíku. Nutno vzít v úvahu u pacientů na dietě s nízkým obsahem sodíku.
3. Jak se Coagadex používá
Léčba má být zahájena lékařem se zkušenostmi s léčbou krvácivých poruch.
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Coagadex se podává injekcí přímo do žíly. Aplikace injekcí tohoto přípravku můžete provádět také doma po patřičném vyškolení zdravotnickým pracovníkem.
Lékař Vám vysvětlí, jakou dávku máte použít, kdy ji použít a jak dlouho. Lékař Vám obvykle předepíše dávku z hlediska počtu celých injekčních lahviček, který obsahuje dávku, která je pro Vás nejvhodnější.
Dospělí
Jaké množství přípravku Coagadex se podává při léčbě krvácení nebo k prevenci dalšího krvácení?
Lékař Vám sdělí, jaké množství přípravku Coagadex máte podat k léčbě krvácení a prevenci dalšího krvácení; požadovaná dávka bude záviset na Vaší normální hladině faktoru X v krvi
Jaké množství se podává před velkým chirurgickým zákrokem, během něj a po něm?
Před operací: Použitá dávka přípravku Coagadex má být dostatečně vysoká, aby došlo ke zvýšení hladiny faktoru X na 70 jednotek/dl, ale jeho hladina nemá překročit 100 jednotek/dl. Požadovanou dávku vypočte lékař podle Vaší normální hladiny faktoru X v krvi.
Po operaci: Během několika prvních dnů po chirurgickém zákroku bude Vaše koncentrace faktoru X v plazmě pravidelně kontrolována. Vaše hladina faktoru X v krvi má být udržována na více než 50 jednotkách/dl. Dávku, kterou budete potřebovat, vypočte Váš lékař.
Pokud bude Vaše hladina faktoru X v krvi příliš nízká (dle stanovení Vašeho lékaře), nebo pokud dojde k jejímu snížení rychleji, než je běžné, může být v krvi přítomen inhibitor faktoru X, který brání působení přípravku Coagadex. Váš lékař provede náležitá laboratorní vyšetření ke stanovení přítomnosti těchto inhibitorů v krvi.
Jaké množství se pravidelně podává při dlouhodobé prevenci krvácení?
Váš lékař Vás bude informovat, zda je tento přípravek pro Vás vhodný, a pokud ano, předepíše vhodnou dávku.
Použití u dětí a dospívajících
Váš lékař Vám doporučí vhodnou dávku. Při výpočtu dávek u těchto věkových skupin se má postupovat stejně jako u dospělých.
Kdy je třeba podat injekci přípravku Coagadex
• Přípravek má být podán při výskytu prvních známek krvácení.
• Injekci je třeba dle potřeby podat opakovaně, aby došlo k zástavě krvácení.
• Každé jednotlivé krvácení je nutné posoudit z hlediska závažnosti.
• Pokud tento lék používáte poprvé, budete pod lékařským dohledem.
Rekonstituce přípravku před použitím
Tento přípravek musí být rekonstituován pouze v rozpouštědle, které je součástí balení.
|
Množství přípravku Coagadex |
Množství rozpouštědla |
|
250 IU |
2,5 ml |
|
500 IU |
5 ml |
Coagadex je dodáván s množstvím rozpouštědla uvedeném v tabulce.
Přípravek Coagadex můžete rozpustit pomocí filtračního přepouštěcího adaptéru Mix2Vial, který je součástí každého balení.
Před smícháním zahřejte lahvičku přípravku Coagadex na pokojovou teplotu.
Při přípravě léku postupujte podle níže uvedených kroků:




1. krok
• Odstraňte uzávěr z injekční lahvičky s práškem a očistěte horní část zátky pomocí alkoholového vatového tamponu.
• Stejně postupujte i s lahvičkou s rozpouštědlem.
• Odtrhněte horní část obalu adaptéru, ale ponechte jej v obalu.
2. krok
• Umístěte modrou část adaptéru na injekční lahvičku s rozpouštědlem a stlačujte, dokud hrot nepropíchne pryžovou zátku a nezacvakne na místo.
• Odstraňte vnější plastový obal z adaptéru a zlikvidujte jej. Dbejte na to, abyste se nedotkl(a) odkrytého konce adaptéru.
3. krok
• Otočte injekční lahvičku s rozpouštědlem s nasazeným adaptérem dnem nahoru.
• Umístěte průhlednou část adaptéru na injekční lahvičku s práškem a stlačujte, dokud hrot nepropíchne pryžovou zátku a nezacvakne na místo.
4. krok
• Rozpouštědlo začne pomocí vakua vtékat do injekční lahvičky s práškem.
• Injekční lahvičkou jemně otáčejte, aby se prášek řádně promíchal. Injekční lahvičkou netřepejte.
• Měl(a) byste získat čirý až jemně perleťový roztok, obvykle během 1 minuty (nebo nanejvýš do 5 minut).
5. krok
• Odšroubujte prázdnou injekční lahvičku, ve které bylo rozpouštědlo, a modrou část adaptéru od průhledné části adaptéru proti směru hodinových ručiček.
• Nasajte vzduch do injekční stříkačky vytažením pístu do požadovaného množství přidané vody.
• Injekční stříkačku nasaďte na průhlednou část adaptéru a stlačte vzduch v injekční stříkačce do injekční lahvičky.
6. krok
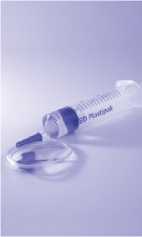
• Injekční lahvičku s roztokem, který se natáhne do injekční stříkačky, ihned převraťte.
• Vyjměte naplněnou stříkačku z injekční lahvičky.
• Přípravek je nyní připraven k použití. Dodržujte běžné bezpečnostní postupy k podání. Přípravek použijte do jedné hodiny po přípravě.
Tento přípravek nepoužívejte v těchto případech:
- jestliže rozpouštědlo nebylo nataženo do injekční lahvičky (znamená to, že došlo ke ztrátě vakua v lahvičce, a proto nesmí být prášek použit).
- jestliže rozpuštěný prášek a rozpouštědlo vytvoří gel nebo se srazí (pokud k tomu dojde, informujte o tom svého poskytovatele zdravotní péče a uveďte číslo šarže vytištěné na injekční lahvičce).
Jestliže jste použil(a) více přípravku Coagadex, než jste měl(a)
Pokud jste podal(a) více přípravku Coagadex, než Vám předepsal lékař, je možné, že u Vás dojde ke vzniku krevní sraženiny. Pokud se domníváte, že jste použil(a) příliš velkou dávku, injekci neaplikujte a oznamte to lékaři, lékárníkovi nebo zdravotní sestře. Jestliže víte, že jste použil(a) příliš velkou dávku, oznamte to lékaři, lékárníkovi nebo zdravotní sestře co nejdříve.
Jestliže jste zapomněl(a) použít Coagadex
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku. Aplikujte si svou běžnou dávku, jakmile si vzpomenete, a pak pokračujte v aplikaci dávek podle pokynů svého lékaře.
Jestliže jste přestal(a) používat Coagadex
Vždy se poraďte se svým lékařem dříve, než se rozhodnete léčbu ukončit.
Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Alergické reakce (hypersenzitivní reakce) se během léčby krvácivých příhod podobnými léky vyskytly vzácně (vyskytly se až u 1 z 1000 osob), a někdy se mohou vyvinout v šok. Známky těchto reakcí mohou zahrnovat kožní vyrážku (včetně kopřivky), brnění, návaly horka, pocit na zvracení, zvracení, bolest hlavy, kašel, sípot, tlak na hrudi, zimnici, zrychlenou srdeční frekvenci, závrať, letargii, neklid, otok obličeje, stažení hrdla, nepříjemný pocit v místě vpichu.
Pokud se u Vás vyskytne kterýkoli z těchto účinků, vyhledejte svého lékaře.
V souvislosti s přípravkem Coagadex byly hlášeny tyto nežádoucí účinky:
Časté (mohou postihnout až 1 z 10 pacientů):
• bolest nebo zarudnutí v místě vpichu
• únava
• bolest zad
Nežádoucí účinky u dětí a dospívajících
Očekává se, že nežádoucí účinky u dětí budou stejné jako u dospělých.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Coagadex uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na lahvičkách za zkratkou „EXP“. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Neuchovávejte při teplotě nad 30 °C.
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
Nepoužívejte tento přípravek, pokud si všimnete malých částic v rekonstituovaném přípravku. Přípravek Coagadex musí být použit do jedné hodiny po přípravě.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Vaše zdravotnické zařízení Vám poskytne speciální nádobu k likvidaci veškerého zbylého roztoku, použitých injekčních stříkaček, injekčních jehel a prázdných obalů. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co Coagadex obsahuje
- Léčivou látkou je lidský koagulační faktor X. Jedna injekční lahvička obsahuje nominálně 250 IU nebo 500 IU lidského koagulačního faktoru X.
- Dalšími složkami jsou: kyselina citronová, dihydrogenfosforečnan sodný, chlorid sodný hydroxid sodný a sacharóza (další informace o složkách viz bod 2).
- Rozpouštědlo: voda na inj ekci.
Jak Coagadex vypadá a co obsahuje toto balení
Coagadex je bílý až téměř bílý prášek, který je dodáván v množství 250 IU a 500 IU. Po přípravě je roztok bezbarvý, čirý nebo perleťový (opalescentní). Před podáním injekce si roztok prohlédněte. Pokud bude roztok zakalený nebo bude obsahovat jakékoli částice, nepoužívejte jej.
Součástí balení je také filtrační přepouštěcí adaptér Mix2Vial.
Balení
1 injekční lahvička obsahující 250 IU prášku 1 injekční lahvička obsahující 2,5 ml vody na injekci 1 adaptér (Mix2Vial)
nebo
1 injekční lahvička obsahující 500 IU prášku 1 injekční lahvička obsahující 5 ml vody na injekci 1 adaptér (Mix2Vial)
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
Bio Products Laboratory Limited
Dagger Lane
Elstree,
Hertfordshire WD6 3BX Velká Británie
Tel: +44 (0) 20 8957 2200 e-mail: medinfo@bpl.co.uk
Další informace o tomto přípravku získáte u držitele rozhodnutí o registraci:
Tato příbalová informace byla naposledy revidována v
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
32