Buprenorphine Actavis 35 Mikrogramů/H Transdermální Náplast
Sp.zn.sukls176462/2014
Příbalová informace: informace pro uživatele
Buprenorphine Actavis 35 mikrogramů/h transdermální náplast Buprenorphine Actavis 52,5 mikrogramů/h transdermální náplast Buprenorphine Actavis 70 mikrogramů/h transdermální náplast
buprenorphinum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Buprenorphine Actavis a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Buprenorphine Actavis používat
3. Jak se přípravek Buprenorphine Actavis používá
4. Možné nežádoucí účinky
5 Jak přípravek Buprenorphine Actavis uchovávat
6. Obsah balení a další informace
1. Co je přípravek Buprenorphine Actavis a k čemu se používá
Buprenorphine Actavis je analgetikum (lék k tlumení bolesti), který se používá k tlumení středně silné až silné bolesti při nádorovém onemocnění a silné bolesti, která nereaguje na jiné léky proti bolesti. Přípravek Buprenorphine Actavis náplasti se aplikuje na kůži a léčivá látka buprenorfin se vstřebává kůží do krve.
Buprenorfin je opioid (silný lék k tlumení bolesti), který tlumí bolest tím, že působí na centrální nervový systém (na určité buňky v mozku a míše). Účinek transdermální náplasti trvá až 3 dny. Buprenorphine Actavis není vhodný k léčení akutní (krátkodobé) bolesti.
2. Čemu musíte věnovat pozornost, než začnete přípravek Buprenorphine Actavis používat Nepoužívejte přípravek Buprenorphine Actavis
- jestliže jste alergický(á) na buprenorfin, sóju, arašídy nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud jste závislý(á) na silných lécích proti bolesti (opioidních analgetikách)
- pokud trpíte chorobami, při kterých máte velké dýchací obtíže nebo při kterých se mohou tyto obtíže objevit
- pokud současně užíváte inhibitory MAO (určité léky k léčbě deprese) nebo pokud jste tyto léky užíval(a) během posledních 2 týdnů (viz „Další léčivé přípravky a přípravek Buprenorphine Actavis“)
- pokud trpíte myastenií gravis (určitý typ těžké svalové slabosti)
- pokud trpíte deliriem tremens (zmatenost a třes po abstinenci alkoholu po dlouhodobé nadměrné konzumaci spojené se závislostí )
- jste-li těhotná.
Buprenorphine Actavis nesmí být užíván k léčbě abstinenčních příznaků u drogově závislých osob. Upozornění a opatření
Před použitím přípravku Buprenorphine Actavis se poraďte se svým lékařem nebo lékárníkem:
- pokud jste požil(a) velké množství alkoholu
- pokud trpíte onemocněním, které je doprovázeno záchvaty
- při poruchách vědomí (mdloby, závrať) neznámého původu
- při šokových stavech (příznakem může být studený pot)
- při zvýšeném nitrolebním tlaku (např. po poraněních hlavy nebo při onemocněních mozku), když není dostupné umělé dýchání
- při dýchacích potížích, nebo pokud užíváte jiné léky, které mohou dýchání zpomalovat nebo zeslabovat. (viz „Další léčivé přípravky a přípravek Buprenorphine Actavis“)
- pokud Vaše játra správně nefungují
- pokud máte sklon ke zneužívání léků nebo drog.
Věnujte také, prosím, pozornost následujícím upozorněním:
• Někteří lidé se mohou stát závislými, pokud užívají silné léky proti bolesti jako je Buprenorphine Actavis delší dobu. Pokud užívání ukončí, mohou mít abstinenční příznaky (viz „Jestliže jste přestal (a) používat přípravek Buprenorphine Actavis“).
• Horečka nebo vnější teplo mohou vést k vyšším hodnotám buprenorfinu v krvi než obvykle. Vnější teplo může také zabránit náplasti správně přilnout. Proto se nevystavujte vnějšímu teplu (např. sauna, infračervená lampa, elektrické deky, termolahve) a pokud máte horečku, poraďte se se svým lékařem.
Buprenorphine Actavis nesmí užívat osoby mladší 18 let, protože dosud nejsou zkušenosti s používáním v této věkové skupině.
Další léčivé přípravky a přípravek Buprenorphine Actavis
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
• Buprenorphine Actavis se nesmí užívat spolu s inhibitory MAO (určité léky k léčbě deprese) nebo pokud jste je užíval(a) v posledních dvou týdnech.
• Buprenorphine Actavis může způsobovat u některých lidí únavu, ospalost, nevolnost nebo mdloby nebo zpomalovat a zeslabovat dýchání. Tyto nežádoucí účinky mohou být ještě zesíleny, pokud zároveň užíváte jiné léky, které mohou vyvolat stejné účinky. Tyto jiné léky zahrnují jiné silné přípravky proti bolesti (opioidy), přípravky na spaní, anestetika (léčiva k vyvolání narkózy), léky užívané k léčbě určitých psychických onemocnění - trankvilizéry (proti úzkosti a strachu), antidepresiva a neuroleptika.
• Užívá-li se Buprenorphine Actavis spolu s některými jinými léky, může být působení náplasti zesíleno. Tyto léky zahrnují např. určité přípravky proti infekčním a plísňovým onemocněním (např.léky obsahující erythromycin, ketokonazol) nebo léky proti HIV (obsahující např. ritonavir). .
• Je-li Buprenorphine Actavis používán s některými jinými léky, působení náplasti je oslabeno. Mezi tyto léky patří např. dexamethason, určité léky k léčbě epilepsie (obsahující např. karbamazepin nebo fenytoin), léky k léčbě tuberkulózy (např.rifampicin).
Buprenorphine Actavis s jídlem, pitím a alkoholem
Během používání náplasti Buprenorphine Actavis nesmíte pít alkohol. Alkohol může zesílit určité nežádoucí účinky přípravku a nemusíte se cítit dobře.
Grapefruitová šťáva může zesílit účinky přípravku Buprenorphine Actavis.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Dosud není dostatek zkušeností s používáním přípravku u těhotných. Z toho důvodu se nesmí přípravek Buprenorphine Actavis během těhotenství používat.
Kojení
Buprenorfin, léčivá látka obsažená v náplasti, snižuje tvorbu mléka a je vylučován do mateřského mléka. Proto používání přípravku Buprenorphine Actavis během kojení není vhodné a je třeba se ho vyvarovat.
Řízení dopravních prostředků a obsluha strojů
Buprenorphine Actavis může způsobovat závratě, ospalost, rozmazané nebo dvojité vidění a ovlivnit Vaše reakce do té míry, že byste nemusel(a) reagovat přiměřeně nebo dostatečně rychle v neočekávaných nebo náhlých situacích.
Toto platí zejména:
• na začátku léčby
• při změně dávkování
• pokud přecházíte na přípravek Buprenorphine Actavis z jiného přípravku
• pokud zároveň užíváte jiné přípravky, které působí na mozek
• pokud pijete alkohol.
Jste-li takto ovlivněn(a), nesmíte během používání přípravku Buprenorphine Actavis řídit nebo obsluhovat stroje. To platí rovněž při ukončení léčby přípravkem Buprenorphine Actavis. Neřiďte a neobsluhujte stroje nejméně 24 hodin po odstranění náplasti.
Jestliže si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Buprenorphine Actavis obsahuje sójový olej. Pokud jste alergický(á) na arašídy nebo sóju, nepoužívejte tento přípravek.
3. Jak se přípravek Buprenorphine Actavis používá
K dispozici jsou tři síly transdermální náplasti: Buprenorphine Actavis 35 mikrogramů/h, Buprenorphine Actavis 52,5 mikrogramů/h a Buprenorphine Actavis 70 mikrogramů/h.
Váš lékař vybere takovou sílu náplasti, která je pro vás nejvhodnější. Během léčby může lékař sílu změnit na nižší nebo vyšší, pokud je to nutné.
Vždy používejte přípravek Buprenorphine Actavis přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Doporučená dávka je:
Dospělí
Pokud neurčil lékař jinak, nalepte jednu náplast přípravku Buprenorphine Actavis (způsobem, jak je níže podrobně popsáno) a vyměňte ji nejpozději po 3 dnech. K lepšímu zapamatování, kdy je třeba náplast vyměnit, si udělejte poznámku na obalu přípravku. Pokud Vám Váš lékař předepsal k náplasti další léky proti bolesti, dodržujte přesně jeho rady a doporučení, jinak nebudete mít z léčby prospěch.
Pacienti mladší 18 let
Buprenorphine Actavis se nemá používat u osob mladších 18 let, protože s touto věkovou skupinou nejsou žádné zkušenosti.
Starší pacienti
Starší pacienti nevyžadují úpravu dávkování přípravku Buprenorphine Actavis.
Pacienti s onemocněním ledvin /dialyzovaní pacienti
U pacientů s onemocněním ledvin a u dialyzovaných pacientů nejsou žádné úpravy dávkování nutné.
Pacienti s onemocněním jater
U pacientů s onemocněními jater mohou být intenzita a trvání účinku náplasti Buprenorphine Actavis
ovlivněny. Pokud patříte k této skupině pacientů, měli byste být pod pečlivým lékařským dohledem.
Instrukce k otevření bezpečnostně uzavřeného sáčku
1. Nastřihněte v místě zářezu/šipek na obou stranách.
2. Roztrhněte v místě zářezu a podél zatavení.
3. Otevřete sáček a vyjměte náplast.
Způsob podání
Než nalepíte transdermální náplast
• Zvolte si na Vaší horní části těla ploché, neochlupené místo, pokud možno vpředu pod klíční kostí na hrudníku nebo na horní části zad. Jestliže nemůžete náplast nalepit sám(a), požádejte někoho o pomoc.
• Jestliže je vybrané místo ochlupené, ostřihejte ochlupení nůžkami. Nesmí se holit!
• Vyvarujte se zarudlé, podrážděné nebo jinak poškozené kůže, např. většími jizvami.
• Vybraná část kůže musí být suchá a čistá. Je-li zapotřebí, umyjte ji studenou nebo vlažnou vodou. Nepoužívejte mýdlo nebo jiné prostředky. Po horké koupeli nebo sprše počkejte, dokud není Vaše kůže úplně suchá a ochlazená. Nenanášejte na místo, kam budete lepit náplast, žádné krémy, masti, pleťová mléka. Mohly by zabránit správnému přilnutí náplasti.
Nalepení náplasti
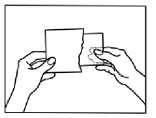
1.
Neotvírejte sáček, pokud nemáte v úmyslu náplast ihned nalepit. Každá transdermální náplast je balena samostatně v sáčku.
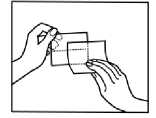
2.
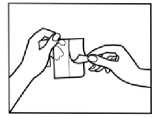
3.
Odstraňte separační fólii.
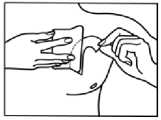
4.
Odlepte polovinu ochranné fólie. Nedotýkejte se přilnavé části.
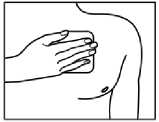
5.
Nalepte náplast na vybrané místo na kůži a odstraňte zbytek ochranné fólie.
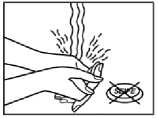
Přitlačte náplast na kůži celou dlaní po dobu 30 až 60 sekund. Ujistěte se, že je náplast na kůži nalepená v celé ploše, zejména při okrajích.
Po nalepení náplasti si umyjte ruce. Nepoužívejte mýdlo ani jiné mycí prostředky.
Nošení náplasti
Můžete nechat náplast na kůži až 3 dny. Předpokládá se, že pokud je náplast správně připevněna, riziko jejího uvolnění je malé. Můžete se s ní sprchovat, koupat a plavat. Ale nevystavujte náplast působení nadměrného tepla (např. v sauně, infračervené lampy, elektrické deky, termolahve).
V nepravděpodobném případě, že se náplast uvolní dříve než je potřeba ji vyměnit, nepoužívejte znovu stejnou náplast. Nalepte si rovnou novou náplast (viz odstavec níže „Výměna náplasti“).
Výměna náplasti
• Odstraňte starou náplast.
• Složte ji napůl přilnavou stranou k sobě.
• Pečlivě ji zlikvidujte. Nesmí zůstat v dosahu a dohledu dětí.
• Nalepte novou náplast na vhodné místo na kůži (jak je popsáno výše). Nejméně jeden týden vyčkejte před nalepením náplasti na stejné místo.
Délka léčby
Váš lékař rozhodne, jak dlouho máte být léčeni přípravkem Buprenorphine Actavis. Nesmíte léčbu ukončit na základě vlastního uvážení, protože bolest by se mohla vrátit a nemuseli byste se cítit dobře (viz také „Jestliže jste přestal(a) používat přípravek Buprenorphine Actavis“).
Pokud máte pocit, že účinek náplastí Buprenorphine Actavis je příliš slabý nebo příliš silný, sdělte to svému lékaři nebo lékárníkovi.
Jestliže jste použil(a) více přípravku Buprenorphine Actavis, než jste měl(a)
Pokud se to stane, může dojít k předávkování buprenorfinem. Předávkování může zesílit nežádoucí účinky buprenorfinu jako je ospalost, nevolnost a zvracení. Můžete mít zúžené zornice a dýchání se může zpomalit a zeslabit. Může také dojít ke kardiovaskulárnímu kolapsu.
Jakmile zjistíte, že jste použil(a) více náplastí, než máte, odstraňte přebytečné náplasti a poraďte se se svým lékařem nebo lékárníkem.
Jestliže jste zapomněl(a) použít přípravek Buprenorphine Actavis
Pokud jste si zapomněl(a) náplast nalepit, nalepte novou náplast hned, jakmile to zjistíte. Pokud si vyměníte náplast velmi pozdě, bolest se může vrátit. V tomto případě kontaktujte svého lékaře. Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku!
Jestliže jste přestal(a)používat přípravek Buprenorphine Actavis
Jestliže přerušíte nebo ukončíte léčbu přípravkem Buprenorphine Actavis příliš brzy, bolest se vrátí. Pokud si přejete ukončit léčbu z důvodu nežádoucích účinků, poraďte se, prosím, se svým lékařem. Řekne Vám, jaké jsou další možnosti, popř. jaké jiné léčivé přípravky by pro Vás přicházely v úvahu.
Někteří lidé po déletrvajícím používání silných léků proti bolesti, které je ukončeno nebo náhle přerušeno, mohou mít tzv. abstinenční příznaky (příznaky z vysazení). Riziko těchto účinků po ukončení užívání přípravku Buprenorphine Actavis je velmi nízké. Přesto, jestliže cítíte neklid, úzkost, nervozitu, třes, jestliže jste abnormálně aktivní, máte obtíže se spaním nebo zažíváním, sdělte to svému lékaři.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Byly hlášeny následující nežádoucí účinky:
Velmi časté (mohou postihnout více než 1 z 10 osob):
nauzea (pocit na zvracení), zarudnutí, svědění
Časté (mohou postihnout až 1 z 10 osob):
závratě, bolesti hlavy, dušnost, zvracení, zácpa, změny na kůži (vyrážka, obvykle při opakovaném podání), pocení, otoky (např. nohou), únava
Méně časté (mohou postihnout až 1 ze 100 osob):
zmatenost, poruchy spánku, neklid, různé stupně útlumu (sedace), v rozpětí od únavy po otupělost, poruchy oběhu (jako je nízký krevní tlak nebo vzácně i oběhový kolaps), sucho v ústech, vyrážka, potíže s vylučováním, retence moči (méně moči než obvykle), únava
Vzácné (mohou postihnout až 1 z 1000 osob):
ztráta chuti k jídlu, klamné představy jako halucinace, úzkost a noční můry, snížený zájem o pohlavní život, obtížné soustředění, poruchy řeči, otupělost, poruchy rovnováhy, abnormální kožní vjemy (necitlivost, píchání nebo pálení), poruchy vidění, rozmazané vidění, otoky víček, návaly horka, obtížné dýchání (pokles dýchání), pálení žáhy, kopřivka, potíže s erekcí, abstinenční příznaky (viz níže), reakce v místě aplikace
Velmi vzácné (mohou postihnout až 1 z 10 000 osob):
závažné alergické reakce (viz níže), závislost, střídání nálad, svalové záškuby, poruchy vnímání chuti, „špendlíkové“ zornice, bolesti uší, abnormálně rychlý dech, škytavka, říhání, vřídky, malé puchýře, bolesti na hrudi
V některých případech se mohou objevit závažné opožděné alergické reakce se znaky zánětu.
V takovém případě přestaňte přípravek Buprenorphine Actavis používat a oznamte to Vašemu lékaři.
Pokud se u Vás objeví otoky paží, nohou, kotníků, obličeje, rtů, úst nebo hrdla, které mohou způsobit dýchací nebo polykací potíže, kopřivka, mdloby, zažloutnutí kůže nebo bělma (tzv. žloutenka), odstraňte náplast a okamžitě přivolejte lékaře nebo vyhledejte pohotovost v nejbližší nemocnici. Může se jednat o příznaky velmi vzácné závažné alergické reakce.
Někteří lidé mohou mít abstinenční příznaky (příznaky z přerušení podávání), pokud užívali silné léky proti bolesti po dlouhou dobu a náhle je přestali užívat. Riziko, že budete mít následné účinky, když přestanete náplasti přípravku Buprenorphine Actavis používat, je malé. Avšak cítíte-li neklid, úzkost, nervozitu nebo třes, nebo jste-li příliš aktivní, máte potíže se spaním nebo se zažíváním, informujte svého lékaře.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv Šrobárova 48 100 41 Praha 10
webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Buprenorphine Actavis uchovávat Uchovávejte tento přípravek mimo dosah a dohled dětí
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na krabičce a sáčku za „Použitelné do:/EXP (měsíc/rok)“.
Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte při teplotě do 25°C.
Chraňte před mrazem.
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak máte likvidovat přípravky, které již nepotřebujete. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co přípravek Buprenorphine Actavis obsahuje
Léčivou látkou je buprenorphinum.
Buprenorphine Actavis 35 mikrogramů/h transdermální náplast: Jedna transdermální náplast obsahuje 20 mg buprenorfinu a uvolňuje 35 mikrogramů buprenorfinu za hodinu. Plocha obsahující léčivou látku je 25 cm2.
Buprenorphine Actavis 52,5 mikrogramů/h transdermální náplast: Jedna transdermální náplast obsahuje 30 mg buprenorfinu a uvolňuje 52,5 mikrogramů buprenorfinu za hodinu. Plocha obsahující léčivou látku je 37,5 cm2.
Buprenorphine Actavis 70 mikrogramů/h transdermální náplast: Jedna transdermální náplast obsahuje 40 mg buprenorfinu a uvolňuje 70 mikrogramů buprenorfinu za hodinu. Plocha obsahující léčivou látku je 50 cm2.
Pomocnými látkami jsou:
Adhezivní vrstva obsahující léčivou látku: blokové kopolymery styren-butadien-styrenový a styren-butadienový, kalafunová pryskyřice, antioxidanty (2,4-Bis(1,1-dimethylethyl)fenyl)fosfit (3:1); tris(2,4-di-terc-butylfenyl)fosfát), olejový extrakt z listů aloe vera (obsahuje také čištěný sójový olej a tokoferol-alfa-acetát)
Krycí vrstva: složená polyethylenová fólie (barevný polyethylen, termoplastická pryskyřice a hliníkem potažený polyester), modrý inkoust
Ochranná vrstva: silikonizovaná pegoterátová fólie 100 pm (nutné odstranit před aplikací)
Jak přípravek Buprenorphine Actavis vypadá a co obsahuje toto balení
Buprenorphine Actavis 35 mikrogramů/h transdermální náplast: béžově zbarvená náplast
obdélníkového tvaru se zaoblenými rohy označená Buprenorphin 35 pg/h.
Buprenorphine Actavis 52,5 mikrogramů/h transdermální náplast: béžově zbarvená náplast
obdélníkového tvaru se zaoblenými rohy označená Buprenorphin 52,5 pg/h.
Buprenorphine Actavis 70 mikrogramů/h transdermální náplast: béžově zbarvená náplast
obdélníkového tvaru se zaoblenými rohy a označená Buprenorphin 70 pg/h.
Náplasti jsou baleny jednotlivě v sáčku.
Velikosti balení:
Buprenorphine Actavis 35 mikrogramů/h transdermální náplast - 4, 5, 8, 10, 16, 24 (6 x 4) jednotlivě balených náplastí.
Buprenorphine Actavis 52,5 mikrogramů/h transdermální náplast - 4, 5, 8, 10, 16, 24 (6 x 4) jednotlivě balených náplastí.
Buprenorphine Actavis 70 mikrogramů/h transdermální náplast - 4, 5, 8, 10, 16, 24 (6 x 4) jednotlivě balených náplastí.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci
Actavis Group PTC ehf.
Reykjavikurvegur 76-78 220 Hafnarfjordur Island
Výrobci
Acino AG Am Windfeld 35 D-83714 Miesbach Německo
Actavis Group PTC ehf.
Reykjavikurvegur 76-78 220 Hafnarfjordur Island
G.L. Pharma GmbH Schlossplatz 1 8502 Lannach Rakousko (pro Polsko)
Tento léčivý přípravek je v členských státech EHP registrován pod těmito názvy:
Německo:
Polsko:
Portugalsko:
Česká republika Buprenorphine Actavis 35 pg/h transdermální náplast Buprenorphine Actavis 52,5 pg/h transdermální náplast Buprenorphine Actavis 70 pg/h transdermální náplast Buvera 35 Mikrogramm/Stunde Transdermales Pflaster Buvera 52,5 Mikrogramm/Stunde Transdermales Pflaster Buvera 70 Mikrogramm/Stunde Transdermales Pflaster Melodyn 35 mikrogramów/godzine, system transdermalny Melodyn 52,5 mikrogramów/godzine, system transdermalny Melodyn 70 mikrogramów/godzine, system transdermalny Buprenorfina Actavis 35 microgramas/h sistema transdermico Buprenorfina Actavis 52,5 microgramas/h sistema transdermico Buprenorfina Actavis 70 microgramas/h sistema transdermico
Tato příbalová informace byla naposledy schválena: Prosinec 2014
8