Brilique 60 Mg
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Brilique 60 mg potahované tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta obsahuje ticagrelorum 60 mg. Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Potahovaná tableta (tableta).
Kulaté bikonvexní růžové tablety označené „60“ nad „T“ na jedné straně a bez označení na druhé straně.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek Brilique podávaný s kyselinou acetylsalicylovou (ASA) je indikován k prevenci aterotrombotických příhod u dospělých pacientů s
- akutním koronárním syndromem (ACS) nebo
- infarktem myokardu (IM) v anamnéze a vysokým rizikem vývoje aterotrombotických příhod (viz body 4.2 a 5.1).
4.2 Dávkování a způsob podání
Dávkování
Pacienti užívající přípravek Brilique mají též užívat nízkou udržovací dávku ASA 75-150 mg denně, pokud není specificky kontraindikována.
Akutní koronární syndromy
Léčba přípravkem Brilique se zahajuje podáním jedné iniciální dávky 180 mg (dvě tablety po 90 mg) a dále se pokračuje dávkou 90 mg dvakrát denně.
Léčba přípravkem Brilique 90 mg dvakrát denně se doporučuje u pacientů s ACS po dobu 12 měsíců, pokud není přerušení léčby klinicky indikováno (viz bod 5.1).
Infarkt myokardu v anamnéze
U pacientů s anamnézou IM a vysokým rizikem aterotrombotických příhod se doporučuje podávat přípravek Brilique 60 mg dvakrát denně po dobu nejméně jednoho roku (viz bod 5.1). Léčbu lze zahájit bez přerušení jako pokračování po úvodní jednoroční léčbě přípravkem Brilique 90 mg nebo jiné léčby inhibitory receptoru pro adenosin difosfát (ADP) u pacientů s ACS a vysokým rizikem aterotrombotických příhod. Léčbu lze též zahájit až dva roky od ataky IM nebo v průběhu jednoho roku od ukončení předchozí léčby inhibitorem ADP receptoru. Existují pouze omezené údaje o účinnosti a bezpečnosti přípravku Brilique při léčbě delší než 3 roky.
Pokud je třeba změna medikace, první dávka přípravku Brilique se má podat 24 hodin po poslední dávce jiného antiagregačního léčivého přípravku.
Vynechaná dávka
Je třeba předcházet vynechání dávky. Pokud pacient zapomene na dávku přípravku Brilique, užije tabletu (další dávku) v pravidelném čase.
Zvláštní populace Starší pacienti
U starších pacientů není nutná úprava dávky (viz bod 5.2).
Porucha funkce ledvin
U pacientů s poruchou ledvin není nutná úprava dávky (viz bod 5.2). Nejsou dostupné informace týkající se léčby dialyzovaných pacientů, a proto se podávání tikagreloru u těchto pacientů nedoporučuje.
Porucha funkce jater
Tikagrelor nebyl hodnocen u pacientů se závažnou poruchou funkce jater a použití u těchto pacientů je tedy kontraindikováno (viz bod 4.3). U pacientů se středně závažnou poruchou funkce jater jsou dostupné pouze omezené informace. Nedoporučuje se upravovat dávku, ale tikagrelor se má užívat s opatrností (viz body 4.4 a 5.2). U pacientů s mírnou poruchou funkce jater není nutná úprava dávky (viz bod 5.2).
Pediatrická populace
Bezpečnost a účinnost tikagreloru u dětí ve věku do 18 let nebyla stanovena. Nejsou dostupné žádné údaje.
Způsob podání Perorální podání.
Přípravek Brilique lze podat s jídlem i bez jídla.
U pacientů, kteří nemohou tabletu(y) spolknout celou(é), lze tablety rozdrtit na jemný prášek a smísit s polovinou sklenice vody a ihned vypít. Sklenici je třeba vypláchnout polovinou sklenice vody a obsah vypít. Směs lze podat též přes nazogastrickou sondu (CH8 nebo větší). Po podání směsi je důležité nazogastrickou sondu propláchnout vodou.
4.3 Kontraindikace
• Hypersenzitivita na léčivou látku nebo na kteroukoliv pomocnou látku tohoto přípravku uvedenou v bodě 6.1 (viz bod 4.8).
• Patologické aktivní krvácení.
• Anamnéza intrakraniálního krvácení (viz bod 4.8).
• Závažná porucha funkce jater (viz body 4.2, 4.4 a 5.2).
• Souběžné podávání tikagreloru se silnými inhibitory CYP3A4 (např. ketokonazolem, klarithromycinem, nefazodonem, ritonavirem a atazanavirem) je kontraindikováno, neboť souběžné podávání může vést k podstatnému zvýšení expozice tikagreloru (viz bod 4.5).
4.4 Zvláštní upozornění a opatření pro použití
Riziko krvácení
Použití tikagreloru u pacientů se známým zvýšeným rizikem krvácení se má zvážit s ohledem na prospěch z pohledu prevence aterotrombotických příhod (viz body 4.8 a 5.1). Pokud je klinicky indikováno, tikagrelor se má podávat opatrně u následujích skupin pacientů:
• Pacienti se sklonem ke krvácení (např. v důsledku nedávného traumatu, nedávného chirurgického výkonu, poruchy koagulace, akutního nebo recentního gastrointestinálního krvácení). Použití tikagreloru je kontraindikováno u pacientů s aktivním patologickým krvácením u pacientů s anamnézou intrakraniálního krvácení a pacientů se závažnou poruchou funkce jater (viz bod 4.3).
• Pacienti, kteří souběžně užívají přípravky, které mohou zvyšovat riziko krvácení (např. nesteroidní protizánětlivé léky (NSAID), perorální antikoagulancia a/nebo fibrinolytika v průběhu 24 hodin od podání tikagreloru).
Nejsou dostupné informace u pacientů na tikagreloru týkající se hemostatického prospěchu po podání transfuze krevních destiček; cirkulující tikagrelor může inhibovat infundované krevní destičky. Souběžné podání tikagreloru a desmopresinu nesnižuje dobu krvácení, a tak je nepravděpodobné, že by byl desmopresin účinný v klinické léčbě krvácivých příhod (viz bod 4.5).
Antifibrinolytická léčba (kyselina aminokapronová nebo kyselina tranexanová) a/nebo léčba rekombinantním faktorem VIIa mohou zvyšovat hemostázu. V léčbě tikagrelorem lze pokračovat, pokud byl zjištěn důvod krvácení a krvácení je pod kontrolou.
Chirurgická léčba
Pacienti mají být poučeni, že mají informovat lékaře a zubní lékaře, že užívají tikagrelor, před jakoukoliv plánovanou operací a předtím, než začnou užívat jakýkoliv nový léčivý přípravek.
U pacientů, kteří podstoupili koronární arteriální bypass (CABG) ve studii PLATO, měl tikagrelor vyšší počet krvácení než klopidogrel, pokud byla léčba tikagrelorem přerušena v průběhu 1 dne před chirurgickým zákrokem, ale podobnou frekvenci závažných krvácení jako klopidogrel, když byla léčba přerušena 2 nebo více dnů před chirurgickým zákrokem (viz bod 4.8). Pokud je u pacienta plánována operace a není žádoucí protidestičkový účinek, je třeba tikagrelor vysadit 7 dnů před operací (viz bod 5.1).
Pacienti s anamnézou ischemické cévní mozkové příhody
Pacienti s ACS a anamnézou ischemické cévní mozkové příhody mohou být léčeni přípravkem Brilique po dobu až 12 měsíců (studie PLATO).
Pacienti s anamnézou IM a předchozí anamnézou ischemické cévní mozkové příhody nebyli zařazeni do studie PEGASUS. Protože nejsou dostupné údaje, nedoporučuje se pokračovat v léčbě po jednom roce.
Porucha funkce jater
Tikagrelor je kontraindikován u pacientů se závažnou poruchou funkce jater (viz body 4.2 a 4.3). Zkušenosti s tikagrelorem u pacientů se středně závažnou poruchou funkce jater jsou pouze omezené, a proto se u těchto pacientů doporučuje opatrnost (viz body 4.2 a 5.2).
Pacienti s rizikem bradykardie
Na základě pozorování většinou asymptomatických komorových pauz v časných fázích klinického vývoje, byli pacienti se zvýšeným rizikem bradykardie (např. pacienti bez kardiostimulátoru se sick sinus syndromem, AV blokádou 2. a 3. stupně nebo synkopou vyvolanou bradykardií) vyloučeni ze studií hodnotících bezpečnost a účinnost tikagreloru. Vzhledem k tomu, že jsou klinické zkušenosti s tikagrelorem u těchto pacientů omezené, doporučuje se opatrnost (viz bod 5.1).
Dále je třeba opatrnosti, pokud je tikagrelor podáván souběžně s léčivými přípravky, které vyvolávají bradykardii. Při souběžném podávání jednoho nebo více léčivých přípravků ve studii PLATO, které vyvolávají bradykardii (tj. 96 % betablokátory, 33 % blokátory kalciového kanálu diltiazem a verapamil a 4 % digoxin) (viz bod 4.5) nebyly prokázány klinicky významné nežádoucí účinky.
V průběhu podstudie Holter studie PLATO mělo v akutní fázi ACS více pacientů léčených tikagrelorem než pacientů léčených klopidogrelem komorové pauzy > 3 sekundy. Zvýšení komorových pauz v průběhu akutní fáze ACS detekovaných Holterem bylo vyšší u pacientů s chronickým srdečním selháním (CHF) ve srovnání s celkovou studijní populací, ale nikoliv po jednom měsíci, nebo ve srovnání s klopidogrelem. S touto dysbalancí nebyly v této populaci pacientů spojeny žádné nežádoucí klinické konsekvence (včetně synkopy nebo voperování kardiostimulátoru) (viz bod 5.1).
Dusnost
Dušnost byla hlášena u pacientů léčených tikagrelorem. Dušnost je obvykle mírné až střední intenzity a často ustupuje bez nutnosti přerušit léčbu. Pacienti s astmatem/chronickou obstrukční plicní nemocí (CHOPN) mohou mít zvýšené absolutní riziko výskytu dušnosti při užívání tikagreloru (viz bod 4.8). Tikagrelor se má používat opatrně u pacientů s anamnézou astmatu a/nebo CHOPN. Mechanismus nebyl zjištěn. Pokud si pacient stěžuje na nově vzniklou, protrahovanou nebo zhoršující se dušnost, je třeba ji zevrubně zhodnotit a pokud není tolerována, je třeba léčbu tikagrelorem přerušit. Další údaje viz bod 4.8.
Zvýšení hladin kreatininu
V průběhu léčby tikagrelorem se mohou zvyšovat hladiny kreatininu (viz bod 4.8). Mechanismus nebyl vysvětlen. Funkce ledvin se má kontrolovat podle obvyklé lékařské praxe. U pacientů s ACS se doporučuje zkontrolovat funkci ledvin též jeden měsíc po zahájení léčby tikagrelorem a se zvláštní pozorností věnovanou pacientům >75 let, pacientům se středně závažnou/závažnou poruchou funkce ledvin a pacientům léčeným blokátory angiotezinových receptorů (ARB).
Zvýšení hladin kyseliny močové
V průběhu léčby tikagrelorem se může objevit hyperurikemie (viz bod 4.8). Je třeba opatrnosti, pokud je tikagrelor podáván pacientům s anamnézou hyperurikemie nebo dnavé artritidy. Jako preventivní opatření se nedoporučuje podávat tikagrelor pacientům s nefropatií vyvolanou kyselinou močovou.
Další
Na základě vztahu pozorovaného ve studii PLATO mezi udržovací dávkou ASA a relativní účinností tikagreloru ve srovnání s klopidogrelem se nedoporučuje souběžně podávat tikagrelor a vysoké udržovací dávky ASA (> 300 mg) (viz bod 5.1).
Předčasné přerušení léčby
Předčasné přerušení jakékoli protidestičkové léčby, včetně přípravku Brilique, může vést ke zvýšení rizika kardiovaskulární (CV) smrti nebo IM v důsledku základního onemocnění. Proto se má předčasné přerušení léčby vyloučit.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Tikagrelor je převážně substrátem pro CYP3A4 a mírným inhibitorem CYP3A4. Tikagrelor je též substrátem pro glykoprotein-P (P-gp) a slabým inhibitorem P-gp a může zvyšovat expozici k substrátům pro P-gp.
Vliv jiných léčivých přípravků na tikagrelor
Léčivé přípravky metabolizované CYP3A4 Inhibitory CYP3A4
• Silné inhibitory CYP3A4 - souběžné podávání tikagreloru a ketokonazolu zvyšovalo Cmax a AUC až 2,4krát, resp. 7,3krát. Hodnoty Cmax a AUC aktivního metabolitu byly sníženy o 89 %, resp. 56 %. Jiné účinné inhibitory CYP3A4 (klarithromycin, nefazodon, ritonavir a atazanavir) budou mít pravděpodobně stejný vliv, a proto je souběžné podávání silných inhibitorů CYP3A4 s tikagrelorem je kontraindikováno (viz bod 4.3).
• Středně silné inhibitory CYP3A4 - souběžné podávání diltiazemu a tikagreloru zvyšovalo hodnoty Cmax o 69 % a AUC až 2,7krát u tikagreloru a snižovalo hodnotu Cmax o 38 % a neměnilo AUC aktivního metabolitu. Nebyl prokázán vliv tikagreloru na plazmatické koncentrace diltiazemu. Lze očekávat, že jiné středně účinné inhibitory CYP3A4 (např. amprenavir, aprepitant, erythromycin a flukonazol) mohou mít podobný efekt a mohou být podávány souběžně s tikagrelorem.
Induktory CYP3A
Souběžné podávání rifampicinu a tikagreloru snižovalo hodnoty Cmax a AUC tikagreloru o 73 %, resp. 86 %. Hodnota Cmax aktivního metabolitu zůstala nezměněna a hodnota AUC se snížila o 46 %.
U jiných induktorů CYP3A4 (např. fenytoin, karbamazepin a fenobarbital) lze očekávat snížení expozice tikagreloru. Souběžné podávání tikagreloru a účinných induktorů CYP3A4 může snižovat expozici a účinnost tikagreloru, a proto se jejich souběžné podávání s tikagrelorem nedoporučuje.
Cyklosporin (inhibitor P-gp a CYP3A4)
Souběžné podávání cyklosporinu (600 mg) a tikagreloru zvyšovalo Cmax a AUC tikagreloru 2,3násobně, resp. 2,8násobně. V přítomnosti cyklosporinu byla AUC aktivního metabolitu zvýšena o 32 % a Cmax snížena o 15 %.
Nejsou dostupné údaje o souběžném podávání tikagreloru s dalšími aktivními látkami, které jsou také silnými inhibitory P-gp a středně silnými inhibitory CYP3A4 (např. verapamil, chinidin), které také mohou zvyšovat expozici tikagreloru. Pokud nelze souběžné podávání vyloučit, je třeba opatrnosti.
Další
Klinicko farmakologické interakční studie prokázaly, že souběžné podávání tikagreloru s heparinem, enoxaparinem a kyselinou acetylsalicylovou nebo desmopresinem nemá vliv na farmakokinetiku tikagreloru nebo jeho aktivního metabolitu nebo na ADP indukovanou agregaci destiček ve srovnání se samotným tikagrelorem. Pokud je to klinicky indikováno, je třeba podávat léčivé přípravky, která ovlivňují hemostázu, v kombinaci s tikagrelorem opatrně.
Při denní konzumaci velkého množství grapefruitové šťávy (3 x 200 ml) bylo pozorováno 2násobné zvýšení expozice tikagreloru. Předpokládá se, že u většiny pacientů není takto velké zvýšení expozice klinicky relevantní.
Vliv tikagreloru na jiné léčivé přípravky Léčivé přípravky metabolizované CYP3A4
• Simvastatin - souběžné podávání tikagreloru a simvastatinu zvyšovalo Cmax a AUC simvastatinu o 81 %, resp. 56 % a zvyšovalo Cmax a AUC kyseliny simvastatinu o 64 %, resp. 52 %
s individuálním zvýšením až na 2-3násobek. Souběžné podávání tikagreloru a simvastatinu v dávkách vyšších než 40 mg denně může vyvolat nežádoucí účinky simvastatinu a má být zváženo z pohledu možného prospěchu. Nebyl prokázán vliv simvastatinu na plazmatické koncentrace tikagreloru. Tikagrelor může mít podobný vliv na lovastatin. Nedoporučuje se souběžné podávání tikagreloru a simvastatinu nebo lovastatinu v dávkách vyšších než 40 mg.
• Atorvastatin - souběžné podávání atorvastatinu a tikagreloru zvýšilo hodnoty Cmax a AUC kyseliny atorvastatinu o 23 %, resp. 36 %. Podobný vzestup Cmax a AUC byl pozorován u všech kyselých metabolitů atorvastatinu. Tyto změny nejsou považovány za klinicky významné.
• Nelze vyloučit podobný vliv na jiné statiny metabolizované CYP3A4. Pacienti zařazení do studie PLATO dostávali tikagrelor a různé jiné statiny bez problémů spojených s bezpečností, přičemž tyto přípravky užívalo celkem 93 % pacientů zařazených do studie PLATO.
Tikagrelor je mírný inhibitor CYP3A4. Souběžné podávání tikagreloru a substrátů pro CYP3A4 s úzkým terapeutickým indexem (např. cisaprid nebo námelové alkaloidy) se nedoporučuje, neboť tikagrelor může zvyšovat expozici těmto léčivým přípravkům.
Substráty P-gp (včetně digoxinu a cyklosporinu)
Souběžné podávání tikagreloru zvyšuje Cmax a AUC digoxinu o 75 %, resp. o 28 %. Průměrné hodnoty koncentrací digoxinu byly při současném podávání tikagreloru zvýšeny o přibližně 30 % s jednotlivými až 2násobnými maximy. Hodnoty Cmax a AUC tikagreloru a aktivního metabolitu se v přítomnosti digoxinu nemění. Z tohoto důvodu se doporučuje pečlivé klinické a/nebo laboratorní monitorování, pokud se souběžně s tikagrelorem podávají léčiva s úzkých terapeutickým indexem a metabolismem závislým na P-gp, jako je např. digoxin.
Nebyl zjištěn vliv tikagreloru na sérové hladiny cyklosporinu. Vliv tikagreloru na jiné substráty P-gp nebyl studován.
Léčivé přípravky metabolizované CYP2C9
Souběžné podávání tikagreloru a tolbutamidu nemělo za následek změnu plazmatických koncentrací obou léčivých přípravků, což předpokládá, že tikagrelor není inhibitorem CYP2C9 a je nepravděpodobné, že by tikagrelor ovlivňoval metabolismus léčivých přípravků jako je warfarin a tolbutamid zprostředkovaný CYP2C9.
Perorální antikoncepce
Souběžné podávání tikagreloru a levonorgestrelu a ethinylestradiolu zvyšovalo expozici ethinyl estradiolu o asi 20 %, ale neměnilo farmakokinetiku levonorgestrelu. Nepředpokládá se klinicky významný vliv na účinnost perorální antikoncepce, pokud je levonorgestrel a ethinylestradiol podáván souběžně s tikagrelorem.
Léčivé přípravky vyvolávající bradykardii
Při podávání tikagreloru souběžně s léčivými přípravky, které vyvolávají bradykardii, se doporučuje opatrnost, vzhledem k pozorovaným a obvykle asymptomatickým komorovým pauzám a bradykardii (viz bod 4.4). Ve studii PLATO však při současném podávání jednoho nebo více léčivých přípravků vyvolávajících bradykardii (tj. 96 % betablokátory, 33 % blokátory kalciového kanálu diltiazem a verapamil a 4 % digoxin) nebyly pozorovány klinicky významné nežádoucí účinky.
Jiná souběžná léčba
V klinických studiích byl tikagrelor podáván souběžně s ASA, inhibitory protonové pumpy, statiny, betablokátory, inhibitory angiotenzin konvertujícího enzymu (ACE) a blokátory receptoru pro angiotenzin podle potřeby k dlouhodobé léčbě doprovodných onemocnění a krátkodobě také heparin, nízkomolekulární heparin a intravenózní inhibitory GplIb/IIIa (viz bod 5.1). Neprokázalo se, že by docházelo ke klinicky významným nežádoucím interakcím s těmito léčivými přípravky.
Souběžné podávání tikagreloru a heparinu, enoxaparinu nebo desmopresinu nemá vliv na parciální aktivovaný tromboplastinový čas (aPTT), aktivovaný koagulační čas (ACT) nebo výsledky stanovení faktoru Xa. Vzhledem k potenciálu farmakodynamické interakce je však třeba opatrnosti při souběžném podávání tikagreloru a léčivých přípravků ovlivňujících hemostázu.
Vzhledem k hlášení kožního krvácení při podávání SSRIs (tj. paroxetin, sertralin a citalopram) se doporučuje opatrnost při souběžném podávání SSRIs a tikagreloru, neboť může dojít ke zvýšení rizika krvácení.
4.6 Fertilita, těhotenství a kojení
Ženy ve fertilním věku
Ženy v plodném věku mají v průběhu léčby tikagrelorem používat vhodnou antikoncepci, aby se předešlo otěhotnění.
Údaje o podávání tikagreloru těhotným ženám jsou omezené nebo nejsou k dispozici. Studie na zvířatech prokázaly reprodukční toxicitu (viz bod 5.3). Podávání tikagreloru se v průběhu těhotenství nedoporučuje.
Kojení
Dostupné farmakodynamické/toxikologické údaje u zvířat prokázaly vylučování tikagreloru a jeho metabolitů do mléka (viz bod 5.3). Riziko pro kojené novorozence/děti nelze vyloučit. Na základě posouzení prospěšnosti kojení pro dítě a prospěšnosti léčby pro matku je nutno rozhodnout, zda přerušit kojení nebo přerušit podávání tikagreloru.
Fertilita
Tikagrelor nemá vliv na samčí nebo samičí fertilitu u zvířat (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Tikagrelor nemá žádný vliv nebo má pouze zanedbatelný vliv na schopnost řídit a ovládat stroje.
V průběhu léčby tikagrelorem byly hlášeny případy závratě a zmatenosti. Pacienti, kteří zaznamenají tyto příznaky, by měli být opatrní, pokud řídí nebo obsluhují stroje.
4.8 Nežádoucí účinky
Shrnutí bezpečnostního profilu
Bezpečnostní profil tikagreloru byl hodnocen ve dvou velkých „outcome“ klinických studiích fáze 3 (PLATO a PEGASUS), které zařadily více než 39000 pacientů (viz bod 5.1).
Ve studii PLATO byl u pacientů na tikagreloru zjištěn vyšší výskyt přerušení léčby v důsledku nežádoucích účinků než u klopidogrelu (7,4 % vs 5.4 %). Ve studii PEGASUS byl u pacientů na tikagreloru zjištěn vyšší výskyt přerušení léčby v důsledku nežádoucích účinků ve srovnání se samotnou ASA (16,1 % pro tikagrelor 60 mg a ASA vs 8,5 % pro samotnou ASA). Nejčastěji hlášeným nežádoucím účinkem u pacientů léčených tikagrelorem bylo krvácení a dušnost (viz bod 4.4).
Tabulkový přehled nežádoucích účinků
Následující nežádoucí účinky byly identifikovány ve studiích s tikagrelorem nebo byly hlášeny z poregistračního sledování (Tabulka 1).
Nežádoucí účinky jsou uvedeny podle terminologie MedDRA tříd orgánových systémů (SOC).
V každé SOC jsou nežádoucí účinky uvedeny podle kategorií četností. Četnosti jsou definovány podle následující konvence: velmi časté (> 1/10). časté (> 1/100 až < 1/10), méně časté (> 1/1000 až
< 1/100), vzácné (> 1/10 000 až < 1/1000), velmi vzácné (< 1/10 000), není známo (z dostupných údajů nelze určit).
Tabulka 1 Nežádoucí účinky podle četnosti a třídy orgánových systémů (SOC)
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
|
Novotvary benigní, maligní a blíže neurčené (zahrnující cysty a polypy) |
Krvácení z nádoru3 | ||
|
Poruchy krve a lymfatického systému |
Krvácení v důsledku poruchy krveb | ||
|
Poruchy imunitního systému |
Hypersensitivita zahrnující angioedémc | ||
|
Poruchy metabolismu a výživy |
Hyperurikemied |
Dna/dnavá artritida | |
|
Psychiatrické poruchy | |||
|
Poruchy nervového systému |
Závrať, synkopa, bolest hlavy |
Intrakraniální krvácení | |
|
Poruchy oka |
Oční krváceníe | ||
|
Poruchy oka a labyryntu |
Krvácení z ucha |
např. krvácení z karcinomu močového měchýře, žaludečního karcinomu, karcinomu tlustého střeva např. zvýšená tendence k tvorbě modřin, spontánní hematomy, hemoragická diatéza identifikované z poregistračních zkušeností
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
|
Cévní poruchy | |||
|
Respirační, hrudní a mediastinální poruchy |
Krvácení z respiračního f systému | ||
|
Gastrointestinální poruchy |
Gastrointestinální krváceníg, průjem, nauzea, dyspepsie, zácpa |
Retroperitoneální krvácení | |
|
Poruchy kůže a podkožní tkáně |
Subkutánní nebo kožní krváceníh, vyrážka, svědění | ||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Svalové krvácení1 | ||
|
Poruchy ledvin a močových cest |
Krvácení z močových cestj | ||
|
Poruchy reprodukčního systému a prsu |
Krvácení z reprodukčních k orgánů | ||
|
Vyšetření |
Zvýšený kreatinin v krvid | ||
|
Poranění, otravy a procedurální komplikace |
Krvácení po chirurgickém zákroku, traumatické krvácení' |
a
b
c
d
e
f
g
h
i
J
k
l
četnosti odvozené z laboratorních měření (zvýšení kyseliny močové na > horní limit normálních hodnot z výchozí hodnoty pod nebo v rozmezí normálních referenčních hodnot. Zvýšení kreatininu o > 50 % oproti výchozí hodnotě) a nikoliv z hrubé frekvence hlášení nežádoucích příhod. např. krvácení ze spojivky, sítnice a nitrooční krvácení např. epistaxe, hemoptýza
např. krvácení z dásní, konečníku, žaludečních vředů např. ekchymóza, kožní krvácení, petechie např. hemartróza, svalové krvácení např. hematurie, hemoragická cystitida
např. vaginální krvácení, hematospermie, postmenopauzální krvácení např. kontuze, traumatický hematom, traumatické krvácení
Popis vybraných nežádoucích účinků
Krvácení
Zjištění o krvácení ve studii PLATO
Celkový přehled krvácivých příhod ve studii PLATO je uveden v Tabulce 2.
Tabulka 2 Analýza všech krvácivých příhod, odhady ve škále Kaplan-Meier po 12 měsících _(PLATO)_
|
Tikagrelor 90 mg dvakrát denně N=9235 |
Klopidogrel N=9186 |
p-hodnota* | |
|
PLATO celkem velké |
11,6 |
11,2 |
0,4336 |
|
PLATO velké fatální/život ohrožující |
5,8 |
5,8 |
0,6988 |
|
Non-CABG PLATO velké |
4,5 |
3,8 |
0,0264 |
|
Neprocedurální PLATO velké |
3,1 |
2,3 |
0,0058 |
|
PLATO celkem velké + malé |
16,1 |
14,6 |
0,0084 |
|
Neprocedurální PLATO velké + malé |
5,9 |
4,3 |
< 0,0001 |
|
Definované podle TIMI-velké |
7,9 |
7,7 |
0,5669 |
|
Definované podle TIMI- -velké + malé |
11,4 |
10,9 |
0,3272 |
Definice kategorií krvácení:
Velké fatální/život ohrožující krvácení: klinicky zjevné s poklesem hemoglobinu o >50 g/l nebo podání > 4 transfuzí červených krvinek; nebo fatální; nebo intrakraniální; nebo intraperikardiální se srdeční tamponádou; nebo s hypovolemickým šokem nebo těžkou hypotenzí vyžadující podání vosopresorů nebo chirurgický zákrok.
Velké ostatní: klinicky zjevné s poklesem hemoglobinu o 30-50 g/l nebo podání 2-3 transfuzí červených krvinek; nebo významně invalidizující.
Malé krvácení: vyžadující lékařskou intervenci k zastavení nebo léčbě krvácení.
TIMI velké krvácení: klinicky zjevné s poklesem hemoglobinu o > 50 g/l nebo intrakraniální krvácení.
TIMI malé krvácení: klinicky zjevné s poklesem hemoglobinu o 30-50 g/l.
* p-hodnota vypočtena z Cox proporcionálního modelu rizik s léčebnými skupinami jako jedinou vysvětlující proměnnou
Tikagrelor a klopidogrel se neliší ve frekvenci PLATO velké fatální/život ohrožující krvácení, PLATO celkové velké krvácení, TIMI velké krvácení nebo TIMI malé krvácení (Tabulka 2). S přípravkem Brilique se objevilo více PLATO kombinovaných velkých + malých krvácení ve srovnání s klopidogrelem. Několik pacientů ve studii PLATO mělo fatální krvácení: 20 (0,2 %) s tikagrelorem a 23 (0,3 %) s klopidogrelem (viz bod 4.4).
Věk, pohlaví, tělesná hmotnost, rasa, geografická příslušnost, jiné ovlivňující podmínky, souběžná léčba a lékařská anamnéza, včetně předchozí cévní mozkové příhody nebo tranzitorní ischemické ataky, nemají předpovědní hodnotu ve vztahu k celkovému nebo neprocedurálnímu velkému PLATO krvácení. Nebyla identifikována žádná specifická skupina s rizikem jakéhokoliv krvácení.
Krvácení vztahující se k CABG: Ve studii PLATO mělo 42 % z 1584 pacientů (12 % kohorty), kteří podstoupili chirurgický zákrok voperování koronárního arteriálního bypassu (CABG) velké fatální/život ohrožující krvácení, což nepředstavuje rozdíl mezi léčebnými skupinami. Fatální CABG krvácení se objevilo u 6 pacientů v každé léčebné skupině (viz bod 4.4).
Non-CABG krvácení a krvácení, které není spojeno s výkonem: tikagrelor a klopidogrel se neliší v non-CABG krvácení definovaném podle PLATO jako velké fatální/život ohrožující krvácení, ale krvácení definovaná podle PLATO jako celkem velká krvácení, TIMI velká, TIMI velká + malá jsou častější u tikagreloru. Podobně, pokud se neuvažují krvácení, která souvisejí s výkonem, je krvácení častější u tikagreloru ve srovnání s klopidogrelem (Tabulka 2). Přerušení léčby v důsledku neprocedurálního krvácení bylo častější u tikagreloru (2,9 %) než u klopidogrelu (1,2 %; p < 0,001).
Intrakraniální krvácení: Více intrakraniálních krvácení bylo u tikagreloru (n=27 krvácení u 26 pacientů; 0,3 %) než u klopidogrelu (n=14 krvácení; 0,2 %), z nichž bylo 11 smrtelných krvácení u tikagreloru a 1 u klopidogrelu. Nebyl zjištěn rozdíl v celkovém počtu smrtelných krvácení.
Krvácení ve studii PEGASUS
Celkové výsledky krvácivých příhod ve studii PEGASUS jsou uvedeny v Tabulce 3.
Tabulka 3 Analýza všech krvácivých příhod, odhady ve škále Kaplan-Meier po 36 měsících (PEGASUS)
|
Tikagrelor 60 mg dvakrát denně + ASA N = 6958 |
Samotná ASA N = 6996 | |||
|
Cílové parametry bezpečnosti |
KM% |
Poměr rizik (95% CI) |
KM% |
^-hodnota |
|
TIMI-definované kategorie krvácení | ||||
|
TIMI velké |
2,3 |
2,32 (1,68; 3,21) |
1,1 |
<0,0001 |
|
fatální |
0,3 |
1,00 (0,44; 2,27) |
0,3 |
1,0000 |
|
ICH |
0,6 |
1,33 (0,77; 2,31) |
0,5 |
0,3130 |
|
jiné TIMI velké |
1,6 |
3,61 (2,31; 5,65) |
0,5 |
<0,0001 |
|
TIMI velké nebo malé |
3,4 |
2,54 (1,93; 3,35) |
1,4 |
<0,0001 |
|
TIMI velké nebo malé nebo vyžadující lékařskou pozornost |
16,6 |
2,64 (2,35; 2,97) |
7,0 |
<0,0001 |
|
PLATO-definované kategorie krvácení | ||||
|
PLATO velké |
3,5 |
2,57 (1,95; 3,37) |
1,4 |
<0,0001 |
|
Fatální/život ohrožující |
2,4 |
2,38 (1,73; 3,26) |
1,1 |
<0,0001 |
|
Jiné PLATO velké |
1,1 |
3,37 (1,95; 5,83) |
0,3 |
<0,0001 |
|
PLATO velké nebo malé |
15,2 |
2,71 (2,40; 3,08) |
6,2 |
<0,0001 |
Definice kategorií krvácení:
TIMI velké: Fatální krvácení, nebo jakékoli intrakraniální krvácení, nebo klinicky zjevné krvácení doprovázené poklesem hemoglobinu (Hb) o > 50 g/l, nebo, pokud vyšetření haemoglobinu není dostupné, pokles hematokritu (Hct) o 15 %.
Fatální: Krvácivá příhoda, která přímo vede ke smrti v průběhu 7 dnů.
ICH: Intrakraniální krvácení.
Jiné TIMI velké: Nefatální non-ICH TIMI velké krvácení.
TIMI malé: Klinicky zjevné s poklesem hemoglobinu o 30-50 g/l.
TIMI vyžadující lékařskou pozornost: Vyžadující intervenci, nebo vedoucí k hospitalizaci, nebo urychlené vyhodnocení.
PLATO velké fatální/život ohrožující: Fatální krvácení, nebo intrakraniální krvácení, nebo intraperikardiální nebo s tamponádou srdce, nebo hypovolemickým šokem nebo závažnou hypotenzí vyžadující podání vasopresorů/inotropních látek nebo operaci nebo klinicky zjevné krvácení s poklesem hemoglobinu o 30-50 g/l nebo podání >4 transfuzí červených krvinek.
PLATO velké jiné: Významně omezující, nebo klinicky zjevné krvácení s poklesem hemoglobinu o 30-50 g/l, nebo podání 2-3 transfuzí červených krvinek.
PLATO malé: Vyžadující lékařskou intervenci k zastavení nebo léčbě krvácení.
Ve studii PEGASUS bylo TIMI velké krvácení častější u tikagreloru 60 mg dvakrát denně než u samotné ASA. Nebylo pozorováno vyšší riziko fatálních krvácení a byl pozorován pouze mírný vzestup intrakraniálních krvácení ve srovnání se samotnou ASA. Ve studii bylo pouze několik fatálních krvácivých příhod, 11 (0,3 %) u tikagreloru 60 mg a 12 (0,3 %) u samotné ASA. Pozorované zvýšené riziko TIMI velkých krvácení u tikagreloru 60 mg bylo způsobeno primárně vyšší četností jiných TIMI velkých krvácení, zvláště příhodami v gastrointestinálním traktu.
Zvýšený charakter krvácení podobný TIMI velké byl pozorován v kategoriích krvácení TIMI velké nebo malé a PLATO velké a PLATO velké nebo malé (viz Tabulka 3). Přerušení léčby jako důsledek krvácení bylo častější utikagreloru 60 mg ve srovnání se samotnou ASA (6,2 %, resp. 1,5 %). Vetšina těchto krvácení nižší závažnosti (klasifikované jako TIMI vyžadující lékařskou pozornost), např. epistaxe, tvorba modřin a hematomů.
Profil krvácení u tikagreloru 60 mg byl konzistentní v předem definovaných podskupinách (např. podle věku, pohlaví, tělesné hmotnosti, rasy, geografické příslušnosti, souběžných podmínek, souběžné léčby a lékařské anamnézy) pro TIMI velké, TIMI velké nebo malé a PLATO velké krvácivé příhody.
Intrakraniální krvácení: Intrakraniální krvácení (ICH) bylo hlášeno s podobnou četností u tikagreloru 60 mg a samotné ASA (n = 13, 0,2 % v obou léčebných skupinách). Traumatické a chirurgické ICH vykázalo mírné zvýšení u léčby tikagrelorem 60 mg (n = 15, 0,2 %) ve srovnání se samotnou ASA (n = 10, 0,1 %). U tikagreloru 60 mg bylo 6 fatálních ICH a u ASA samotné 5 fatálních ICH. Výskyt intrakraniálního krvácení byl v obou skupinách nízký s ohledem na významné komorbidity a CV rizikové faktory ve studijní populaci.
Dusnost
U pacientů léčených přípravkem Brilique byla hlášena dušnost a pocit tíže na hrudi. Nežádoucí příhody (AEs) zahrnuté pod pojem dušnost (dušnost, klidová dušnost, dušnost při fyzické námaze, paroxysmální noční dušnost a noční dušnost) byly ve studii PLATO hlášeny u 13,8 % pacientů léčených tikagrelorem a u 7,8 % pacientů léčených klopidogrelem. U 2,2 % pacientů užívajících tikagrelor a u 0,6 % pacientů užívajících klopidogrel ve studii PLATO byla dušnost podle zkoušejícího lékaře v příčinné souvislosti s prováděnou léčbou a několik případů bylo závažných (0,14 % tikagrelor; 0,02 % klopidogrel) (viz bod 4.4). Většina hlášených případů dušnosti byla mírné až střední intenzity a většina byla hlášena jako jednotlivá epizoda brzy po zahájení léčby.
Ve srovnání s klopidogrelem mohou mít pacienti s astmatem/CHOPN léčení tikagrelorem zvýšené riziko vývoje nezávažné dušnosti (3,29 % tikagrelor vs. 0,53 % klopidogrel) a závažné dušnosti (0,38 % tikagrelor vs. 0,00 % klopidogrel). V absolutních číslech je toto riziko vyšší než pro celkovou populaci studie PLATO. U pacientů s anamnézou astmatu a/nebo CHOPN je třeba podávat tikagrelor opatrně (viz bod 4.4).
Asi 30 % epizod odeznělo v průběhu 7 dnů. Do studie PLATO byli zařazováni pacienti s kongestivním srdečním selháním, CHOPN nebo astmatem; tito pacienti a starší pacienti hlásili častěji dušnost. Celkem 0,9 % pacientů na Brilique přerušilo léčbu studovanou léčivou látkou v důsledku dušnosti ve srovnání s 0,1 % pacientů užívajících klopidogrel. Vyšší výskyt dušnosti ve skupině s přípravkem Brilique není spojen s novým výskytem nebo zhoršením onemocnění plic nebo srdce (viz bod 4.4). Přípravek Brilique neovlivňuje funkční plicní testy.
Ve studii PEGASUS byla dušnost hlášena u 14,2 % pacientů, kterým byl podáván tikagrelor 60 mg dvakrát denně a u 5,5 % pacientů na samotné ASA. Podobně jako v PLATO byla většina hlášených případů dušnosti byla mírné až střední intenzity (viz bod 4.4) Pacienti, kteří hlásili dušnost byli poněkud starší a častěji měli dušnost, CHOPN nebo astma již při vstupu do studie.
Vyšetření
Zvýšení koncentrací kyseliny močové: Koncentrace kyseliny močové v séru se u 22 % pacientů užívajících tikagrelor ve studii PLATO zvýšila na více než horní hranici normy ve srovnání s 13 % pacientů na klopidogrelu. Odpovídající počty ve studii PEGASUS byly 9,1 %, resp. 8,8 %, resp. 5,5 % pro tikagrelor 90 mg, resp. 60 mg, resp. placebo. Střední sérová koncentrace kyseliny močové se zvýšila o přibližně 15 % u tikagreloru ve srovnání s přibližně 7,5 % u klopidogrelu. Po ukončení léčby klesla tato hodnota u tikagreloru na 7 %, ale u klopidogrelu nebyl pozorován pokles. Ve studii PEGASUS byl u tikagreloru zjištěn reverzibilní vzestup střední sérové koncentrace kyseliny močové o 6,3 %, resp. 5,6 % ve srovnání s 1,5 % v placebové skupině. Ve studii PLATO byly hlášeny nežádoucí příhody dnavé artritidy u 0,2 % případů u tikagreloru a 0,1 % u klopidogrelu. Odpovídající počty dny/dnavé artritidy ve studii PEGASUS byly 1,6 %, resp. 1,5 %, resp. 1,1 % u tikagreloru 90 mg, resp. 60 mg, resp. placeba.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Tikagrelor je dobře tolerován v jednotlivých dávkách až 900 mg. Ve studii se zvyšujícími se jednotlivými dávkami byla limitujícím faktorem dávky gastrointestinální toxicita. Dalšími klinicky významnými nežádoucími účinky, které se mohou objevit při předávkování je dušnost a komorové pauzy (viz bod 4.8).
V případě předávkování se mohou objevit výše uvedené potenciální nežádoucí účinky a je nutné uvažovat o monitorování EKG.
V současné době není známo antidotum účinků tikagreloru a nepředpokládá se, že tikagrelor lze odstranit dialýzou (viz bod 4.4). Léčba předávkování má zahrnovat standardní postupy místní lékařské praxe. Očekávaným účinkem při předávkování tikagrelorem je riziko dlouhodobějšího krvácení spojeného s inhibicí krevních destiček. Pokud dojde ke krvácení, je třeba zahájit standardní podpůrnou léčbu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antiagregancia kromě heparinu,
ATC kód: B01AC24
Mechanismus účinku
Přípravek Brilique obsahuje tikagrelor, který patří chemicky mezi cyklopentyltriazolopyrimidiny (CPTP). Tikagrelor je perorální přímý selektivní reverzibilní antagonista receptoru P2Y12, který brání aktivaci a agregaci destiček závislé na P2Y12 a zprostředkované ADP. Tikagrelor neinteraguje přímo s vazným místem pro ADP, ale pokud je navázán na receptor P2YJ2, brání ADP-indukované signální transdukci. Vzhledem ktomu, že se destičky podílí na spouštění a/nebo vývoji trombotických komplikací aterosklerózy, bylo prokázáno, že inhibice funkce destiček má za následek snížení rizika CV příhod jako je smrt, IM nebo cévní mozková příhoda.
Tikagrelor též zvyšuje lokální hladiny endogenního adenosinu inhibicí rovnovážného nukleosidového transportéru-1 (ENT-1).
Bylo prokázáno, že tikagrelor zesiluje u zdravých lidí a u pacientů s ACS následující účinky indukované adenosinem: vazodilatace (průtok koronárními cévami se zvyšuje u zdravých dobrovolníků a pacientů s ACS; bolest hlavy), inhibice funkce destiček (v celé lidské krvi in vitro) a dušnost. Ovšem vztah mezi pozorovaným vzestupem adenosinu a klinickými důsledky (např. nemocnost-úmrtnost) nebyl jasně vysvětlen.
Farmakodynamické účinky
Nástup účinku
U pacientů se stabilní koronární arteriální nemocí na ASA vykazuje tikagrelor rychlý nástup farmakologického účinku, což bylo demonstrováno průměrnou inhibicí agregace krevních destiček (IPA) v rozsahu asi 41 % 0,5 hodiny po podání iniciální dávky 180 mg tikagreloru, s maximem IPA účinku 89 % 2-4 hodiny po podání a přetrváváním účinku 2-8 hodin. Devadesát procent pacientů vykazovalo konečný rozsah IPA >70 % 2 hodiny po podání.
Odeznění účinku
Pokud je plánován výkon CABG, je riziko krvácení pro tikagrelor vyšší ve srovnání s klopidogrelem, pokud je léčba vysazena v době kratší než 96 hodin do výkonu.
Převod z jiné léčby
Převod z léčby klopidogrelem 75 mg na tikagrelor 90 mg dvakrát denně má za následek absolutní vzestup IPA o 26,4 % a převod z tikagreloru na klopidogrel má za následek pokles absolutní hodnoty IPA o 24,5 %. Pacienti mohou být převedeni z klopidogrelu na tikagrelor bez ztráty antiagregačního účinku (viz bod 4.2).
Klinická účinnost a bezpečnost
Klinické důkazy účinnosti a bezpečnosti tikagreloru byly získány ve dvou klinických studiích fáze 3:
• Studii PLATO [PLATelet Inhibition and Patient Outcomes], srovnání léčby tikagrelorem a klopidogrelem, oba podávané v kombinaci s ASA a jinou standardní léčbou.
• Studii PEGASUS TIMI-54 [PrEvention with TicaGrelor of SecondAry Thrombotic Events in High-RiSk AcUte Coronary Syndrome Patients], srovnání léčby tikagrelorem v kombinaci s ASA se samotnou ASA.
Studie PLATO (Akutní koronární syndrom)
Ve studii PLATO bylo zařazeno 18 624 pacientů, kteří byli v průběhu 24 hodin od nástupu symptomů nestabilní anginy pectoris (UA), infarktu myokardu bez elevace úseku ST (NSTEMI) nebo infarktu myokardu s elevací úseku ST (STEMI) přijati a ošetřeni medikamentózně, nebo u nich byla provedena perkutánní koronární intervence (PCI), nebo CABG.
Klinická účinnost
Při denní dávce ASA prokázal tikagrelor 90 mg dvakrát denně lepší výsledky než klopidogrel 75 mg denně v prevenci složeného cílového parametru CV smrti, IM nebo cévní mozkové příhody, s tím, že rozdíl byl hlavně u CV smrti a MI. Pacientům byla podána iniciální dávka 300 mg klopidogrelu (až 600 mg, pokud měli PCI) nebo 180 mg tikagreloru.
Tento rozdíl byl zaznamenán časně (absolutní snížení rizika [ARR] 0,6 % a relativní snížení rizika [RRR] o 12 % po 30 dnech) a léčebný efekt byl konstantní po celou dobu 12 měsíců, vedoucí k ARR
1,9 % za rok a RRR o 16 %. Tyto výsledky předpokládají, že je vhodné pacienty léčit tikagrelorem 90 mg dvakrát denně po dobu 12 měsíců (viz bod 4.2). Léčba 54 pacientů s ACS tikagrelorem namísto klopidogrelem vede k prevenci 1 aterotrombotické příhody; léčba 91 pacientů vede k prevenci 1 CV smrti (viz Obrázek 1 a Tabulka 4).
Lepší léčebný efekt tikagreloru ve srovnání s klopidogrelem je konzistentní v mnoha podskupinách, včetně tělesné hmotnosti; pohlaví; lékařské anamnézy diabetes mellitus, tranzitorní ischemické ataky nebo nehemorhagické cévní mozkové příhody, nebo revaskularizace; souběžně podávaných léčiv zahrnujících hepariny, GpIIb/IIIa inhibitory a inhibitory protonové pumpy (viz bod 4.5); konečné diagnózy příhody (STEMI, NSTEMI nebo UA); a léčebné taktiky sledované při randomizaci (invazivní nebo farmakologická).
Slabě významná léčebná interakce byla pozorována s regionem, kde poměr rizik (HR) pro primární cílový parametr upřednostňuje tikagrelor mimo severní Ameriku, ale klopidogrel v severní Americe, což reprezentuje přibližně 10 % celkové studované populace (hodnota p=0,045 pro tuto interakci). Exploratorní analýza předpokládá možný vztah mezi dávkou ASA takového charakteru, že byla pozorována snížená účinnost tikagreloru se zvyšující se dávkou ASA. Dlouhodobá denní dávka ASA podávaná spolu s přípravkem Brilique má být 75-150 mg (viz body 4.2 a 4.4).
Obrázek 1 ukazuje odhadované riziko do výskytu jakékoliv příhody ve složeném primárním cílovém parametru účinnosti.
Analýza primárního složeného cílového parametru CV smrti, IM a cévní mozkové příhody (PLATO)
Obrázek 1
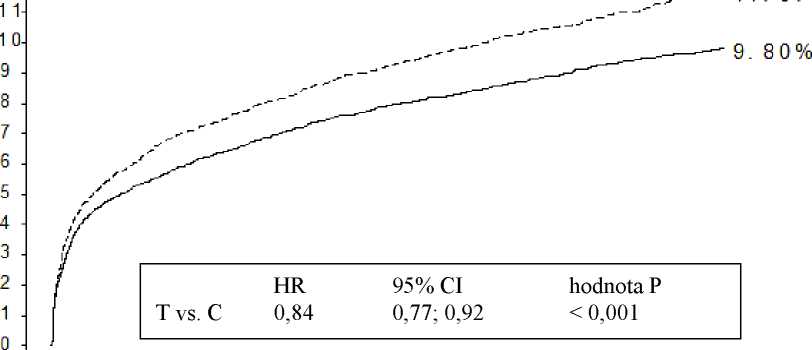
0 60 120 180 240 300 360
9 3 33 929 1
8628 8 52 1
Dny od randomizace
8460
8362
8219
8124
6743
6650
5161
5096
4147
4074
|
tikagrelor (T) |
[864/9333] |
|
klopidogrel (C) |
[1014/9291] |
Tikagrelor snižoval výskyt primárního složeného cílového parametru ve srovnání s klopidogrelem jak v populaci UA/NSTEMI, tak STEMI (Tabulka 4). Přípravek Brilique 90 mg dvakrát denně v kombinaci s nízkou dávkou ASA lze použít u pacientů s ACS (nestabilní anginou pectoris, s infarktem myokardu bez-ST elevace [NSTEMI] nebo s infarktem myokardu s elevací ST [STEMI]); včetně pacientů léčených a pacientů, kteří byli ošetřeni perkutánní koronární intervencí (PCI) nebo kterým byl voperován koronární arteriální by-pass (CABG).
Tabulka 4 Analýza primárních a sekundárních cílových parametrů (PLATO)
|
Tikagrelor 90 mg dvakrát denně (% pacientů s příhodou) N = 9333 |
Klopidogrel 75 mg jednou denně (% pacientů s příhodou) N = 9291 |
ARRa (%/rok) |
RRRa (%) (95% CI) |
p-hodnota | |
|
CV smrt, IM (kromě němého IM) nebo cévní mozková příhoda |
9,3 |
10,9 |
1,9 |
16 (8; 23) |
0,0003 |
|
Invazivní taktika |
8,5 |
10,0 |
1,7 |
16 (6; 25) |
0,0025 |
|
Neinvazivní taktika |
11,3 |
13,2 |
2,3 |
15 (0,3; 27) |
0,0444d |
|
CV smrt |
3,8 |
4,8 |
1,1 |
21 (9 ; 31) |
0,0013 |
|
IM (kromě němého |
5,4 |
6,4 |
1,1 |
16 (5; 25) |
0,0045 |
ARR = absolutní snížení rizika; RRR = relativní snížení rizika = (1 - poměr rizik) x 100 %. Záporná hodnota RRR ukazuje na zvýšení relativního rizika. kromě němého infarktu myokardu.
|
IM)b | |||||
|
Cévní mozková příhoda |
1,3 |
1,1 |
-0,2 |
-17(-52; 9) |
0,2249 |
|
Smrt ze všech příčin, IM (kromě němého IM) nebo cévní mozková příhody |
9,7 |
11,5 |
2,1 |
16 (8; 23) |
0,0001 |
|
CV smrt, celkem IM, cévní mozková příhoda, SRI, RI, TIA nebo jiné ATEc |
13,8 |
15,7 |
2,1 |
12 (5; 19) |
0,0006 |
|
Úmrtnost ze všech příčin |
4,3 |
5,4 |
1,4 |
22 (11; 31) |
0,0003d |
|
Trombóza do definitivního stentu |
1,2 |
1,7 |
0,6 |
32 (8; 49) |
0,0123d |
a
b
c
d
SRI = závažná rekurentní ischemie; RI = rekurentní ischemie; TIA = tranzitorní ischemická ataka; ATE = arteriální trombotická příhoda. Celkem IM zahrnuje němý IM, kde datum příhody je uveden jako datum, kdy byl odhalen.
nominální hodnota významnosti; všechny ostatní jsou formálně statisticky významné podle předdefinovaného hierarchického testování.
PLATO genetická_podstudie
Genotypizace CYP2C19 a ABCB1 u 10285 pacientů ve studii PLATO poskytuje asociaci mezi genotypem a výsledky studie PLATO. Vyšší účinnost tikagreloru ve srovnání s klopidogrelem na snížení CV příhod nebyla významně ovlivněna CYP2C19 u pacientů s genotypem ABCB1. Podobně jako v celé studii PLATO, se neliší velká krvácení PLATO celkem mezi tikagrelorem a klopidogrelem bez ohledu na CYP2C19 nebo ABCB1 genotyp. Velká non-CABG krvácení PLATO byla u pacientů s jednou nebo více chybějícími funkčními alelami CYP2C19 zvýšena u tikagreloru ve srovnání s klopidogrelem, ale byla podobná jako u klopidogrelu u pacientů bez ztracených funkčních alel.
Souhrnný kombinovaný parametr účinnosti a bezpečnosti
Souhrnný kombinovaný parametr účinnosti a bezpečnosti (CV smrt, IM, cévní mozková příhoda, nebo „celkem velké“ krvácení definované podle PLATO) ukazuje, že celkově lepší účinnost tikagreloru ve srovnání s klopidogrelem není negována velkými krvácivými příhodami (ARR 1,4 %; RRR 8 %; HR 0,92; p=0,0257) po dobu 12 měsíců po ACS.
Klinická bezpečnost
Podstudie Holter
V průběhu studie PLATO řešitelé prováděli u podskupiny téměř 3000 pacientů Holterovo monitorování všech komorových pauz a jiných arytmií. U přibližně 2000 pacientů bylo monitorování provedeno v akutní fázi ACS a po jednom měsíci. Primární sledovaným parametrem byl výskyt komorových pauz > 3 sekundy. V akutní fázi mělo komorové pauzy více pacientů na tikagreloru (6,0 %) než na klopidogrelu (3,5 %), po jednom měsíci 2,2 %, resp. 1,6 % (viz bod 4.4). Zvýšení počtu komorových pauz v akutní fázi ACS bylo více vyznačeno u pacientů na tikagreloru s anamnézou chronického srdečního selhání (9,2 % vs. 5,4 % u pacientů bez této anamnézy; u pacientů na klopidogrelu 4,0 % s anamnézou chronického srdečního selhání vs. 3,6 % u pacientů bez této anamnézy). Tato nerovnováha se neprojevila po jednom měsíci: 2,0 % vs. 2,1 % pro pacienty na tikagreloru s- resp. bez anamnézy chronického srdečního selhání; 3,8 % vs. 1,4 % u klopidogrelu. Nebyly zaznamenány žádné nežádoucí klinické následky spojené s touto nerovnováhou (včetně voperování kardiostimulátoru) u této populace pacientů.
Studie PEGASUS (anamnéza infarktu myokardu)
Studie PEGASUS TIMI-54 byla „event.-driven“ randomizovaná dvojitě zaslepená placebem kontrolovaná mezinárodní multicentrická klinická studie v paralelních skupinách, která zařadila 21162 pacientů. Hodnotila prevenci aterotrombotických příhod tikagrelorem ve dvou dávkách (90 mg dvakrát denně nebo 60 mg dvakrát denně) v kombinaci s nízkou dávkou ASA (75-150 mg) ve srovnání se samotnou ASA u pacientů s anamnézou IM a dalších rizikových faktorů aterotrombózy.
Pacienti vhodní k zařazení do studie byli ve věku 50 let a starší, s anamnézou IM (1 až 3 roky před randomizací) a nejméně jedním z následujících rizikových faktorů aterotrombózy: věk > 65 let, diabetes mellitus vyžadující farmakologickou léčbu, anamnéza druhého dřívějšího IM, průkaz vícečetného postižení CAD nebo chronická renální dysfunkce v konečném stádiu.
Pacienti nebyli vhodní pro zařazení do studie, pokud u nich bylo plánováno nasazení antagonistů P2Y12 receptoru, dipyridamolu, cilostazolu nebo antikoagulační léčby v průběhu studijního období; pokud měli poruchu krvácení nebo ischemickou cévní mozkovou příhodu nebo intrakraniální krvácení v anamnéze, nádor centrální nervové soustavy, nebo abnormalitu intrakraniálních cév, pokud krváceli z gastrointestinálního traktu v uplynulých 6 měsících nebo podstoupili chirurgický výkon v posledních 30 dnech.
Obrázek 2 Analýza primárních klinických složených cílových parametrů CV smrti, IM a cévní mozkové příhody (PEGASUS)
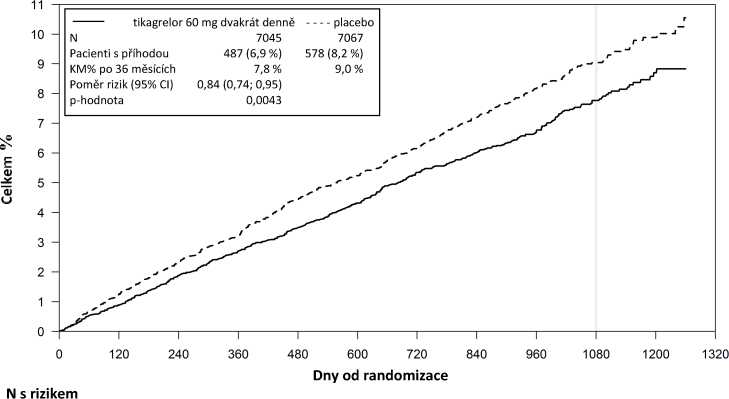
Ti 60 mg 7045 6948 6857
Placebo 7067 6950 6842
6784
6761
6711 6357 5904 4926
6658 6315 5876 4899
3698 2055 710
3646 2028 714
Tabulka 5 Analýza primárních a sekundárních cílových parametrů účinnosti (PEGASUS)
|
Tikagrelor 60 mg dvakrát denně +ASA N = 7045 |
Samotná ASA N = 7067 |
p-hodnota | ||||
|
Charakteristika |
Patienti s příhodou |
KM % |
HR (95% CI) |
Patienti s příhodou |
KM % | |
|
Primární cílový parametr | ||||||
|
Složený parametr CV smrti/IM /cévní mozkové příhody |
487 (6,9 %) |
7,8 % |
0,84 (0,74; 0,95) |
578 (8,2 %) |
9,0 % |
0,0043 (s) |
|
CV smrt |
174 (2,5 %) |
2,9 % |
0,83 (0,68; 1,01) |
210 (3,0%) |
3,4 % |
0,0676 |
|
IM |
285 (4,0 %) |
4,5 % |
0,84 (0,72; 0,98) |
338 (4,8%) |
5,2 % |
0,0314 |
|
Cévní mozková příhoda |
91 (1,3 %) |
1,5 % |
0,75 (0,57; 0,98) |
122 (1,7%) |
1,9 % |
0,0337 |
|
Tikagrelor 60 mg dvakrát denně +ASA N = 7045 |
Samotná ASA N = 7067 |
p-hodnota | ||||
|
Charakteristika |
Patienti s příhodou |
KM % |
HR (95% CI) |
Patienti s příhodou |
KM % | |
|
Sekundární cílové parametry | ||||||
|
CV smrt |
174 (2,5 %) |
2,9 % |
0,83 (0,68; 1,01) |
210 (3,0%) |
3,4 % |
- |
|
Všechny příčiny úmrtí |
289 (4,1 %) |
4,7 % |
0,89 (0,76; 1,04) |
326 (4,6 %) |
5,2 % |
- |
Poměr rizik a p-hodnota jsou vypočteny odděleně pro tikagrelor vs léčba samotnou ASA za použití Cox modelu proporcionálních rizik s léčebnými skupinami jako jedinou vysvětlující proměnnou.
KM podíl (%) vypočtený pro 36 měsíců.
Poznámka: počet prvních příhod pro komponenty CV smrti, IM a cévní mozkové příhody vyjadřuje aktuální počet prvních příhod pro každou komponentu zvlášť a nepřipočítavají se k počtu příhod ve složeném cílovém parametru
(s) vyjadřuje statistickou významnost.
CI = konfidenční interval; CV = kardiovaskulární; HR = poměr rizik; KM = Kaplan-Meier; IM = infarkt myokardu; N = počet pacientů.
Jak režim tikagrelor 60 mg dvakrát denně, tak 90 mg dvakrát denně v kombinaci s ASA byly výhodnější než samotná ASA v prevenci aterotrombotických příhod (složený cílový parametr: CV smrt, IM a cévní mozková příhoda) s konzistentním léčebným účinkem po celou dobu trvání studie. Tím bylo dosaženo 16% RRR, resp.1,27% ARR pro tikagrelor 60 mg a 15 % RRR, resp. 1,19% ARR pro tikagrelor 90 mg.
Ačkoli byl profil účinnosti 90 mg a 60 mg podobný, existují důkazy, že nižší dávka je lépe tolerována a má lepší bezpečnostní profil ve vztahu k riziku krvácení a dušnosti. Z tohoto důvodu se k prevenci aterotrombotických příhod (CV smrt, IM a cévní mozková příhoda) u pacientů s anamnézou IM a vysokým rizikem vývoje aterotrombotických příhod doporučuje pouze Brilique 60 mg v kombinaci sASA.
Tikagrelor 60 mg dvakrát denně ve srovnání se samotnou ASA snižoval významně primární složený cílový parametr CV smrti, IM a cévní mozkové příhody. Každá z komponent přispívala ke snížení primárního složeného cílového parametru (CV smrt 17% RRR, IM 16% RRR a cévní mozková příhoda 25% RRR).
RRR pro složený cílový parametr v období od 1 do 360 dnů (17% RRR) a od 361 dnů dále (16% RRR) bylo podobné. Existují pouze omezené údaje o účinnosti a bezpečnosti podávání tikagreloru po dobu delší než 3 roky.
Neexistují důkazy o prospěchu tikagreloru (žádné snížení primárního složeného cílového parametru CV smrti, IM a cévné mozkové příhody), pokud byl tikagrelor 60 mg dvakrát denně podáván klinicky stabilním pacientům > 2 roky od IM, nebo více než 1 rok po přerušení předchozí léčby inhibitorem ADP receptoru (viz též bod 4.2).
Klinická bezpečnost
Četnost přerušení léčby tikagrelorem 60 mg dvakrát denně v důsledku krvácení nebo dušnosti byla vyšší u pacientů > 75 let (42 %) než u mladších pacientů (rozmezí: 23-31%) s rozdílem oproti placebu vyšším než 10 % (42 % vs 29 %) u pacientů >75 let.
Pediatrická populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem Brilique u všech podskupin pediatrické populace ve schválené indikaci (informace o použití u dětí viz bod 4.2).
5.2 Farmakokinetické vlastnosti
Tikagrelor vykazuje lineární farmakokinetiku a expozice tikagreloru a aktivnímu metabolitu tikagreloru (AR-C124910XX) přibližně odpovídá podané dávce až do 1260 mg.
Absorpce
Absorpce tikagreloru je rychlá se střední hodnotou tmax přibližně 1,5 hodiny. Tvorba hlavního metabolitu v plazmě AR-C124910XX (též aktivní) z tikagreloru je rychlá se střední hodnotou tmax přibližně 2,5 hodiny. Po perorálním podání jedné dávky tikagreloru 90 mg nalačno zdravým subjektům je Cmax 529 ng/ml a AUC je 3451 ng.h/ml. Poměr metabolitu a mateřské látky je 0,28 pro Cmax a 0,42 pro AUC. Farmakokinetika tikagreloru a AR-C124910XX pacientům s anamnézou IM byla obecně podobná jako u ACS populace. Na základě populační farmakokinetické analýzy studie PEGASUS byl medián Cmax, resp AUC v rovnovážném stavu po podání tikagreloru 60 mg 391 ng/ml, resp. 3801 ng.h/ml. Pro tikagrelor 90 mg byl medián Cmax, resp. AUC v rovnovážném stavu 627 ng/ml, resp. 6255 ng.h/ml.
Průměrná absolutní hodnota biologické dostupnosti tikagreloru je odhadnuta na 36 %. Příjem stravy s vysokým obsahem tuků vedl k 21% zvýšení AUC tikagreloru a 22% snížení Cmax aktivního metabolitu, ale neměl vliv na Cmax ticagreloru nebo AUC aktivního metabolitu. Tyto malé změny mají pravděpodobně minimální klinické důsledky, a proto lze tikagrelor podávat s jídlem i bez jídla. Tikagrelor i jeho aktivní metabolit jsou substráty pro P-gp.
Tikagrelor podaný perorálně nebo přes nazogastrickou sondu do žaludku jako rozdrcené tablety smísené s vodou, má srovnatelnou biologickou dostupnost jako celé tablety s ohledem na AUC a Cmax pro tikagrelor a aktivní metabolit. Úvodní expozice (0,5 a 1 hodinu po podání) po podání rozdrcených tablet ve směsi s vodou byla vyšší ve srovnání s celými tabletami a s celkově stejným koncentračním profilem v dalším období (2 až 48 hodin).
Distribuce
Distribuční objem tikagreloru v ustáleném stavu je 87,5 l. Tikagrelor a aktivní metabolit jsou z velké části vázány na plazmatické bílkoviny (>99,0 %).
Biotransformace
CYP3A4 je hlavním enzymem zodpovědným za metabolismus tikagreloru, tvorbu aktivního metabolitu a interakce se substráty pro CYP3A4 ve smyslu aktivace až inhibice.
Hlavním metabolitem tikagreloru je AR-C124910XX, který je též aktivní, což bylo potvrzeno v podmínkách in vitro vazbou na destičkový P2YJ2 ADP-receptor. Systémová expozice aktivnímu metabolitu je přibližně 30-40 % expozice tikagreloru.
Eliminace
Hlavní cestou vylučování tikagreloru je eliminace jaterním metabolismem. Pokud je podán radioaktivně značený tikagrelor, vyloučí se průměrně 84 % radioaktivity (57,8 % do stolice, 26,5 % do moči). Z podané dávky se do moči vyloučí méně než 1 % tikagreloru a aktivního metabolitu. Hlavní cestou vylučování aktivního metabolitu je pravděpodobně biliární sekrece. Průměrný tm je přibližně 7 h pro tikagrelor a 8,5 h pro aktivní metabolit.
Zvláštní populace
Starší pacienti
U starších pacientů (> 75 let) byla ve srovnání s mladými pozorována vyšší expozice tikagreloru i aktivnímu metabolitu (přibližně o 25 % pro Cmax i AUC) u pacientů s ACS ve srovnání s mladšími pacienty ve farmakokinetické populační analýze. Tyto rozdíly se nepovažují za klinicky významné (viz bod 4.2).
Pediatrická populace
Tikagrelor nebyl hodnocen u pediatrické populace (viz body 4.2 a 5.1).
Pohlaví
U žen ve srovnání s muži byla pozorována vyšší expozice tikagreloru a aktivnímu metabolitu. Rozdíly se nepovažují za klinicky významné.
Porucha funkce ledvin
U pacientů se závažnou poruchou funkce ledvin (clearance kreatininu <30 ml/min) ve srovnání s pacienty s normální funkcí ledvin byla pozorována o přibližně 20 % nižší expozice tikagreloru a expozice aktivnímu metabolitu byla přibližně o 17 % vyšší (viz bod 4.2).
Porucha funkce jater
U pacientů s mírnou poruchou funkce byly hodnoty Cmax, resp. AUC pro tikagrelor o 12 %, resp. 23 % vyšší ve srovnání se zdravými jedinci, avšak IPA účinek tikagreloru byl podobný mezi oběma skupinami. U pacientů s mírnou poruchou funkce ledvin není nutné upravovat dávku. Tikagrelor nebyl studován u pacientů se závažnou poruchou funkce jater a neexistují žádné farmakokinetické údaje u pacientů se středně závažnou poruchou funkce jater. U pacientů, kteří měli střední nebo závažnou elevaci v jednom nebo více jaterních funkčních testech na vstupu byly plazmatické koncentrace tikagreloru v průměru podobné nebo mírně vyšší ve srovnání se subjekty bez elevací. U pacientů s mírnou poruchou funkce jater se nodoporučuje upravovat dávku (viz body 4.2 a 4.4).
Rasa
Pacienti asijského původu mají v průměru o 39 % vyšší biologickou dostupnost ve srovnání s bělošskou populací. Pacienti, kteří se sami identifikují s černou populací mají o 18 % nižší biologickou dostupnost tikagreloru ve srovnání s bělošskou populací. V klinicko-farmakologických studiích byla expozice (Cmax a AUC) japonské populace tikagreloru o přibližně 40 % (20 % po úpravě na tělesnou hmotnost) vyšší ve srovnání s bělošskou populací. Expozice pacientů, kteří se sami identifikovali jako hispánci nebo jihoameričani, byla podobná jako u kavkazské populace.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje pro tikagrelor a jeho hlavní metabolit neprokázaly neakceptovatelné riziko nežádoucích účinků pro člověka na základě konvenčních farmakologických studií bezpečnosti, toxikologických studií po jednorázovém a opakovaném podání dávky a hodnocení genotoxického potenciálu.
U několika zvířecích modelů byla pozorována gastrointestinální iritace v rozmezí klinicky relevantních expozic (viz bod 4.8).
Tikagrelor podávaný ve vysokých dávkách samicím laboratorních potkanů vykazoval zvýšený výskyt děložních tumorů (adenokarcinomy) a zvýšený výskyt jaterních adenomů. Pravděpodobným mechanismem vzniku děložních tumorů je hormonální nerovnováha, která může vést ke vzniku nádorů u laboratorních potkanů. Mechanismem pro tvorbu jaterních adenomů je pravděpodobně pro hlodavce specifická enzymová indukce v játrech. Z tohoto důvodu nejsou pozorované kancerogenní účinky pravděpodobně relevantní pro lidi.
U laboratorních potkanů byly pozorovány menší vývojové anomálie po podání dávek toxických pro matku (bezpečnostní poměr 5,1). U králíků bylo pozorováno mírné zpoždění vyzrávání jater a skeletu u plodů po podání vysoké dávky při absenci známek toxicity pro matku (bezpečnostní poměr 4,5).
Studie u laboratorních potkanů a králíků prokázaly reprodukční toxicitu, s mírně sníženým přírůstkem tělesné hmotnosti březích samic a sníženou životaschopností mláďat, sníženou porodní hmotností a zpomaleným růstem. Tikagrelor vyvolával nepravidelné cykly (převážné prodloužené) u samic laboratorních potkanů, ale neovlivnil celkovou plodnost samců a samic laboratorních potkanů. Farmakokinetické studie provedené s radioaktivně značeným tikagrelorem ukázaly, že se mateřská látka i její metabolity vylučují do mléka laboratorních potkanů (viz bod 4.6).
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Jádro tablety Mannitol (E421)
Dihydrát hydrogenfosforečnanu vápenatého Magnesium-stearát (E470b)
Sodná sůl karboxymethylškrobu (typ A)
Hyprolosa (E463)
Potah tablety Oxid titaničitý (E171)
Černý oxid železitý (E172)
Červený oxid železitý (E172)
Makrogol 400 Hypromelosa (E464)
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
• Transparentní PVC-PVDC/Al blistr (se symbolem slunce/měsíce) po 10 tabletách; krabičky po 60 tabletách (6 blistrů) a 180 tabletách (18 blistrů).
• Transparentní PVC-PVDC/Al kalendářní blistr (se symbolem slunce/měsíce) po 14 tabletách; krabičky po 14 tabletách (1 blistr), 56 tabletách (4 blistry) a 168 tabletách (12 blistrů).
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci
Žádné zvláštní požadavky na likvidaci. Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
AstraZeneca AB SE-151 85 Sodertálje Švédsko
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/10/655/007-011
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 3. prosince 2010
Datum posledního prodloužení registrace: 17. července 2015
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
NÁZEV PŘÍPRAVKU
1.
Brilique 90 mg potahované tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta obsahuje ticagrelorum 90 mg. Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Potahovaná tableta (tableta).
Kulaté bikonvexní žluté tablety označené „90“ nad „T“ na jedné straně a bez označení na druhé straně.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Přípravek Brilique podávaný s kyselinou acetylsalicylovou (ASA) je indikován k prevenci aterotrombotických příhod u dospělých pacientů s
- akutním koronárním syndromem (ACS) nebo
- infarktem myokardu (IM) v anamnéze a vysokým rizikem vývoje aterotrombotických příhod (viz body 4.2 a 5.1).
4.2 Dávkování a způsob podání
Dávkování
Pacienti užívající přípravek Brilique mají též užívat nízkou udržovací dávku ASA 75-150 mg denně, pokud není specificky kontraindikována.
Akutní koronární syndromy
Léčba přípravkem Brilique se zahajuje podáním jedné iniciální dávky 180 mg (dvě tablety po 90 mg) a dále se pokračuje dávkou 90 mg dvakrát denně.
Léčba přípravkem Brilique 90 mg dvakrát denně se doporučuje u pacientů s ACS po dobu 12 měsíců, pokud není přerušení léčby klinicky indikováno (viz bod 5.1).
Infarkt myokardu v anamnéze
U pacientů s anamnézou IM a vysokým rizikem aterotrombotických příhod se doporučuje podávat přípravek Brilique 60 mg dvakrát denně po dobu nejméně jednoho roku (viz bod 5.1). Léčbu lze zahájit bez přerušení jako pokračování po úvodní jednoroční léčbě přípravkem Brilique 90 mg nebo jiné léčby inhibitory receptoru pro adenosin difosfát (ADP) u pacientů s ACS a vysokým rizikem aterotrombotických příhod. Léčbu lze též zahájit až dva roky od ataky IM nebo v průběhu jednoho roku od ukončení předchozí léčby inhibitorem ADP receptoru. Existují pouze omezené údaje o účinnosti a bezpečnosti přípravku Brilique při léčbě delší než 3 roky.
Pokud je třeba změna medikace, první dávka přípravku Brilique se má podat 24 hodin po poslední dávce jiného antiagregačního léčivého přípravku.
Vynechaná dávka
Je třeba předcházet vynechání dávky. Pokud pacient zapomene na dávku přípravku Brilique, užije tabletu (další dávku) v pravidelném čase.
Zvláštní populace
Starší pacienti
U starších pacientů není nutná úprava dávky (viz bod 5.2).
Porucha funkce ledvin
U pacientů s poruchou funkce ledvin není nutná úprava dávky (viz bod 5.2). Nejsou dostupné informace týkající se léčby dialyzovaných pacientů, a proto se podávání tikagreloru u těchto pacientů nedoporučuje.
Porucha funkce jater
Tikagrelor nebyl hodnocen u pacientů se závažnou poruchou funkce jater a použití u těchto pacientů je tedy kontraindikováno (viz body 4.3). U pacientů se středně závažnou poruchou funkce jater jsou dostupné pouze omezené informace. Nedoporučuje se upravovat dávku, ale tikagrelor se má užívat s opatrností (viz body 4.4 a 5.2).U pacientů se mírnou poruchou funkce jater není nutná úprava dávky viz bod 5.2).
Pediatrická populace
Bezpečnost a účinnost tikagreloru u dětí ve věku do 18 let nebyla stanovena. Nejsou dostupná žádná data.
Způsob podání Perorální podání.
Přípravek Brilique lze podat s jídlem i bez jídla.
U pacientů, kteří nemohou tabletu(y) spolknout celou(é), lze tablety rozdrtit na jemný prášek a smísit s polovinou sklenice vody a ihned vypít. Sklenici je třeba vypláchnout polovinou sklenice vody a obsah vypít. Směs lze podat též přes nazogastrickou sondu (CH8 nebo větší). Po podání směsi je důležité nazogastrickou sondu propláchnout vodou.
4.3 Kontraindikace
• Hypersenzitivita na léčivou látku nebo na kteroukoliv pomocnou látku tohoto přípravku uvedenou v bodě 6.1 (viz bod 4.8).
• Patologické aktivní krvácení.
• Anamnéza intrakraniálního krvácení (viz bod 4.8).
• Závažná porucha funkce jater (viz body 4.2, 4.4 a 5.2).
• Souběžné podávání tikagreloru se silnými inhibitory CYP3A4 (např. ketokonazolem, klarithromycinem, nefazodonem, ritonavirem a atazanavirem) je kontraindikováno, neboť souběžné podávání může vést k podstatnému zvýšení expozice tikagreloru (viz bod 4.5).
4.4 Zvláštní upozornění a opatření pro použití
Riziko krvácení
Použití tikagreloru u pacientů se známým zvýšeným rizikem krvácení se má zvážit s ohledem na prospěch z pohledu prevence aterotrombotických příhod (viz body 4.8 a 5.1). Pokud je klinicky indikováno, tikagrelor se má podávat opatrně u následujících skupin pacientů:
• Pacienti se sklonem ke krvácení (např. v důsledku nedávného traumatu, nedávného chirurgického výkonu, poruchy koagulace, akutního nebo recentního gastrointestinálního krvácení). Použití tikagreloru je kontraindikováno u pacientů s aktivním patologickým krvácením u pacientů s anamnézou intrakraniálního krvácení a pacientů se závažnou poruchou funkce jater (viz bod 4.3).
• Pacienti, kteří souběžně užívají přípravky, které mohou zvyšovat riziko krvácení (např. nesteroidní protizánětlivé léky (NSAID), perorální antikoagulancia a/nebo fibrinolytika v průběhu 24 hodin od podání tikagreloru).
Nejsou dostupné informace u pacientů na tikagreloru týkající se hemostatického prospěchu po podání transfuze krevních destiček; cirkulující tikagrelor může inhibovat infundované krevní destičky. Souběžné podání tikagreloru a desmopresinu nesnižuje dobu krvácení, a tak je nepravděpodobné, že by byl desmopresin účinný v klinické léčbě krvácivých příhod (viz bod 4.5).
Antifibrinolytická léčba (kyselina aminokapronová nebo kyselina tranexanová) a/nebo léčba rekombinantním faktorem VIIa mohou zvyšovat hemostázu. V léčbě tikagrelorem lze pokračovat, pokud byl zjištěn důvod krvácení a krvácení je pod kontrolou.
Chirurgická léčba
Pacienti mají být poučeni, že mají informovat lékaře a zubní lékaře, že užívají tikagrelor, před jakoukoliv plánovanou operací a předtím, než začnou užívat jakýkoliv nový léčivý přípravek.
U pacientů, kteří podstoupili koronární arteriální bypass (CABG) ve studii PLATO, měl tikagrelor vyšší počet krvácení než klopidogrel, pokud byla léčba tikagrelorem přerušena v průběhu 1 dne před chirurgickým zákrokem, ale podobnou frekvenci závažných krvácení jako klopidogrel, když byla léčba přerušena 2 nebo více dnů před chirurgickým zákrokem (viz bod 4.8). Pokud je u pacienta plánována operace a není žádoucí protidestičkový účinek, je třeba tikagrelor vysadit 7 dnů před operací (viz bod 5.1).
Pacienti s anamnézou ischemické cévní mozkové příhody
Pacienti s ACS a anamnézou ischemické cévní mozkové příhody mohou být léčeni přípravkem Brilique po dobu až 12 měsíců (studie PLATO).
Pacienti s anamnézou IM a předchozí anamnézou ischemické cévní mozkové příhody nebyli zařazeni do studie PEGASUS. Protože nejsou dostupné údaje, nedoporučuje se pokračovat v léčbě po jednom roce.
Porucha funkce jater
Tikagrelor je kontraindikován u pacientů se závažnou poruchou funkce jater (viz body 4.2 a 4.3).
U pacientů se středně závažnou poruchou funkce jater jsou pouze omezené, a proto se u těchto pacientů doporučuje opatrnost (viz body 4.2 a 5.2).
Pacienti s rizikem bradykardie
Na základě pozorování většinou asymptomatických komorových pauz v časných fázích klinického vývoje, byli pacienti se zvýšeným rizikem bradykardie (např. pacienti bez kardiostimulátoru se sick sinus syndromem, AV blokádou 2. a 3. stupně nebo synkopou vyvolanou bradykardií) vyloučeni ze stěžejních studií hodnotící bezpečnost a účinnost tikagreloru. Vzhledem k tomu, že jsou klinické zkušenosti s tikagrelorem u těchto pacientů omezené, doporučuje se opatrnost (viz bod 5.1).
Dále je třeba opatrnosti, pokud je tikagrelor podáván souběžně s léčivými přípravky, které vyvolávají bradykardii. Při souběžném podávání jednoho nebo více léčivých přípravků ve studii PLATO, které vyvolávají bradykardii (tj. 96 % betablokátory, 33 % blokátory kalciového kanálu diltiazem a verapamil a 4 % digoxin) (viz bod 4.5) nebyly prokázány klinicky významné nežádoucí účinky.
V průběhu podstudie Holter studie PLATO mělo v akutní fázi ACS více pacientů léčených tikagrelorem než pacientů léčených klopidogrelem komorové pauzy > 3 sekundy. Zvýšení komorových pauz v průběhu akutní fáze ACS detekovaných Holterem bylo vyšší u pacientů s chronickým srdečním selháním (CHF) ve srovnání s celkovou studijní populací, ale nikoliv po jednom měsíci, nebo ve srovnání s klopidogrelem. S touto dysbalancí nebyly v této populaci pacientů spojeny žádné nežádoucí klinické konsekvence (včetně synkopy nebo voperování kardiostimulátoru) (viz bod 5.1).
Dusnost
Dušnost byla hlášena u pacientů léčených tikagrelorem Dušnost je obvykle mírné až střední intenzity a často ustupuje bez nutnosti přerušit léčbu. Pacienti s astmatem/ chronickou obstrukční plicní nemocí (CHOPN) mohou mít zvýšené absolutní riziko výskytu dušnosti při užívání tikagreloru (viz bod 4.8). Tikagrelor se má používat opatrně u pacientů s anamnézou astmatu a/nebo CHOPN. Mechanismus nebyl zjištěn. Pokud si pacient stěžuje na nově vzniklou, protahovanou nebo zhoršující se dušnost, je třeba ji zevrubně zhodnotit a pokud není tolerována, je třeba léčbu tikagrelorem přerušit. Další údaje viz bod 4.8.
Zvýšení hladin kreatininu
V průběhu léčby tikagrelorem se mohou zvyšovat hladiny kreatininu (viz bod 4.8). Mechanismus nebyl vysvětlen. Funkce ledvin se má kontrolovat podle obvyklé lékařské praxe. U pacientů s ACS se doporučuje zkontrolovat funkci ledvin též jeden měsíc po zahájení léčby tikagrelorem a se zvláštní pozorností věnovanou pacientům >75 let, pacientům se středně závažnou/závažnou poruchou funkce ledvin a pacientům léčeným blokátory angiotezinových receptorů (ARB).
Zvýšení hladin kyseliny močové
V průběhu léčby tikagrelorem se může objevit hyperurikemie (viz bod 4.8). Je třeba opatrnosti, pokud je tikagrelor podáván pacientům s anamnézou hyperurikemie nebo dnavé artritidy. Jako preventivní opatření se nedoporučuje podávat tikagrelor pacientům s nefropatií vyvolanou kyselinou močovou.
Další
Na základě vztahu pozorovaného ve studii PLATO mezi udržovací dávkou ASA a relativní účinností tikagreloru ve srovnání s klopidogrelem se nedoporučuje podávat tikagrelor a vysoké udržovací dávky ASA (> 300 mg) (viz bod 5.1).
Předčasné přerušení léčby
Předčasné přerušení jakékoli protidestičkové léčby, včetně přípravku Brilique, může vést ke zvýšení rizika kardiovaskulární (CV) smrti nebo IM v důsledku základního onemocnění. Proto se má předčasné přerušení léčby vyloučit.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Tikagrelor je převážně substrátem pro CYP3A4 a mírným inhibitorem CYP3A4. Tikagrelor je též substrátem pro glykoprotein-P (P-gp) a slabým inhibitorem P-gp a může zvyšovat expozici k substrátům pro P-gp.
Vliv jiných léčivých přípravků na tikagrelor
Léčivé přípravky metabolizované CYP3A4 Inhibitory CYP3A4
• Silné inhibitory CYP3A4 - souběžné podávání tikagreloru a ketokonazolu zvyšovalo Cmax a AUC až 2,4krát, resp. 7,3krát. Hodnoty Cmax a AUC aktivního metabolitu byly sníženy o 89 %, resp. 56 %. Jiné účinné inhibitory CYP3A4 (klarithromycin, nefazodon, ritonavir a atazanavir) budou mít pravděpodobně stejný vliv, a proto je souběžné podávání silných inhibitorů CYP3A4 s tikagrelorem je kontraindikováno (viz bod 4.3).
• Středně silné inhibitory CYP3A4 - souběžné podávání diltiazemu a tikagreloru zvyšovalo hodnoty Cmax o 69 % a AUC až 2,7krát u tikagreloru a snižovalo hodnotu Cmax o 38 % a neměnilo AUC aktivního metabolitu. Nebyl prokázán vliv tikagreloru na plazmatické koncentrace diltiazemu. Lze očekávat, že jiné středně účinné inhibitory CYP3A4 (např. amprenavir, aprepitant, erythromycin a flukonazol) mohou mít podobný efekt a mohou být podávány souběžně s tikagrelorem.
Induktory CYP3A
Souběžné podávání rifampicinu a tikagreloru snižovalo hodnoty Cmax a AUC tikagreloru o 73 %, resp. 86 %. Hodnota Cmax aktivního metabolitu zůstala nezměněna a hodnota AUC se snížila o 46 %.
U jiných induktorů CYP3A4 (např. fenytoin, karbamazepin a fenobarbital) lze očekávat snížení expozice tikagreloru. Souběžné podávání tikagreloru a účinných induktorů CYP3A4 může snižovat expozici a účinnost tikagreloru, a proto se jejich souběžné podávání s tikagrelorem nedoporučuje.
Cyklosporin (inhibitor P-gpa CYP3A4)
Souběžné podávání cyklosporinu (600 mg) a tikagreloru zvyšovalo Cmax a AUC tikagreloru 2,3násobně, resp. 2,8násobně. V přítomnosti cyklosporinu byla AUC aktivního metabolitu zvýšena o 32 % a Cmax snížena o 15 %.
Nejsou dostupné údaje o souběžném podávání tikagreloru s dalšími aktivními látkami, které jsou také silnými inhibitoryP-gp a středně silnými inhibitory CYP3A4 (např. verapamil, chinidin), které také mohou zvyšovat expozici tikagreloru. Pokud nelze souběžné podávání vyloučit, je třeba opatrnosti.
Další
Klinicko farmakologické interakční studie prokázaly, že souběžné podávání tikagreloru s heparinem, enoxaparinem a kyselinou acetylsalicylovou nebo desmopresinem nemá vliv na farmakokinetiku tikagreloru nebo jeho aktivního metabolitu nebo na ADP indukovanou agregaci destiček ve srovnání se samotným tikagrelorem. Pokud je to klinicky indikováno, je třeba podávat léčivé přípravky, která ovlivňují hemostázu, v kombinaci s tikagrelorem opatrně.
Při denní konzumaci velkého množství grapefruitové šťávy (3 x 200 ml) bylo pozorováno 2násobné zvýšení expozice tikagreloru. Předpokládá se, že u většiny pacientů není takto velké zvýšení expozice klinicky relevantní.
Vliv tikagreloru na jiné léčivé přípravky Léčivé přípravky metabolizované CYP3A4
• Simvastatin - souběžné podávání tikagreloru a simvastatinu zvyšovalo Cmax a AUC simvastatinu o 81 %, resp. 56 % a zvyšovalo Cmax a AUC kyseliny simvastatinu o 64 %, resp. 52 %
s individuálním zvýšením až na 2-3násobek. Souběžné podávání tikagreloru a simvastatinu v dávkách vyšších než 40 mg denně může vyvolat nežádoucí účinky simvastatinu a má být zváženo z pohledu možného prospěchu. Nebyl prokázán vliv simvastatinu na plazmatické koncentrace tikagreloru. Tikagrelor může mít podobný vliv na lovastatin. Nedoporučuje se souběžné podávání tikagreloru a simvastatinu nebo lovastatinu v dávkách vyšších než 40 mg.
• Atorvastatin - souběžné podávání atorvastatinu a tikagreloru zvýšilo hodnoty Cmax a AUC kyseliny atorvastatinu o 23 %, resp. 36 %. Podobný vzestup Cmax a AUC byl pozorován u všech kyselých metabolitů atorvastatinu. Tyto změny nejsou považovány za klinicky významné.
• Nelze vyloučit podobný vliv na jiné statiny metabolizované CYP3A4. Pacienti zařazení do studie PLATO dostávali tikagrelor a různé jiné statiny bez problémů spojených s bezpečností, přičemž tyto přípravky užívalo celkem 93 % pacientů zařazených do studie PLATO.
Tikagrelor je mírný inhibitor CYP3A4. Souběžné podávání tikagreloru a substrátů pro CYP3A4 s úzkým terapeutickým indexem (např. cisaprid nebo námelové alkaloidy) se nedoporučuje, neboť tikagrelor může zvyšovat expozici těmto léčivým přípravkům.
Substráty P-gp (včetně digoxinu a cyklosporinu)
Souběžné podávání tikagreloru zvyšuje Cmax a AUC digoxinu o 75 %, resp. o 28 %. Průměrné hodnoty koncentrací digoxinu byly při současném podávání tikagreloru zvýšeny o přibližně 30 % s jednotlivými až 2násobnými maximy. Hodnoty Cmax a AUC tikagreloru a aktivního metabolitu se v přítomnosti digoxinu nemění. Z tohoto důvodu se doporučuje pečlivé klinické a/nebo laboratorní monitorování, pokud se souběžně s tikagrelorem podávají léčiva s úzkých terapeutickým indexem a metabolismem závislým na P-gp, jako je např. digoxin.
Nebyl zjištěn vliv tikagreloru na sérové hladiny cyklosporinu. Vliv tikagreloru na jiné substráty P-gp nebyl studován.
Léčivé přípravky metabolizované CYP2C9
Souběžné podávání tikagreloru a tolbutamidu nemělo za následek změnu plazmatických koncentrací obou léčivých přípravků, což předpokládá, že tikagrelor není inhibitorem CYP2C9 a je nepravděpodobné, že by tikagrelor ovlivňoval metabolismus léčivých přípravků jako je warfarin a tolbutamid zprostředkovaný CYP2C9.
Perorální antikoncepce
Souběžné podávání tikagreloru a levonorgestrelu a ethinylestradiolu zvyšovalo expozici ethinyl estradiolu o asi 20 %, ale neměnilo farmakokinetiku levonorgestrelu. Nepředpokládá se klinicky významný vliv na účinnost perorální antikoncepce, pokud je levonorgestrel a ethinylestradiol podáván souběžně s tikagrelorem.
Léčivé přípravky vyvolávající bradykardii
Při podávání tikagreloru současně s léčivými přípravky, které vyvolávají bradykardii, se doporučuje opatrnost, vzhledem k pozorovaným a obvykle asymptomatickým komorovým pauzám a bradykardii (viz bod 4.4). Ve studii PLATO však při současném podávání jednoho nebo více léčivých přípravků vyvolávajících bradykardii (tj. 96 % betablokátory, 33 % blokátory kalciového kanálu diltiazem a verapamil a 4 % digoxin) nebyly pozorovány klinicky významné nežádoucí účinky.
Jiná souběžná léčba
V klinických studiích byl tikagrelor podáván souběžně s ASA, inhibitory protonové pumpy, statiny, betablokátory, inhibitory angiotenzin konvertujícího enzymu (ACE) a blokátory receptoru pro angiotenzin podle potřeby k dlouhodobé léčbě doprovodných onemocnění a krátkodobě také heparin, nízkomolekulární heparin a intravenózní inhibitory GplIb/IIIa (viz bod 5.1). Neprokázalo se, že by docházelo ke klinicky významným nežádoucím interakcím s těmito léčivými přípravky.
Souběžné podávání tikagreloru a heparinu, enoxaparinu nebo desmopresinu nemá vliv na parciální aktivovaný tromboplastinový čas (aPTT), aktivovaný koagulační čas (ACT) nebo výsledky stanovení faktoru Xa. Vzhledem k potenciálu farmakodynamické interakce je však třeba opatrnosti při souběžném podávání tikagreloru a léčivých přípravků ovlivňujících hemostázu.
Vzhledem k hlášení kožního krvácení při podávání SSRIs (tj. paroxetin, sertralin a citalopram) se doporučuje opatrnost při souběžném podávání SSRIs a tikagreloru, neboť může dojít ke zvýšení rizika krvácení.
4.6 Fertilita, těhotenství a kojení
Ženy ve fertilním věku.
Ženy v plodném věku mají v průběhu léčby tikagrelorem používat vhodnou antikoncepci, aby se předešlo otěhotnění.
Údaje o podávání tikagreloru těhotným ženám jsou omezené nebo nejsou k dispozici. Studie na zvířatech prokázaly reprodukční toxicitu (viz bod 5.3). Podávání tikagreloru se v průběhu těhotenství nedoporučuje.
Kojení
Dostupné farmakodynamické/toxikologické údaje u zvířat prokázaly vylučování tikagreloru a jeho metabolitů do mléka (viz bod 5.3). Riziko pro kojené novorozence/děti nelze vyloučit. Na základě posouzení prospěšnosti kojení pro dítě a prospěšnosti léčby pro matku je nutno rozhodnout, zda přerušit kojení nebo přerušit podávání tikagreloru.
Fertilita
Tikagrelor nemá vliv na samčí nebo samičí fertilitu u zvířat (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Tikagrelor nemá žádný vliv nebo má pouze zanedbatelný vliv na schopnost řídit a ovládat stroje.
V průběhu léčby tikagrelorem byly hlášeny případy závratě a zmatenosti. Pacienti, kteří zaznamenají tyto příznaky, by měli být opatrní, pokud řídí nebo obsluhují stroje.
4.8 Nežádoucí účinky
Shrnutí bezpečnostního profilu
Bezpečnostní profil tikagreloru byl hodnocen ve dvou velkých „outcome“ klinických studiích fáze 3 (PLATO a PEGASUS), které zařadily více než 39000 pacientů (viz bod 5.1).
Ve studii PLATO byl u pacientů na tikagreloru zjištěn vyšší výskyt přerušení léčby v důsledku nežádoucích účinků než u klopidogrelu (7,4 % vs 5.4 %). Ve studii PEGASUS byl u pacientů na tikagreloru zjištěn vyšší výskyt přerušení léčby v důsledku nežádoucích účinků ve srovnání se samotnou ASA (16,1 % pro tikagrelor 60 mg a ASA vs 8,5 % pro samotnou ASA). Nejčastěji hlášeným nežádoucím účinkem u pacientů léčených tikagrelorem bylo krvácení a dušnost (viz bod 4.4).
Tabulkový přehled nežádoucích účinků
Následující nežádoucí účinky byly identifikovány ve studiích s tikagrelorem nebo byly hlášeny z poregistračního sledování (Tabulka 1).
Nežádoucí účinky jsou uvedeny podle terminologie MedDRA tříd orgánových systémů (SOC).
V každé SOC jsou nežádoucí účinky uvedeny podle kategorií četností. Četnosti jsou definovány podle následující konvence: velmi časté (> 1/10). časté (> 1/100 až < 1/10), méně časté (> 1/1000 až
< 1/100), vzácné (> 1/10 000 až < 1/1000), velmi vzácné (< 1/10 000), není známo (z dostupných údajů nelze určit).
Tabulka 1 Nežádoucí účinky podle četnosti a třídy orgánových systémů (SOC)
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
|
Novotvary benigní, maligní a blíže neurčené (zahrnující cysty a polypy) |
Krvácení z nádoru3 | ||
|
Poruchy krve a lymfatického systému |
Krvácení v důsledku poruchy krveb | ||
|
Poruchy imunitního systému |
Hypersensitivita zahrnující angioedémc | ||
|
Poruchy metabolismu a výživy |
Hyperurikemied |
Dna/dnavá artritida | |
|
Psychiatrické poruchy | |||
|
Poruchy nervového systému |
Závrať, synkopa, bolest hlavy |
Intrakraniální krvácení | |
|
Poruchy oka |
Oční krváceníe | ||
|
Poruchy oka a labyryntu |
Krvácení z ucha | ||
|
Cévní poruchy |
např. krvácení z karcinomu močového měchýře, žaludečního karcinomu, karcinomu tlustého střeva např. zvýšená tendence k tvorbě modřin, spontánní hematomy, hemoragická diatéza identifikované z poregistračních zkušeností
|
Třída orgánových systémů |
Velmi časté |
Časté |
Méně časté |
|
Respirační, hrudní a mediastinální poruchy |
Krvácení z respiračního systémuf | ||
|
Gastrointestinální poruchy |
Gastrointestinální krváceníg, průjem, nauzea, dyspepsie, zácpa |
Retroperitoneální krvácení | |
|
Poruchy kůže a podkožní tkáně |
Subkutánní nebo kožní krváceníh, vyrážka, svědění | ||
|
Poruchy svalové a kosterní soustavy a pojivové tkáně |
Svalové krvácenť | ||
|
Poruchy ledvin a močových cest |
Krvácení z močových cestj | ||
|
Poruchy reprodukčního systému a prsu |
Krvácení z reprodukčních k orgánů | ||
|
Vyšetření |
Zvýšený kreatinin v krvid | ||
|
Poranění, otravy a procedurální komplikace |
Krvácení po chirurgickém zákroku, traumatické krváceníl |
a
b
c
d
e
f
g
h
i
J
k
l
četnosti odvozené z laboratorních měření (zvýšení kyseliny močové na > horní limit normálních hodnot z výchozí hodnoty pod nebo v rozmezí normálních referenčních hodnot. Zvýšení kreatininu o > 50 % oproti výchozí hodnotě) a nikoliv z hrubé frekvence hlášení nežádoucích příhod. např. krvácení ze spojivky, sítnice a nitrooční krvácení např. epistaxe, hemoptýza
např. krvácení z dásní, konečníku, žaludečních vředů např. ekchymóza, kožní krvácení, petechie např. hemartróza, svalové krvácení např. hematurie, hemoragická cystitida
např. vaginální krvácení, hematospermie, postmenopauzální krvácení např. kontuze, traumatický hematom, traumatické krvácení
Popis vybraných nežádoucích účinků
Krvácení
Zjištění o krvácení ve studii PLATO
Celkový přehled krvácivých příhod ve studii PLATO je uveden v Tabulce 2.
Tabulka 2 Analýza všech krvácivých příhod, odhady ve škále Kaplan-Meier po 12 měsících
(PLATO)
|
Brilique (%/rok) N = 9235 |
klopidogrel (%/rok) N = 9186 |
P | |
|
PLATO celkem velké |
11,6 |
11,2 |
0,4336 |
|
PLATO velké fatální/život ohrožující |
5,8 |
5,8 |
0,6988 |
|
Non-CABG PLATO velké |
4,5 |
3,8 |
0,0264 |
|
Neprocedurální PLATO velké |
3,1 |
2,3 |
0,0058 |
|
PLATO celkem velké + malé |
16,1 |
14,6 |
0,0084 |
|
Neprocedurální PLATO velké + malé |
5,9 |
4,3 |
< 0,0001 |
|
Definované podle TIMI-velké |
7,9 |
7,7 |
0,5669 |
|
Definované podle TIMI- -velké + malé |
11,4 |
10,9 |
0,3272 |
Definice kategorií krvácení:
Velké fatální/život ohrožující krvácení: klinicky zjevné s poklesem hemoglobinu o > 50 g/l nebo podání > 4 transfuzí červených krvinek; nebo fatální; nebo intrakraniální; nebo intraperikardiální se srdeční tamponádou; nebo s hypovolémickým šokem nebo těžkou hypotenzí vyžadující podání vosopresorů nebo chirurgický zákrok.
Velké ostatní: klinicky zjevné s poklesem hemoglobinu o 30-50 g/l nebo podání 2-3 transfuzí červených krvinek; nebo významně invalidizující.
Malé krvácení: vyžadující lékařskou intervenci k zastavení nebo léčbě krvácení.
TIMI velké krvácení: klinicky zjevné s poklesem hemoglobinu o > 50 g/l nebo intrakraniální krvácení.
TIMI malé krvácení: klinicky zjevné s poklesem hemoglobinu o 30-50 g/l.
* p-hodnota vypočtena z Cox proporcionálního modelu rizik s léčebnými skupinami jako jedinou vysvětlující proměnnou
Tikagrelor a klopidogrel se neliší ve frekvenci PLATO velké fatální/život ohrožující krvácení, PLATO celkové velké krvácení, TIMI velké krvácení nebo TIMI malé krvácení (Tabulka 2). S tikagrelorem se objevilo více PLATO kombinovaných velkých + malých krvácení ve srovnání s klopidogrelem. Několik pacientů ve studii PLATO mělo fatální krvácení: 20 (0,2 %) s tikagrelorem a 23 (0,3 %) s klopidogrelem (viz bod 4.4).
Věk, pohlaví, tělesná hmotnost, rasa, geografická příslušnost, jiné ovlivňující podmínky, souběžná léčba a lékařská anamnéza, včetně předchozí cévní mozkové příhody nebo tranzitorní ischemické ataky, nemají předpovědní hodnotu ve vztahu k celkovému nebo neprocedurálnímu velkému PLATO krvácení. Nebyla identifikována žádná specifická skupina s rizikem jakéhokoliv krvácení.
Krvácení vztahující se k CABG: Ve studii PLATO mělo 42 % z 1584 pacientů (12 % kohorty), kteří podstoupili chirurgický zákrok voperování koronárního arteriálního bypassu (CABG) velké fatální/život ohrožující krvácení, což nepředstavuje rozdíl mezi léčebnými skupinami. Fatální CABG krvácení se objevilo u 6 pacientů v každé léčebné skupině (viz bod 4.4).
Non-CABG krvácení a krvácení, které není spojeno s výkonem: tikagrelor a klopidogrel se neliší v non-CABG krvácení definovaném podle PLATO jako velké fatální/život ohrožující krvácení, ale krvácení definovaná podle PLATO jako celkem velká krvácení, TIMI velká, TIMI velká + malá jsou častější u tikagreloru. Podobně, pokud se neuvažují krvácení, která souvisejí s výkonem, je krvácení častější u tikagreloru ve srovnání s klopidogrelem (Tabulka 2). Přerušení léčby v důsledku neprocedurálního krvácení bylo častější u tikagreloru (2,9 %) než u klopidogrelu (1,2 %; p < 0,001).
Intrakraniální krvácení: Více intrakraniálních krvácení bylo u tikagreloru (n=27 krvácení u 26 pacientů; 0,3 %) než u klopidogrelu (n=14 krvácení; 0,2 %), z nichž bylo 11 smrtelných krvácení u tikagreloru a 1 u klopidogrelu. Nebyl zjištěn rozdíl v celkovém počtu smrtelných krvácení.
Krvácení ve studii PEGASUS
Celkové výsledky krvácivých příhod ve studii PEGASUS jsou uvedeny v Tabulce 3.
Tabulka 3 Analýza všech krvácivých příhod, odhady ve škále Kaplan-Meier po 36 měsících
(PEGASUS)
|
Tikagrelor 60 mg dvakrát denně + ASA N = 6958 |
Samotná ASA N = 6996 | |||
|
Cílové parametry bezpečnosti |
KM% |
Poměr rizik (95% CI) |
KM% |
p-hodnota |
|
TIMI-definované kategorie krvácení | ||||
|
TIMI velké |
2,3 |
2,32 (1,68; 3,21) |
1,1 |
<0,0001 |
|
fatální |
0,3 |
1,00 (0,44; 2,27) |
0,3 |
1,0000 |
|
ICH |
0,6 |
1,33 (0,77; 2,31) |
0,5 |
0,3130 |
|
jiné TIMI velké |
1,6 |
3,61 (2,31; 5,65) |
0,5 |
<0,0001 |
|
TIMI velké nebo malé |
3,4 |
2,54 (1,93; 3,35) |
1,4 |
<0,0001 |
|
TIMI velké nebo malé nebo vyžadující lékařskou pozornost |
16,6 |
2,64 (2,35; 2,97) |
7,0 |
<0,0001 |
|
PLATO-definované kategorie krvácení | ||||
|
PLATO velké |
3,5 |
2,57 (1,95; 3,37) |
1,4 |
<0,0001 |
|
Fatální/život ohrožující |
2,4 |
2,38 (1,73; 3,26) |
1,1 |
<0,0001 |
|
Jiné PLATO velké |
1,1 |
3,37 (1,95; 5,83) |
0,3 |
<0,0001 |
|
PLATO velké nebo malé |
15,2 |
2,71 (2,40; 3,08) |
6,2 |
<0,0001 |
Definice kategorií krvácení:
TIMI velké: Fatální krvácení, nebo jakékoli intrakraniální krvácení, nebo klinicky zjevné krvácení doprovázené poklesem hemoglobinu (Hb) o > 50 g/l, nebo, pokud vyšetření haemoglobinu není dostupné, pokles hematokritu (Hct) o 15 %.
Fatální: Krvácivá příhoda, která přímo vede ke smrti v průběhu 7 dnů.
ICH: Intrakraniální krvácení.
Jiné TIMI velké: Nefatální non-ICH TIMI velké krvácení.
TIMI malé: Klinicky zjevné s poklesem hemoglobinu o 30-50 g/l.
TIMI vyžadující lékařskou pozornost: Vyžadující intervenci, nebo vedoucí k hospitalizaci, nebo urychlené vyhodnocení.
PLATO velké fatální/život ohrožující: Fatální krvácení, nebo intrakraniální krvácení, nebo intraperikardiální nebo s tamponádou srdce, nebo hypovolemickým šokem nebo závažnou hypotenzí vyžadující podání vasopresorů/inotropních látek nebo operaci nebo klinicky zjevné krvácení s poklesem hemoglobinu o 30-50 g/l nebo podání >4 transfuzí červených krvinek.
PLATO velké jiné: Významně omezující, nebo klinicky zjevné krvácení s poklesem hemoglobinu o 30-50 g/l, nebo podání 2-3 transfuzí červených krvinek.
PLATO malé: Vyžadující lékařskou intervenci k zastavení nebo léčbě krvácení.
Ve studii PEGASUS bylo TIMI velké krvácení častější u takagreloru 60 mg dvakrát denně než u samotné ASA. Nebylo pozorováno vyšší riziko fatálních krvácení a byl pozorován pouze mírný vzestup intrakraniálních krvácení ve srovnání se samotnou ASA. Ve studii bylo pouze několik fatálních krvácivých příhod, 11 (0,3 %) u tikagreloru 60 mg a 12 (0,3 %) u samotné ASA. Pozorované zvýšené riziko TIMI velkých krvácení u tikagreloru 60 mg bylo způsobeno primárně vyšší četností jiných TIMI velkých krvácení, zvláště příhodami v gastrointestinálním traktu.
Zvýšený charakter krvácení podobný TIMI velké byl pozorován v kategoriích krvácení TIMI velké nebo malé a PLATO velké a PLATO velké nebo malé (viz Tabulka 3). Přerušení léčby jako důsledek krvácení bylo častější u tikagreloru 60 mg ve srovnání se samotnou ASA (6,2 %, resp. 1,5 %). Vetšina těchto krvácení nižší závažnosti (klasifikované jako TIMI vyžadující lékařskou pozornost), např. epistaxe, tvorba modřin a hematomů.
Profil krvácení u tikagreloru 60 mg byl konzistentní v předem definovaných podskupinách (např. podle věku, pohlaví, tělesné hmotnosti, rasy, geografické příslušnosti, souběžných podmínek, souběžné léčby a lékařské anamnézy) pro TIMI velké, TIMI velké nebo malé a PLATO velké krvácivé příhody.
Intrakraniální krvácení: Intrakraniální krvácení (ICH) bylo hlášeno s podobnou četností u tikagreloru 60 mg a samotné ASA (n = 13, 0,2 % v obou léčebných skupinách). Traumatické a chirurgické ICH vykázalo mírné zvýšení u léčby tikagrelorem 60 mg (n = 15, 0,2 %) ve srovnání se samotnou ASA (n = 10, 0,1 %). U tikagreloru 60 mg bylo 6 fatálních ICH a u ASA samotné 5 fatálních ICH. Výskyt intrakraniálního krvácení byl v obou skupinách nízký s ohledem na významné komorbidity a CV rizikové faktory ve studijní populaci.
Dusnost
U pacientů léčených přípravkem Brilique byla hlášena dušnost a pocit tíže na hrudi. Nežádoucí příhody (AEs) zahrnuté pod pojem dušnost (dušnost, klidová dušnost, dušnost při fyzické námaze, paroxysmální noční dušnost a noční dušnost) byly ve studii PLATO hlášeny u 13,8 % pacientů léčených tikagrelorem a u 7,8 % pacientů léčených klopidogrelem. U 2,2 % pacientů užívajících tikagrelor a u 0,6 % pacientů užívajících klopidogrel ve studii PLATO byla dušnost podle zkoušejícího lékaře v příčinné souvislosti s prováděnou léčbou a několik případů bylo závažných (0,14 % tikagrelor; 0,02 % klopidogrel) (viz bod 4.4). Většina hlášených případů dušnosti byla mírné až střední intenzity a většina byla hlášena jako jednotlivá epizoda brzy po zahájení léčby.
Ve srovnání s klopidogrelem mohou mít pacienti s astmatem/CHOPN léčení tikagrelorem zvýšené riziko vývoje nezávažné dušnosti (3,29 % tikagrelor vs. 0,53 % klopidogrel) a závažné dušnosti (0,38 % tikagrelor vs. 0,00 % klopidogrel). V absolutních číslech je toto riziko vyšší než pro celkovou populaci studie PLATO. U pacientů s anamnézou astmatu a/nebo CHOPN je třeba podávat tikagrelor opatrně (viz bod 4.4).
Asi 30 % epizod odeznělo v průběhu 7 dnů. Do studie PLATO byli zařazováni pacienti s kongestivním srdečním selháním, CHOPN nebo astmatem; tito pacienti a starší pacienti hlásili častěji dušnost. Celkem 0,9 % pacientů na přípravku Brilique přerušilo léčbu studovanou léčivou látkou v důsledku dušnosti ve srovnání s 0,1 % pacientů užívajících klopidogrel. Vyšší výskyt dušnosti ve skupině s přípravkem Brilique není spojen s novým výskytem nebo zhoršením onemocnění plic nebo srdce (viz bod 4.4). Přípravek Brilique neovlivňuje funkční plicní testy.
Ve studii PEGASUS byla dušnost hlášena u 14,2 % pacientů, kterým byl podáván tikagrelor 60 mg dvakrát denně a u 5,5 % pacientů na samotné ASA. Podobně jako v PLATO byla většina hlášených případů dušnosti byla mírné až střední intenzity (viz bod 4.4) Pacienti, kteří hlásili dušnost byli poněkud starší a častěji měli dušnost, CHOPN nebo astma již při vstupu do studie.
Vyšetření
Zvýšení koncentrací kyseliny močové: Koncentrace kyseliny močové v séru se u 22 % pacientů užívajících tikagrelor ve studii PLATO zvýšila na více než horní hranici normy ve srovnání s 13 % pacientů na klopidogrelu. Odpovídající počty ve studii PEGASUS byly 9,1 %, resp. 8,8 %, resp. 5,5 % pro tikagrelor 90 mg, resp. 60 mg, resp. placebo. Střední sérová koncentrace kyseliny močové se zvýšila o přibližně 15 % u tikagreloru ve srovnání s přibližně 7,5 % u klopidogrelu. Po ukončení léčby klesla tato hodnota u tikagreloru na 7 %, ale u klopidogrelu nebyl pozorován pokles. Ve studii PEGASUS byl u tikagreloru zjištěn reverzibilní vzestup střední sérové koncentrace kyseliny močové o 6,3 %, resp. 5,6 % ve srovnání s 1,5 % v placebové skupině. Ve studii PLATO byly hlášeny nežádoucí příhody dnavé artritidy u 0,2 % případů u tikagreloru a u 0,1 % u klopidogrelu. Odpovídající počty dny/dnavé artritidy ve studii PEGASUS byly 1,6 %, resp. 1,5 %, resp. 1,1 % u tikagreloru 90 mg, resp. 60 mg, resp. placeba.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Tikagrelor je dobře tolerován v jednotlivých dávkách až 900 mg. Ve studii se zvyšujícími se jednotlivými dávkami byla limitujícím faktorem dávky gastrointestinální toxicita. Dalšími klinicky významnými nežádoucími účinky, které se mohou objevit při předávkování je dušnost a komorové pauzy (viz bod 4.8).
V případě předávkování se mohou objevit výše uvedené potenciální nežádoucí účinky a je nutné uvažovat o monitorování EKG.
V současné době není známo antidotum účinků tikagreloru a nepředpokládá se, že tikagrelor lze odstranit dialýzou (viz bod 4.4). Léčba předávkování má zahrnovat standardní postupy místní lékařské praxe. Očekávaným účinkem při předávkování tikagrelorem je riziko dlouhodobějšího krvácení spojeného s inhibicí krevních destiček. Pokud dojde ke krvácení, je třeba zahájit standardní podpůrnou léčbu.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antiagregancia kromě heparinu,
ATC kód: B01AC24
Mechanismus účinku
Přípravek Brilique obsahuje tikagrelor, který patří chemicky mezi cyklopentyltriazolopyrimidiny (CPTP). Tikagrelor je perorální přímý selektivní reverzibilní antagonista receptoru P2Y12, který brání aktivaci a agregaci destiček závislé na P2Y12 a zprostředkované ADP. Tikagrelor neinteraguje přímo s vazným místem pro ADP, ale pokud je navázán na receptor P2Y12, brání ADP-indukované signální transdukci. Vzhledem ktomu, že se destičky podílí na spouštění a/nebo vývoji trombotických komplikací aterosklerózy, bylo prokázáno, že inhibice funkce destiček má za následek snížení rizika CV příhod jako je smrt, IM nebo cévní mozková příhoda.
Tikagrelor též zvyšuje lokální hladiny endogenního adenosinu inhibicí rovnovážného nukleosidového transportéru-1 (ENT-1).
Bylo prokázáno, že tikagrelor zesiluje u zdravých lidí a u pacientů s ACS následující účinky indukované adenosinem: vazodilatace (průtok koronárními cévami se zvyšuje u zdravých dobrovolníků a pacientů s ACS; bolest hlavy), inhibice funkce krevních destiček (v celé lidské krvi in vitro) a dušnost. Ovšem vztah mezi pozorovaným vzestupem adenosinu a klinickými důsledky (např. nemocnost-úmrtnost) nebyl jasně vysvětlen.
Farmakodynamické účinky
Nástup účinku
U pacientů se stabilní koronární arteriální nemocí (CAD) na ASA vykazuje tikagrelor rychlý nástup farmakologického účinku, což bylo demonstrováno průměrnou inhibicí agregace krevních destiček (IPA) v rozsahu asi 41 % 0,5 hodiny po podání iniciální dávky 180 mg tikagreloru, s maximem IPA účinku 89 % 2-4 hodiny po podání a přetrváváním účinku 2-8 hodin. Devadesát procent pacientů vykazovalo konečný rozsah IPA >70 % 2 hodiny po podání.
Odeznění účinku
Pokud je plánován výkon CABG, je riziko krvácení pro tikagrelor vyšší ve srovnání s klopidogrelem, pokud je léčba vysazena v době kratší než 96 hodin do výkonu.
Převod z jiné léčby
Převod z léčby klopidogrelem 75 mg na tikagrelor 90 mg dvakrát denně má za následek absolutní vzestup IPA o 26,4 % a převod z tikagreloru na klopidogrel má za následek pokles absolutní hodnoty IPA o 24,5 %. Pacienti mohou být převedeni z klopidogrelu na tikagrelor bez ztráty antiagregačního účinku (viz bod 4.2).
Klinická účinnost a bezpečnost
Klinické důkazy účinnosti a bezpečnosti tikagreloru byly získány ve dvou klinických studiích fáze 3:
• Studii PLATO [PLATelet Inhibition and Patient Outcomes], srovnání léčby tikagrelorem a klopidogrelem, oba podávané v kombinaci s ASA a jinou standardní léčbou.
• Studii PEGASUS TIMI-54 [PrEvention with TicaGrelor of SecondAry Thrombotic Events in High-RiSk AcUte Coronary Syndrome Patients], srovnání léčby tikagrelorem v kombinaci s ASA se samotnou ASA.
Studie PLATO (Akutní koronární syndrom)
Ve studii PLATO bylo zařazeno 18 624 pacientů, kteří byli v průběhu 24 hodin od nástupu symptomů nestabilní anginy pectoris (UA), infarktu myokardu bez elevace úseku ST (NSTEMI) nebo infarktu myokardu s elevací úseku ST (STEMI) přijati a ošetřeni medikamentózně, nebo u nich byla provedena perkutánní koronární intervence (PCI), nebo CABG.
Klinická účinnost
Při denní dávce ASA prokázal tikagrelor 90 mg dvakrát denně lepší výsledky než klopidogrel 75 mg denně v prevenci složeného cílového parametru CV smrti, IM nebo cévní mozkové příhody, s tím, že rozdíl byl hlavně u CV smrti a IM. Pacientům byla podána iniciální dávka 300 mg klopidogrelu (až 600 mg, pokud měli PCI) nebo 180 mg tikagreloru.
Tento rozdíl byl zaznamenán časně (absolutní snížení rizika [ARR] 0,6 % a relativní snížení rizika [RRR] o 12 % po 30 dnech) a léčebný efekt byl konstantní po celou dobu 12 měsíců, vedoucí k ARR
1,9 % za rok a RRR o 16 %. Tyto výsledky předpokládají, že je vhodné pacienty léčit tikagrelorem 90 mg dvakrát denně po dobu 12 měsíců (viz bod 4.2). Léčba 54 pacientů s ACS tikagrelorem namísto klopidogrelem vede k prevenci 1 aterotrombotické příhody; léčba 91 pacientů vede k prevenci 1 CV smrti (viz Obrázek 1 a Tabulka 4).
Lepší léčebný efekt tikagreloru ve srovnání s klopidogrelem je konzistentní v mnoha podskupinách, včetně tělesné hmotnosti; pohlaví; lékařské anamnézy diabetes mellitus, tranzitorní ischemické ataky nebo nehemorhagické cévní mozkové příhody, nebo revaskularizace; souběžně podávaných léčiv zahrnujících hepariny, GpIIb/nIa inhibitory a inhibitory protonové pumpy (viz bod 4.5); konečné diagnózy příhody (STEMI, NSTEMI nebo UA); a léčebné taktiky sledované při randomizaci (invazivní nebo farmakologická).
Slabě významná léčebná interakce byla pozorována s regionem, kde poměr rizik (HR) pro primární cílový parametr upřednostňuje tikagrelor mimo severní Ameriku, ale klopidogrel v severní Americe, což reprezentuje přibližně 10 % celkové studované populace (hodnota p = 0,045 pro tuto interakci).
Exploratorní analýza předpokládá možný vztah mezi dávkou ASA takového charakteru, že byla pozorována snížená účinnost tikagreloru se zvyšující se dávkou ASA. Dlouhodobá denní dávka ASA podávaná spolu s přípravkem Brilique má být 75-150 mg (viz body 4.2 a 4.4).
Obrázek 1 ukazuje odhadované riziko do výskytu jakékoliv příhody ve složeném primárním cílovém parametru účinnosti.
Obrázek 1 Analýza primárního složeného cílového parametru CV smrti, IM a cévní mozkové příhody (PLATO)
|
tikagrelor (T) |
[864/9333] |
|
klopidogrel (C) |
[1014/9291] |
„----11 6 7%
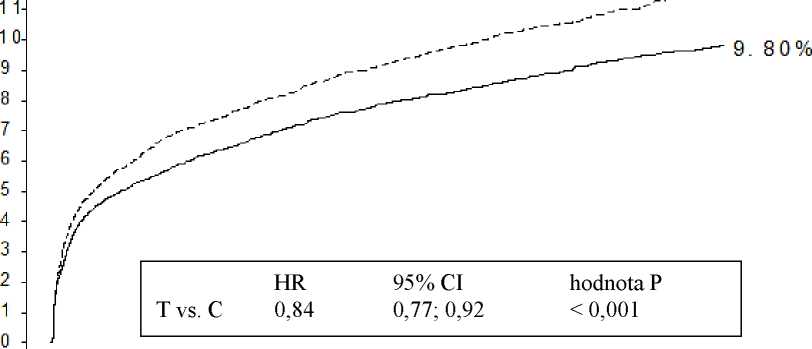
O 60 120 180 240 300 360
N at risk
Dny od randomizace
9333 8628 8460 8219 6743
9291 8521 8362 8124 6650
5161
5096
4147
4074
Tikagrelor snižoval výskyt primárního složeného cílového parametru ve srovnání s klopidogrelem jak v populaci UA/NSTEMI, tak STEMI (Tabulka 4). Přípravek Brilique 90 mg dvakrát denně v kombinaci s nízkou dávkou ASA lze použít u pacientů s ACS (nestabilní anginou pectoris, s infarktem myokardu bez-ST elevace [NSTEMI] nebo s infarktem myokardu s elevací ST [STEMI]); včetně pacientů léčených a pacientů, kteří byli ošetřeni perkutánní koronární intervencí (PCI) nebo kterým byl voperován koronární arteriální by-pass (CABG).
Tabulka 4 Analýza primárních a sekundárních cílových parametrů (PLATO)
|
Tikagrelor 90 mg dvakrát denně (% pacientů s příhodou) N = 9333 |
Klopidogrel 75 mg jednou denně (% pacientů s příhodou) N = 9291 |
ARRa (%/rok) |
RRRa (%) (95% CI) |
p-hodnota | |
|
CV smrt, IM (kromě němého IM) nebo cévní mozková příhoda |
9,3 |
10,9 |
1,9 |
16 (8 ; 23) |
0,0003 |
|
Invazivní taktika |
8,5 |
10,0 |
1,7 |
16 (6; 25) |
0,0025 |
|
Neinvazivní taktika |
11,3 |
13,2 |
2,3 |
15 (0,3; 27) |
0,0444d |
|
CV smrt |
3,8 |
4,8 |
1,1 |
21 (9 ; 31) |
0,0013 |
|
IM (kromě němého IM)b |
5,4 |
6,4 |
1,1 |
16 (5; 25) |
0,0045 |
|
Cévní mozková příhoda |
1,3 |
1,1 |
-0,2 |
-17(-52; 9) |
0,2249 |
|
Smrt ze všech příčin, IM (kromě němého |
ARR = absolutní snížení rizika; RRR = relativní snížení rizika = (1 - poměr rizik) x 100 %. Záporná hodnota RRR ukazuje na zvýšení relativního rizika. kromě němého IM.
a
b
c
d
|
IM) nebo cévní mozkové příhody |
9,7 |
11,5 |
2,1 |
16 (8; 23) |
0,0001 |
|
CV smrt, celkem IM, cévní mozková příhoda, SRI, RI, TIA nebo jiné ATEc |
13,8 |
15,7 |
2,1 |
12 (5; 19) |
0,0006 |
|
Úmrtnost ze všech příčin |
4,3 |
5,4 |
1,4 |
22 (11; 31) |
0,0003d |
|
Trombóza do definitivního stentu |
1,2 |
1,7 |
0,6 |
32 (8; 49) |
0012? |
SRI = závažná rekurentní ischemie; RI = rekurentní ischemie; TIA = tranzitorní ischemická ataka; ATE = arteriální trombotická příhoda. Celkem IM zahrnuje němý IM, kde datum příhody je uveden jako datum, kdy byl odhalen.
nominální hodnota významnosti; všechny ostatní jsou formálně statisticky významné podle předdefinovaného hierarchického testování.
PLATO genetická podstudie
Genotypizace CYP2C19 a ABCB1 u 10285 pacientů ve studii PLATO poskytuje asociaci mezi genotypem a výsledky studie PLATO. Vyšší účinnost tikagreloru ve srovnání s klopidogrelem na snížení CV příhod nebyla významně ovlivněna CYP2C19 u pacientů s genotypem ABCB1. Podobně jako v celé studii PLATO, se neliší velká krvácení PLATO celkem mezi tikagrelorem a klopidogrelem bez ohledu na CYP2C19 nebo ABCB1 genotyp. Velká non-CABG krvácení PLATO byla u pacientů s jednou nebo více chybějícími funkčními alelami CYP2C19 zvýšena u tikagreloru ve srovnání s klopidogrelem, ale byla podobná jako u klopidogrelu u pacientů bez ztracených funkčních alel.
Souhrnný kombinovaný _parametr účinnosti a bezpečnosti
Souhrnný kombinovaný parametr účinnosti a bezpečnosti (CV smrt, IM, cévní mozková příhoda, nebo „celkem velké“ krvácení definované podle PLATO) ukazuje, že celkově lepší účinnost tikagreloru ve srovnání s klopidogrelem není negována velkými krvácivými příhodami (ARR 1,4 %; RRR 8 %; HR 0,92; p = 0,0257) po dobu 12 měsíců po ACS.
Klinická bezpečnost Podstudie Holter
V průběhu studie PLATO řešitelé prováděli u podskupiny téměř 3000 pacientů Holterovo monitorování všech komorových pauz a jiných arytmií. U přibližně 2000 pacientů bylo monitorování provedeno v akutní fázi ACS a po jednom měsíci. Primární sledovaným parametrem byl výskyt komorových pauz > 3 sekundy. V akutní fázi mělo komorové pauzy více pacientů na tikagreloru (6,0 %) než na klopidogrelu (3,5 %), po jednom měsíci 2,2 %, resp. 1,6 % (viz bod 4.4). Zvýšení počtu komorových pauz v akutní fázi ACS bylo více vyznačeno u pacientů na tikagreloru s anamnézou chronického srdečního selhání (9,2 % vs. 5,4 % u pacientů bez této anamnézy; u pacientů na klopidogrelu 4,0 % s anamnézou chronického srdečního selhání vs. 3,6 % u pacientů bez této anamnézy). Tato nerovnováha se neprojevila po jednom měsíci: 2,0 % vs. 2,1 % pro pacienty na tikagreloru s- resp. bez anamnézy chronického srdečního selhání; 3,8 % vs. 1,4 % u klopidogrelu. Nebyly zaznamenány žádné nežádoucí klinické následky spojené s touto nerovnováhou (včetně voperování kardiostimulátoru) u této populace pacientů.
Studie PEGASUS (anamnéza infarktu myokardu)
Studie PEGASUS TIMI-54 byla „event.-driven“ randomizovaná dvojitě zaslepená placebem kontrolovaná mezinárodní multicentrická klinická studie v paralelních skupinách, která zařadila 21162 pacientů. Hodnotila prevenci aterotrombotických příhod tikagrelorem ve dvou dávkách (90 mg dvakrát denně nebo 60 mg dvakrát denně) v kombinaci s nízkou dávkou ASA (75-150 mg) ve srovnání se samotnou ASA u pacientů s anamnézou IM a dalších rizikových faktorů aterotrombózy.
Pacienti vhodní k zařazení do studie byli ve věku 50 let a starší, s anamnézou IM (1 až 3 roky před randomizací) a nejméně jedním z následujících rizikových faktorů aterotrombózy: věk > 65 let, diabetes mellitus vyžadující farmakologickou léčbu, anamnéza druhého dřívějšího IM, průkaz vícečetného postižení CAD nebo chronická renální dysfunkce v konečném stádiu.
Pacienti nebyli vhodní pro zařazení do studie, pokud u nich bylo plánováno nasazení antagonistů P2Y12 receptoru, dipyridamolu, cilostazolu nebo antikoagulační léčby v průběhu studijního období; pokud měli poruchu krvácení nebo ischemickou cévní mozkovou příhodu nebo intrakraniální krvácení v anamnéze, nádor centrální nervové soustavy, nebo abnormalitu intrakraniálních cév, pokud krváceli z gastrointestinálního traktu v uplynulých 6 měsících nebo podstoupili chirurgický výkon v posledních 30 dnech.
Obrázek 2 Analýza primárních klinických složených cílových parametrů CV smrti, IM a cévní mozkové příhody (PEGASUS)
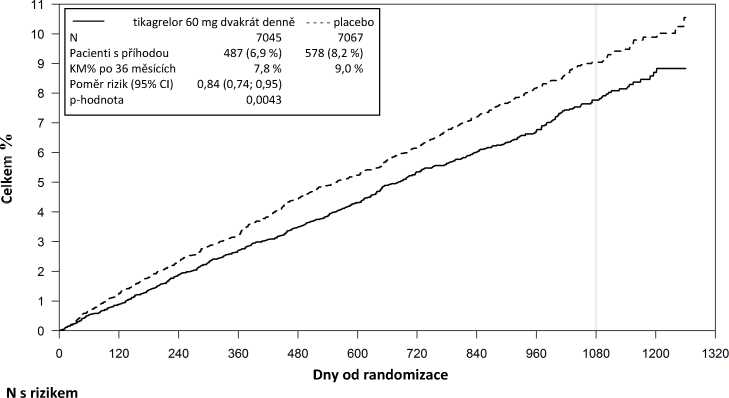
Ti 60 mg 7045 6948 6857
Placebo 7067 6950 6842
6784
6761
6711 6357 5904 4926
6658 6315 5876 4899
3698 2055 710
3646 2028 714
Tabulka 5 Analýza primárních a sekundárních cílových parametrů účinnosti (PEGASUS)
|
Tikagrelor 60 mg dvakrát denně +ASA N = 7045 |
Samotná ASA N = 7067 |
p-hodnota | ||||
|
Charakteristika |
Patienti s příhodou |
KM % |
HR (95% CI) |
Patienti s příhodou |
KM % | |
|
Primární cílový parametr | ||||||
|
Složený parametr CV smrti/IM /cévní mozkové příhody |
487 (6,9 %) |
7,8 % |
0,84 (0,74; 0,95) |
578 (8,2 %) |
9,0 % |
0,0043 (s) |
|
CV smrt |
174 (2,5 %) |
2,9 % |
0,83 (0,68; 1,01) |
210 (3,0%) |
3,4 % |
0,0676 |
|
IM |
285 (4,0 %) |
4,5 % |
0,84 (0,72; 0,98) |
338 (4,8%) |
5,2 % |
0,0314 |
|
Cévní mozková příhoda |
91 (1,3 %) |
1,5 % |
0,75 (0,57; 0,98) |
122 (1,7%) |
1,9 % |
0,0337 |
|
Tikagrelor 60 mg dvakrát denně +ASA N = 7045 |
Samotná ASA N = 7067 |
p-hodnota | ||||
|
Charakteristika |
Patienti s příhodou |
KM % |
HR (95% CI) |
Patienti s příhodou |
KM % | |
|
Sekundární cílové parametry | ||||||
|
CV smrt |
174 (2,5 %) |
2,9 % |
0,83 (0,68; 1,01) |
210 (3,0%) |
3,4 % |
- |
|
Všechny příčiny úmrtí |
289 (4,1 %) |
4,7 % |
0,89 (0,76; 1,04) |
326 (4,6 %) |
5,2 % |
- |
Poměr rizik a p-hodnota jsou vypočteny odděleně pro tikagrelor vs léčba samotnou ASA za použití Cox modelu proporcionálních rizik s léčebnými skupinami jako jedinou vysvětlující proměnnou.
KM podíl (%) vypočtený pro 36 měsíců.
Poznámka: počet prvních příhod pro komponenty CV smrti, IM a cévní mozkové příhody vyjadřuje aktuální počet prvních příhod pro každou komponentu zvlášť a nepřipočítavají se k počtu příhod ve složeném cílovém parametru
(s) vyjadřuje statistickou významnost.
CI = konfidenční interval; CV = kardiovaskulární; HR = poměr rizik; KM = Kaplan-Meier; IM = infarkt myokardu; N = počet pacientů.
Jak režim tikagrelor 60 mg dvakrát denně, tak 90 mg dvakrát denně v kombinaci s ASA byly výhodnější než samotná ASA v prevenci aterotrombotických příhod (složený cílový parametr: CV smrt, IM a cévní mozková příhoda) s konzistentním léčebným účinkem po celou dobu trvání studie. Tím bylo dosaženo 16% RRR, resp.1,27% ARR pro tikagrelor 60 mg a 15 % RRR, resp. 1,19% ARR pro tikagrelor 90 mg.
Ačkoli byl profil účinnosti 90 mg a 60 mg podobný, existují důkazy, že nižší dávka je lépe tolerována a má lepší bezpečnostní profil ve vztahu k riziku krvácení a dušnosti. Z tohoto důvodu se k prevenci aterotrombotických příhod (CV smrt, IM a cévní mozková příhoda) u pacientů s anamnézou IM a vysokým rizikem vývoje aterotrombotických příhod doporučuje pouze Brilique 60 mg v kombinaci sASA.
Tikagrelor 60 mg dvakrát denně ve srovnání se samotnou ASA snižoval významně primární složený cílový parametr CV smrti, IM a cévní mozkové příhody. Každá z komponent přispívala ke snížení primárního složeného cílového parametru (CV smrt 17% RRR, IM 16% RRR a cévní mozková příhoda 25% RRR).
RRR pro složený cílový parametr v období od 1 do 360 dnů (17% RRR) a od 361 dnů dále (16% RRR) bylo podobné. Existují pouze omezené údaje o účinnosti a bezpečnosti podávání tikagreloru po dobu delší než 3 roky.
Neexistují důkazy o prospěchu tikagreloru (žádné snížení primárního složeného cílového parametru CV smrti, IM a cévné mozkové příhody), pokud byl tikagrelor 60 mg dvakrát denně podáván klinicky stabilním pacientům > 2 roky od IM, nebo více než 1 rok po přerušení předchozí léčby inhibitorem ADP receptoru (viz též bod 4.2).
Klinická bezpečnost
Četnost přerušení léčby tikagrelorem 60 mg dvakrát denně v důsledku krvácení nebo dušnosti byla vyšší u pacientů > 75 let (42 %) než u mladších pacientů (rozmezí: 23-31%) s rozdílem oproti placebu vyšším než 10 % (42 % vs 29 %) u pacientů >75 let.
Pediatrická populace
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s přípravkem Brilique u všech podskupin pediatrické populace ve schválené indikaci (informace o použití u dětí viz bod 4.2).
5.2 Farmakokinetické vlastnosti
Tikagrelor vykazuje lineární farmakokinetiku a expozice tikagreloru a aktivnímu metabolitu tikagreloru (AR-C124910XX) přibližně odpovídá podané dávce až do 1260 mg.
Absorpce
Absorpce tikagreloru je rychlá se střední hodnotou tmax přibližně 1,5 hodiny. Tvorba hlavního metabolitu v plazmě AR-C124910XX (též aktivní) z tikagreloru je rychlá se střední hodnotou tmax přibližně 2,5 hodiny. Po perorálním podání jedné dávky tikagreloru 90 mg nalačno zdravým subjektům je Cmax 529 ng/ml a AUC je 3451 ng.h/ml. Poměr metabolitu a mateřské látky je 0,28 pro Cmax a 0,42 pro AUC. Farmakokinetika tikagreloru a AR-C124910XX pacientům s anamnézou IM byla obecně podobná jako u ACS populace. Na základě populační farmakokinetické analýzy studie PEGASUS byl medián Cmax, resp AUC v rovnovážném stavu po podání tikagreloru 60 mg 391 ng/ml, resp. 3801 ng.h/ml. Pro tikagrelor 90 mg byl medián Cmax, resp. AUC v rovnovážném stavu 627 ng/ml, resp. 6255 ng.h/ml.
Průměrná absolutní hodnota biologické dostupnosti tikagreloru je odhadnuta na 36 %. Příjem stravy s vysokým obsahem tuků vedl k 21% zvýšení AUC tikagreloru a 22% snížení Cmax aktivního metabolitu, ale neměl vliv na Cmax ticagreloru nebo AUC aktivního metabolitu. Tyto malé změny mají pravděpodobně minimální klinické důsledky, a proto lze tikagrelor podávat s jídlem i bez jídla. Tikagrelor i jeho aktivní metabolit jsou substráty pro P-gp.
Tikagrelor podaný perorálně nebo přes nazogastrickou sondu do žaludku jako rozdrcené tablety smísené s vodou, má srovnatelnou biologickou dostupnost jako celé tablety s ohledem na AUC a Cmax pro tikagrelor a aktivní metabolit. Úvodní expozice (0,5 a 1 hodinu po podání) po podání rozdrcených tablet ve směsi s vodou byla vyšší ve srovnání s celými tabletami a s celkově stejným koncentračním profilem v dalším období (2 až 48 hodin).
Distribuce
Distribuční objem tikagreloru v ustáleném stavu je 87,5 l. Tikagrelor a aktivní metabolit jsou z velké části vázány na plazmatické bílkoviny (>99,0 %).
Biotransformace
CYP3A4 je hlavním enzymem zodpovědným za metabolismus tikagreloru, tvorbu aktivního metabolitu a interakce se substráty pro CYP3A4 ve smyslu aktivace až inhibice.
Hlavním metabolitem tikagreloru je AR-C124910XX, který je též aktivní, což bylo potvrzeno v podmínkách in vitro vazbou na destičkový P2YJ2 ADP-receptor. Systémová expozice aktivnímu metabolitu je přibližně 30-40 % expozice tikagreloru.
Eliminace
Hlavní cestou vylučování tikagreloru je eliminace jaterním metabolismem. Pokud je podán radioaktivně značený tikagrelor, vyloučí se průměrně 84 % radioaktivity (57,8 % do stolice, 26,5 % do moči). Z podané dávky se do moči vyloučí méně než 1 % tikagreloru a aktivního metabolitu. Hlavní cestou vylučování aktivního metabolitu je pravděpodobně biliární sekrece. Průměrný tm je přibližně 7 h pro tikagrelor a 8,5 h pro aktivní metabolit.
Zvláštní populace
Starší pacienti
U starších pacientů (> 75 let) byla ve srovnání s mladými pozorována vyšší expozice tikagreloru i aktivnímu metabolitu (přibližně o 25 % pro Cmax i AUC) u pacientů s ACS ve srovnání s mladšími pacienty ve farmakokinetické populační analýze. Tyto rozdíly se nepovažují za klinicky významné (viz bod 4.2).
Pediatrická populace
Tikagrelor nebyl hodnocen u pediatrické populace (viz body 4.2 a 5.1).
Pohlaví
U žen ve srovnání s muži byla pozorována vyšší expozice tikagreloru a aktivnímu metabolitu. Rozdíly se nepovažují za klinicky významné.
Porucha funkce ledvin
U pacientů se závažnou poruchou funkce ledvin (clearance kreatininu <30 ml/min) ve srovnání s pacienty s normální funkcí ledvin byla pozorována o přibližně 20 % nižší expozice tikagreloru a expozice aktivnímu metabolitu byla přibližně o 17 % vyšší (viz bod 4.2).
Porucha funkce jater
U pacientů s mírnou poruchou funkce jater byly hodnoty Cmax, resp. AUC pro tikagrelor o 12 %, resp. 23 % vyšší ve srovnání se zdravými jedinci, avšak IPA účinek tikagreloru byl podobný mezi oběma skupinami. U pacientů s mírnou poruchou funkce ledvin není nutné upravovat dávku. Tikagrelor nebyl studován u pacientů se závažnou poruchou funkce jater a neexistují žádné farmakokinetické údaje u pacientů se středně závažnou poruchou funkce jater. U pacientů, kteří měli střední nebo závažnou elevaci v jednom nebo více jaterních funkčních testech na vstupu byly plazmatické koncentrace tikagreloru v průměru podobné nebo mírně vyšší ve srovnání se subjekty bez elevací. U pacientů s mírnou poruchou funkce jater se nodoporučuje upravovat dávku (viz body 4.2 a 4.4).
Rasa
Pacienti asijského původu mají v průměru o 39 % vyšší biologickou dostupnost ve srovnání s bělošskou populací. Pacienti, kteří se sami identifikují s černou populací mají o 18 % nižší biologickou dostupnost tikagreloru ve srovnání s bělošskou populací. V klinicko-farmakologických studiích byla expozice (Cmax a AUC) japonské populace tikagreloru o přibližně 40 % (20 % po úpravě na tělesnou hmotnost) vyšší ve srovnání s bělošskou populací. Expozice pacientů, kteří se sami identifikovali jako hispánci nebo jihoameričani, byla podobná jako u bělošské populace.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje pro tikagrelor a jeho hlavní metabolit neprokázaly neakceptovatelné riziko nežádoucích účinků pro člověka na základě konvenčních farmakologických studií bezpečnosti, toxikologických studií po jednorázovém a opakovaném podání dávky a hodnocení genotoxického potenciálu.
U několika zvířecích modelů byla pozorována gastrointestinální iritace v rozmezí klinicky relevantních expozic (viz bod 4.8).
Tikagrelor podávaný ve vysokých dávkách samicím laboratorních potkanů vykazoval zvýšený výskyt děložních tumorů (adenokarcinomy) a zvýšený výskyt jaterních adenomů. Pravděpodobným mechanismem vzniku děložních tumorů je hormonální nerovnováha, která může vést ke vzniku nádorů u laboratorních potkanů. Mechanismem pro tvorbu jaterních adenomů je pravděpodobně pro hlodavce specifická enzymová indukce v játrech. Z tohoto důvodu nejsou pozorované kancerogenní účinky pravděpodobně relevantní pro lidi.
U laboratorních potkanů byly pozorovány menší vývojové anomálie po podání dávek toxických pro matku (bezpečnostní poměr 5,1). U králíků bylo pozorováno mírné zpoždění vyzrávání jater a skeletu u plodů po podání vysoké dávky při absenci známek toxicity pro matku (bezpečnostní poměr 4,5).
Studie u laboratorních potkanů a králíků prokázaly reprodukční toxicitu, s mírně sníženým přírůstkem tělesné hmotnosti březích samic a sníženou životaschopností mláďat, sníženou porodní hmotností a zpomaleným růstem. Tikagrelor vyvolával nepravidelné cykly (převážné prodloužené) u samic laboratorních potkanů, ale neovlivnil celkovou plodnost samců a samic laboratorních potkanů. Farmakokinetické studie provedené s radioaktivně značeným tikagrelorem ukázaly, že se mateřská látka i její metabolity vylučují do mléka laboratorních potkanů (viz bod 4.6).
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Jádro tablety Mannitol (E421)
Dihydrát hydrogenfosforečnanu vápenatého Magnesium-stearát (E470b)
Sodná sůl karboxymethylškrobu (typ A)
Hyprolosa (E463)
Potah tablety Mastek
Oxid titaničitý (E171)
Žlutý oxid železitý (E172)
Makrogol 400 Hypromelosa (E464)
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
• Transparentní PVC-PVDC/Al blistr (se symbolem slunce/měsíce) po 10 tabletách; krabičky po 60 tabletách (6 blistrů) a 180 tabletách (18 blistrů).
• Transparentní PVC-PVDC/Al kalendářní blistr (se symbolem slunce/měsíce) po 14 tabletách; krabičky po 14 tabletách (1 blistr), 56 tabletách (4 blistry) a 168 tabletách (12 blistrů).
• Transparentní perforovaný jednodávkový PVC-PVDC/Al blistr po 10 tabletách; krabičky po 100x1 tableta (10 blistrů).
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Žádné zvláštní požadavky na likvidaci. Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
AstraZeneca AB SE-151 85 Sodertálje
Švédsko
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/10/655/001-006
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 3. prosince 2010
Datum posledního prodloužení registrace: 17. července 2015
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
PŘÍLOHA II
A. VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce odpovědného za propouštění šarží
AstraZeneca AB Gartunavagen SE-151 85 Sodertalje Švédsko
AstraZeneca UK Limited Silk Road Business Park Macclesfield, Cheshire, SK10 2NA Velká Británie
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propouštění dané šarže.
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
PŘÍLOHA III
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 60 mg potahované tablety ticagrelorum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna potahovaná tableta obsahuje ticagrelorum 60 mg.
3. SEZNAM POMOCNÝCH LÁTEK
4. LÉKOVÁ FORMA A OBSAH BALENÍ
14 potahovaných tablet 56 potahovaných tablet 60 potahovaných tablet 168 potahovaných tablet 180 potahovaných tablet
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB SE-151 85
Sodertálje
Švédsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/10/655/007 14 potahovaných tablet EU/1/10/655/008 56 potahovaných tablet EU/1/10/655/009 60 potahovaných tablet EU/1/10/655/010 168 potahovaných tablet EU/1/10/655/011 180 potahovaných tablet
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis. 15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
brilique 60 mg
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 60 mg tablety ticagrelorum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
symbol slunce/měsíc
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 60 mg tablety ticagrelorum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
Po Út St Čt Pá So Ne symbol slunce/měsíc
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 90 mg potahované tablety ticagrelorum
2. OBSAH LÉČIVÉ LÁTKY/LÉČIVÝCH LÁTEK
Jedna potahovaná tableta obsahuje ticagrelorum 90 mg.
3. SEZNAM POMOCNÝCH LÁTEK
4. LÉKOVÁ FORMA A OBSAH BALENÍ
14 potahovaných tablet 56 potahovaných tablet 60 potahovaných tablet 100x1 potahovaných tablet 168 potahovaných tablet 180 potahovaných tablet
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Perorální podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB
SE-151 85 Sodertálje Švédsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/10/655/001 60 potahovaných tablet EU/1/10/655/002 180 potahovaných tablet EU/1/10/655/003 14 potahovaných tablet EU/1/10/655/004 56 potahovaných tablet EU/1/10/655/005 168 potahovaných tablet EU/1/10/655/006 100x1 potahovaných tablet
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
brilique 90 mg
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 90 mg tablety ticagrelorum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 90 mg tablety ticagrelorum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
symbol slunce/měsíc
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Brilique 90 mg tablety ticagrelorum
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
AstraZeneca AB
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE <, KÓD DÁRCE A KÓD LÉČIVÉHO PŘÍPRAVKU>
Lot
5. JINÉ
Po Út St Čt Pá So Ne symbol slunce/měsíc
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro uživatele
Brilique 60 mg potahované tablety
ticagrelorum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků v závažné míře, prosím, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Brilique a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Brilique užívat
3. Jak se Brilique užívá
4. Možné nežádoucí účinky
5. Jak Brilique uchovávat
6. Obsah balení a další informace
1. Co je Brilique a k čemu se používá Co je Brilique
Brilique obsahuje léčivou látku nazývanou tikagrelor. Tikagrelor patří do skupiny léčiv označovaných jako protidestičkové léčivé látky.
K čemu se Brilique používá
Přípravek Brilique je v kombinaci s kyselinou acetylsalicylovou (další protidestičková látka) určen k léčbě dospělých pacientů. Přípravek Brilique Vám byl předepsán, neboť jste měl(a):
• Infarkt myokardu déle než před rokem
Přípravek Brilique snižuje pravděpodobnost, že dostanete další srdeční infark /infarkt myokardu) nebo cévní mozkovou příhodu nebo že zemřete na komplikace spojené s postižením srdce nebo krevních cév.
Jak Brilique účinkuje
Brilique působí na buňky označované jako krevní destičky (také označované trombocyty). Tyto velmi malé krevní buňky pomáhají zastavovat krvácení tím, že se shlukují dohromady a vyplní otvor v krevní cévě způsobený pořezáním nebo jiným poraněním.
Krevní destičky se však mohou shlukovat i uvnitř nemocných krevních cév v srdci a mozku. To může být velmi nebezpečné, neboť:
• Tyto shluky/sraženiny mohou zcela zastavit průtok krve, což vyvolá srdeční infarkt (infarkt myokardu) nebo cévní mozkovou příhodu, nebo
• Tyto shluky/sraženiny mohou částečně zastavit průtok krve do srdce, což sníží zásobení srdce krví a může vyvolat bolest na hrudi, která se čas od času vrací (nestabilní angina pectoris).
Brilique zabraňuje vzniku shluků krevních destiček. Tím se snižuje možnost, že dojde ke vzniku krevní sraženiny, která může snížit průtok krve.
Neužívejte Brilique
• Jestliže jste alergický(á) na tikagrelor nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
• Jestliže nyní krvácíte.
• Měl(a) jste cévní mozkovou příhodu způsobenou krvácením do mozku.
• Máte závažnou poruchu funkce jater.
• Užíváte některý z následujích léků:
- ketokonazol (používaný k léčbě plísňových infekcí),
- klaritromycin (používaný k léčbě bakteriálních infekcí),
- nefazodon (antidepresivum)
- ritonavir a atazanavir (používané k léčbě infekce HIV a AIDS).
Neužívejte Brilique, pokud se některá z výše uvedených informací vztahuje právě na Vás. Pokud si nejste jistý(á) poraďte se s lékařem nebo lékárníkem předtím, než začnete tento léčivý přípravek užívat.
Upozornění a opatření
Poraďte se s lékařem, nebo lékárníkem předtím, než začnete užívat Brilique
• Jestliže máte zvýšené riziko krvácení v důsledku:
- nedávného závažného poranění
- nedávného operačního výkonu (včetně zubního zákroku, poraďte se o tom se zubním lékařem)
- komplikací, které ovlivňují srážení krve
- nedávného krvácení do žaludku nebo střeva (např. žaludeční vřed nebo střevní „polypy“)
• Jestliže se chystáte na operační výkon (včetně výkonů u zubaře) kdykoliv v průběhu léčby přípravkem Brilique. Je to dáno tím, že riziko krvácení je zvýšené. Lékař Vám může říci, abyste 7 dnů před chirurgickým zákrokem přerušil(a) léčbu tímto léčivým přípravkem.
• Jestliže máte pomalou srdeční frekvenci (obvykle méně než 60 tepů za minutu) a nemáte voperován přístroj, který řídí srdeční akci (kardiostimulátor).
• Jestliže máte astma nebo jiné plicní onemocnění nebo dýchací obtíže.
• Jestliže jste někdy měl(a) poruchu funkce játer nebo prodělal(a) nemoc, která mohla mít vliv na Vaše játra.
• Jestliže při vyšetření Vaší krve bylo zjištěno, že máte neobvyklé množství kyseliny močové v krvi.
Pokud se výše uvedené informace vztahují právě na Vás, nebo si nejste jistý(á), poraďte se s lékařem, nebo lékárníkem předtím než začnete tento léčivý přípravek užívat.
Děti a dospívající
Brilique se nedoporučuje podávat dětem a dospívajícím do 18 let.
Další léčivé přípravky a Brilique
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné užíval(a) nebo které možná budete užívat. Důvodem je skutečnost, že Brilique může ovlivňovat účinek jiných léčiv a jiná léčiva mohou ovlivňovat Brilique.
Informujte lékaře nebo lékárníka, jestliže užíváte některý z následujících léků:
• simvastatin nebo lovastatin v dávce vyšší než 40 mg denně (léky k léčbě vysoké hladiny cholesterolu)
• rifampicin (antibiotikum),
• fenytoin, karbamazepin a fenobarbital (léky k léčbě křečí),
• digoxin (k léčbě srdečního selhání),
• cyklosporin (k potlačení vlastní imunity),
• chinidin a diltiazem (k léčbě poruch srdečního rytmu),
• betablokátory a verapamil (k léčbě vysokého krevního tlaku).
Nezapomeňte informovat lékaře nebo lékárníka zejména o užívání následujích léků, které zvyšují riziko krvácení:
• „léky tlumící krevní srážlivost podávané ústy“ často označované jako léky na ředění krve zahrnující warfarin.
• nesteroidní protozánětlivé léky (ve zkratce NSAID) často užívané k odstranění bolesti, např. ibuprofen a naproxen.
• selektivní blokátory zpětného vychytávání serotoninu (ve zkratce SSRI) užívané k léčbě deprese, např. paroxetin, sertralin a citalopram.
• jiné léky, např. ketokonazol (používaný k léčbě plísňových infekcí), klaritromycin (používaný k léčbě bakteriálních infekcí), nefazodon (antidepresivum), ritonavir a atazanavir (používané k léčbě infekce HIV a AIDS), cisaprid (používaný k léčbě pálení žáhy), námelové alkaloidy (používané k léčbě migrény a bolesti hlavy).
Informujte svého lékaře o tom, že užíváte Brilique, a máte tedy zvýšené riziko krvácení, pokud Vám lékař předepíše fibinolytika, léky, které rozpouštějí krevní sraženiny, např. streptokináza nebo altepláza.
Těhotenství a kojení
Přípravek Brilique se nemá užívat v průběhu těhotenství nebo v době, kdy můžete být těhotná.
V průběhu užívání přípravku Brilique ženy mají používat vhodnou antikoncepci k vyloučení těhotenství.
Poraďte se se svým lékařem dříve, než začnete užívat Brilique, pokud kojíte. Lékař zváží prospěch z léčby a možná rizika při užívání Brilique v tomto období.
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat.
Řízení dopravních prostředků a obsluha strojů
Brilique pravděpodobně neovlivňuje Vaši schopnost řídit a obsluhovat stroje. Buďte opatrní při řízení nebo obsluze strojů, pokud při užívání tohoto léčivého přípravku pociťujete závrať nebo zmatenost.
3. Jak se Brilique užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Kolik tablet užívat
• Obvyklá počáteční dávka je jedna tableta 60 mg dvakrát denně. Pokračujte v užívání přípravku Brilique tak dlouho, jak Vám řekl Váš lékař.
• Tento léčivý přípravek užívejte přibližně ve stejnou denní dobu (např. jednu tabletu ráno a jednu tabletu večer).
Užívání přípravku Brilique s dalším léčivým přípravkem proti srážení krve
Váš lékař Vám obvykle řekne, abyste užíval(a) kyselinu acetylsalicylovou. Tato léčivá látka je obsažena v mnoha lécích určených k prevenci krevního srážení. Váš lékař Vám řekne, jakou dávku máte užívat (obvykle mezi 75-150 mg denně).
Jak užívat Brilique
• Tablety můžete užívat spolu s jídlem nebo bez něj.
• Na blistru si můžete zkontrolovat, kdy jste užil(a) poslední tabletu. Na blistru je vyznačeno slunce (ranní dávka) a měsíc (večerní dávka). Tak si připomenete, kdy jste užil(a) poslední dávku.
Jestliže máte problém s polykáním tablety
Jestliže máte problém s polykáním tablety, můžete ji rozdrtit a smísit s vodou následujícím způsobem:
• Rozdrťte tabletu na jemný prášek
• Nasypte prášek do sklenice naplněné do poloviny vodou
• Zamíchejte a ihned vypijte
• Naplňte sklenici ještě jednou do poloviny vodou a vypijte, abyste užil(a) veškerý léčivý přípravek
Jestliže jste užil(a) více Brilique, než jste měl(a)
Jestliže jste užil(a) více přípravku Brilique než Vám bylo předepsáno, obraťte se na lékaře nebo jděte přímo do nemocnice. V tomto případě si vezměte Brilique s sebou. Riziko krvácení může být zvýšené.
Jestliže jste zapomněl(a) užít Brilique
• Jestliže jste zapomněl(a) užít pravidelnou dávku, užijte až další dávku.
• Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste přestal(a) užívat Brilique
Nepřestávejte užívat Brilique bez vědomí lékaře. Užívejte tento léčivý přípravek pravidelně po celou dobu, kdy Vám lékař bude Brilique předepisovat. Pokud přestanete užívat Brilique, může se zvýšit riziko dalšího srdečního infarktu nebo cévní mozkové příhody nebo smrti v důsledku onemocnění srdce nebo cév.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. U tohoto přípravku se mohou objevit následující nežádoucí účinky.
Brilique ovlivňuje srážení krve, takže většina nežádoucích účinků souvisí s krvácením. Krvácení se může objevit v kterékoli části těla. Některá krvácení jsou běžná (jako je tvorba modřin nebo krvácení z nosu). Závažná krvácení nejsou běžná, ale mohou být život ohrožující.
Navštivte ihned lékaře, pokud se objeví následující nežádoucí účinky - můžete potřebovat rychlou lékařskou pomoc:
• Krvácení do mozku nebo nitrolební krvácení je méně častým nežádoucím účinkem a může se projevovat známkami cévní mozkové příhody (mrtvice), např.:
- náhlá necitlivost nebo slabost v pažích, nohách nebo obličeji, zvláště, pokud je postižena pouze polovina těla
- náhlá zmatenost, obtíže při mluvení nebo porozumění jiným lidem
- náhlé obtíže při chůzi nebo ztráta rovnováhy nebo koordinace
- náhlý pocit závratí nebo náhlá silná bolest hlavy z neznámých příčin
• Známky krvácení jako je:
- silné krvácení nebo krvácení, které nemůžete zvládnout
- neočekávané krvácení nebo krvácení, které trvá dlouho
- růžová, červená nebo hnědá moč
- zvracení červené krve nebo zvratky, které se podobají „kávové sedlině“
- červená nebo černá stolice (vypadá jako tmavá mazlavá hmota)
- vykašlávání krve nebo zvracení krevní sraženiny
• mdloba (synkopa)
- dočasná ztráta vědomí v důsledku náhlého poklesu toku krve do mozku (časté)
Poraďte se se svým lékařem, pokud máte:
• Pocit dusnosti - tento nežádoucí účinek je velmi častý. Může to být v důsledku onemocnění Vašeho srdce nebo z jiných příčin, nebo může jít o nežádoucí účinek Brilique. Dušnost
v důsledku užívání Brilique je obecně mírná a lze ji charakterizovat jako náhlý, neočekávaný nedostatek vzduchu, který se obvykle objeví v klidu a může se objevit v prvních týdnech léčby a u mnohých pacientů zcela vymizí. Pokud se dušnost zhoršuje nebo trvá delší dobu, řekněte to Vašemu lékaři. Lékař rozhodne o tom, zda je třeba dušnost léčit nebo provede potřebná vyšetření.
Další možné nežádoucí účinky
Velmi časté (mohou postihnout více než 1 z 10 pacientů)
• Vysoká hladina kyseliny močové ve Vaší krvi (prokázaná při vyšetření)
• Krvácení způsobené poruchou krve
Časté (mohou postihnout až 1 z 10 pacientů)
• Tvorba modřin
• Bolest hlavy
• Pocit závratě nebo pocit točícího se prostoru
• Průjem nebo nechutenství
• Pocit na zvracení (nauzea)
• Zácpa
• Vyrážka na kůži
• Svědění kůže
• Silná bolest a otk kloubů - to jsou známky dny
• Pociť závratě nebo obluzení, nebo neostré vidění - to jsou známky nízkého krevního tlaku
• Krvácení z nosu
• Krvácení po chirurgickém výkonu nebo z řezných ran (např. při holení) či poranění je větší než obvykle
• Krvácení ze žaludeční sliznice (vřed)
• Krvácení z dásní
Méně časté (mohou postihnout až 1 ze 100 pacientů)
• Alergická reakce - možnými známkami alergické reakce mohou být vyrážka, svědění kůže nebo otok obličeje nebo rtů/jazyka
• Zmatenost
• Problémy s viděním v důsledku krve ve Vašem oku
• Krvácení z pochvy, které je silnější, nebo se dostaví v jinou než obvyklou dobu pro menstruační krvácení
• Krvácení do kloubů a svalů, které způsobuje bolestivé otoky
• Krvácení do ucha
• Vnitřní krvácení, které může vyvolat závrať nebo pocit točící se hlavy Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na blistru nebo krabičce za EXP (zkratka používaná pro dobu použitelnosti). Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co Brilique obsahuje
• Léčivou látkou je ticagrelorum (tikagrelor). Jedna potahovaná tableta obsahuje ticagrelorum 60 mg.
• Dalšími složkami jsou:
Jádro tablety: mannitol (E421), dihydrát hydrogenfosforečnanu vápenatého, sodná sůl karboxymethylškrobu typu A, hyprolosa (E463), magnesium-stearát (E470b).
Potah tablety: hypromelosa (E464), oxid titaničitý (E171), makrogol 400, černý oxid železitý (E172) a červený oxid železitý (E172).
Jak Brilique vypadá a co obsahuje toto balení
Potahovaná tableta (tableta): Tableta je kulatá bikonvexní růžová potahovaná a na jedné straně je označena „60“ nad „T“.
Brilique se dodává v:
• standardních blistrech (se symboly slunce/měsíce) v krabičce po 60 a 180 tabletách.
• kalendářních blistrech (se symboly slunce/měsíce) v krabičce po 14, 56 a 168 tabletách.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
Držitel rozhodnutí o registraci:
AstraZeneca AB SE-151 85 Sodertalje Švédsko
Výrobce:
AstraZeneca AB Gartunavagen SE-151 85 Sodertalje Švédsko
Výrobce:
AstraZeneca UK Limited Silk Road Business Park Maccelsfield, Cheshire, SK10 2NA Velká Británie
|
Další informace o tomto přípravku získáte |
u místního zástupce držitele rozhodnutí o registraci: |
|
Belgie/Belgique/Belgien AstraZeneca S.A./N.V. Tel: +32 2 370 48 11 |
Lietuva UAB AstraZeneca Lietuva Tel: +370 5 2660550 |
|
Btarapna Acrpa3eHeKa Etarapna EOOfl Tea.: +359 2 44 55 000 |
Luxembourg/Luxemburg AstraZeneca S.A./N.V. Tél/Tel: + 32 2 370 48 11 |
|
Česká republika AstraZeneca Czech Republic s.r.o Tel: +420 222 807 111 |
Magyarország AstraZeneca Kft. Tel.: + 36 1 883 6500 |
|
Danmark AstraZeneca A/S Tlf: +45 43 66 64 62 |
Malta Associated Drug Co. Ltd Tel: + 356 2277 8000 |
|
Deutschland AstraZeneca GmbH Tel: + 49 41 03 7080 |
Nederland AstraZeneca BV Tel: +31 79 363 2222 |
|
Eesti AstraZeneca Tel: +372 654 9 6 00 |
Norge AstraZeneca AS Tlf: + 47 21 00 64 00 |
|
EXláSa AstraZeneca A.E. T^: + 30 2 10 68 71 500 |
Osterreich AstraZeneca Osterreich GmbH Tel: +43 1 711 31 0 |
|
Espaňa AstraZeneca Farmacéutica Spain, S.A. Tel: + 34 91 301 91 00 |
Polska AstraZeneca Pharma Poland Sp. z o.o. Tel.: + 48 22 245 73 00 |
|
France AstraZeneca Tél: + 33 1 41 29 40 00 |
Portugal AstraZeneca Produtos Farmaceuticos, Lda. Tel: + 351 21 434 61 00 |
|
Hrvatska AstraZeneca d.o.o. Tel: +385 1 4628 000 |
Románia AstraZeneca Pharma SRL Tel: + 40 21 317 60 41 |
|
Ireland AstraZeneca Pharmaceuticals (Ireland) Ltd Tel: + 353 1 609 7100 |
Slovenija AstraZeneca UK Limited Tel: + 386 1 51 35 600 |
|
Ísland Vistor hf. Sími: + 354 535 7000 |
Slovenská republika AstraZeneca AB, o.z. Tel: + 421 2 5737 7777 |
|
Italia |
Suomi/Finland |
AstraZeneca S.p.A.
Tel: + 39 02 98011
Kúrcpog
A^skt^p Oap^aKeuxiKq AtS Tr^: +357 22490305
Latvija
SIA AstraZeneca Latvija Tel: + 371 67377 100
AstraZeneca Oy Puh/Tel: + 358 10 23 010
Sverige
AstraZeneca AB Tel: +46 8 553 26 000
United Kingdom
AstraZeneca UK Ltd Tel: + 44 1582 836 836
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
Příbalová informace: informace pro uživatele
Brilique 90 mg potahované tablety
ticagrelorum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek užívat,
protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře nebo lékárníka.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků v závažné míře, prosím, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Brilique a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Brilique užívat
3. Jak se Brilique užívá
4. Možné nežádoucí účinky
5. Jak Brilique uchovávat
6. Obsah balení a další informace
1. Co je Brilique a k čemu se používá Co je Brilique
Brilique obsahuje léčivou látku nazývanou tikagrelor. Tikagrelor patří do skupiny léčiv označovaných jako protidestičkové léčivé látky.
K čemu se Brilique používá
Přípravek Brilique je v kombinaci s kyselinou acetylsalicylovou (další protidestičková látka) určen k léčbě dospělých pacientů. Přípravek Brilique Vám byl předepsán, neboť jste měl(a):
• Infarkt myokardu nebo
• Nestabilní angina pectoris (bolest na prsou, která není dobře kontrolována)
Přípravek Brilique snižuje pravděpodobnost, že dostanete další srdeční infarkt /infarkt myokardu) nebo cévní mozkovou příhodu nebo že zemřete na komplikace spojené s postižením srdce nebo krevních cév.
Jak Brilique účinkuje
Brilique působí na buňky označované jako krevní destičky (také označované trombocyty). Tyto velmi malé krevní buňky pomáhají zastavovat krvácení tím, že se shlukují dohromady a vyplní otvor v krevní cévě způsobený pořezáním nebo jiným poraněním.
Krevní destičky se však mohou shlukovat i uvnitř nemocných krevních cév v srdci a mozku. To může být velmi nebezpečné, neboť:
• Tyto shluky/sraženiny mohou zcela zastavit průtok krve, což vyvolá srdeční infarkt (infarkt myokardu) nebo cévní mozkovou příhodu, nebo
• Tyto shluky/sraženiny mohou částečně zastavit průtok krve do srdce, což sníží zásobení srdce krví a může vyvolat bolest na hrudi, která se čas od času vrací (nestabilní angina pectoris).
Brilique zabraňuje vzniku shluků krevních destiček. Tím se snižuje možnost, že dojde ke vzniku krevní sraženiny, která může snížit průtok krve.
2. Čemu musíte věnovat pozornost, než začnete Brilique užívat.
Neužívejte Brilique
• Jestliže jste alergický(á) na tikagrelor nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
• Jestliže nyní krvácíte.
• Měl(a) jste cévní mozkovou příhodu způsobenou krvácením do mozku.
• Máte závažnou poruchu funkce jater.
• Užíváte některý z následujích léků:
- ketokonazol (používaný k léčbě plísňových infekcí),
- klaritromycin (používaný k léčbě bakteriálních infekcí),
- nefazodon (antidepresivum)
- ritonavir a atazanavir (používané k léčbě infekce HIV a AIDS).
Neužívejte Brilique, pokud se některá z výše uvedených informací vztahuje právě na Vás. Pokud si nejste jistý(á) poraďte se s lékařem nebo lékárníkem předtím, než začnete tento léčivý přípravek užívat.
Upozornění a opatření
Poraďte se s lékařem, nebo lékárníkem předtím, než začnete užívat Brilique
• Jestliže máte zvýšené riziko krvácení v důsledku:
- nedávného závažného poranění
- nedávného operačního výkonu (včetně zubního zákroku, poraďte se o tom se zubním lékařem)
- komplikací, které ovlivňují srážení krve
- nedávného krvácení do žaludku nebo střeva (např. žaludeční vřed nebo střevní „polypy“)
• Jestliže se chystáte na operační výkon (včetně výkonů u zubaře) kdykoliv v průběhu léčby přípravkem Brilique. Je to dáno tím, že riziko krvácení je zvýšené. Lékař Vám může říci, abyste 7 dnů před chirurgickým zákrokem přerušil(a) léčbu tímto léčivým přípravkem.
• Jestliže máte pomalou srdeční frekvenci (obvykle méně než 60 tepů za minutu) a nemáte voperován přístroj, který řídí srdeční akci (kardiostimulátor).
• Jestliže máte astma nebo jiné plicní onemocnění nebo dýchací obtíže.
• Jestliže jste někdy měl(a) poruchu funkce jater nebo prodělal(a) nemoc, která mohla mít vliv na Vaše játra.
• Jestliže při vyšetření Vaší krve bylo zjištěno, že máte neobvyklé množství kyseliny močové v krvi.
Pokud se výše uvedené informace vztahují právě na Vás, nebo si nejste jistý(á), poraďte se s lékařem, nebo lékárníkem předtím než začnete tento léčivý přípravek užívat.
Děti a dospívající
Brilique se nedoporučuje podávat dětem a dospívajícím do 18 let.
Další léčivé přípravky a Brilique
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné užíval(a) nebo které možná budete užívat. Důvodem je skutečnost, že Brilique může ovlivňovat účinek jiných léčiv a jiná léčiva mohou ovlivňovat Brilique.
Informujte lékaře nebo lékárníka, jestliže užíváte některý z následujících léků:
• simvastatin nebo lovastatin v dávce vyšší než 40 mg denně (léky k léčbě vysoké hladiny cholesterolu)
• rifampicin (antibiotikum),
• fenytoin, karbamazepin a fenobarbital (léky k léčbě křečí),
• digoxin (k léčbě srdečního selhání),
• cyklosporin (k potlačení vlastní imunity),
• chinidin a diltiazem (k léčbě poruch srdečního rytmu),
• betablokátory a verapamil (k léčbě vysokého krevního tlaku).
Nezapomeňte informovat lékaře nebo lékárníka zejména o užívání následujích léků, které zvyšují riziko krvácení:
• „léky tlumící krevní srážlivost podávané ústy“ často označované jako léky na ředění krve zahrnující warfarin.
• nesteroidní protozánětlivé léky (ve zkratce NSAID) často užívané k odstranění bolesti, např. ibuprofen a naproxen.
• selektivní blokátory zpětného vychytávání serotoninu (ve zkratce SSRI) užívané k léčbě deprese, např. paroxetin, sertralin a citalopram.
• jiné léky, např. ketokonazol (používaný k léčbě plísňových infekcí), klaritromycin (používaný k léčbě bakteriálních infekcí), nefazodon (antidepresivum), ritonavir a atazanavir (používané k léčbě infekce HIV a AIDS), cisaprid (používaný k léčbě pálení žáhy), námelové alkaloidy (používané k léčbě migrény a bolesti hlavy).
Informujte svého lékaře o tom, že užíváte Brilique, a máte tedy zvýšené riziko krvácení, pokud Vám lékař předepíše fibinolytika, léky, které rozpouštějí krevní sraženiny, např. streptokináza nebo altepláza.
Těhotenství a kojení
Přípravek Brilique nemá užívat v průběhu těhotenství nebo v době, kdy můžete být těhotná. V průběhu užívání přípravku Brilique ženy mají používat vhodnou antikoncepci k vyloučení těhotenství.
Poraďte se se svým lékařem dříve, než začnete užívat Brilique, pokud kojíte. Lékař zváží prospěch z léčby a možná rizika při užívání Brilique v tomto období.
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat.
Řízení dopravních prostředků a obsluha strojů
Brilique pravděpodobně neovlivňuje Vaši schopnost řídit a obsluhovat stroje. Buďte opatrní při řízení nebo obsluze strojů, pokud při užívání tohoto léčivého přípravku pociťujete závrať nebo zmatenost.
3. Jak se Brilique užívá
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Kolik tablet užívat
• Počáteční dávka jsou dvě tablety ve stejnou dobu (nárazová dávka 180 mg). Tuto dávku obvykle dostanete v nemocnici.
• Po této počáteční dávce je obvyklá dávka jedna tableta 90 mg dvakrát denně po dobu až 12 měsíců, pokud Vám lékař neřekne jinak.
• Užívejte tento přípravek přibližně ve stejnou denní dobu (např. jednu tabletu ráno a jednu tabletu večer).
Užívání přípravku Brilique s dalším léčivým přípravkem proti srážení krve
Váš lékař Vám obvykle řekne, abyste užíval(a) kyselinu acetylsalicylovou. Tato léčivá látka je obsažena v mnoha lécích určených k prevenci krevního srážení. Váš lékař Vám řekne, jakou dávku máte užívat (obvykle mezi 75-150 mg denně).
Jak užívat Brilique
• Tablety můžete užívat spolu s jídlem i bez něj.
• Na blistru si můžete zkontrolovat, kdy jste užil(a) poslední tabletu. Na blistru je vyznačeno slunce (ranní dávka) a měsíc (večerní dávka). Tak si připomenete, kdy jste užil(a) poslední dávku.
Jestliže máte problém s polykáním tablety
Jestliže máte problém s polykáním tablety, můžete ji rozdrtit a smísit s vodou následujícím způsobem:
• Rozdrťte tabletu na jemný prášek
• Nasypte prášek do sklenice naplněné do poloviny vodou
• Zamíchejte a ihned vypijte
• Naplňte sklenici ještě jednou do poloviny vodou a vypijte, abyste užil(a) veškerý léčivý přípravek
Jestliže jste užil(a) více Brilique, než jste měl(a)
Jestliže jste užil(a) více přípravku Brilique než Vám bylo předepsáno, obraťte se na lékaře nebo jděte přímo do nemocnice. V tomto případě si vezměte Brilique s sebou. Riziko krvácení může být zvýšené.
Jestliže jste zapomněl(a) užít Brilique
• Jestliže jste zapomněl(a) užít pravidelnou dávku, užijte až další dávku.
• Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste přestal(a) užívat Brilique
Nepřestávejte užívat Brilique bez vědomí lékaře. Užívejte tento léčivý přípravek pravidelně po celou dobu, kdy Vám lékař bude Brilique předepisovat. Pokud přestanete užívat Brilique, může se zvýšit riziko dalšího srdečního infarktu nebo cévní mozkové příhody nebo smrti v důsledku onemocnění srdce nebo cév.
Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. U tohoto přípravku se mohou objevit následující nežádoucí účinky.
Brilique ovlivňuje srážení krve, takže většina nežádoucích účinků souvisí s krvácením. Krvácení se může objevit v kterékoli části těla. Některá krvácení jsou běžná (jako je tvorba modřin nebo krvácení z nosu). Závažná krvácení nejsou běžná, ale mohou být život ohrožující.
Navštivte ihned lékaře, pokud se objeví následující nežádoucí účinky - můžete potřebovat rychlou lékařskou pomoc:
• Krvácení do mozku nebo nitrolební krvácení je méně častým nežádoucím účinkem a může se projevovat známkami cévní mozkové příhody (mrtvice), např.:
- náhlá necitlivost nebo slabost v pažích, nohách nebo obličeji, zvláště, pokud je postižena pouze polovina těla
- náhlá zmatenost, obtíže při mluvení nebo porozumění jiným lidem
- náhlé obtíže při chůzi nebo ztráta rovnováhy nebo koordinace
- náhlý pocit závratí nebo náhlá silná bolest hlavy z neznámých příčin
• Známky krvácení jako je:
- silné krvácení nebo krvácení, které nemůžete zvládnout
- neočekávané krvácení nebo krvácení, které trvá dlouho
- růžová, červená nebo hnědá moč
- zvracení červené krve nebo zvratky, které se podobají „kávové sedlině“
- červená nebo černá stolice (vypadá jako tmavá mazlavá hmota)
- vykašlávání krve nebo zvracení krevní sraženiny
• mdloba (synkopa)
- dočasná ztráta vědomí v důsledku náhlého poklesu toku krve do mozku (časté)
Poraďte se se svým lékařem, pokud máte:
• Pocit dusnosti - tento nežádoucí účinek je velmi častý. Může to být v důsledku onemocnění Vašeho srdce nebo z jiných příčin, nebo může jít o nežádoucí účinek Brilique. Dušnost
v důsledku užívání Brilique je obecně mírná a lze ji charakterizovat jako náhlý, neočekávaný nedostatek vzduchu, který se obvykle objeví v klidu a může se objevit v prvních týdnech léčby a u mnohých pacientů zcela vymizí. Pokud se dušnost zhoršuje nebo trvá delší dobu, řekněte to Vašemu lékaři. Lékař rozhodne o tom, zda je třeba dušnost léčit nebo provede potřebná vyšetření.
Další možné nežádoucí účinky
Velmi časté (mohou postihnout více než 1 z 10 pacientů)
• Vysoká hladina kyseliny močové ve Vaší krvi (prokázaná při vyšetření)
• Krvácení způsobené poruchou krve
Časté (mohou postihnout až 1 z 10 pacientů)
• Tvorba modřin
• Bolest hlavy
• Pocit závratě nebo pocit točícího se prostoru
• Průjem nebo nechutenství
• Pocit na zvracení (nauzea)
• Zácpa
• Vyrážka na kůži
• Svědění kůže
• Silná bolest a otk kloubů - to jsou známky dny
• Pociť závratě nebo obluzení, nebo neostré vidění - to jsou známky nízkého krevního tlaku
• Krvácení z nosu
• Krvácení po chirurgickém výkonu nebo z řezných ran (např. při holení) či poranění je větší než obvykle
• Krvácení ze žaludeční sliznice (vřed)
• Krvácení z dásní
Méně časté (mohou postihnout až 1 ze 100 pacientů)
• Alergická reakce - možnými známkami alergické reakce mohou být vyrážka, svědění kůže nebo otok obličeje nebo rtů/jazyka
• Zmatenost
• Problémy s viděním v důsledku krve ve Vašem oku
• Krvácení z pochvy, které je silnější, nebo se dostaví v jinou než obvyklou dobu pro menstruační krvácení
• Krvácení do kloubů a svalů, které způsobuje bolestivé otoky
• Krvácení do ucha
• Vnitřní krvácení, které může vyvolat závrať nebo pocit točící se hlavy Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Brilique uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na blistru nebo krabičce za EXP (zkratka používaná pro dobu použitelnosti). Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co Brilique obsahuje
• Léčivou látkou je ticagrelorum (tikagrelor). Jedna potahovaná tableta obsahuje ticagrelorum 90 mg.
• Dalšími složkami jsou:
Jádro tablety: mannitol (E421), dihydrát hydrogenfosforečnanu vápenatého, sodná sůl karboxymethylškrobu typu A, hyprolosa (E463), magnesium-stearát (E470b).
Potah tablety: hypromelosa (E464), oxid titaničitý (E171), mastek, makrogol 400, žlutý oxid železitý (E172).
Jak Brilique vypadá a co obsahuje toto balení
Potahovaná tableta (tableta): Tableta je kulatá bikonvexní žlutá potahovaná a na jedné straně je označena „90“ nad „T“.
Brilique se dodává v:
• standardních blistrech (se symboly slunce/měsíce) v krabičce po 60 a 180 tabletách.
• kalendářních blistrech (se symboly slunce/měsíce) v krabičce po 14, 56 a 168 tabletách.
• Perforovaných jednodávkových blistrech v krabičce po 100 x 1 tabletách.
Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
Držitel rozhodnutí o registraci:
AstraZeneca AB SE-151 85 Sodertálje Švédsko
Výrobce: AstraZeneca AB Gártunavágen
SE-151 85 Sodertálje Švédsko
Výrobce:
AstraZeneca UK Limited Silk Road Business Park Maccelsfield, Cheshire, SK10 2NA Velká Británie
|
Další informace o tomto přípravku získáte |
u místního zástupce držitele rozhodnutí o registraci: |
|
Belgie/Belgique/Belgien AstraZeneca S.A./N.V. Tel: +32 2 370 48 11 |
Lietuva UAB AstraZeneca Lietuva Tel: +370 5 2660550 |
|
Btarapna Acrpa3eHeKa Etarapna EOOfl Tea.: +359 2 44 55 000 |
Luxembourg/Luxemburg AstraZeneca S.A./N.V. Tél/Tel: + 32 2 370 48 11 |
|
Česká republika AstraZeneca Czech Republic s.r.o Tel: +420 222 807 111 |
Magyarország AstraZeneca Kft. Tel.: + 36 1 883 6500 |
|
Danmark AstraZeneca A/S Tlf: +45 43 66 64 62 |
Malta Associated Drug Co. Ltd Tel: + 356 2277 8000 |
|
Deutschland AstraZeneca GmbH Tel: + 49 41 03 7080 |
Nederland AstraZeneca BV Tel: +31 79 363 2222 |
|
Eesti AstraZeneca Tel: +372 654 9 6 00 |
Norge AstraZeneca AS Tlf: + 47 21 00 64 00 |
|
EXláSa AstraZeneca A.E. T^: + 30 2 10 68 71 500 |
Osterreich AstraZeneca Osterreich GmbH Tel: +43 1 711 31 0 |
|
Espaňa AstraZeneca Farmacéutica Spain, S.A. Tel: + 34 91 301 91 00 |
Polska AstraZeneca Pharma Poland Sp. z o.o. Tel.: + 48 22 245 73 00 |
|
France AstraZeneca Tél: + 33 1 41 29 40 00 |
Portugal AstraZeneca Produtos Farmaceuticos, Lda. Tel: + 351 21 434 61 00 |
|
Hrvatska AstraZeneca d.o.o. Tel: +385 1 4628 000 |
Románia AstraZeneca Pharma SRL Tel: + 40 21 317 60 41 |
|
Ireland AstraZeneca Pharmaceuticals (Ireland) Ltd Tel: + 353 1 609 7100 |
Slovenija AstraZeneca UK Limited Tel: + 386 1 51 35 600 |
|
Ísland |
Slovenská republika |
Vistor hf.
Sími: + 354 535 7000 Italia
AstraZeneca S.p.A.
Tel: + 39 02 98011
Kúrcpog
A^skt^p Oap^aKeuxiKq AtS Tr^: +357 22490305
Latvija
SIA AstraZeneca Latvija Tel: + 371 67377 100
AstraZeneca AB, o.z.
Tel: + 421 2 5737 7777
Suomi/Finland
AstraZeneca Oy Puh/Tel: + 358 10 23 010
Sverige
AstraZeneca AB Tel: +46 8 553 26 000
United Kingdom
AstraZeneca UK Ltd Tel: + 44 1582 836 836
Tato příbalová informace byla naposledy revidována Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu.
76