Armisarte 25 Mg/Ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Armisarte 25 mg/ml koncentrát pro infuzní roztok
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden ml koncentrátu obsahuje pemetrexedum 25 mg (jako pemetrexedum dinatricum dihemihydricum).
Jedna injekční lahvička s 4 ml koncentrátu obsahuje pemetrexedum 100 mg (jako jako pemetrexedum dinatricum dihemihydricum).
Jedna injekční lahvička s 20 ml koncentrátu obsahuje pemetrexedum 500 mg (jako jako pemetrexedum dinatricum dihemihydricum).
Jedna injekční lahvička s 40 ml koncentrátu obsahuje pemetrexedum 1000 mg(jako jako pemetrexedum dinatricum dihemihydricum).
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Koncentrát pro infuzní roztok.
Koncentrát je čirý, bezbarvý až lehce nažloutlý nebo zelenožlutý roztok. pH je mezi 7,0 a 8,0.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Maligní mezoteliom pleury
Přípravek Pemetrexed je v kombinaci s cisplatinou indikován k léčbě pacientů bez předchozí chemoterapie s neresekovatelným maligním mezoteliomem pleury.
Nemalobuněčný karcinom plic
Přípravek Pemetrexed je v kombinaci s cisplatinou indikován v první linii k léčbě pacientů s lokálně pokročilým nebo metastazujícím nemalobuněčným karcinomem plic jiného histologického typu, než predominantně z dlaždicových buněk (viz bod 5.1).
Přípravek Pemetrexed je indikován jako monoterapie k udržovací léčbě lokálně pokročilého nebo metastazujícího nemalobuněčného karcinomu plic jiného histologického typu, než predominantně z dlaždicových buněk u pacientů, u kterých po chemoterapii založené na platině nedošlo k bezprostřední progresi onemocnění. (viz bod 5.1).
Přípravek Pemetrexed je indikován ve druhé linii jako monoterapie k léčbě pacientů s lokálně pokročilým nebo metastazujícím nemalobuněčným karcinomem plic jiného histologického typu, než predominantně z dlaždicových buněk (viz bod 5.1).
4.2 Dávkování a způsob podání
Pemetrexed se smí podávat pouze pod dohledem lékaře s kvalifikací pro podávání protinádorové
chemoterapie.
Dávkování
Pemetrexed v kombinaci s cisplatinou
Doporučená dávka přípravku pemetrexed je 500 mg/m2 tělesného povrchu (body surface area - BSA) podávaná jako intravenózní infuze po dobu 10 minut první den každého -21denního cyklu. Doporučená dávka cisplatiny je 75 mg/m2 BSA, podaná infuzí během dvou hodin přibližně 30 minut po ukončení infuze pemetrexedu první den každého -21denního cyklu. Pacienti musejí dostávat přiměřenou anti-emetickou terapii a hydrataci před podáním cisplatiny, případně i po jejím podání (informace o dávkování cisplatiny - viz rovněž souhrn údajů o přípravku pro přípravky s obsahem cisplatiny).
Pemetrexed v monoterapii
U pacientů léčených pro nemalobuněčný karcinom plic po předcházející chemoterapii je doporučená dávka přípravku pemetrexed 500 mg/m2 BSA podávaná jako intravenózní infuze po dobu 10 minut první den každého -21denního cyklu.
Režim premedikace
Ke snížení incidence a závažnosti kožních reakcí se podá kortikosteroid den před podáním pemetrexedu, v den jeho podání a v den po jeho podání. Kortikoid má být ekvivalentní 4 mg dexamethasonu podávanému perorálně 2x denně (viz bod 4.4).
Ke snížení toxicity musí pacienti léčení pemetrexedem dostávat rovněž vitaminovou suplementaci (viz bod 4.4). Pacienti musí denně užívat kyselinu listovou perorálně nebo multivitaminy s obsahem kyseliny listové (350 - 1 000 mikrogramů). Během sedmi dnů před první dávkou pemetrexedu se musí podat nejméně pět dávek kyseliny listové a její podávání musí pokračovat v průběhu celé léčby a po dobu 21 dní po poslední dávce pemetrexedu. Pacienti musejí rovněž dostat intramuskulární injekci vitaminu B12 (1000 mikrogramů) v týdnu před první dávkou pemetrexedu a poté jednou za každé tři cykly. Další injekce vitaminu B12 se mohou podávat ve stejný den jako pemetrexed.
Monitorování
Pacienti používající pemetrexed musejí mít před každou dávkou monitorovaný celý krevní obraz, včetně diferenciálního bílého krevního obrazu (white cell count WCC) a počtu trombocytů. Před každým podáním chemoterapie musí být provedeno biochemické vyšetření za účelem vyhodnocení funkce ledvin a jater. Před zahájením každého cyklu chemoterapie je nutné, aby pacienti měli následující výsledky vyšetření: absolutní počet neutrofilů musí být > 1500 buněk/mm3 a počet trombocytů musí být > 100 000 buněk/mm3. Clearance kreatininu musí být > 45 ml/min.
Celkový bilirubin musí být < 1,5násobek horní hranice normálních hodnot. Alkalická fosfatáza (AP), aspartátaminotransferáza (AST) a alaninaminotransferáza (ALT) musejí být < 3násobek horní hranice normálních hodnot. V případě postižení jater tumorem jsou akceptovatelné hodnoty alkalické fosfatázy, AST a ALT < 5násobek horní hranice normálních hodnot.
Úprava dávek
Úprava dávky při zahájení následného cyklu se provede na základě krevního obrazu v době nejhlubšího poklesu nebo na základě maximální nehematologické toxicity zjištěné v předchozím cyklu terapie. Léčbu lze odložit, aby byl dostatek času k úpravě. Po úpravě se pacienti léčí podle pokynů uvedených v tabulce 1, 2 a 3, které se použijí v případě podávání přípravku pemetrexed v monoterapii nebo v kombinaci s cisplatinou.
|
Tabulka 1 -Úprava dávek pro pemetrexed (v monoterapii nebo v kombinaci ) a cisplatinu -hematologické toxicity | |
|
Absolutní počet neutrofilů v době nejhlubšího poklesu < 500 /mm3 a počet trombocytů v době nejhlubšího poklesu > 50 000 /mm3 |
75% předchozí dávky (pemetrexedu i cisplatiny) |
|
Počet trombocytů v době nejhlubšího poklesu < 50 000 /mm3 bez ohledu na absolutní počet neutrofilů v době nejhlubšího poklesu |
75% předchozí dávky (pemetrexedu i cisplatiny) |
|
Počet trombocytů v době nejhlubšího poklesu < 50 000 /mm3 s krváceníma bez ohledu na absolutní počet neutrofilů v době nejhlubšího poklesu |
50% předchozí dávky (pemetrexedu i cisplatiny) |
a dle obecných kritérií toxicity (CTC) podle National Cancer Institute (CTC v2.0, NCI 1998) definice CTC krvácení > stupeň 2.
Pokud u pacientů dojde k rozvoji nehematologické toxicity > 3. stupně (s výjimkou neurotoxicity), musí se pemetrexed vysadit až do úpravy na hodnoty nižší nebo stejné, jako byly hodnoty před léčbou. Léčba se zahájí podle pokynů uvedených v tabulce 2.
|
T abulka . 2 - Úprava dávek pro pemetrexed (v monoterapii nebo v kombinaci ) a cisplatinu -nehematologické toxicity3’ b | ||
|
Dávka pemetrexedu (mg/m2) |
Dávka cisplatiny (mg/m2) | |
|
Jakákoli toxicita stupně 3 nebo 4 s výjimkou mukozitidy |
75% předchozí dávky |
75% předchozí dávky |
|
Jakýkoli průjem s nutností hospitalizace (bez ohledu na stupeň) nebo průjem stupně 3 nebo 4 |
75% předchozí dávky |
75% předchozí dávky |
|
Mukozitida stupně 3 nebo 4 |
50% předchozí dávky |
100% předchozí dávky |
aObecná kritéria toxicity podle National Cancer Institute (CTC v2.0; NCI 1998) bS výjimkou neurotoxicity
V případě neurotoxicity je doporučená úprava dávky pro pemetrexed a cisplatinu uvedena v tabulce 3. Pokud se vyskytnou projevy neurotoxicity stupně 3 nebo 4, musejí pacienti léčbu přerušit.
|
Tabulka. 3 - Úprava dávek pro pemetrexed (v monoterapii nebo v kombinaci ) a cisplatinu -neurotoxicita | ||
|
Stupeň toxicity dle CTC a |
Dávka pemetrexedu (mg/m2) |
Dávka cisplatiny (mg/m2) |
|
0 - 1 |
100% předchozí dávky |
100% předchozí dávky |
|
2 |
100% předchozí dávky |
50% předchozí dávky |
a Obecná kritéria toxicity podle National Cancer Institute (CTC v2.0, NCI 1998)
Léčba pemetrexedem musí být přerušena, pokud se u pacienta vyskytnou jakékoli projevy hematologické nebo nehematologické toxicity stupně 3 nebo 4 po 2 sníženích dávky nebo ihned, pokud se vyskytnou projevy neurotoxicity stupně 3 nebo 4.
Starší pacienti
V klinických studiích nebyly žádné známky, že by se u pacientů ve věku 65 let nebo staršíchzvýšilo riziko nežádoucích účinků v porovnání s pacienty mladšími 65 let. Není nutné žádné snížení dávky, kromě případů, kdy je toto snížení nezbytné pro všechny pacienty.
Pediatrická populace
Použití pemetrexedu u maligního mezoteliomu pleury a nemalobuněčného karcinomu plic není u pediatrické populace relevantní.
Pacienti s poruchou funkce ledvin
(standardní Cockroftův a Gaultův vzorec nebo rychlost glomerulární filtrace měřená metodou clearance Tc99m-DPTA v séru): Pemetrexed se primárně vylučuje v nezměněné formě ledvinami. V klinických studiích nebyla u pacientů s clearance kreatininu > 45 ml/min. zapotřebí žádná úprava dávky, kromě úprav doporučovaných pro všechny pacienty. Údaje o použití pemetrexedu u pacientů s clearance kreatininu pod 45 ml/min jsou nedostatečné, a proto se u těchto pacientů používání pemetrexedu nedoporučuje (viz bod 4.4).
Pacienti s poruchou funkce jater
Nebyl zjištěn žádný vztah mezi AST, ALT nebo celkovým bilirubinem a farmakokinetikou pemetrexedu. Nicméně, pacienti s poruchou funkce jater a bilirubinem > 1,5 x vyšším, než je horní hranice normální hodnoty nebo aminotransferázami > 3,0 x vyššími, než je horní hranice normálních hodnot (při absenci metastáz v játrech) nebo > 5,0 x vyššími, než je horní hranice normálních hodnot (při přítomnosti metastáz v játrech), nebyli specificky studováni.
Způsob podání
Opatření, která je nutno učinit před zacházením s pemetrexedem nebo před jeho podáním, naleznete v bodě 6.6.
Přípravek Armisarte se podává jako intravenózní infuze po dobu 10 minut první den každého -21denního cyklu. Pokyny pro naředění přípravku Armisarte před jeho podáním naleznete v bodě 6.6.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Kojení (viz bod 4.6).
Současné podávání vakcíny proti žluté zimnici (viz bod 4.5).
4.4 Zvláštní upozornění a opatření pro použití
Pemetrexed může potlačit funkci kostní dřeně, která se manifestuje jako neutropenie, trombocytopenie a anémie (nebo pancytopenie) (viz bod 4.8). Myelosuprese představuje obvykle toxicitu, která limituje velikost použité dávky. Pacienti musejí být během léčby sledováni z hlediska myelosuprese a pemetrexed se nesmí podat do doby, než se absolutní počet neutrofilů (ANC) nevrátí na hodnoty > 1500 buněk/mm3 a počet trombocytů se nevrátí na hodnoty > 100 000 buněk/mm3. Úprava dávek v následujících cyklech je dána hodnotami absolutního počtu neutrofilů (ANC) v době nejhlubšího poklesu, počtu trombocytů a maximální nehematologickou toxicitou pozorovanými v předchozím cyklu (viz bod 4.2).
Pokud byla před léčbou podávána kyselina listová a vitamin B12, byla hlášena menší toxicita a snížení hematologické a nehematologické toxicity stupně 3 nebo 4, jako je neutropenie, febrilní neutropenie a infekce s neutropenií stupně 3 nebo 4. Proto musejí být všichni pacienti léčení pemetrexedem poučeni, aby
užívali kyselinu listovou a vitamin Bi2 jako profylaktické opatření ke snížení toxicity související s léčbou (viz bod 4.2).
U pacientů, kteří nedostávali před léčbou kortikosteroid, byly popsány kožní reakce. Podávání dexamethasonu (nebo ekvivalentního kortikosteroidu) před léčbou pemetrexedem může snížit výskyt a závažnost kožních reakcí (viz bod 4.2).
Nebyl studován dostatečný počet pacientů s clearance kreatininu pod 45 ml/min.. Proto se nedoporučuje používání pemetrexedu u pacientů s clearance kreatininu < 45 ml/min. (viz bod 4.2).
Pacienti s lehkou až středně těžkou renální insuficiencí (clearance kreatininu od 45 do 79 ml/min) se mají vyvarovat užívání nesteroidních protizánětlivých léků (NSAID), jako je ibuprofen a kyselina acetylsalicylová (> 1,3 g denně) dva dny před podáním pemetrexedu, v den jeho podání a dva dny po podání pemetrexedu (viz bod 4.5).
U pacientů s lehkou až středně těžkou renální insuficiencí, u kterých je terapie pemetrexedem vhodná, má být přerušeno užívání NSAID s dlouhým eliminačním poločasem nejméně pět dnů před podáním pemetrexedu, v den jeho podání a nejméně dva dny po podání pemetrexedu. (viz bod 4.5).
V souvislosti s podáváním pemetrexedu samotného nebo v kombinaci s jinými chemoterapeutiky byly hlášeny závažné renální příhody, včetně akutního selhání ledvin. U mnoha pacientů, u kterých k renálním příhodám došlo, existovaly rizikové faktory pro rozvoj těchto příhod, včetně dehydratace, preexistující hypertenze nebo diabetu mellitu.
Efekt tekutiny ve třetím prostoru, jako je pleurální výpotek nebo ascites, na pemetrexed není zcela stanoven. Klinická studie fáze 2 s pemetrexedem u 31 pacientů se solidním tumorem a se stabilním výpotkem ve třetím prostoru neprokázala žádný rozdíl v plazmatických koncentracích normalizovaných podle dávky a v clearance pemetrexedu oproti pacientům bez přítomnosti tekutiny v třetím prostoru. Proto je vhodné před začátkem léčby pemetrexedem zvážit drenáž tekutiny z třetího prostoru, ale nemusí to být nutné.
V důsledku gastrointestinální toxicity pemetrexedu podávaného v kombinaci s cisplatinou byly popsány případy vážné dehydratace. Proto mají pacienti dostávat přiměřenou antiemetickou terapii a odpovídající hydrataci před podáním a případně i po podání medikace.
V průběhu klinických studií s pemetrexedem byly méně často hlášeny závažné kardiovaskulární příhody, zahrnující infarkt myokardu a cerebrovaskulární příhody obvykle, když byl pemetrexed podáván
v kombinaci s dalšími cytostatiky. Většina pacientů, u kterých byly tyto příhody pozorovány, měla preexistující kardiovaskulární rizikové faktory (viz bod 4.8).
Pokles imunity je častým jevem u pacientů s onkologickým onemocněním. Proto současné používání živých oslabených vakcín není doporučeno (viz bod 4.3 a 4.5).
Pemetrexed může mít geneticky škodlivé účinky. Pohlavně zralým mužům se doporučuje, aby během léčby a až 6 měsíců po jejím ukončení nepočali dítě. Doporučuje se používání antikoncepčních metod nebo abstinence. Vzhledem k možnosti, že by pemetrexed způsobil ireverzibilní infertilitu, se mužům doporučuje, aby před zahájením léčby vyhledali konzultaci o možnosti uchování spermií.
Ženy ve fertilním věku musejí během léčby pemetrexedem používat účinnou antikoncepční metodu (viz bod 4.6).
U pacientů léčených ozařováním před léčbou, v průběhu nebo následovně po léčbě pemetrexedem byly hlášeny případy postradiační pneumonitidy. Těmto pacientům má být věnována zvýšená pozornost a opatrnost je také zapotřebí při použití dalších radiosenzibilizujících látek.
Byly hlášeny případy kožní reakce v místě předchozího ozařování (radiation recall) u pacientů ozařovaných před delší dobou - před týdny až roky.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Pemetrexed se vylučuje hlavně ledvinami v nezměněné formě, a to tubulární sekrecí a v menším rozsahu glomerulární filtrací. Souběžné podávání nefrotoxických léků (např. aminoglykosidy, kličková diuretika, sloučeniny platiny, cyklosporin) může vést k opožděné clearance pemetrexedu. Tato kombinace se musí používat s opatrností. Pokud je to nutné, má být pečlivě monitorována clearance kreatininu.
Souběžné podávání látek, které se rovněž vylučují tubulární sekrecí (např. probenecid, penicilin), může vést k opožděné clearance pemetrexedu. Při kombinaci těchto látek je zapotřebí zvýšené opatrnosti. Pokud je to nutné, má být pečlivě monitorována clearance kreatininu.
U pacientů s normální renální funkcí (clearance kreatininu > 80 ml/min) mohou vysoké dávky nesteroidních protizánětlivých léků (NSAID, jako je ibuprofen > 1600 mg denně) a vysoké dávky kyseliny acetylsalicylové (> 1,3 g denně) snížit eliminaci pemetrexedu a tím zvýšit výskyt nežádoucích účinků. Proto je zapotřebí při současném podávání vyšších dávek NSAID nebo kyseliny acetylsalicylové společně s pemetrexedem u pacientů s normální renální funkcí (clearance kreatininu > 80 ml/min) zvýšené opatrnosti.
Pacienti s lehkou až středně těžkou renální insuficiencí (clearance kreatininu od 45 do 79 ml/min) se mají vyvarovat současného používání pemetrexedu s NSAID (např. ibuprofen) nebo s vyššími dávkami kyseliny acetylsalicylové 2 dny před podáním pemetrexedu, v den jeho podání a 2 dny po podání pemetrexedu ( viz bod 4.4).
Jelikož nejsou k dispozici údaje o potenciální interakci mezi pemetrexedem a NSAID s delším poločasem, jako je piroxikam a rofekoxib je potřebné jejich podávání u pacientů s lehkou až středně těžkou renální insuficiencí přerušit nejméně 5 dní před podáním pemetrexedu, v den jeho podání a nejméně 2 dny po podání pemetrexedu (viz bod 4.4). Pokud je současné podávání NSAID nezbytné, mají být pacienti důkladně monitorováni z hlediska toxicity, zejména myelosuprese a gastrointestinální toxicity.
Pemetrexed prochází omezeným jaterním metabolismem. Výsledky studií in vitro s lidskými jaterními mikrozomy ukázaly, že nelze předpovědět, zda pemetrexed způsobí klinicky významnou inhibici metabolické clearance léků metabolizovaných CYP3A, CYP2D6, CYP2C9 a CYP1A2.
Interakce běžné u všech cytotoxických látek:
Vzhledem ke zvýšenému riziku trombózy u pacientů s maligním onemocněním je časté používání antikoagulační léčby. Vysoká intraindividuální variabilita koagulačního stavu při těchto chorobách a možnost interakce mezi perorálními antikoagulancii a protinádorovou chemoterapií vyžaduje zvýšenou frekvenci monitorování INR (International Normalised Ratio), pokud se rozhodneme léčit pacienta perorálními antikoagulancii.
Kontraindikované souběžné používání: vakcína proti žluté zimnici: riziko fatálního generalizovaného vakcinačního onemocnění (viz bod 4.3/
Nedoporučené současné používání: živé oslabené vakcíny (vyjma žluté zimnice, kdy je současné používání kontraindikováno): riziko systémové reakce s možným fatálním průběhem. Toto riziko je zvýšeno u osob s již existujícím poklesem imunity způsobeným základním onemocněním. Kde je to možné použijte inaktivované vakcíny (poliomyelitida) (viz bod 4.4).
4.6 F ertilita, těh otenství a kojení
Antikoncepce u mužů a u žen
Ženy ve fertilním věku musí v průběhu léčby pemetrexedem používat účinnou antikoncepci. Pemetrexed může mít geneticky škodlivé účinky. Pohlavně zralým mužům se doporučuje, aby během léčby a až 6 měsíců po jejím ukončení nepočali dítě. Doporučuje se používání antikoncepčních metod nebo abstinence.
Neexistují údaje o použití pemetrexedu u těhotných žen, avšak je podezření, že pemetrexed tak jako ostatní antimetabolity způsobuje vážné kongenitální vady, pokud je podáván v těhotenství. Studie na zvířatech prokázaly reprodukční toxicitu (viz bod 5.3). Pemetrexed se nemá používat v těhotenství, pokud to není jednoznačně nezbytné a po pečlivém zvážení potřeby léčby u matky a rizika pro plod (viz bod 4.4).
Kojení
Není známo, zda se pemetrexed vylučuje do lidského mateřského mléka a nežádoucí účinky u kojeného dítěte nelze vyloučit. Při léčbě pemetrexedem musí být kojení přerušeno (viz bod 4.3).
Fertilita
Vzhledem k možnosti způsobit léčbou pemetrexedem ireverzibilní infertilitu, se mužům doporučuje, aby před zahájením léčby vyhledali konzultaci o možnosti uchování spermií.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Studie hodnotící účinky na schopnost řídit a obsluhovat stroje nebyly provedeny. Bylo však popsáno, že pemetrexed může způsobovat únavu. Pacienti proto mají být upozorněni, aby neřídili nebo neobsluhovali stroje v případě, že se tyto nežádoucí účinky objeví.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Nejčastěji hlášenými nežádoucími účinky v souvislosti s pemetrexedem používaným ať už v monoterapii nebo v kombinaci, jsou myelosuprese, manifestující se jako anemie, neutropenie, leukopenie, trombocytopenie; a gastrointestinální toxicita, manifestující se jako anorexie, nauzea, zvracení, průjem, zácpa, faryngitida, mukozitida a stomatitida. Další nežádoucí účinky zahrnují renální toxicitu, zvýšení hladin aminotransferáz, alopecii, únavu, dehydrataci, vyrážku, infekci/sepsi a neuropatii. Mezi vzácné nežádoucí účinky patří Stevens-Johnsonův syndrom a toxická epidermální nekrolýza.
Tabulkový seznam nežádoucích účinků
V tabulce níže je uvedena frekvence a závažnost nežádoucích účinků, které byly hlášeny u více než 5 % ze 168 pacientů s mezoteliomem, kteří byli randomizováni k léčbě cisplatinou a pemetrexedem a u 163 pacientů s mezoteliomem, kteří byli randomizováni k léčbě cisplatinou v monoterapii. V obou léčebných ramenech byla pacientům, u kterých dosud nebyla prováděna chemoterapie, přidána kyselina listová a vitamin B12.
Frekvence nežádoucích účinků je definována: velmi časté (> 1/10); časté (> 1/100 až <1/10); méně časté (> 1/1000 až <1/100); vzácné (> 1/10000 až <1/1000); velmi vzácné(<1/10000) a není známo (z dostupných údajů spontánních hlášení nelze určit),
V každé skupině četností jsou nežádoucí účinky seřazeny podle klesající závažnosti.
|
Třída orgánových systémů |
Frekvence |
Nežádoucí účinek* |
Pemetrexed/cisplatina |
Cisplatina | ||
|
(n=168) |
(n=163) | |||||
|
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) |
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) | |||
|
Poruchy krve a lymfatického systému |
Velmi časté |
Snížení počtu neutrofilů/ granulocytů - |
56,0 |
23,2 |
13,5 |
3,1 |
|
Snížení počtu leukocytů - |
53,0 |
14,9 |
16,6 |
0,6 | ||
|
Snížení hladiny hemoglobinu - |
26,2 |
4,2 |
10,4 |
0,0 | ||
|
Snížení počtu trombocytů - |
23,2 |
5,4 |
8,6 |
0,0 | ||
|
Poruchy metabolismu a výživy |
v Časté |
Dehydratace |
6,5 |
4,2 |
0,6 |
0,6 |
|
Poruchy nervového systému |
Velmi časté |
Senzorická neuropatie - |
10,1 |
0,0 |
9,8 |
0,6 |
|
Časté |
Porucha chuti |
7,7 |
0,0*** |
6,1 |
0,0*** | |
|
Poruchy oka |
v Časté |
Konjunktivitida |
5,4 |
0,0 |
0,6 |
0,0 |
|
Gastro- intestinální poruchy |
Velmi časté |
16,7 |
3,6 |
8,0 |
0,0 | |
|
56,5 |
10,7 |
49,7 |
4,3 | |||
|
Stomatitida/ faryngitida |
23,2 |
3,0 |
6,1 |
0,0 | ||
|
82,1 |
11,9 |
76,7 |
5,5 | |||
|
20,2 |
1,2 |
14,1 |
0,6 | |||
|
Zácpa |
11,9 |
0,6 |
7,4 |
0,6 | ||
|
Časté |
5,4 |
0,6 |
0,6 |
0,0 | ||
|
Poruchy kůže a podkožní tkáně |
Velmi časté |
16,1 |
0,6 |
4,9 |
0,0 | |
|
Alopecie |
11,3 |
0,0*** |
5,5 |
0,0*** | ||
|
Poruchy ledvin a močových cest |
Velmi časté |
Zvýšení hladiny kreatininu |
10,7 |
0,6 |
9,8 |
1,2 |
|
Snížení clearance kreatininu** |
16,1 |
0,6 |
17,8 |
1,8 | ||
|
Celkové poruchy a reakce v místě aplikace |
Velmi časté |
Únava |
47,6 |
10,1 |
42,3 |
9,2 |
* Viz obecná kritéria toxicity podle National Cancer Institute, verze 2 pro každý stupeň toxicity s výjimkou termínu „snížení clearance kreatininu“
**, který je odvozen z termínu „renální/urogenitální, jiné“.
***V souladu s National Cancer Institute CTC (v2.0, NCI 1998), mají být případy poruchy chuti a alopecie hlášeny pouze jako stupeň 1 nebo 2.
Pro účely této tabulky byla použita hraniční hodnota 5 % pro zařazení všech příhod, kdy hlásící osoba považovala příhodu za možnou souvislost s léčbou pemetrexedem a cisplatinou.
Klinicky relevantní projevy toxicity (dle CTC), které byly hlášeny v > 1 % a < 5 % u pacientů náhodným výběrem přidělených k léčbě cisplatinou a pemetrexedem, jsou: renální selhání, infekce, horečka, febrilní neutropenie, zvýšení AST, ALT a GGT, kopřivka a bolest na hrudi.
Klinicky relevantní projevy toxicity (dle CTC), které byly hlášeny v < 1 % pacientů náhodným výběrem přidělených k léčbě cisplatinou a pemetrexedem, jsou: arytmie a motorická neuropatie.
V tabulce je uvedena frekvence a závažnost nežádoucích účinků, které byly hlášeny u více než 5 % z 265 pacientů, kteří byli randomizováni k léčbě pemetrexedem v monoterapii se suplementací kyselinou listovou a vitaminem B12 a u 276 pacientů, kteří byli randomizováni k léčbě docetaxelem v monoterapii. U všech pacientů byla stanovena diagnóza lokálně pokročilého nebo metastazujícího nemalobuněčného karcinomu plic a již byli léčeni chemoterapií.
|
Třída orgánových systémů |
Frekvence |
Nežádoucí účinek* |
Pemetrexed n=265 |
Docetaxel n=276 | ||
|
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) |
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) | |||
|
Poruchy krve a lymfatického systému |
Velmi časté |
Snížení počtu neutrofilů/ granulocytů - |
10,9 |
5,3 |
45,3 |
40,2 |
|
Snížení počtu leukocytů - |
12,1 |
4,2 |
34,1 |
27,2 | ||
|
Snížení hladiny hemoglobinu |
19,2 |
4,2 |
22,1 |
4,3 | ||
|
Časté |
Snížení počtu trombocytů - |
8,3 |
1,9 |
1,1 |
0,4 | |
|
Gastro- intestinální poruchy |
Velmi časté |
12,8 |
0,4 |
24,3 |
2,5 | |
|
16,2 |
1,5 |
12,0 |
1,1 | |||
|
Stomatitida/ faryngitida |
14,7 |
1,1 |
17,4 |
1,1 | ||
|
30,9 |
2,6 |
16,7 |
1,8 | |||
|
21,9 |
1,9 |
23,9 |
2,5 | |||
|
Časté |
Zácpa |
5,7 |
0,0 |
4,0 |
0,0 | |
|
Poruchy jater a žlučových cest |
Časté |
Zvýšení hladiny ALT- |
7,9 |
1,9 |
1,4 |
0,0 |
|
Zvýšení hladiny AST |
6,8 |
1,1 |
0,7 |
0,0 | ||
|
Poruchy kůže a podkožní tkáně |
Velmi časté |
Vyrážka/ deskvamace |
14,0 |
0,0 |
6,2 |
0,0 |
|
Časté |
Pruritus |
6,8 |
0,4 |
1,8 |
0,0 | |
|
Alopecie |
6,4 |
0,4** |
37,7 |
2,2** | ||
|
Celkové poruchy a rekce v místě aplikace |
Velmi časté |
Únava |
34,0 |
5,3 |
35,9 |
5,4 |
|
Časté |
8,3 |
0,0 |
7,6 |
0,0 | ||
* Viz obecná kritéria toxicity podle National Cancer Institute, verze 2 pro každý stupeň toxicity.
** V souladu s National Cancer Institute CTC (v2.0, NCI 1998), mají být případy alopecie hlášeny pouze jako stupeň 1 nebo 2.
Pro účely této tabulky byla použita hraniční hodnota 5 % pro zařazení všech příhod, kdy hlásící osoba považovala příhodu za možnou souvislost s léčbou pemetrexedem).
Klinicky relevantní projevy toxicity (dle CTC), které byly hlášeny ve > 1 % a <5 % u pacientů náhodným výběrem přidělených k léčbě pemetrexedem, jsou: infekce bez neutropenie, febrilní neutropenie, alergická reakce/hypersenzitivita, zvýšení kreatininu, motorická neuropatie, senzorická neuropatie, erythema multiforme a bolest břicha.
Klinicky relevantní projevy toxicity (dle CTC), které byly hlášeny v < 1 % pacientů náhodným výběrem přidělených k léčbě pemetrexedem, jsou: supraventrikulární arytmie.
Klinicky relevantní laboratorní projevy toxicity stupně 3 a 4 byly obdobné při hodnocení integrovaných výsledků 3 studií fáze 2 sledujících monoterapii pemetrexedem (n = 164) a studie fáze 3 sledující monoterapii pemetrexedem (popsána výše), s výjimkou neutropenie (12,8 % oproti 5,3 %) a zvýšení alaninaminotransferázy (15,2 % oproti 1,9 %). Tyto rozdíly byly pravděpodobně dány rozdíly v populaci pacientů, protože do studií fáze 2 byli zařazeni pacienti dosud neléčení chemoterapií a pacientky s karcinomem prsu, předem intenzivně léčené s již existujícími metastázami do jater a/nebo s patologickými výchozími funkčními jaterními testy.
V tabulce níže je uvedena frekvence a závažnost nežádoucích účinků pravděpodobně souvisejících se studovanou medikací, které byly hlášeny u více než 5 % z 839 pacientů s NSCLC, kteří byli randomizováni k léčbě cisplatinou v kombinaci s pemetrexedem a z 830 pacientů s NSCLC, kteří byli randomizováni k léčbě cisplatinou v kombinaci s gemcitabinem. Všichni pacienti dostali studijní léčbu jako zahajovací léčbu lokálně pokročilého nebo metastazujícího nemalobuněčného karcinomu plic a pacienti v obou skupinách byli plně suplementováni kyselinou listovou a vitaminem B12.
|
Třída orgánových systémů |
Frekvence |
Nežádoucí účinek* |
Pemetrexed/cisplatina (n=839) |
Gemcitabin/cisplatina (n=830) | ||
|
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) |
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) | |||
|
Poruchy krve a lymfatického systému |
Velmi časté |
Snížení hladiny hemoglobinu |
33,0* |
5,6* |
45,7* |
9,9* |
|
Snížení po č tu neutrofilů/ granulocytů |
29,0* |
15,1* |
38,4* |
26,7* | ||
|
Snížení počtu leukocytů |
17,8 |
4,8* |
20,6 |
7,6* | ||
|
Snížení počtu trombocytů |
10,1* |
4,1* |
26,6* |
12,7* | ||
|
Poruchy nervového systému |
Časté |
Senzorická neuropatie |
8,5* |
0,0* |
12,4* |
0,6* |
|
Porucha chuti |
8,1 |
0,0*** |
8,9 |
0,0*** | ||
|
Gastrointestinální poruchy |
Velmi časté |
56,1 |
7,2* |
53,4 |
3,9* | |
|
39,7 |
6,1 |
35,5 |
6,1 | |||
|
26,6 |
2,4* |
24,2 |
0,7* | |||
|
Zácpa |
21,0 |
0,8 |
19,5 |
0,4 | ||
|
Stomatitida/ faryngitida |
13,5 |
0,8 |
12,4 |
0,1 | ||
|
Průjem bez kolostomie |
12,4 |
1,3 |
12,8 |
1,6 | ||
|
Časté |
Dyspepsie/ pálení žáhy |
5,2 |
0,1 |
5,9 |
0,0 | |
|
Poruchy kůže a podkožní tkáně |
Velmi časté |
Alopecie |
11,9* |
0*** |
21,4* |
0,5*** |
|
Časté |
Vyrážka/deskvamace |
6,6 |
0,1 |
8,0 |
0,5 | |
|
Poruchy ledvin a močových cest |
Velmi časté |
Zvýšení sérové hladiny kreatininu - |
10,1* |
0,8 |
6,9* |
0,5 |
|
Celkové poruchy a reakce v místě aplikace |
Velmi časté |
Únava |
42,7 |
6,7 |
44,9 |
4,9 |
* hodnota p <0,05 při srovnání kombinace pemetrexed/cisplatina a gemcitabin/cisplatina při použití Fisherova exaktního testu.
** Viz obecná kritéria toxicity podle National Cancer Institute, verze 2 pro každý stupeň toxicity.
*** V souladu s National Cancer Institute CTC (v2.0, NCI 1998), mají být případy poruchy chuti a alopecie hlášeny pouze jako stupeň 1 nebo 2.
Pro účely této tabulky byla použita hraniční hodnota 5 % pro zařazení všech příhod, kdy hlásící osoba považovala příhodu za eventuálně související s léčbou pemetrexedem a cisplatinou.
Klinicky relevantní toxicita, která byla hlášena u > 1 % a < 5 % pacientů náhodným výběrem přidělených k léčbě pemetrexedem a cisplatinou, zahrnovala: zvýšení hodnot AST, zvýšení hodnot ALT, infekci, febrilní neutropenii, renální selhání, pyrexii, dehydrataci, konjunktivitidu a snížení clearance kreatininu.
Klinicky relevantní toxicita, která byla hlášena u < 1 % pacientů náhodným výběrem přidělených k léčbě pemetrexedem a cisplatinou, zahrnovala: zvýšení hodnot GGT, bolest na hrudi, arytmie a motorickou neuropatii.
Klinicky relevantní toxicita byla v celkové populaci u pacientů používajících pemetrexed v kombinaci s cisplatinou podobná bez ohledu na pohlaví.
V tabulce níže je uvedena frekvence a závažnost nežádoucích účinků pravděpodobně souvisejících se studijní medikací, které byly v klinických hodnoceních udržovací léčby pemetrexedem v monoterapii (JMEN: n=663) a pokračující udržovací léčby pemetrexedem (PARAMOUNT: n=539) hlášeny u více než 5 % z 800 pacientů, kteří byli randomizováni k léčbě samotným pemetrexedem a 402 pacientů, kteří byli randomizováni k léčbě placebem. U všech pacientů byl diagnostikován NSCLC stadia IIIB nebo IV a všichni podstoupili předchozí terapii založenou na platině. Pacienti v obou ramenech studie byli plně suplementováni kyselinou listovou a vitaminem B12.
|
Třída orgánových systémů |
Frekvence* |
Nežádoucí účinek** |
Pemetrexed*** (n=800) |
Placebo*** (n=402) | ||
|
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) |
Všechny stupně toxicity (%) |
Toxicita stupně 3 - 4 (%) | |||
|
Poruchy krve a lymfatického systému |
Velmi časté |
Snížení hladiny hemoglobinu |
18,0 |
4,5 |
5,2 |
0,5 |
|
Časté |
Snížení počtu leukocytů - |
5,8 |
1,9 |
0,7 |
0,2 | |
|
Snížení počtu neutrofilů - |
8,4 |
4,4 |
0,2 |
0,0 | ||
|
Poruchy nervového systému |
Časté |
Senzorická neuropatie |
7,4 |
0,6 |
5,5 |
0,2 |
|
Gastrointestinální poruchy |
Velmi časté |
17,3 |
0,8 |
4,0 |
0,2 | |
|
12,8 |
1,1 |
3,2 |
0,0 | |||
|
Časté |
8,4 |
0,3 |
1,5 |
0,0 | ||
|
Mukozitida/ stomatitida |
6,8 |
0,8 |
1,7 |
0,0 | ||
|
Poruchy jater a žlučových cest |
Časté |
Zvýšení hladiny ALT vzestup |
6,5 |
0,1 |
2,2 |
0,0 |
|
Zvýšení hladiny AST vzestup |
5,9 |
0,0 |
1,7 |
0,0 | ||
|
Poruchy kůže a podkožní tkáně |
Časté |
Vyrážka/ deskvamace |
8,1 |
0,1 |
3,7 |
0,0 |
|
Celkové poruchy a reakce v místě aplikace |
Velmi časté |
Únava |
24,1 |
5,3 |
10,9 |
0,7 |
|
Časté |
Bolest |
7,6 |
0,9 |
4,5 |
0,0 | |
|
Edém |
5,6 |
0,0 |
1,5 |
0,0 | ||
|
Poruchy ledvin a močových cest |
Časté |
Renální poruchy**** |
7,6 |
0,9 |
1,7 |
0,0 |
Zkratky: ALT = alaninaminotransferáza; AST = aspartátaminotrasferáza; CTCAE = obecná terminologická kritéria nežádoucích účinků (Common Terminology Criteria for Adverse Event); NCI = National Cancer Institute.
* Definice frekvence nežádoucích účinků: velmi časté - > 10%; časté - > 5% a < 10%. Pro účely této tabulky byla použita hraniční hodnota 5 % pro zařazení všech příhod, kdy hlásící osoba považovala příhodu za možnou souvislost s léčbou pemetrexedem.
** Viz NCI CTCAE kritéria (verze 3.0; NCI 2003) pro každý stupeň toxicity. Výskyt toxicit uveden podle CTCAE verze 3.0
*** V integrované tabulce nežádoucích účinků jsou kombinovány výsledky klinických hodnocení udržovací léčby pemetrexedem JMEN (n=663) a pokračující udržovací léčby pemetrexedem PARAMOUNT (n=539). ****Souhrnné označení zahrnuje zvýšení kreatininu v séru/krvi, pokles glomerulární filtrace, renální selhání a renální/urogenitální- jiné.
Klinicky relevantní projevy toxicity (dle CTC) jakéhokoli stupně, které byly hlášeny u > 1 % a < 5 % pacientů náhodným výběrem přidělených k léčbě pemetrexedem zahrnují: febrilní neutropenii, infekci, snížení počtu trombocytů, průjem, zácpu, alopecii, pruritus/svědění, horečku (bez neutropenie), onemocnění očního povrchu (včetně konjunktivitidy), zvýšené slzení, závrať a motorickou neuropatii.
Klinicky relevantní projevy toxicity (dle CTC), které byly hlášeny u < 1 % pacientů náhodným výběrem přidělených k léčbě pemetrexedem, jsou: alergická reakce/hypersenzitivita, , erythema multiforme, supraventikulární arytmie a plicní embolie.
Bezpečnost byla hodnocena u pacientů, kteří byli randomizováni k léčbě pemetrexedem (n=800). Výskyt nežádoucích účinků byl hodnocen u pacientů, kteří dostali < 6 cyklů udržovací léčby pemetrexedem (n=519)a srovnán s výskytem u pacientů, kteří dostali > 6 cyklů léčby pemetrexedem. (n=281). S déle trvající expozicí bylo pozorováno zvýšení výskytu nežádoucích účinků (všech stupňů). Významné zvýšení výskytu neutropenie stupně 3 nebo 4 potenciálně související s hodnoceným lékem, bylo pozorováno při delší expozici pemetrexedu (< 6 cyklů: 3,3 %, > 6 cyklů: 6,4 %: p=0,046). U jednotlivých stupňů 3/4/5 dalších nežádoucích účinků, nebyly při delší expozici pozorovány statisticky významné rozdíly.
V průběhu klinických studií s pemetrexedem byly méně často hlášeny závažné kardiovaskulární a cerebrovaskulární příhody, zahrnující infarkt myokardu, anginu pectoris a tranzitorní ischemické ataky obvykle, když byl pemetrexed podáván v kombinaci s dalšími cytostatiky. Většina pacientů, u kterých byly tyto příhody pozorovány, měla preexistující kardiovaskulární rizikové faktory.
V průběhu klinických studií s pemetrexedem byly hlášeny potenciálně závažné vzácné případy hepatitidy.
Méně často byla u pacientů v průběhu klinických studií s pemetrexedem hlášena pancytopenie.
Méně často byly v klinických studiích u pacientů léčených pemetrexedem hlášeny případy kolitidy (včetně intestinálního a rektálního krvácení, někdy s fatálním průběhem, intestinální perforace, nekrózy a tyflitidy).
Méně často byly v klinických studiích u pacientů léčených pemetrexedem hlášeny případy intersticiální pneumonitidy s respirační nedostatečností, někdy s fatálním průběhem.
U pacientů léčených pemetrexedem byly méně často hlášeny případy edému.
Méně často byla u pacientů v průběhu klinických studií s pemetrexedem hlášena ezofagitida/radiační ezofagitida.
V průběhu klinických studií s pemetrexedem byly často hlášeny sepse, někdy s fatálním průběhem.
V průběhu postmarketingového sledování byly hlášeny u pacientů léčených pemetrexedem následující nežádoucí účinky:
V souvislosti s podáváním pemetrexedu samotného nebo v kombinaci s jinými chemoterapeutiky byly méně často hlášeny případy akutního selhání ledvin (viz bod 4.4).
U pacientů léčených ozařováním před léčbou, v průběhu nebo následně po léčbě pemetrexedem byly méně často hlášeny případy postradiační pneumonitidy (viz bod 4.4).
U pacientů, kteří podstoupili léčbu ozařováním, byly vzácně hlášeny případy kožní reakce v místě předchozího ozařování (radiation recall) (viz bod 4.4).
Méně často byly hlášeny případy periferní ischémie, které někdy vedly k nekróze končetiny.
Vzácně byly hlášeny případy tvorby puchýřů včetně Stevens-Johnsonova syndromu a toxické epidermální nekrolýzy, které byly v některých případech s fatálním průběhem.
Vzácně byla u pacientů léčených pemetrexedem hlášena hemolytická anemie vyvolaná imunitní reakcí.
Vzácně byly hlášeny případy anafylaktického šoku.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
K popsaným symptomům předávkování patří neutropenie, anemie, trombocytopenie, mukozitida, senzorická polyneuropatie a vyrážka. K předpokládaným komplikacím předávkování patří myelosuprese, která se manifestuje neutropenií, trombocytopenií a anemií. Kromě toho lze pozorovat infekce s horečkou nebo bez ní, průjema/nebo mukozitidu. V případě podezření na předávkování, musí být u pacientů sledován krevní obraz a pacienti mají dostávat podle potřeby podpůrnou léčbu.
V léčbě předávkování pemetrexedem se má zvážit podávání kalcium- folinátu nebo kyseliny folinové.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: cytostatika, analoga kyseliny listové,
ATC kód: L01BA04
Pemetrexed je tzv. „multi-targeted“ antifolikum, protinádorová látka působící narušení klíčových metabolických procesů závislých na kyselině listové, které jsou nezbytné pro replikaci buněk.
Studie in vitro prokázaly, že pemetrexed se chová jako „multi-targeted“ antifolikum tím, že inhibuje thymidylátsyntázu (TS), dihydrofolátreduktázu (DHFR) a glycinamid ribonukleotid formyltransferázu (GARFT), které jsou klíčové enzymy závislé na folátu pro biosyntézu thymidinu a purinových nukleotidů de novo. Pemetrexed je transportován do buněk redukovaným nosičem folátu a membránovým folátovým vazebným proteinovým transportním systémem. Jakmile je pemetrexed v buňce, přeměňuje se rychle a efektivně na polyglutamátové formy pomocí enzymu folylpolyglutamátsyntetáza. Polyglutamátové formy se zadržují v buňkách a jsou ještě silnějšími inhibitory TS a GARFT. Polyglutamace je proces závislý na čase a koncentraci, ke kterému dochází v nádorových buňkách a v menší míře i v normálních tkáních. Polyglutamátové metabolity mají zvýšený intracelulární poločas, což vede k protrahovanému účinku léku v maligních buňkách.
Evropská agentura pro léčivé přípravky rozhodla o zproštění povinnosti předložit výsledky studií s pemetrexedem u všech podskupin pediatrické populace ve schválených indikacích (viz bod 4.2).
Klinická účinnost
Mezoteliom
Studie EMPHACIS byla multicentrická, randomizovaná, jednoduše zaslepená studie fáze 3 s pemetrexedem a cisplatinou oproti cisplatině u pacientů s maligním mezoteliomem pleury, kteří dosud nepodstoupili chemoterapii. V této studii bylo prokázáno, že pacienti léčení pemetrexedem a cisplatinou měli klinicky významnou výhodu mediánu přežití, trvající 2,8 měsíce v porovnání s pacienty léčenými cisplatinou v monoterapii.
Během studie byla k léčbě zavedena dlouhodobá suplementace nízkými dávkami kyseliny listové a vitaminu B12 s cílem snížit toxicitu. Primární analýza této studie byla provedena na populaci všech pacientů randomizovaně přidělených do léčebné skupiny, kteří dostávali hodnocený lék (randomizovaní a léčení). Byla provedena analýza podskupin u pacientů, kteří dostávali suplementaci kyselinou listovou a vitaminem B12 v průběhu celé léčebné kúry hodnoceným lékem (úplná suplementace). Výsledky těchto analýz účinnosti jsou shrnuty v tabulce:
Účinnost pemetrexedu v kombinaci s cisplatinou oproti cisplatině u pacientů s maligním _ mezoteliomem pleury__
|
Randomizovaní a léčení pacienti |
Plně suplementovaní pacienti | |||
|
Parametr účinnosti |
Pemetrexed/ |
Cisplatina |
Pemetrexed/ |
Cisplatina |
|
cisplatina |
cisplatina | |||
|
(n=226) |
(n=222) |
(n=168) |
(n=163) | |
|
Medián celkového přežití (měsíce) |
12,1 |
9,3 |
13,3 |
10,0 |
|
(95 % CI) |
(10,0 - 14,4) |
(7,8 - 10,7) |
(11,4 - 14,9) |
(8,4 - 11,9) |
|
Log Rank hodnota p* |
0,020 |
0,051 | ||
|
Medián doby do progrese tumoru |
5,7 |
3,9 |
6,1 |
3,9 |
|
(měsíce) | ||||
|
(95 % CI) |
(4,9 - 6,5) |
(2,8 - 4,4) |
(5,3 - 7,0) |
(2,8 - 4,5) |
|
Log Rank hodnota p* |
0,001 |
0,008 | ||
|
Doba do selhání léčby (měsíce) |
4,5 |
2,7 |
4,7 |
2,7 |
|
(95 % CI) |
(3,9 - 4,9) |
(2,1 - 2,9) |
(4,3 - 5,6) |
(2,2 - 3,1) |
|
Log Rank hodnota p* |
0,001 |
0,001 | ||
|
Výskyt celkové odpovědi* |
41,3 % |
16,7 % |
45,5 % |
19,6 % |
|
(95 % CI) |
(34,8 - 48,1) |
(12,0 - 22,2) |
(37,8 - 53,4) |
(13,8 - 26,6) |
|
Fisherova přesná hodnota p* |
< 0,001 |
< 0,001 | ||
Zkratky: CI = interval spolehlivosti * hodnota p se týká srovnání mezi rameny
** V rameni pemetrexed/cisplatina, randomizovaní a léčení (n = 225) a plně suplementovaní (n = 167) pacienti
Statisticky významné zlepšení klinicky významných symptomů (bolest a dušnost) vyskytujících se při maligním mezoteliomu pleury v rameni s pemetrexedem/cisplatinou (212 pacientů) oproti rameni s léčbou pouze cisplatinou (218 pacientů) bylo prokázáno pomocí škály symptomů karcinomu plic. Byly rovněž pozorovány statisticky významné rozdíly v plicních funkčních testech. Oddělení mezi léčebnými rameny bylo dosaženo zlepšením plicní funkce v rameni pemetrexed/cisplatina a zhoršením plicní funkce v čase u kontrolního ramene.
Existují omezené údaje u pacientů s maligním mezoteliomem pleury, léčených pemetrexedem v monoterapii. Pemetrexed v dávce 500 mg/m2 byl studován jako lék podávaný v monoterapii u 64 pacientů s maligním mezoteliomem pleury dosud neléčených chemoterapií. Celkový výskyt odpovědi na léčbu byl 14,1 %.
NSCLC, léčba v druhé linii
V multicentrické, randomizované, otevřené studii fáze 3 s pemetrexedem a docetaxelem u pacientů s lokálně pokročilým nebo metastatickým nemalobuněčným karcinomem plic po předchozí chemoterapii byl prokázán medián doby přežití 8,3 měsíce u pacientů léčených pemetrexedem (ITT populace se záměrem léčit, n=283) a 7,9 měsíců u pacientů léčených docetaxelem (ITT populace se záměrem léčit, n=288). Předchozí chemoterapie nezahrnovala pemetrexed. Výsledky analýzy vlivu histologie NSCLC na celkové přežití svědčí ve prospěch pemetrexedu oproti docetaxelu u pacientů s NSCLC jiného histologického typu, než predominantně z dlaždicových buněk (n=399; 9,3 oproti 8,0 měsíců, adjustovaný HR=0,78; 95 CI=0,61-1,00, p=0,047) a ve prospěch docetaxelu u karcinomu s histologickou strukturou z dlaždicových buněk (n=172; 6,2 oproti 7,4 měsíců, adjustovaný HR=1,56; 95% CI =1,08-2,26; p = 0,018). V histologických podskupinách nebyly pozorovány žádné klinicky důležité rozdíly v bezpečnostním profilu pemetrexedu.
Omezené klinické údaje z jiného randomizovaného kontrolovaného klinického hodnocení fáze 3 naznačují, že údaje o účinnosti pemetrexedu (Overall survival OS - celková doba přežití, Progression free survival PFS - doba přežití bez progrese) jsou podobné pro skupinu pacientů s předchozí léčbou docetaxelem (n=41) a pacientů bez předchozí léčby docetaxelem (n=540).
Účinnost pemetrexedu oproti docetaxelu u pacientů s nemalobuněčným karcinomem plic _- ITT populace__
|
Pemetrexed |
Docetaxel | |
|
Doba přežití (měsíce) • Medián (m) • 95 % CI pro medián • HR • 95 % CI pro HR • Hodnota p pro neinferioritu (HR) |
(n = 283) (n = 288) 8,3 7,9 (7,0 - 9,4) (6,3 - 9,2) 0,99 (0,82 - 1,20) 0,226 | |
|
Doba přežití bez progrese (měsíce) • Medián • HR (95 % CI) |
(n = 283) (n = 288) 2,9 2,9 0,97 (,82 - 1,16) | |
|
Doba do selhání léčby (TTTF - měsíce) • Medián • HR (95 % CI) |
(n = 283) (n = 288) 2,3 2,1 0,84 (,71 - ,997) | |
|
Odpověď (n: kvalifikovaní pro odpověď) • Výskyt odpovědi (%) (95 % CI) • Stabilní onemocnění (%) |
(n = 264) 9,1 (5,9 - 13,2) 45,8 |
(n = 274) 8,8 (5,7 - 12,8) 46,4 |
Zkratky: CI = interval spolehlivosti; HR = poměr rizik; ITT = záměr léčit; n = celková velikost populace
NSCLC, léčba v první linii
Multicentrická, randomizovaná, otevřená studie fáze 3 s pemetrexedem a cisplatinou oproti gemcitabinu s cisplatinou u pacientů bez předchozí chemoterapie s lokálně pokročilým nebo metastazujícím (stadium IIIB nebo IV) nemalobuněčným karcinomem plic (NSCLC) prokázala, že pemetrexed v kombinaci s cisplatinou (populace ITT Intent-to-treat, n=862) dosáhl primárního cílového parametru a prokázal podobný klinický účinek jako gemcitabin v kombinaci s cisplatinou (ITT n=863) na celkové přežití (adjustovaný poměr rizik 0,94; 95 % CI 0,84-1,05). Všichni pacienti účastnící se této studie měli ECOG výkonnostní stav 0 nebo 1.
Primární analýza účinnosti byla založena na ITT populaci. Analýzy citlivosti pro hlavní cílové parametry studie byly také vyhodnoceny u populace pacientů splňujících vstupní kritéria protokolu (Protocol Qualified -PQ). Výsledky analýz účinnosti u populace PQ jsou v souladu s analýzami populace ITT a podporují non-inferioritu kombinace AC oproti GC.
Doba přežití bez progrese (Progression free survival - PFS) a výskyt celkové odpovědi byly podobné v obou ramenech léčby: medián PFS byl 4,8 měsíců pro pemetrexed v kombinaci s cisplatinou oproti 5,1 měsíců pro gemcitabin v kombinaci s cisplatinou (adjustovaný poměr rizik 1,04; 95 % CI 0,94-1,15) a četnost celkové odpovědi byla 30,6% (95 % CI 27,3- 33,9) pro pemetrexed s cisplatinou oproti 28,2%
(95 % CI 25,0-31,4) pro gemcitabin s cisplatinou. Údaje o PFS byly částečně potvrzeny nezávislým přezkoumáním (pro přezkoumání bylo náhodně vybráno 400/1725 pacientů).
Analýza vlivu histologického původu NSCLC na celkovou dobu přežití prokázala klinicky významné rozdíly mezi jednotlivými histologickými typy, viz níže uvedená tabulka.
Účinnost kombinace pemetrexed + cisplatina oproti kombinaci gemcitabin + cisplatina v první linii nemalobuněčného karcinomu plic - ITT populace a histologické podskupiny.
|
ITT populace a histologické podskupiny |
Medián celkové doby přežití v měsících (95% CI) |
Adjustovaný poměr rizik (HR) (95% CI) |
Superiorita hodnota p | |||
|
pemetrexed + cisplatina |
gemcitabin + cisplatina | |||||
|
ITT populace (n=1725) |
10,3 (9,8 - 11,2) |
n=862 |
10,3 (9,6 - 10,9) |
n=863 |
0,94a (0,84 - 1,05) |
0,259 |
|
Adenokarcinom (n=847) |
12,6 (10,7 - 13,6) |
n=436 |
10,9 (10,2 - 11,9) |
n=411 |
0,84 (0,71-0,99) |
0,033 |
|
Velkobuněčný (n=153) |
10,4 (8,6 - 14,1) |
n=76 |
6,7 (5,5 - 9,0) |
n=77 |
0,67 (0,48-0,96) |
0,027 |
|
Jiný (n=252) |
8,6 (6,8 - 10,2) |
n=106 |
9,2 (8,1 - 10,6) |
n=146 |
1,08 (0,81-1,45) |
0,586 |
|
Dlaždicobuněčný (n=473) |
9,4 (8,4 - 10,2) |
n=244 |
10,8 (9,5 - 12,1) |
n=229 |
1,23 (1,00-1,51) |
0,050 |
Zkratky: CI = interval spolehlivosti; ITT = záměr léčit; n = celková velikost souboru.
a Statisticky významné pro noninferioritu, s celkovým intervalem spolehlivosti pro HR dostatečně pod hranicí noninferiority 1,17645 (p <0,001).
Kaplan-Meierova křivka celkové doby přežití podle histologického typu
Adenokarcinom
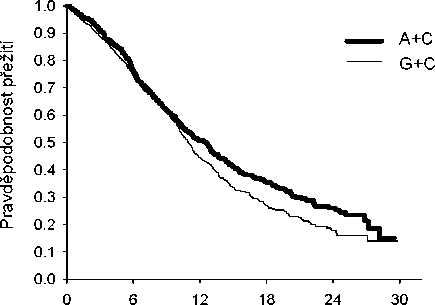
Doba přežití (měsíce)
Velkobuněčný karcinom
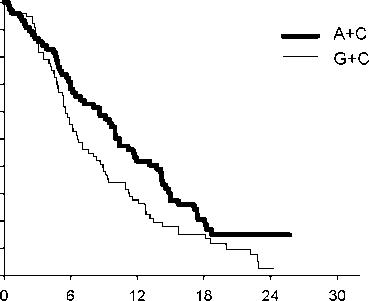
Doba ařežití (měsíce)
V histologických podskupinách nebyly pozorovány žádné klinicky významné rozdíly v bezpečnostním profilu pemetrexedu v kombinaci s cisplatinou.
U pacientů léčených pemetrexedem v kombinaci s cisplatinou byl zapotřebí menší počet transfúzí (16,4 % oproti 28,9 %, p<0,001), transfuzí erytrocytů (16,1% oproti 27,3 %, p<0,001) a transfuzí trombocytů (1,8 % oproti 4,5 %, p=0,002). Rovněž byl zapotřebí menší počet podání erytropoetinu/darbopoetinu (10,4 % oproti 18,1 %, p<0,001), G-CSF/GM-CSF (3,1 % oproti 6,1 %, p=0,004) a přípravků obsahujících železo (4,3 % oproti 7,0 %, p=0,021).
NSCLC, udržovací léčba
JMEN
Multicentrická, randomizovaná, dvojitě zaslepená studie fáze 3 kontrolovaná placebem (JMEN), srovnávala účinnost a bezpečnost udržovací léčby pemetrexedem spolu s nejlepší možnou podpůrnou léčbou (BSC) (n=441) a podávání placeba spolu s BSC (n=222) u pacientů s lokálně pokročilým (stadium IIIB) nebo metastazujícím (stadium IV) nemalobuněčným karcinomem plic (NSCLC), u kterých nedošlo k progresi po 4 cyklech terapie první linie dvojkombinací obsahující cisplatinu nebo karboplatinu v kombinaci s gemcitabinem, paklitaxelem nebo docetaxelem. Kombinovaná léčba obsahující v první linii v dvojkombinaci pemetrexed nebyla zahrnuta. Všichni pacienti účastnící se této studie měli ECOG výkonnostní stav 0 nebo 1. Udržovací léčba byla pacientům podávána do doby progrese nemoci. Účinnost a bezpečnost byly měřeny od doby randomizace po dokončení (indukční) terapie první linie. Střední hodnota počtu cyklů podaných pacientům byla 5 cyklů udržovací léčby pemetrexedem a 3,5 cyklů podávání placeba. Celkem 213 pacientů (48,3%) dokončilo > 6 cyklů 103 pacientů (23,4%) > 10 cyklů léčby pemetrexedem.
Studie dosáhla primárního cílového parametru a prokázala statisticky významné zlepšení PFS ve skupině pemetrexedu oproti skupině placeba (n=581, nezávisle hodnocená populace, medián 4,0 měsíce, resp. 2,0 měsíce) (poměr rizika=0,60, 95 % CI=0,49-0,73, p < 0,00001). Nezávislé hodnocení pacientských skenů potvrdilo závěry hodnocení PFS ze strany zkoušejících. Střední hodnota celkové doby přežití (OS) pro celkovou populaci (n=663) byla 13,4 měsíců ve skupině pemetrexedu a 10,6 měsíců ve skupině placeba, poměr rizik=0,79 (95 % CI=0,65-0,95; p=0,01192).
V souladu s dalšími studiemi pemetrexedu byl ve studii JMEN pozorován rozdíl v účinnosti s ohledem na histologii NSCLC. U pacientů s NSCLC jiného histologického typu, než predominantně z dlaždicových buněk (n=430, nezávisle hodnocená populace) byla střední doba přežití bez progrese (PFS) 4,4 měsíce u pemetrexedu a 1,8 měsíců u skupiny placeba, poměr rizik=0,47 (95 % 0=0,37-0,60, p= 0,00001). Střední hodnota celkové doby přežití (OS) u pacientů s NSCLC jiného histologického typu, než predominantně
z dlaždicových buněk (n=481) byla 15,5 měsíců ve skupině pemetrexed a 10,3 měsíce ve skupině placeba poměr rizik=0,70 (95 % 0=0,56-0,88, p=0,002). Střední doba OS včetně indukční fáze byla u pacientů s NSCLC jiného histologického typu, než predominantně z dlaždicových buněk 18,6 měsíců ve skupině pemetrexedu a 13,6 měsíců ve skupině placeba poměr rizik=0,71 (95 % 0=0,56-0,88, p=0,002).
U pacientů s karcinomem histologického typu z dlaždicových buněk nenaznačují výsledky PFS a OS výhodu léčby pemetrexedem oproti placebu.
V histologických podskupinách nebyly pozorovány žádné klinicky důležité rozdíly v bezpečnostním profilu pemetrexedu.
JMEN: Kaplan-Meierova křivka doby přežití bez progrese (PFS) a celkové doby přežití u pacientů s NSCLC jiného histologického typu, než predominantně z dlaždicových buněk, užívajících pemetrexed nebo placebo:
Doba přežití bez progrese Celková doba přežití
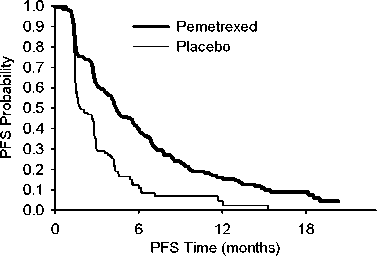
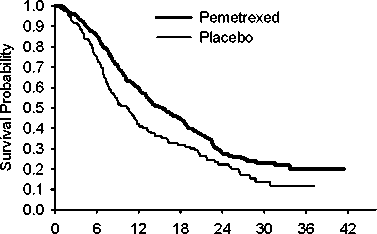
Survival Time (months)
PARAMOUNT
Mutlicentrická, randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze 3 (PARAMOUNT) porovnávala účinnost a bezpečnost pokračující udržovací léčby pemetrexedem plus BSC_(n=359) s léčbou placebem plus BSC (n=180) u pacientů s lokálně pokročilým (stadium IIIB) nebo metastazujícím (stadium IV) NSCLC jiného histologického typu, než predominantně z dlaždicových buněk, u kterých nedošlo k progresi onemocnění po 4 cyklech první linie léčby dvojkombinací pemetrexedu a cisplatiny.
Z celkového počtu 939 pacientů léčených indukcí pemetrexedem s cisplatinou, bylo 539 pacientů randomizováno na udržovací léčbu pemetrexedem nebo placebem. Z randomizovaných pacientů mělo 44,9% úplnou/částečnou odpověď a u 51,9% došlo ke stabilizaci onemocnění po indukci pemetrexedem s cisplatinou. Pacienti, kteří byli randomizováni k udržovací léčbě, museli mít výkonnostní stav ECOG 0 nebo 1. Medián doby od začátku indukční léčby pemetrexedem s cisplatinou do začátku udržovací léčby byl 2,96 měsíce jak v rameni s pemetrexedem, tak v rameni s placebem. Randomizovaní pacienti dostávali udržovací léčbu do doby progrese onemocnění. Účinnost a bezpečnost byly měřeny od doby randomizace po ukončení prvoliniové (indukční) léčby. Střední hodnoty počtu cyklů podaných pacientům byly 4 cykly léčby pemetrexedem a 4 cykly placeba. Celkem dokončilo > 6 cyklů udržovací léčby pemetrexedem 169 pacientů (47,1 %), což představovalo nejméně 10 cyklů pemetrexedu celkem.
Studie splnila svůj primární cílový parametr a ukázala statisticky významné zlepšení PFS v rameni s pemetrexedem ve srovnání s placebovým ramenem (n=472, nezávisle hodnocená populace, medián 3,9 měsíců a 2,6 měsíců v tomto pořadí) (poměr rizik=0,64, 95 % CI=0,51-0,81, p=0,0002). Nezávislé posouzení skenů pacientů potvrdilo nálezy z hodnocení PFS zkoušejícími. Pro randomizované pacienty byl, měřeno od zahájení první linie indukční léčby pemetrexedem s cisplatinou, medián PFS stanovený zkoušejícím 6,9 měsíců v rameni s pemetrexedem a 5,6 měsíce v rameni s placebem (poměr rizik=0,59, 95 % CI=0,47-0,74).
Po indukci pemetrexedem s cisplatinou (4 cykly), byla léčba pemetrexedem statisticky lepší než placebo z hlediska celkového přežití (medián 13,9 měsíce versus 11,0 měsíců, poměr rizik=0,78, 95 % CI=0,64-0,96, p=0,0195). V době, kdy byla tato finální analýza doby přežití provedena, bylo v rameni s pemetrexedem 28,7 % pacientů naživu nebo byl kontakt s nimi ztracen oproti 21,7% pacientů v rameni s placebem. Relativní léčebný účinek pemetrexedu byl napříč podskupinami (včetně stadia nemoci, odpovědi na indukci, ECOG PS, kuřáckého statusu, pohlaví, histologie a věku) vnitřně konzistentní a podobný tomu, který byl pozorován v neadjustovaných analýzách OS a PFS. Jednoletá a 2letá četnost přežití pacientů s pemetrexedem byla 58% a 32% dle uvedeného pořadí, ve srovnání s 45 % a 21 % u pacientů s placebem. Od začátku indukční léčby pemetrexedem s cisplatinou v první linii byl medián OS pacientů 16,9 měsíce u ramene s pemetrexedem a 14,0 měsíců u ramene s placebem (poměr rizik=0,78,
95 % CI=0,64-0,96). Procento pacientů, kteří dostali postudijní léčbu bylo 64,3 % u pemetrexedu a 71,7 % u placeba.
PARAMOUNT: Kaplan Meierova křivka doby přežití bez progrese (PFS) a celkové doby přežití (OS) u pacientů s NSCLC jiného histologického typu, než predominantně z dlaždicových buněk, pokračujících v udržovací léčbě pemetrexedem nebo placebem ( měřeno od randomizace)
Celková doba přežití (OS)
Doba přežití bez progrese (PFS)
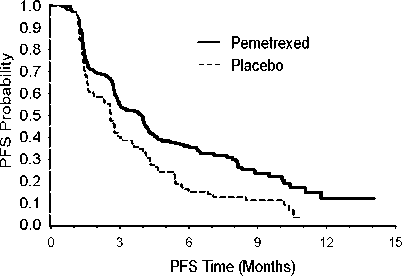
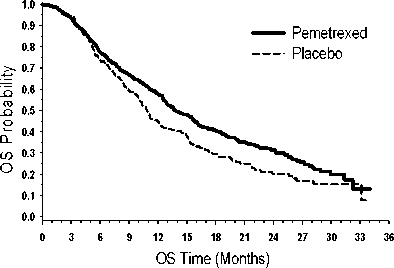
Bezpečnostní profily udržovací léčby pemetrexedem ze dvou klinických hodnocení JMEN a PARAMOUNT byly podobné.
5.2 Farmakokinetické vlastnosti
Farmakokinetické vlastnosti pemetrexedu po jeho podání v monoterapii byly hodnoceny u 426 pacientů s různými maligními solidními tumory, kterým byl lék podáván v dávkách od 0,2 do 83 8 mg/m2 infuzí po dobu 10 minut. Distribuční objem pemetrexedu v ustáleném stavu činil 9 l/m2. Studie in vitro ukazují, že pemetrexed se přibližně z 81 % váže na plazmatické proteiny. Různý stupeň poruchy funkce ledvin nevede k významnému ovlivnění této vazby. Pemetrexed se podstupuje v omezené míře metabolismu v játrech. Pemetrexed se primárně vylučuje močí, přičemž 70 - 90 % podané dávky se odstraní močí v nezměněné formě během prvních 24 hodin po jeho podání. Studie in vitro naznačují, že pemetrexed je aktivně vylučován pomocí OAT3 (přenašeč organických aniontů). Celková systémová clearance pemetrexedu je 91,8 ml/min. a eliminační poločas plazmy je 3,5 hodin u pacientů s normální funkcí ledvin (clearance kreatininu 90 ml/min.). Variabilita clearance mezi pacienty je střední, a to 19,3 %. Celková systémová expozice pemetrexedu (AUC) a maximální plazmatická koncentrace rostou proporcionálně s dávkou. Farmakokinetika pemetrexedu je stejná i při více léčebných cyklech.
Farmakokinetické vlastnosti pemetrexedu nejsou ovlivněny souběžně podanou cisplatinou. Suplementace kyselinou listovou perorálně a vitaminem B12 intramuskulárně neovlivňuje farmakokinetiku pemetrexedu.
5.3 Předklinické údaje vztahující se k bezpečnosti
Podání pemetrexedu březím myším vedlo ke snížení viability plodů, ke snížení hmotnosti plodů, neúplné osifikaci některých kosterních struktur a rozštěpu patra.
Podání pemetrexedu samcům myší vedlo k reprodukční toxicitě charakterizované snížením fertility a testikulární atrofií. V devítiměsíční studii provedené na bíglech s použitím intravenózní bolusové injekce byl pozorován nález na varlatech (degenerace/nekróza seminiferní výstelky). To naznačuje, že pemetrexed může poškodit mužskou fertilitu. Fertilita žen nebyla studována.
Pemetrexed nebyl mutagenní in vitro ani u testu chromozomální aberace na buňkách ovarií čínských křečků ani u Amesova testu. V mikronukleárním testu in vivo u myši bylo prokázáno, že pemetrexed je klastogenní.
Studie hodnotící kancerogenní potenciál pemetrexedu nebyly provedeny.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Trometamol (k úpravě pH)
Bezvodá kyselina citronová Monohydrát cystein-hydrochloridu Voda na injekci
6.2 Inkompatibility
Pemetrexed je fyzikálně inkompatibilní s diluenty obsahujícími kalcium, jako je laktátový Ringerův roztok a Ringerův roztok. Studie kompatibility nejsou k dispozici, a proto nesmí být tento léčivý přípravek mísen s jinými léčivými přípravky.
Přípravek Armisarte obsahuje pomocnou látku trometamol. Trometamol je inkompatibilní s cisplatinou, způsobuje rozklad cisplatiny Tento léčivý přípravek nesmí být mísen s jinými léčivými přípravky. Po podání přípravku Armisarte mají být intravenózní linky propláchnuty.
6.3 Doba použitelnosti
Neotevřená lahvička 18 měsíců.
Naředěný roztok
Chemická a fyzikální stabilita infuzního roztoku pemetrexedu po otevření před použitím byla prokázána na dobu 3 dní při pokojové teplotě a 21 dní při uchovávání v chladničce. Z mikrobiologického hlediska má být přípravek použit okamžitě. Není-li použit okamžitě, doba a podmínky uchovávání před použitím jsou v odpovědnosti uživatele a normálně nemá být doba delší než 24 hodin při teplotě 2 °C - 8 °C, pokud ředění neproběhlo za kontrolovaných a validovaných aseptických podmínek.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte a přepravujte v chladu (2 °C - 8 °C)
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
Podmínky uchovávání tohoto léčivého přípravku po jeho naředění jsou uvedeny v bodě 6.3.
6.5 Druh obalu a obsah balení
Bezbarvá skleněná injekční lahvička ( třída I) s pryžovou (brombutylovou) zátkou a hliníkovým uzávěrem s polypropylenovým víčkem. Lahvičky mohou být potaženy ochranným pouzdrem.
Balení
1 x 4ml lahvička (100 mg/4 ml)
1 x 20ml lahvička (500 mg/20 ml)
1 x 40ml lahvička (1000 mg/40 ml)
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a zacházení s ním
1. Při ředění pemetrexedu k podání intravenózní infuze používejte aseptickou techniku.
2. Vypočtěte dávku a počet potřebných injekčních lahviček přípravku Armisarte.
3. Přípravek Armisarte musí být ředěn pouze 5% roztokem glukózy, bez konzervačních látek. Náležitý objem koncentrátu pemetrexedu musí být naředěn na 100 ml injekčním roztokem 5% glukózy a podá se intravenózní infuzí po dobu 10 minut.
4. Infuzní roztoky pemetrexedu připravené podle návodu jsou kompatibilní s polyvinylchloridovými a polyolefinovými infuzními sety a infuzními vaky.
5. Léčivé přípravky pro parenterální použití se musí před podáním vizuálně zkontrolovat, zda neobsahují pevné částice a nedošlo ke změně barvy. Jestliže zpozorujete pevné částice, přípravek nepodávejte.
6. Roztok pemetrexedu je určen pouze na jedno použití. Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
Bezpečnostní opatření při přípravě a podání
Tak jako i u jiných potenciálně toxických cytostatických látek je nutné udržovat pozornost při zacházení s infuzním roztokem pemetrexedu a při jeho přípravě. Doporučuje se používat ochranné rukavice. Pokud
dojde ke kontaktu roztoku pemetrexedu s kůží, umyjte ihned a důkladně kůži mýdlem a vodou. Pokud dojde ke kontaktu roztoku pemetrexedu se sliznicemi, opláchněte je důkladně vodou. Pemetrexed není puchýřotvorná látka. V případě podání paravazálně neexistuje specifické antidotum. Bylo popsáno několik případů podání pemetrexedu paravazálně, které hodnotící lékař nepovažoval za závažné. Únik pemetrexedu mimo žílu se léčí místními standardními postupy jako u jiných nepuchýřotvorných látek.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Actavis Group PTC ehf.
Reykjavíkurvegi 76-78 220 Hafnarfjordur Island
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/15/1063/001
EU/1/15/1063/002
EU/1/15/1063/003
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 18. ledna 2016
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky na adrese http://www.ema.europa.eu.
A. VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE ODPOVĚDNÝ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce odpovědného za propouštění šarží
Actavis Italy S.p.A Via Pasteur, 10 20014
Nerviano, Milan Itálie
S.C. SINDAN-PHARMA S.R.L.
11 Ion Mihalache Blvd.
RO-011171 Bucharest Rumunsko
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propuštění dané šarže.
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis s omezením (viz Příloha I: Souhrn údajů o přípravku, 4.2).
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Požadavky na předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny na seznamu referenčních údajů Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a jakékoli následné změny zveřejněny na evropském webovém portálu pro léčivé přípravky
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
• Opatření k minimalizaci rizik
Neuplatňuje se.
Povinnost uskutečnit poregistrační opatření
Neuplatňuje se.
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Armisarte 25 mg/ml koncentrát pro infuzní roztok pemetrexedum
2. OBSAH LÉČIVÉ LÁTKY/LÁTEK
Jeden ml obsahuje 25 mg pemetrexedum 25 mg (jako pemetrexedum dinatricum dihemihydricum).
Jedna 4ml injekční lahvička obsahuje pemetrexedum 100 mg (jako pemetrexedum dinatricum dihemihydricum).
|
dihemihydricum). | |
|
Jedna 40ml injekční lahvička obsahuje pemetrexedum 1000 mg (jako pemetrexedum dinatricum | |
|
dihemihydricum). | |
3. SEZNAM POMOCNÝCH LÁTEK
Jedna 20ml injekční lahvička obsahuje pemetrexedum 500 mg(jako pemetrexedum dinatricum
Pomocné látky: trometamol, bezvodá kyselina citronová, monohydrát cystein-hydrochloridu a vodu na injekci.
Koncentrát pro infuzní roztok.
4ml injekční lahvička 20ml injekční lahvička 40 ml injekční lahvička
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní podání a naředění.
Pouze pro jednorázové podání.
Uchovávejte mimo dohled a dosah dětí.
Cytotoxická látka.
Musí být ředěn pouze 5 % roztokem glukózy.
8 POUŽITELNOST
Použitelné do:
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte a přepravujte v chladu.
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKU NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ_
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Actavis Group PTC ehf. Reykjavíkurvegi 76-78 220 Hafnarfjoróur Island
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/15/1063/001 4ml lahvička EU/1/15/1063/002 20ml lahvička EU/1/15/1063/003 40ml lahvička
13. ČÍSLO ŠARŽE
Č.šarže:
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVE PÍSMU
Nevyžaduje se - odůvodnění přijato.
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITRNÍM OBALU ŠTÍTEK INJEKČNÍ LAHVIČKY
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Armisarte 25 mg/ml koncentrát pro infuzní roztok
pemetrexedum
i.v.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
100 mg/4 ml 500 mg/20 ml 1000 mg/40 ml
5. JINÉ
Cytotoxická látka
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: Informace pro pacienta
Armisarte 25 mg/ml koncentrát pro infuzní roztok
pemetrexedum
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete dostávat tento přípravek, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoliv další otázky, zeptejte se svého lékaře nebo lékárníka.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků , sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je přípravek Armisartea k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete přípravek Armisarte používat
3. Jak se přípravek Armisarte používá
4. Možné nežádoucí účinky
5. Jak přípravek Armisarte uchovávat
6. Obsah balení s další informace
1. Co je přípravek Armisarte a k čemu se používá
Přípravek Armisarte je léčivý přípravek používaný k léčbě zhoubných nádorů. Obsahuje léčivou látku pemetrexed. Pemetrexed patří do skupiny léčiv znamých jako analoga kyseliny listové, které narušují procesy nezbytné pro buněčné dělení.
Přípravek Armisarte se podává pacientům bez předchozí chemoterapie v kombinaci s dalším protinádorovým lékem cisplatinou k léčbě maligního mezoteliomu pleury, což je forma zhoubného nádoru postihující výstelku dutiny hrudní a pokrývající plíce.
Přípravek Armisarte se v kombinaci s cisplatinou podává také jako počáteční léčba u pacientů s pokročilým stadiem rakoviny plic.
Přípravek Armisarte Vám může být předepsán i pokud máte rakovinu plic v pokročilém stadiu a pokud Vaše onemocnění příznivě reagovalo na léčbu nebo zůstalo po počáteční chemoterapii převážně nezměněno.
Přípravek Armisarte je rovněž určena k léčbě pacientů s pokročilým stadiem rakoviny plic, u kterých došlo k dalšímu rozvoji onemocnění poté, co byla použita jiná úvodní chemoterapie.
2. Čemu musíte věnovat pozornost, než začnete přípravek Armisarte používat Nepoužívejte přípravek Armisarte
- jestliže jste alergický(á) na pemetrexed nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
- pokud kojíte, musíte během léčby přípravkem Armisarte přestat kojit.
- pokud jste nedávno byl(a) nebo máte být očkován(a) vakcínou proti žluté zimnici.
Upozornění a opatření
Před použitím přípravku Armisarte se poraďte se svým lékařem nebo nemocničním lékárníkem.
Pokud máte nebo jste měl(a) problémy s ledvinami, oznamte to svému lékaři nebo nemocničnímu lékárníkovi, protože by nemuselo být vhodné, abyste dostával(a) přípravek Armisarte.
Před každou infuzí Vám bude odebrána krev k vyšetření, zda máte v pořádku funkci ledvin a jater a ke kontrole, zda máte dostatečný počet krvinek, abyste mohl(a) dostat přípravek Armisarte. Váš lékař se může rozhodnout změnit dávku nebo odložit léčbu v závislosti na Vašem celkovém zdravotním stavu a v případě, že máte příliš nízký počet krvinek. Pokud je Vám podána rovněž cisplatina, Váš lékař zkontroluje, zda jste dostatečně hydratován(a) a před léčbou cisplatinou a po ní dostanete vhodné léky, které zabrání zvracení.
Oznamte svému lékaři, pokud jste podstoupil(a) nebo máte podstoupit léčbu ozařováním, protože může dojít k časné nebo opožděné reakci na ozařování při používání přípravku Armisarte.
Oznamte svému lékaři, jestliže jste byl(a) nedávno očkován(a), protože pak může při používání přípravku Armisarte dojít nežádoucím účinkům.
Oznamte svému lékaři, že máte nebo jste měl(a) srdeční onemocnění.
Pokud u Vás došlo k nahromadění tekutiny okolo plic, může se lékař rozhodnout před podáním přípravku Armisarte tuto tekutinu odstranit.
Děti a dospívající
Použití přípravku Armisarte u dětí a dospívajících není relevantní.
Další léčivé přípravky a přípravek Armisarte
Oznamte svému lékaři nebo lékárníkovi, pokud užíváte, jste v nedávné době užíval nebo možná budete užívat nějaké léky proti bolesti nebo zánětu (otokům), jako jsou tzv. nesteroidní protizánětlivé léky (NSA), včetně léků, které jsou volně prodejné bez lékařského předpisu ( jako je např. ibuprofen). Existuje mnoho druhů NSA s různou dobou účinnosti. Na základě plánovaného data infuze přípravku Armisarte a stavu funkce ledvin Vám lékař doporučí, které léky smíte používat a kdy je smíte používat. Pokud si nejste jistý(á), zeptejte se svého lékaře nebo lékárníka, zda některý z Vašich léků není NSA.
U přípravku Armisarte, stejně jako u jiných chemoterapeutik, není doporučeno kombinování s živými oslabenými vakcínami. Pokud možno mají být použity inaktivní vakcíny.
Těhotenství, kojení a plodnost
Pokud jste těhotná, domníváte se, že můžete být těhotná nebo plánujete otěhotnět, oznamte to svému lékaři a požádejte svého lékaře o radu dříve, než je Vám tento přípravek podán. Přípravku Armisarte je třeba se v těhotenství vyvarovat. Váš lékař s Vámi probere možná rizika používání přípravku Armisarte během těhotenství. Během léčby přípravkem Armisarte musejí ženy používat vhodnou antikoncepci.
Kojení
Pokud kojíte, oznamte to svému lékaři.
Během léčby přípravkem Armisarte se musí kojení přerušit.
Plodnost
Muži nemají počít dítě během léčby a po dobu 6 měsíců po skončení léčby přípravkem Armisarte a z těchto důvodů by měli během léčby přípravkem Armisarte a po dobu 6 měsíců po jejím skončení používat účinnou antikoncepci. Pokud během léčby tímto přípravkem nebo během 6 měsíců po ukončení této léčby chcete počít dítě, poraďte se se svým lékařem nebo lékárníkem. Můžete vyhledat konzultaci ohledně uchování spermií před zahájením léčby.
Řízení dopravních prostředků a obsluha strojů
Přípravek Armisarte může vyvolat únavu. Při řízení dopravních prostředků a obsluze strojů buďte opatrný(á).
3. Jak se přípravek Armisarte používá
Přípravek Armisarte 25/ml koncentrát pro infuzní roztok Vám bude vždy podán zdravotnickým pracovníkem. Dávka přípravku Armisarte je 500 mg na jeden čtvereční metr plochy povrchu těla. Tato plocha se vypočítá z Vaší výšky a tělesné hmotnosti. Lékař poté z tohoto údaje vypočte potřebnou dávku. Tato dávka může být upravena, případně léčba může být oddálena v závislosti na počtu krvinek a celkovém zdravotním stavu. Než Vám přípravek podán, nemocniční lékárník, zdravotní sestra nebo lékař smísí přípravek Armisarte koncentrát se sterilním roztokem o koncentraci 5% glukózy.
Přípravek Armisarte dostanete vždy v infuzi do žíly. Tato infuze bude trvat přibližně 10 minut.
Pokud dostanete přípravek Armisarte s cisplatinou:
Lékař nebo nemocniční lékárník vypočítá potřebnou dávku na základě Vaší výšky a tělesné hmotnosti. Cisplatina se podává rovněž do žíly a podává se přibližně 30 minut po ukončení infuze přípravku Armisarte. Infuze cisplatiny bude trvat přibližně 2 hodiny.
Infuze budete obvykle dostávat 1x za 3 týdny.
Další léky:
Kortikosteroidy: Váš lékař Vám předepíše tablety se steroidem (v dávce odpovídající 4 mg dexamethasonu dvakrát denně), které budete užívat den před léčbou přípravkem Armisarte, v den jeho podání a následující den po jeho podání. Tento lék budete dostávat ke snížení frekvence a závažnosti kožních reakcí, které lze předpokládat během protinádorové léčby.
Doplňování léčby o vitaminy: během léčby přípravkem Armisarte Vám Váš lékař předepíše užívat kyselinu listovou (vitamin) nebo multivitamin s obsahem kyseliny listové (350 až 1000 mikrogramů), který musíte užívat 1x denně. Během sedmi dní před první dávkou přípravku Armisarte si musíte vzít nejméně 5 dávek kyseliny listové. Po poslední dávce přípravku Armisarte musíte pokračovat 21 dní v užívání kyseliny listové. Dostanete rovněž injekci vitaminu BJ2 (1000 mikrogramů), a to v týdnu před podáním přípravku Armisarte a dále přibližně každých 9 týdnů (což odpovídá 3 cyklům léčby přípravkem Armisarte). Vitamin B12 a kyselinu listovou dostanete ke snížení možných toxických účinků protinádorové léčby.
V průběhu léčby budete pečlivě sledováni. To běžně zahrnuje krevní testy, včetně kontrol správné funkce jater a ledvin. Na základě výsledků těchto testů může být Vaše dávka změněna nebo léčba oddálena.
Máte-li jakékoli další otázky, týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Jestliže zaznamenáte jakýkoliv z níže uvedených nežádoucích účinků, musíte ihned kontaktovat svého
lékaře:
- Horečka nebo infekce (časté): pokud máte teplotu 38 °C nebo vyšší, pocení nebo jiné známky infekce (protože můžete mít méně bílých krvinek než je obvyklé, což je velmi časté). Infekce (sepse) může mít závažný průběh a může vést k úmrtí
- Pokud začnete pociťovat bolest na hrudi (časté) nebo máte rychlou srdeční frekvenci (méně časté)
- Pokud máte bolesti, zarudnutí, otok nebo vřídky v ústech (velmi časté)
- Alergické reakce: pokud se vyvine kožní vyrážka (velmi časté) / pocity pálení nebo brnění (časté), případně horečka (časté). Ve vzácných případech může být kožní reakce závažná a může vést k úmrtí. Obraťte se na svého lékaře, pokud se u Vás vyskytne závažná vyrážka nebo svědění anebo puchýře (Stevens-Johnsonův syndrom nebo toxická epidermální nekrolýza)
- Pokud pozorujete únavu, slabost, snadnější zadýchávání nebo jste bledý(á) (protože můžete mít méně krevního barviva hemoglobinu, než je obvyklé, což je velmi časté)
- Pokud pozorujete krvácení z dásní, nosu nebo úst, případně jiné krvácení, které se obtížně zastavuje, načervenalou nebo narůžovělou moč, neočekávanou tvorbu modřin (protože můžete mít nižší počet krevních destiček, než je obvyklé, což je velmi časté)
- Pokud pozorujete náhlou dušnost, intenzivní bolest na hrudi nebo kašel s vykašláváním krve (méně časté) (může to znamenat přítomnost krevní sraženiny v plicních cévách)
Další nežádoucí účinky:
Velmi časté (může se vyskytnout u více než 1 z 10pacientů)
- Snížení počtu bílých krvinek
- Nízké hladiny hemoglobinu (anemie)
- Snížení počtu krevních destiček
- Průjem
- Zvracení
- Bolesti, zarudnutí, otok nebo vřídky v ústech
- Pocit na zvracení
- Ztráta chuti k jídlu
- Únava
- Kožní vyrážka, ztráta ochlupení
- Vypadávání vlasů
- Zácpa
- Ztráta hmatového citu
- Ledviny: abnormální nálezy při vyšetření krve
Časté (může se vyskytnout až u 1 ze 10pacienta)
- Alergické reakce: kožní vyrážka/pocity pálení nebo brnění
- Infekce včetně sepse
- Horečka
- Dehydratace
- Selhání ledvin
- Podráždění kůže a svědění
- Kopřivka
- Bolest na hrudi
- Svalová slabost
- Zánět spojivek
- Žaludeční nevolnost
- Bolesti břicha
- Změny vnímání chuti
- Játra: abnormální nálezy při vyšetření krve
- Zvýšené slzení
- Pocit na zvracení
Méně časté (může se vyskytnout až u 1 ze 100 pacientů)
- Náhlé selhání ledvin
- Zrychlení nebo nepravidelnosti srdečního tepu
- Zánět sliznice jícnu byl zaznamenán při kombinaci pemetrexedu a ozařování
- Kolitida (zánět tlustého střeva, který může být doprovázen střevním krvácením nebo krvácením z konečníku)
- Intersticiální pneumonitida (zjizvení plicních sklípků)
- Otoky (hromadění tekutin v tělesných tkáních vedoucím k otokům)
U některých pacientů se při léčbě pemetrexedem vyskytla srdeční příhoda, cévní mozková příhoda nebo malá mozková příhoda, obvykle při používání v kombinaci s další protinádorovou terapií.
- Pancytopenie-kombinované nízké počty bílých krvinek, červených krvinek a destiček
- U některých pacientů, kteří podstoupili před léčbou, v průběhu nebo po léčbě pemetrexedem ozařování, se může vyskytnout postradiační pneumonitida (zjizvení plicních sklípků v souvislosti s léčbou ozařováním)
- Byly hlášeny případy bolesti, snížené teploty a změny zbarvení končetin
- Krevní sraženiny v plicních cévách (plicní embolie)
Vzácné (může se vyskytnout až u 1 z 1 000 pacientů)
- Reakce nazývaná „radiation recall“ (kožní vyrážka podobná výraznému spálení od sluníčka), která se objeví na kůži, která byla před delší dobou vystavena záření -dny až roky.
- Výskyt puchýřů (zpuchýřující onemocnění kůže)-včetně Stevens-Johnsonova syndromu a toxické epidermální nekrolýzy
- Hemolytická anemie, vyvolaná imunitní reakcí (chudokrevnost způsobená rozpadem červených krvinek vyvolaným protilátkami)
- Hepatitida (zánět jater)
- Anafylaktický šok (těžká alergická reakce)
Může se u Vás vyskytnout jakýkoliv z těchto příznaků a/nebo onemocnění. Pokud zpozorujete některý z těchto nežádoucích účinků, musíte to oznámit svému lékaři, jakmile to bude možné.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak přípravek Armisarte uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, vyznačené na krabičce a štítku za Použitelné do:/EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte a přepravujte v chladu (2 °C - 8 °C).
Chraňte před mrazem.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
Infuzní roztok:
Chemická a fyzikální stabilita infuzního roztoku pemetrexedu po optevření před použitím byla prokázána na dobu 3 dní při pokojové teplotě a 21 dní při uchovávání v chladničce. Z mikrobiologického hlediska má být přípravek použit okamžitě. Není-li použit okamžitě, doba a podmínky uchovávání před použitím jsou v odpovědnosti uživatele a normálně nemá být doba delší než 24 hodin při teplotě 2 °C - 8 °C, pokud ředění neproběhlo za kontrolovaných a validovaných aseptických podmínek.
Přípravek Armisarte se nesmí používat, pokud jsou v roztoku přítomny částice.
Tento léčivý přípravek je určen pouze pro jednorázové podání, jakýkoliv nespotřebovaný roztok je nutné zlikvidovat v souladu s místními požadavky.
6. Obsah balení a další informace Co přípravek Armisarte obsahuje
Léčivou látkou je pemetrexedum. Jeden ml koncentrátu obsahuje pemetrexedum 25 mg (jako jako pemetrexedum dinatricum dihemihydricum).
Před podáním je nutné další naředění, které provede zdravotní personál.
Jedna 4ml injekční lahvička koncentrátu obsahuje pemetrexedum 100 mg (jako pemetrexedum dinatricum dihemihydricum).
Jedna 20ml injekční lahvička koncentrátu obsahuje pemetrexedum 500 mg (jako pemetrexedum dinatricum dihemihydricum).
Jedna 40ml injekční lahvička koncentrátu obsahuje pemetrexedum 1000 mg (jako pemetrexedum dinatricum dihemihydricum).
Pomocné látky jsou trometamol (k úpravě pH), bezvodá kyselina citronová, monohydrát cystein-hydrochloridu a voda na injekci.
Jak přípravek Armisarte vypadá a co obsahuje toto balení
Armisarte je čirý, bezbarvý až lehce nažloutlý nebo zeleně-žlutý roztok.
Přípravek Armisarte je k dispozici v bezbarvé skleněné injekční lahvičce s pryžovou zátkou a hliníkovým uzávěrem s polypropylenovým diskem. Lahvičky mohou být potaženy ochranným pouzdrem.
Jedno balení přípravku Armisarte obsahuje 1 injekční lahvičku.
Balení
1 x 4ml lahvička (100 mg/4 ml)
1 x 20ml lahvička (500 mg/20 ml)
1 x 40ml lahvička (1000 mg/40 ml)
Na trhu nemusí být všechny velikosti balení. Držitel rozhodnutí o registraci
Actavis Group PTC ehf. Reykjavíkurvegi 76-78 220 Hafnarfjoróur Island
Výrobce
Actavis Italy S.p.A. Viale Pasteur 10 200 14 Nerviano (Milan) Itálie
|
S.C. Sindan-Pharma S.R.L. | ||
|
11 Ion Mihalache Blvd. | ||
|
011171 Bucharest | ||
Rumunsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Belgie/Belgique/Belgien
Actavis Group PTC ehf.
IJsland
Bt^rapHH
AKTaBHC EAfl Tem: +359 2 9321 861
Česká republika
Actavis CZ a.s.
Tel: +420 251 113 002
Danmark
Actavis A/S
Tlf: +45 72 22 30 00
Deutschland
ratiopharm GmbH Tel: +49 731 402 02
Eesti
UAB “Actavis Baltics” Eesti Filiaal Tel: +372 6100 565
EkkáSa
Specifar ABEE
Tpk: +30 210 5401500
Espaňa
Teva Pharma, S.L.U.
Tél: +(34) 91 387 32 80
Lietuva
UAB “Actavis Baltics”
Tel: +370 5 260 9615
Luxembourg/Luxemburg
Actavis Group PTC ehf. Islande
Magyarország
Actavis Hungary Kft.
Tel.: +36 1 501 7001
Malta
Actavis Ltd.
Tel: +35621693533
Nederland
Actavis Group PTC ehf. IJsland
Norge
Actavis Norway AS Tlf: +47 815 22 099
Osterreich
Actavis GmbH
Tel: +43 (0)662 435 235 00
Polska
Actavis Export Int. Ltd., Malta Kontakt w Polsce:
Tel.: (+48 22) 512 29 00
France
Teva Santé
Tél: +(33) 1 55 91 7800
Hrvatska
PharmaVigil d.o.o.
Tel: +385(1)3890676
Ireland
Actavis Ireland Limited Tel: +353 (0)21 4619040
Ísland
Actavis Group PTC ehf.
Sími: +354 550 3300
Italia
Teva Italia S.r.l.
Tel: +(39) 028917981
Knnpoq
A. Potamitis Medicare Ltd Tr|k: +357 22583333
Latvija
UAB “Actavis Baltics” Latvijas filiále Tel: +371 67304300
Portugal
Actavis Group PTC ehf.
Islándia
Románia
Actavis SRL
Tel: +40 21 318 17 77
Slovenija
Apta Medica Internacional d.o.o. Tel: +386 51 615 015
Slovenská republika
Actavis s.r.o.
Tel: +421 2 3255 3800
Suomi/Finland
Actavis Oy
Puh/Tel: +358 (0)9 348 233
Sverige
Actavis AB Tel: +46 8 13 63 70
United Kingdom
Actavis UK Limited Tel: +44 1271 385257
Tato příbalová informace byla naposledy revidována:
Další zdroje informací
Podrobné informace o tomto přípravku jsou uveřejněny na webových stránkách Evropské lékové agentury (EMEA) http://www.emea.europa.eu/
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Návod k použití přípravku, zacházení s ním a k jeho likvidaci
1. Při ředění pemetrexedu k podání intravenózní infuze používejte aseptickou techniku.
2. Vypočtěte dávku a počet potřebných injekčních lahviček přípravku Armisarte.
3. Přípravek Armisarte musí být ředěn 5% injekčním roztokem glukózy, bez konzervačních látek. Náležitý objem roztoku pemetrexedu musí být dále naředěna 100 ml injekčním roztokem 5% glukózy a podá se intravenózní infuzí po dobu 10 minut.
4. Infuzní roztoky pemetrexedu, připravené podle návodu, jsou kompatibilní s polyvinylchloridovými a polyolefinovými infuzními sety a infuzními vaky. Pemetrexed je inkompatibilní s rozpouštědly obsahujícími kalcium, jako je laktátový Ringerův roztok a Ringerův roztok.
Přípravek Armisarte obsahuje pomocnou látku trometamol. Trometamol je inkompatibilní s cisplatinou, způsobuje rozklad cisplatiny Tento léčivý přípravek nesmí být smíchán s dalšími léčivými přípravky. Po podání přípravku Armisarte mají být intravenozní linky propláchnuty.
5. Léčivé přípravky pro parenterální použití se musí před podáním vizuálně prohlédnout, zda neobsahují částečky a nedošlo ke změně barvy. Jestliže zpozorujete pevné částice, přípravek nepodávejte.
6. Roztok pemetrexedu je určen pouze na jedno použití. Veškerý nepoužitý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
Bezpečnostní opatření při přípravě a podání:
Tak jako i u jiných potenciálně toxických cytostatických látek je nutné udržovat pozornost při zacházení s infuzním roztokem pemetrexedu a při jeho přípravě. Doporučuje se používat ochranné rukavice. Pokud dojde ke kontaktu roztoku pemetrexedu s kůží, umyjte ihned a důkladně kůži mýdlem a vodou. Pokud dojde ke kontaktu roztoku pemetrexedu se sliznicemi, opláchněte je důkladně vodou. Pemetrexed není puchýřotvorná látka. V případě podání paravazálně neexistuje specifické antidotum. Bylo popsáno několik případů podání pemetrexedu paravazálně, které hodnotící lékař nepovažoval za závažné. Únik pemetrexedu mimo žílu se léčí podle místních standardních postupů jako u jiných nepuchýřotvorných látek.
Po naředění roztoku
Chemická a fyzikální stabilita infuzního roztoku pemetrexedu po otevření před použitím byla prokázána na dobu 3 dní při pokojové teplotě a 21 dní při uchovávání v chladničce. Z mikrobiologického hlediska má být přípravek použit okamžitě. Není-li použit okamžitě, doba a podmínky uchovávání před použitím jsou v odpovědnosti uživatele a normálně nemá být doba delší než 24 hodin při teplotě 2 °C - 8 °C, pokud ředění neproběhlo za kontrolovaných a validovaných aseptických podmínek.
43