Aranesp 300 Mikrogramů
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce. Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce.
Aranesp 10 mikrogramů, injekční roztok v předplněném peru.
Aranesp 15 mikrogramů, injekční roztok v předplněném peru.
Aranesp 20 mikrogramů, injekční roztok v předplněném peru.
Aranesp 30 mikrogramů, injekční roztok v předplněném peru.
Aranesp 40 mikrogramů, injekční roztok v předplněném peru.
Aranesp 50 mikrogramů, injekční roztok v předplněném peru.
Aranesp 60 mikrogramů, injekční roztok v předplněném peru.
Aranesp 80 mikrogramů, injekční roztok v předplněném peru.
Aranesp 100 mikrogramů, injekční roztok v předplněném peru.
Aranesp 130 mikrogramů, injekční roztok v předplněném peru.
Aranesp 150 mikrogramů, injekční roztok v předplněném peru.
Aranesp 300 mikrogramů, injekční roztok v předplněném peru.
Aranesp 500 mikrogramů, injekční roztok v předplněném peru.
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce.
Aranesp 40 mikrogramů injekční roztok v injekční lahvičce.
Aranesp 60 mikrogramů injekční roztok v injekční lahvičce.
Aranesp 100 mikrogramů injekční roztok v injekční lahvičce.
Aranesp 200 mikrogramů injekční roztok v injekční lahvičce.
Aranesp 300 mikrogramů injekční roztok v injekční lahvičce.
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 10 mikrogramů (darbepoetin alfa) v 0,4 ml (25 pg/ml).
Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 15 mikrogramů (darbepoetin alfa) v 0,375 ml (40 pg/ml).
Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 20 mikrogramů (darbepoetin alfa) v 0,5 ml (40 pg/ml).
Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 30 mikrogramů (darbepoetin alfa) v 0,3 ml (100 pg/ml).
Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 40 mikrogramů (darbepoetin alfa) v 0,4 ml (100 pg/ml).
Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 50 mikrogramů (darbepoetin alfa) v 0,5 ml (100 pg/ml).
Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 60 mikrogramů (darbepoetin alfa) v 0,3 ml (200 pg/ml).
Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 80 mikrogramů (darbepoetin alfa) v 0,4 ml (200 pg/ml).
Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 100 mikrogramů (darbepoetin alfa) v 0,5 ml (200 pg/ml).
Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 130 mikrogramů (darbepoetin alfa) v 0,65 ml (200 pg/ml).
Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 150 mikrogramů (darbepoetin alfa) v 0,3 ml (500 pg/ml).
Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 300 mikrogramů (darbepoetin alfa) v 0,6 ml (500 pg/ml).
Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce
Jedna předplněná injekční stříkačka obsahuje darbepoetinum alfa 500 mikrogramů (darbepoetin alfa) v 1 ml (500 pg/ml).
Aranesp 10 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 10 mikrogramů (darbepoetin alfa) v 0,4 ml (25 pg/ml).
Aranesp 15 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 15 mikrogramů (darbepoetin alfa) v 0,375 ml (40 pg/ml).
Aranesp 20 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 20 mikrogramů (darbepoetin alfa) v 0,5 ml (40 pg/ml).
Aranesp 30 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 30 mikrogramů (darbepoetin alfa) v 0,3 ml (100 pg/ml).
Aranesp 40 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 40 mikrogramů (darbepoetin alfa) v 0,4 ml (100 pg/ml).
Aranesp 50 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 50 mikrogramů (darbepoetin alfa) v 0,5 ml (100 pg/ml).
Aranesp 60 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 60 mikrogramů (darbepoetin alfa) v 0,3 ml (200 pg/ml).
Aranesp 80 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 80 mikrogramů (darbepoetin alfa) v 0,4 ml (200 pg/ml).
Aranesp 100 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 100 mikrogramů (darbepoetin alfa) v 0,5 ml (200 pg/ml).
Aranesp 130 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 130 mikrogramů (darbepoetin alfa) v 0,65 ml (200 pg/ml).
Aranesp 150 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 150 mikrogramů (darbepoetin alfa) v 0,3 ml (500 pg/ml).
Aranesp 300 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 300 mikrogramů (darbepoetin alfa) v 0,6 ml (500 pg/ml).
Aranesp 500 mikrogramů, injekční roztok v předplněném peru
Jedno předplněné pero obsahuje darbepoetinum alfa 500 mikrogramů (darbepoetin alfa) v 1 ml (500 pg/ml).
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce
Jedna injekční lahvička obsahuje darbepoetinum alfa 25 mikrogramů (darbepoetin alfa) v 1ml (25 pg/ml).
Aranesp 40 mikrogramů injekční roztok v injekční lahvičce
Jedna injekční lahvička obsahuje darbepoetinum alfa 40 mikrogramů (darbepoetin alfa) v 1 ml (40 pg/ml).
Aranesp 60 mikrogramů injekční roztok v injekční lahvičce
Jedna injekční lahvička obsahuje darbepoetinum alfa 60 mikrogramů (darbepoetin alfa) v 1 ml (60 pg/ml).
Aranesp 100 mikrogramů injekční roztok v injekční lahvičce
Jedna injekční lahvička obsahuje darbepoetinum alfa 100 mikrogramů (darbepoetin alfa) v 1 ml (100 pg/ml).
Aranesp 200 mikrogramů injekční roztok v injekční lahvičce
Jedna injekční lahvička obsahuje darbepoetinum alfa 200 mikrogramů (darbepoetin alfa) v 1 ml (200 pg/ml).
Aranesp 300 mikrogramů injekční roztok v injekční lahvičce
Jedna injekční lahvička obsahuje darbepoetinum alfa 300 mikrogramů (darbepoetin alfa) v 1 ml (300 pg/ml).
Darbepoetin alfa je vyroben genovou technologií v ovariálních buňkách čínského křečka (CHO-K1). Pomocná látka se známým účinkem:
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačceJedna předplněná injekční stříkačka obsahuje 1,52 mg sodíku v 0,4 ml.
Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,42 mg sodíku v 0,375 ml.
Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,90 mg sodíku v 0,5 ml.
Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,14 mg sodíku v 0,3 ml.
Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,52 mg sodíku v 0,4 ml.
Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,90 mg sodíku v 0,5 ml.
Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,14 mg sodíku v 0,3 ml.
Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,52 mg sodíku v 0,4 ml.
Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,90 mg sodíku v 0,5 ml.
Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 2,46 mg sodíku v 0,65 ml.
Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 1,14 mg sodíku v 0,3 ml.
Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 2,27 mg sodíku v 0,6 ml.
Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce Jedna předplněná injekční stříkačka obsahuje 3,79 mg sodíku v 1 ml.
Aranesp 10 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,52 mg sodíku v 0,4 ml. Aranesp 15 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,42 mg sodíku v 0,375 ml. Aranesp 20 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,90 mg sodíku v 0,5 ml. Aranesp 30 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,14 mg sodíku v 0,3 ml. Aranesp 40 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,52 mg sodíku v 0,4 ml. Aranesp 50 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,90 mg sodíku v 0,5 ml. Aranesp 60 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,14 mg sodíku v 0,3 ml. Aranesp 80 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,52 mg sodíku v 0,4 ml. Aranesp 100 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,90 mg sodíku v 0,5 ml. Aranesp 130 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 2,46 mg sodíku v 0,65 ml. Aranesp 150 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 1,14 mg sodíku v 0,3 ml. Aranesp 300 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 2,27 mg sodíku v 0,6 ml. Aranesp 500 mikrogramů, injekční roztok v předplněném peru Jedno předplněné pero obsahuje 3,79 mg sodíku v 1 ml.
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce Jedna injekční lahvička obsahuje 3,79 mg sodíku.
Aranesp 40 mikrogramů injekční roztok v injekční lahvičce Jedna injekční lahvička obsahuje 3,79 mg sodíku.
Aranesp 60 mikrogramů injekční roztok v injekční lahvičce Jedna injekční lahvička obsahuje 3,79 mg sodíku.
Aranesp 100 mikrogramů injekční roztok v injekční lahvičce Jedna injekční lahvička obsahuje 3,79 mg sodíku.
Aranesp 200 mikrogramů injekční roztok v injekční lahvičce Jedna injekční lahvička obsahuje 3,79 mg sodíku.
Aranesp 300 mikrogramů injekční roztok v injekční lahvičce Jedna injekční lahvička obsahuje 3,79 mg sodíku.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Injekční roztok (injekce) v předplněné injekční stříkačce. Injekční roztok (injekce) v předplněném peru (SureClick). Injekční roztok (injekce) v injekční lahvičce.
Čirý, bezbarvý roztok.
KLINICKÉ ÚDAJE
4.
4.1 Terapeutické indikace
Léčba symptomatické anémie doprovázející chronické selhání ledvin u dospělých a dětských pacientů (viz bod 4.2).
Léčba symptomatické anémie u dospělých pacientů s maligním nádorovým onemocněním nemyeloidního typu, kteří dostávají chemoterapii.
4.2 Dávkování a způsob podání
Terapie Aranespem by měla být zahajována lékařem se zkušenostmi ve výše uvedených indikacích. Dávkování
Léčba symptomatické anémie u dospělých a dětských pacientů s chronickým selháním ledvin
Symptomy a následky anemie mohou být různé podle věku, pohlaví a celkové závažnosti nemoci; je nezbytné, aby lékař individuálně zvážil průběh nemoci a stav pacienta. Aranesp má být podáván buď subkutánně nebo intravenózně pro zvýšení hemoglobinu na hladinu ne vyšší než 12 g/dl (7,5 mmol/l). U nedialyzovaných pacientů je upřednostňováno subkutánní podání z důvodu zamezení vpichů do periferních žil.
Je třeba pacienty pečlivě sledovat, aby byla zajištěna adekvátní kontrola symptomů anemie za použití co nejnižší schválené dávky Aranespu při současném udržení koncentrace hemoglobinu nižší nebo rovné 12 g/dl (7,5 mmol/l).
U pacientů s chronickým selháním ledvin je třeba zvyšovat dávky Aranespu opatrně. U pacientů se slabou odpovědí hemoglobinu na Aranesp je třeba zvážit alternativní vysvětlení pro tuto slabou odpověď (viz bod 4.4 a 5.1).
Z důvodu individuálních rozdílů mezi pacienty mohou být příležitostně pozorovány koncentrace hemoglobinu vyšší či nižší než požadované. Variabilita hodnot hemoglobinu by měla být řešena pomocí úprav dávkování, přičemž cílová hladina hemoglobinu je mezi 10 g/dl (6,2 mmol/l) a 12 g/dl (7,5 mmol/l). Je třeba vyvarovat se koncentrace hemoglobinu trvale vyšší než 12 g/dl (7,5 mmol/l); níže je popsána úprava dávky v případě, kdy jsou pozorovány koncentrace hemoglobinu převyšující 12 g/dl (7,5 mmol/l). Je třeba se vyhnout vzestupu hemoglobinu o více než 2 g/dl (1,25 mmol/l) za čtyři týdny. V případě, že k němu dojde, je třeba upravit dávkování, jak je uvedeno.
Léčbu Aranespem rozdělujeme do dvou stupňů, na korekční a udržovací fázi: Pokyny jsou samostatné pro dospělé a dětské pacienty.
Dospělí pacienti s chronickým selháním ledvin
Korekční fáze:
Úvodní dávka pro subkutánní i intravenózní aplikaci je 0,45 pg/kg tělesné hmotnosti v jedné injekci podávaná jednou týdně. V případě, že je lék podáván nedialyzovaným pacientům, mohou být následuj ící úvodní dávky také podávány v jedné subkutánní inj ekci: 0,75 pg/kg j ednou za dva týdny nebo 1,5 mg/kg jednou za měsíc. Pokud vzestup koncentrace hemoglobinu není dostatečný (nižší než 1 g/dl (0,6 mmol/l) za čtyři týdny) zvyšte dávku přibližně o 25%. Dávka nesmí být zvýšena častěji než jednou za čtyři týdny.
Pokud vzestup koncentrace hemoglobinu je vyšší než 2 g/dl (1,25 mmol/l) za čtyři týdny, snižte dávku přibližně o 25%. Pokud koncentrace hemoglobinu překročí 12 g/dl (7,5 mmol/l), je třeba zvážit snížení dávky. Jestliže hemoglobin stále stoupá, dávka by měla být snížena přibližně o 25%. Pokud hemoglobin stoupá i po snížení dávky, léčba by měla být dočasně vysazena, dokud se hladina hemoglobinu nezačne snižovat. V ten okamžik by měla být léčba znovu zahájena, a to dávkou přibližně o 25% nižší než předchozí dávka.
Koncentrace hemoglobinu je nutné sledovat jednou týdně nebo jednou za 2 týdny, dokud nebudou stabilní. V dalším průběhu je možno hemoglobin kontrolovat v delších intervalech.
Udržovací fáze:
U dialyzovaných pacientů je možno pokračovat s dávkami Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny. Dialyzovaným pacientům, kteří přecházejí z aplikace Aranespu jedenkrát týdně na jedenkrát za dva týdny by měla být zpočátku podávána dávka odpovídající dvojnásobku dávky podávané jedenkrát týdně.
U nedialyzovaných pacientů se může pokračovat s podáváním Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny nebo jednou měsíčně. Pokud je u pacientů léčených Aranespem jednou za dva týdny dosaženo požadované koncentrace hemoglobinu, může být Aranesp podáván subkutánně jednou měsíčně, počáteční dávka přitom odpovídá dvojnásobku předchozí dávky podávané jednou za dva týdny.
Dávkování by mělo být upravováno tak, aby byla udržena požadovaná koncentrace hemoglobinu.
Pokud je nutné dávku přizpůsobit, aby bylo možné koncentrace hemoglobinu udržet na žádoucích hodnotách, doporučuje se dávku upravit přibližně o 25%.
Pokud bude vzestup hladiny hemoglobinu vyšší než 2 g/dl (1,25 mmol/l) v průběhu čtyř týdnů, snižte v závislosti na rychlosti vzestupu dávku asi o 25 %. Pokud koncentrace hemoglobinu překročí 12 g/dl (7,5 mmol/l), je třeba zvážit snížení dávky. Jestliže hemoglobin stále stoupá, dávka by měla být snížena přibližně o 25%. Pokud hemoglobin stoupá i po snížení dávky, léčba by měla být dočasně vysazena, dokud se hladina hemoglobinu nezačne snižovat. V ten okamžik by měla být léčba znovu zahájena, a to dávkou přibližně o 25% nižší než předchozí dávka.
Po každé změně dávky nebo dávkovacího intervalu je nutné kontrolovat koncentrace hemoglobinu po týdnu nebo každý druhý týden. Změna dávky během udržovacího období léčby by se neměla provádět častěji než jednou za dva týdny.
Při změně způsobu podání se musí použít stejná dávka a koncentrace hemoglobinu je nutné kontrolovat jednou týdně nebo jednou za 2 týdny, aby bylo možné případně upravit dávku a udržet hemoglobin na žádoucích hodnotách.
Klinickými studiemi bylo prokázáno, že dospělí pacienti léčení pomocí r-HuEPO jedenkrát, dvakrát nebo třikrát týdně mohou přejít na terapii Aranespem jedenkrát týdně nebo jedenkrát za dva týdny. Úvodní týdenní dávku Aranespu (^g/týden) lze vypočítat vydělením celkové týdenní dávky r-HuEPO (IU/týden) číslem 200. Úvodní dávku Aranespu pro podávání jedenkrát za dva týdny (^g/jedenkrát za dva týdny) lze určit vydělením celkové dávky r-HuEPO podané v průběhu dvou týdnů číslem 200.
Z důvodu individuálních rozdílů je dále zapotřebí provést titraci na optimální terapeuticky účinnou dávku pro daného pacienta. Pokud dochází k převedení léčby z r-HuEPO na Aranesp, je zapotřebí kontrolovat koncentrace hemoglobinu jednou týdně nebo jednou za 2 týdny a je nutné použít stejný způsob podání.
Pediatrická populace s chronickým selháním ledvin
Léčba dětských pacientů mladších než 1 rok nebyla studována v randomizovaných klinických studiích (viz bod 5.1).
Korekční fáze:
Pro pacienty od 1 roku je úvodní dávka pro subkutánní i intravenózní aplikaci 0,45 pg/kg tělesné hmotnosti v jedné injekci podávaná jednou týdně. V případě, že je lék podáván nedialyzovaným pacientům, může být zahajovací dávka 0,75 pg/kg podávána v jedné subkutánní injekci jednou za dva týdny. Pokud vzestup hemoglobinu není dostatečný (nižší než 1 g/dl (0,6 mmol/l) za čtyři týdny) zvyšte dávku přibližně o 25%. Dávka nesmí být zvýšena častěji než jednou za čtyři týdny.
Pokud vzestup hemoglobinu je vyšší než 2 g/dl (1,25 mmol/l) za čtyři týdny, snižte dávku přibližně o 25%, podle rychlosti vzestupu. Pokud koncentrace hemoglobinu překročí 12 g/dl (7,5 mmol/l), je třeba zvážit snížení dávky. Jestliže hemoglobin stále stoupá, dávka by měla být snížena přibližně o 25%. Pokud hemoglobin stoupá i po snížení dávky, léčba by měla být dočasně vysazena, dokud se hladina hemoglobinu nezačne snižovat. V ten okamžik by měla být léčba znovu zahájena, a to dávkou přibližně o 25% nižší než předchozí dávka.
Hodnotu hemoglobinu je nutné sledovat jednou týdně nebo jednou za 2 týdny, dokud nebude stabilní. V dalším průběhu je možno hemoglobin kontrolovat v delších intervalech.
Korekce anémie u dětských pacientů dávkami Aranespu jednou měsíčně nebyla studována.
Udržovací fáze:
Pro dětské pacienty od 1 roku v udržovací fázi je možno pokračovat s dávkami Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny. Pacienti mladší 6 let mohou potřebovat k udržení koncentrace hemoglobinu vyšší dávky než pacienti starší. Dialyzovaným pacientům, kteří přecházejí z aplikace Aranespu jedenkrát týdně na jedenkrát za dva týdny by měla být zpočátku podávána dávka odpovídající dvojnásobku dávky podávané jedenkrát týdně.
Pokud je u nedialyzovaných pacientů ve věku 11 let a více dosaženo požadované koncentrace hemoglobinu dávkou j ednou za dva týdny, může být Aranesp podáván subkutánně j ednou měsíčně, počáteční dávka přitom odpovídá dvojnásobku předchozí dávky podávané jednou za dva týdny.
Klinická data dětských pacientů léčených pomocí r-HuEPO dvakrát nebo třikrát týdně prokázala, žemohou přejít na terapii Aranespem jedenkrát týdně a pacienti léčení pomocí r-HuEPO jedenkrát týdně mohou přejít na terapii Aranespem jedenkrát za dva týdny. Úvodní týdenní dětskou dávku Aranespu (pg/týden) lze vypočítat vydělením celkové týdenní dávky r-HuEPO (IU/týden) číslem 240. Úvodní dvoutýdenní dávku Aranespu (pg/každý druhý týden) lze vypočítat vydělením celkové kumulativní dávky r-HuEPO podané za dobu dvou týdnů číslem 240. Z důvodu individuálních rozdílů je dále zapotřebí provést titraci na optimální terapeuticky účinnou dávku pro daného pacienta. Pokud dochází k převedení léčby z r-HuEPO na Aranesp, je zapotřebí kontrolovat koncentrace hemoglobinu jednou týdně nebo jednou za 2 týdny a je nutné použít stejný způsob podání.
Dávkování by mělo být upravováno tak, aby byla udržena požadovaná koncentrace hemoglobinu.
Pokud je nutné dávku přizpůsobit, aby bylo možné hemoglobin udržet na žádoucích hodnotách, doporučuje se dávku upravit přibližně o 25%.
Pokud bude vzestup hladiny hemoglobinu vyšší než 2 g/dl (1,25 mmol/l) v průběhu čtyř týdnů, snižte v závislosti na rychlosti vzestupu dávku asi o 25 %. Pokud koncentrace hemoglobinu překročí 12 g/dl (7,5 mmol/l), je třeba zvážit snížení dávky. Jestliže hemoglobin stále stoupá, dávka by měla být snížena přibližně o 25%. Pokud hemoglobin stoupá i po snížení dávky, léčba by měla být dočasně vysazena, dokud se hladina hemoglobinu nezačne snižovat. V ten okamžik by měla být léčba znovu zahájena, a to dávkou přibližně o 25% nižší než předchozí dávka.
Pacienty zahajující dialýzu během léčby přípravkem Aranesp je třeba pečlivě sledovat, aby byla zajištěna adekvátní kontrola hladiny hemoglobinu.
Po každé změně dávky nebo dávkovacího intervalu je nutné kontrolovat koncentrace hemoglobinu po týdnu nebo každý druhý týden. Změna dávky během udržovacího období léčby by se neměla provádět častěji než jednou za dva týdny.
Při změně způsobu podání se musí použít stejná dávka a koncentrace hemoglobinu je nutné kontrolovat jednou týdně nebo jednou za 2 týdny, aby bylo možné případně upravit dávku a udržet hemoglobin na žádoucích hodnotách.
Léčba symptomatické anémie navozené chemoterapií u pacientů s maligním nádorovým onemocněním
Pacientům s anémií (např. koncentrace hemoglobinu ^ 10 g/dl (6,2 mmol/l)) by měl být Aranesp aplikován subkutánní injekcí pro zvýšení hemoglobinu na hladinu ne vyšší než 12 g/dl (7,5 mmol/l). Symptomy a následky anemie mohou být různé podle věku, pohlaví a celkové závažnosti nemoci; je nezbytné, aby lékař individuálně zvážil průběh nemoci a stav pacienta.
Z důvodu individuálních rozdílů mezi pacienty mohou být příležitostně pozorovány koncentrace hemoglobinu vyšší či nižší než požadované. Variabilita hodnot hemoglobinu by měla být řešena pomocí úprav dávkování, přičemž cílová hladina hemoglobinu je mezi 10 g/dl (6,2 mmol/l) a 12 g/dl (7,5 mmol/l). Je třeba vyvarovat se koncentrace hemoglobinu trvale vyšší než 12 g/dl (7,5 mmol/l); níže je popsána úprava dávky v případě, kdy jsou pozorovány koncentrace hemoglobinu převyšující 12 g/dl (7,5 mmol/l).
Doporučená úvodní dávka je 500 pg (6,75 pg/kg) podávaná jednou za tři týdny nebo podávání 2,25 pg/kg tělesné hmotnosti jednou týdně. Není-li klinická odpověď pacienta (únava, koncentrace hemoglobinu) po 9 týdnech léčby dostatečná, nebude pravděpodobně další léčba účinná.
Léčba Aranespem by měla být ukončena přibližně čtyři týdny po ukončení chemoterapie.
Jakmile bylo u pacienta dosaženo terapeutického cíle, dávka přípravku by měla být snížena o 25 až 50%, aby byla zajištěna hladina hemoglobinu na úrovni omezující symptomy anémie za použití nejnižší schválené dávky Aranespu. Je třeba zvážit titraci dávky mezi 500 pg, 300 pg a 150 pg.
Pacienti musí být pečlivě monitorováni, pokud koncentrace hemoglobinu převýší 12 g/dl (7,5 mmol/l), dávka by měla být snížena přibližně o 25-50%. Pokud hladina hemoglobinu přesáhne 13 g/dl (8,1 mmol/l), léčba Aranespem by měla být dočasně přerušena. Poté, co hladina hemoglobinu klesne na 12 g/dl (7,5 mmol/l) nebo níže, léčba by měla být znovu zahájena dávkou přibližně o 25% nižší než předchozí dávka.
Bude-li během 4 týdnů vzestup hladiny hemoglobinu vyšší než 2 g/dl (1,25 mmol/l), dávka přípravku by měla být snížena o 25 až 50%.
Způsob podání
Aranesp 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300, 500 mikrogramů injekční roztok v předplněné injekční stříkačce
Aranesp se podává subkutánně nebo intravenózně tak, jak je popsáno v dávkování.
Měňte místa vpichu a aplikujte pomalu, aby podání léku nebylo nepříjemné.
Aranesp se dodává připravený k okamžitému použití v předplněné injekční stříkačce.
Aranesp 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300, 500 mikrogramů injekční roztok v předplněném peru
Aranesp v předplněném peru je určen pouze k subkutánnímu podání.
Měňte místa vpichu, aby podání léku nebylo nepříjemné.
Aranesp se dodává připravený k okamžitému použití v předplněném peru.
Aranesp 25, 40, 60, 100, 200, 300 mikrogramů injekční roztok v injekční lahvičce Aranesp se podává subkutánně nebo intravenózně tak, jak je popsáno v dávkování.
Měňte místa vpichu a aplikujte pomalu, aby podání léku nebylo nepříjemné.
Aranesp se dodává připravený k okamžitému použití v injekční lahvičce.
Pokyny k použití přípravku, zacházení s ním a k jeho likvidaci jsou uvedeny v bodě 6.6.
4.3 Kontraindikace
Hypersensitivita na na léčivou látku nebo na kteroukoliv pomocnou látku uvedenou v bodě 6.1. Neuspokojivě léčená hypertenze.
4.4 Zvláštní upozornění a opatření pro použití Obecné
Pro lepší dohledatelnost erytropoezu stimulujících faktorů (ESA) se má v dokumentaci pacienta zřetelně zaznamenávat (nebo uvádět) obchodní název podaného ESA.
U všech pacientů, zvláště během zahájení léčby Aranespem, je zapotřebí kontrolovat krevní tlak. Pokud je krevní tlak obtížně kontrolovatelný zavedením vhodných opatření, poklesu hemoglobinu může být dosaženo snížením nebo pozdržením dávky Aranespu (viz bod 4.2). U pacientů s chronickým selháním ledvin léčených Aranespem byly pozorovány případy závažné hypertenze zahrnující hypertenzní krizi, hypertenzní encefalopatii a křeče.
Aby byla zaručena efektivní erytropoeza, měla by být u všech pacientů vyšetřena hladina železa, a to před léčbou i během léčby a mělo by být zváženo případné doplňkové podávání přípravků železa.
Absence odpovědi na léčbu Aranespem byl měla být pobídkou k hledání příčiny. Nedostatek železa, kyseliny listové nebo vitaminu B12 snižuje účinnost ESA a měl by být upraven. Odpověď na terapii erytropoetinem může být také nepříznivě ovlivněna interkurentní infekcí, zánětlivým procesem nebo traumatem, okultní krevní ztrátou, hemolýzou, těžkou otravou hliníkem, vlastním hematologickým onemocněním nebo fibrózou kostní dřeně. Jako součást hodnocení by měl být uvažován počet retikulocytů. Pokud jsou vyloučeny typické příčiny negativní odpovědi a pacient má retikulopenii, mělo by se zvážit vyšetření kostní dřeně. Jestliže je kostní dřeň shodná s PRCA, měl by být proveden test na anti-erytropoetinové protilátky.
Čistá aplasie červených buněk způsobená neutralizací anti-erytropoetinovými protilátkami byla hlášena v souvislosti s ESA včetně Aranespu. Tato hlášení se týkala převážně subkutánně léčených pacientů s chronickým selháním ledvin. Tyto protilátky reagovaly křížově se všemi erytropoetinovými proteiny a pacienti s podezřením nebo s potvrzenými neutralizujícími protilátkami k erytropoetinu by neměli být převedeni na Aranesp (viz bod 4.8).
V případě paradoxního poklesu hemoglobinu a vzniku závažné anémie spojené s nízkým počtem retikulocytů je nutné přerušit léčbu epoetinem a provést vyšetření anti-erytropoetinových protilátek. Byly hlášeny případy pacientů s hepatitidou C léčených interferonem a ribavirinem a současně epoetiny. Epoetiny nejsou schváleny pro léčbu anémie spojené s hepatitidou C.
Aktivní onemocnění jater bylo vylučovacím kritériem ve všech studiích s Aranespem; data od pacientů s poškozenou funkcí jater nejsou proto dostupná. Játra jsou považována za hlavní cestu eliminace darbepoetinu alfa a r-HuEPO. Z tohoto důvodu by Aranesp měl být pacientům s jaterním onemocněním podáván pouze s nezbytnou opatrností.
Aranesp by měl rovněž být podáván opatrně pacientům se srpkovitou anémií.
Nesprávné použití Aranespu zdravými osobami může vést k excesivnímu nárůstu objemu zhuštěných buněk. To může být doprovázeno život ohrožujícími kardiovaskulárními komplikacemi.
Kryt jehly předplněné injekční stříkačky nebo předplněného pera obsahuje suchou přírodní gumu (derivát latexu), která může způsobovat alergické reakce.
Aranesp by měl být s opatrností používán u pacientů s epilepsií. U pacientů, kteří dostávali Aranesp, byly hlášeny křeče.
Tento přípravek obsahuje méně než 1 mmol sodíku (23 mg) v dávce, to znamená, že je v podstatě bez sodíku.
Pacienti s chronickým selháním ledvin
U pacientů s chronickým selháním ledvin je potřeba zvyšovat dávky Aranespu s opatrností, protože vysoké kumulující se dávky epoetinu mohou být spojeny se zvýšeným rizikem mortality, závažnými kardiovaskulárními a cerebrovaskulárními příhodami. U pacientů se slabou odpovědí hemoglobinu na epoetiny je třeba zvážit alternativní vysvětlení pro tuto slabou odpověď (viz body 4.2 a 5.1).
Udržovací koncentrace hemoglobinu by u pacientů s chronickým selháním ledvin neměla překročit horní limit cílové koncentrace doporučované v bodě 4.2. V klinických studiích bylo pozorováno zvýšené riziko úmrtí, závažných kardiovaskulárních a cerebrovaskulárních příhod včetně iktu a trombóz cévních přístupů, pokud byly ESA podávány ke zvýšení hemoglobinu na cílovou hladinu vyšší než 12 g/dl (7.5 mmol/l).
Kontrolované klinické studie neukázaly signifikantní přínosy, které by bylo možno zdůvodnit podáváním epoetinů v případě, kdy byla koncentrace hemoglobinu zvýšena nad úroveň nezbytnou ke kontrole symptomů anémie a zamezení krevních transfuzí.
Doplňková terapie přípravky železa se doporučuje pro všechny pacienty s hodnotou ferritinu v séru pod 100 pg/l anebo se saturací transferrinu pod 20%.
Během léčby Aranespem je zapotřebí pravidelně sledovat hladiny kalia v séru. Zvýšení hladiny kalia bylo hlášeno u několika pacientů léčených Aranespem, i když příčinná souvislost nebyla stanovena. Pokud bude zaznamenána zvýšená nebo stoupající hladina kalia, je třeba zvážit ukončení podávání Aranespu, dokud nedojde k úpravě hladiny kalia.
Pacienti s maligním nádorovým onemocněním
Účinek na růst nádorů
Epoetiny jsou růstové faktory, které v první řadě stimulují tvorbu červených krvinek. Receptory pro erytropoetin se však mohou vyskytovat i na povrchu nejrůznějších nádorových buněk. Podobně jako u všech růstových faktorů, i zde existuje obava z toho, že by epoetiny mohly stimulovat růst maligních nádorů. V několika kontrolovaných studiích u anemických pacientů s maligním nádorovým onemocněním epoetiny nezlepšovaly celkové přežití ani nesnižovaly riziko progrese nádoru.
Použití Aranespu a jiných ESA v kontrolovaných klinických studiích ukázalo:
• zkrácení doby do progrese nádoru u pacientů s pokročilým nádorem hlavy a krku léčených radioterapií při podávání na cílovou hladinu vyšší než 14 g/dl (8,7 mmol/l), ESA nejsou indikovány pro použití u této skupiny pacientů.
• zkrácení celkového přežití a zvýšení počtu úmrtí v důsledku progrese onemocnění během 4 měsíců u pacientů s metastazujícím karcinomem prsu léčených chemoterapií při podávání na cílovou hladinu 12-14 g/dl (7,5-8,7 mmol/l).
• zvýšení rizika úmrtí při podání na cílovou hladinu 12 g/dl (7,5 mmol/l) u pacientů s aktivním maligním onemocněním neléčených ani chemoterapiíí ani radioterapií. ESA nejsou indikovány pro použití u této skupiny pacientů.
Na základě výše uvedené skutečnosti má být v některých klinických situacích preferovanou léčbou na zvládnutí anémie u pacientů s rakovinou krevní transfúze. Rozhodnutí podat rekombinantní erytropoetiny má vycházet z hodnocení přínosu a rizika s účastí pacienta, které má zohlednit specifický klinický kontext. Faktory, které je třeba zvážit, mají zahrnovat typ nádoru a jeho stádium; stupeň anémie, prognózu prežití, celkové prostředí, v kterém je pacient léčený; a preference pacienta (viz bod 5.1).
U pacientů se solidními nádory nebo s lymfoproliferativními malignitami, pokud hodnota hemoglobinu překročí 12 g/dl (7,5 mmol/l), je nutné přesně dodržovat schéma úpravy dávek popsané v bodě 4.2, aby bylo potenciální riziko tromboembolických příhod sníženo na minimum. V pravidelných intervalech je nutné kontrolovat počty krevních destiček a koncentrace hemoglobinu.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Dosud získané klinické výsledky nenaznačují žádné vzájemné působení darbepoetinu alfa s jinými léky. Potenciálně by však mohlo docházet k interakcím s látkami s vysokou vazbou na erytrocyty, jako jsou např. cyklosporin nebo takrolimus. Jestliže je Aranesp podáván souběžně s některou z těchto látek, je zapotřebí sledovat hladiny těchto látek v krvi a dávku upravit podle nárůstu hladin hemoglobinu.
4.6 Těhotenství a kojení
Nejsou k dispozici odpovídající a dobře kontrolované studie s Aranespem u těhotných žen.
Studie na zvířatech nenaznačují přímý škodlivý účinek na těhotenství, vývoj embrya nebo plodu, porod nebo vývoj po narození. Změna fertility nebyla zaznamenána.
Těhotným ženám je nutné Aranesp předepisovat s nezbytnou opatrností.
Ženám, které otěhotní během léčby Aranespem, je doporučeno přihlásit se do Programu sledování těhotenství firmy Amgen. Kontaktní údaje jsou uvedeny v bodě 6 Příbalové informace.
Kojení
Není známo, zda se Aranesp vylučuje do mateřského mléka. Riziko pro kojené děti nelze vyloučit. Je třeba rozhodnout, zda přerušit kojení nebo přerušit či odložit léčbu Aranespem při zvážení přínosu kojení pro dítě a přínosu léčby pro matku.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Aranesp nemá žádný vliv nebo má zanedbatelný vliv na schopnost řídit motorová vozidla nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Souhrn bezpečnostního profilu
Nežádoucí účinky zjištěné v souvislosti s Aranespem jsou hypertenze, iktus, tromboembolické příhody, křeče, alergické reakce, vyrážka/erytém a čistá aplazie červené krevní řady (PRCA); viz bod 4.4.
Ve studiích, ve kterých byl Aranesp aplikován subkutánně, byla v souvislosti s léčbou udávána bolestivost v místě vpichu. Obtíže pociťované v místě vpichu byly všeobecně mírné a přechodné povahy a vyskytovaly se převážně po prvním injekčním podání.
Tabulkový přehled nežádoucích účinků
Incidence nežádoucích účinků je uvedena níže podle tříd orgánových systémů a četnosti. Četnost je definována jako: Velmi časté (> 1/10); časté (> 1/100 až < 1/10); méně časté (> 1/1000 až < 1/100); vzácné (> 1/10000 až < 1/1000); velmi vzácné (< 1/10000), není známo (nelze odhadnout z dostupných dat).
Data jsou uvedena zvlášť pro pacienty s chronickým selháním ledvin (CRF) a onkologické pacienty z důvodu rozdílného profilu nežádoucích účinků v těchto skupinách.
Pacienti s chronickým selháním ledvin
Prezentované údaje o bezpečnosti čerpají z kontrolovaných studií, které zahrnovaly 1357 pacientů, z nichž 766 bylo léčeno Aranespem a 591 r-HuEPO. 83% pacientů léčených Aranespem bylo dialyzováno, zatímco 17% nikoli. Iktus byl identifikován jako nežádoucí účinek v dodatečné klinické studii (TREAT, viz bod 5.1).
Incidence nežádoucích účinků z kontrolovaných klinických studií a postmarketingového sledování je následující:
|
Třídy orgánových systémů podle MedDra |
Incidence |
Nežádoucí účinek |
|
Poruchy krve a lymfatického systému |
Není známo* |
Čistá aplazie červené krevní řady |
|
Poruchy imunitního systému |
Velmi časté* |
Hypersenzitivita |
|
Poruchy nervového systému |
Časté |
Iktus |
|
Méně časté* |
Křeče | |
|
Srdeční poruchy |
Velmi časté |
Hypertenze |
|
Cévní poruchy |
Méně časté |
Tromboembolické příhody |
|
Poruchy kůže a podkožní tkáně |
Časté |
Vyrážka/erytém |
|
Celkové poruchy a reakce v místě aplikace |
Časté |
Bolestivost v místě vpichu |
*viz bod „Popis vybraných nežádoucích účinků“
Pacienti s maligním nádorovým onemocněním
Nežádoucí účinky byly stanoveny na základě údajů shromážděných ze sedmi randomizovaných, dvojitě zaslepených, placebem kontrolovaných studií s Aranespem s celkovým počtem 2 112 pacientů (Aranesp 1 200, placebo 912). Klinické studie zahrnovaly pacienty se solidními tumory (např. plic, prsu, tlustého střeva, vaječníků) a s lymfatickými zhoubnými nádory (např. lymfom, mnohonásobný myelom).
Incidence nežádoucích účinků z kontrolovaných klinických studií a postmarketingového sledování je následující:
|
Třídy orgánových systémů podle MedDra |
Incidence |
Nežádoucí účinek |
|
Poruchy imunitního systému |
Velmi časté* |
Hypersenzitivita |
|
Poruchy nervového systému |
Méně časté* |
Křeče |
|
Srdeční poruchy |
Časté* |
Hypertenze |
|
Cévní poruchy |
Časté |
Tromboembolické příhody včetně plicní embolie |
|
Poruchy kůže a podkožní tkáně |
Časté |
Vyrážka/erytém |
|
Celkové poruchy a reakce v místě aplikace |
Velmi časté |
Edém |
|
Časté |
Bolestivost v místě vpichu |
*viz bod „Popis vybraných nežádoucích účinků“
Popis vybraných nežádoucích účinků
Pacienti s chronickým selháním ledvin
Iktus byl hlášen jako častý u CRF pacientů ve studii TREAT (viz bod 5.1).
Ve vzácných případech, a to převážně u subkutánně léčených pacientů s chronickým selháním ledvin, byl v souvislosti s léčbou Aranespem hlášen vznik aplazie červené krevní řady (PRCA), zprostředkovaný neutralizujicími protilátkami proti erytropoetinu. Pokud je stanovena diagnóza aplazie červené krevní řady, podávání Aranespu musí být přerušeno a pacienti by neměli být převáděni na jiný typ rekombinatního erytropoezu stimulujícího proteinu (viz bod 4.4).
Četnost všech reakcí hypersenzitivity byla odhadnuta z klinických studií jako velmi častá u CRF pacientů. V souvislosti s darbepoetinem alfa byly hlášeny závažné reakce hypersentivity včetně anafylaktické reakce, angioedému, alergického bronchospasmu, kožní vyrážky a kopřivky.
U pacientů dostávajících darbepoetin alfa byly hlášeny křeče (viz bod 4.4). U CRF pacientů je četnost z klinických studií odhadována jako méně častá.
Pacienti s maligním nádorovým onemocněním
U pacientů s maligním nádorovým onemocněním byla hypertenze pozorována v postmarketingovém sledování (viz bod 4.4). U těchto pacientů je četnost odhadována z klinických studií jako častá a byla rovněž častá ve skupinách s placebem.
Reakce hypersenzitivity byly pozorovány u pacientů s maligním nádorovým onemocněním v postmarketingovém sledování. Četnost všech reakcí hypersenzitivity byla odhadnuta z klinických studií jako velmi častá u těchto pacientů. Reakce hypersenzitivity byly rovněž velmi časté ve skupinách s placebem.V souvislosti s darbepoetinem alfa byly hlášeny závažné reakce hypersentivity včetně anafylaktické reakce, angioedému, alergického bronchospasmu, kožní vyrážky a kopřivky.
U pacientů dostávajících darbepoetin alfa byly hlášeny křeče v postmarketingovém sledování (viz bod 4.4). U pacientů s maligním nádorovým onemocněním je četnost z klinických studií odhadována jako méně častá. Ve skupinách s placebem byly křeče časté.
Pediatrická _populace s chronickým selháním ledvin
Ve všech studiích s pediatrickými CRF pacienty nebyly v porovnání s dospělými pacienty u pediatrických pacientů identifikovány žádné další nežádoucí účinky (viz bod 5.1).
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Nebylo stanoveno maximální množství Aranespu, které lze podat jednorázově nebo vícenásobně. Léčba Aranespem může způsobit polycytémii, pokud není pečlivě monitorován hemoglobin a dávky nejsou přiměřeně upravovány. Po předávkování Aranespem byly pozorovány případy závažné hypertenze (viz bod 4.4).
V případě polycytémie je třeba podávání Aranespu dočasně pozastavit (viz. bod 4.2). Pokud je klinicky indikováno, může být provedena flebotomie.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Antianemika, jiná antianemika ATC kód: B03XA02. Mechanismus účinku
Humánní erytropoetin je endogenním glykoproteinovým hormonem, který je primárním regulátorem erytropoezy prostřednictvím specifické interakce s receptorem erytropoetinu na erytroidních progenitorových buňkách v kostní dřeni. K tvorbě erytropoetinu a k její regulaci dochází primárně v ledvinách na základě změn tkáňové oxygenace. Tvorba endogenního erytropoetinu je narušena u pacientů s chronickým selháním ledvin a deficience erytropoetinu je primární příčinou anémie u těchto pacientů. U pacientů s maligním nádorovým onemocněním, kteří užívají chemoterapeutika, je etiologie anémie multifaktoriální. U těchto pacientů ke vzniku anémie významně přispívá nedostatek erytropoetinu a snížená odpověď erytroidních progenitorových buněk na endogenní erytropoetin.
Farmakodynamické účinky
Darbepoetin alfa stimuluje erytropoezu pomocí stejného mechanismu, jako je tomu u endogenního hormonu. Darbepoetin alfa má pět uhlohydrátových řetězců vázaných na dusík, zatímco endogenní hormon a rekombinantní humánní erytropoetiny (r-HuEPO) mají tři. Přídavná sacharidová rezidua jsou molekulárně neodlišitelná od reziduí na endogenním hormonu. Díky svému zvýšenému obsahu uhlohydrátů má darbepoetin alfa delší terminální poločas než r-HuEPO a v důsledku toho vyšší aktivitu in vivo. Navzdory molekulárním odlišnostem si darbepoetin alfa zachovává velmi úzkou specifitu pro receptor erytropoetinu.
Klinická účinnost a bezpečnost
Pacienti s chronickým selháním ledvin
U pacientů s chronickým selháním ledvin bylo ve dvou klinických studiích zjištěno vyšší riziko úmrtí a závažných kardiovaskulárních příhod, pokud jim byly podávány ESA na vyšší cílovou hladinu hemoglobinu ve srovnání s nižší cílovou hladinou (13,5 g/dl (8,4 mmol/l) oproti 11,3 g/dl (7,1 mmol/l); 14 g/dl (8,7 mmol/l) oproti 10 g/dl (6,2 mmol/l)).
V randomizované, dvojitě zaslepené korekční studii (n = 358) srovnávající dávkovací režim jednou za dva týdny a jednou měsíčně u nedialyzovaných pacientů s chronickým selháním ledvin nedosahovalo dávkování darbepoetinu alfa jednou měsíčně korekce anémie hůře než dávkování jednou za dva týdny.
Medián (interkvartilové rozmezí 1 - 3) doby do dosažení korekce hemoglobinu (> 10.0 g/dl a zvýšení > 1.0 g/dl od výchozí hodnoty) byl 5 týdnů pro oba dávkovači režimy, jednou za dva týdny (Q1, Q3 - 3, 7 týdnů) a jednou měsíčně (Q1, Q3 - 3, 9 týdnů). Po dobu hodnocení (týden 29 - 33) byla průměrná (95 % Cl) týdenní ekvivalentní dávka 0,20 (0,17; 0,24) gg/kg v rameni jednou za dva týdny a 0,27 (0,23; 0,32) gg/kg v rameni jednou za měsíc.
V randomizované, dvojitě zaslepené, placebem kontrolované studii (TREAT), které se zúčastnilo 4038 nedialyzovaných pacientů s chronickým selháním ledvin s diabetem typu II a hladinami hemoglobinu < 11 g/dl, dostávali pacienti buď darbepoetin alfa k dosažení hladiny hemoglobinu 13 g/dl nebo placebo (se záchranným podáním darbepoetinu alfa u hladin hemoglobinu nižších než 9 g/dl). Studie nesplnila ani primární cílový ukazatel důkazem snížení rizika celkové mortality nebo kardiovaskulární morbidity (darbepoetin alfa vs placebo; Hazard Ratio 1,05; 95% CI (0,94; 1,17)), nebo celkové mortality nebo konečného stadia onemocnění ledvin (ESRD) (darbepoetin alfa vs placebo; HR 1,06; 95% CI (0,95; 1,19)). Analýza jednotlivých složek komplexních cílů ukázala následující HR (95%
CI): úmrtí 1,05 (0,92; 1,21), městnavé srdeční selhání (ChF) 0,89 (0,74; 1,08), infarkt myokardu (MI) 0,96 (0,75; 1,23), iktus 1,92 (1,38; 2,68), hospitalizace z důvodu ischemie myokardu 0,84 (0,55; 1,27), ESRD 1,02 (0,87; 1,18).
Souhrnné post-hoc analýzy klinických studií s ESA byly provedeny u pacientů s chronickým selháním ledvin (dialyzovaných, nedialyzovaných, s diabetem a bez diabetu). Byla pozorována tendence směrem ke zvýšení odhadovaného rizika mortality z jakýchkoliv příčin, kardiovaskulárních a cerebrovaskulárních příhod spojených s vyššími kumulativními dávkami ESA nezávisle na diabetu nebo dialyzační léčbě (viz body 4.2 a 4.4).
Pediatrická populace
V randomizované klinické studii se 114 dialyzovanými i nedialyzovanými pediatrickými pacienty ve věku 2 - 18 let s chronickým onemocněním ledvin, kteří trpěli anémií (hemoglobin pod 10,0 g/dl) a nebyli léčeni ESA, byl pro korekci anémie podáván darbepoetin alfa jednou týdně (n = 58), nebo jednou za dva týdny (n = 56). Koncentrace hemoglobinu byly upraveny na hodnotu > 10 g/dl u více než 98 % (p < 0,001) dětských pacientů podáváním darbepoetinu alfa jednou týdně a u 84 %
(p = 0,293) podáváním jednou za dva týdny. V období, kdy bylo poprvé dosaženo koncentrace hemoglobinu > 10,0 g/dl, byla průměrná dávka (SD) vztažená na tělesnou hmotnost 0,48 (0,24) gg/kg (rozmezí: 0,0 až 1,7 gg/kg) týdně pro skupinu s podáváním jednou týdně a 0,76 (0,21) gg/kg (rozmezí: 0,3 až 1,5 gg/kg) dvoutýdennně pro skupinu s podáváním jednou za dva týdny.
V klinické studii se 124 dialyzovanými i nedialyzovanými pediatrickými pacienty s chronickým onemocněním ledvin ve věku 1 - 18 let, kteří byli stabilní na léčbě epoetinem alfa, byla provedena randomizace buď k podávání darbepoetinu alfa jednou týdně (subkutánně nebo intravenózně) za použití konverzního poměru 238: 1, nebo pokračovala léčba s epoetinem alfa dle aktuální dávky, harmonogramu a způsobu podání. Primární cílový parametr účinnosti [změna hemoglobinu mezi vstupním a hodnoceným obdobím (týden 21-28)] byl srovnatelný mezi oběma skupinami. Průměrné vstupní hladiny hemoglobinu byly pro rHuEPO 11,1 (SD 0,7) g/dl a pro darbepoetin alfa 11,3 (SD 0,6) g/dl. Průměrné hladiny hemoglobinu byly ve 28. týdnu pro rHuEPO 11,1 (SD 1,4) g/dl a pro darbepoetin alfa 11,1 (SD 1,1) g/dl.
Ve studii Evropského observačního registru, do které bylo zařazeno 319 pediatrických pacientů s chronickým onemocněním ledvin (13 (4,1 %) pacientů do 1 roku věku, 83 (26,0 %) pacientů od 1 roku do 6 let, 90 (28,2 %) pacientů od 6 do 12 let věku a 133 (41,7 %) pacientů od 12 let), kterým byl podáván darbepoetin alfa, byly průměrné koncentrace hemoglobinu v rozmezí mezi 11,3 a 11,5 g/dl a průměrné dávky darbepoetinu alfa vztažené na tělesnou hmotnost zůstávaly relativně konstantní (mezi 2,31 gg/kg za měsíc a 2,67 gg/kg za měsíc) v průběhu sledovaného období u celé studované populace.
V těchto studiích nebyly zjištěny žádné významné rozdíly mezi bezpečnostním profilem u pediatrických pacientů a již dříve uvedeným bezpečnostním profilem u dospělých pacientů (viz bod 4.8).
V prospektivní, randomizované, dvojitě slepé, placebem kontrolované studii prováděné u 314 pacientů s karcinomem plic, kteří byli léčeni chemoterapií zahrnující platinu, byla signifikantně redukována nutnost podání krevní transfúze (p < 0,001).
Klinické studie prokázaly, že darbepoetin alfa má obdobnou účinnost, je-li podáván v jedné injekci jednou za tři týdny, jednou za dva týdny nebo jednou týdně, a to bez nutnosti zvýšení celkové dávky.
V randomizované, dvojitě slepé mezinárodní studii byla posuzována bezpečnost a účinnost léčby přípravkem Aranesp při podávání jednou za tři týdny na snižování nutnosti transfuze erytrocytů u pacientů léčených chemoterapií. Studie se účastnilo 705 anemických pacientů s nemyleloidními malignitami léčených několika cykly chemoterapie. Pacienti byli randomizováni do skupiny, kde dostávali 500 pg Aranespu jednou za tři týdny, nebo do skupiny, ve které dostávali dávku 2,25 pg/kg jednou za týden. V obou skupinách byla dávka snížena o 40% (např. při prvním snížení na 300pg u dávkování jednou za tři týdny a na 1,35pg/kg u skupiny s dávkováním jednou za týden), pokud se hladina hemoglobinu zvýšila o více než 1g/dl během 14 dnů. Ve skupině s podáváním jednou za tři týdny vyžadovalo snížení dávky 72% pacientů. Ve skupině s dávkováním jednou za týden vyžadovalo snížení dávky 75% pacientů. Tato studie podporuje dávkování 500 pg jednou za tři týdny jako srovnatelné s podáváním jednou týdně co se týká incidence subjektů, které dostávají alespoň jednu transfuzi erytrocytů od týdne 5 do konce léčebné fáze.
V prospektivní, randomizované, dvojitě slepé, placebem kontrolované studii prováděné u 344 anemických pacientů s lymfoproliferativními maligními onemocněními, kteří byli léčeni chemoterapií, byla signifikantně redukována nutnost podání krevní transfúze a došlo ke zlepšení hemoglobinové odezvy (p < 0,001). Bylo rovněž zaznamenáno zlepšení únavnosti pacientů, které bylo hodnoceno pomocí škály pro Funkční hodnocení únavnosti při léčbě rakoviny (Functional Assessment of Cancer Therapy-fatigue, FACT-fatigue).
Erytropoetin je růstový faktor, který v první řadě stimuluje tvorbu červených krvinek. Receptory pro erytropoetin se však mohou vyskytovat i na povrchu nejrůznějších nádorových buněk.
V pěti velkých kontrolovaných studiích o celkovém počtu 2833 pacientů, z nichž čtyři byly dvojitě zaslepené a placebem kontrolované a jedna otevřená, bylo sledováno přežití a progrese nádoru. Dvě z těchto studií zahrnovaly pacienty léčené chemoterapií. Cílová koncentrace hemoglobinu byla ve dvou studiích >13 g/dl; ve třech zbývajících studiích byla 12-14 g/dl. V otevřené studii nebyl žádný rozdíl v celkovém přežití mezi pacienty léčenými rekombinantním humánním erytropoetinem a kontrolní skupinou. Ve čtyřech placebem kontrolovaných studiích byl hazard ratio (poměr rizika) pro celkové přežití mezi 1,25 a 2,47 ve prospěch kontrolních skupin. Tyto studie ukázaly konzistentní nevysvětlitelné statisticky významné zvýšení mortality u pacientů s anémií spojenou s různými běžnými maligními nádory, kteří dostávali rekombinantní humánní erytropetin v porovnání
s kontrolními skupinami. Výsledné celkové přežití ve studiích nemohlo být dostatečně vysvětleno rozdíly v incidenci trombózy a příbuzných komplikací mezi pacienty léčenými rekombinantním humánním erytropoetinem a těmi z kontrolní skupiny.
Byla rovněž provedena systematická kontrola zahrnující 9000 pacientů s maligními nádory v 57 klinických studiích. Z metaanalýzy údajů o celkovém přežití vyplynul odhad míry rizika přežití přibližně 1,08 ve prospěch kontrolních skupin (95%CI: 0,99; 1,18; 42 studií a 8167 pacientů).
U pacientů léčených rekombinantním humánním erytropoetinem bylo pozorováno zvýšení relativního rizika tromboembolických příhod (RR 1,67; 95%CI: 1,35; 2,06; 35 studií a 6769 pacientů). Je zde tedy konzistentní důkaz pro tvrzení, že může existovat významné poškození pacientů se zhoubným nádorovým onemocněním, kteří jsou léčeni rekombinantním humánním erytropoetinem. Není jasné, v jakém rozsahu lze tyto výsledky aplikovat na podávání rekombinantního humánního erytropoetinu pacientům s maligními nádory, léčeným chemoterapií k dosažení koncentrace hemoglobinu méně než 13 g/dl, protože v kontrolovaných datech bylo zahrnuto jen málo pacientů s těmito charakteristikami.
Byla provedena analýza dat na úrovni pacienta u více než 13 900 pacientů s karcinomem (léčených chemoterapií, radioterapií, oběma nebo bez léčby), kteří se účastnili 53 kontrolovaných klinických studií s několika epoetiny. Metaanalýza dat celkového přežití ukázala poměr rizika přibližně 1,06 ve prospěch kontrol (95%CI: 1,00; 1,12; 53 studií a 13933 pacientů) a pro pacienty s malignitou léčených chemoterapií byl poměr rizika celkového přežití 1,04 (95%CI: 0,97; 1,11; 38 studií a 10441 pacientů). Metaanalýza také ukazuje trvale a významně zvýšené relativní riziko tromboembolických příhod u pacientů s karcinomem léčených rekombinantním lidským erytropoetinem (viz bod 4.4).
5.2 Farmakokinetické vlastnosti
Díky zvýšenému obsahu uhlohydrátů zůstává hladina darbepoetinu alfa v cirkulaci nad minimální stimulační koncentrací erytropoezy déle, než je tomu v případě ekvivalentní molární dávky r-HuEPO, což dovoluje dosáhnout stejné biologické odezvy při méně častém podávání darbepoetinu alfa.
Pacienti s chronickým selháním ledvin
Farmakokinetika darbepoetinu alfa byla klinicky hodnocena u pacientů s chronickým selháním ledvin, a to po intravenózním a subkutánním podání. Terminální poločas darbepoetinu alfa je 21 hodin (SD 7,5) po intravenózní aplikaci. Clearance darbepoetinu alfa je 1,9 ml/hod/kg (SD 0,56) a distribuční objem (Vss) je přibližně roven plazmatickému objemu (50 ml/kg). Biologická dostupnost dosahuje 37% při subkutánním podání. Po měsíčním subkutánním podávání darbepoetinu alfa v dávkách od 0,6 do 2,1 pg/kg byl jeho terminální poločas 73 hodin (SD 24). Delší konečný poločas darbepoetinu alfa podávaného subkutánně ve srovnání s intravenózním podáním je způsoben kinetikou subkutánního vstřebávání. V klinických studiích byla pozorována minimální akumulace při kterémkoliv ze způsobů podání. V preklinických studiích bylo prokázáno, že renální clearance je minimální (nejvýše 2 % celkové clearance) a neovlivňuje poločas v séru.
Údaje od 809 pacientů užívajících Aranesp v evropských klinických studiích byly podrobeny analýze s cílem stanovit dávku nutnou pro udržení koncentrace hemoglobinu; mezi průměrnou týdenní dávkou podávanou intravenózně nebo aplikovanou subkutánně nebyl pozorován žádný rozdíl.
Farmakokinetika darbepoetinu alfa u dialyzovaných nebo nedialyzovaných pediatrických pacientů (216 let) s chronickým selháním ledvin (CRF) byla vyhodnocena na základě vzorků odebíraných po dobu 2 týdnů (336 hodin) po jedné nebo dvou subkutánních nebo intravenózních dávkách. Tam, kde byla dodržena stejná doba odebírání vzorků, pozorovaná farmakokinetická data a populační farmakokinetické modelování ukázala, že farmakokinetika darbepoetinu alfa byla stejná u pediatrických i dospělých pacientů s CRF.
Ve farmakokinetické studii fáze I byl po intravenózní aplikaci pozorován přibližně 25%-ní rozdíl v ploše pod křivkou od času 0 do nekonečna (AUC[0-w]) mezi pediatrickými a dospělými pacienty; avšak tento rozdíl byl nižší než dvojnásobný rozsah AUC(0-<») pozorovaný u pediatrických pacientů. AUC(0 -<») byla stejná u dospělých i pediatrických pacientů s CRF po subkutánním podání. Poločas byl také stejný u dospělých i pediatrických pacientů s CRF po intravenózní i subkutánní aplikaci.
Pacienti s maligním nádorovým onemocněním léčení chemoterapií
Po subkutánním podání dávky 2,25 pg/kg dospělým pacientům s maligním nádorovým onemocněním bylo dosaženo průměrné maximální koncentrace 10,6 ng/ml (SD 5,9) darbepoetinu alfa za průměrnou dobu 91 hodin (SD 19,7). Tyto parametry byly v souladu s farmakokinetikou při lineárním dávkování v širokém rozpětí dávek (0,5 až 8 pg/kg týdně a 3 až 9 pg/kg každé dva týdny). Farmakokinetické parametry se neměnily při vícenásobném dávkování během 12 týdnů (dávky každý týden nebo každé dva týdny). Jakmile bylo dosaženo rovnovážného stavu, došlo k očekávanému mírnému (méně než dvojnásobnému) zvýšení koncentrace v séru, nikoliv však k nepředpokládané akumulaci po opakovaném podání. Farmakokinetická studie prováděná u pacientů s anémií indukovanou chemoterapií s dávkou 6,75 pg/kg darbepoetinu alfa podávaného subkutánně 1 krát za 3 týdny v kombinaci s chemoterapií umožnila sledování terminálního poločasu. V této studii byl průměr (SD) terminálního poločasu 74 (SD 27) hodin.
5.3 Předklinické údaje vztahující se k bezpečnosti
Ve všech studiích prováděných na potkanech a psech darbepoetin alfa způsoboval značné zvýšení koncentrací hemoglobinu, vzestup hematokritu a nárůst počtu erytrocytů a retikulocytů, což koresponduje s očekávanými farmakologickými účinky. Nežádoucí příhody, které se vyskytly při aplikaci velmi vysokých dávek, byly přisouzeny vystupňovanému farmakologickému efektu (snížená perfuze tkání při zvýšené viskozitě krve). Tyto příhody zahrnovaly myelofibrózu a hypertrofii sleziny a dále rozšíření QRS komplexu na EKG u psů. Nebyl však pozorován žádný vliv na QT interval a nebyly zaznamenány žádné dysrytmie.
U darbepoetinu alfa se neprokázal žádný genotoxický potenciál a ani žádný účinek na proliferaci nehematologických buněk in vivo a in vitro. Ve studiích chronické toxicity nebyl u žádného typu tkáně pozorován tumorigenní efekt ani neočekávaná mitogenní odezva. Kancerogenní potenciál darbepoetinu alfa v dlouhodobých studiích na zvířatech nebyl hodnocen.
Ve studiích prováděných na potkanech a králících nebyl zaznamenán žádný klinicky relevantní průkaz škodlivého účinku na těhotenství, vývoj embrya nebo plodu, porod nebo vývoj po narození. Průnik placentou byl minimální. Nebyl rovněž zjištěn žádný vliv na plodnost.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Dihydrogenfosforenčnan sodný Hydrogenfosforenčnan sodný Chlorid sodný Polysorbát 80 Voda na injekci
6.2 Inkompatibility
Studie kompatibility nejsou k dispozici, a proto nesmí být tento léčivý přípravek mísen ani podáván jako infúze s jinými léčivými přípravky.
6.3 Doba použitelnosti
3 roky
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v chladničce (2 °C - 8 °C).
Chraňte před mrazem.
Uchovávejte vnitřní obal v krabičce, aby byl přípravek chráněn před světlem.
Pro účely ambulantního použití smí být Aranesp přemístěn z místa uchovávání do prostředí o pokojové teplotě (do 25 °C), a to pouze jednou a maximálně na jedno období sedmi dnů. Jestliže byl přípravek vyjmut z chladničky a dosáhl pokojové teploty (do 25 °C), musí být buď během 7 dnů použit, nebo se musí zlikvidovat.
6.5 Druh obalu a obsah balení
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce
0,4 ml injekčního roztoku (25 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky.
Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce
0,375 ml injekčního roztoku (40 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce
0,5 ml injekčního roztoku (40 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce
0,3 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce
0,4 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce
0,5 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce
0,3 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce
0,4 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce
0,5 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce
0,65 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce
0,3 ml injekčního roztoku (500 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce
0,6 ml injekčního roztoku (500 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky. Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce
1 ml injekčního roztoku (500 pg/ml darbepoetinu alfa) v předplněné injekční stříkačce ze skla třídy 1 s jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněné injekční stříkačky.
Injekční stříkačky mohou být v balení v blistru (1 nebo 4 kusy) s nebo bez automatického chrániče jehly, nebo bez blistru (pouze 1 kus).
Kryt jehly předplněné injekční stříkačky obsahuje suchou přírodní gumu (derivát latexu). Viz bod 4.4. Aranesp 10 mikrogramů injekční roztok v předplněném peru
0,4 ml injekčního roztoku (25 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 15 mikrogramů injekční roztok v předplněném peru
0,375 ml injekčního roztoku (40 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 20 mikrogramů injekční roztok v předplněném peru
0,5 ml injekčního roztoku (40 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 30 mikrogramů injekční roztok v předplněném peru
0,3 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 40 mikrogramů injekční roztok v předplněném peru
0,4 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera.
Aranesp 50 mikrogramů injekční roztok v předplněném peru
0,5 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 60 mikrogramů injekční roztok v předplněném peru
0,3 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 80 mikrogramů injekční roztok v předplněném peru
0,4 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 100 mikrogramů injekční roztok v předplněném peru
0,5 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 130 mikrogramů injekční roztok v předplněném peru
0,65 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 150 mikrogramů injekční roztok v předplněném peru
0,3 ml injekčního roztoku (500 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 300 mikrogramů injekční roztok v předplněném peru
0,6 ml injekčního roztoku (500 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera. Aranesp 500 mikrogramů injekční roztok v předplněném peru
1 ml injekčního roztoku (500 pg/ml darbepoetinu alfa) v předplněném peru s injekční stříkačkou ze skla třídy 1 a jehlou velikosti 27 z nerezavějící oceli. Velikost balení 1 nebo 4 předplněná pera.
Kryt jehly předplněného pera obsahuje suchou přírodní gumu (derivát latexu). Viz bod 4.4.
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce
1 ml injekčního roztoku (25 pg/ml darbepoetinu alfa) v injekční lahvičce ze skla třídy 1 s elastomerovou zátkou potaženou fluoropolymerem, s hliníkovým závěrem a odtrhovacím (flip-off) protiprachovým víčkem. Velikost balení 1 nebo 4 injekční lahvičky.
Aranesp 40 mikrogramů injekční roztok v injekční lahvičce
1 ml injekčního roztoku (40 pg/ml darbepoetinu alfa) v injekční lahvičce ze skla třídy 1 s elastomerovou zátkou potaženou fluoropolymerem, s hliníkovým závěrem a odtrhovacím (flip-off) protiprachovým víčkem. Velikost balení 1 nebo 4 injekční lahvičky.
Aranesp 60 mikrogramů injekční roztok v injekční lahvičce
1 ml injekčního roztoku (60 pg/ml darbepoetinu alfa) v injekční lahvičce ze skla třídy 1 s elastomerovou zátkou potaženou fluoropolymerem, s hliníkovým závěrem a odtrhovacím (flip-off) protiprachovým víčkem. Velikost balení 1 nebo 4 injekční lahvičky.
Aranesp 100 mikrogramů injekční roztok v injekční lahvičce
1 ml injekčního roztoku (100 pg/ml darbepoetinu alfa) v injekční lahvičce ze skla třídy 1 s elastomerovou zátkou potaženou fluoropolymerem, s hliníkovým závěrem a odtrhovacím (flip-off) protiprachovým víčkem. Velikost balení 1 nebo 4 injekční lahvičky.
Aranesp 200 mikrogramů injekční roztok v injekční lahvičce
1 ml injekčního roztoku (200 pg/ml darbepoetinu alfa) v injekční lahvičce ze skla třídy 1 s elastomerovou zátkou potaženou fluoropolymerem, s hliníkovým závěrem a odtrhovacím (flip-off) protiprachovým víčkem. Velikost balení 1 nebo 4 injekční lahvičky.
Aranesp 300 mikrogramů injekční roztok v injekční lahvičce
1 ml injekčního roztoku (300 pg/ml darbepoetinu alfa) v injekční lahvičce ze skla třídy 1 s elastomerovou zátkou potaženou fluoropolymerem, s hliníkovým závěrem a odtrhovacím (flip-off) protiprachovým víčkem. Velikost balení 1 nebo 4 injekční lahvičky.
Na trhu nemusí být k dispozici všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Krabička obsahuje příbalovou informaci s úplnými pokyny k použití a zacházení.
Předplněným perem Aranesp (SureClick) je aplikována úplná dávka každé prezentace.
Aranesp je sterilní léčivo bez konzervačních přísad. Nepodávejte více než jednu dávku. Všechen zbývající léčivý přípravek je třeba zlikvidovat.
Před podáním roztok Aranespu zkontrolujte, zda-li v něm nejsou viditelné částice. Smí se podávat pouze roztok, který je bezbarvý, čirý nebo lehce opalescentní. Neprotřepávejte. Před injekčním podáním nechte balení dosáhnout pokojové teploty.
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
8. REGISTRAČNÍ ČÍSLO(A)
Aranesp 10 pg injekční roztok v předplněné injekční stříkačce
EU/1/01/185/001 Balení s blistrem 1 ks
EU/1/01/185/002 Balení s blistrem 4 ks
EU/1/01/185/033 Balení bez blistru 1 ks
EU/1/01/185/074 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/075 Balení s blistrem 4 ks s chráničem jehly
Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/003 Balení s blistrem 1 ks
EU/1/01/185/004 Balení s blistrem 4 ks
EU/1/01/185/034 Balení bez blistru 1 ks
EU/1/01/185/076 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/077 Balení s blistrem 4 ks s chráničem jehly
Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/005 Balení s blistrem 1 ks
EU/1/01/185/006 Balení s blistrem 4 ks
EU/1/01/185/035 Balení bez blistru 1 ks
EU/1/01/185/078 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/079 Balení s blistrem 4 ks s chráničem jehly
Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/007 Balení s blistrem 1 ks
EU/1/01/185/008 Balení s blistrem 4 ks
EU/1/01/185/036 Balení bez blistru 1 ks
EU/1/01/185/080 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/081 Balení s blistrem 4 ks s chráničem jehly
Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/009 Balení s blistrem 1 ks
EU/1/01/185/010 Balení s blistrem 4 ks
EU/1/01/185/037 Balení bez blistru 1 ks
EU/1/01/185/082 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/083 Balení s blistrem 4 ks s chráničem jehly
Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/011 Balení s blistrem 1 ks
EU/1/01/185/012 Balení s blistrem 4 ks
EU/1/01/185/038 Balení bez blistru 1 ks
EU/1/01/185/084 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/085 Balení s blistrem 4 ks s chráničem jehly
Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/013 Balení s blistrem 1 ks
EU/1/01/185/014 Balení s blistrem 4 ks
EU/1/01/185/039 Balení bez blistru 1 ks
EU/1/01/185/086 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/087 Balení s blistrem 4 ks s chráničem jehly
Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/015 Balení s blistrem 1 ks
EU/1/01/185/016 Balení s blistrem 4 ks
EU/1/01/185/040 Balení bez blistru 1 ks
EU/1/01/185/088 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/089 Balení s blistrem 4 ks s chráničem jehly
Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/017 Balení s blistrem 1 ks
EU/1/01/185/018 Balení s blistrem 4 ks
EU/1/01/185/041 Balení bez blistru 1 ks
EU/1/01/185/090 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/091 Balení s blistrem 4 ks s chráničem jehly
Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/069 Balení s blistrem 1 ks
EU/1/01/185/070 Balení s blistrem 4 ks
EU/1/01/185/071 Balení bez blistru 1 ks
EU/1/01/185/092 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/093 Balení s blistrem 4 ks s chráničem jehly
Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/019 Balení s blistrem 1 ks
EU/1/01/185/020 Balení s blistrem 4 ks
EU/1/01/185/042 Balení bez blistru 1 ks
EU/1/01/185/094 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/095 Balení s blistrem 4 ks s chráničem jehly
Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/021 Balení s blistrem 1 ks
EU/1/01/185/022 Balení s blistrem 4 ks
EU/1/01/185/043 Balení bez blistru 1 ks
EU/1/01/185/096 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/097 Balení s blistrem 4 ks s chráničem jehly
Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce
EU/1/01/185/031 Balení s blistrem 1 ks
EU/1/01/185/032 Balení s blistrem 4 ks
EU/1/01/185/044 Balení bez blistru 1 ks
EU/1/01/185/098 Balení s blistrem 1 ks s chráničem jehly
EU/1/01/185/099 Balení s blistrem 4 ks s chráničem jehly
Aranesp 10 mikrogramů injekční roztok v předplněném peru EU/1/01/185/045 - 1 ks EU/1/01/185/057 - 4 ks
Aranesp 15 mikrogramů injekční roztok v předplněném peru EU/1/01/185/046 - 1 ks EU/1/01/185/058 - 4 ks
Aranesp 20 mikrogramů injekční roztok v předplněném peru EU/1/01/185/047 - 1 ks EU/1/01/185/059 - 4 ks
Aranesp 30 mikrogramů injekční roztok v předplněném peru EU/1/01/185/048 - 1 ks EU/1/01/185/060 - 4 ks
Aranesp 40 mikrogramů injekční roztok v předplněném peru EU/1/01/185/049 - 1 ks EU/1/01/185/061 - 4 ks
Aranesp 50 mikrogramů injekční roztok v předplněném peru EU/1/01/185/050 - 1 ks EU/1/01/185/062 - 4 ks
Aranesp 60 mikrogramů injekční roztok v předplněném peru EU/1/01/185/051 - 1 ks EU/1/01/185/063 - 4 ks
Aranesp 80 mikrogramů injekční roztok v předplněném peru EU/1/01/185/052 - 1 ks EU/1/01/185/064 - 4 ks
Aranesp 100 mikrogramů injekční roztok v předplněném peru EU/1/01/185/053 - 1 ks EU/1/01/185/065 - 4 ks
Aranesp 130 mikrogramů injekční roztok v předplněném peru EU/1/01/185/072 - 1 ks EU/1/01/185/073 - 4 ks k
Aranesp 150 mikrogramů injekční roztok v předplněném peru EU/1/01/185/054 - 1 ks EU/1/01/185/066 - 4 ks
Aranesp 300 mikrogramů injekční roztok v předplněném peru EU/1/01/185/055 - 1 ks EU/1/01/185/067 - 4 ks
Aranesp 500 mikrogramů injekční roztok v předplněném peru EU/1/01/185/056 - 1 ks EU/1/01/185/068 - 4 ks
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce EU/1/01/185/100 1 ks EU/1/01/185/101 4 ks
Aranesp 40 mikrogramů injekční roztok v injekční lahvičce EU/1/01/185/102 1 ks EU/1/01/185/103 4 ks
Aranesp 60 mikrogramů injekční roztok v injekční lahvičce EU/1/01/185/104 1 ks EU/1/01/185/105 4 ks
Aranesp 100 mikrogramů injekční roztok v injekční lahvičce EU/1/01/185/106 1 ks EU/1/01/185/107 4 ks
Aranesp 200 mikrogramů injekční roztok v injekční lahvičce a EU/1/01/185/108 1 ks EU/1/01/185/109 4 ks
Aranesp 300 mikrogramů injekční roztok v injekční lahvičce EU/1/01/185/110 1 ks EU/1/01/185/111 4 ks
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 8. června 2001
Datum posledního prodloužení registrace: 19. květen 2006
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky na adrese http://www.ema.europa.eu
A. VÝROBCE/VÝROBCI BIOLOGICKÉ LÉČIVÉ LÁTKY /BIOLOGICKÝCH LÉČIVÝCH LÁTEK A VÝROBCE ODPOVĚDNÝ/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE/VÝROBCI BIOLOGICKÉ LÉČIVÉ LÁTKY A VÝROBCE/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce biologické léčivé látky (látek)
Amgen Manufacturing Limited PO Box 4060, Road 31 km 24.6 Juncos, PR 00777-4060 Puerto Rico
Název a adresa výrobců odpovědných za propouštění šarží
Amgen Europe B.V.
Minervum 7061 4817 ZK Breda The Netherlands
Amgen Technology Ireland (ADL)
Pottery Road Dun Laoghaire Co Dublin Irsko
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propouštění dané šarže.
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis s omezením (viz Příloha I: Souhrn údajů o přípravku, odstavec 4.2).
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE • Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,4 ml obsahuje 10 mikrogramů darbepoetinu alfa (25 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/001 1 ks EU/1/01/185/002 4 ks EU/1/01/185/074 1 ks s chráničem jehly EU/1/01/185/075 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 10 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 10 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,4 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 10 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,4 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 10 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,4 ml obsahuje darbepoetinum alfa 10 mikrogramů (25 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/033
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 10 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 10 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,375 ml obsahuje 15 mikrogramů darbepoetinu alfa (40 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/003 1 ks EU/1/01/185/004 4 ks EU/1/01/185/076 1 ks s chráničem jehly EU/1/01/185/077 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 15 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 15 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,375 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 15 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,375 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 15 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,375 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,375 ml obsahuje darbepoetinum alfa 15 mikrogramů (40 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/034
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 15 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 15 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,375 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,5 ml obsahuje 20 mikrogramů darbepoetinu alfa (40 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/005 1 ks EU/1/01/185/006 4 ks EU/1/01/185/078 1 ks s chráničem jehly EU/1/01/185/079 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 20 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 20 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,5 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 20 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,5 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 20 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,5 ml obsahuje darbepoetinum alfa 20 mikrogramů (40 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/035
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 20 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 20 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,3 ml obsahuje 30 mikrogramů darbepoetinu alfa (100 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/007 1 ks EU/1/01/185/008 4 ks EU/1/01/185/080 1 ks s chráničem jehly EU/1/01/185/081 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 30 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 30 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,3 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 30 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,3 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 30 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,3 ml obsahuje darbepoetinum alfa 30 mikrogramů (100 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/036
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 30 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 30 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,4 ml obsahuje 40 mikrogramů darbepoetinu alfa (100 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/009 1 ks EU/1/01/185/010 4 ks EU/1/01/185/082 1 ks s chráničem jehly EU/1/01/185/083 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 40 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 40 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,4 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 40 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
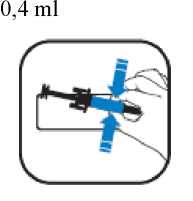
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 40 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,4 ml obsahuje darbepoetinum alfa 40 mikrogramů (100 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/037
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 40 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 40 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,5 ml obsahuje 50 mikrogramů darbepoetinu alfa (100 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/011 1 ks EU/1/01/185/012 4 ks EU/1/01/185/084 1 ks s chráničem jehly EU/1/01/185/085 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 50 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 50 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,5 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 50 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,5 ml
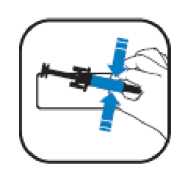
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 50 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,5 ml obsahuje darbepoetinum alfa 50 mikrogramů (100 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/038
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 50 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 50 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,3 ml obsahuje 60 mikrogramů darbepoetinu alfa (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/013 1 ks EU/1/01/185/014 4 ks EU/1/01/185/086 1 ks s chráničem jehly EU/1/01/185/087 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 60 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 60 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,3 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 60 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,3 ml
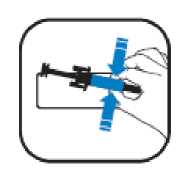
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 60 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,3 ml obsahuje darbepoetinum alfa 60 mikrogramů (200 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN
MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/039
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 60 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 60 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,4 ml obsahuje 80 mikrogramů darbepoetinu alfa (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/015 1 ks EU/1/01/185/016 4 ks EU/1/01/185/088 1 ks s chráničem jehly EU/1/01/185/089 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 80 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 80 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,4 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 80 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,4 ml
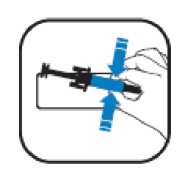
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 80 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,4 ml obsahuje darbepoetinum alfa 80 mikrogramů (200 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/040
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 80 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 80 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,5 ml obsahuje 100 mikrogramů darbepoetinu alfa (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/017 1 ks EU/1/01/185/018 4 ks EU/1/01/185/090 1 ks s chráničem jehly EU/1/01/185/091 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 100 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 100 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,5 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 100 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,5 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 100 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,5 ml obsahuje darbepoetinum alfa 100 mikrogramů (200 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/041
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 100 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 100 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,65 ml obsahuje 130 mikrogramů darbepoetinu alfa (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/069 1 ks EU/1/01/185/070 4 ks EU/1/01/185/092 1 ks s chráničem jehly EU/1/01/185/093 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 130 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 130 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,65 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 130 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,65 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 130 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,65 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,65 ml obsahuje darbepoetinum alfa 130 mikrogramů (200 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/071
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 130 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 130 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,65 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,3 ml obsahuje 150 mikrogramů darbepoetinu alfa (500 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/019 1 ks EU/1/01/185/020 4 ks EU/1/01/185/094 1 ks s chráničem jehly EU/1/01/185/095 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 150 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 150 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,3 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 150 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,3 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 150 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,3 ml obsahuje darbepoetinum alfa 150 mikrogramů (500 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/042
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 150 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 150 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU
KRABIČKA S PLASTOVÝM PŘÍŘEZEM OBSAHUJÍCÍM INJEKČNÍ STŘÍKAČKU 1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 0,6 ml obsahuje 300 mikrogramů darbepoetinu alfa (500 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/021 1 ks EU/1/01/185/022 4 ks EU/1/01/185/096 1 ks s chráničem jehly EU/1/01/185/097 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 300 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 300 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 0,6 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 300 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c.
0,6 ml
OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 300 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,6 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 0,6 ml obsahuje darbepoetinum alfa 300 mikrogramů (500 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/043
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 300 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 300 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,6 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
Jedna předplněná injekční stříkačka o objemu 1 ml obsahuje 500 mikrogramů darbepoetinu alfa (500 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 předplněná injekční stříkačka pro jedno použití 4 předplněné injekční stříkačky pro jedno použití
1 předplněná injekční stříkačka pro jedno použití s automatickým chráničem jehly 4 předplněné injekční stříkačky pro jedno použití s automatickým chráničem jehly
Před použitím si přečtěte příbalovou informaci.
Důležité: než začnete používat předplněnou injekční stříkačku, přečtěte si příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/031 1 ks EU/1/01/185/032 4 ks EU/1/01/185/098 1 ks s chráničem jehly EU/1/01/185/099 4 ks s chráničem jehly
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 500 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 500 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 1 ml
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU_
Aranesp 500 pg injekce Darbepoetin alfa
2. NÁZEV DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. JINÉ
i.v./s.c. 1 ml

OZNAČENÍ INJEKČNÍ STŘÍKAČKY POKUD JE V PLASTOVÉM PŘÍŘEZU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 500 pg Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Amgen Europe B.V.
KRABIČKA BEZ PLASTOVÉHO PŘÍŘEZU OBSAHUJÍCÍ INJEKČNÍ STŘÍKAČKU
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna předplněná injekční stříkačka o objemu 1 ml obsahuje darbepoetinum alfa 500 mikrogramů (500 mikrogramů/ml).
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 předplněná injekční stříkačka pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
EU/1/01/185/044
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 500 injekční stříkačka
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ_
Aranesp 500 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 10 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,4 ml předplněné pero obsahuje darbepoetinum alfa 10 mikrogramů (25 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/045 1 kus EU/1/01/185/057 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 10 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 10 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 15 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,375 ml předplněné pero obsahuje darbepoetinum alfa 15 mikrogramů (40 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/046 1 kus EU/1/01/185/058 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 15 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 15 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,375 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 20 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,5 ml předplněné pero obsahuje darbepoetinum alfa 20 mikrogramů (40 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/047 1 kus EU/1/01/185/059 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 20 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 20 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 30 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,3 ml předplněné pero obsahuje darbepoetinum alfa 30 mikrogramů (100 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/048 1 kus EU/1/01/185/060 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 30 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 30 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 40 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,4 ml předplněné pero obsahuje darbepoetinum alfa 40 mikrogramů (100 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/049 1 kus EU/1/01/185/061 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 40 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 40 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 50 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,5 ml předplněné pero obsahuje darbepoetinum alfa 50 mikrogramů (100 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/050 1 kus EU/1/01/185/062 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 50 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 50 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 60 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,3 ml předplněné pero obsahuje darbepoetinum alfa 60 mikrogramů (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/051 1 kus EU/1/01/185/063 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 60 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 60 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 80 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,4 ml předplněné pero obsahuje darbepoetinum alfa 80 mikrogramů (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/052 1 kus EU/1/01/185/064 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 80 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 80 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,4 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 100 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,5 ml předplněné pero obsahuje darbepoetinum alfa 100 mikrogramů (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/053 1 kus EU/1/01/185/065 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 100 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 100 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,5 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 130 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,65 ml předplněné pero obsahuje darbepoetinum alfa 130 mikrogramů (200 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/072 1 kus EU/1/01/185/073 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 130 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 130 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,65 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 150 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,3 ml předplněné pero obsahuje darbepoetinum alfa 150 mikrogramů (500 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/054 1 kus EU/1/01/185/066 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 150 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 150 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,3 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 300 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 0,6 ml předplněné pero obsahuje darbepoetinum alfa 300 mikrogramů (500 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/055 1 kus EU/1/01/185/067 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Aranesp 300 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 300 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
0,6 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 500 mikrogramů injekční roztok v předplněném peru Darbepoetinum alfa
Jedno 1 ml předplněné pero obsahuje darbepoetinum alfa 500 mikrogramů (500 mikrogramů/ml).
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
SureClick x1
1 předplněné pero pro jedno použití
Tato krabička s jedním předplněným perem je součástí balení po 4 kusech. SureClick x4
4 předplněná pera pro jedno použití
Před použitím si přečtěte příbalovou informaci. subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
>y
EU/1/01/185/056 1 kus EU/1/01/185/068 4 kus
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
ranesp 500 pero
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 500 pg injekce Darbepoetin alfa s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Amgen Europe B.V.
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna injekční lahvička o objemu 1 ml obsahuje darbepoetinum alfa 25 mikrogramů
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 injekční lahvička pro jedno použití 4 injekční lahvičky pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
sy
EU/1/01/185/100 1 kus EU/1/01/185/101 4 ku;
Lot
Výdej léčivého přípravku vázán na lékařský předpis.
Nevyžaduje se - odůvodnění přijato
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 25 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Aranesp 40 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
2. OBSAH LÉČIVÉ LÁTKY/ LÉČIVÝCH LÁTEK
Jedna injekční lahvička o objemu 1 ml obsahuje darbepoetinum alfa 40 mikrogramů
3. SEZNAM POMOCNÝCH LÁTEK
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
4. LÉKOVÁ FORMA A OBSAH BALENÍ
1 injekční lahvička pro jedno použití 4 injekční lahvičky pro jedno použití
5. ZPŮSOB A CESTA PODÁNÍ
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
8. POUŽITELNOST
EXP
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Uchovávejte v chladničce. Chraňte před mrazem.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z TAKOVÝCH LÉČIVÝCH PŘÍPRAVKŮ, POKUD JE TO VHODNÉ
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
sy
EU/1/01/185/102 1 kus EU/1/01/185/103 4 ku;
Lot
Výdej léčivého přípravku vázán na lékařský předpis.
Nevyžaduje se - odůvodnění přijato
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 40 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Aranesp 60 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
Jedna injekční lahvička o objemu 1 ml obsahuje darbepoetinum alfa 60 mikrogramů
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 injekční lahvička pro jedno použití 4 injekční lahvičky pro jedno použití
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
sy
EU/1/01/185/104 1 kus EU/1/01/185/105 4 ku;
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Nevyžaduje se - odůvodnění přijato
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 60 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Aranesp 100 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
Jedna injekční lahvička o objemu 1 ml obsahuje darbepoetinum alfa 100 mikrogramů
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 injekční lahvička pro jedno použití 4 injekční lahvičky pro jedno použití
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
sy
EU/1/01/185/106 1 kus EU/1/01/185/107 4 ku;
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Nevyžaduje se - odůvodnění přijato
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 100 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Aranesp 200 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
Jedna injekční lahvička o objemu 1 ml obsahuje darbepoetinum alfa 200 mikrogramů
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 injekční lahvička pro jedno použití 4 injekční lahvičky pro jedno použití
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
sy
EU/1/01/185/108 1 kus EU/1/01/185/109 4 ku;
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Nevyžaduje se - odůvodnění přijato
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 200 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
Aranesp 300 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
Jedna injekční lahvička o objemu 1 ml obsahuje darbepoetinum alfa 300 mikrogramů
Pomocné látky: dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80, voda na injekci.
1 injekční lahvička pro jedno použití 4 injekční lahvičky pro jedno použití
Před použitím si přečtěte příbalovou informaci. Intravenózní nebo subkutánní podání.
Uchovávejte mimo dohled a dosah dětí.
EXP
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Amgen Europe B.V. Minervum 7061 NL-4817 ZK Breda Nizozemsko
12. REGISTRAČNÍ ČÍSLO(A)
sy
EU/1/01/185/110 1 kus EU/1/01/185/111 4 ku;
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
Výdej léčivého přípravku vázán na lékařský předpis.
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Nevyžaduje se - odůvodnění přijato
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTY PODÁNÍ
Aranesp 300 pg injekce Darbepoetin alfa i.v./s.c.
2. ZPŮSOB PODÁNÍ
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET DÁVEK
1 ml
6. JINÉ
B. PŘÍBALOVÁ INFORMACE
Příbalová informace: informace pro uživatele
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce
Darbepoetinum alfa
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry .
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí
ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Aranesp a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
3. Jak se Aranesp používá
4. Možné nežádoucí účinky
5. Jak Aranesp uchovávat
6. Obsah balení a další informace
7. Pokyny k injekčnímu podání Aranespu v předplněné injekční stříkačce
1. Co je Aranesp a k čemu se používá
Lékař Vám předepsal Aranesp (antianemikum) k léčbě anémie. Anémie je onemocněním, kdy krev neobsahuje dostatek červených krvinek. Jejími příznaky mohou být únavnost, slabost a nedostatek dechu.
Aranesp účinkuje přesně stejným způsobem jako přirozený hormon erytropoetin. Erytropoetin vzniká v ledvinách a podněcuje kostní dřeň k tvorbě většího množství červených krvinek. Účinnou látkou obsaženou v Aranespu je darbepoetin alfa, vyrobený genovou technologií v buňkách vaječníku čínského křečka (CHO-K1).
Pokud máte chronické selhávání ledvin
Aranesp se používá k léčbě symptomatické anémie, která doprovází chronické selhávání ledvin, a to u dospělých a u dětí. Při selhávání ledvin se v nich nevytváří dostatek přirozeného hormonu erytropoetinu, což často způsobuje anémii.
Organismus potřebuje k vytvoření většího počtu červených krvinek určitý čas; proto účinek léčby zaznamenáte přibližně po čtyřech týdnech. Váš obvyklý dialyzační režim neovlivní schopnost Aranespu léčit anémii.
Pokud dostáváte chemoterapii
Aranesp se používá k léčbě anémie s příznaky u dospělých pacientů se zhoubnými nádory kromě nádorů kostní dřeně (nemyeloidními malignitami), kteří dostávají chemoterapii.
Jedním z hlavních nežádoucích účinků chemoterapie je, že tlumí tvorbu krevních buněk v kostní dřeni. K poklesu počtu červených krvinek a ke vzniku anémie může dojít spíše v období na konci chemoterapie, zvláště pokud se jednalo o podávání většího množství chemoterapeutik.
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
Nepoužívejte Aranesp:
- jestliže jste alergický(á) na darbepoetin alfa nebo na kteroukoliv další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže Vám byl zjištěn vysoký krevní tlak, který není kontrolován jiným lékem předepsaným Vaším lékařem.
Upozornění a opatření
Před použitím Aranespu se poraďte se svým lékařem, lékarníkem nebo zdravotní sestrou.
Oznamte prosím svému lékaři, jestliže v současné době trpíte nebo jste v minulosti trpěl(a):
- vysokým krevním tlakem, který je léčen jinými léky předepsanými Vaším lékařem;
- srpkovitou anémií;
- epileptickými záchvaty;
- křečemi (záchvaty);
- onemocněním jater;
- výrazně nedostatečnou odpovědí na léky používané k léčbě anémie;
- alergií na latex. Kryt jehly předplněné injekční stříkačky obsahuje derivát latexu; nebo
- infekční žloutenkou typu C.
Zvláštní upozornění:
- Pokud máte příznaky zahrnující neobvyklou únavu a nedostatek energie, může to znamenat že máte aplazii červené krevní řady (PRCA), která byla hlášena u některých pacientů. PRCA znamená, že organismus buď významně snížil produkci červených krvinek nebo dokonce zcela přestal s jejich tvorbou, což má za následek závažnou anémii. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře, který určí nejvhodnější postup léčby Vaší anémie.
- Buďte zvlášť opatrní u ostatních léků, které stimulují tvorbu červených krvinek. Aranesp je jedním ze skupiny léků, které stimulují tvorbu červených krvinek stejně jako lidská bílkovina erytropoetin. Váš lékař má vždy zaznamenat přesný název léku, který dostávate.
- Jestliže máte chronické selhání ledvin a zejména pokud patřičně nereagujete na léčbu Aranespem, Váš lékař by měl zkontrolovat Vaši dávku Aranespu, protože opakované zvyšování dávky Aranespu v případě, že nereagujete na léčbu, může zvyšovat riziko problémů se srdcem nebo krevními cévami a mohlo by zvýšit riziko srdečního infarktu, mrtvice a úmrtí.
- Váš lékař by se měl snažit udržovat Vaši hladinu hemoglobinu mezi 10 a 12 g/dl.Váš lékař bude dohlížet, aby hladina Vašeho hemoglobinu nepřekročila stanovenou hodnotu, protože vysoké hladiny hemoglobinu Vás mohou vystavovat riziku srdečních obtíží nebo obtíží s cévami a zvyšovat riziko srdečního infarktu, mrtvice nebo úmrtí.
- Pokud máte příznaky zahrnující silnou bolest hlavy, netečnost, zmatenost, obtíže se zrakem, nevolnost, zvracení nebo záchvaty (křeče), může to znamenat, že máte velmi vysoký krevní tlak. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře.
- V případě, že trpíte nádorovým onemocněním, mějte na paměti, že Aranesp může působit jako růstový faktor krvinek a za určitých okolností může mít negativní vliv na Vaše nádorové onemocnění. Podle Vaší individuální situace může být vhodnější krevní transfúze. Projednejte prosím tuto skutečnost s Vaším ošetřujícím lékařem.
- Nesprávné podávání zdravým osobám může způsobit život ohrožující srdeční nebo cévní komplikace.
Další léčivé přípravky a Aranesp
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Počtem červených krvinek mohou být ovlivněny cyklosporin a takrolimus (léky potlačující imunitní odpověď organismu). Je důležité, abyste svému lékaři sdělil(a), zda některý z těchto léků užíváte.
Aranesp s jídlem a pitím
Jídlo a pití Aranesp neovlivňuje.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Aranesp nebyl testován u těhotných žen. Je důležité, abyste svému lékaři sdělila, zda
• jste těhotná;
• myslíte si, že byste mohla být těhotná;
• plánujete otěhotnět.
Není známo, zda se darbepoetin alfa vylučuje do lidského mateřského mléka. Pokud užíváte Aranesp, musíte přestat kojit.
Řízení dopravních prostředků a obsluha strojů
Aranesp by neměl ovlivnit schopnost řídit dopravní prostředky a obsluhovat stroje.
Aranesp obsahuje sodík
Tento přípravek obsahuje méně než 1 mmol sodíku (23 mg) v dávce, to znamená, že je v podstatě bez sodíku.
3. Jak se Aranesp používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Na základě vyšetření krve rozhodl Váš lékař o léčbě Aranespem, protože Vaše hladina hemoglobinu je 10 g/dl nebo nižší. Lékař také rozhodne o tom, jaké množství léku budete užívat a jak často, aby se Vaše hladina hemoglobinu udržela mezi 10 a 12 g/dl. To se může výrazně lišit pro dospělé a děti.
Podávání injekcí Aranespu pacientem samotným
Váš lékař může rozhodnout, že by pro Vás bylo nejvhodnější, abyste si podával(a) injekce Aranespu sám (sama) nebo aby Vám ji podával Váš pečovatel. Postup, jakým si sám (sama) budete injekce podávat, Vám ukáže lékař, sestra nebo lékárník. Nepokoušejte si dát injekci sám (sama), pokud jste k tomu nebyl(a) vyškolen(a). Nikdy si sám (sama) nepodávejte Aranesp do žíly.
Pokud trpíte chronickým selháváním ledvin
Všem dospělým a dětským pacientům od 1 roku s chronickým selháváním ledvin je Aranesp podáván v jedné injekci, a to buď podkožně (subkutánní podání) nebo do žíly (intravenózní podání).
Pro léčbu anémie bude úvodní dávka Aranespu na kilogram Vaší tělesné hmotnosti buď:
• 0,75 mikrogramů jednou za dva týdny nebo
• 0,45 mikrogramů j ednou týdně.
U dospělých nedialyzovaných pacientů může být jako úvodní dávka použito také 1,5 mikrogramu/kg jednou měsíčně.
U všech dospělých a dětských pacientů od 1 roku s chronickým selháváním ledvin, u kterých je dosaženo korekce anémie, je pokračováno v podávání Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny. Všichni dospělí a děti od 11 let, kteří nejsou na dialýze, mohou Aranesp dostávat v injekci jednou za měsíc.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a jednou za čtyři týdny může upravit dávku podle potřeby, aby byla dosažena trvalá kontrola Vaší anémie.
Váš lékař bude používat nejnižší účinnou látku, aby byly příznaky anémie pod kontrolou.
Pokud nereagujete přiměřeně na léčbu Aranespem, Váš lékař zkontroluje Vaši dávku a informuje Vás, pokud je potřeba Vaši dávku Aranespu změnit.
Pravidelně bude sledován také Váš krevní tlak, a to zvláště na začátku léčby.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Lékař může rozhodnout o změně způsobu podávání injekcí (buďto podkožně nebo do žíly). V případě změny začnete na stejné dávce, kterou právě dostáváte a Váš lékař provede odběr krve, aby se zajistilo, že je anémie stále léčena odpovídajícím způsobem.
Pokud lékař rozhodl Vaši léčbu změnit z r-HuEPO (erytropoetin vyrobený genovou technologií) na Aranesp, stanoví, zda budete dostávat dávku Aranespu jednou týdně nebo jednou za dva týdny.
Způsob podání injekce je stejný jako v případě r-HuEPO, ale Váš lékař Vám sdělí, jakou dávku máte užívat a kdy, a bude-li to nutné, dávku upraví.
Pokud dostáváte chemoterapii
Aranesp budete dostávat v jedné podkožní injekci jednou týdně nebo jednou za tři týdny.
Pro léčbu anémie bude úvodní dávka
• 500 mikrogramů jednou za tři týdny (6,75 mikrogramů Aranespu na kilogram Vaší tělesné hmotnosti) nebo
• 2,25 mikrogramů (jednou týdně) Aranespu na kilogram Vaší tělesné hmotnosti.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a může upravit dávku podle potřeby. Léčba bude trvat přibližně čtyři týdny po ukončení chemoterapie. Lékař Vám sdělí, kdy přesně máte Aranesp přestat užívat.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Jestliže jste použil(a) více Aranespu, než jste měl(a)
Jestliže jste užil(a) více Aranespu, než potřebujete, mohlo by dojít k závažným potížím, například k velmi vysokému krevnímu tlaku. Pokud k tomu dojde, obraťte se prosím na svého lékaře. V případě, že se v jakémkoliv ohledu nebudete cítit dobře, neprodleně vyhledejte svého lékaře, sestru nebo lékárníka.
Jestliže jste zapomněl(a) použít Aranesp
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste zapomněl(a) podat dávku Aranespu, měl(a) byste se spojit se svým lékařem a dohodnout se, kdy byste měl(a) další dávku podat.
Jestliže jste přestal(a) používat Aranesp
Pokud chcete přestat používat Aranesp, poraďte se nejdříve se svým lékařem.
4. Možné nežádoucí účinky
Podobně jako všechny léky může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
U některých pacientů užívajících Aranesp se vyskytly následující nežádoucí účinky:
Pacienti s chronickým selháním ledvin
Velmi časté: mohou postihnout více než 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Alergické reakce
Časté: mohou postihnout až 1 z 10 osob
• Mozková mrtvice
• Bolest okolo místa vpichu
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Krevní sraženiny (trombóza)
• Křeče (záchvaty)
Není známo: z dostupných údajů nelze četnost určit
• Čistá aplazie červených krvinek (PRCA) - (chudokrevnost, neobvyklá únava, nedostatek energie)
Pacienti se zhoubným onemocněním
Velmi časté: mohou postihnout více než 1 z 10 osob
• Alergické reakce
• Zadržování tekutin (edém)
Časté: mohou postihnout až 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Krevní sraženiny (trombóza)
• Bolest okolo místa vpichu injekce
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Křeče (záchvaty)
Všichni pacienti
Není známo: z dostupných údajů nelze četnost určit
• Závažné alergické reakce , které mohou zahrnovat:
- Náhlé život ohrožující alergické reakce (anafylaxe)
- Otok obličeje, rtů, úst, jazyka nebo hrdla který může činit potíže při polykání nebo dýchání (angioedém)
- Dušnost (alergický bronchospasmus)
- Kožní vyrážka
- Kopřivka
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Aranesp uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a štítku za EXP:. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2°C - 8°C). Chraňte před mrazem. Nepoužívejte Aranesp, jestliže si myslíte, že mohlo dojít k jeho zmrznutí.
Uchovávejte předplněnou injekční stříkačku v krabičce, aby byl přípravek chráněn před světlem.
Poté, co injekční stříkačku vyndáte z chladničky a necháte ji stát při pokojové teplotě přibližně 30 minut, musí být přípravek buď použit do 7 dnů nebo zlikvidován.
Nepoužívejte tento přípravek, pokud je zakalený nebo pokud jsou v něm patrné částice.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace Co Aranesp obsahuje
- Léčivou látkou je darbepoetinum alfa, r-HuEPO (erytropoetin vyráběný genovou technologií). Aranesp předplněná injekční stříkačka obsahuje darbepoetinum alfa 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300 nebo 500 mikrogramů.
- Dalšími složkami jsou dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80 a voda na injekci.
Jak Aranesp vypadá a co obsahuje toto balení
Aranesp je čirý, bezbarvý nebo lehce perleťově zabarvený injekční roztok v předplněné injekční stříkačce.
Aranesp je k dispozici v baleních po 1 nebo 4 předplněných injekčních stříkačkách . Stříkačky mohou být v balení s blistrem (1 nebo 4 kusy) nebo bez blistru (pouze 1 kus). Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Držitel rozhodnutí o registraci:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Výrobce:
Amgen Technology Ireland (ADL)
Pottery Road Dun Laoghaire Co Dublin Irsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci.
Belgie/Belgique/Belgien
s.a. Amgen n.v.
Tel/Tél: +32 (0)2 7752711
Eb^rapHu
AMg^eH Etnrapna EOOfl Ten.: +359 (0)2 424 7440
Česká republika
Amgen s.r.o.
Tel: +420 221 773 500
Danmark
Amgen, filial af Amgen AB, Sverige Tlf: +45 39617500
Deutschland
AMGEN GmbH Tel.: +49 89 1490960
Lietuva
Amgen Switzerland AG Vilniaus filialas Tel: +370 5 219 7474
Luxembourg/Luxemburg
s.a. Amgen Belgique/Belgien Tel/Tél: +32 (0)2 7752711
Magyarország
Amgen Kft.
Tel.: +36 1 35 44 700
Malta
Amgen B.V.
The Netherlands Tel: +31 (0)76 5732500
Nederland
Amgen B.V.
Tel: +31 (0)76 5732500
Eesti
Norge
Amgen AB Tel: +47 23308000
Amgen Switzerland AG Vilniaus filialas Tel: +372 5125 501
|
EXláda Amgen ETAág OappaKswiKá E.n.E. TpL: +30 210 3447000 |
Osterreich Amgen GmbH Tel: +43 (0)1 50 217 |
|
Espaňa Amgen S.A. Tel: +34 93 600 18 60 |
Polska Amgen Biotechnologia Sp. z o.o. Tel.: +48 22 581 3000 |
|
France Amgen S.A.S. Tél: +33 (0)9 69 363 363 |
Portugal Amgen Biofarmaceutica, Lda. Tel: +351 21 4220550 |
|
Hrvatska Amgen d.o.o. Tel: +385 (1) 562 57 20 |
Románia Amgen Románia SRL Tel: +4021 527 3000 |
|
Ireland Amgen Limited United Kingdom Tel: +44 (0)1223 420305 |
Slovenija AMGEN zdravila d.o.o. Tel: +386 (0)1 585 1767 |
|
Island Vistor hf. Sími: +354 535 7000 |
Slovenská republika Amgen Slovakia s.r.o. Tel: +421 33 321 13 22 |
|
Italia Amgen S.r.l. Tel: +39 02 6241121 |
Suomi/Finland Amgen AB, sivuliike Suomessa/Amgen AB, filial i Finland Puh/Tel: +358 (0)9 54900500 |
|
Kúnpoq Papaellinas & Co Ltd TpL: +357 22741 741 |
Sverige Amgen AB Tel: +46 (0)8 6951100 |
|
Latvija Amgen Switzerland AG Rrgas filiale Tel: +371 292 84807 |
United Kingdom Amgen Limited Tel: +44 (0)1223 420305 |
Tato příbalová informace byla naposledy revidována.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky na adrese http://www.ema.europa.eu
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
Pokyny k injekčnímu podání Aranespu v předplněné injekční stříkačce
7.
Tento oddíl obsahuje pokyny, jak se postupuje při podávání Aranespu pacientem samotným. Je důležité, abyste se nepokoušel(a) sám (sama) sobě podávat Aranesp, dokud Vám lékař, sestra nebo lékárník neposkytne odborný zácvik. Pokud si nejste jist(a) způsobem podávání injekcí nebo pokud máte jakékoliv další otázky, požádejte, prosím, svého lékaře, sestru nebo lékárníka o pomoc.
Jak použijete vy nebo jiná osoba Aranesp předplněnou stříkačku?
Lékař vám předepsal Aranesp přeplněnou stříkačku k injekci do podkožní tkáně. Váš lékař, sestra nebo lékárník Vám řekne, jaké množství léku budete užívat a jak často si ho budete podávat.
Vybavení:
K podání injekce budete potřebovat:
• novou Aranesp předplněnou injekční stříkačku; a
• alkoholový tampón nebo podobný.
Co mám udělat před podáním subkutánní injekce Aranespu?
1. Vyjměte předplněnou injekční stříkačku Aranespu z chladničky. Ponechte předplněnou injekční stříkačku stát po dobu 30 minut, aby dosáhla pokojové teploty. Injekce bude poté příjemnější. Aranesp neohřívejte žádným jiným způsobem (například jej neohřívejte v mikrovlnné troubě nebo v horké vodě). Nenechávejte stříkačku na přímém slunečním světle.
2. Předplněnou injekční stříkačkou netřepte.
3. Nesnímejte kryt ze stříkačky, dokud nejste připraven(a) k injekci.
4. Zkontrolujte, zda se jedná o správnou dávku, která Vám byla lékařem předepsána.
5. Zkontrolujte dobu použitelnosti na označení předplněné injekční stříkačky (Použitelné do:). Nepoužívejte po uplynutí posledního dne uvedeného měsíce.
6. Zkontrolujte vzhled Aranespu. Musí jít o čirou, bezbarvou nebo lehce perleťově zabarvenou tekutinu. Přípravek nesmíte použít, pokud je zakalený nebo pokud jsou v něm patrné částice.
7. Důkladně si umyjte ruce.
8. Najděte si pohodlné, dobře osvětlené a čisté místo a do dosahu si připravte vše, co potřebujete. Jak budu postupovat při přípravě injekce Aranespu?
Před podáním injekce Aranespu musíte provést následující kroky:

1. Jemně, bez kroucení, odstraňte kryt z jehly, aby nedošlo k jejímu ohnutí, jak je zobrazeno na obrázcích 1 a 2.
2. Nedotýkejte se jehly a nestlačujte píst.
3. Můžete si všimnout malých vzduchových bublin v předplněné injekční stříkačce. Nemusíte vzduchové bubliny před podáním injekce odstraňovat. Podání injekce se vzduchovými bublinami je neškodné.
4. Předplněnou injekční stříkačku můžete nyní použít.
Kam si mám injekce podávat?

Nejlepšími místy k podávání injekcí jsou horní zevní strana stehen a břicho. Pokud Vám injekci bude podávat někdo další, může použít také zadní stranu paží.
Pokud zpozorujete, že je místo vpichu zarudlé nebo bolestivé, můžete jej změnit.
Jak si mám injekce podávat?
1. Vydezinfikujte kůži pomocí alkoholového tampónu a uchopte záhyb kůže (bez stlačení) mezi palec a ukazováček.
2. Proveďte vpich jehlou do kůže tak, jak Vám ukázal Váš lékař, sestra nebo lékárník.
3. Aplikujte si předepsanou dávku podkožně dle pokynů Vašeho lékaře, sestry nebo lékárníka.
4. Píst stlačujte pomalu a rovnoměrně za stálého držení záhybu kůže, dokud není stříkačka prázdná.
5. Vyjměte jehlu z kůže.
6. Pokud si všimnete drobné kapky krve v místě vpichu, můžete ji otřít tampónem. Místo vpichu nemasírujte.V případě potřeby překryjte místo vpichu náplastí s polštářkem.
7. Injekční stříkačku můžete použít pouze k jedné injekci. Neužívejte Aranesp, který zbyl v injekční stříkačce.
Zapamatujte si, prosím: Pokud budete mít jakékoliv problémy, obraťte se s žádostí o radu či pomoc
na svého lékaře nebo sestru.
Likvidace použitých injekčních stříkaček
• Nenasazujte kryt zpět na použité jehly, mohl(a) byste se náhodou píchnout.
• Použité stříkačky uchovávejte mimo dosah a dohled dětí.
• Použité injekční stříkačky musí být zlikvidovány v souladu s místními požadavky. Zeptejte se svého lékárníka, jak máte likvidovat přípravky, které již nepotřebujete. Tato opatření pomáhají chránit životní prostředí.
Příbalová informace: informace pro uživatele
Aranesp 10 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 15 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 20 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 30 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 40 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 50 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 60 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 80 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 100 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 130 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 150 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 300 mikrogramů, injekční roztok v předplněném peru (SureClick)
Aranesp 500 mikrogramů, injekční roztok v předplněném peru (SureClick)
darbepoetinum alfa
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry .
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí
ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Aranesp a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
3. Jak se Aranesp používá
4. Možné nežádoucí účinky
5. Jak Aranesp uchovávat
6. Obsah balení a další informace
7. Pokyny k injekčnímu podání Aranespu v předplněném peru
1. Co je Aranesp a k čemu se používá
Lékař Vám předepsal Aranesp (antianemikum) k léčbě anémie. Anémie je onemocněním, kdy krev neobsahuje dostatek červených krvinek. Jejími příznaky mohou být únavnost, slabost a dušnost.
Aranesp účinkuje přesně stejným způsobem jako přirozený hormon erytropoetin. Erytropoetin vzniká v ledvinách a podněcuje kostní dřeň k tvorbě většího množství červených krvinek. Účinnou látkou obsaženou v Aranespu je darbepoetin alfa, vyrobený genovou technologií v buňkách vaječníku čínského křečka (CHOK1).
Pokud máte chronické selhávání ledvin
Aranesp se používá k léčbě symptomatické anémie, která doprovází chronické selhávání ledvin, a to u dospělých a u dětí. Při selhávání ledvin se v nich nevytváří dostatek přirozeného hormonu erytropoetinu, což často způsobuje anémii.
Organismus potřebuje k vytvoření většího počtu červených krvinek určitý čas; proto účinek léčby zaznamenáte přibližně po čtyřech týdnech. Váš obvyklý dialyzační režim neovlivní schopnost Aranespu léčit anémii.
Pokud dostáváte chemoterapii
Aranesp se používá k léčbě anémie s příznaky u dospělých pacientů se zhoubnými nádory kromě nádorů kostní dřeně (nemyeloidními malignitami), kteří dostávají chemoterapii.
Jedním z hlavních nežádoucích účinků chemoterapie je, že tlumí tvorbu krevních buněk v kostní dřeni. K poklesu počtu červených krvinek a ke vzniku anémie může dojít spíše v období na konci chemoterapie, zvláště pokud se jednalo o podávání většího množství chemoterapeutik.
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
Nepoužívejte Aranesp:
- jestliže jste alergický(á) na darbepoetin alfa nebo na kteroukoliv další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže Vám byl zjištěn vysoký krevní tlak, který není kontrolován jiným lékem předepsaným Vaším lékařem;
Upozornění a opatření
Před použitím Aranespu se poraďte se svým lékařem, lékarníkem nebo zdravotní sestrou.
Oznamte prosím svému lékaři , jestliže v současné době trpíte nebo jste v minulosti trpěl(a):
- vysokým krevním tlakem, který je léčen jinými léky předepsanými Vaším lékařem;
- srpkovitou anémií;
- epileptickými záchvaty;
- křečemi (záchvaty);
- onemocněním jater;
- výrazně nedostatečnou odpovědí na léky používané k léčbě anémie;
- alergií na latex. Kryt jehly předplněného pera obsahuje derivát latexu; nebo
- infekční žloutenkou typu C.
Zvláštní upozornění:
- Pokud máte příznaky zahrnující neobvyklou únavu a nedostatek energie, může to znamenat, že máte aplazii červené krevní řady (PRCA), která byla hlášena u některých pacientů. PRCA znamená, že organismus buď významně snížil produkci červených krvinek, nebo dokonce zcela přestal s jejich tvorbou, což má za následek závažnou anémii. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře, který určí nejvhodnější postup léčby Vaší anémie.
- Buďte zvlášť opatrní u ostatních léků, které stimulují tvorbu červených krvinek. Aranesp je jedním ze skupiny léků, které stimulují tvorbu červených krvinek stejně jako lidská bílkovina erytropoetin. Váš lékař má vždy zaznamenat přesný název léku, který dostávate.
- Jestliže máte chronické selhání ledvin a zejména pokud patřičně nereagujete na léčbu Aranespem, Váš lékař by měl zkontrolovat Vaši dávku Aranespu, protože opakované zvyšování dávky Aranespu v případě, že nereagujete na léčbu, může zvyšovat riziko problémů se srdcem nebo krevními cévami a mohlo by zvýšit riziko srdečního infarktu, mrtvice a úmrtí.
- Váš lékař by se měl snažit udržovat Vaši hladinu hemoglobinu mezi 10 a 12 g/dl. Váš lékař bude dohlížet, aby hladina Vašeho hemoglobinu nepřekročila stanovenou hodnotu, protože vysoké hladiny hemoglobinu Vás mohou vystavovat riziku srdečních obtíží nebo obtíží s cévami a zvyšovat riziko srdečního infarktu, mrtvice nebo úmrtí.
- Pokud máte příznaky zahrnující silnou bolest hlavy, netečnost, zmatenost, obtíže se zrakem, nevolnost, zvracení nebo záchvaty (křeče), může to znamenat, že máte velmi vysoký krevní tlak. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře.
- V případě, že trpíte nádorovým onemocněním, mějte na paměti, že Aranesp může působit jako růstový faktor krvinek a za určitých okolností může mít negativní vliv na Vaše nádorové onemocnění. Podle Vaší individuální situace může být vhodnější krevní transfúze. Projednejte prosím tuto skutečnost s Vaším ošetřujícím lékařem.
- Nesprávné podávání zdravým osobám může způsobit život ohrožující srdeční nebo cévní komplikace.
Další léčivé přípravky a Aranesp
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Počtem červených krvinek mohou být ovlivněny cyklosporin a takrolimus (léky potlačující imunitní odpověď organismu). Je důležité, abyste svému lékaři sdělil(a), zda některý z těchto léků užíváte.
Aranesp s jídlem a pitím
Jídlo a pití Aranesp neovlivňuje.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Aranesp nebyl testován u těhotných žen. Je důležité, abyste svému lékaři sdělila, zda
• jste těhotná;
• myslíte si, že byste mohla být těhotná;
• plánujete otěhotnět.
Není známo, zda se darbepoetin alfa vylučuje do lidského mateřského mléka. Pokud užíváte Aranesp, musíte přestat kojit.
Řízení dopravních prostředků a obsluha strojů
Aranesp by neměl ovlivnit schopnost řídit dopravní prostředky a obsluhovat stroje.
Aranesp obsahuje sodík
Tento přípravek obsahuje méně než 1 mmol sodíku (23 mg) v dávce, to znamená, že je v podstatě bez sodíku.
3. Jak se Aranesp používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Na základě vyšetření krve rozhodl Váš lékař o léčbě Aranespem, protože Vaše hladina hemoglobinu je 10 g/dl nebo nižší. Lékař také rozhodne o tom, jaké množství léku budete užívat a jak často, aby se Vaše hladina hemoglobinu udržela mezi 10 a 12 g/dl. To se může výrazně lišit pro dospělé a děti.
Podávání injekcí Aranespu pacientem samotným
Váš lékař může rozhodnout, že by pro Vás bylo nejvhodnější, abyste si podával(a) injekce Aranespu sám (sama) nebo aby Vám ji podával Váš pečovatel. Postup, jakým si sám (sama) budete injekce podávat, Vám ukáže lékař, sestra nebo lékárník. Nepokoušejte si dát injekci sám (sama), pokud jste k tomu nebyl(a) vyškolen(a). Nikdy si sám (sama) nepodávejte Aranesp do žíly. Předplněné pero je určeno pouze k podkožnímu podání injekce.
Pro návod k použití předplněného pera čtěte část na konci tohoto letáku.
Pokud trpíte chronickým selháváním ledvin
Všem dospělým a dětským pacientům od 1 roku s chronickým selháváním ledvin je Aranesp v předplněném peru podáván v jedné injekci podkožně (subkutánní podání).
Pro léčbu anémie bude úvodní dávka Aranespu na kilogram Vaší tělesné hmotnosti buď:
• 0,75 mikrogramů jednou za dva týdny nebo
• 0,45 mikrogramů j ednou týdně.
U dospělých nedialyzovaných pacientů může být jako úvodní dávka použito také 1,5 mikrogramu/kg jednou měsíčně.
U všech dospělých a dětských pacientů od 1 roku s chronickým selháváním ledvin, u kterých je dosaženo korekce anémie, je pokračováno v podávání Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny. Všichni dospělí a děti od 11 let, kteří nejsou na dialýze, mohou Aranesp dostávat v injekci jednou za měsíc.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a jednou za čtyři týdny může upravit dávku podle potřeby, aby byla dosažena trvalá kontrola Vaší anémie.
Váš lékař bude používat nejnižší účinnou látku, aby byly příznaky anémie pod kontrolou.
Pokud nereagujete přiměřeně na léčbu Aranespem, Váš lékař zkontroluje Vaši dávku a informuje Vás, pokud je potřeba Vaši dávku Aranespu změnit.
Pravidelně bude sledován také Váš krevní tlak, a to zvláště na začátku léčby.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Lékař může rozhodnout o změně způsobu podávání injekcí (buďto podkožně nebo do žíly). V případě změny začnete na stejné dávce, kterou právě dostáváte a Váš lékař provede odběr krve, aby se zajistilo, že je anémie stále léčena odpovídajícím způsobem.
Pokud lékař rozhodl Vaši léčbu změnit z r-HuEPO (erytropoetin vyrobený genovou technologií) na Aranesp, stanoví, zda budete dostávat dávku Aranespu jednou týdně nebo jednou za dva týdny.
Způsob podání injekce je stejný jako v případě r-HuEPO, ale Váš lékař Vám sdělí, jakou dávku máte užívat a kdy, a bude-li to nutné, dávku upraví.
Pokud dostáváte chemoterapii
Aranesp budete dostávat v jedné podkožní injekci jednou týdně nebo jednou za tři týdny.
Pro léčbu anémie bude úvodní dávka
• 500 mikrogramů jednou za tři týdny (6,75 mikrogramů Aranespu na kilogram Vaší tělesné hmotnosti) nebo
• 2,25 mikrogramů (jednou týdně) Aranespu na kilogram Vaší tělesné hmotnosti.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a může upravit dávku podle potřeby. Léčba bude trvat přibližně čtyři týdny po ukončení chemoterapie. Lékař Vám sdělí, kdy přesně máte Aranesp přestat užívat.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Jestliže jste použil(a) více Aranespu, než jste měl(a)
Jestliže jste užil(a) více Aranespu, než potřebujete, mohlo by dojít k závažným potížím, například k velmi vysokému krevnímu tlaku. Pokud k tomu dojde, obraťte se prosím na svého lékaře. V případě, že se v jakémkoliv ohledu nebudete cítit dobře, neprodleně vyhledejte svého lékaře, sestru nebo lékárníka.
Jestliže jste zapomněl(a) použít Aranesp
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste zapomněl(a) podat dávku Aranespu, měl(a) byste se spojit se svým lékařem a dohodnout se, kdy byste měl(a) další dávku podat.
Jestliže jste přestal(a) používat Aranesp
Pokud chcete přestat používat Aranesp, poraďte se nejdříve se svým lékařem.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i Aranesp nežádoucí účinky, které se ale nemusí vyskytnout u každého.
U některých pacientů užívajících Aranesp se vyskytly následující nežádoucí účinky:
Pacienti s chronickým selháním ledvin
Velmi časté: mohou postihnout více než 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Alergické reakce
Časté: mohou postihnout až 1 z 10 osob
• Mozková mrtvice
• Bolest okolo místa vpichu
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Krevní sraženiny (trombóza)
• Křeče (záchvaty)
Není známo: z dostupných údajů nelze četnost určit
• Čistá aplazie červených krvinek (PRCA) - (anémie, neobvyklá únava, nedostatek energie) Pacienti se zhoubným onemocněním
Velmi časté: mohou postihnout více než 1 z 10 osob
• Alergické reakce
• Zadržování tekutin (edém)
Časté: mohou postihnout až 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Krevní sraženiny (trombóza)
• Bolest okolo místa vpichu injekce
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Křeče (záchvaty)
Všichni pacienti
Není známo: z dostupných údajů nelze četnost určit
• Závažné alergické reakce, které mohou zahrnovat:
- Náhlé život ohrožující alergické reakce (anafylaxe)
- Otok obličeje, rtů, úst, jazyka nebo hrdla který může činit potíže při polykání nebo dýchání (angioedém)
- Dušnost (alergický bronchospasmus)
- Kožní vyrážka
- Kopřivka
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Aranesp uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na krabičce a štítku za EXP:. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2°C - 8°C). Chraňte před mrazem. Nepoužívejte Aranesp, jestliže si myslíte, že mohlo dojít k jeho zmrznutí.
Uchovávejte předplněné pero v krabičce, aby byl přípravek chráněn před světlem.
Poté, co pero vyndájte z chladničky a necháte ho stát při pokojové teplotě přibližně 30 minut, musí být přípravek buď použit do 7 dnů nebo zlikvidován.
Nepoužívejte tento přípravek, pokud je zakalený nebo pokud jsou v něm patrné částice.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte.
6. Obsah balení a další informace Co Aranesp obsahuje
- Léčivou látkou je darbepoetinum alfa, r-HuEPO (erytropoetin vyráběný genovou technologií).
Předplněné pero obsahuje buď darbepoetinum alfa 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300 nebo 500 mikrogramů.
- Dalšími složkami jsou dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid
sodný, polysorbát 80 a voda na injekci.
Jak Aranesp vypadá a co obsahuje toto balení
Aranesp je čirý, bezbarvý nebo lehce perleťově zabarvený injekční roztok v předplněném peru.
Aranesp (SureClick) je k dispozici v balení obsahujícím 1 nebo 4 předplněná pera. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Držitel rozhodnutí o registraci:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Výrobce:
Amgen Technology Ireland (ADL)
Pottery Road Dun Laoghaire Co Dublin Irsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci.
Belgie/Belgique/Belgien
s.a. Amgen n.v.
Tel/Tél: +32 (0)2 7752711
BtnrapHH
AMg^eH Etnrapna EOOfl Ten.: +359 (0)2 424 7440
Česká republika
Amgen s.r.o.
Tel: +420 221 773 500
Danmark
Amgen, filial af Amgen AB, Sverige Tlf: +45 39617500
Deutschland
AMGEN GmbH Tel.: +49 89 1490960
Lietuva
Amgen Switzerland AG Vilniaus filialas Tel: +370 5 219 7474
Luxembourg/Luxemburg
s.a. Amgen Belgique/Belgien Tel/Tél: +32 (0)2 7752711
Magyarország
Amgen Kft.
Tel.: +36 1 35 44 700
Malta
Amgen B.V.
The Netherlands Tel: +31 (0)76 5732500
Nederland
Amgen B.V.
Tel: +31 (0)76 5732500
Eesti
Norge
Amgen AB Tel: +47 23308000
Amgen Switzerland AG Vilniaus filialas Tel: +372 5125 501
|
EXláda Amgen ETAág OappaKsurixá E.n.E. TnL: +30 210 3447000 |
Osterreich Amgen GmbH Tel: +43 (0)1 50 217 |
|
Espaňa Amgen S.A. Tel: +34 93 600 18 60 |
Polska Amgen Biotechnologia Sp. z o.o. Tel.: +48 22 581 3000 |
|
France Amgen S.A.S. Tél: +33 (0)9 69 363 363 |
Portugal Amgen Biofarmaceutica, Lda. Tel: +351 21 4220550 |
|
Hrvatska Amgen d.o.o. Tel: +385 (1) 562 57 20 |
Románia Amgen Románia SRL Tel: +4021 527 3000 |
|
Ireland Amgen Limited United Kingdom Tel: +44 (0)1223 420305 |
Slovenija AMGEN zdravila d.o.o. Tel: +386 (0)1 585 1767 |
|
Island Vistor hf. Sími: +354 535 7000 |
Slovenská republika Amgen Slovakia s.r.o. Tel: +421 33 321 13 22 |
|
Italia Amgen S.r.l. Tel: +39 02 6241121 |
Suomi/Finland Amgen AB, sivuliike Suomessa/Amgen AB, filial i Finland Puh/Tel: +358 (0)9 54900500 |
|
Kúnpoq Papaellinas & Co Ltd TnL: +357 22741 741 |
Sverige Amgen AB Tel: +46 (0)8 6951100 |
|
Latvija Amgen Switzerland AG Rrgas filiale Tel: +371 292 84807 |
United Kingdom Amgen Limited Tel: +44 (0)1223 420305 |
Tato příbalová informace byla naposledy revidována.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky na adrese http://www.ema.europa.eu.
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
Pokyny k injekčnímu podání Aranespu v předplněném injekčním peru (SureClick)
7.
Tento bod obsahuje pokyny, jak se správně používá Aranesp předplněné pero. Je důležité, abyste se nepokoušel(a) sám (sama) sobě podávat Aranesp. dokud Vám lékař, sestra nebo lékárník neposkytne odborný zácvik. Pokud si nejste jist(a) způsobem podávání injekcí nebo pokud máte jakékoliv další otázky. požádejte. prosím. svého lékaře. zdravotní sestru nebo lékárníka o pomoc.
Jak použijete vy nebo jiná osoba Aranesp předplněné pero?
Lékař vám předepsal Aranesp předplněné pero k injekci do podkožní tkáně. Váš lékař. sestra nebo lékárník vám řekne. jaké množství léku budete užívat a jak často si ho budete podávat. Každé Aranesp předplněné pero použijte pouze jednou.
Vybavení:
K podání injekce budete potřebovat:
• nové Aranesp předplněné pero; a
• alkoholový tampón nebo podobný.
Příprava na injekci Aranespu?
1. Vyjměte předplněné pero z chladničky. Aby byla injekce příjemnější. ponechte předplněné pero stát po dobu 30 minut při pokojové teplotě. Aranesp neohřívejte žádným jiným způsobem (neohřívejte jej například v mikrovlnné troubě nebo v horké vodě). Předplněné pero navíc nevystavujte přímému slunečnímu světlu.
2. Předplněným perem netřepte.
3. Neodstraňujte šedý kryt jehly z předplněného pera dříve. než jste připraven(a) k injekci.
4. Zkontrolujte. zda se jedná o správnou dávku. která Vám byla lékařem předepsána.
5. Zkontrolujte dobu použitelnosti na etiketě předplněného pera (Použitelné do:). Nepoužívejte po uplynutí posledního dne uvedeného měsíce.
6. Zkontrolujte vzhled Aranespu přes kontrolní okénko v předplněném peru. Musí jít o čirou. bezbarvou nebo lehce perleťově zabarvenou tekutinu. Předplněné pero nepoužívejte. pokud:
• Roztok j e zakalený nebo pokud jsou v něm patrné částice
• Předplněné pero nebo jehla vypadají poškozeně nebo rozbitě:
- Stříkačka v předplněném peru může být po pádu na tvrdý povrch poškozená a poškození nemusí být vidět.
7. Důkladně si umyjte ruce.
8. Najděte si pohodlné. dobře osvětlené a čisté místo a na dosah si připravte vše. co potřebujete.
šedý kryt jehly červené tlačítko

kontrolní okénko
1. Vyberte místo vpichu
Aby pero správně pracovalo, musí být místo vpichu pevné.
Nejvhodnějším místem pro injekci předplněným perem Aranesp je přední strana stehna.
Změna místa vpichu:
Můžete pravidelně měnit místo vpichu pro každou injekci, abyste předešel(a) jeho bolestivosti.
Injekci nepodávejte do místa, kde je kůže jemná, otlačená, červená nebo tvrdá. Vyhněte se zjizveným místům.
2a. Pokyny pro nejvhodnější místo vpichu

Pokud použijete jiná místa vpichu, je velmi důležité dostatečně napnout povrch místa vpichu, aby bylo možno injekci úspěšně podat.

Technika napnutí
Ujistěte se, že kůže pod a okolo předplněného pera je pevná a napnutá a poskytuje dostatečný odpor, aby se bezpečnostní kryt úplně zasunul a odblokoval pero.

Můžete použít břicho, kromě oblasti 5 cm okolo pupku. Pro podání do břicha se doporučuje lehnout si na záda a napnout kůži v místě vpichu, aby se vytvořil pevný a napnutý povrch.

Bude-li Vám injekci podávat někdo jiný, může použít též zadní stranu paží. Pro paže se doporučuje natáhnout kůži v místě vpichu, aby se vytvořil pevný a napnutý povrch.
Pro přípravu oblasti kůže, kam bude Aranesp aplikován, vydezinfikujte kůži pomocí alkoholového tampónu. Před podáním injekce se tohoto místa znovu nedotýkejte.
7b. Injekce Aranespu za použití předplněného pera
1. Když jste připraveni na injekci, stáhněte rovně šedý kryt jehly tak, aby nedošlo k poškození jehly uvnitř předplněného pera. Při stahování šedého krytu jehly neotáčejte ani neohýbejte. Nepokoušejte se nasadit šedý kryt jehly zpět na předplněné pero.
Po odstranění šedého krytu jehly může být na konci jehly kapka, to je obvyklé.
|
0 0 |
Neotáčejte šedým krytem jehly Nepokoušejte se nasadit kryt zpět na předplněné pero |
|
a |
Stahujte šedý kryt přímo |
Stáhněte šedý kryt jehly.

2.
Nedotýkejte se červeného tlačítka. Přitiskněte předplněné pero na kůži, aby došlo k odblokování bezpečnostního chrániče.

Zablokované vysunutým bezpečnostním chráničem
Odblokované zasunutím bezpečnostního chrániče
0_Nestlačujte červené tlačítko, dokud se úplně nezasune bezpečnostní chránič.
a Udržujte dostatečný tlak směrem dolů, aby se žlutý bezpečnostní chránič úplně zasunul a červené tlačítko zůstalo odblokované.
a_Držte předplněné pero v pravém úhlu (90°) k místu vpichu._
3. Krátce stlačte a uvolněte červené tlačítko.

Uvolnit tlačítko

a_Udržujte tlak na kůži během injekce
4. Pomalu odpočítávejte 15 sekund do ukončení injekce

Lék se automaticky aplikuje.
0_Nehýbejte předplněným perem během injekce.
a Počkejte na ukončení injekce před uvolněním tlaku. a_Můžete slyšet druhé kliknutí, když červené tlačítko vyskočí zpět.
5. Zkontrolujte okénko, abyste se ujistil(a), že byla aplikována celá dávka

a Prohlédněte kontrolní okénko, jestli zežloutlo.
! Pokud kontrolní okénko není žluté, musíte
kontaktovat Vašeho lékaře, sestru nebo lékárníka.
Bezpečnostní chránič po použití.
Můžete si povšimnout drobné kapky krve v místě vpichu. Na místo vpichu můžete přiložit tampón. Místo vpichu nemasírujte. V případě potřeby překryjte místo vpichu náplastí s polštářkem.
Zapamatujte si:
Pokud budete mít jakékoliv problémy, obraťte se s žádostí o radu či pomoc na svého lékaře nebo sestru.
Likvidace použitých předplněných per
• Aranesp předplněné pero nesmí být NIKDY znovu použito.
• Na použité předplněné pero NIKDY nenasazujte zpět šedý kryt jehly.
• Použité předplněné pero musí být zlikvidováno v souladu s místními požadavky. Zeptejte se svého lékárníka, jak máte likvidovat přípravky, které již nepotřebujete. Tato opatření pomáhají chránit životní prostředí.
Nepovinný samostatný přídatný leták:
Přední strana - Návod jak začít s podáváním Aranespu:
|
ČESKY |
Aranesp SureClick předplněné pero - Před použitím si přečtěte příbalovou informaci | |||
|
Nejvhodnějším místem je přední strana stehna |
Jiná vhodná místa jsou břicho a zevní strana paží. |
Na jiných místech vpichu napněte kůži Napnout Místo vpichu musí být pevné a napnuté |
Pokyny pro injekci na druhé straně | |
Zadní strana - Návod jak začít s podáváním Aranespu:
|
ČESKY |
^H(1)Stáhněte šedý kryt jehly |
(2) Nedotýkejte se červeného tlačítka. Přitiskněte pero na kůži, aby došlo k odblokování bezpečnostního chrániče |
^H(3)|Krátce stlačte a uvolněte červené tlačítko |
^H(4)|Pomalu počítejte do 15 do ukončení injekce |
(5) Zkontrolujte okénko |
|
0 Neotáčejte šedým krytem jehly |
X Zablokováno |
Klik |
Z Pokud zežloutlo, je injekce dokončena. | ||
|
Z Odblokováno |
Tlačte stále odblokovaným perem proti kůži |
Příbalová informace: informace pro uživatele
Aranesp 10 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 15 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 20 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 30 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 40 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 50 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 60 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 80 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 100 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 130 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 150 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 300 mikrogramů injekční roztok v předplněné injekční stříkačce Aranesp 500 mikrogramů injekční roztok v předplněné injekční stříkačce
Darbepoetinum alfa
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat,
protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry .
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí
ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je Aranesp a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
3. Jak se Aranesp používá
4. Možné nežádoucí účinky
5. Jak Aranesp uchovávat
6. Obsah balení a další informace 1. Co je Aranesp a k čemu se používá
Lékař Vám předepsal Aranesp (antianemikum) k léčbě anémie. Anémie je onemocněním, kdy krev neobsahuje dostatek červených krvinek. Jejími příznaky mohou být únavnost, slabost a nedostatek dechu.
Aranesp účinkuje přesně stejným způsobem jako přirozený hormon erytropoetin. Erytropoetin vzniká v ledvinách a podněcuje kostní dřeň k tvorbě většího množství červených krvinek. Účinnou látkou obsaženou v Aranespu je darbepoetin alfa, vyrobený genovou technologií v buňkách vaječníku čínského křečka (CHO-K1).
Pokud máte chronické selhávání ledvin
Aranesp se používá k léčbě symptomatické anémie, která doprovází chronické selhávání ledvin, a to u dospělých a u dětí. Při selhávání ledvin se v nich nevytváří dostatek přirozeného hormonu erytropoetinu, což často způsobuje anémii.
Organismus potřebuje k vytvoření většího počtu červených krvinek určitý čas; proto účinek léčby zaznamenáte přibližně po čtyřech týdnech. Váš obvyklý dialyzační režim neovlivní schopnost Aranespu léčit anémii.
Pokud dostáváte chemoterapii
Aranesp se používá k léčbě anémie s příznaky u dospělých pacientů se zhoubnými nádory kromě nádorů kostní dřeně (nemyeloidními malignitami), kteří dostávají chemoterapii.
Jedním z hlavních nežádoucích účinků chemoterapie je, že tlumí tvorbu krevních buněk v kostní dřeni. K poklesu počtu červených krvinek a ke vzniku anémie může dojít spíše v období na konci chemoterapie, zvláště pokud se jednalo o podávání většího množství chemoterapeutik.
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
Nepoužívejte Aranesp:
- jestliže j ste alergický(á) na darbepoetin alfa nebo na kteroukoliv další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže Vám byl zjištěn vysoký krevní tlak, který není kontrolován jiným lékem předepsaným Vaším lékařem
Upozornění a opatření
Před použitím Aranespu se poraďte se svým lékařem, lékarníkem nebo zdravotní sestrou.
Oznamte prosím svému lékaři, jestliže v současné době trpíte nebo jste v minulosti trpěl(a):
- vysokým krevním tlakem, který je léčen jinými léky předepsanými Vaším lékařem;
- srpkovitou anémií;
- epileptickými záchvaty;
- křečemi (záchvaty);
- onemocněním jater;
- výrazně nedostatečnou odpovědí na léky používané k léčbě anémie;
- alergií na latex. Kryt jehly předplněné injekční stříkačky obsahuje derivát latexu; nebo
- infekční žloutenkou typu C.
Zvláštní upozornění:
- Pokud máte příznaky zahrnující neobvyklou únavu a nedostatek energie, může to znamenat že máte aplazii červené krevní řady (PRCA), která byla hlášena u některých pacientů. PRCA znamená, že organismus buď významně snížil produkci červených krvinek nebo dokonce zcela přestal s jejich tvorbou, což má za následek závažnou anémii. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře, který určí nejvhodnější postup léčby Vaší anémie.
- Buďte zvlášť opatrní u ostatních léků, které stimulují tvorbu červených krvinek. Aranesp je jedním ze skupiny léků, které stimulují tvorbu červených krvinek stejně jako lidská bílkovina erytropoetin. Váš lékař má vždy zaznamenat přesný název léku, který dostávate.
- Jestliže máte chronické selhání ledvin a zejména pokud patřičně nereagujete na léčbu Aranespem, Váš lékař by měl zkontrolovat Vaši dávku Aranespu, protože opakované zvyšování dávky Aranespu v případě, že nereagujete na léčbu, může zvyšovat riziko problémů se srdcem nebo krevními cévami a mohlo by zvýšit riziko srdečního infarktu, mrtvice a úmrtí.
- Váš lékař by se měl snažit udržovat Vaši hladinu hemoglobinu mezi 10 a 12 g/dl. Váš lékař bude dohlížet, aby hladina Vašeho hemoglobinu nepřekročila stanovenou hodnotu, protože vysoké hladiny hemoglobinu Vás mohou vystavovat riziku srdečních obtíží nebo obtíží s cévami a zvyšovat riziko srdečního infarktu, mrtvice nebo úmrtí.
- Pokud máte příznaky zahrnující silnou bolest hlavy, netečnost, zmatenost, obtíže se zrakem, nevolnost, zvracení nebo záchvaty (křeče), může to znamenat, že máte velmi vysoký krevní tlak. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře.
- V případě, že trpíte nádorovým onemocněním, mějte na paměti, že Aranesp může působit jako růstový faktor krvinek a za určitých okolností může mít negativní vliv na Vaše nádorové onemocnění. Podle Vaší individuální situace může být vhodnější krevní transfúze. Projednejte prosím tuto skutečnost s Vaším ošetřujícím lékařem.
- Nesprávné podávání zdravým osobám může způsobit život ohrožující srdeční nebo cévní komplikace.
Další léčivé přípravky a Aranesp
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Počtem červených krvinek mohou být ovlivněny cyklosporin a takrolimus (léky potlačující imunitní odpověď organismu). Je důležité, abyste svému lékaři sdělil(a), zda některý z těchto léků užíváte.
Aranesp s jídlem a pitím
Jídlo a pití Aranesp neovlivňuje.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Aranesp nebyl testován u těhotných žen. Je důležité, abyste svému lékaři sdělila, zda
• jste těhotná;
• myslíte si, že byste mohla být těhotná;
• plánujete otěhotnět.
Není známo, zda se darbepoetin alfa vylučuje do lidského mateřského mléka. Pokud užíváte Aranesp, musíte přestat kojit.
Řízení dopravních prostředků a obsluha strojů
Aranesp by neměl ovlivnit schopnost řídit dopravní prostředky a obsluhovat stroje.
Aranesp obsahuje sodík
Tento přípravek obsahuje méně než 1 mmol sodíku (23 mg) v dávce, to znamená, že je v podstatě bez sodíku.
3. Jak se Aranesp používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Na základě vyšetření krve rozhodl Váš lékař o léčbě Aranespem, protože Vaše hladina hemoglobinu je 10 g/dl nebo nižší. Lékař Vám řekne, jaké množství léku budete užívat a jak často, aby se Vaše hladina hemoglobinu udržela mezi 10 a 12 g/dl. To se může výrazně lišit pro dospělé a děti.
Podávání injekcí Aranespu pacientem samotným
Váš lékař rozhodl, že pro Vás bude nejvhodnější, abyste si podával(a) injekce Aranespu sám (sama) nebo aby Vám ji podával Váš pečovatel či sestra předplněným perem. Postup, jakým si sám (sama) budete injekce předplněným perem podávat, Vám ukáže lékař, sestra nebo lékárník. Nepokoušejte si dát injekci sám (sama), pokud jste k tomu nebyl(a) vyškolen(a). Nikdy si sám (sama) nepodávejte Aranesp do žíly.
Pokud trpíte chronickým selháváním ledvin
Všem dospělým a dětským pacientům od 1 roku s chronickým selháváním ledvin je Aranesp podáván v jedné injekci, a to buď podkožně (subkutánní podání) nebo do žíly (intravenózní podání).
Pro léčbu anémie bude úvodní dávka Aranespu na kilogram Vaší tělesné hmotnosti buď:
• 0,75 mikrogramů jednou za dva týdny nebo;
• 0,45 mikrogramů j ednou týdně.
U dospělých nedialyzovaných pacientů může být jako úvodní dávka použito také 1,5 mikrogramu/kg jednou měsíčně.
U všech dospělých a dětských pacientů od 1 roku s chronickým selháváním ledvin, u kterých je dosaženo korekce anémie, je pokračováno v podávání Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny. Všichni dospělí a děti od 11 let, kteří nejsou na dialýze, mohou Aranesp dostávat v injekci jednou za měsíc.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a jednou za čtyři týdny může upravit dávku podle potřeby, aby byla dosažena trvalá kontrola Vaší anémie.
Váš lékař bude používat nejnižší účinnou látku, aby byly příznaky anémie pod kontrolou.
Pokud nereagujete přiměřeně na léčbu Aranespem, Váš lékař zkontroluje Vaši dávku a informuje Vás, pokud je potřeba Vaši dávku Aranespu změnit.
Pravidelně bude sledován také Váš krevní tlak, a to zvláště na začátku léčby.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Lékař rozhodl o změně způsobu podávání injekcí (přechod od podkožní aplikace k podávání nitrožilnímu). V případě změny začnete na stejné dávce, kterou právě dostáváte a Váš lékař provede odběr krve, aby se zajistilo, že je anémie stále léčena odpovídajícím způsobem.
Pokud lékař rozhodl Vaši léčbu změnit z r-HuEPO (erytropoetin vyrobený genovou technologií) na Aranesp, stanoví, zda budete dostávat dávku Aranespu jednou týdně nebo jednou za dva týdny.
Způsob podání injekce je stejný jako v případě r-HuEPO, ale Váš lékař Vám sdělí, jakou dávku máte užívat a kdy, a bude-li to nutné, dávku upraví.
Pokud dostáváte chemoterapii
Aranesp budete dostávat v jedné podkožní injekci buď jednou týdně, nebo jednou za tři týdny.
Pro léčbu anémie bude úvodní dávka buď
• 500 mikrogramů jednou za tři týdny (6,75 mikrogramů Aranespu na kilogram Vaší tělesné hmotnosti) nebo;
• 2,25 mikrogramů (jednou týdně) Aranespu na kilogram tělesné hmotnosti.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a může upravit dávku podle potřeby. Léčba bude trvat přibližně čtyři týdny po ukončení chemoterapie. Lékař Vám sdělí, kdy přesně máte Aranesp přestat užívat.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Jestliže jste použil(a) více Aranespu, než jste měl(a)
Jestliže jste užil(a) více Aranespu, než potřebujete, mohlo by dojít k závažným potížím, například k velmi vysokému krevnímu tlaku. Pokud k tomu dojde, obraťte se prosím na svého lékaře. V případě, že se v jakémkoliv ohledu nebudete cítit dobře, neprodleně vyhledejte svého lékaře, sestru nebo lékárníka.
Jestliže jste zapomněl(a) použít Aranesp
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste zapomněl(a) podat dávku Aranespu, měl(a) byste se spojit se svým lékařem a dohodnout se, kdy byste měl(a) další dávku podat.
Jestliže jste přestal(a) používat Aranesp
Pokud chcete přestat používat Aranesp, poraďte se nejdříve se svým lékařem.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i Aranesp nežádoucí účinky, které se ale nemusí vyskytnout u každého.
U některých pacientů užívajících Aranesp se vyskytly následující nežádoucí účinky:
Pacienti s chronickým selháním ledvin
Velmi časté: mohou postihnout více než 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Alergické reakce
Časté: mohou postihnout až 1 z 10 osob
• Mozková mrtvice
• Bolest okolo místa vpichu
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Krevní sraženiny (trombóza)
• Křeče (záchvaty)
Není známo: z dostupných údajů nelze četnost určit
• Čistá aplazie červených krvinek (PRCA) - (anémie, neobvyklá únava, nedostatek energie) Pacienti se zhoubným onemocněním
Velmi časté: mohou postihnout více než 1 z 10 osob
• Alergické reakce
• Zadržování tekutin (edém)
Časté: mohou postihnout až 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Krevní sraženiny (trombóza)
• Bolest okolo místa vpichu injekce
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Křeče (záchvaty)
Všichni pacienti
Není známo: z dostupných údajů nelze četnost určit
• Závažné alergické reakce, které mohou zahrnovat:
- Náhlé život ohrožující alergické reakce (anafylaxe)
- Otok obličeje, rtů, úst, jazyka nebo hrdla který může činit potíže při polykání nebo dýchání (angioedém)
- Dušnost (alergický bronchospasmus)
- Kožní vyrážka
- Kopřivka
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Aranesp uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na krabičce a štítku za EXP:. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2°C - 8°C). Chraňte před mrazem. Nepoužívejte Aranesp, jestliže si myslíte, že mohlo dojít k jeho zmrznutí.
Uchovávejte předplněnou injekční stříkačku v krabičce, aby byl přípravek chráněn před světlem.
Poté, co injekční stříkačku vyndáte z chladničky a necháte ji stát při pokojové teplotě přibližně 30 minut, musí být přípravek buď použit do 7 dnů nebo zlikvidován.
Nepoužívejte tento přípravek, pokud je zakalený nebo pokud jsou v něm patrné částice.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte.
6. Obsah balení a další informace Co Aranesp obsahuje
- Léčivou látkou je darbepoetinum alfa, r-HuEPO (erytropoetin vyráběný genovou technologií). Předplněná injekční stříkačka obsahuje darbepoetinum alfa 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300 nebo 500 mikrogramů.
- Dalšími složkami jsou dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80 a voda na injekci.
Jak Aranesp vypadá a co obsahuje toto balení
Aranesp je čirý, bezbarvý nebo lehce perleťově zabarvený injekční roztok v předplněné injekční stříkačce.
Aranesp je k dispozici v baleních po 1 nebo 4 předplněných injekčních stříkačkách s automatickým chráničem jehly v balení s blistrem. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Držitel rozhodnutí o registraci:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Výrobce:
Amgen Technology Ireland (ADL)
Pottery Road Dun Laoghaire Co Dublin Irsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci.
Belgie/Belgique/Belgien
s.a. Amgen n.v.
Tel/Tél: +32 (0)2 7752711
Eb^rapHu
AMg^eH Etnrapna EOOfl Ten.: +359 (0)2 424 7440
Česká republika
Amgen s.r.o.
Tel: +420 221 773 500
Danmark
Amgen, filial af Amgen AB, Sverige
Tlf: +45 39617500
Deutschland
AMGEN GmbH Tel.: +49 89 1490960
Lietuva
Amgen Switzerland AG Vilniaus filialas Tel: +370 5 219 7474
Luxembourg/Luxemburg
s.a. Amgen Belgique/Belgien Tel/Tél: +32 (0)2 7752711
Magyarország
Amgen Kft.
Tel.: +36 1 35 44 700
Malta
Amgen B.V.
The Netherlands Tel: +31 (0)76 5732500
Nederland
Amgen B.V.
Tel: +31 (0)76 5732500
Eesti
Norge
Amgen AB Tel: +47 23308000
Amgen Switzerland AG Vilniaus filialas Tel: +372 5125 501
|
EXláda Amgen ETAág OappaKsurixá E.n.E. TpL: +30 210 3447000 |
Osterreich Amgen GmbH Tel: +43 (0)1 50 217 |
|
Espaňa Amgen S.A. Tel: +34 93 600 18 60 |
Polska Amgen Biotechnologia Sp. z o.o. Tel.: +48 22 581 3000 |
|
France Amgen S.A.S. Tél: +33 (0)9 69 363 363 |
Portugal Amgen Biofarmaceutica, Lda. Tel: +351 21 4220550 |
|
Hrvatska Amgen d.o.o. Tel: +385 (1) 562 57 20 |
Románia Amgen Románia SRL Tel: +4021 527 3000 |
|
Ireland Amgen Limited United Kingdom Tel: +44 (0)1223 420305 |
Slovenija AMGEN zdravila d.o.o. Tel: +386 (0)1 585 1767 |
|
Island Vistor hf. Sími: +354 535 7000 |
Slovenská republika Amgen Slovakia s.r.o. Tel: +421 33 321 13 22 |
|
Italia Amgen S.r.l. Tel: +39 02 6241121 |
Suomi/Finland Amgen AB, sivuliike Suomessa/Amgen AB, filial i Finland Puh/Tel: +358 (0)9 54900500 |
|
Kúnpoq Papaellinas & Co Ltd TpL: +357 22741 741 |
Sverige Amgen AB Tel: +46 (0)8 6951100 |
|
Latvija Amgen Switzerland AG Rrgas filiale Tel: +371 292 84807 |
United Kingdom Amgen Limited Tel: +44 (0)1223 420305 |
Tato příbalová informace byla naposledy revidována.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky na adrese http://www.ema.europa.eu.
Popis jednotlivých částí
Před použitím
Po použití
Opěrky pro prsty
Štítek stříkačky Kartuše stříkačky
Bezpečnostní chránič stříkačky
Bezpečnostní pružina jehly
Nasazený šedý kryt jehly
Píst


Použitý píst
Štítek stříkačky
Použitá kartuše stříkačky
Použitá jehla

Sejmutý šedý kryt jehly
Použitá bezpečnostní pružina jehly
Důležité
Před použitím Aranespu předplněné injekční stříkačky s automatickým chráničem jehly si přečtěte
tyto důležité informace:
• Je důležité, abyste se nepokoušel(a) podat si sám(sama) injekci, dokud vás neproškolí váš lékař nebo zdravotnický pracovník.
• Aranesp je podáván jako injekce do tkáně těsně pod kůží (subkutánní injekce).
• Řekněte svému lékaři, pokud jste alergický(á) na latex. Kryt jehly předplněné injekční stříkačky obsahuje derivát latexu, který může způsobovat závažné alergické reakce.
X Nesnímejte z předplněné stříkačky šedý kryt jehly, dokud nejste připraven(a) na podání injekce.
X Nepoužívejte předplněnou injekční stříkačku, pokud vám upadla na tvrdý povrch. Použijte novou předplněnou injekční stříkačku a informujte svého lékaře nebo zdravotnického pracovníka.
X Nepokoušejte se aktivovat předplněnou injekční stříkačku před podáním injekce.
X Nepokoušejte se z předplněné injekční stříkačky.odstranit průhledný bezpečnostní chránič.
X Nesnažte se vyjmout oddělitelný štítek z kartuše předplněné stříkačky před podáním injekce.
V případě otázek zavolejte svému lékaři nebo zdravotnickému pracovníkovi.
|
Krok 1: Příprava | |
|
A |
Vyjměte z obalu vaničku s předplněnou injekční stříkačkou a připravte si všechny pomůcky pro podání injekce: lihové tampóny, buničinový nebo gázový polštářek, náplast a nádobu na ostrý odpad (nejsou součástí balení). |
Balení s nepoužitými předplněnými injekčními stříkačkami vraťte do chladničky.
Aby byla injekce příjemnější, ponechte předplněnou injekční stříkačku při pokojové teplotě po dobu asi 30 minut. Pečlivě si umyjte ruce vodou a mýdlem.
Novou předplněnou injekční stříkačku a ostatní pomůcky dejte na čistou, dobře osvětlenou plochu.
X Neohřívejte předplněnou injekční stříkačku pomocí zdrojů tepla, např. v horké vodě nebo v mikrovlnné troubě.
X Nenechávejte předplněnou injekční stříkačku na přímém slunečním světle.
X Netřepte předplněnou injekční stříkačkou.
• Uchovávejte předplněné injekční stříkačky mimo dohled a dosah dětí.
B
Otevřete vaničku odtržením fólie. Uchopte bezpečnostní kryt stříkačky a předplněnou injekční stříkačku vyjměte z vaničky.

Uchopit zde
Z důvodu bezpečnosti:
íf Neberte stříkačku za píst
íf Neberte stříkačku za šedý kryt jehly
C
Kontrola léku a předplněné injekční stříkačky.
Lék

>; Předplněnou injekční stříkačku nepoužívejte, pokud:
• Je lék zakalen nebo obsahuje pevné částice. Musí to být čirá a bezbarvá tekutina.
• Se některá část zdá být prasklá nebo rozbitá.
• Chybí šedý kryt jehly nebo není bezpečně nasazen.
• Uplynul poslední den měsíce uvedeného u doby použitelnosti na štítku.
Ve všech těchto případech volejte svému lékaři nebo zdravotnickému pracovníkovi.
A
Krok 2: Před podáním injekce
Pečlivě si umyjte ruce. Připravte si a očistěte místo pro aplikaci injekce.
Můžete použít:
• Horní část stehna

Horní část paže
Břicho
Horní strana stehna
• Břicho kromě oblasti 5 cm okolo pupku
• Vněj ší stranu horní části paže (pouze pokud vám injekci podává někdo jiný)
Místo aplikace očistěte lihovým tamponem. Pokožku nechte uschnout.
X

Před aplikací se místa injekce nedotýkejte.
Pro každou injekci, kterou si budete podávat, vyberte jinou oblast aplikace. Pokud si potřebujete podat injekci do stejné oblasti, dbejte na to, abyste si ji nepodali do stejného místa jako předchozí injekci.
Injekci nepodávejte do míst, kde je kůže jemná, pohmožděná, červená nebo tvrdá. Nepodávejte injekci do oblastí s jizvami nebo strijemi.



Při aplikaci injekce je důležité držet kůži stisknutou.

STLAČUJTE píst pomalu a rovnoměrně, dokud neucítíte nebo neuslyšíte “cvaknutí”. Píst stlačte zcela dolů až do cvaknutí.
B


Je důležité stlačit píst zcela dolů až do “cvaknutí”, aby byla podána celá vaše dávka.
C
UVOLNĚTE palec. Pak VYTÁHNĚTE stříkačku z pokožky.

Po uvolnění pístu bezpečnostní chránič předplněné injekční stříkačky bezpečně zakryje jehlu. >; Nenasazujte šedý kryt jehly zpět na použitou předplněnou injekční stříkačku.
Pouze pro zdravotnické pracovníky
Oddělte a uschovejte štítek předplněné injekční stříkačky.

Otáčejte pístem tak, aby se štítek stříkačky dostal do pozice, kde ho můžete oddělit.
A
Krok 4: Dokončení
Předplněnou injekční stříkačku a další potřeby vyhoďte do nádoby na ostrý odpad.

Léky musí být zlikvidovány v souladu s místními požadavky. Zeptejte se svého lékárníka, jak zlikvidovat léky, které už nepotřebujete. Tato opatření pomohou chránit životní prostředí.
Stříkačku a nádobu na ostrý odpad uchovávejte mimo dohled a dosah dětí. íť Předplněnou injekční stříkačku nepoužívejte znovu.
X Předplněné injekční stříkačky nerecyklujte , ani je nevyhazujte do domácího odpadu.
B Zkontrolujte místo vpichu.
Pokud se objeví krev, přiložte na místo injekce buničinový nebo gázový polštářek. Místo vpichu netřete. Pokud je třeba, přelepte místo vpichu náplastí.
Příbalová informace: informace pro uživatele
Aranesp 25 mikrogramů injekční roztok v injekční lahvičce Aranesp 40 mikrogramů injekční roztok v injekční lahvičce Aranesp 60 mikrogramů injekční roztok v injekční lahvičce Aranesp 100 mikrogramů injekční roztok v injekční lahvičce Aranesp 200 mikrogramů injekční roztok v injekční lahvičce Aranesp 300 mikrogramů injekční roztok v injekční lahvičce Darbepoetinum alfa
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry .
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci:
1. Co je Aranesp a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
3. Jak se Aranesp používá
4. Možné nežádoucí účinky
5. Jak Aranesp uchovávat
6. Obsah balení a další informace 1. Co je Aranesp a k čemu se používá
Lékař Vám předepsal Aranesp (antianemikum) k léčbě anémie. Anémie je onemocněním, kdy krev neobsahuje dostatek červených krvinek. Jejími příznaky mohou být únavnost, slabost a nedostatek dechu.
Aranesp účinkuje přesně stejným způsobem jako přirozený hormon erytropoetin. Erytropoetin vzniká v ledvinách a podněcuje kostní dřeň k tvorbě většího množství červených krvinek. Účinnou látkou obsaženou v Aranespu je darbepoetin alfa, vyrobený genovou technologií v buňkách vaječníku čínského křečka (CHOK1).
Pokud máte chronické selhávání ledvin
Aranesp se používá k léčbě symptomatické anémie, která doprovází chronické selhávání ledvin, a to u dospělých a u dětí. Při selhávání ledvin se v nich nevytváří dostatek přirozeného hormonu erytropoetinu, což často způsobuje anémii.
Organismus potřebuje k vytvoření většího počtu červených krvinek určitý čas; proto účinek léčby zaznamenáte přibližně po čtyřech týdnech. Váš obvyklý dialyzační režim neovlivní schopnost Aranespu léčit anémii.
Pokud dostáváte chemoterapii
Aranesp se používá k léčbě anémie s příznaky u dospělých pacientů se zhoubnými nádory kromě nádorů kostní dřeně (nemyeloidními malignitami), kteří dostávají chemoterapii.
Jedním z hlavních nežádoucích účinků chemoterapie je, že tlumí tvorbu krevních buněk v kostní dřeni. K poklesu počtu červených krvinek a ke vzniku anémie může dojít spíše v období na konci chemoterapie, zvláště pokud se jednalo o podávání většího množství chemoterapeutik.
2. Čemu musíte věnovat pozornost, než začnete Aranesp používat
Nepoužívejte Aranesp:
- jestliže jste alergický(á) na darbepoetin alfa nebo na kteroukoliv další složku tohoto přípravku (uvedenou v bodě 6).
- jestliže Vám byl zjištěn vysoký krevní tlak, který není kontrolován jiným lékem předepsaným Vaším lékařem
Upozornění a opatření
Před použitím Aranespu se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou.
Oznamte prosím svému lékaři, jestliže v současné době trpíte nebo jste v minulosti trpěl(a):
- vysokým krevním tlakem, který je léčen jinými léky předepsanými Vaším lékařem;
- srpkovitou anémií;
- epileptickými záchvaty;
- křečemi (záchvaty);
- onemocněním jater;
- výrazně nedostatečnou odpovědí na léky používané k léčbě anémie;
- infekční žloutenkou typu C.
Zvláštní upozornění:
- Pokud máte příznaky zahrnující neobvyklou únavu a nedostatek energie, může to znamenat že máte aplazii červené krevní řady (PRCA), která byla hlášena u některých pacientů. PRCA znamená, že organismus buď významně snížil produkci červených krvinek nebo dokonce zcela přestal s jejich tvorbou, což má za následek závažnou anémii. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře, který určí nejvhodnější postup léčby Vaší anémie.
- Buďte zvlášť opatrní u ostatních léků, které stimulují tvorbu červených krvinek. Aranesp je jedním ze skupiny léků, které stimulují tvorbu červených krvinek stejně jako lidská bílkovina erytropoetin. Váš lékař má vždy zaznamenat přesný název léku, který dostávate.
- Jestliže máte chronické selhání ledvin a zejména pokud patřičně nereagujete na léčbu Aranespem, Váš lékař by měl zkontrolovat Vaši dávku Aranespu, protože opakované zvyšování dávky Aranespu v případě, že nereagujete na léčbu, může zvyšovat riziko problémů se srdcem nebo krevními cévami a mohlo by zvýšit riziko srdečního infarktu, mrtvice a úmrtí.
- Váš lékař by se měl snažit udržovat Vaši hladinu hemoglobinu mezi 10 a 12 g/dl. Váš lékař bude dohlížet, aby hladina Vašeho hemoglobinu nepřekročila stanovenou hodnotu, protože vysoké hladiny hemoglobinu Vás mohou vystavovat riziku srdečních obtíží nebo obtíží s cévami a zvyšovat riziko srdečního infarktu, mrtvice nebo úmrtí.
- Pokud máte příznaky zahrnující silnou bolest hlavy, netečnost, zmatenost, obtíže se zrakem, nevolnost, zvracení nebo záchvaty (křeče), může to znamenat, že máte velmi vysoký krevní tlak. Začnete-li pociťovat tyto příznaky, měl(a) byste vyhledat svého ošetřujícího lékaře.
- V případě, že trpíte nádorovým onemocněním, mějte na paměti, že Aranesp může působit jako růstový faktor krvinek a za určitých okolností může mít negativní vliv na Vaše nádorové onemocnění. Podle Vaší individuální situace může být vhodnější krevní transfúze. Projednejte prosím tuto skutečnost s Vaším ošetřujícím lékařem.
- Nesprávné podávání zdravým osobám může způsobit život ohrožující srdeční nebo cévní komplikace.
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Počtem červených krvinek mohou být ovlivněny cyklosporin a takrolimus (léky potlačující imunitní odpověď organismu). Je důležité, abyste svému lékaři sdělil(a), zda některý z těchto léků užíváte.
Aranesp s jídlem a pitím
Jídlo a pití Aranesp neovlivňuje.
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Aranesp nebyl testován u těhotných žen. Je důležité, abyste svému lékaři sdělila, zda
• jste těhotná;
• myslíte si, že byste mohla být těhotná;
• plánujete otěhotnět.
Není známo, zda se darbepoetin alfa vylučuje do lidského mateřského mléka. Pokud užíváte Aranesp, musíte přestat kojit.
Řízení dopravních prostředků a obsluha strojů
Aranesp by neměl ovlivnit schopnost řídit dopravní prostředky a obsluhovat stroje.
Aranesp obsahuje sodík
Tento přípravek obsahuje méně než 1 mmol sodíku (23 mg) v dávce, to znamená, že je v podstatě bez sodíku.
3. Jak se Aranesp používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Na základě vyšetření krve rozhodl Váš lékař o léčbě Aranespem, protože Vaše hladina hemoglobinu je 10 g/dl nebo nižší. Lékař také rozhodne o tom, jaké množství léku budete užívat a jak často, aby se Vaše hladina hemoglobinu udržela mezi 10 a 12 g/dl. To se může výrazně lišit pro dospělé a děti.
Injekci Vám podá zdravotnický pracovník.
Pokud trpíte chronickým selháváním ledvin
Všem dospělým a dětským pacientům od 1 roku s chronickým selháváním ledvin je Aranesp podáván zdravotnickým pracovníkem v jedné injekci, a to buď podkožně (subkutánní podání) nebo do žíly (intravenózní podání).
Pro léčbu anémie bude úvodní dávka Aranespu na kilogram Vaší tělesné hmotnosti buď:
• 0,75 mikrogramů j ednou za dva týdny nebo
• 0,45 mikrogramů j ednou týdně.
U dospělých nedialyzovaných pacientů může být jako úvodní dávka použito také 1,5 mikrogramu/kg jednou měsíčně.
U všech dospělých a dětských pacientů od 1 roku s chronickým selháváním ledvin, u kterých je dosaženo korekce anémie, je pokračováno v podávání Aranespu v jedné injekci jednou týdně nebo jednou za dva týdny. Všichni dospělí a děti od 11 let, kteří nejsou na dialýze, mohou Aranesp dostávat v injekci jednou za měsíc.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a jednou za čtyři týdny může upravit dávku podle potřeby, aby byla dosažena trvalá kontrola Vaší anémie.
Váš lékař bude používat nejnižší účinnou látku, aby byly příznaky anémie pod kontrolou.
Pokud nereagujete přiměřeně na léčbu Aranespem, Váš lékař zkontroluje Vaši dávku a informuje Vás, pokud je potřeba Vaši dávku Aranespu změnit.
Pravidelně bude sledován také Váš krevní tlak, a to zvláště na začátku léčby.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Lékař může rozhodnout o změně způsobu podávání injekcí (buďto podkožně nebo do žíly). V případě změny začnete na stejné dávce, kterou právě dostáváte a Váš lékař provede odběr krve, aby se zajistilo, že je anémie stále léčena odpovídajícím způsobem.
Pokud lékař rozhodl Vaši léčbu změnit z r-HuEPO (erytropoetin vyrobený genovou technologií) na Aranesp, stanoví, zda budete dostávat dávku Aranespu jednou týdně nebo jednou za dva týdny.
Způsob podání injekce je stejný jako v případě r-HuEPO, ale Váš lékař Vám sdělí, jakou dávku máte užívat a kdy, a bude-li to nutné, dávku upraví.
Pokud dostáváte chemoterapii
Aranesp budete dostávat v jedné podkožní injekci jednou týdně nebo jednou za tři týdny.
Pro léčbu anémie bude úvodní dávka
• 500 mikrogramů jednou za tři týdny (6,75 mikrogramů Aranespu na kilogram Vaší tělesné hmotnosti) nebo
• 2,25 mikrogramů (jednou týdně) Aranespu na kilogram Vaší tělesné hmotnosti.
Váš lékař bude provádět pravidelné odběry krve, aby zkontroloval, jak anémie reaguje na léčbu a může upravit dávku podle potřeby. Léčba bude trvat přibližně čtyři týdny po ukončení chemoterapie. Lékař Vám sdělí, kdy přesně máte Aranesp přestat užívat.
V některých případech může lékař doporučit doplňkové podávání přípravků železa.
Jestliže jste použil(a) více Aranespu, než jste měl(a)
Jestliže jste dostal(a) více Aranespu, než potřebujete, mohlo by dojít k závažným potížím, například k velmi vysokému krevnímu tlaku. Pokud k tomu dojde, obraťte se prosím na svého lékaře. V případě, že se v jakémkoliv ohledu nebudete cítit dobře, neprodleně vyhledejte svého lékaře, sestru nebo lékárníka.
Jestliže jste zapomněl(a) použít Aranesp
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku.
Jestliže jste vynechal(a) dávku Aranespu, měl(a) byste se spojit se svým lékařem a dohodnout se, kdy byste měl(a) další dávku dostat.
Pokud chcete přestat používat Aranesp, poraďte se nejdříve se svým lékařem.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i Aranesp nežádoucí účinky, které se ale nemusí vyskytnout u každého.
U některých pacientů užívajících Aranesp se vyskytly následující nežádoucí účinky:
Pacienti s chronickým selháním ledvin
Velmi časté: mohou postihnout více než 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Alergické reakce
Časté: mohou postihnout až 1 z 10 osob
• Mozková mrtvice
• Bolest okolo místa vpichu
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Krevní sraženiny (trombóza)
• Křeče (záchvaty)
Není známo: z dostupných údajů nelze četnost určit
• Čistá aplazie červených krvinek (PRCA) - (anémie, neobvyklá únava, nedostatek energie) Pacienti se zhoubným onemocněním
Velmi časté: mohou postihnout více než 1 z 10 osob
• Alergické reakce
• Zadržování tekutin (edém)
Časté: mohou postihnout až 1 z 10 osob
• Vysoký krevní tlak (hypertenze)
• Krevní sraženiny (trombóza)
• Bolest okolo místa vpichu injekce
• Vyrážka a/nebo zčervenání kůže
Méně časté: mohou postihnout až 1 ze 100 osob
• Křeče (záchvaty)
Všichni pacienti
Není známo: z dostupných údajů nelze četnost určit
• Závažné alergické reakce, které mohou zahrnovat:
- Náhlé život ohrožující alergické reakce (anafylaxe)
- Otok obličeje, rtů, úst, jazyka nebo hrdla který může činit potíže při polykání nebo dýchání (angioedém)
- Dušnost (alergický bronchospasmus)
- Kožní vyrážka
- Kopřivka
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Aranesp uchovávat
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti, uvedené na krabičce a štítku za EXP:. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v chladničce (2°C - 8°C). Chraňte před mrazem. Nepoužívejte Aranesp, jestliže si myslíte, že mohlo dojít k jeho zmrznutí.
Uchovávejte injekční lahvičku v krabičce, aby byl přípravek chráněn před světlem.
Poté, co injekční lahvičku vyndáte z chladničky a necháte ji stát při pokojové teplotě přibližně 30 minut, musí být přípravek buď použit do 7 dnů nebo zlikvidován.
Nepoužívejte tento přípravek, pokud je zakalený nebo pokud jsou v něm patrné částice.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte.
6. Obsah balení a další informace Co Aranesp obsahuje
- Léčivou látkou je darbepoetinum alfa, r-HuEPO (erytropoetin vyráběný genovou technologií). Injekční lahvička obsahuje darbepoetinum alfa 25, 40, 60, 100, 200, nebo 300 mikrogramů.
- Dalšími složkami jsou dihydrogenfosforečnan sodný, hydrogenfosforečnan sodný, chlorid sodný, polysorbát 80 a voda na injekci.
Jak Aranesp vypadá a co obsahuje toto balení
Aranesp je čirý, bezbarvý nebo lehce perleťově zabarvený injekční roztok v injekční lahvičce.
Aranesp je k dispozici v baleních po 1 nebo 4 injekčních lahvičkách. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Držitel rozhodnutí o registraci:
Amgen Europe B.V.
Minervum 7061 NL-4817 ZK Breda Nizozemsko
Výrobce:
Amgen Technology Ireland (ADL)
Pottery Road
Dun Laoghaire
Co Dublin
Irsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci
Belgie/Belgique/Belgien
s.a. Amgen n.v.
Tel/Tél: +32 (0)2 7752711
Eb^rapufl
AMg^eH Etnrapna EOOfl Ten.: +359 (0)2 424 7440
Česká republika
Amgen s.r.o.
Tel: +420 221 773 500
Danmark
Amgen, filial af Amgen AB, Sverige Tlf: +45 39617500
Deutschland
AMGEN GmbH Tel.: +49 89 1490960
Eesti
Amgen Switzerland AG Vilniaus filialas Tel: +372 5125 501
EXláSa
Amgen ETAág OappaKsurixá E.n.E. TpL: +30 210 3447000
Espaňa
Amgen S.A.
Tel: +34 93 600 18 60
France
Amgen S.A.S.
Tél: +33 (0)9 69 363 363
Lietuva
Amgen Switzerland AG Vilniaus filialas Tel: +370 5 219 7474
Luxembourg/Luxemburg
s.a. Amgen Belgique/Belgien Tel/Tél: +32 (0)2 7752711
Magyarország
Amgen Kft.
Tel.: +36 1 35 44 700
Malta
Amgen B.V.
The Netherlands Tel: +31 (0)76 5732500
Nederland
Amgen B.V.
Tel: +31 (0)76 5732500
Norge
Amgen AB Tel: +47 23308000
Osterreich
Amgen GmbH Tel: +43 (0)1 50 217
Polska
Amgen Biotechnologia Sp. z o.o.
Tel.: +48 22 581 3000
Portugal
Amgen Biofarmaceutica, Lda.
Tel: +351 21 4220550
|
Hrvatska Amgen d.o.o. Tel: +385 (1) 562 57 20 |
Románia Amgen Románia SRL Tel: +4021 527 3000 |
|
Ireland Amgen Limited United Kingdom Tel: +44 (0)1223 420305 |
Slovenija AMGEN zdravila d.o.o. Tel: +386 (0)1 585 1767 |
|
Island Vistor hf. Sími: +354 535 7000 |
Slovenská republika Amgen Slovakia s.r.o. Tel: +421 33 321 13 22 |
|
Italia Amgen S.r.l. Tel: +39 02 6241121 |
Suomi/Finland Amgen AB, sivuliike Suomessa/Amgen AB, filial i Finland Puh/Tel: +358 (0)9 54900500 |
|
Kónpoq Papaellinas & Co Ltd TpL: +357 22741 741 |
Sverige Amgen AB Tel: +46 (0)8 6951100 |
|
Latvija Amgen Switzerland AG Rrgas filiale Tel: +371 292 84807 |
United Kingdom Amgen Limited Tel: +44 (0)1223 420305 |
Tato příbalová informace byla naposledy revidována.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky na adrese http://www.ema.europa.eu.
Na webových stránkách Evropské agentury pro léčivé přípravky je tato příbalová informace k dispozici ve všech úředních jazycích EU/EHP.
238