Airexar Spiromax 50 Mikrogramů/500 Mikrogramů
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Airexar Spiromax 50 mikrogramů/500 mikrogramů prášek k inhalaci
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna odměřená dávka obsahuje 50 mikrogramů salmeterolum (ve formě salmeteroli xinafoas) a 500 mikrogramů flutikasoni propionas.
Jedna podaná dávka (dávka, která je uvolněna přes náustek) obsahuje 45 mikrogramů salmeterolum (ve formě salmeteroli xinafoas) a 465 mikrogramů flutikasoni propionas.
Pomocná látka/Pomocné látky se známým účinkem:
Jedna dávka obsahuje přibližně 10 miligramů laktózy (ve formě monohydrátu).
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Prášek k inhalaci.
Bílý prášek.
Bílý inhalátor s poloprůhledným žlutým krytem náustku.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Airexar Spiromax je indikován pouze k léčbě dospělých ve věku od 18 let.
Airexar Spiromax je indikován k pravidelné léčbě pacientů se závažným astmatem, u nichž je vhodné použití kombinovaného přípravku (inhalační kortikosteroid a dlouhodobě působící p2 agonista):
- pacientů nedostatečně kontrolovaných kombinovaným přípravkem s nižší dávkou kortikosteroidu nebo
- pacientů již kontrolovaných vysokou dávkou inhalačního kortikosteroidu a dlouhodobě působícího P2 agonisty.
Chronická obstrukční plicní nemoc (CHOPN)
Airexar Spiromax je indikován k symptomatické léčbě pacientů s CHOPN s FEVi <60 % předpokládané normální hodnoty (před podáním bronchodilatátoru) a s anamnézou opakovaných exacerbací, kteří mají závažné příznaky přes pravidelnou léčbu bronchodilatátory.
4.2 Dávkování a způsob podání
Airexar Spiromax je indikován pouze u dospělých ve věku od 18 let.
Airexar Spiromax není indikován k použití u dětí ve věku do 12 let a u dospívajících ve věku od 13 do 17 let.
Dávkování
Způsob podání: inhalační podání
Pacienty je nutno upozornit, že k dosažení optimálního léčebného přínosu musí Airexar Spiromax používat denně, i když jsou asymptomatičtí.
Pacienti musí být pravidelně kontrolováni lékařem, aby byla síla inhalátoru se salmeterolem/flutikason-propionátem stále optimální; mění se pouze na radu lékaře. Dávku je nutno postupně upravovat na nejnižší možnou dávku, při které je zachována účinná kontrola příznaků. Airexar Spiromax není na trhu dostupný v menší síle než 50/500 mikrogramů. Pokud je vhodné snižování dávky na nižší hodnoty, kterých není možné s přípravkem Airexar Spiromax dosáhnout, je potřebné převedení na alternativní kombinovaný přípravek s fixními dávkami salmeterolu a flutikason-propionátu, který obsahuje nižší dávku inhalačního kortikosteroidu.
Pacienti by měli dostat sílu inhalátoru obsahujícího salmeterol/flutikason-propionát, která obsahuje dávku flutikason-propionátu odpovídající závažnosti jejich onemocnění. Přípravek Airexar Spiromax je vhodný pouze pro léčbu pacientů se závažným astmatem. Pokud jednotlivý pacient vyžaduje dávkování mimo doporučený režim, měly by být předepsány příslušné dávky p2 agonisty a/nebo kortikosteroidu.
Doporučené dávky:
Dospělí ve věku od 18 let.
Jedna inhalace 50 mikrogramů salmeterolu a 500 mikrogramů flutikason-propionátu dvakrát denně.
Jakmile je dosaženo kontroly astmatu, je nutno léčbu přezkoumat a zvážit, zda nemá být dávka snížena a zda nemají být pacienti převedeni na alternativní kombinovaný přípravek s fixními dávkami salmeterolu a flutikason-propionátu obsahující nižší dávku inhalačního kortikosteroidu a nakonec na inhalační kortikosteroid samotný. Při snižování dávky jsou důležité pravidelné kontroly pacientů.
Při porovnání s inhalačním flutikason-propionátem samotným použitým jako zahajovací udržovací léčba nebyl jasně prokázán přínos, když chybělo jedno nebo dvě z kritérií závažnosti. Obecně zůstávají inhalační kortikosteroidy u většiny pacientů léčbou první linie.
Airexar Spiromax jen určen pouze k léčbě pacientů se závažným astmatem. Neměl by se používat k léčbě pacientů s lehkým nebo středně závažným astmatem ani k zahájení léčby u pacientů se závažným astmatem, pokud nebyla již dříve zjištěna potřeba vysoké dávky kortikosteroidů spolu s dlouhodobě působícím P2 agonistou.
Airexar Spiromax není určen k léčbě astmatu, pokud má být kombinovaný přípravek s fixními dávkami salmeterolu a flutikason-propionátu použit poprvé. Pacienti by měli zahájit léčbu kombinovaným přípravkem s fixními dávkami obsahujícím nižší dávku kortikosteroidové složky a pak by měla být dávka kortikosteroidu postupně zvyšována, dokud nebude dosaženo kontroly astmatu. Po dosažení kontroly astmatu by pacienti měli být pravidelně kontrolováni a dávka inhalačního kortikosteroidu by měla být snižována, jak je zapotřebí ke kontrole onemocnění.
U pacientů se závažným astmatem se doporučuje, aby bylo vhodné dávkování inhalačního kortikosteroidu stanoveno dříve, než bude moci být použita jakákoliv léčba s fixními kombinovanými dávkami.
Pediatrická populace
Použití přípravku Airexar Spiromax se nedoporučuje u dětí ve věku do 12 let ani u dospívajících ve věku od 13 do 17 let. Bezpečnost a účinnost přípravku Airexar Spiromax nebyly u dětí a dospívajících ve věku do 18 let stanoveny.
Nejsou dostupné žádné údaje.
CHOPN
Jedna inhalace 50 mikrogramů salmeterolu a 500 mikrogramů flutikason-propionátu dvakrát denně.
Zvláštní skupiny _pacientů
U starších pacientů ani u pacientů s poruchou funkce ledvin není nutná úprava dávkování.
U pacientů s poruchou funkce jater nejsou dostupné žádné údaje o použití přípravku Airexar Spiromax. Způsob podání/Návod k použití
Inhalátor Spiromax je aktivován nádechem, tj. léčivé látky se dostávají do dýchacích cest spolu se vdechovaným vzduchem, j akmile se pacient nadechne přes náustek inhalátoru. Bylo prokázáno, že pacienti se závažným astmatem jsou schopni vytvořit dostatečný inspirační průtok pro Spiromax k dodání terapeutické dávky (viz bod 5.1).
Požadovaný nácvik
Aby bylo dosaženo účinné léčby, musí se Airexar Spiromax používat správně. Proto by se mělo pacientům doporučit, aby si pozorně přečetli příbalovou informaci pro pacienty a řídili se návodem k použití, který je podrobně uvedený v příbalové informaci. Všem pacientům musí předepisující zdravotnický pracovník zajistit instruktáž, jak Airexar Spiromax používat. Jejím účelem je zajistit, aby pacienti pochopili, jak správně inhalátor používat, a aby pochopili, že se musí při inhalaci usilovně nadechnout, aby bylo zajištěno podání správné dávky. Je důležité inhalovat správně, aby bylo zajištěno optimální dávkování.
Použití přípravku Airexar Spiromax spočívá ve třech jednoduchých krocích: otevření, nádech a uzavření, jak je uvedeno níže.
Otevření: Spiromax držte s krytem náustku směrem dolů. Kryt náustku otevřete sklopením dolů; až bude náustek úplně otevřený, bude slyšitelné jedno klapnutí.
Nádech: Pomalu vydechněte (jak to bude pohodlné). Nedýchejte inhalátorem. Náustek vložte mezi zuby se rty uzavřenými kolem náustku; nekousejte náustek inhalátoru. Usilovně se zhluboka nadechněte náustkem. Vyjměte Spiromax z úst a zadržte dech na dobu 10 sekund, nebo tak dlouho, jak je to pohodlné.
Uzavření: Pomalu vydechněte a zavřete kryt náustku.
Pacienti nesmějí nikdy blokovat otvory pro vzduch, ani nesmějí vydechovat přes inhalátor Spiromax, když se připravují na krok „Nádech“. Pacienti nemusí před použitím inhalátor protřepávat.
Pacientům, je nutno také doporučit, aby si po inhalaci vypláchli ústa vodou a vodu vyplivli, a/nebo aby si po inhalaci vyčistili zuby (viz bod 4.4)
Pacienti při použití přípravku Airexar Spiromax mohou pocítit určitou příchuť způsobenou pomocnou látkou laktózou.
4.3 Kontraindikace
Hypersenzitivita na léčivou látku(y) nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Airexar Spiromax je určen k použití pouze u pacientů se závažným astmatem. Neměl by se používat k léčbě akutních příznaků astmatu, u kterých je vhodný rychle a krátkodobě působící bronchodilatátor. Pacientům je nutno doporučit, aby u sebe měli neustále inhalátor, který lze použít k úlevě u akutního astmatického záchvatu.
Pacienti by neměli zahajovat léčbu přípravkem Airexar Spiromax během exacerbace, ani pokud u nich došlo k významnému nebo akutnímu zhoršení astmatu.
Během léčby přípravkem Airexar Spiromax se mohou vyskytnout závažné nežádoucí účinky související s astmatem a exacerbace. Pacienty je nutno požádat, aby pokračovali v léčbě, ale pokud budou příznaky astmatu po zahájení léčby přípravkem Airexar Spiromax nekontrolované nebo se zhorší, aby vyhledali lékařskou pomoc.
Zvýšená potřeba úlevových léků (krátkodobě působících bronchodilatátorů) nebo snížená odpověď na úlevové léky ukazují na zhoršení kontroly astmatu a pacienty by měl prohlédnout lékař.
Náhlé a progresivní zhoršení kontroly astmatu je potenciálně život ohrožující a pacient by měl být urgentně vyšetřen lékařem. Je nutno zvážit zvýšení dávky kortikosteroidů.
Jakmile budou příznaky astmatu kontrolovány, lze zvážit postupné snižování dávky inhalačních kortikosteroidů a tedy převedení na alternativní kombinovaný přípravek s fixními dávkami salmeterolu a flutikason-propionátu s nižším obsahem inhalačního kortikosteroidu. Při snižování dávky jsou důležité pravidelné kontroly pacientů. Je nutno použít co nejnižší dávku inhalačního kortikosteroidu.
CHOPN
Léčba systémovými kortikosteroidy je obvykle indikována u pacientů s CHOPN, u kterých dochází k exacerbacím, a proto je pacienty nutno poučit, že pokud se příznaky při léčbě přípravkem Airexar Spiromax zhorší, mají vyhledat lékařské ošetření.
Ukončení léčby
Léčba přípravkem Airexar Spiromax by neměla být u pacientů s astmatem ukončena náhle vzhledem k riziku exacerbace. Léčbu je nutno vysazovat postupně za dohledu lékaře. U pacientů s CHOPN může být ukončení léčby také spojeno se symptomatickou dekompenzací; pacienti by měli být sledováni lékařem.
Opatrnost u určitých onemocnění
Airexar Spiromax by měl být podáván s opatrností u pacientů s aktivní tuberkulózou nebo s tuberkulózou v klidovém stadiu a u plísňových, virových či jiných infekcí dýchacích cest. V případě indikace je nutno okamžitě zahájit příslušnou léčbu.
Vzácně může Airexar Spiromax při vysokých terapeutických dávkách způsobit srdeční arytmii, např. supraventrikulární tachykardii, extrasystoly a fibrilaci síní, a mírné přechodné snížení draslíku v séru.
Airexar Spiromax je nutno používat opatrně u pacientů se závažnými kardiovaskulárními poruchami či abnormalitami srdečního rytmu a u pacientů s diabetes mellitus, thyreotoxikózou, nekorigovanou hypokalémií nebo u pacientů s predispozicí k nízkým hladinám draslíku.
Velmi vzácně bylo hlášeno zvýšení glykémie (viz bod 4.8); to je nutno zvážit při léčbě pacientů s diabetes mellitus v anamnéze.
Paradoxní bronchospasmus
Po aplikaci dávky může dojít k paradoxnímu bronchospasmu s bezprostředním zhoršením pískotů (hvízdavé dýchaní) a dušnosti. Paradoxní bronchospasmus odpovídá na rychle působící bronchodilatátory; měl by být okamžitě léčen. Je nutno okamžitě vysadit Airexar Spiromax, pacienta vyšetřit a v případě potřeby nasadit alternativní léčbu.
Agonisté P2 adrenergních receptorů
Byly hlášeny farmakologické účinky léčby p2 agonisty, jako je např. třes, palpitace a bolest hlavy, ale ty jsou obvykle přechodné a zmírňují se po pravidelné léčbě.
Systémové účinky
Systémové účinky se mohou vyskytnout u všech inhalačních kortikosteroidů, zejména při vysokých dávkách podávaných po delší dobu. Výskyt těchto účinků je mnohem méně pravděpodobný než u perorálních kortikosteroidů. K možným systémovým účinkům patří Cushingův syndrom, cushingoidní rysy, suprese nadledvin, snížení kostní minerální denzity, katarakta a glaukom a vzácněji řada psychologických poruch nebo poruch chování včetně psychomotorické hyperaktivity, poruch spánku, úzkosti, deprese nebo agresivita (zejména u dětí) (informace o systémových účincích inhalačních kortikosteroidů u dětí a dospívajících viz podtitul Pediatrická populace níže). Je proto důležité, aby byli pacienti pravidelně kontrolováni a aby byla dávka inhalačních kortikosteroidů snížena na nejnižší dávku, při které je astma účinně kontrolováno.
Funkce nadledvin
Déletrvající léčba pacientů vysokými dávkami inhalačních kortikosteroidů může vést k supresi nadledvin a k akutní adrenální krizi. U dávek flutikason-propionátu od 500 do méně než 1 000 mikrogramů byly také popsány velmi vzácné případy suprese nadledvin a akutní adrenální krize. Mezi situace, které by mohly potenciálně spustit akutní adrenální krizi, patří trauma, chirurgický výkon, infekce či jakékoli rychlé snížení dávky. Příznaky, kterými se projevuje, jsou obvykle neurčité a mohou zahrnovat anorexii, bolest břicha, úbytek hmotnosti, únavnost, bolest hlavy, nauzeu, zvracení, hypotenzi, sníženou úroveň vědomí, hypoglykémii a křeče. V obdobích stresové zátěže nebo s elektivním chirurgickým výkonem je nutno zvážit použití dalších systémových kortikosteroidů.
Příznivé účinky inhalační léčby flutikason-propionátem by měly minimalizovat potřebu perorálních steroidů, ale u pacientů převáděných z perorálních steroidů může existovat po značnou dobu riziko snížené adrenální rezervy. Tito pacienti by proto měli být léčeni se zvláštní opatrností a měla by u nich být pravidelně monitorována adrenokortikální funkce. Riziko může být také u pacientů, u kterých byla v minulosti nutná léčba akutních stavů vysokými dávkami kortikosteroidů. Na tuto možnost reziduální poruchy je nutno myslet vždy v akutních situacích a při elektivních výkonech, u kterých je pravděpodobnost vzniku stresu, a je zde nutno zvážit vhodnou léčbu kortikosteroidy. Rozsah poruchy nadledvin může vyžadovat před elektivními výkony radu specialisty.
Interakce s jinými léčivými přípravky
Ritonavir může významně zvyšovat koncentraci flutikason-propionátu v plazmě. Proto je nutno vyhnout se souběžnému použití, ledaže by potenciální benefit pro pacienta převážil riziko nežádoucích účinků léčby systémovými kortikosteroidy. Zvýšené riziko systémových nežádoucích účinků je rovněž při kombinaci flutikason-propionátu s jinými silnými inhibitory CYP3A (viz bod 4.5).
Souběžné podávání systémového ketokonazolu významně zvyšuje systémovou expozici salmeterolu. To může vést ke zvýšení incidence systémových účinků (např. prodloužení intervalu QTc a palpitací). Souběžné léčbě ketokonazolem nebo jinými silnými inhibitory CYP3A4 je proto nutné se vyhnout, ledaže by prospěch převážil potenciálně zvýšené riziko systémových nežádoucích účinků léčby salmeterolem (viz bod 4.5).
Infekce dýchacího traktu
Ve studii TORCH s pacienty s CHOPN léčenými salmeterolem/flutikason-propionátem 50/500 mikrogramů dvakrát denně a také ve studiích SCO40043 a SCO100250 porovnávajících nižší dávku salmeterolu/flutikason-propionátu 50/250 mikrogramů dvakrát denně neschválenou pro CHOPN se samotným salmeterolem 50 mikrogramů dvakrát denně (viz bod 4.8 a bod 5.1) byl v porovnání s placebem zvýšený počet hlášení infekcí dolních dýchacích cest (zejména pneumonie a bronchitidy). Ve skupině se salmeterolem/flutikason-propionátem byla podobná incidence pneumonie pozorována ve všech studiích. Ve studii TORCH měli nejvyšší riziko rozvoje pneumonie starší pacienti, pacienti s nižším body mass indexem (<25 kg/m2) a pacienti s velmi závažným onemocněním (FEVi<30 % předpokládané hodnoty), bez ohledu na léčbu.
Lékaři musí být u pacientů s CHOPN opatrní a hledat známky možného rozvoje pneumonie a jiných infekcí dolních cest dýchacích, protože klinické rysy těchto infekcí a exacerbace se často překrývají. Pokud pacient se závažnou CHOPN dostane pneumonii, je nutno léčbu přípravkem Airexar Spiromax znovu zvážit.
Pneumonie u pacientů s CHOPN
U pacientů léčených inhalačními kortikosteroidy byla pozorována zvýšená incidence pneumonií včetně pneumonií vyžadujících hospitalizaci. Existuje určitý průkaz zvýšeného rizika pneumonie se zvyšující se dávkou steroidů, ale to nebylo přesvědčivě prokázáno ve všech studiích.
Neexistuje přesvědčivý klinický průkaz rozdílů ve velikosti rizika pneumonie uvnitř jednotlivých tříd inhalačních kortikosteroidních přípravků.
Lékaři by měli být opatrní s ohledem na možný vývoj pneumonie u pacientů s CHOPN, jelikož klinické známky, jako jsou infekce, zakryjí příznaky exacerbace CHOPN. Pokud má pacient se závažnou CHOPN pneumonii, měla by být léčba přípravkem Airexar Spiromax přehodnocena.
Mezi rizikové faktory pneumonie patří u pacientů s CHOPN kouření v současné době, starší věk, nízký body mass index (BMI) a závažná CHOPN.
Etnické populace
Údaje z velké klinické studie (SMART, SalmeterolMulti-Center Asthma Research Trial) ukazují, že afroameričtí pacienti léčení salmeterolem měli v porovnání s placebem vyšší riziko závažných příhod souvisejících s dýchacím traktem nebo úmrtí (viz bod 5.1). Není známo, zda to bylo v důsledku farmakogenetických či jiných faktorů. Pacientům s africkými nebo afro-karibskými předky by proto mělo být doporučeno, aby pokračovali v léčbě, ale aby vyhledali lékařskou pomoc, pokud by během léčby přípravkem Airexar Spiromax byly příznaky astmatu nekontrolované nebo se zhoršily.
Pediatrická populace
Airexar Spiromax není indikován k léčbě dětí a dospívajících ve věku do 18 let (viz bod 4.2). Je nutno si však povšimnout, že zvláštní riziko může být u dětí a dospívajících ve věku do 16 let léčených vysokými dávkami flutikason-propionátu (obvykle >1 000 mikrogramů/den). Mohou se vyskytnout systémové účinky, zejména u vysokých dávek podávaných po delší dobu. Mezi možné systémové účinky u dětí a dospívajících patří Cushingův syndrom, cushingoidní rysy, suprese nadledvin, akutní adrenální krize a růstová retardace, a vzácněji řada psychologických poruch nebo poruch chování včetně psychomotorické hyperaktivity, poruch spánku, úzkosti, deprese nebo agresivita. Je nutno zvážit doporučení dítěte nebo dospívajícího k pediatrovi specializovanému na respirační onemocnění. U dítěte léčeného dlouhodobě inhalačními kortikosteroidy se doporučuje pravidelné sledování výšky. Dávku inhalačních kortikosteroidů je vždy nutno snížit na nejnižší dávku, při které je astma účinně kontrolováno.
Infekce dutiny ústní
Vzhledem k obsahu flutikason-propionátu se u některých pacientů může vyskytnout chrapot a kandidóza dutiny ústní a hrdla (moučnivka) a vzácně jícnu. Chrapot i incidenci kandidózy dutiny ústní a hrdla lze zmírnit vypláchnutím úst vodou, vyplivnutím vody a/nebo vyčištěním zubů po použití léčivého přípravku. Symptomatickou kandidózu dutiny ústní a hrdla lze léčit topickými antimykotiky a přitom pokračovat v léčbě přípravkem Airexar Spiromax.
Pomocné látky
Tento léčivý přípravek obsahuje laktózu. Pacienti se vzácnými dědičnými problémy s intolerancí galaktózy, hereditárním deficitem laktázy nebo malabsorpcí glukózy a galaktózy by tento přípravek neměli užívat. Pomocná látka laktóza může obsahovat malé množství mléčných bílkovin, které mohou způsobit alergické reakce u pacientů se závažnou hypersenzitivitou nebo alergií na mléčné bílkoviny.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Beta adrenergní blokátory mohou oslabit účinek salmeterolu nebo působit proti němu. Je nutno vyhnout se jak neselektivním, tak selektivním p-blokátorům, pokud nejsou důvody pro jejich použití závažné. Léčba p2-agonisty může mít za následek potenciálně závažnou hypokalémii. Zvláštní opatrnost se doporučuje při akutním závažném astmatu, protože tento účinek může být potencován souběžnou léčbou deriváty xanthinu, steroidy a diuretiky.
Souběžná léčba léčivými přípravky obsahujícími jiné p-adrenergní látky může mít potenciálně aditivní účinek.
Flutikason-propionát
Za běžných okolností se po inhalačním podání dosahuje nízkých koncentrací flutikason-propionátu vzhledem k efektu prvního průchodu a vysoké systémové clearance zprostředkované cytochromem P450 3A4 ve střevě a játrech. Proto jsou klinicky významné lékové interakce způsobené flutikason-propionátem nepravděpodobné.
Ve studii lékových interakcí u zdravých subjektů s intranazálním flutikason-propionátem zvýšil ritonavir (velmi silný inhibitor cytochromu P450 3A4) v dávce 100 mg dvakrát denně plazmatickou koncentraci flutikason-propionátu o několik set procent, což mělo za následek významně snížené koncentrace kortisolu v séru. Informace o této interakci u inhalovaného flutikason-propionátu chybí, ale předpokládá se významné zvýšení plazmatických hladin flutikason-propionátu. Byly hlášeny případy Cushingova syndromu a adrenální suprese. Této kombinaci je nutno se vyhnout, pokud přínos nepřeváží zvýšené riziko nežádoucích účinků systémových glukokortikoidů.
V malé studii se zdravými dobrovolníky zvýšil poněkud méně silný inhibitor CYP3A, ketokonazol, expozici flutikason-propionátu po jediné inhalaci o 150 %. To mělo v porovnání s flutikason-propionátem samotným za následek větší snížení plazmatického kortisolu. Předpokládá se také, že souběžná léčba jinými silnými inhibitory CYP3A, jako je např. itrakonazol, a středně silnými inhibitory CYP3A, jako je např. erythromycin, zvýší systémovou expozici flutikason-propionátu a riziko systémových nežádoucích účinků. Doporučuje se opatrnost a dlouhodobé léčbě takovými léky je nutno se vyhnout, je-li to možné.
Salmeterol
Silné inhibitory CYP3A4
Souběžné podávání ketokonazolu (400 mg perorálně jednou denně) a salmeterolu (50 mikrogramů inhalačně dvakrát denně) u 15 zdravých subjektů po dobu 7 dnů vedlo k významnému zvýšení plazmatické expozice salmeterolu (1,4násobně u Cmax a 15násobně u AUC). To může vést v porovnání se samostatnou léčbou salmeterolem nebo ketokonazolem ke zvýšení incidence jiných systémových účinků léčby salmeterolem (např. prodloužení intervalu QTc a palpitací) (viz bod 4.4).
Nebyly pozorovány žádné klinicky významné účinky na krevní tlak, srdeční frekvenci, hladinu glukózy v krvi a draslíku v krvi. Souběžné podávání s ketokonazolem nezvýšilo eliminační poločas salmeterolu, ani nezvýšilo akumulaci salmeterolu při opakovaném podání.
Je třeba se vyhnout současnému podávání ketokonazolu, pokud přínos nepřeváží potenciálně zvýšené riziko systémových nežádoucích účinků léčby salmeterolem. Je pravděpodobné, že existuje podobné riziko interakce s jinými silnými inhibitory CYP3A4 (např. itrakonazolem, telithromycinem, ritonavirem).
Středně silné inhibitory CYP 3A4
Souběžné podávání erythromycinu (500 mg perorálně třikrát denně) a salmeterolu (50 mikrogramů inhalačně dvakrát denně) u 15 zdravých jedinců po dobu 6 dnů vedlo k malému, ale staticky nevýznamnému zvýšení expozice salmeterolu (1,4násobně u Cmx a 1,2násobně u AUC). Souběžné podávání s erythromycinem nebylo spojeno s žádnými závažnými nežádoucími účinky.
4.6 Fertilita, těhotenství a kojení
Údaje získané ze středně velkého souboru těhotných žen (mezi 300-1 000 ukončených těhotenství) nenaznačují žádné malformační účinky nebo fetální/neonatální toxicitu u salmeterolu a flutikason-propionátu. Studie na zvířatech prokázaly reprodukční toxicitu po podání agonistů p2-adrenergních receptorů a glukokortikosteroidů (viz bod 5.3).
Podání přípravku Airexar Spiromax těhotným ženám je třeba zvážit pouze v případě, že očekávaný přínos pro matku je větší než jakékoli možné riziko pro plod.
Při léčbě těhotných žen by měla být použita nejnižší účinná dávka flutikason-propionátu potřebná k udržení dostatečné kontroly astmatu.
Kojení
Není známo, zda se salmeterol a flutikason-propionát nebo jejich metabolity vylučují do lidského mateřského mléka.
Ve studiích bylo prokázáno, že se salmeterol a flutikason-propionát a jejich metabolity vylučují do mléka kojících samic potkanů.
Riziko pro kojené novorozence/kojence nelze vyloučit. Na základě posouzení prospěšnosti kojení pro dítě a prospěšnosti léčby pro matku je nutno rozhodnout, zda přerušit kojení nebo ukončit/přerušit léčbu přípravkem Airexar Spiromax.
Fertilita
U lidí nejsou dostupné žádné údaje. Ve studiích na zvířatech však nebyly prokázány žádné účinky salmeterolu či flutikason-propionátu na fertilitu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Airexar Spiromax nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
4.8 Nežádoucí účinky Souhrn bezpečnostního profilu
Vzhledem k tomu, že přípravek Airexar Spiromax obsahuje salmeterol a flutikason-propionát, lze očekávat typ a závažnost nežádoucích účinků související s každou z těchto dvou léčivých látek. Při souběžném podání obou léčivých látek nedochází k výskytu dalších nežádoucích účinků.
Nežádoucí účinky, které souvisejí se salmeterolem/flutikason-propionátem, jsou uvedeny níže podle tříd orgánových systémů a frekvence výskytu. Frekvence výskytu je definována takto: velmi časté (> 1/10), časté (>1/100 až <1/10), méně časté (>1/1 000 až <1/100), vzácné (>1/10 000 až <1/1 000) a není známo (frekvenci z dostupných údajů nelze určit). Frekvence byly odvozeny z údajů z klinických studií. Incidence u placeba nebyla brána v úvahu.
|
Třída orgánových systémů |
Nežádoucí účinky |
Frekvence |
|
Infekce a infestace |
Kandidóza dutiny ústní a hrdla |
Časté |
|
Pneumonie (u pacientů s CHOPN) |
Časté1,3,5 | |
|
Bronchitis |
Časté1,3 | |
|
Kandidóza jícnu |
Vzácné | |
|
Poruchy imunitního systému |
Hypersenzitivní reakce s následujícími manifestacemi: |
|
Třída orgánových systémů |
Nežádoucí účinky |
Frekvence |
|
Kožní hypersenzitivní reakce |
Méně časté | |
|
Angioedém (hlavně edém obličeje a orofaryngeální edém) |
Vzácné | |
|
Respirační příznaky (dušnost) |
Méně časté | |
|
Respirační příznaky (bronchospasmus) |
Vzácné | |
|
Anafylaktické reakce včetně anafylaktického šoku |
Vzácné | |
|
Endokrinní poruchy |
Cushingův syndrom, cushingoidní rysy, suprese nadledvin, růstová retardace u dětí a dospívajících, snížená kostní minerální denzita |
Vzácné4 |
|
Poruchy metabolismu |
Hypokalémie |
Časté3 |
|
a výživy |
Hyperglykémie |
Méně časté4 |
|
Psychiatrické poruchy |
Úzkost |
Méně časté |
|
Poruchy spánku |
Méně časté | |
|
Změny chování včetně psychomotorické hyperaktivity a podrážděnosti (převážně u dětí) |
Vzácné | |
|
Deprese, agresivita (převážně u dětí) |
Není známo | |
|
Poruchy nervového |
Velmi časté1 | |
|
systému |
Méně časté | |
|
Poruchy oka |
Katarakta |
Méně časté |
|
Glaukom |
Vzácné4 | |
|
Srdeční poruchy |
Palpitace |
Méně časté |
|
Méně časté | ||
|
Srdeční arytmie (včetně supraventrikulární tachykardie a extrasystol) |
Vzácné | |
|
Fibrilace síní |
Méně časté | |
|
Angina pectoris |
Méně časté | |
|
Respirační, hrudní a mediastinální |
Nasofaryngitis |
Velmi časté2,3 |
|
poruchy |
Podráždění hrdla |
Časté |
|
Chrapot/dysfonie |
Časté |
1. Často hlášené u placeba
|
Třída orgánových systémů |
Nežádoucí účinky |
Frekvence |
|
Sinusitis |
Časté1,3 | |
|
Paradoxní bronchospasmus |
Vzácné4 | |
|
Poruchy kůže a |
Kontuze |
Časté1,3 |
|
podkožní tkáně | ||
|
Poruchy svalové a |
Svalové křeče |
Časté |
|
kosterní soustavy a |
Časté1,3 | |
|
pojivové tkáně |
Traumatické zlomeniny | |
|
Artralgie |
Časté | |
|
Myalgie |
Časté |
2. Velmi často hlášené u placeba
3. Hlášené v průběhu 3 let ve studii s pacienty s CHOPN
4. Viz bod 4.4
5. Viz bod 5.1.
Popis vybraných nežádoucích účinků
Při léčbě p2 agonisty byly hlášeny farmakologické účinky jako je třes, palpitace a bolesti hlavy, ale obvykle byly přechodné a zmírňovaly se po pravidelné léčbě.
Může se vyskytnout paradoxní bronchospasmus s okamžitým zhoršením pískotů (hvízdavé dýchaní) a dušnosti po podání. Paradoxní bronchospasmus odpovídá na rychle působící bronchodilatátory a měl by být okamžitě léčen. Je nutno okamžitě vysadit Airexar Spiromax, vyšetřit pacienta a v případě potřeby zahájit alternativní léčbu.
Vzhledem k obsahu flutikason-propionátu se u některých pacientů může vyskytnout chrapot a kandidóza dutiny ústní a hrdla (moučnivka) a vzácně jícnu. Chrapot i incidenci kandidózy dutiny ústní a hrdla lze zmírnit vypláchnutím úst vodou, vyplivnutím vody a/nebo vyčištěním zubů po použití léčivého přípravku. Symptomatickou kandidózu dutiny ústní a hrdla lze léčit topickými antimykotiky a přitom pokračovat v léčbě přípravkem Airexar Spiromax.
Pediatrická populace
Airexar Spiromax není indikován k léčbě dětí a dospívajících ve věku do 18 let (viz bod 4.2). Mezi možné systémové účinky u této věkové skupiny patří Cushingův syndrom, cushingoidní rysy, suprese nadledvin a růstová retardace (viz bod 4.4). U dětí se může vyskytnout také úzkost, poruchy spánku a změny chování včetně hyperaktivity a podrážděnosti.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V.
4.9 Předávkování
Z klinických studií nejsou k dispozici žádné údaje o předávkování přípravkem Airexar Spiromax, níže jsou však uvedeny údaje o předávkování oběma léčivými látkami:
Salmeterol
Příznaky předávkování salmeterolem jsou závratě, zvýšení systolického krevního tlaku, třes, bolest hlavy a tachykardie. Pokud musí být léčba přípravkem Airexar Spiromax vysazena kvůli předávkování beta-agonistické složky tohoto léčivého přípravku, je třeba zvážit vhodnou substituční léčbu steroidy. Kromě toho se může vyskytnout i hypokalémie, proto je nutné monitorovat sérové hladiny draslíku. Je nutno zvážit substituci draslíku.
Flutikason-propionát
Akutní: Akutní inhalace vyšších než doporučených dávek flutikason-propionátu může vést k přechodné supresi funkce nadledvin. To nevyžaduje okamžitý zásah, protože funkce nadledvin se během několika dnů zotaví, což bylo ověřeno měřením plazmatických hladin kortisolu.
Chronické předávkování: Měla by se monitorovat adrenální rezerva a může být nezbytná systémová léčba kortikosteroidy. Po stabilizaci by se mělo pokračovat v léčbě inhalačními kortikosteroidy v doporučené dávce. Viz bod 4.4: „Funkce nadledvin“.
Jak při akutním, tak při chronickém předávkování flutikason-propionátem by se v léčbě přípravkem Airexar Spiromax mělo pokračovat v dávce vhodné ke kontrole příznaků.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Léčivé přípravky k terapii onemocnění spojených s obstrukcí dýchacích cest, adrenergika v kombinaci s kortikosteroidy nebo jinými léčivými přípravky vyjma anticholinergik, ATC kód: R03AK06
Mechanismus účinku a farmakodynamické účinky
Airexar Spiromax obsahuje salmeterol a flutikason-propionát, které mají odlišné mechanismy účinku. Příslušné mechanismy účinku obou léčivých látek jsou pojednány níže.
Salmeterol:
Salmeterol je selektivní dlouhodobě (12 hodin) působící agonista p2 adrenergních receptorů s dlouhým postranním řetězcem, který se váže na zevní místo receptoru.
Salmeterol způsobuje bronchodilataci trvající déle, nejméně po dobu 12 hodin, než doporučené dávky běžných krátkodobě působících p2 agonistů.
Flutikason-propionát:
Flutikason-propionát podávaný inhalačně v doporučených dávkách má glukokortikoidní protizánětlivý účinek v plicích, který vede ke zmírnění příznaků a exacerbací astmatu s menším množstvím nežádoucích účinků než při systémovém podávání kortikosteroidů.
Klinická účinnost a bezpečnost
Studie popsané níže (GOAL, TORCH a SMART) byly provedeny s touto stejnou fixní kombinací, salmeterol-xinafoát a flutikason-propionát, ale hodnotily dříve schválený přípravek; popsané studie nebyly provedeny s přípravkem Airexar Spiromax.
Salmeterol/flutikason-propionát - klinická studie u astmatu
Ve dvanáct měsíců trvající studii (Gaining Optimal Asthma ControL, GOAL) u 3 416 dospělých a dospívajících pacientů s perzistentním astmatem byla porovnávána bezpečnost a účinnost salmeterolu/ flutikason-propionátu se samotným inhalačním kortikosteroidem (flutikason-propionátem) za účelem zjištění, zda byly dosažitelné cíle při léčbě astmatu. Léčba byla stupňována každých 12 týdnů, dokud nebylo dosaženo **úplné kontroly, nebo dokud nebylo dosaženo nejvyšší dávky hodnoceného přípravku. Ve studii GOAL se prokázalo, že kontroly astmatu bylo dosaženo u většího počtu pacientů léčených kombinovaným přípravkem salmeterol/flutikason-propionát než u pacientů léčených samotnými inhalačními kortikosteroidy, a že kontroly bylo dosaženo při nižších dávkách kortikosteroidů.
* Dobré kontroly astmatu bylo dosaženo rychleji u salmeterolu/flutikason-propionátu než u samotného inhalačního kortikosteroidu. U 50 % subjektů byla doba léčby k dosažení prvního jednotlivého týdne s dobrou kontrolou 16 dnů u salmeterolu/flutikason-propionátu v porovnání s 37 dny ve skupině s inhalačním kortikosteroidem. V podskupině astmatiků bez předchozí léčby steroidy byla doba léčby salmeterolem/flutikason-propionátem k dosažení prvního jednotlivého týdne s dobrou kontrolou 16 dnů v porovnání s 23 dny po léčbě inhalačními kortikosteroidy.
Celkové výsledky studie ukázaly:
|
Procentuální podíl pacientů, kteří dosáhli *dobré kontroly (Well Controlled - WC) a **úplné kontroly (Totally Controlled - TC) astmatu během 12 měsíců | ||||
|
Léčba před zahájením studie |
Salmeterol/FP |
FP | ||
|
WC |
TC |
WC |
TC | |
|
Bez inhalačních kortikosteroidů (pouze SABA) |
78 % |
50 % |
70 % |
40 % |
|
Nízká dávka inhalačního kortikosteroidu ( <500 mikrogramů BDP nebo ekvivalentu/den) |
75 % |
44 % |
60 % |
28 % |
|
Střední dávka inhalačního kortikosteroidu (>500 až 1 000 mikrogramů BDP nebo ekvivalentu/den) |
62 % |
29 % |
47 % |
16 % |
|
Souhrnné výsledky ze 3 úrovní léčby |
71 % |
41 % |
59 % |
28 % |
* Dobře kontrolované astma; 2 dny nebo méně s příznakovým skóre vyšším než 1 (příznakové skóre 1 je definováno jako „příznaky po jeden krátký časový úsek během dne“), použití SABA po 2 dny nebo méně a ve 4 případech nebo méně za týden, ranní vrcholová výdechová rychlost 80 % předpokládané hodnoty nebo vyšší, bez nočního probouzení, bez exacerbací a bez nežádoucích účinků vynucujících změnu léčby **Úplná kontrola astmatu; žádné příznaky; bez použití SABA, ranní vrcholová výdechová rychlost 80 % předpokládané hodnoty nebo vyšší, bez nočního probouzení, bez exacerbací a bez nežádoucích účinků vynucujících změnu léčby
Výsledky této studie ukazují, že salmeterol/flutikason-propionát 50/100 mikrogramů dvakrát denně lze zvažovat při zahájení udržovací léčby u pacientů se středně závažným perzistentním astmatem, u kterých je považována za nezbytnou rychlá kontrola astmatu (viz bod 4.2).
Ve dvojitě zaslepené randomizované studii s paralelními skupinami u 318 pacientů s perzistentním astmatem ve věku >18 let byla hodnocena bezpečnost a tolerance salmeterolu/flutikason-propionátu při podávání dvou inhalací (dvojité dávky) dvakrát denně po dobu dvou týdnů. Studie ukázala, že zdvojnásobení inhalací salmeterolu/flutikason-propionátu v obou silách po dobu až 14 dnů mělo v porovnání s jednou inhalací dvakrát denně za následek mírné zvýšení nežádoucích účinků souvisejících s P agonisty (třes - 1 pacient [1 %] oproti 0, palpitace - 6 [3 %] oproti 1 [<1 %], svalové křeče - 6 [3 %] oproti 1 [<1 %]) a podobnou incidenci nežádoucích účinků souvisejících s inhalačními kortikosteroidy (např. kandidóza dutiny ústní - 6 [6 %] oproti 16 [8 %], chrapot - 2 [2 %] oproti 4 [2 %]). Pokud lékař zvažuje zdvojnásobení dávky salmeterolu/flutikason-propionátu u dospělých pacientů vyžadujících přídavnou krátkodobou léčbu (do 14 dnů) inhalačními kortikosteroidy, je třeba vzít v úvahu malé zvýšení nežádoucích účinků souvisejících s P agonisty.
Salmeterol/flutikason-propionát - klinické studie u CHOPN
Studie TORCH byla 3 roky trvající studie hodnotící účinek léčby salmeterolem/flutikason-propionátem prášku k inhalaci 50/500 mikrogramů dvakrát denně, salmeterolem prášku k inhalaci 50 mikrogramů dvakrát denně, flutikason-propionátem (FP) prášku k inhalaci 500 mikrogramů dvakrát denně nebo placebem na úmrtnost ze všech příčin u pacientů s CHOPN. Pacienti s CHOPN s výchozí hodnotou (před podáním bronchodilatátoru) FEVj <60 % předpokládané normální hodnoty byli randomizováni ke dvojitě zaslepené léčbě. Během studie byla pacientům povolena běžná léčba CHOPN s výjimkou jiných inhalačních kortikosteroidů, dlouhodobě působících bronchodilatátorů a dlouhodobé systémové léčby kortikosteroidy. Stav přežívání ve 3 letech byl zjišťován u všech pacientů bez ohledu na vysazení hodnocených přípravků. Primárním cílovým ukazatelem bylo snížení úmrtnosti ze všech příčin ve 3 letech u salmeterolu/flutikason-propionátu oproti placebu.
|
Placebo N = 1 524 |
Salmeterol 50 N = 1 521 |
FP 500 N = 1 534 |
Salmeterol/flutikason-propionát 50/500 N = 1 533 | |
|
Úmrtnost ze všech příčin ve 3 letech | ||||
|
Počet úmrtí (%) |
231 (15,2 %) |
205 (13,5 %) |
246 (16,0 %) |
193 (12,6 %) |
|
Poměr rizik vs placebo (CI) p hodnota |
N/A |
0,879 (0,73, 1,06) 0,180 |
1,060 (0,89, 1,27) 0,525 |
0,825 (0,68, 1,00) 0,052' |
|
Poměr rizik u flutikason- propionátu/salmeterolu 500/50 vs u jednotlivých složek (CI) p hodnota |
N/A |
0,932 (0,77, 1,13) 0,481 |
0,774 (0,64, 0,93) 0,007 |
N/A |
1. p hodnota nižší než hladina významnosti po úpravě pro 2 průběžné analýzy k porovnání primární účinnosti z log-rank analýzy stratifikované podle stavu kuřáctví
U subjektů léčených salmeterolem/flutikason-propionátem byl ve 3 letech v porovnání s placebem zjištěn trend ke zlepšení přežití, nedosahoval však hladiny statistické významnosti p<0,05.
Procentuální podíl pacientů, kteří během 3 let zemřeli z příčin souvisejících s CHOPN, byl 6,0 % u placeba,
6,1 % u salmeterolu, 6,9 % u FP a 4,7 % u salmeterolu/flutikason-propionátu.
Průměrný počet středně závažných až závažných exacerbací za rok byl významně snížen u salmeterolu/flutikason-propionátu (FP) v porovnání s léčbou salmeterolem, FP a placebem (průměrný výskyt byl ve skupině se salmeterolemflutikason-propionátem 0,85 v porovnání s 0,97 ve skupině se salmeterolem, 0,93 ve skupině s FP a 1,13 u placeba). To znamená snížení výskytu středně závažných až závažných exacerbací o 25 % (95% CI: 19 % až 31 %; p<0,001) v porovnání s placebem, o 12 % v porovnání se salmeterolem (95% CI: 5 % až 19 %, p=0,002) a o 9 % v porovnání s FP (95% CI: 1 % až 16 %, p=0,024). Salmeterol a FP významně snižovaly výskyt exacerbací v porovnání s placebem o 15 % (95% CI: 7 % až 22 %; p<0,001), resp. o 18 % (95% CI: 11 % až 24 %; p<0,001).
Kvalita života související se zdravím měřená podle dotazníku St George’s Respirátory Questionnaire (SGRQ) byla v porovnání s placebem zlepšena u všech léčivých látek. Průměrné zlepšení v průběhu tří let bylo u salmeteroluflutikason-propionátu v porovnání s placebem -3,1 jednotek (95% CI: -4,1 ž -2,1; p<0,001), v porovnání se salmeterolem -2,2 jednotek (p<0,001) a v porovnání s FP -1,2 jednotek (p=0,017). Za klinicky relevantní je považován pokles o 4 jednotky.
Odhadovaná pravděpodobnost onemocnění pneumonií hlášené jako nežádoucí účinek v průběhu 3 let byla 12,3 % u placeba, 13,3 % u salmeterolu, 18,3 % u FP a 19,6 % u salmeterolu/flutikason-propionátu (poměr rizik u flutikason-propionátu/salmeterolu oproti placebu: 1,64, 95% CI: 1,33 až 2,01, p<0,001). Nebylo zjištěno zvýšení počtu úmrtí souvisejících s pneumonií; počet úmrtí v průběhu léčby, u kterých byla pneumonie posouzena jako hlavní příčina, byl 7 u placeba, 9 u salmeterolu, 13 u FP a 8 u salmeteroluflutikason-propionátu. Nebyl zjištěn významný rozdíl v pravděpodobnosti zlomenin kostí (5,1 % u placeba, 5,1 % u salmeterolu, 5,4 % u FP a 6,3 % u salmeterolu/flutikason-propionátu; poměr rizik u salmeterolu/flutikason-propionátu oproti placebu byl: 1,22, 95% CI: 0,87 až 1,72, p=0,248).
Placebem kontrolované klinické studie trvající 6 a 12 měsíců prokázaly, že pravidelné podávání salmeterolu/flutikason-propionátu 50/500 mikrogramů zlepšuje plicní funkce a snižuje dušnost a používání úlevových léků.
Studie SCO40043 a SCO100250 byly randomizované dvojitě zaslepené replikační studie s paralelními skupinami porovnávající účinek salmeterolu/flutikason-propionátu 50/250 mikrogramů dvakrát denně (tato dávka není v Evropské unii schválena pro léčbu CHOPN) se salmeterolem 50 mikrogramů dvakrát denně na roční výskyt středně závažných/závažných exacerbací u subjektů s CHOPN s FEVi nižším než 50 % předpokládané hodnoty a s exacerbacemi v anamnéze. Středně závažné/závažné exacerbace byly definovány jako zhoršení příznaků, které vyžaduje léčbu perorálními kortikosteroidy a/nebo antibiotiky nebo hospitalizaci pacientů.
Klinická studie měla 4týdenní přípravnou fázi, během které byly subjekty léčeny nezaslepeným salmeterolem/FP 50/250 za účelem standardizace farmakoterapie CHOPN a stabilizace onemocnění před randomizací k zaslepené léčbě ve studii po dobu 52 týdnů. Subjekty byly randomizovány v poměru 1:1 k salmeterolu/FP 50/250 (celkový počet ITT n=776) nebo k salmeterolu (celkový počet ITT n=778). Před přípravnou fází byla subjektům vysazena předchozí léčba CHOPN vyjma krátkodobě působících bronchodilatátorů. Během léčebné fáze nebylo povoleno souběžné použití inhalačních dlouhodobě působících p2 agonistů a anticholinergik, kombinovaných přípravků salbutamol/ipratropium-bromid, perorálních p2 agonistů a theofylinových přípravků. Perorální kortikosteroidy a antibiotika byly povoleny pro akutní léčbu exacerbací CHOPN se specifikovanými pokyny k použití. V průběhu studií subjekty užívaly salbutamol podle potřeby.
Výsledky obou studií ukázaly, že léčba salmeterolem/flutikason-propionátem 50/250 vedla k významně nižšímu ročnímu výskytu středně závažných/závažných exacerbací CHOPN v porovnání se salmeterolem (SCO40043: 1,06 resp. 1,53 na subjekt a rok, míra výskytu 0,70, 95% CI: 0,58 až 0,83, p<0,001;
SCO100250: 1,10 resp. 1,59 na subjekt a rok, míra výskytu 0,70, 95% CI: 0,58 až 0,83, p<0,001). Výsledky sekundárních ukazatelů účinnosti (doba do první středně závažné/závažné exacerbace, roční výskyt exacerbací vyžadujících perorální kortikosteroidy a ranní FEV1 před podáním dávky) významně favorizovaly salmeterol/flutikason-propionát 50/250 mikrogramů dvakrát denně před salmeterolem. Profily nežádoucích účinků byly podobné s výjimkou vyšší incidence pneumonií a známých lokálních nežádoucích účinků (kandidózy a dysfonie) ve skupině se salmeterolem/flutikason-propionátem 50/250 mikrogramů dvakrát denně v porovnání se salmeterolem. Příhody související s pneumonií byly hlášeny u 55 (7 %) subjektů ve skupině se salmeterolem/flutikason-propionátem 50/250 mikrogramů dvakrát denně a u 25 (3 %) ve skupině se salmeterolem. Zdá se, že zvýšená incidence hlášených pneumonií u salmeterolu/flutikason-propionátu 50/250 mikrogramů dvakrát denně je v podobném rozsahu jako incidence hlášená po léčbě salmeterolem/flutikason-propionátem 50/500 mikrogramů dvakrát denně ve studii TORCH.
Studie SMART (Salmeterol Multi-center Asthma Research Trial)
SMART byla multicentrická randomizovaná dvojitě zaslepená a placebem kontrolovaná 28 týdnů trvající studie s paralelními skupinami prováděná v USA, ve které bylo randomizováno 13 176 pacientů k léčbě salmeterolem (50 mikrogramů dvakrát denně) a 13 179 pacientů k placebu, přičemž oba tyto přípravky byly přidány k obvyklé léčbě astmatu. Pacienti byli zařazeni do studie, pokud byli ve věku >12 let, měli astma a byli aktuálně léčeni antiastmatiky (nikoli však LABA). Při vstupu do studie bylo výchozí používání inhalačních kortikosteroidů zaznamenáno, ale ve studii nebylo vyžadováno. Primárním cílovým ukazatelem ve studii SMART byl kombinovaný počet úmrtí souvisejících s respiračním onemocněním a život ohrožujících příhod souvisejících s respiračním onemocněním.
Hlavní výsledky studie SMART: primární cílový ukazatel
|
Skupina pacientů |
Počet příhod primárního cílového ukazatele/počet pacientů |
Relativní riziko (95% interval spolehlivosti) | |
|
salmeterol |
placebo | ||
|
Všichni pacienti |
50/13 176 |
36/13 179 |
1,40 (0,91, 2,14) |
|
Pacienti používající inhalační steroidy |
23/6 127 |
19/6 138 |
1,21 (0,66, 2,23) |
|
Pacienti nepoužívající inhalační steroidy |
27/7 049 |
17/7 041 |
1,60 (0,87, 2,93) |
|
Afro-američtí pacienti |
20/2 366 |
5/2 319 |
4,10 (1/54, 10,90) |
(Riziko tučným písmem je statisticky významné na 95% hladině.)
Hlavní výsledky studie SMART u používání inhalačních steroidů ve výchozím stavu: sekundární cílové ukazatele
|
Počet příhod sekundárního cílového ukazatele/počet pacientů |
Relativní riziko (95% interval spolehlivosti) | ||
|
salmeterol |
placebo | ||
|
Úmrtí související s respiračním onemocněním | |||
|
Pacienti používající inhalační steroidy |
10/6 127 |
5/6 138 |
2.01 (0,69, 5,86) |
|
Pacienti nepoužívající inhalační steroidy |
14/7 049 |
6/7 041 |
2.28 (0,88, 5,94) |
|
Kombinovaná úmrtí související s astmatem a život ohrožující příhody související s astmatem | |||
|
Pacienti používající inhalační steroidy |
16/6 127 |
13/6 138 |
1,24 (0,60, 2,58) |
|
Pacienti nepoužívající inhalační steroidy |
21/7 049 |
9/7 041 |
2,39 (1,10, 5,22) |
|
Úmrtí související s astmatem | |||
|
Pacienti používající inhalační steroidy |
4/6 127 |
3/6 138 |
1,35 (0,30, 6,04) |
|
Pacienti nepoužívající inhalační steroidy |
9/7 049 |
0/7 041 |
* |
|
(*=nebylo možné vypočítat, protože ve skupině s placebem ne |
byly žádné příhody. Tučně vyznačené hodnoty | ||
rizika jsou statisticky významné na 95% hladině. Sekundární cílové ukazatele ve výše uvedené tabulce dosáhly statistické významnosti v celé populaci.) Sekundární cílové ukazatele kombinovaných úmrtí ze všech příčin a život ohrožujících příhod a hospitalizací ze všech příčin nedosáhly v celé populaci statistické významnosti.
Vrcholová inspirační průtoková rychlost u inhalátoru Spiromax
Randomizovaná otevřená studie se zkříženým uspořádáním byla provedena u dětí a dospívajících s astmatem (ve věku 4-17 let), dospělých s astmatem (ve věku 18-45 let), dospělých s chronickou obstrukční plicní nemocí (CHOPN) (ve věku nad 55 let) a u zdravých dobrovolníků (ve věku 18-45 let) k vyhodnocení vrcholové inspirační průtokové rychlosti (PIFR) a dalších souvisejících inhalačních parametrů po inhalaci z inhalátoru Spiromax (obsahujícího placebo) v porovnání s inhalací z vícedávkového inhalátoru se suchým práškem již uvedeného na trh (obsahujícího placebo). U těchto skupin byl zhodnocen vliv optimálního nácviku (tj. usilovného nádechu při inhalaci) inhalační techniky z inhalátoru se suchým práškem na rychlost inhalace a na inhalovaný objem spolu s posouzením potenciálních rozdílů v inhalačním výkonu podle použitých inhalátorů.
Údaje ze studie ukazují, že bez ohledu na věk a základní onemocnění byli děti, dospívající a dospělí s astmatem a také pacienti s CHOPN u prostředku Spiromax schopni dosáhnout inspiračních průtokových rychlostí podobných průtokovým rychlostem u vícedávkového inhalátoru se suchým práškem již uvedeného na trh. Průměrná PIFR dosažená u pacientů s astmatem nebo s CHOPN po optimálním nácviku (tj. nácviku usilovné inhalace) byla vyšší než 60 l/min, tj. než průtoková rychlost, o které je známo, že při ní oba zkoumané prostředky vydávají do plic srovnatelná množství léčivého přípravku.
Všechny subjekty s astmatem nebo s CHOPN dosáhly po optimálním nácviku hodnot PIFR nad 60 l/min. Je důležité inhalovat správně, aby bylo zajištěno optimální dávkování.
Průtoková rychlost vyšší než 60 l/min je potřebná k optimálnímu dodání léčivých přípravků do plic inhalátorem Spiromax vícedávkovým inhalátorem se suchým práškem.
Aby bylo zajištěno, že pacienti dosáhnou PIFR potřebnou k dodání požadované dávky, musí pacient absolvovat nácvik použití inhalátorem Spiromax včetně poučení o nutnosti usilovného nádechu (viz bod 4.2).
Pediatrická populace
Přípravek Airexar Spiromax není doporučen pro použití u dětí a dospívajících do 18 let věku. Bezpečnost a účinnost přípravku Airexar Spiromax u této mladé populace nebyla stanovena. Data uvedená níže se týkají nižší dávky fixní kombinace obsahující dvě léčivé látky, jejichž dávka a síla není u přípravku Airexar Spiromax k dispozici. Popsané studie byly provedeny s dříve schváleným přípravkem, který je k dispozici ve třech různých silách; studie nebyly provedeny s přípravkem Airexar Spiromax.
Ve studii u 158 dětí ve věku 6 až 16 let se symptomatickým astmatem je kombinace flutikason-propionát/salmeterol stejně účinná jako zdvojnásobení dávky flutikason-propionátu s ohledem na kontrolu příznaků a funkci plic. Tato studie nebyla navržena pro hodnocení účinku na exacerbace.
Ve 12týdenní studii u dětí ve věku 4 až 11 let [n=257] léčených buď kombinací salmeterol/flutikason-propionát 50/100 nebo salmeterol 50 mikrogramů + flutikason-propionát 100 mikrogramů dvakrát denně měla obě léčebná ramena 14% zvýšení vrcholové výdechové rychlosti a rovněž zlepšení skóre příznaků a použití záchranného salbutamolu. Nevyskytly se žádné rozdíly mezi léčebnými rameny. Mezi oběma léčebnými rameny nebyly žádné rozdíly v bezpečnostních parametrech.
Ve 12týdenní studii u dětí ve věku 4 až 11 let [n=203] randomizovaných ve studii s paralelními skupinami s perzistentním astmatem, které byly symptomatické při léčbě inhalačním kortikosteroidem, byla primárním cílem bezpečnost. Děti dostávaly buď salmeterol/flutikason-propionát (50/100 mikrogramů) nebo flutikason-propionát (100 mikrogramů) samotný dvakrát denně. Dvě děti na flutikason-propionátu/salmeterolu a 5 dětí na flutikason-propionátu byly vyřazeny z důvodu zhoršení astmatu. Po 12 týdnech nemělo žádné z dětí v žádné léčebné skupině abnormálně nízké 24hodinové vylučování kortisolu v moči. Mezi léčebnými rameny se nevyskytly žádné rozdíly v bezpečnostním profilu.
5.2 Farmakokinetické vlastnosti
Pro farmakokinetické účely lze každou složku zvažovat samostatně.
Salmeterol
Salmeterol působí lokálně v plicích a proto jeho plazmatické hladiny nejsou ukazatelem léčebných účinků. Kromě toho jsou dostupné pouze omezené údaje o farmakokinetice salmeterolu z důvodu technické obtížnosti jeho stanovení v plazmě, protože plazmatické koncentrace dosahované po inhalačním podání terapeutických dávek jsou velmi nízké (přibližně 200 pikogramů/ml nebo méně).
Flutikason-propionát
Absolutní biologická dostupnost jedné dávky inhalačního flutikason-propionátu u zdravých subjektů je v rozmezí přibližně 5 až 11 % nominální dávky v závislosti na použitém inhalačním prostředku. U pacientů s astmatem nebo s CHOPN byl zjištěn nižší stupeň systémové expozice inhalačnímu flutikason-propionátu.
Absorpce
K systémové absorpci dochází hlavně v plicích, je zpočátku rychlá a potom se prodlužuje. Zbytek inhalované dávky flutikason-propionátu může být spolknut, ale jen minimálně přispívá k systémové expozici z důvodu nízké rozpustnosti ve vodě a presystémového metabolizmu, což má při perorálním podání za následek dostupnost nižší než 1 %. Se zvyšující se inhalační dávkou dochází k lineárnímu zvýšení systémové expozice.
Distribuce
Distribuce flutikason-propionátu je charakterizována vysokou plazmatickou clearence (1 150 ml/min), velkým distribučním objemem v rovnovážném stavu (přibližně 300 l) a terminálním poločasem přibližně 8 hodin. Vazba na plazmatické proteiny je 91 %.
Biotransformace
Flutikason-propionát je velmi rychle odstraňován ze systémové cirkulace. Hlavní cestou je metabolizace na neaktivní metabolit, kyselinu karboxylovou, působením enzymu CYP3A4 cytochromu P450. Další neidentifikované metabolity se rovněž nacházejí ve stolici.
Eliminace
Renální clearence flutikason-propionátu je zanedbatelná. Močí se vylučuje méně než 5 % dávky, převážně ve formě metabolitů. Hlavní část dávky se vylučuje stolicí ve formě metabolitů a jako nezměněná látka.
Pediatrická populace
Přípravek Airexar Spiromax není doporučen pro použití u dětí a dospívajících do 18 let věku. Bezpečnost a účinnost přípravku Airexar Spiromax u této mladé populace nebyla stanovena. Data uvedená níže se týkají nižší dávky fixní kombinace obsahující dvě léčivé látky, jejichž dávka a síla není u přípravku Airexar Spiromax k dispozici.
V populační farmakokinetické analýze z 9 kontrolovaných klinických studií u 350 pacientů s astmatem ve věku 4 až 77 let (174 pacientů ve věku 4 až 17 let) byla pozorována vyšší systémová expozice flutikason-propionátu po léčbě kombinací salmeterol/flutikason-propionát prášek k inhalaci 50/100 v porovnání s flutikason-propionátem práškem k inhalaci 100.
5.3 Předklinické údaje vztahující se k bezpečnosti
Jediné obavy týkající se bezpečnosti při použití u člověka pocházejí ze studií na zvířatech, jimž byly salmeterol a flutikason-propionát podávány samostatně, a jsou to účinky spojené s nadměrným farmakologickým působením.
V reprodukčních studiích na zvířatech bylo prokázáno, že glukokortikosteroidy způsobují malformace (rozštěp patra, malformace skeletu). Tyto výsledky experimentů na zvířatech se však u člověka nezdají být při podávání doporučených dávek relevantní. Studie na zvířatech se salmeterolem prokázaly embryofetální toxicitu pouze při vysokých expozičních úrovních. Po současném podávání byl zjištěn zvýšený výskyt transpozice umbilikální artérie a neúplné osifikace okcipitální kosti u potkanů při dávkách spojených se známými abnormalitami způsobenými glukokortikoidy.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Monohydrát laktózy.
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti 2 roky.
Po otevření fóliového obalu: 3 měsíce.
6.4 Zvláštní opatření pro uchovávání
Neuchovávejte při teplotě nad 25 °C.
Po odstranění fóliového obalu ponechejte kryt náustku zavřený.
6.5 Druh obalu a obsah balení
Inhalátor je bílý s poloprůhledným žlutým krytem náustku. Součásti inhalátoru přicházející do kontaktu s léčivým přípravkem/se sliznicí jsou vyrobeny z akrylonitril-butadien-styrenu (ABS), polyetylénu (PE) a polypropylenu (PP). Jeden inhalátor obsahuje 60 dávek a je zabalen do fólie.
Velikost balení: 1 nebo 3 inhalátory.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Teva B.V.,
Swensweg 5,
2031 GA Haarlem Nizozemsko
8. REGISTRAČNÍ ČÍSLO(A)
EU/1/16/1123/001
EU/1/16/1123/002
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace:
10. DATUM REVIZE TEXTU
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
A. VÝROBCE/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
A. VÝROBCE/VÝROBCI ODPOVĚDNÍ ZA PROPOUŠTĚNÍ ŠARŽÍ
Název a adresa výrobce odpovědného/výrobců odpovědných za propouštění šarží
Norton (Waterford) Limited
T/A Teva Pharmaceuticals Ireland
Unit 27/35 IDA Industrial Park
Cork Road
Waterford
Irsko
Teva Pharmaceuticals Europe B.V.
Swensweg 5 2031 GA Haarlem Nizozemsko
Teva Operations Poland Sp. z.o.o. ul. Mogilska 80 31-546 Kraków POLSKO
V příbalové informaci k léčivému přípravku musí být uveden název a adresa výrobce odpovědného za propouštění dané šarže.
B. PODMÍNKY NEBO OMEZENÍ VÝDEJE A POUŽITÍ
Výdej léčivého přípravku je vázán na lékařský předpis.
C. DALŠÍ PODMÍNKY A POŽADAVKY REGISTRACE
• Pravidelně aktualizované zprávy o bezpečnosti
Požadavky pro předkládání pravidelně aktualizovaných zpráv o bezpečnosti pro tento léčivý přípravek jsou uvedeny v seznamu referenčních dat Unie (seznam EURD) stanoveném v čl. 107c odst. 7 směrnice 2001/83/ES a jakékoli následné změny jsou zveřejněny na evropském webovém portálu pro léčivé přípravky.
Držitel rozhodnutí o registraci předloží první pravidelně aktualizovanou zprávu o bezpečnosti pro tento léčivý přípravek do 6 měsíců od jeho registrace.
D. PODMÍNKY NEBO OMEZENÍ S OHLEDEM NA BEZPEČNÉ A ÚČINNÉ POUŽÍVÁNÍ LÉČIVÉHO PŘÍPRAVKU
• Plán řízení rizik (RMP)
Držitel rozhodnutí o registraci uskuteční požadované činnosti a intervence v oblasti farmakovigilance podrobně popsané ve schváleném RMP uvedeném v modulu 1.8.2 registrace a ve veškerých schválených následných aktualizacích RMP.
Aktualizovaný RMP je třeba předložit:
• na žádost Evropské agentury pro léčivé přípravky,
• při každé změně systému řízení rizik, zejména v důsledku obdržení nových informací, které mohou vést k významným změnám poměru přínosů a rizik, nebo z důvodu dosažení význačného milníku (v rámci farmakovigilance nebo minimalizace rizik).
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
ÚDAJE UVÁDĚNÉ NA VNĚJŠÍM OBALU VNĚJŠÍ KRABICE
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU
Airexar Spiromax 50 mikrogramů/500 mikrogramů prášek k inhalaci salmeterolum/flutikasoni propionas
2. OBSAH LÉČIVÉ LÁTKY / LÉČIVÝCH LÁTEK
Jedna odměřená dávka obsahuje 50 mikrogramů salmeterolum (ve formě salmeteroli xinafoas) a 500 mikrogramů flutikasoni propionas.
Jedna podaná dávka (dávka, která je uvolněna přes náustek) obsahuje 45 mikrogramů salmeterolum (ve formě salmeteroli xinafoas) a 465 mikrogramů flutikasoni propionas.
3. SEZNAM POMOCNÝCH LÁTEK
Obsahuje laktózu. Další informace viz příbalovou informaci
4. LÉKOVÁ FORMA A OBSAH BALENÍ
Prášek k inhalaci 1 inhalátor obsahující 60 dávek.
3 inhalátory, z nichž každý obsahuje 60 dávek
5. ZPŮSOB A CESTA/CESTY PODÁNÍ
Před použitím si pozorně přečtěte příbalovou informaci. Inhalační podání.
6. ZVLÁŠTNÍ UPOZORNĚNÍ, ŽE LÉČIVÝ PŘÍPRAVEK MUSÍ BÝT UCHOVÁVÁN MIMO DOHLED A DOSAH DĚTÍ
Uchovávejte mimo dohled a dosah dětí.
7. DALŠÍ ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE POTŘEBNÉ
Používejte podle pokynů lékaře.
Čelní panel: Není určeno k použití u dětí a dospívajících.
Boční panel: Určeno k použití pouze u dospělých ve věku nad 18 let. Není určeno k použití u dětí a dospívajících ve věku do 18 let.
8. POUŽITELNOST
EXP
Používejte do 3 měsíců po odstranění fóliového obalu.
9. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
Neuchovávejte při teplotě nad 25 °C. Po odstranění fóliového obalu ponechejte kryt náustku zavřený.
10. ZVLÁŠTNÍ OPATŘENÍ PRO LIKVIDACI NEPOUŽITÝCH LÉČIVÝCH PŘÍPRAVKŮ NEBO ODPADU Z NICH, POKUD JE TO VHODNÉ
11. NÁZEV A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Teva B.V., Swensweg 5, 2031 GA Haarlem, Nizozemsko
12. REGISTRAČNÍ ČÍSLO/ČÍSLA
EU/1/16/1123/001
EU/1/16/1123/002
13. ČÍSLO ŠARŽE
Lot
14. KLASIFIKACE PRO VÝDEJ
15. NÁVOD K POUŽITÍ
16. INFORMACE V BRAILLOVĚ PÍSMU
Airexar Spiromax 50 pg/500 pg
17. JEDINEČNÝ IDENTIFIKÁTOR - 2D ČÁROVÝ KÓD
<2D čárový kód s jedinečným identifikátorem .>
18. JEDINEČNÝ IDENTIFIKÁTOR - DATA ČITELNÁ OKEM
PC:
SN:
NN:
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU FÓLIE_
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Airexar Spiromax 50 mikrogramů/500 mikrogramů prášek k inhalaci salmeterolum/flutikasoni propionas Inhalační podání
2. ZPŮSOB PODÁNÍ_
Přečtěte si příbalovou informaci
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
Obsahuje 1 inhalátor
6. JINÉ_
Po odstranění fóliového obalu ponechejte kryt náustku zavřený a používejte do 3 měsíců od odstranění fóliového obalu.
Teva B.V.
MINIMÁLNÍ ÚDAJE UVÁDĚNÉ NA MALÉM VNITŘNÍM OBALU INHALÁTOR
1. NÁZEV LÉČIVÉHO PŘÍPRAVKU A CESTA/CESTY PODÁNÍ
Airexar Spiromax 50 mikrogramů/500 mikrogramů Prášek k inhalaci
salmeterolum/flutikasoni propionas Inhalační podání
2. ZPŮSOB PODÁNÍ
Před použitím si přečtěte pečlivě příbalovou informaci.
3. POUŽITELNOST
EXP
4. ČÍSLO ŠARŽE
Lot
5. OBSAH UDANÝ JAKO HMOTNOST, OBJEM NEBO POČET
60 dávek
6. JINÉ
Pouze pro dospělé. Obsahuje laktózu. Začátek:
Teva B.V.
B. PŘÍBALOVÁ INFORMACE
Airexar Spiromax 50 mikrogramů/500 mikrogramů prášek k inhalaci
salmeterolum/flutikasoni propionas
Přečtěte si pozorně celou příbalovou informaci dříve, než začnete tento přípravek používat, protože obsahuje pro Vás důležité údaje.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu.
- Máte-li jakékoli další otázky, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
- Tento přípravek byl předepsán výhradně Vám. Nedávejte jej žádné další osobě. Mohl by jí ublížit, a to i tehdy, má-li stejné známky onemocnění jako Vy.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Viz bod 4.
Co naleznete v této příbalové informaci
1. Co je Airexar Spiromax a k čemu se používá
2. Čemu musíte věnovat pozornost, než začnete Airexar Spiromax používat
3. Jak se Airexar Spiromax používá
4. Možné nežádoucí účinky
5. Jak Airexar Spiromax uchovávat
6. Obsah balení a další informace
1. Co je Airexar Spiromax a k čemu se používá
Airexar Spiromax obsahuje dvě léčivé látky, salmeterol a flutikason-propionát:
• Salmeterol je dlouhodobě působící bronchodilatátor. Bronchodilatátory pomáhají udržet dýchací cesty průchodné. To usnadňuje průnik vzduchu dovnitř a ven. Účinky trvají po dobu nejméně 12 hodin.
• Flutikason-propionát je kortikosteroid, který zmírňuje otok a podráždění v plicích.
Váš lékař Vám tento přípravek předepsal pro léčbu buď:
• těžkého astmatu, aby pomáhal při předcházení záchvatů dušnosti a sípání, nebo
• chronické obstrukční plicní nemoci (CHOPN), ke snížení počtu vzplanutí příznaků.
Airexar Spiromax musíte používat každý den, jak Vám doporučil Váš lékař. Tím bude zajištěno, že bude při kontrole astmatu nebo CHOPN správně účinkovat.
Airexar Spiromax pomáhá k zastavení nástupu dušnosti a sípání. Airexar Spiromax by však neměl být používán k úlevě při záchvatu dušnosti nebo sípání. Pokud k takovému záchvatu dojde, musíte použít rychle působící „úlevový“ (záchranný) inhalátor, jako je např. salbutamol. Rychle působící „úlevový“ inhalátor byste měl(a)mít neustále u sebe.
Airexar Spiromax by měl být používán pouze k léčbě těžkého astmatu u dospělých ve věku nad 18 let a u dospělých s CHOPN.
2. Čemu musíte věnovat pozornost, než začnete Airexar Spiromax používat Nepoužívejte Airexar Spiromax:
- jestliže jste alergický(á) (přecitlivělý(á)) na salmeterol, flutikason-propionát nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
Upozornění a opatření
Před použitím Airexar Spiromax se poraďte se svým lékařem, lékárníkem nebo zdravotní sestrou, jestliže se léčíte s:
• onemocněním srdce, včetně nepravidelnosti srdečního rytmu nebo rychlé srdeční činnosti;
• zvýšenou činností štítné žlázy;
• vysokým krevním tlakem;
• cukrovkou (diabetes mellitus) (Airexar Spiromax může zvyšovat hladinu cukru v krvi);
• nízkou hladinou draslíku v krvi;
• tuberkulózou nebo jste se léčil(a) s tuberkulózou nebo s jinými plicními infekcemi.
Děti a dospívající
Tento léčivý přípravek se nemá používat u dětí nebo dospívajících ve věku do 18 let.
Další léčivé přípravky a Airexar Spiromax
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat. To zahrnuje jiné léky na astma i všechny léky, které jste obdržel(a) bez předpisu. Airexar Spiromax nemusí být vhodný k používání s některými jinými léky.
Než začnete používat Airexar Spiromax, informujte svého lékaře, pokud užíváte tyto léčivé přípravky:
• Beta blokátory (jako je např. atenolol, propranolol či sotalol). Beta blokátory se většinou používají na vysoký krevní tlak nebo srdeční onemocnění, jako je např. angina pectoris.
• Léky k léčbě infekcí (jako je např. ritonavir, ketokonazol, itrakonazol a erythromycin). Některé z těchto léků mohou zvyšovat množství salmeterolu nebo flutikason-propionátu v těle. Tím se může u přípravku Airexar Spiromax zvýšit riziko nežádoucích účinků včetně nepravidelného bušení srdce, anebo se mohou nežádoucí účinky zhoršit.
• Kortikosteroidy (podávané ústy nebo injekčně). Léčba těmito léky v nedávné minulosti může zvýšit riziko, že Airexar Spiromax bude ovlivňovat funkci nadledvin.
• Diuretika, léky zvyšující močení, která se používají k léčbě vysokého tlaku.
• Jiné bronchodilatátory (např. salbutamol).
• Xanthinové léky, jako je např. aminofylin a teofylin. Ty se často používají k léčbě astmatu.
Těhotenství a kojení
Pokud jste těhotná, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek používat.
Není známo, zda se tento lék může vylučovat mateřským mlékem. Pokud kojíte, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek používat.
Řízení dopravních prostředků a obsluha strojů
Není pravděpodobné, že by Airexar Spiromax měl vliv na schopnost řídit dopravní prostředky nebo obsluhovat stroje.
Airexar Spiromax obsahuje laktózu
Laktóza je druh cukru, který se nachází v mléce. Laktóza obsahuje malá množství mléčné bílkoviny, která mohou způsobovat alergické reakce. Pokud Vám lékař řekl, že nesnášíte nebo máte alergii na laktózu, jiné cukry nebo mléko, poraďte se se svým lékařem dříve, než začnete tento přípravek používat.
3. Jak se Airexar Spiromax používá
Vždy používejte tento přípravek přesně podle pokynů svého lékaře nebo lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
• Airexar Spiromax používejte každý den, dokud Vám lékař nedoporučí, abyste jej vysadil(a).
Nepoužívejte větší než doporučenou dávku. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
• Nepřestaňte používat Airexar Spiromax ani nesnižujte dávku Airexar Spiromax, aniž byste se předem poradil(a) s lékařem.
• Airexar Spiromax se má vdechovat ústy do plic.
Doporučená dávka přípravku je:
Těžké astma u dospělých ve věku od 18 let
Jedna inhalace dvakrát denně
Chronická obstrukční plicní nemoc (CHOPN)
Jedna inhalace dvakrát denně
Pokud používáte Airexar Spiromax na astma, lékař bude u Vás pravidelně kontrolovat příznaky.
Lékař Vám pomůže s léčbou astmatu a upraví dávku tohoto léčivého přípravku na nejnižší dávku, která potlačí příznaky onemocnění. Pokud se bude lékař domnívat, že potřebujete dávku nižší, než je dávka z inhalátoru Airexar Spiromax, může Vám předepsat jiný inhalátor, který obsahuje stejné léčivé látky jako Airexar Spiromax, ale s nižší dávkou kortikosteroidu. Neměňte však počet dávek, který Vám lékař předepsal, aniž byste se s ním předem poradil(a).
Pokud se u Vás astma nebo dušnost zhorší, řekněte to ihned svému lékaři. Pokud máte větší sípání, častý pocit tísně na hrudi nebo musíte užívat rychle působící „úlevový“ lék, možná se Vaše onemocnění zhoršuje a mohl(a) byste vážně onemocnět. Měl(a) byste dále používat Airexar Spiromax, ale nezvyšovat počet dávek. Navštivte ihned svého lékaře, protože možná potřebujete další léky.
Návod k použití
Nácvik
Váš lékař, zdravotní sestra nebo lékárník by s Vámi měli nacvičit, jak inhalátor používat, včetně toho, jak účinně využít dávku. Tento nácvik je důležitý k zajištění, abyste dostal(a) dávku, kterou potřebujete. Pokud jste nácvik neobdržel(a), požádejte svého lékaře, zdravotní sestru nebo lékárníka dříve, než inhalátor použijete poprvé, aby Vám ukázali, jak se má inhalátor správně používat.
Váš lékař, zdravotní sestra nebo lékárník by také měli čas od času zkontrolovat to, jak používáte svůj inhalátor Spiromax, aby se zajistilo, že inhalátor používáte správně a podle předpisu. Pokud nepoužíváte inhalátor Airexar Spiromax správně a/nebo se z něj nenadechujete ústy dostatečně usilovně, může to znamenat, že se do Vašich plic nedostává dostatek léku. Pokud se do Vašich plic nedostává dostatek léku, nebude pomáhat při léčbě astmatu nebo CHOPN tak, jak by měl.
Příprava inhalátoru Airexar Spiromax
Než použijete Airexar Spiromax poprvé, musíte jej připravit podle následujících pokynů:
• Zkontrolujte na ukazateli dávek, zda je v inhalátoru 60 inhalací.
• Napište datum, kdy jste otevřel(a) fóliový obal, na štítek inhalátoru.
• S inhalátorem není nutné před použitím třepat.
Jak inhalovat
1. Držte inhalátor s poloprůhledným žlutým krytem náustku směrem dolů. Inhalátor nemusíte protřepávat.
2. Otevřete kryt náustku sklopením dolů, až uslyšíte jedno hlasité klapnutí. Inhalátor je nyní připravený k použití.
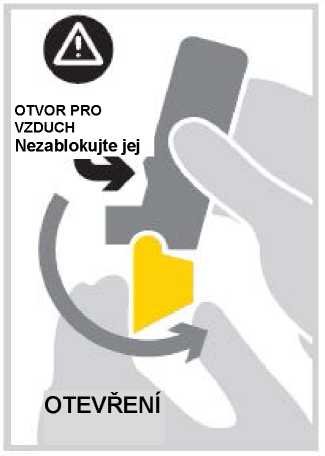

3. Lehce vydechněte (co nejpohodlněji). Nevydechujte přes inhalátor.
4. Náustek vložte mezi zuby. Náustek nekousejte. Uzavřete rty kolem náustku. Dejte pozor, abyste nezablokoval(a) otvory pro vzduch.
Nadechněte se ústy, co nejhlouběji a co nej usilovněji.
Uvědomte si, že je důležité, abyste se nadechl(a) usilovně.

NÁDECH
5. Zadržte dech na dobu 10 sekund, nebo tak dlouho, jak je to pohodlné.
6. Vyjměte inhalátor z úst. Při inhalaci můžete pocítit určitou příchuť.
7. Pak pomalu vydechněte (nevydechujte přes inhalátor). Uzavřete kryt náustku.

UZAVŘENÍ
Poté vypláchněte ústa vodou a vodu vyplivněte, a/nebo si vyčistěte zuby. To může pomoci při předcházení moučnivce v ústech a/nebo chrapotu.
Nepokoušejte se inhalátor rozebírat, odstranit kryt náustku nebo jím kroutit. Kryt náustku je připevněn k inhalátoru a nesmí se odstranit. Inhalátor nepoužívejte, pokud je poškozený nebo pokud se kryt náustku od inhalátoru oddělil. Neotevírejte ani neuzavírejte kryt náustku, pokud inhalátor právě nepoužíváte.
Pokud náustek otevřete a uzavřete, aniž byste provedl(a) inhalaci, zůstane dávka bezpečně zajištěna uvnitř inhalátoru připravena do příští inhalace. Není možné náhodné podání další dávky ani zdvojnásobení dávky při jedné inhalaci.
Pokud nechcete inhalátor právě použít, zachovávejte náustek neustále uzavřený.
Čištění inhalátoru
Inhalátor udržujte suchý a čistý.
V případě potřeby můžete náustek inhalátoru otřít suchým hadříkem.
Kdy začít používat nový Airexar Spiromax
• Ukazatel dávek na zadní straně prostředku ukazuje, kolik dávek (inhalací) v inhalátoru zůstává. Když je inhalátor plný, obsahuje 60 inhalací.

• Ukazatel dávek ukazuje počet zbývajících inhalací pouze v sudých číslech.
• Když zbývá 20 a méně inhalací, jsou čísla od 20 do „8“, „6“, „4“ a „2“ zobrazena červeně na bílém pozadí. Když se barva čísel v okénku změní na červenou, měl(a) byste navštívit svého lékaře a požádat o nový inhalátor.
Poznámka:
• Náustek bude stále „klapat“, i když bude inhalátor již prázdný. Když náustek otevřete a zavřete, aniž byste provedl(a) inhalaci, bude to ukazatel dávek počítat jako odebranou dávku.
Jestliže jste použil(a) více dávek Airexar Spiromax, než jste měl(a)
Je důležité, abyste používal(a) inhalátor podle pokynů. Pokud náhodně použijete více dávek, než Vám bylo doporučeno, poraďte se se svým lékařem nebo lékárníkem. Možná si povšimnete, že Vám srdce buší rychleji než obvykle a že se cítíte nejistý(á). Můžete mít také závratě, bolest hlavy, svalovou slabost a bolesti kloubů.
Pokud používáte příliš mnoho dávek z inhalátoru Airexar Spiromax po dlouhou dobu, měl(a) byste požádat o radu svého lékaře nebo lékárníka. To proto, že používání příliš velkého množství přípravku Airexar Spiromax může snižovat hladinu steroidních hormonů vytvářených nadledvinami.
Jestliže jste zapomněl(a) Airexar Spiromax použít
Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku. Další dávku použijte v obvyklou dobu.
Jestliže jste přestal(a) Airexar Spiromax používat
Je velmi důležité, abyste používal(a) Airexar Spiromax každý den, jak Vám bylo doporučeno. V používání pokračujte, dokud Vám lékař neřekne, abyste přestal(a). Přípravek nevysazujte ani nesnižujte dávku Airexar Spiromax. Mohlo by pak u Vás dojít ke zhoršení dýchání.
Kromě toho, pokud náhle přestanete Airexar Spiromax používat nebo snížíte dávku Airexar Spiromax, může Vám to (velmi vzácně) způsobit problémy s nadledvinami (nadledvinovou nedostatečnost), která někdy způsobuje nežádoucí účinky.
Mezi tyto nežádoucí účinky mohou patřit kterékoli z níže uvedených:
• bolest žaludku;
• únava a ztráta chuti k j ídlu, pocit nevolnosti;
• nevolnost a průjem;
• úbytek tělesné hmotnosti;
• bolest hlavy nebo ospalost;
• nízké hladiny cukru v krvi;
• nízký krevní tlak a záchvaty (křeče).
Když je tělo ve stresu, např. při horečce, úrazu (např. při nehodě nebo poranění), infekci nebo operaci, může se nadledvinová nedostatečnost zhoršit a mohou se u Vás vyskytnout kterékoli z výše uvedených příznaků.
Pokud se u Vás vyskytnou některé nežádoucí účinky, řekněte to svému lékaři nebo lékárníkovi. Aby se těmto příznakům předešlo, může Vám lékař předepsat další kortikosteroidy ve formě tablet (např. prednisolon).
Máte-li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4. Možné nežádoucí účinky
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého. Aby se snížila pravděpodobnost výskytu nežádoucích účinků, lékař Vám předepíše nejnižší dávkou této lékové kombinace, která u Vás bude stačit ke kontrole astmatu nebo CHOPN.
Alergické reakce: můžete si povšimnout, že se Vám okamžitě po použití přípravku Airexar Spiromax náhle zhoršilo dýchání. Můžete sípat a mít kašel nebo dušnost. Můžete si také povšimnout svědění, vyrážky (kopřivky) a otoků (obvykle na tváři, rtech, jazyku nebo v hrdle), nebo můžete náhle pocítit, že Vám srdce buší velmi rychle, nebo máte pocit na omdlení a závratě (což může vést k mdlobám nebo ztrátě vědomí). Pokud se u Vás vyskytne kterýkoli z těchto účinků nebo pokud se objeví náhle po použití přípravku Airexar Spiromax, přestaňte Airexar Spiromax používat a řekněte to ihned svému lékaři. Alergické reakce na Airexar Spiromax jsou méně časté (mohou postihovat až 1 ze 100 lidí).
Níže jsou uvedeny další nežádoucí účinky:
Velmi časté (mohou postihovat více než 1 z 10 lidí)
• Bolest hlavy - ta se obvykle při pokračování léčby zmírňuje.
• U pacientů s chronickou obstrukční plicní nemocí (CHOPN) byl hlášen zvýšený výskyt nachlazení.
Časté (mohou postihovat až 1 z 10 lidí)
• Moučnivka (bolavá krémově žlutá vyvýšená místa) dutiny ústní a hrdla. Také bolestivost jazyka, hrdla a chrapot a podráždění hrdla. Pomoci může vypláchnutí úst vodou, okamžité vyplivnutí vody a/nebo vyčištění zubů okamžitě po použití každé dávky léčivého přípravku. Lékař Vám může k léčbě moučnivky předepsat lék k léčbě plísní.
• Bolestivé a oteklé klouby a svalová bolest.
• Svalové křeče.
U pacientů s chronickou obstrukční plicní nemocí (CHOPN) byly také hlášeny tyto nežádoucí účinky:
• Pneumonie a bronchitis (plicní infekce). Řekněte svému lékaři, pokud si během používání přípravku Airexar Spiromax povšimnete některého z následujících příznaků, protože to mohou být příznaky plicní infekce: horečka nebo zimnice; zvýšená tvorba hlenu, změny barvy hlenu; zhoršení kašle nebo zhoršení potíží s dýcháním.
• Podlitiny a zlomeniny.
• Zánět vedlejších nosních dutin (sinusitis, pocit tlaku v nose nebo ucpaného nosu, tlaku v tvářích nebo za očima, někdy s pulzující bolestí).
• Snížené množství draslíku v krvi (mohou se vyskytnout i nepravidelná srdeční činnost, svalová slabost, křeče).
Méně časté (mohou postihovat až 1 ze 100 lidí)
• Zvýšení cukru (glukózy) v krvi (hyperglykémie). Máte-li diabetes, může být nutná častější kontrola cukru v krvi a případně úprava léčby diabetu.
• Katarakta (zakalená oční čočka).
• Velmi rychlá srdeční činnost (tachykardie).
• Pocit třesu (třes) a rychlé nebo nepravidelné srdeční akce (palpitace) - nejsou obvykle závažné a zmenšují se při pokračování léčby.
• Bolest na hrudi.
• Pocit úzkosti (i když tento účinek se vyskytuje hlavně u dětí, když je předepsána tato léková kombinace, ale v nižší síle).
• Poruchy spánku.
• Alergická kožní vyrážka.
Vzácné (mohou postihovat až 1 z 1 000 lidí)
• Dýchací potíže nebo sípání, které se zhoršují ihned po použití Airexar Spiromax. Pokud k tomu dojde, přestaňte inhalátor Airexar Spiromax používat. Použijte rychle působící „úlevový“ inhalátor, aby se Vám lépe dýchalo, a informujte okamžitě svého lékaře.
• Airexar Spiromax může mít vliv na normální tvorbu steroidních hormonů v těle, zejména když užíváte vysoké dávky po dlouhou dobu. Mezi tyto účinky patří:
- Zpomalení růstu u dětí a dospívajících
- Řídnutí kostí
- Glaukom (zelený zákal)
- Přírůstek tělesné hmotnosti
- Zaokrouhlení obličeje (měsíčkovitý tvar) (Cushingův syndrom)
Lékař bude pravidelně kontrolovat, zda se u Vás některé z těchto nežádoucích účinků nevyskytují, a
zajistí, abyste ke kontrole astmatu používal(a) co nejnižší dávku této lékové kombinace.
• Změny chování, jako je např. neobvyklá aktivita a podrážděnost (i když tyto účinky se vyskytují hlavně u dětí, když je předepsána tato léková kombinace, ale v nižší síle).
• Nepravidelná nebo nevyrovnaná srdeční činnost nebo předčasné srdeční stahy (arytmie). Informujte svého lékaře, ale nepřestaňte používat Airexar Spiromax, pokud Vám lékař neřekne, abyste jej přestal(a) používat.
• Plísňová infekce v jícnu, která může působit potíže při polykání.
Frekvence není známá, ale mohou se také vyskytnout:
• Deprese nebo agresivita (i když pravděpodobnost výskytu těchto účinků je vyšší u dětí, když je předepsána tato léková kombinace, ale v nižší síle).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři, lékárníkovi nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků uvedeného v Dodatku V. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. Jak Airexar Spiromax uchovávat
• Uchovávejte tento přípravek mimo dohled a dosah dětí.
• Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a na štítku inhalátoru za EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce.
• Neuchovávejte při teplotě nad 25 °C. Po odstranění fóliového obalu ponechejte kryt náustku zavřený.
• Používejte do 3 měsíců po odstranění fóliového obalu. Datum, kdy jste otevřel(a) fóliový obal, napište na štítek inhalátoru.
• Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
Co Airexar Spiromax obsahuje
- Léčivými látkami jsou salmeterolum a flutikasoni propionas. Jedna odměřená dávka obsahuje 50 mikrogramů salmeterolum (ve formě salmeteroli xinafoas) a 500 mikrogramů flutikasoni propionas. Jedna podaná dávka (dávka, která je uvolněna přes náustek) obsahuje 45 mikrogramů salmeterolum (ve formě salmeteroli xinafoas) a 465 mikrogramů flutikasoni propionas.
- Další pomocnou látkou je monohydrát laktózy (viz bod 2, odstavec „Airexar Spiromax obsahuje laktózu“).
Jak Airexar Spiromax vypadá a co obsahuje toto balení
Airexar Spiromax je prášek k inhalaci.
Jeden inhalátor Airexar Spiromax obsahuje 60 inhalací a má bílé tělo s poloprůhledným žlutým krytem
náustku.
Balení obsahující 1 a 3 inhalátory. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci
Teva B.V.
Swensweg 5, 2031 GA Haarlem, Nizozemsko
Výrobce
Norton (Waterford) Limited T/A Teva Pharmaceuticals Ireland Unit 27/35, IDA Industrial Park, Cork Road, Waterford, Irsko
Teva Pharmaceuticals Europe B.V., Swensweg 5, 2031 GA Haarlem, Nizozemsko (Pouze pro Polsko) Teva Operations Poland Sp. z o.o. Mogilska 80 Str. 31-546 Kraków, Polsko
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Belgie/Belgique/Belgien
Teva Pharma Belgium N.V./S.A./AG
Tel/Tél: +32 3 820 73 73
Bt^rapnn
TeBa ^apMacroTHKKnc Bt^rapnn EOO^ Te.m +359 2 489 95 82
Česká republika
Teva Pharmaceuticals CR, s.r.o.
Tel: +420 251 007 111
Danmark
Teva Denmark A/S
Tlf: +45 44 98 55 11
Deutschland Teva GmbH Tel: +49 731 402 08
Lietuva
UAB “Sicor Biotech”
Tel: +370 5 266 02 03
Luxembourg/Luxemburg
Teva Pharma Belgium N.V./S.A./AG
Tel/Tél: +32 3 820 73 73
Magyarország
Teva Magyarország Zrt
Tel.: +36 1 288 64 00
Malta
Teva Pharmaceuticals Ireland L-Irlanda
Tel: +353 51 321 740
Nederland
Teva Nederland B.V.
Tel: +31 800 0228 400
Eesti
Teva Eesti esindus UAB Sicor Biotech Eesti filiaal
Tel: +372 661 0801 Ekkába
Teva Ekkág A.E.
T nk: +30 210 72 79 099
Espaňa
Teva Pharma S.L.U.
Tél: +34 91 387 32 80
France
Teva Santé
Tél: +33 1 55 91 7800
Hrvatska
Pliva Hrvatska d.o.o Tel: + 385 1 37 20 000
Ireland
Teva Pharmaceuticals Ireland Tel: +353 51 321 740
Island
Vistor
Simi: +354 535 7000 Italia
Teva Italia S.r.l.
Tel: +39 028 917 981
Kúrcpog
Teva Ekkág A.E.
Ekkába
Tnk: +30 210 72 79 099 Latvija
Sicor Biotech filiale Latvija Tel: +371 67 323 666
Norge
Teva Norway AS Tlf: +47 6677 55 90
Osterreich
ratiopharm Arzneimittel Vertriebs GmbH Tel: +43 1 97007 0
Polska
Teva Pharmaceuticals Polska Sp. z o.o.
Tel.: +48 22 345 93 00
Portugal
Teva Pharma - Produtos Farmaceuticos Lda Tel: +351 21 476 75 50
Románia
Teva Pharmaceuticals S.R.L Tel: +4021 230 6524
Slovenija
Pliva Ljubljana d.o.o.
Tel: +386 1 58 90 390
Slovenská republika
Teva Pharmaceuticals Slovakia s.r.o.
Tel: +421 2 5726 7911
Suomi/Finland
Teva Finland
Puh/Tel: +358 20 180 5900
Sverige
Teva Sweden AB Tel: +46 42 12 11 00
United Kingdom Teva UK Limited Tel: +44 1977 628 500
Tato příbalová informace byla naposledy revidována v měsíc RRRR.
Další zdroje informací
Podrobné informace o tomto léčivém přípravku jsou k dispozici na webových stránkách_Evropské agentury pro léčivé přípravky http://www.ema.europa.eu
39