Procox 0,9 + 18 Mg/Ml
SOUHRN ÚDAJŮ O PŘÍPRAVKU
PŘÍLOHA I
Procox 0,9 mg/ml + 18 mg/ml perorální suspenze pro psy
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ml obsahuje:
Léčivé látky:
emodepsidum 0,9 mg toltrazurilum 18mg
Pomocné látky:
butylhydroxytoluen (E321; jako antioxidant) 0,9 mg kyselina sorbová (E200; jako konzervant) 0,7 mg
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Perorální suspenze.
Bílá až nažloutlá suspenze.
4. KLINICKÉ ÚDAJE
4.1 Cílové druhy zvířat
Psi.
4.2 Indikace s upřesněním pro cílový druh zvířat
Určeno pro psy při suspektních nebo prokázaných smíšených parazitárních infekcích vyvolaných oblými
červy a kokcidiemi následujících druhů:
Oblí červi (Nematoda):
- Toxocara canis (dospělá stádia, juvenilní stádia, larvální stádia L4)
- Uncinaria stenocephala (dospělá stádia)
- Ancylostoma caninum (dospělá stádia)
- Trichuris vulpis (dospělá stádia)
Kokcidie:
- Isospora ohioensis komplex
- Isospora canis
Procox zabraňuje rozmnožování kokcidií Isospora a také vylučování oocyst. Léčba sice zabrání rozšiřování infekce, nebude však účinná proti klinickým příznakům infekce u již nakažených zvířat.
4.3 Kontraindikace
Nepodávat psům/štěňatům mladším 2 týdnů nebo s živou hmotností nižší než 0,4 kg.
Nepoužívat v případě přecitlivělosti na léčivé látky nebo na některou z pomocných látek.
4.4 Zvláštní upozornění
Procox zabraňuje rozmnožování kokcidií a vylučování oocyst. Množení parazitů poškozuje sliznici střeva psa, což může vést ke vzniku enteritidy. Proto léčba Procoxem neřeší klinické příznaky způsobené poškozením sliznice střeva (např. průjem), které se objevily před ošetřením. V takových případech může být potřebná podpůrná léčba.
Terapie proti Isospora může minimalizovat vylučování oocyst do vnějšího prostředí, čímž se sníží riziko reinfekce ve skupinách /v kotcích s potvrzenou a opakovanou infekcí Isospora.
Zároveň by měla být zahájena strategie prevence, včetně úsilí o snížení infekce. Léčba Procoxem je jedním z nezbytných opatření této strategie.
Aby se zabránilo reinfekci z prostředí, je důležité zavést hygienická opatření, zvláště pak je důležité zajistit co nejsušší a nejčistší prostředí. Oocysty Isospory jsou odolné vůči mnoha dezinfekčním prostředkům a můžou přežít ve vnějším prostředí po velmi dlouhou dobu. Včasné odstranění výkalů před sporulací oocyst (do 12 hodin) snižuje pravděpodobnost přenosu infekce. Jedna aplikace Procoxu ve vrhu/skupině je obecně dostačující ke snížení vylučování oocyst Isospora. V kotcích s opakujícím se výskytem klinických projevů infekcí Isospora by měl být každý vrh léčen po delší dobu z důvodu kontroly a postupného snižování stupně infekce. Všichni psi ve skupině, kteří jsou ohroženi infekcí, by měli být ošetřeni současně, včetně dospělých zvířat, která mohou být infikována subklinicky. Ke sledování úspěšnosti kontrolního programu je vhodné na závěr použít diagnostické metody (flotace exkrementů), které určí přítomnost a stupeň vylučování oocyst ve skupině zvířat.
Podobně jako u ostatních antiparazitárních přípravků může vést časté a dlouhodobé používání anthelmintik nebo antiprotozoik ke vzniku rezistence. Vhodný léčebný režim doporučený veterinářem zajistí adekvátní kontrolu parazitů a sníží pravděpodobnost vzniku rezistence. Je třeba vyhnout se zbytečnému podávání. Opakované ošetření je indikováno jen tehdy, pokud smíšená infekce kokcidiemi a nematody, jak je popsáno v bodě 4.2., je stále suspektní nebo klinická.
4.5 Zvláštní opatření pro použití
Zvláštní opatření pro použití u zvířat
Procox se nedoporučuje podávat koliím a jim příbuzným plemenům, které jsou nositeli mdr1 -/- mutace a nebo se tato mutace předpokládá. Prokázalo se, že u těchto mdr1 -/- mutantních štěňat je přípravek snášen méně než u štěňat ostatních. Emodepsid je substrát pro P-glykoprotein.
Zkušenosti s podáváním přípravku u závažně oslabených psů nebo psů s porušenou funkcí ledvin či jater jsou omezené. Proto je vhodné u těchto zvířat přípravek použít pouze na základě posouzení terapeutického prospěchu a rizika ošetřujícím veterinárním lékařem.
Zvláštní opatření určené osobám, které podávají veterinární léčivý přípravek zvířatům
Nejezte, nepijte a nekuřte při manipulaci s přípravkem.
Po aplikaci si umyjte ruce vodou.
V případě náhodného potřísnění kůže, umyjte postižené místo neprodleně mýdlem a vodou.
V případě, že se přípravek náhodně dostane do očí, vypláchněte oči neprodleně velkým množstvím vody.
V případě náhodného pozření přípravku, zvláště pak u dětí, vyhledejte ihned lékařskou pomoc a ukažte příbalovou informaci nebo etiketu praktickému lékaři.
4.6 Nežádoucí účinky (frekvence a závažnost)
Ve velmi vzácných případech se mohou objevit mírné a přechodné poruchy trávicího traktu (např. zvracení nebo měkká stolice).
Četnost nežádoucích účinků se určuje na základě následujících pravidel:
- velmi časté (více jak 1 z 10 zvířat vykazuje nežádoucí účinky v průběhu jednoho ošetření)
- časté (postihují více než 1, ale méně než 10 zvířat ze 100)
- méně časté (postihují více než 1, ale méně než 10 zvířat z 1000)
- vzácné (postihují více než 1, ale méně 10 zvířat z 10 000)
- velmi vzácné (postihují méně jak 1 zvíře z 10 000, včetně jednotlivých hlášených případů)
4.7 Použití v průběhu březosti, laktace nebo snášky
Nebyla stanovena bezpečnost veterinárního léčivého přípravku pro březí feny a laktující feny. Použití u březích fen a laktujících fen v průběhu prvních dvou týdnů laktace se proto nedoporučuje.
4.8 Interakce s dalšími léčivými přípravky a další formy interakce
Emodepsid slouží jako substrát pro P-glykoprotein, takže současné podávání dalších veterinárních léčivých přípravků s podobnou funkcí či léků inhibujících P-glykoprotein (například ivermektin a další antiparazitární makrocyklické laktony, erytromycin, prednisolon a cyklosporin) může vyvolat farmakokinetické interakce. Možné klinické dopady těchto interakcí nebyly zkoumány.
4.9 Podávané množství a způsob podání
Dávkování a léčebné schéma
Pro perorální podání u psů starších 2 týdnů a s hmotností minimálně 0,4 kg
Doporučená minimální dávka je 0,5 ml/kg živé hmotnosti (ž.hm.), což odpovídá 0,45 mg emodepsidu/kg ž.hm. a 9 mg toltrazurilu/kg ž.hm.
Doporučené dávkování je uvedeno v následující tabulce:
|
Hmotnost [kg] |
Dávka [ml] |
|
0,4 |
0,2 |
|
> 0,4 - 0,6* |
0,3 |
|
> 0,6 - 0,8 |
0,4 |
|
> 0,8 - 1 |
0,5 |
|
> 1,0 - 1,2 |
0,6 |
|
> 1,2 - 1,4 |
0,7 |
|
> 1,4 - 1,6 |
0,8 |
|
> 1,6 - 1,8 |
0,9 |
|
> 1,8 - 2 |
1,0 |
|
> 2,0 - 2,2 |
1,1 |
|
> 2,2 - 2,4 |
1,2 |
|
> 2,4 - 2,6 |
1,3 |
|
> 2,6 - 2,8 |
1,4 |
|
> 2,8 - 3 |
1,5 |
|
> 3,0 - 3,2 |
1,6 |
|
> 3,2 - 3,4 |
1,7 |
|
> 3,4 - 3,6 |
1,8 |
|
> 3,6 - 3,8 |
1,9 |
|
> 3,8 - 4 |
2,0 |
|
> 4 - 5 |
2,5 |
|
> 5 - 6 |
3,0 |
|
> 6 - 7 |
3,5 |
|
> 7 - 8 |
4,0 |
|
> 8 - 9 |
4,5 |
|
> 9 - 10 |
5,0 |
|
> 10 kg: Pokračujte v dávkování 0,5 ml/kg ž.hm. | |
*= více než 0,4 a do 0,6 kg
Jednorázové podání je obecně dostačující pro snížení vylučování oocyst Isospora. Opakovaná terapie je indikována jen tehdy, pokud smíšená infekce kokcidiemi a nematody, jak je popsáno v bodě 4.2, je i nadále suspektní nebo klinická. Strategie léčby by měla být přizpůsobena v každém kotci infekčnímu tlaku prostředí (viz také bod 4.4).
Způsob _ podávání
Před použitím dobře protřepejte.
Odšroubujte uzávěr přípravku. Použijte standardní jednorázovou stříkačku s ústím typu Luer pro každé ošetření. Pro přesné dávkování u psů o hmotnosti do 4 kg použijte stříkačku se stupnicí po 0,1 ml. U psů o hmotnosti nad 4 kg lze využít stříkačku se stupnicí po 0,5 ml. Nasaďte ústí stříkačky pevně do otvoru lahvičky a pak obraťte lahvičku dnem vzhůru a natáhněte příslušné množství přípravku. Před vytažením ústí stříkačky musí být lahvička opět dnem dolů. Po použití zašroubujte šroubový uzávěr. Aplikujte suspenzi do dutiny ústní psa.
Po aplikaci stříkačku vyhoďte (pokud není možné ji vyčistit).
4.10 Předávkování (symptomy, první pomoc, antidota), pokud je to nutné
Bezpečnost doporučené dávky byla sledována u štěňat, která byla ošetřena každé 2 týdny až 5krát po sobě.
Při opakovaném podávání veterinárního léčivého přípravku v dávce až 5x vyšší než je doporučená dávka se občas objevily mírné a přechodné poruchy trávicího traktu v podobě měkké stolice nebo zvracení.
4.11 Ochranné lhůty
Není určeno pro potravinová zvířata.
5. FARMAKOLOGICKÉ VLASTNOSTI
Farmakoterapeutická skupina: antiparazitikum, jiná anthelmintika ATC vet kód: QP52AX60
5.1 Farmakodynamické vlastnosti
Emodepsid je semisyntetická látka patřící do chemické skupiny depsipeptidů. Tato látka působí na oblé červy (škrkavky, měchovce a tenkohlavce). V tomto přípravku působí emodepsid proti Toxocara canis, Uncinaria stenocephala, Ancylostoma caninum a Trichuris vulpis.
Jeho účinek se odehrává na neuromuskulárních spojeních, kde stimulací presynaptických receptorů pro sekretin vyvolává paralýzu a úhyn parazitů.
Toltrazuril je derivátem triazinonu. Působí proti kokcidiím rodu Eimeria a Isospora. Jeho účinek zasahuje všechna intracelulární stádia kokcidií jak ve fázi merogonie (nepohlavní rozmnožování) tak v gamogonii (pohlavní fáze). V rámci působení jsou zničena všechna stádia parazita, takže účinek toltrazurilu lze označit za kokcidiocidní.
5.2 Farmakokinetické údaje
Po perorální aplikaci potkanům se emodepsid dostává do všech orgánů. Nejvyšší koncentrace se nalézá v tukové tkáni. Hlavními exkrečními metabolity jsou nezměněný emodepsid a jeho hydroxylované deriváty.
U savců je toltrazuril po perorálním podání pomalu vstřebáván. Hlavním metabolitem je toltrazuril sulfon. Kinetika perorální suspenze:
Po podání dávky přibližně 0,45 mg emodepsidu a 9 mg toltrazurilu na kg živé hmotnosti jednoročním psům byla zaznamenán geometrický průměr maximální koncentrace v séru 39 pg emodepsidu/l a 17,28 mg toltrazurilu/l. Maximálních koncentrací emodepsidu a toltrazurilu bylo dosaženo 2 a 18 hodin po aplikaci. Biologický poločas emodepsidu v séru byl 10 hodin a v případě toltrazurilu to bylo 138 hodin.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
butylhydroxytoluen (E321) kyselina sorbová (E200) čištěný slunečnicový olej
glycerol-dibehenát
6.2 Inkompatibility
Nemísit s jiným veterinárním léčivým přípravkem
6.3 Doba použitelnosti
Doba použitelnosti veterinárního léčivého přípravku v neporušeném obalu: 3 roky Doba použitelnosti po prvním otevření vnitřního obalu: 10 týdnů 6.4. Zvláštní opatření pro uchovávání
Tento veterinární léčivý přípravek nevyžaduje žádné zvláštní podmínky pro uchovávání.
6.5 Druh a složení vnitřního obalu
Jantarová lahvička o obsahu 7,5 ml nebo 20 ml s polyetylenovým adaptérem Luer a nerozbitným polypropylenovým dětským bezpečnostním uzávěrem.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro zneškodňování nepoužitého veterinárního léčivého přípravku nebo odpadu, který pochází z tohoto přípravku
Všechen nepoužitý veterinární léčivý přípravek nebo odpad, který pochází z tohoto přípravku, musí být likvidován podle místních právních předpisů. Přípravek nesmí kontaminovat vodní toky, protože může být nebezpečný pro ryby a jiné vodní organismy.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Bayer Animal Health GmbH 51368 Leverkusen Německo
8. REGISTRAČNÍ ČÍSLO(A)
EU/2/11/123/001-002
9. DATUM REGISTRACE/ PRODLOUŽENÍ REGISTRACE
Datum registrace: 20/04/2011 Datum posledního prodloužení:
10. DATUM REVIZE TEXTU
Podrobné informace o tomto veterinárním léčivém přípravku najdete na internetové adrese Evropské lékové agentury http://www.ema.europa.eu.
ZÁKAZ PRODEJE, VÝDEJE A/NEBO POUŽITÍ
Neuplatňuje se.
PŘÍLOHA II
A. DRŽITEL POVOLENÍ K VÝROBĚ ODPOVĚDNÝ ZA UVOLNĚNÍ ŠARŽE
B. PODMÍNKY REGISTRACE NEBO OMEZENÍ TÝKAJÍCÍ SE VÝDEJE A POUŽITÍ
C. DEKLARACE HODNOT MRL
A. DRŽITEL POVOLENÍ K VÝROBĚ ODPOVĚDNÝ ZA UVOLNĚNÍ ŠARŽE
Jméno a adresa výrobce odpovědného za uvolnění šarže
KVP Pharma + Veterinář Produkte GmbH Projensdorfer Str. 324 24106 Kiel Německo
B. PODMÍNKY REGISTRACE NEBO OMEZENÍ TÝKAJÍCÍ SE VÝDEJE NEBO POUŽITÍ
Veterinární léčivý přípravek je vydáván pouze na předpis.
C. DEKLARACE HODNOT MRL
Neuplatňuje se.
PŘÍLOHA III
OZNAČENÍ NA OBALU A PŘÍBALOVÁ INFORMACE
A. OZNAČENÍ NA OBALU
Procox 0,9 mg/ml + 18 mg/ml perorální suspenze pro psy emodepsidum/toltrazurilum
1 ml obsahuje:
Léčivé látky: emodepsidum 0,9 mg, toltrazurilum 18 mg
Pomocné látky: butylhydroxytoluen (E321; jako antioxidant) 0,9 mg, kyselina sorbová(E200; jako konzervant) 0,7 mg
Perorální suspenze
7,5 ml 20 ml
Pro psy.
Před použitím dobře protřepejte.
Před použitím čtěte příbalovou informaci. Perorální podání.
|
9. ZVLÁŠTNÍ UPOZORNĚNÍ, POKUD JE (JSOU) NUTNÉ(Á) | |
|
Před použitím čtěte příbalovou informaci | |
|
10. DATUM EXSPIRACE | |
EXP: {měsíc/rok}
Po 1. otevření spotřebujte do 10 týdnů.
11. ZVLÁŠTNÍ PODMÍNKY PRO UCHOVÁVÁNÍ
12. ZVLÁŠTNÍ OPATŘENÍ PRO ZNEŠKODŇOVÁNÍ NEPOUŽITÝCH PŘÍPRAVKŮ NEBO ODPADU, POKUD JE JICH TŘEBA
Likvidace: čtěte příbalovou informaci.
13. OZNAČENÍ „POUZE PRO ZVÍŘATA“ A PODMÍNKY NEBO OMEZENÍ TÝKAJÍCÍ SE VÝDEJE A POUŽITÍ, POKUD JE JICH TŘEBA
Pouze pro zvířata. Veterinární léčivý přípravek je vydáván pouze na předpis.
14. OZNAČENÍ „UCHOVÁVAT MIMO DOSAH DĚTÍ“
Uchovávat mimo dosah dětí.
15. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI
Bayer Animal Health GmbH, 51368 Leverkusen, Německo
16. REGISTRAČNÍ ČÍSLO(A)
EU/2/11/123/001 7,5 ml
EU/2/11/123/002 20 ml
17. ČÍSLO ŠARŽE OD VÝROBCE
Lot:
1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU
Procox 0,9 mg/ml + 18 mg/ml perorální suspenze pro psy emodepsidum/toltrazurilum
2. MNOŽSTVÍ LÉČIVÉ(ÝCH) LÁTKY(EK)
0,9 mg/ml emodepsidum a 18 mg/ml toltrazurilum
3. OBSAH VYJÁDŘENÝ HMOTNOSTÍ, OBJEMEM NEBO POČTEM DÁVEK
7,5 ml 20 ml
4. CESTA(Y) PODÁNÍ
Před použitím dobře protřepejte. Perorální podání.
5. OCHRANNÁ LHŮTA
6. ČÍSLO ŠARŽE
Lot:
7. DATUM EXSPIRACE
EXP: {měsíc/rok}
Po 1. otevření spotřebujte do:...
8. OZNAČENÍ „POUZE PRO ZVÍŘATA“
Pouze pro zvířata.
B. PŘÍBALOVÁ INFORMACE
PŘÍBALOVÁ INFORMACE PRO Procox 0,9 mg/ml + 18 mg/ml perorální suspenze pro psy
1. JMÉNO A ADRESA DRŽITELE ROZHODNUTÍ O REGISTRACI A DRŽITELE POVOLENÍ K VÝROBĚ ODPOVĚDNÉHO ZA UVOLNĚNÍ ŠARŽE, POKUD SE NESHODUJE
Držitel rozhodnutí o registraci: Bayer Animal Health GmbH 51368 Leverkusen Německo
Výrobce odpovědný za uvolnění šarže: KVP Pharma + Veterinář Produkte GmbH Projensdorfer Str. 324 24106 Kiel Německo
2. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU
Procox 0,9 mg/ml + 18 mg/ml perorální suspenze pro psy emodepsidum/toltrazurilum
3. OBSAH LÉČIVÝCH A OSTATNÍCH LÁTEK
1 ml obsahuje:
Léčivé látky:
emodepsidum 0,9 mg
toltrazurilum 18 mg
Pomocné látky:
butylhydroxytoluen (E321; jako antioxidant) 0,9 mg kyselina sorbová (E200; jako konzervant) 0,7 mg
4. INDIKACE
Určeno pro psy při suspektních nebo prokázaných smíšených parazitárních infekcích vyvolaných oblými červy a kokcidiemi následujících druhů:
Oblí červi (Nematoda):
- Toxocara canis (dospělá stádia, juvenilní stádia, larvální stádia L4)
- Uncinaria stenocephala (dospělá stádia)
- Ancylostoma caninum (dospělá stádia)
- Trichuris vulpis (dospělá stádia)
Kokcidie:
- Isospora ohioensis komplex
- Isospora canis
Léčba sníží rozšiřování infekce Isospora, nebude však účinná proti symptomům u již nakažených zvířat.
5. KONTRAINDIKACE
Nepodávat psům/štěňatům mladším 2 týdnů nebo s živou hmotností nižší než 0,4 kg. Nepoužívat v případě přecitlivělosti na léčivé látky nebo na některou z pomocných látek.
6. NEŽÁDOUCÍ ÚČINKY
Ve velmi vzácných případech se mohou objevit mírné a přechodné poruchy trávicího traktu (např. zvracení nebo měkká stolice).
Četnost nežádoucích účinků se určuje na základě následujících pravidel:
- velmi časté (více jak 1 z 10 zvířat vykazuje nežádoucí účinky v průběhu jednoho ošetření)
- časté (postihují více než 1, ale méně než 10 zvířat ze 100)
- méně časté (postihují více než 1, ale méně než 10 zvířat z 1000)
- vzácné (postihují více než 1, ale méně 10 zvířat z 10 000)
- velmi vzácné (postihují méně jak 1 zvíře z 10 000, včetně jednotlivých hlášených případů)
Jestliže zaznamenáte jakékoliv závažné nežádoucí účinky či jiné reakce, které nejsou uvedeny v této příbalové informaci, oznamte to prosím vašemu veterinárnímu lékaři.
7. CÍLOVÝ DRUH ZVÍŘAT
Psi
8. DÁVKOVÁNÍ PRO KAŽDÝ DRUH, CESTA(Y) A ZPŮSOB PODÁNÍ
Dávkování a léčebné schéma
Pro perorální podání u psů starších 2 týdnů a s hmotností minimálně 0,4 kg.
Doporučená minimální dávka je 0,5 ml/kg živé hmotnosti (ž.hm.), což odpovídá 0,45 mg emodepsidu/kg ž.hm. a 9 mg toltrazurilu/kg ž.hm.
Doporučené dávkování je uvedeno v následující tabulce:
|
Hmotnost [kg] |
Dávka [ml] |
|
0,4 |
0,2 |
|
> 0,4 - 0,6* |
0,3 |
|
> 0,6 - 0,8 |
0,4 |
|
> 0,8 - 1 |
0,5 |
|
> 1,0 - 1,2 |
0,6 |
|
> 1,2 - 1,4 |
0,7 |
|
> 1,4 - 1,6 |
0,8 |
|
> 1,6 - 1,8 |
0,9 |
|
> 1,8 - 2 |
1,0 |
|
> 2,0 - 2,2 |
1,1 |
|
> 2,2 - 2,4 |
1,2 |
|
> 2,4 - 2,6 |
1,3 |
|
> 2,6 - 2,8 |
1,4 |
|
> 2,8 - 3 |
1,5 |
|
> 3,0 - 3,2 |
1,6 |
|
> 3,2 - 3,4 |
1,7 |
|
> 3,4 - 3,6 |
1,8 |
|
> 3,6 - 3,8 |
1,9 |
|
> 3,8 - 4 |
2,0 |
|
> 4 - 5 |
2,5 |
|
> 5 - 6 |
3,0 |
|
> 6 - 7 |
3,5 |
|
> 7 - 8 |
4,0 |
|
> 8 - 9 |
4,5 |
|
> 9 - 10 |
5,0 |
|
> 10 Pokračujte v 0,5 ml/kg |
kg: dávkování ž.hm. |
*= více než 0,4 a do 0,6 kg
Jednorázové podání je obecně dostačující pro snížení rozšiřování infekce Isospora. Opakovaná terapie je indikována jen tehdy, pokud smíšená infekce kokcidiemi a oblými červy je i nadále suspektní (podle veterináře) nebo klinická.
9. POKYNY PRO SPRÁVNÉ PODÁNÍ
1. Před použitím dobře protřepejte.
2. Odšroubujte uzávěr přípravku. Použijte standardní jednorázovou stříkačku s ústím typu Luer pro každé ošetření. Pro přesné dávkování u psů do hmotnosti 4 kg použijte stříkačku se stupnicí po 0,1 ml. U psů nad 4 kg lze využít stříkačku se stupnicí po 0,5 ml. Nasaďte ústí stříkačky pevně do otvoru lahvičky.
3. Obraťte lahvičku dnem vzhůru a natáhněte příslušné množství přípravku. Před vytažením ústí stříkačky musí být lahvička opět dnem dolů. Po použití zašroubujte šroubový uzávěr.
4. Podejte přípravek Procox do dutiny ústní psa. Po aplikaci stříkačku vyhoďte (pokud není možné ji vyčistit).
1. Před použitím dobře protřepejte
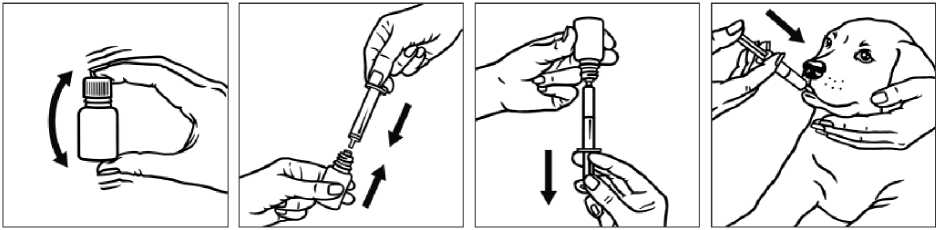
2. Nasaďte ústí stříkačky pevně do otvoru lahvičky
3. Obraťte lahvičku dnem vzhůru a natáhněte příslušné množství přípravku
4. Podejte Procox do dutiny ústní psa
10. OCHRANNÁ LHŮTA
Není určeno pro potravinová zvířata.
11. ZVLÁŠTNÍ OPATŘENÍ PRO UCHOVÁVÁNÍ
Uchovávat mimo dosah dětí.
Nepoužívejte po uplynutí doby použitelnosti uvedené na etiketě a krabičce po EXP Doba použitelnosti končí posledním dnem v uvedeném měsíci.
Doba použitelnosti po prvním otevření balení: 10 týdnů.
Tento veterinární léčivý přípravek nevyžaduje žádné zvláštní podmínky pro uchovávání.
12. ZVLÁŠTNÍ UPOZORNĚNÍ
Zvláštní upozornění pro každý cílový druh:
Ošetření zabraňuje rozšiřování infekce Isospora, ale nebude účinné proti symptomům (např. průjem) u již nakažených zvířat. U zvířat s průjmem může být potřebná dodatečná léčba (veterinárním lékařem).
Aby se zabránilo reinfekci z prostředí, je důležité zavést hygienická opatření, zvláště pak je důležité zajistit co nejsušší a nejčistší prostředí.
Oocysty Isospory jsou odolné vůči mnoha dezinfekčním prostředkům a můžou přežít ve vnějším prostředí po velmi dlouhou dobu. Včasné odstranění výkalů (do 12 hodin) snižuje riziko přenosu infekce. Všichni psi ve skupině, kteří jsou ohroženi infekcí, by měli být ošetřeni současně.
Podobně jako u ostatních antiparazitárních přípravků může vést časté a dlouhodobé používání anthelmintik nebo antiprotozoik ke vzniku rezistence. Vhodný léčebný režim doporučený veterinářem zajistí adekvátní kontrolu parazitů a sníží pravděpodobnost vzniku rezistence.
Zvláštní opatření pro použití u zvířat:
Procox se nedoporučuje podávat koliím a jim příbuzným plemenům, které jsou nositeli mdr1 -/- mutace a nebo se tato mutace předpokládá. Prokázalo se, že u těchto mdr1 -/- mutantních štěňat je přípravek snášen méně než u štěňat ostatních.
Zkušenosti s podáváním přípravku u velmi oslabených psů nebo u psů s porušenou funkcí ledvin či jater jsou omezené. Sdělte, prosím, vašemu veterináři, pokud se toto vašeho psa týká.
Zvláštní opatření určené osobám, které podávají veterinární léčivý přípravek zvířatům:
Nejezte, nepijte a nekuřte při manipulaci s přípravkem.
Po aplikaci si umyjte ruce vodou.
V případě náhodného potřísnění kůže, umyjte postižené místo neprodleně mýdlem a vodou.
V případě, že se přípravek náhodně dostane do očí, vypláchněte oči neprodleně velkým množstvím vody.
V případě náhodného pozření přípravku, zvláště pak u dětí, vyhledejte ihned lékařskou pomoc a ukažte příbalovou informaci nebo etiketu praktickému lékaři.
Březost a laktace:
Nebyla stanovena bezpečnost veterinárního léčivého přípravku pro březí feny a lakující feny. Použití u březích fen a lakujících fen v průběhu prvních dvou týdnů laktace se proto nedoporučuje.
Interakce s dalšími léčivými přípravky a další formy interakce:
Emodepsid může vyvolat interakce s jinými veterinárními léčivými přípravky, které mají stejný systém transportu (například makrocyklické laktony). Možné klinické dopady těchto interakcí nebyly zkoumány.
Předávkování (symptomy, první pomoc, antidota):
Při opakovaném podávání veterinárního léčivého přípravku v dávce až 5x vyšší než je doporučená dávka se občas objevily mírné a přechodné poruchy trávicího traktu v podobě měkké stolice nebo zvracení.
Inkompatibility:
Nemísit s jiným veterinárním léčivým přípravkem
13. ZVLÁŠTNÍ OPATŘENÍ PRO ZNEŠKODŇOVÁNÍ NEPOUŽITÝCH PŘÍPRAVKŮ NEBO ODPADU, POKUD JE JICH TŘEBA
Léčivé přípravky se nesmí likvidovat prostřednictvím odpadních vod. Tato opatření napomáhají chránit životní prostředí. Přípravek nesmí kontaminovat vodní toky, protože může být nebezpečný pro ryby a jiné vodní organismy.
14. DATUM POSLEDNÍ REVIZE PŘÍBALOVÉ INFORMACE
Podrobné informace o tomto přípravku jsou k dispozici na webových stránkách Evropské lékové agentury (http://www.ema.europa.eu/).
15. DALŠÍ INFORMACE
Procox perorální suspenze se dodává ve dvou různých velikostech balení s obsahem: 7,5 ml nebo 20 ml
Na trhu nemusí být všechny velikosti balení.
Pokud chcete získat informace o tomto veterinárním léčivém přípravku, kontaktujte prosím příslušného místního zástupce držitele rozhodnutí o registraci.
|
Belgie/Belgique/Belgien Bayer SA-NV J.E. Mommaertslaan 14 1831 Diegem (Machelen) Tel/Tél: +32 2 535 66 54 |
Lietuva Magnum Veterinaaria AS Vae 16 76401 Laagri Estonia Tel: +372 650 1920 |
|
Peny6^HKa Bt^rapnn B^pa^gaHe-KacHC OOfl 6yn. Etnrapna 102-4 HoBen 5500 Ten: + 359 68 604 111 |
Luxembourg/Luxemburg Bayer SA-NV J.E. Mommaertslaan 14 1831 Diegem (Machelen) Belgique/Belgien Tél/Tel: +32 2 535 66 54 |
|
Česká republika Bayer s.r.o., Animal Health Siemensova 2717/4 155 00 Praha 5 Tel: +420 2 66 10 14 71 |
Magyarország Bayer Hungária Kft. 1123 Budapest Alkotás u. 50 Tel: +36 1 487 4100 |
|
Danmark Bayer A/S, Bayer HealthCare Animal Health Division Arne Jacobsens Allé 13 2300 Kobenhavn S Tlf: +45 4523 5000 |
Malta Bayer Animal Health GmbH 51368 Leverkusen Germany Tel: +49 2173 38 4012 |
|
Deutschland Bayer Vital GmbH Geschaftsbereich Tiergesundheit 51368 Leverkusen Tel: +49 214 301 |
Nederland Bayer B.V., Animal Health Division Energieweg 1 3641 RT Mijdrecht Tel: +31 297 280 666 |
|
Eesti Magnum Veterinaaria AS Vae 16 76401 Laagri Tel: +372 650 1920 |
Norge Bayer AS Bayer HealthCare Animal Health Division Drammensveien 288 0283Oslo Tlf: +47 23 13 05 00 |
|
ElláSa Bayer Ekkág A.B.E.E. Empoó 18-20 151 25 Mapoóar, AOpva |
Osterreich Bayer Austria GmbH Geschaftsbereich Tiergesundheit HerbststraBe 6 - 10 |
|
Tr(k: +30 210 6187 500 PROVET S.A. NiKq^ópou ®©Ká & Ay. Avapyúprov ©sap BpayKÓ 193 00 Aonpónupyog, Attik^ Tn^: +30 210 5575770-3 info@provet.gr |
1160 Wien Tel: +43 1 71146 2850 |
|
Espaňa Bayer Hispania, S.L. División Sanidad Animal Av. Baix Llobregat, 3-5 08970 Sant Joan Despí (Barcelona) Tel: +34 93 4956500 |
Polska Bayer Sp. z o.o. Animal Health Al. Jerozolimskie 158 02-326 Warszawa Tel: +48 22 572 35 00 |
|
France Bayer HealthCare Division Animal Health 13, rue Jean Jaures 92807 Puteaux Cedex Tél: +33 1 49 06 56 00 |
Portugal Bayer Portugal S.A. Divisao de Saúde Animal Rua da Quinta do Pinheiro, 5 2794-003 Carnaxide Tel: +351 21 4172121 |
|
Hrvatska BAYER d.o.o. Radnička cesta 80 10000 Zagreb Tel.: +385 1 65 99 935 |
Románia S.C. Bayer S.R.L. Sos. Pipera nr. 42, sector 2 Bucuresti 020112 Tel: +40 21 529 5900 |
|
Ireland Bayer Limited, Animal Health Division The Atrium, Blackthorn Road Dublin 18 Tel: +353 1 2999313 |
Slovenija Bayer d.o.o Bravničarjeva 13 1000 Ljubljana Tel: +386 1 5814 400 |
|
Ísland Icepharma hf. Lynghálsi 13 110 Reykjavík Sími: +354 540 8000 |
Slovenská republika Bayer s.r.o., Animal Health Siemensova 2717/4 155 00 Praha 5 Česká republika Tel: +420 2 66 10 14 71 |
|
Italia Bayer S.p.A. Viale Certosa, 130 20156 Milano Tel: +39 02 3978 1 |
Suomi/Finland Orion Oyj ORION PHARMA ELÁINLÁÁKKEET Tengstrominkatu 8, PL/PB 425 20101 Turku/Ábo Puh/Tel: +358 10 4261 |
|
Kúrcpog ACTIVET Ltd. Avxpéa Miaoú^n 50 2415 'EyK^^n, AeuKroaía Tr|A2 +357-22-591918 |
Sverige Bayer A/S, Bayer HealthCare Animal Health Division Arne Jacobsens Allé 13 2300 Kopenhamn S Danmark Tel: +46 (0)8-580 223 00 |
|
Latvija Magnum Veterinaaria AS Vae 16 76401 Laagri Estonia Tel: +372 650 1920 |
United Kingdom Bayer plc, Animal Health Division, Bayer House, Strawberry Hill, Newbury, Berkshire RG14 1JA Tel: +44 1635 563000 |
25